Результат интеллектуальной деятельности: Способ раннего прогноза развития нефрита в индуцированной модели аутоиммунного заболевания системной красной волчанки in vivo
Вид РИД
Изобретение
Изобретение относится к способу прогнозирования системных воспалительных состояний в организме животного, способных привести к развитию нефрита в индуцированной модели аутоиммунного заболевания системной красной волчанки.
Системная красная волчанка (СКВ) - системное аутоиммунное заболевание соединительной ткани, при котором сочетание генетических и эпигенетических факторов дает гетерогенную клиническую картину: от кожных проявлений до поражения почек (у 50% больных). Поражение органов патогенетически связано с постоянной выработкой антител к собственной ДНК (антиДНК аутоантител) и иммунных комплексов. Именно антиДНК аутоантитела реагируют с базальной мембраной клубочков, что вызывает развитие гломерулонефрита. Больные с высокими титрами антител к нативной ДНК имеют повышенный риск развития тяжелого гломерулонефрита. Образующиеся комплексы аутоантиген-аутоантитело циркулируют в крови, активируют комплемент и фиксируются в капиллярах и почечных канальцах, приводя к воспалительным реакциям и повреждению тканей, формированию иммунокомплексного гломерулонефрита (волчаночного нефрита).
К сожалению, антинуклеарные антитела не специфичны для системной красной волчанки, т.к. обнаруживаются в крови здоровых, особенно пожилых людей, а также при других аутоиммунных заболеваниях, вирусных инфекциях, хроническом воспалении. Поскольку волчаночный нефрит является одним из серьезных проявлений и одним из самых сильных предикторов неблагоприятного исхода СКВ, актуальным является поиск ранних предикторов нефрита у больных СКВ, когда оценивают разнообразные параметры воспаления (US 2008187944, C12Q 1/46, 2008; KP 101320694, C12Q 1/37, 2013).
Известны попытки лечения СКВ путем уменьшения количества ДНК за счет введения фермента ДНКазы, разрушающего ДНК. Например, известен способ лечения заболеваний человека, сопровождающихся повышенным содержанием дезоксирибонуклеиновой кислоты (ДНК) во внеклеточных пространствах тканей и органов, путем энтерального введения фермента ДНКазы (RU 2308968, A61K 38/43, 2007). Энтеральное введение высоких доз ДНКазы обеспечивает абсорбцию каталитически значимых количеств этого фермента в кровь с достоверным увеличением ДНК-гидролитической активности фермента.
Но феномен повышенной концентрации ДНК в крови и во внеклеточных пространствах тканей и органов человека встречается при разнообразной патологии (инфаркт миокарда, сепсис, онкологические заболевание и пр.) и однозначно связан с развитием любого воспалительного процесса.
Известен способ in vitro для прогнозирования и/или диагностики волчаночного нефрита у субъекта, затронутого или потенциально затронутого системной красной волчанкой, который включает определение концентрации антител подкласса IgG2 при использовании различных антигенов, в том числе ДНК. Увеличение концентрации антител по сравнению с контрольным значением должно указывать на развитие волчаночного нефрита (US 2016349254, G01N 33/564, 2016).
В данном способе не измеряется количество ДНК, а используют ее в качестве антигена.
Известен способ прогнозирования течения системной красной волчанки у пациентов с III степенью активности обостренного заболевания. Для этого в плазме крови пациента в динамике лечения определяют уровни ДНК-содержащей фракции и нуклеотидсодержащей фракции и по их значениям прогнозируют течение системной красной волчанки (RU1783423, G01N 33/48, 1992). Данный способ предназначен для повышения точности оценки состояния больного с III степенью активности заболевания и эффективности лечения и не может быть применен для раннего прогноза заболевания.
Изучение взаимодействия врожденного и адаптивного иммунитета в формировании хронического слабовыраженного воспаления, являющегося ключевой особенностью ряда патологических состояний (атеросклероза, диабета, онкологии, аутоиммунных заболеваний), обуславливает необходимость поиска новых экспериментальных моделей, поиска новых и повышения эффективности использования традиционных маркеров воспаления. К числу таких маркеров относится достаточно простой параметр - индекс N/L - соотношение нейтрофилы/лимфоциты, как биологический маркер системного воспаления и предиктор, положительно коррелирующий с исходом заболеваний, обусловленных наличием хронического системного воспаления низкого уровня. Сегодня он является предиктором неблагоприятного прогноза рака и сердечнососудистых заболеваний среди населения в целом (Li Н., Lu X., Xiong R., Wang S. High Neutrophil-to-Lymphocyte Ratio Predicts Cardiovascular Mortality in Chronic Hemodialysis Patients // Mediators Inflamm. 2017. doi: 10.1155/2017/9327136). По литературным данным известно, что значение индекса N/L является хорошим прогностическим маркером, т.к. у пациентов с СКВ индекс N/L достоверно выше по сравнению со здоровыми людьми. Средние значения индекса у больных СКВ с люпусным нефритом достоверно выше, чем у больных без нефрита, что позволяет отнести его к перспективным маркерам, отражающим поражение почек у пациентов с СКВ, который имеет преимущества по сравнению с определением креатинина и измерением суточной протеинурии: он более дешев, быстро и легко измеряется (Chen Y., Yang X., Chen L, Yang Y. Neutrophil-to-lymphocyte ratio (NLR) and platelet-to-lymphocyte ratio (PLR) were associated with disease activity in patients with systemic lupus erythematosus // International Immunopharmacology. 2016; 36: 94-9).
Известно, что причиной аутоиммунных заболеваний является наличие липополисахарида - эндотоксина - продукта бактерий из желудочно-кишечного тракта, который появляется в крови больных и определяет картину воспаления низкой степени выраженности (WO 2008029897, A61K 38/00, 2008). Для изучения механизмов такого воспаления в настоящее время апробируются разнообразные экспериментальные модели.
Известен способ создания модели СКВ в полуаллогенной модели: перенос клеток селезенки от самок мышей DBA/2 → самкам (C57BL/6 × DBA2) F1 гибридам. После индукции модели через 12 недель в популяции генетически однородных F1 гибридов у всех мышей имеются признаки СКВ: спленомегалия, гипергаммаглобулинемия, продукция аутоантител к ДНК, при этом у части мышей с более выраженными симптомами СКВ развивается нефрит (СКВнефрит+), а у мышей с менее выраженными симптомами СКВ нефрит отсутствует - СКВнефрит- (Колесникова О.П., Кудаева О.Т., Вольский Н.Н., Гойман Е.В., Гаврилова Е.Д., Перминова О.М., Демченко Е.Н., Козлов В.А. Экспериментальная модель аутоиммунного процесса: роль эпигенетической изменчивости в популяции мышей-гибридов. Вестник РАМН 2015; 70 (2): 152-158). Оценка развития нефрита производится через 12 недель после индукции модели по уровню белка в моче. Можно предполагать, что разделение мышей на группы СКВнефрит- и СКВнефрит+, равное примерно 50/50 при индукции модели СКВ, обусловлено у части мышей эпигенетическими изменениями в системе врожденного иммунитета, определяющими более сильный воспалительный ответ, что в дальнейшем приведет к формированию группы СКВнефрит+.
Недостатком способа является диагностика нефрита по количеству белка в моче после 12 недель индукции модели, когда уже имеется развернутая клиническая картина нефрита.
Наиболее близким к заявляемому является способ анализа количества внеклеточной ДНК для определения уровня аутоиммунного заболевания и прогноза лечения. Кроме анализа количества внеклеточной ДНК способ включает оценку размеров фрагментов молекул ДНК и уровня их метилирования (US 2015087529, C12Q 1/68, 26,03.2015).
Задачей изобретения является создание способа определения более раннего и точного прогноза развития нефрита в индуцированной модели системной красной волчанки in vivo.
Поставленная задача решается тем, что в способе раннего прогноза развития нефрита в индуцированной модели аутоиммунного заболевания системной красной волчанки, включающем введение дозы липополисахарида здоровым животным с последующей одновременной оценкой уровня воспаления по клеткам крови и уровню внеклеточной ДНК в плазме крови в определенные промежутки времени, здоровым мышам-гибридам (C57BL/6 × DBA2)F1 внутрибрюшинно вводят липополисахарид в дозе 50 мкг/кг, затем на 2, 4, 8, 11 и 24 час от момента его введения в динамике оценивают в крови индекс соотношения нейтрофилов к лимфоцитам (N/L) и внеклеточную ДНК и через 24 часа после введения липополисахарида индуцируют модель системной красной волчанки путем внутривенного введения клеток селезенки самок мышей линии DBA/2, при этом часть мышей, у которых выявляется максимальный прирост индекса N/L на 4 час относительно 2-го часа и максимальный уровень внеклеточной ДНК - на 8 час относят к группе СКВнефрит+ и прогнозируют возможность развития нефрита в этой группе.
Изобретение, на наш взгляд, является новым и обладает изобретательским уровнем. Существенным является то, что ранее при системной красной волчанке не сравнивали повышенную ДНК с индексом N/L для раннего прогноза развития нефрита при аутоиммунном заболевании СКВ.
Сущность изобретения заключается в том, что введение ЛПС здоровым животным обнаруживает динамику воспалительного ответа не только по индексу N/L, но и по внеклеточной ДНК. У животных, впоследствии сформировавших группу СКВ с нефритом (СКВнефрит+), увеличение уровня внеклеточной ДНК на введение ЛПС наступает позднее, чем прирост индекса N/L. Это объясняется тем, что появление внеклеточной ДНК связано с процессом NETosis, занимающего несколько часов, как одной из форм гибели нейтрофилов, в результате которого именно из нейтрофилов высвобождается внеклеточная ДНК (Boris Pinegin, Nina Vorobjeva, Vladimir Pinegin. Neutrophil extracellular traps and their role in the development of chronic inflammation and autoimmunity. Autoimmunity Reviews, 2015, 14, 633-640).
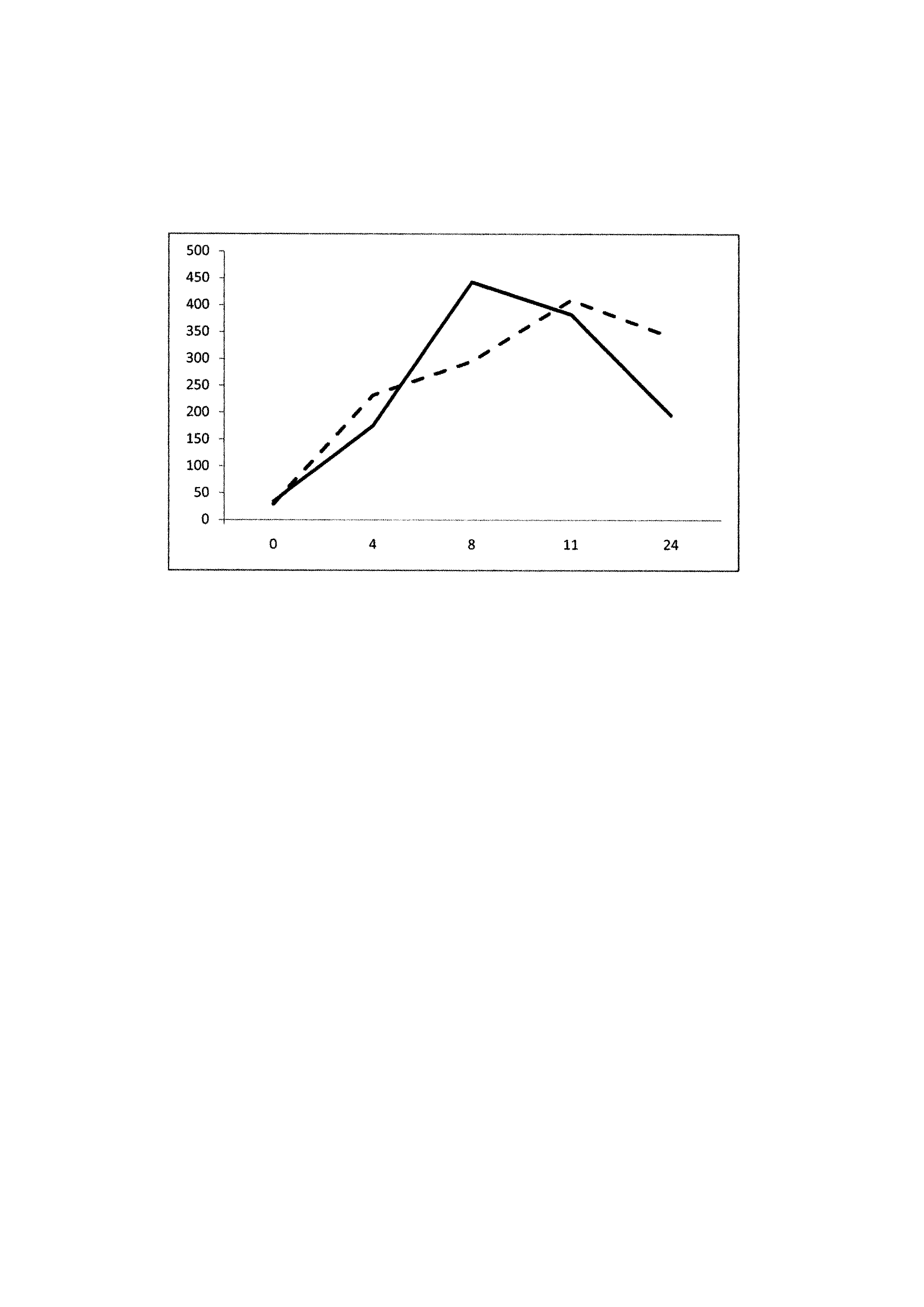
На прилагаемом рисунке представлен ретроспективный анализ средних значений уровня внеклеточной ДНК в плазме интактных животных после введения ЛПС 50 мкг/кг, где
- пунктирная линия - СКВнефрит-
- сплошная линия - СКВнефрит+
- по оси абцисс - время после введения ЛПС, час
- по оси ординат - концентрация внеклеточной ДНК, нг/мл
Способ осуществляется следующим образом.
1) введение 10 здоровым мышам (C57BL/6 × DBA/2)F1 гибридам ЛПС в дозе 50 мкг/кг внутрибрюшинно;
2) в динамике оценивали в крови индекс N/L и внеклкеточную ДНК на 0, 2, 4, 8, 11, 24 часа;
3) у части мышей выявлен больший прирост в крови индекса N/L на 4-й час, а у другой части мышей выявлен меньший прирост индекса на 8-й час с момента введения ЛПС. Аналогичная картина наблюдается для внеклеточной ДНК с отсрочкой на 4 часа для высвобождения внеклеточной ДНК из нейтрофилов.
4) через 24 часа всем мышам вводили внутривенно клетки селезенки мышей линии DBA/2, индуцируя таким образом модель СКВ;
5) через 12 недель после индукции модели у всех 10 мышей измеряем белок в моче для установления развития нефрита;
6) установлено, что у 6 мышей с ранним и более высоким приростом индекса N/L развивается нефрит (белок больше или равен 3 мг/мл), а у 4 с более поздним и меньшим приростом индекса N/L нефрит отсутствует (белок меньше 3 мг/мл).
Важно, что различная динамика и величина прироста индекса N/L и уровень внеклеточной ДНК позволяет прогнозировать развития нефрита до индукции модели СКВ.
Пример. Доза ЛПС 50 мкг/кг и индекс N/L как ранний маркер развития нефрита Ретроспективный анализ ответа интактных мышей на ЛПС в дозе 1 мкг/мышь показал, что мыши в последующем разделившиеся на группу СКВнефрит- и СКВнефрит+ проявляют разную кинетику воспалительного ответа, определяемую по индексу N/L: у мышей СКВнефрит+ ответ на ЛПС развивается быстрее по сравнению с мышами СКВнефрит- (Табл. 1).
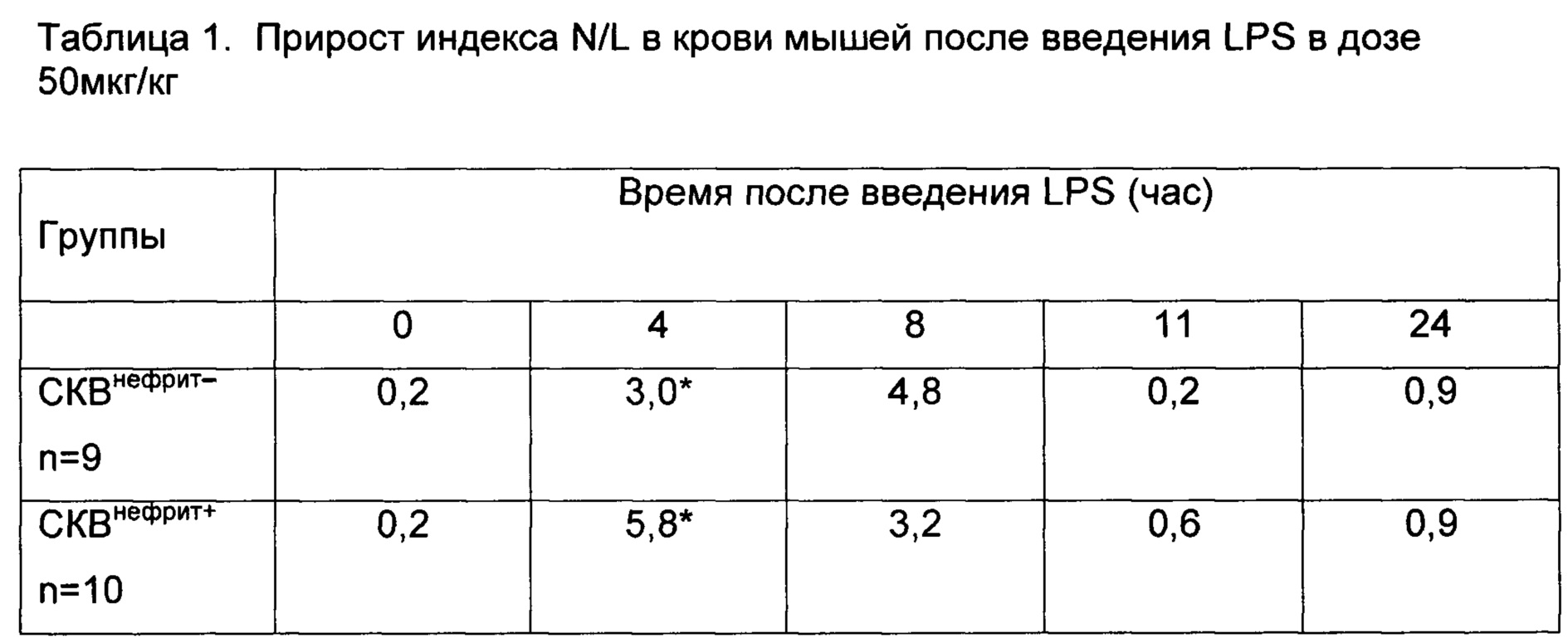
Примечания к таблице 2: n - количество мышей в группе;
* средние значения прироста индекса N/L в группе (во сколько раз)
Таким образом, ретроспективный анализ изменения индекса N/L у мышей при введении ЛПС в дозе 50 мкг/кг до индукции модели показал, что мыши, впоследствии разделившиеся на СКВнефрит+ и СКВнефрит-, проявляют разную динамику воспалительного ответа, определяемую по приросту индекса N/L в каждой определяемой точке - 0, 4, 8, 11, 24 часа относительно предыдущей: у мышей СКВнефрит+ ответ развивается сильнее и быстрее по сравнению с мышами СКВнефрит-. У мышей СКВнефрит+ максимум ответа приходится на 4 часа, у мышей СКВнефрит- - 8 часов.
Ретроспективный анализ показал, что мыши, в последующем разделившиеся на группы СКВнефрит- и СКВнефрит+, имели разную динамику изменения уровня внеклеточной ДНК, в среднем в группе мышей с сквнефрит + уровень внеклеточной ДНК повышался, а затем снижался раньше, чем у мышей с СКВнефрит- (см. чертеж). При сравнении данных табл. 1 и чертежа видно, что изменения индекса N/L и уровня внеклеточной нДНК каждой из подгрупп имеют сходную динамику. Так, в группе СКВнефрит+ на 4 часа выявляется максимум ответа по индексу N/L, а со сдвигом 4 часа определяется максимум уровня внеклеточной ДНК, а в группе СКВнефрит- максимум ответа по индексу N/L выявляется на 8 часов, а со сдвигом на 4 часа определяется максимум уровня внеклеточной ДНК.
Способ позволяет существенно сократить время, необходимое для определения начала развития нефрита в индуцированной модели аутоиммунного заболевания системной красной волчанки in vivo.
Способ раннего прогноза развития нефрита в индуцированной модели аутоиммунного заболевания системной красной волчанки, включающий введение дозы липополисахарида здоровым животным с последующей одновременной оценкой уровня воспаления по клеткам крови и уровню внеклеточной ДНК в плазме крови в определенные промежутки времени, отличающийся тем, что здоровым мышам-гибридам (C57BL/6 × DBA2)F1 внутрибрюшинно вводят липополисахарид в дозе 50 мкг/кг, затем на 2, 4, 8, 11 и 24 час от момента его введения в динамике оценивают в крови индекс соотношения нейтрофилов к лимфоцитам (N/L) и внеклеточную ДНК и через 24 часа после введения липополисахарида индуцируют модель системной красной волчанки путем внутривенного введения клеток селезенки самок мышей линии DBA/2, при этом часть мышей, у которых выявляется максимальный прирост индекса N/L на 4 час относительно 2-го часа и максимальный уровень внеклеточной ДНК - на 8 час, относят к группе СКВ и прогнозируют возможность развития нефрита в этой группе.