Результат интеллектуальной деятельности: ЭКСПЕРИМЕНТАЛЬНЫЙ СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ПЕЧЕНИ ВНУТРИПОРТАЛЬНЫМ ВВЕДЕНИЕМ ЗИМОЗАНА, ИНКОРПОРИРОВАННОГО В ФАГОЦИТИРУЮЩИЕ КЛЕТКИ
Вид РИД
Изобретение
Изобретение относится к медицине и биотехнологии, а именно к способам активации противоопухолевой цитотоксичности макрофагов. Метод может быть использован для лечения злокачественных опухолей и метастазов в печени, а также в качестве метода стимуляции предшественников гранулоцитов и моноцитов в комбинированной терапии злокачественных новообразований различной локализации с применением химио- и лучевой терапии.
Среди активаторов некоторых функций иммунной системы известен бета-глюкан, на который обратили внимание еще в середине 50-х - 60-х годов прошлого века. Он существует в двух формах - это частичковая (водонерастворимая), типичным представителем которой является зимозан и многочисленные разновидности водорастворимой формы бета-глюкана, отличающиеся друг от друга химической разветвленностью макромалекулы биополимера. Известно, что бета-глюкан повышает неспецифическую иммунологическую реактивность в основном за счет активации им системы мононуклеарных фагоцитов (1). Однако вышеупомянутые формы бета-глюкана резко отличаются друг от друга по силе воздействия на макрофаги. Зимозан выгодно отличается от водорастворимых форм тем, что оказывает на макрофаги более выраженное и пролонгированное воздействие. Кроме того, он способен активировать гораздо больший спектр его функций в отличие от растворимых форм глюкана (2, 3, 4). Во-первых, после однократного внутривенного введения зимозана мыши ее печеночные макрофаги могут находиться в функционально-активном состоянии около 30 дней. Во-вторых, фагоцитоз зимозановых частичек сопровождается выбросом огромного количества активных форм кислорода, провоспалительных цитокинов и других флогогенных веществ, что выражается в значительном повышении биоцидного потенциала макрофагов, который играет ведущую роль не только в уничтожении микробов и паразитов, но и в лизисе опухолевых клеток. В-третьих, зимозан способен сильно стимулировать кроветворение и, в частности, его грануломиелоцитарный росток, в результате чего вес селезенки и печени мыши может увеличиться в несколько раз за счет притока в них клеток лимфоидной ткани и прежде всего макрофагов. В-четвертых, биологические механизмы активации макрофагов обеих форм бета-глюкана различны (5).
Однако, несмотря на многолетние исследования, зимозан не нашел своего применения в клинической практике, не считая единичных работ, проведенных в 60-х - 70-х годах прошлого столетия на территории СССР. Нужно отметить, что в этих исследованиях он применялся только для внутримышечных инъекций и в минимальных дозировках (6, 7). В настоящее время применение зимозана в практической медицине на территории России и за рубежом полностью прекращено. И вот почему:
1) Поскольку внутримышечное введение зимозана неминуемо повлечет за собой его «оседание» в макрофагах маргинальной зоны региональных лимфоузлов и резидентных макрофагах в самом месте изначального введения, то естественно, что в кровоток, если он и попадет, то в очень незначительных количествах.
2) Внутримышечное введение зимозана в больших количествах невозможно, поскольку связано с возможностью возникновения болезненных инфильтратов.
3) Внутривенное введение зимозана человеку никогда не проводилось. В экспериментах на животных введение различных микрочастиц, как правило, приводит к образованию микротромбов. Например, в руководствах по наномедицине описаны неединичные случаи образования микротромбов после внутривенного введения микрочастиц различной природы. Эти частицы, попав к кровоток, быстро опсонизируются сывороточными опсонинами и активизируют некоторые компоненты свертывающей системы крови и, как следствие этого, они проявляют склонность к тромбообразованию. Именно по этой причине до сих пор микрочастицы нагруженные различными лекарственными препаратами не нашли своего широкого применения в медицине.
4) Известно, что практически все эффекты зимозана на макрофаги и другие клетки опосредованы через его связывание с маннозным рецептором (Dectin-1) (8). В момент этого связывания на поверхности резидентных макрофагов происходит мощный выброс активных форм кислорода, цитокинов и других флогогенных продуктов (9), что приводит даже к повреждению клеток окружающих тканей. В крайнем случае могут появиться симптомы начала системного воспаления, что влечет за собой мультиорганную недостаточность (10).
5) В клинической практике он применялся только в очень малых дозировках (1 мг/мл) и был рассчитан только для внутримышечного способа введения. Можно с уверенностью сказать, что именно его малые дозировки и внутримышечный способ введения стали причиной получения порой недостоверных и неоднозначных результатов в проведенных многочисленных клинических научных экспериментах.
6) Зимозан, попав в кровь, способен через непосредственный контакт с некоторыми компонентами сывороточного комплемента приводить к появлению в сыворотке многочисленных биологически активных веществ, которые способны вызвать целый ряд нежелательных, а порой смертельно опасных осложнений (11, 12).
Задачей изобретения является разработка безопасного парентерального способа введения зимозана с целью преимущественно локального (органного) повышения противоопухолевой цитотоксичности макрофагов для лечения злокачественных опухолей и метастазов в печени.
Поставленная задача решается путем экранировании поверхности зимозановых гранул (инкапсулирование), дабы не допустить прямого контакта поверхностно-расположенных концевых молекул бета-глюкана с маннозными рецепторами клеток крови и эндотелия сосудов, а также компонентами системы сывороточного комплемента, что позволит избежать развития всевозможных побочных эффектов и адресной их доставки в пораженный орган.
Сущность способа заключается в следующем. Из организма животного или человека выделяют фагоциты (макрофаги), способные активно фагоцитировать опсонизированный зимозан. Затем эти «нагруженные» зимозаном макрофаги вводят в портальную вену печени. Сами же нагруженные зимозаном макрофаги практически не обладают цитотоксическим потенциалом, поскольку основной выброс цитотоксических молекул - активные формы кислорода и фактор некроза опухоли - альфа происходит в условиях ЕХ VIVO, а значит на этапе до введения леток в организм животного или человека. Кроме того, фагоциты, поглотившие опсонозированный зимозан, погибают в течение нескольких часов.
Такая схема использования зимозана может позволить его введение даже внутривенным способом, не приводя к каким-либо неблагоприятным последствиям. Потенциал токсической активности самого «нагруженного» зимозаном макрофага имеет безопасное значение, поскольку основной выброс флогогенных продуктов макрофага завершается, как правило, через 1-3 часа после контакта с макрофагами, а это, как известно, происходит уже вне организма («ex vivo»). Более того, после того как произойдет фагоцитоз зимозана, макрофаг апоптотирует в течение 1-3-х суток (13). Такой функционально «разряженный» зимозаннагруженный макрофаг сохраняет способность к инициации гранулематозного воспаления за счет притока, дифференцировки и активации различных форменных элементов иммунной системы в месте его введения. Здесь необходимо добавить, что такое зимозаниндуцированное гранулематозное воспаление всегда сопровождается признаками гиперчувствительности замедленного типа. Все эти процессы и определяют механизм повышения противоопухолевой цитотоксичности макрофагов в очаге введения вышеупомянутых клеток.
Зимозан известен как индуктор гранулематозного воспаления, следствием чего в месте введения вышеуказанных макрофагов начинает возникать приток функционально активных клеточных элементов иммунной системы (в подавляющем большинстве своем - это макрофаги и в меньшей степени различные популяции лимфоцитов и естественных киллеров - НК-клеток), способных уничтожать различные агенты инфекционного и паразитарного происхождения, а также опухолевые клетки.
Способ применен в эксперименте в лечении печеночных метастазов мышиной злокачественной меланомы В 16. Для этого вводили нагруженные зимозаном макрофаги непосредственно в портальную вену, чтобы клеточная концентрация в органе достигла максимальной своей величины в силу того, что печень является самым большим «органом-депо» системы мононуклеарных фагоцитов любого млекопитающего. Этот факт позволяет надеяться на то, что все вышеперечисленные побочные эффекты будут сведены к минимуму, поскольку почти все введенные макрофаги «осядут» в печени (14).
Предлагаемый способ предусматривает несколько стадий:
1) Получение элиситированных крахмалом перитонеальных макрофагов мыши:
За 4 дня внутрибрюшинно вводили 4% крахмал в объеме 1 мл.
2) Приготовление опсонизированного зимозана:
Гомогенизированный любым способом (механическим или на ультразвуковой установке) зимозан инкубировали при 37 градусах по Цельсию в течение 30 минут в неинактивированной сыворотке мышей. Затем частички зимозана трижды отмывали в 10 миллилитрах забуференного физиологического раствора при 3000 об/мин.
4) Процедура «нагрузки» макрофагов опсонизированными гранулами зимозана:
Одним из условий процедуры «нагрузки» зимозаном макрофагов является избыток гранул зимозана - это не менее 100 гранул на 1 макрофаг, находящийся в плотном монослое культуры, или концентрация зимозана в культуре должна быть примерно 2-4 мг/мл культуральной среды. Фагоцитоз проводят в среде RPMI 1640 с добавлением инактивированной эмбриональной 10% сыворотки мышей.
5) Снятие зимозаннагруженных макрофагов с поверхности пластика:
Пластиковую плашку диаетром 90 мм или флакон для культивирования клеток с площадью не менее 25 кв. см трижды отмывают от непоглощенных частичек зимозана забуференным физиологическим раствором. Монослой клеток открепляют от поверхности резиновым или пластиковым скрепером. Затем полученную суспензию клеток трижды отмывают центрифугированием в 10 мл забуференного физиологического раствора при 1000 об/мин и в течение 8 минут. В дальнейшем осадок ресуспендируют в среде RPMI 1640 и проводят подсчет клеток. Количество введенных внутрипеченочно макрофагов должно быть 15 млн на мышь. Количество введенных в портальную вену печени клеток меланомы В16 было 30000 на одну мышь.
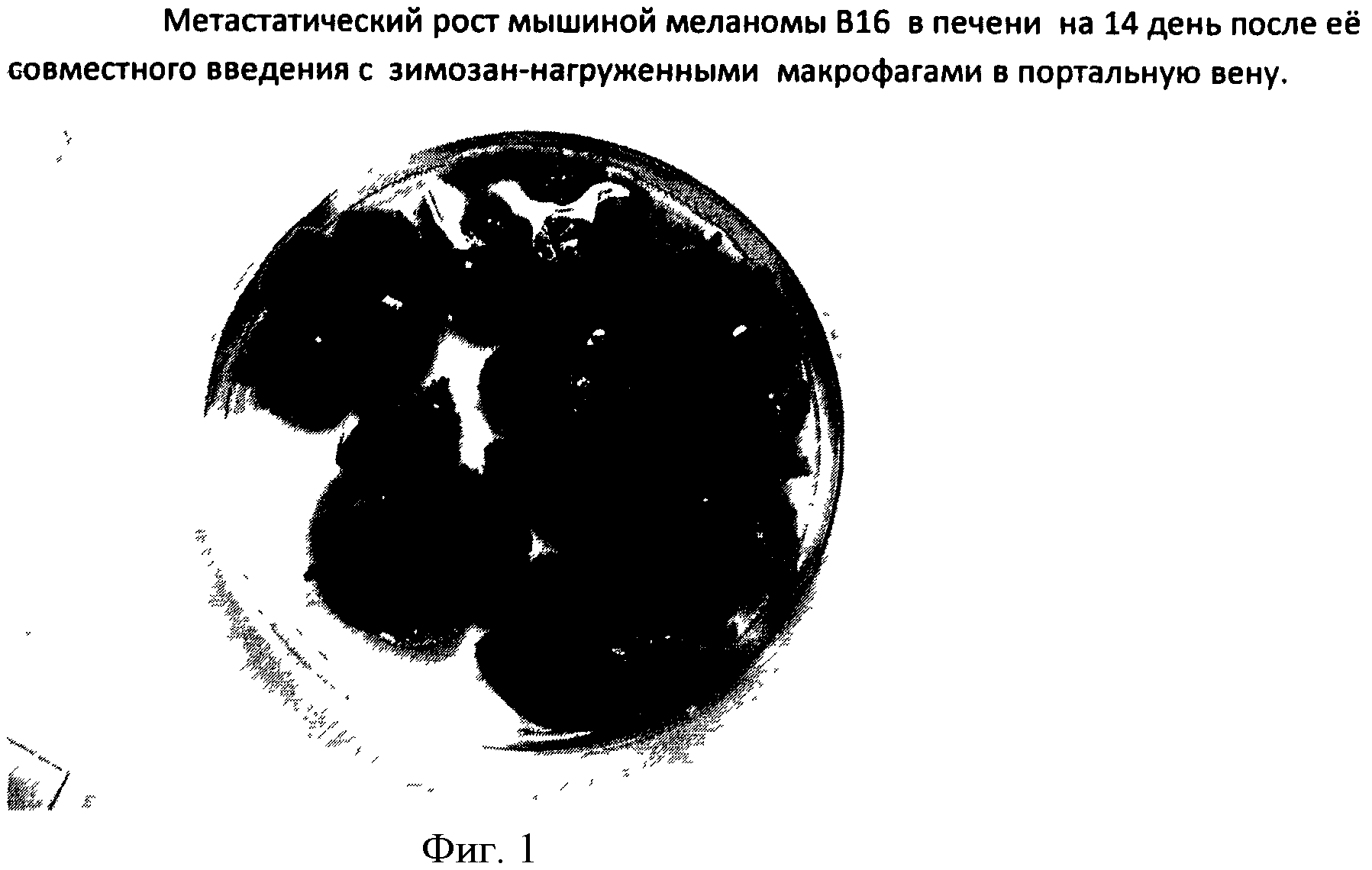
Макрофаги вводились совместно с клетками злокачественной меланомы В16 в портальную вену мышки. Результат регистрировали на 14 день. Оценивался общий вес и относительное число метастазов в печени. Результаты представлены в табл.1 и на фиг.1 и фиг.2
Предложенный способ парентерального введения лекарственного препарата зимозана, инкорпорированного в условиях «ex vivo» в аутологичные макрофаги (фагоциты), позволяет увеличить количество активированных макрофагов в печени.
Основным преимуществом таких зимозаннагруженных макрофагов является:
1) Отсутствие возможности этих «нагруженных» клеток формировать макро- и микротромбы;
2) Учитывая анатомо-физиологические особенности печени, макрофаги в течение достаточно продолжительного времени будут зафиксированы в ее паренхиме, поскольку она является основным естественным резервуаром для клеток системы мононуклеарных фагоцитов.


|