Результат интеллектуальной деятельности: ПРИМЕНЕНИЕ РЕКОМБИНАНТНОГО АНАЛОГА ВОДОРАСТВОРИМОГО ДОМЕНА БЕЛКА LYNX1 ДЛЯ ТОРМОЖЕНИЯ РОСТА КЛЕТОК КАРЦИНОМ
Вид РИД
Изобретение
Изобретение относится к медицине и биологии, к области экспериментальной онкологии. Способ может быть использован для торможения роста и терапии опухолей, в том числе в клинике.
Онкологические заболевания являются второй по распространенности причиной смерти населения после заболеваний сердечно-сосудистой системы, как в России, так и в мире, поэтому поиск новых эффективных стратегий терапии опухолей входит в список приоритетных проблем современной медицины. В настоящее время для торможения роста опухолей используют как классические химиотерапевтические препараты, так и препараты, целенаправленно воздействующие на молекулярную мишень, контролирующую рост опухоли.
Известно, что с употреблением никотина (табака) связано развитие рака головы, шеи, груди, легкого, поджелудочной железы, толстой кишки, желудка и мочевого пузыря. Активация никотинового ацетилхолинового рецептора альфа7 типа (а7-nAChR) никотином стимулирует пролиферацию раковых клеток, запуская, в свою очередь, различные внутриклеточные сигнальные пути, способствующие пролиферации опухолевых клеток [Egleton RD, Brown KC, Dasgupta P. (2008). Trends Pharmacol Sci. 29:151-8]. Таким образом, модуляторы nAChR могут выступать в качестве прототипов новых эффективных таргетных противоопухолевых препаратов.
Известен способ торможения роста опухолей с использованием антагонистов (нейротоксинов), действующих на а7-nAChR [Grozio A, Paleari L, Catassi A, Servent D, Cilli M, Piccardi F, Paganuzzi M, Cesario A, Granone P, Mourier G, Russo P. (2008) Int. J. Cancer. 122(8):1911-5; Zhang H. (2016) Drug Design, Development and Therapy. 10:3867-72; Trombino S, Cesario A, Margaritora S, Granone P, Motta G, Falugi C, Russo P. (2004) Cancer Res. 64(1):135-45]. Недостатком этого способа является необратимость связывания нейротоксинов с рецептором, их низкая специфичность и высокая системная токсичность.
В организме человека обнаружен ряд трехпетельных пептидов, гомологичных по пространственной структуре токсинам змей, и воздействующих на никотиновые ацетилхолиновые рецепторы. Примером таких пептидов может быть мембранозаякоренный белок Lynx1 [Miwa JM, Ibanez-Tallon I, Crabtree GW, Sánchez R, Sali A, Role LW, Heintz N. (1999) Neuron. 23:105-114]. Известно, что нокдаун белка Lynx1 способствует увеличению скорости роста клеток карциномы легкого А549, в то время как гиперэкспрессия мембранозаякоренного белка Lynx1 в клетках А549, наоборот тормозит пролиферацию клеток А549 [Fu XW, Song PF, Spindel ER. (2015) Int Immunopharmacol. 29:93-98]. Показано, что рекомбинантный аналог водорастворимого домена Lynx1 человека (SEQ №1) является модулятором α7-nAChR [Lyukmanova EN, Shenkarev ZO, Shulepko MA, Mineev KS, D'Hoedt D, Kasheverov IE, Filkin SY, Krivolapova AP, Janickova H, Dolezal V, Dolgikh DA, Arseniev AS, Bertrand D, Tsetlin VI, Kirpichnikov MP. (2011) J Biol Chem. 286:10618-10627]. Однако применение рекомбинантного аналога водорастворимого домена Lynx1 (SEQ №1) для торможения роста клеток опухолей никем ранее не предлагалось.
Наиболее близким к заявленному является способ торможения роста опухолевых клеток А549 при гиперэкспрессии в них мембранозаякоренного белка Lynx1 с помощью лентивирусной трансфекции [Fu XW, Song PF, Spindel ER. (2015) Int Immunopharmacol. 29:93-98]. Однако данный способ подразумевает применение для торможения роста клеток с помощью полноразмерного мембранозаякоренного Lynx1, что делает практически невозможным его применение в терапевтических целях.
Таким образом, технической проблемой, на решение которой направлено заявляемое изобретение, является создание нового способа торможения роста опухолей с использованием рекомбинантного белка водорастворимого домена Lynx1 (SEQ №1). Поставленная техническая проблема достигается за счет применения рекомбинантного аналога водорастворимого домена Lynx1 (SEQ №1) для торможения роста клеток опухоли, при этом остановка роста опухолей достигается за счет действия рекомбинантного аналога водорастворимого домена Lynx1 на nAChR α7 типа.
Рекомбинантный аналог водорастворимого домена Lynx1 (SEQ №1) получают в бактериальной системе экспрессии, при которой белок ренатурируют из цитоплазматических телец включения E. coli [М.А. Шулепко, Е.Н. Люкманова, И.Е. Кашеверов, Д.А. Долгих, В.И. Цетлин, М.П. Кирпичников. (2011) Биоорг. хим., 37(5): 609-615].
Изобретение иллюстрируют графические материалы:
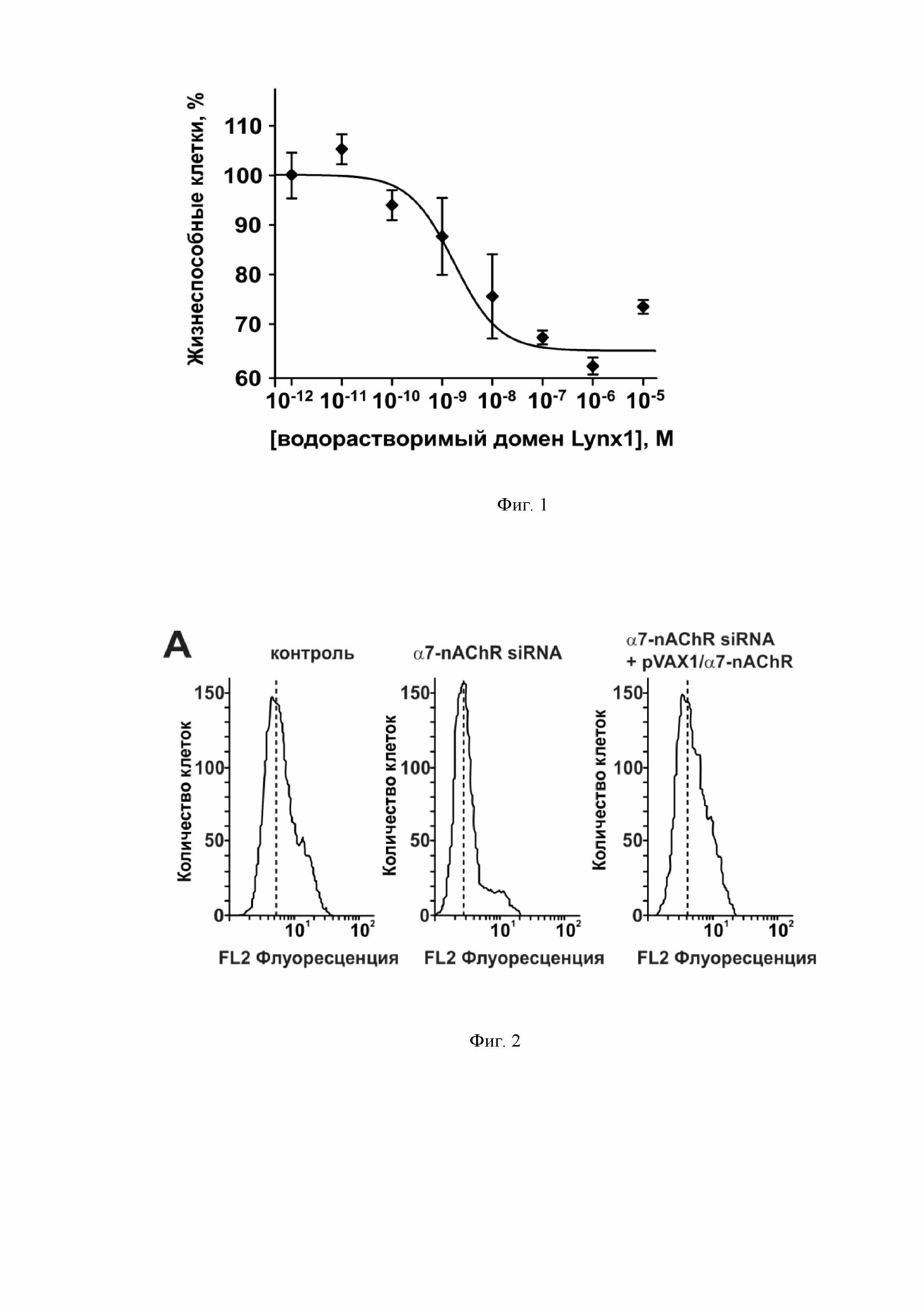
На фиг. 1 представлены данные по влиянию рекомбинантного аналога водорастворимого домена Lynx1 на жизнеспособность клеток карциномы легкого А549. Клетки высевают за 24 часа до эксперимента на 96-луночный культуральный планшет, затем инкубируют с рекомбинантным аналогом водорастворимого домена Lynx1 в течение 72 часов с заменой среды каждые сутки. Жизнеспособность опухолей определяют с помощью WST-1-теста.
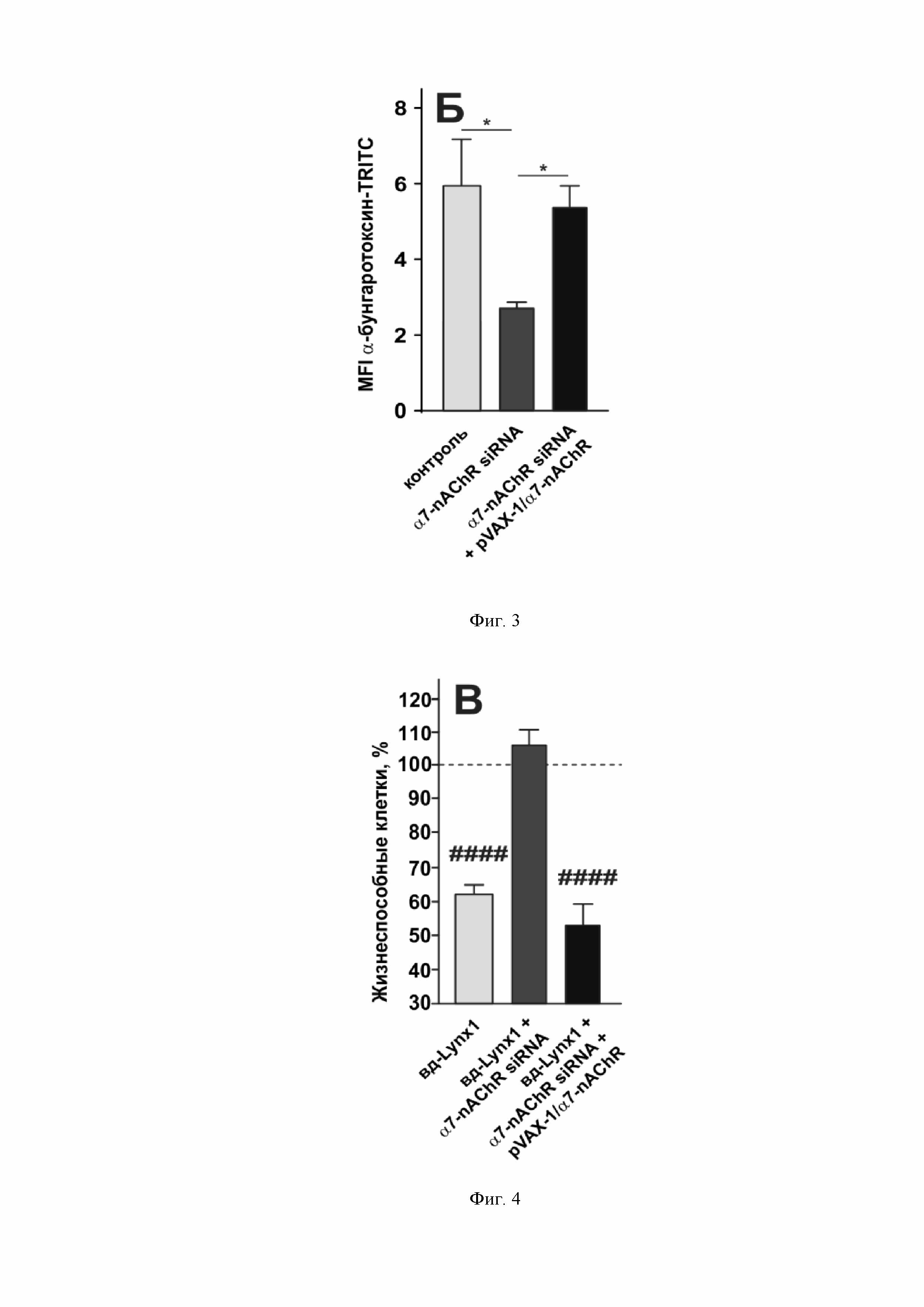
На фиг. 2, 3, 4 представлены данные по антипролиферативной активности рекомбинантного аналога водорастворимого домена Lynx1 на клетках карциномы легкого А549 после нокдауна в них экспрессии α7-nAChR при помощи интерферирующей РНК. Клетки высевают в 6-луночный культуральный планшет, трансфицируют интерферирующими РНК (siRNA), либо интерферирующими РНК и плазмидой, кодирующей ген полноразмерного α7-nAChR (pVAX1/α7-nAChR), после чего анализируют экспрессию α7-nAChR на проточном цитометре (А – репрезентативное распределение экспрессии α7-nAChR в популяции клеток, Б – подсчет медианы флуоресценции (MFI) α-бунгаротоксина) и инкубируют с рекомбинантным аналогом водорастворимого домена Lynx1 (вд-Lynx1) в течение 72 часов с заменой среды каждые сутки. Жизнеспособность опухолей определяют с помощью WST-1-теста (В). * (p<0.05) достоверное отличие между группами данных согласно одностороннему тесту ANOVA с последующим Dunnet's/hoc тестом. #### (p<0.05) означает разницу между контрольными и обработанными вд-Lynx1 клетками согласно двухстороннему t-тесту, количество жизнеспособных контрольных клеток показано пунктирной линией (100 %).
Изобретение иллюстрируют примеры.
Пример 1. Изобретение раскрывается на примере клеток карциномы легкого А549. Клетки культивируются в питательной среде DMEM c добавлением 10% (по объему) эмбриональной бычьей сыворотки и 2мМ глутамина и 25 мМ HEPES. Клетки А549 культивируют в культуральных флаконах объемом 75 мл и пересаживают минимум 2 раза в неделю. Клетки высевают в лунки культурального 96-луночного планшета (5000 клеток на лунку), через сутки добавляют различные концентрации рекомбинантного аналога водорастворимого домена Lynx1 (SEQ №1) и инкубируют 72 часа с заменой среды каждые сутки. Затем определяют жизнеспособность клеток А549 при помощи теста на активность митохондриальной сукцинатдегидрогеназы (WST-1-тест). Для этого, к клеткам добавляют субстрат митохондриальной сукцинатдегидрогеназы WST-1 и переносчик электронов 1-метокси-5-метилфеназин метилсульфат (конечная концентрация составляет 1 мМ WST-1 и 20 мкМ 1-метокси-5-метилфеназин метилсульфата) и инкубируют в течение 4 часов. WST-1 в митохондриях с неповрежденной мембраной при этом восстанавливается сукцинатдегидрогеназой до растворимого формазана. После инкубации определяют поглощение в лунках при 450 нМ с выравниванием на фон при 655 нМ. Пример показывает, что рекомбинантный аналог водорастворимого домена Lynx1 эффективно ингибирует рост клеток А549 до 65,3±1,1 % от контроля при 72-часовой инкубации с полумаксимальной эффективной концентрацией в 2,3±0,4 нМ (фиг. 1).
Пример 2. Изобретение раскрывается на примере клеток А549. Клетки высевают в 6-луночный культуральный планшет и через 24 часа трансфицируют 1 мкг интерферирующих РНК к nAChR α7 типа (GGAAGCUUUACAAGGAGCUGGUCAA и UUGACCAGCUCCUUGUAAAGCUUCC), либо 1 мкг интерфирирующих РНК к α7-nAChR и 10 мкг плазмиды pVAX1/α7-nAChR, которая содержит ген полноразмерного α7-nAChR. Клетки после трансфекции инкубируют 48 часов, затем часть клеток высевают на лунки 96-луночного культурального планшета (5000 клеток на лунку) и инкубируют в течении 72 часов с рекомбинантным аналогом водорастворимого домена Lynx1 (SEQ №1), а другую часть клеток инкубируют с флуоресцентно-меченным α-бунгаротоксином и анализируют на проточном цитометре FACSCalibur для определения уровня экспрессии функциональных α7-nAChR на поверхности клеток. Трансфекция клеток интерферирующими РНК приводит к значительному снижению уровня экспрессии в клетках А549 α7-nAChR, а ко-трансфекция клеток с интерферирующими РНК и плазмидой pVAX1/α7-nAChR полностью восстанавливает уровень экспрессии α7-nAChR в клетках практически до контрольного уровня (фиг. 2). Нокдаун экспрессии α7-nAChR в клетках А549 приводит к полной отмене антипролиферативного эффекта рекомбинантного аналога водорастворимого домена Lynx1 (SEQ №1), в то время как восстановление экспрессии α7-nAChR в клетках сопровождается восстановлением антипролиферативного эффекта рекомбинантного аналога водорастворимого домена Lynx1 (SEQ №1) (фиг. 3). Пример показывает, что антипролиферативный эффект рекомбинантного аналога водорастворимого домена Lynx1 (SEQ №1) в клетках А549 осуществляется посредством взаимодействия с nAChR α7 типа.
--->
SEQ № 1
Met Leu Asp Cys His Val Cys Ala Tyr Asn Gly Asp Asn Cys Phe Asn Pro Met Arg Cys Pro Ala
1 5 10 15 20
Met Val Ala Tyr Cys Met Thr Thr Arg Thr Tyr Tyr Thr Pro Thr Arg Met Lys Val Ser Lys Ser Cys
25 30 35 40 45
Val Pro Arg Cys Phe Glu Thr Val Tyr Asp Gly Tyr Ser Lys His Ala Ser Thr Thr Ser Cys Cys Gln
50 55 60 65
Tyr Asp Leu Cys Asn Gly
70
<---