Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ СИЛАНОЛОВ ИЗ ГИДРОСИЛАНОВ
Вид РИД
Изобретение
Изобретение относится к химической технологии кремнийорганических соединений, конкретно к способу получения силанолов и силоксанолов, широко используемых в качестве реагентов для синтеза полимеров заданной архитектуры [V. Chandrasekhar, R. Boomishankar, S. Nagendran, Chem. Rev. 2004, 104, 5847; A. Shimojima, K. Kuroda, J. Sol-Gel Sci. Technol. 2008, 46, 307; Q. Zhou, S. Yan, С.C. Han, P. Xie, R. Zhang, Adv. Mater. 2008, 20, 2970].
Способ по изобретению позволяет селективно получать силанолы и силоксанолы из соответствующих гидросиланов и силоксанов в довольно мягких условиях с использованием коммерчески доступной окислительной системы.
Известны способы получения силанолов, в которых используется гидролиз хлор- или алкоксисиланов. Однако такие способы очень неудобны с технологической точки зрения, так как для их реализации необходим строгий контроль условий реакции, в частности, значения pH реакционной среды, так как при несоблюдении требуемых условий силанолы легко конденсируются, что приводит к значительному снижению выхода целевых продуктов [Е.G. Rochow, W.F. Gilliam, J. Am. Chem. Soc. 1941, 63, 798; R.O. Sauer, J. Am. Chem. Soc. 1944, 66, 1707; L.J. Tyler, J. Am. Chem. Soc. 1955, 77, 770; S.M. Sieburth, W. Mu, J. Org. Chem. 1993, 58, 7584; K. Hirabayashi, A. Mori, T. Hiyama. Tetrahedron Lett., 1997, 38, 461].
Известны способы получения силанолов, в которых используют окисление связи Si-H в гидросиланах с образованием Si-OH связи. В таких способах в качестве окислителей применяют соли серебра (I) [N. Duffaut, R. Calas, J.-C. Mac, Bull. Chem. Soc. Fr. 1959, 1971], гидропероксиды [L.H. Sommer, L.A. Ulland, G.A. Parker, J. Am. Chem. Soc. 1972, 94, 3469; Y. Nagai, K. Honda, T. Migita, J. Organomet. Chem. 1967, 8, 372], перманганаты [P.D. Lickiss, R. Lucas, J. Organomet. Chem. 1995, 521, 229], диоксираны [W. Adam, R. Mello, R. Curci, Angew. Chem., 1990, 102, 916; Y. Kawakami, Y. Sakuma, T. Wakuda, T. Nakai, M. Shirasaka, Y. Kabe. Organometallics. 2010, 29, 3281-3288], оксид осмия [К. Valliant-Saunders, E. Gunn, G. R. Shelton, D.A. Hrovat, W.T. Borden, J.M. Mayer, Inorg. Chem., 2007, 46, 5212], оксазиридины [M. Cavicchioli, V. Montanari, G. Resnati, Tetrahedron Lett., 1994, 35, 6329], озон [L. Spialter, J.D. Austin, Inorg. Chem., 1966, 5, 1975; L. Spialter, J.D. Austin, J. Am. Chem. Soc., 1965, 87, 4406; L. Spialter, L. Pazdernik, S. Bernstein, W.A. Swansiger, G.R. Buell, M.E. Freeburger, J. Am. Chem. Soc., 1971, 93, 5682; R.J. Ouellette, D.L. Marks, J. Organomet. Chem., 1968, 11, 407] и другие реагенты. Главным недостатком способов, использующих окисление гидросиланов перечисленными окислителями, также является побочная реакция конденсации образующихся целевых продуктов, которая приводит к снижению их выхода.
Известен ряд способов получения силанолов, где используют окисление Si-H связи в гидросиланах, катализируемое металлами. Известно гидролитическое окисление гидросиланов, катализируемое такими металлами, как Rh, Ir-, Ru-, Ag-, Cu-, Cr-, Re-, Pt- и Au [M. Shi, K.M. Nicholas, J. Chem. Research, 1997, 400-401; Y. Lee, D. Seomoon, S. Kim, H. Han, S. Chang, P.H. Lee, J. Org. Chem., 2004, 69, 1741; 
 V. Polo, R. Lalrempuia,
V. Polo, R. Lalrempuia,  L.A. Oro, Chem. Cat. Chem., 2014, 6, 1691-1697; M. Aliaga-Lavrijsen, М. Iglesias, A. Cebollada, K. Garces, N. Garcia, P.J. Sanz Miguel, F.J. Fernandez-Alvarez, J.J. Perez-Torrente, L.A. Oro, Organometallics, 2015, 34 (11), 2378-2385; M. Lee, S. Ko, S. Chang, J. Am. Chem. Soc., 2000, 122, 12011-12012; K. Mori, M. Tano, T. Mizugaki, K. Ebitani, K. Kaneda, New J. Chem., 2002, 26, 1536-1538; E. Choi, C. Lee, Y. Na, S. Chang, Org. Lett., 2002, 4, 2369-2371; T. Mitsudome, S. Arita, H. Mori, T. Mizugaki, K. Jitsukawa, K. Kaneda, Angew. Chem., 2008, 120, 8056-8058; U. Schubert, C. Lorenz, Inorg. Chem. 1997, 36, 1258-1259; K. Motokura, D. Kashiwame, A. Miyaji, T. Baba. Org. Lett., 2012, 14(10), 2642-2645]. Гидролитическим окислением получен целый ряд органосиланолов разнообразной структуры с довольно высокими выходами, но существенным недостатком указанных процессов является необходимость использования дорогих или недоступных катализаторов.
L.A. Oro, Chem. Cat. Chem., 2014, 6, 1691-1697; M. Aliaga-Lavrijsen, М. Iglesias, A. Cebollada, K. Garces, N. Garcia, P.J. Sanz Miguel, F.J. Fernandez-Alvarez, J.J. Perez-Torrente, L.A. Oro, Organometallics, 2015, 34 (11), 2378-2385; M. Lee, S. Ko, S. Chang, J. Am. Chem. Soc., 2000, 122, 12011-12012; K. Mori, M. Tano, T. Mizugaki, K. Ebitani, K. Kaneda, New J. Chem., 2002, 26, 1536-1538; E. Choi, C. Lee, Y. Na, S. Chang, Org. Lett., 2002, 4, 2369-2371; T. Mitsudome, S. Arita, H. Mori, T. Mizugaki, K. Jitsukawa, K. Kaneda, Angew. Chem., 2008, 120, 8056-8058; U. Schubert, C. Lorenz, Inorg. Chem. 1997, 36, 1258-1259; K. Motokura, D. Kashiwame, A. Miyaji, T. Baba. Org. Lett., 2012, 14(10), 2642-2645]. Гидролитическим окислением получен целый ряд органосиланолов разнообразной структуры с довольно высокими выходами, но существенным недостатком указанных процессов является необходимость использования дорогих или недоступных катализаторов.
Известен способ получения силанолов окислением гидросиланов, которое проводят при нагревании в атмосфере диоксида углерода, который в данном случае является окислителем, и используют каталитическую систему, состоящую из моногидрата ацетата меди Cu(OAc)2⋅H2O и бис(дифенилфосфино)бензола. Так, для получения дифенилметилсиланола указанным способом, перемешивают смесь дифенилметилсилана (1.0 ммоль), Cu(OAc)2⋅H2O (Cu: 1.0×10-2 ммоль), 1,2-бис(дифенилфосфино)бензола (1.5×10-2 ммоль) и 1,4-диоксана (2 мл) в атмосфере CO2 при 100°C в течение 16 часов и затем добавляют в реакционную массу 0.2 мл воды [K. Motokura, D. Kashiwame, A. Miyaji, Т. Baba, Org. Lett., 2012, 14(10), 2642-2645]. Выход дифенилметилсиланола составляет 90%. Аналогичным способом получают из соответствующих гидросиланов фенилдиметилсиланол с выходом 90%, триэтилсиланол и триэтоксисиланол с выходом 60%. Недостатками способа являются использование дорогостоящего 1,2-бис(дифенилфосфино)бензола и необходимость проведения реакции в атмосфере диоксида углерода. Данный способ наиболее близок к заявляемому способу по существенным признакам и был выбран в качестве прототипа.
Задачей заявляемого изобретения являлась разработка способа получения силанолов окислением гидросиланов, использующего доступную и дешевую окислительную систему и обеспечивающего высокий выход целевого продукта.
Задача решается заявляемым способом получения силанолов общей формулы R1R2SiOH из гидросиланов общей формулы R1R2R3SiH, где каждый из заместителей R1, R2 и R3 независимо обозначает C1-C3 алкил и/или C1-C3алкилсилокси, включающий окисление гидросилана окислительной системой, состоящей из трет-бутилгидропероксида и соли двухвалентной меди, например хлорида, оксалата, ацетата, ацетилацетоната или карбоната, причем мольное соотношение исходного гидросилана и соли меди (II) составляет от 1:0.005 до 1:1, а соотношение гидросилана и трет-бутилгидропероксида составляет от 1:0.5 до 1:5, окисление проводят в органическом растворителе при температуре от 20°C до 100°C, а в качестве органического растворителя используют ацетонитрил или бензол.
В общем виде заявляемый способ может быть представлен суммарной схемой:
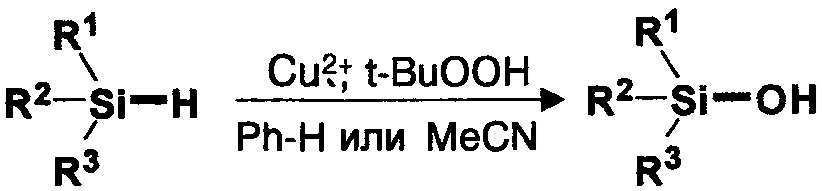
R1, R2, R3 обозначает C1-C3 алкил и/или C1-C3алкилсилокси, анионом соли меди является хлорид, оксалат, ацетат или карбонат-ион.
В отличие от прототипа, где для получения силанолов из гидросиланов используют дорогостоящую окислительную систему, включающую моногидрат ацетата меди Cu(OAc)2⋅H2O и бис(дифенилфосфино)бензол, в заявляемом способе используют окислительную систему, состоящую из дешевых и коммерчески доступных реагентов - карбоната меди и трет-бутилгидропероксида. Кроме того, заявляемый способ не требует проведения процесса в атмосфере диоксида углерода. При этом, выход целевого продукта - триэтилсиланола - составляет 90%, тогда как в способе-прототипе выход триэтилсиланола 60%.
Техническим результатом изобретения является новый способ получения силанолов окислением гидросиланов, использующий доступную и дешевую окислительную систему и обеспечивающий высокий выход целевых продуктов.
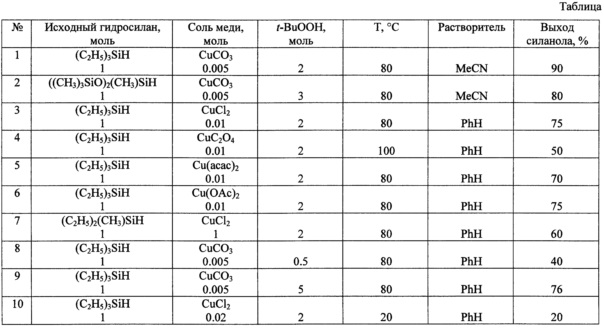
Изобретение иллюстрируется приведенными ниже примерами его осуществления, результаты которых представлены в таблице.
Пример 1. Синтез триэтилсиланола
Смесь 2 г (17.199 ммоль) триэтилсилана, 4.44 г (34.39 ммоль) трет-бутоксипероксида, 0.0106 г (0.086 ммоль) CuCO3 и 20 мл ацетонитрила перемешивают в круглодонной колбе при 80°C в течение 9 ч. Растворитель отгоняют на роторном испарителе (150-200 мбар, Tбани=40°C). Остаток растворяют в гексане (50-60 мл), далее фильтруют через тонкий слой (0.4-0.5 см) целита (Celite 545) и отгоняют гексан на роторном испарителе (250-300 мбар, Tбани=40°C). Выход триэтилсиланола - 90%.
Примеры 2-10, представленные в таблице, осуществляют по методике, аналогичной описанной в примере 1.