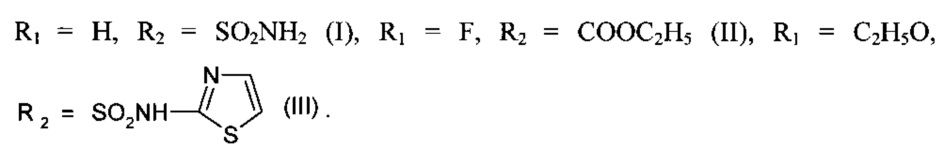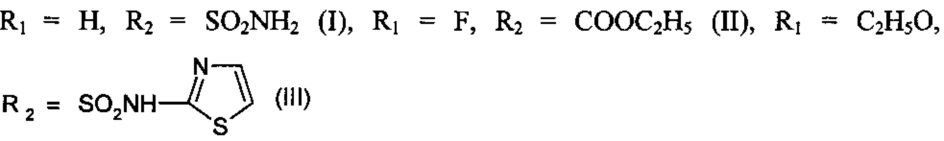Результат интеллектуальной деятельности: Способ получения N-ариламидов ароилпировиноградных кислот
Вид РИД
Изобретение
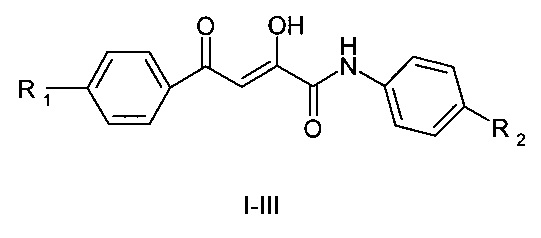
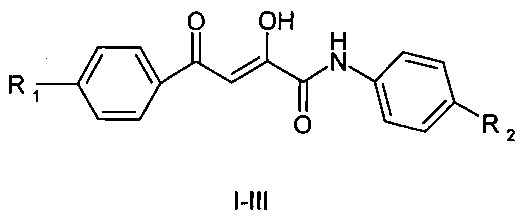
Изобретение относится к способу получения N-ариламидов ароилпировиноградных кислот общей формулы:
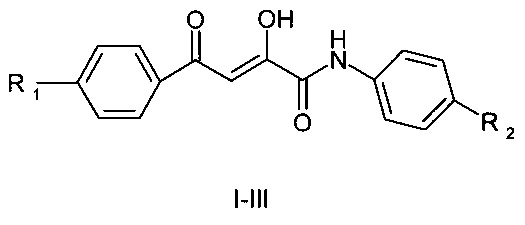
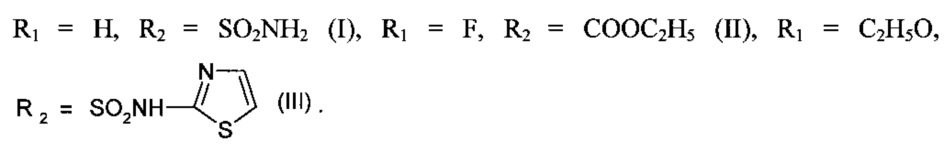
Известен способ синтеза N-ариламидов ароилпировиноградных кислот, заключающийся во взаимодействии 5-арил-2,3-дигидрофуран-2,3-дионов с ариламинами в среде абсолютного толуола, диоксана и других инертных растворителей [1-3]. Недостатком данного способа является труднодоступность 5-арил-2,3-дигидрофуран-2,3-дионов, которые образуются путем циклизации ароилпировиноградных кислот под действием хлористого тионила или уксусного ангидрида. Полученные 5-арил-2,3-дигидрофуран-2,3-дионы представляют собой неустойчивые соединения, которые легко превращаются в исходные ароилпировиноградные кислоты под действием влаги воздуха, что существенно понижает выход и затрудняет синтез N-ариламидов ароилпировиноградных кислот.
Отличительной особенностью предлагаемого изобретения является синтез N-ариламидов ароилпировиноградных кислот при кипячении ариламинов с метиловыми эфирами ароилпировиноградных кислот в среде ледяной уксусной кислоты в течение 15-20 минут в присутствии безводного ацетата натрия по схеме:
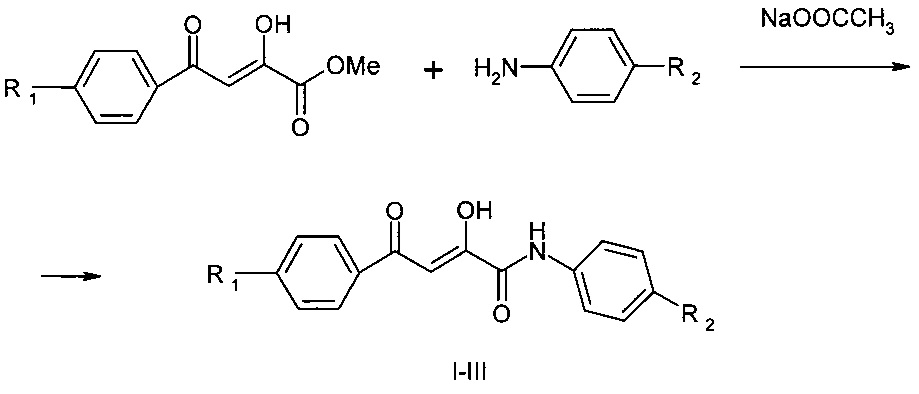
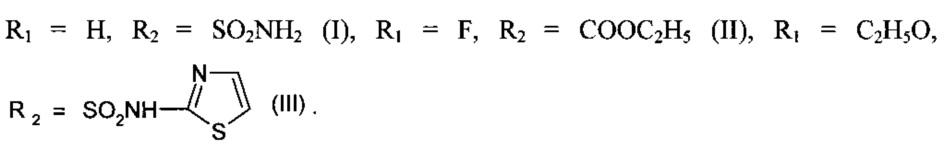
Предлагаемый способ позволяет получать N-ариламиды ароилпировиноградных кислот с высоким выходом 73-81%, для чего не требуется сухих растворителей и токсичных реагентов, а также данный способ более удобен и прост в применении, так как отсутствует трудоемкая стадия получения 5-арил-2,3-дигидрофуран-2,3-дионов.
Синтезированные соединения представляют собой светло-желтые (I, II) или с зеленоватым оттенком (III) кристаллические вещества, растворимые в ДМФА, ДМСО, при нагревании - в диоксане, уксусной кислоте, нерастворимые в воде.
Структура соединений (I-III) доказана методами ИК, ЯМР 1H спектроскопии и масс-спектрометрии. Спектры ЯМР 1H записаны на приборе Bruker DRX 500 (500.13 МГц) в DMSO-d6 и Acetone-d6, внутренний стандарт - TMC. Масс-спектры получены на приборе Finnigan MAT INCOS-50 с энергией ионизации 70 эВ. ИК-спектры записаны на приборе Specord М-80 в пасте вазелинового масла. Элементный анализ проведен на приборе Perkin Elmer 2400. Температура плавления синтезированных соединений определена на приборе Melting Point М-565.
Пример 1. N-(4-Аминосульфонилфенил)амид 2-гидрокси-4-оксо-4-фенил-2-бутеновой кислоты (I). К 1.72 г (0.01 моль) 4-аминобензолсульфамида, растворенного при нагревании в 10 мл ледяной уксусной кислоты, добавляли 2.06 г (0.01 моль) метилового эфира бензоилпировиноградной кислоты и 0.82 г (0.01 моль) безводного ацетата натрия, растворенных в 15 мл ледяной уксусной кислоты. Реакционную смесь кипятили в течение 15 минут. Выпавший при охлаждении осадок отфильтровывали и перекристаллизовывали из диоксана. Выход 2.53 г (73%), т. пл. 220-222°C. ИК спектр, ν, см-1: 3380, 3280 (NH2, NH), 3144 (OH), 1710 (CONH), 1610 (С=O), 1380, 1152 (SO2). Спектр ЯМР 1H, δ, м. д. (Acetone-d6): 4.68 с (2Н, COCH2CO), 6.55 с (2Н, NH2), 7.30 с (1H, CH=), 7.61 т (2Н, Н-3, Н-5 аром.), 7.71 т (1Н, Н-4 аром.), 7.91, 7.93 д (2Н, Н-2, Н-6 аром., J=8.77 Гц), 8.09, 8.11 д (2Н, Н-3, Н-5 аром., J=8.77 Гц), 8.12, 8.13 д (2Н, Н-2, Н-6 аром., J=7.36 Гц), 10.15 с (1H, CONHC6H4), 15.65 уш. с (1H, OH). Масс-спектр: m/z 346 (17.42%) [M]+, m/z 77 (14.21%) [Ph]+, m/z 105 (18.52%) [PhCO]+, m/z 147 (100%) [C6H5COCH=C(OH)]+, m/z 156 (5.01%) [C6H4SO2NH2]+, m/z 172 (19.32%) [H2NC6H4SO2NH2]+. Найдено, %: С 55.36, 55.59; H 4.02, 4.12; N 8.01, 8.18; S 9.18, 9.34. C16H14N2O5S. Вычислено, %: С 55.48; H 4.07; N 8.09; S 9.26. М 346.36.
Пример 2. N-(4-Этоксикарбонилфенил)амид 2-гидрокси-4-оксо-4-(4-фторфенил)-2-бутеновой кислоты (II). К 1.65 г (0.01 моль) этилового эфира 4-аминобензойной кислоты, растворенного при нагревании в 10 мл ледяной уксусной кислоты, добавляли 2.24 г (0.01 моль) метилового эфира 4-фторбензоилпировиноградной кислоты и 0.82 г (0.01 моль) безводного ацетата натрия, растворенных в 15 мл ледяной уксусной кислоты. Реакционную смесь кипятили в течение 15 минут. Выпавший при охлаждении осадок отфильтровывали и перекристаллизовывали из диоксана. Выход 2.71 г (76%), т. пл. 181-183°C. ИК спектр, ν, см-1: 3370 (NH), 3200 (OH), 1712 (CONH, COOEt), 1608 (C=O). Спектр ЯМР 1Н, δ, м. д., (DMSO-d6): 1.32 т (3Н, CH3CH2O), 4.30 к (2Н, CH3CH2O), 4.66 с (2Н, COCH2CO), 7.23 с (1Н, CH=), 7.43 т (2Н, Н-3, Н-5 аром.), 7.41, 7.43 д (2Н, Н-2, Н-6 аром., J=8.97 Гц), 7.98, 8.00 д (2Н, Н-3, Н-5 аром., J=8.97 Гц), 8.18 т (2Н, Н-2, Н-6 аром.), 10.96 с (1Н, CONHC6H4). Масс-спектр: m/z 357 (13.41%) [М]+, m/z 95 (6.51%) [FC6H4]+, m/z 123 (18.72%) [FC6H4CO]+, m/z 165 (100%) [FC6H4COCH=C(OH)]+ и [H2NC6H4COOEt]+. Найдено, %: С 63.75, 63.99; H 4.45, 4.56; N 3.86, 3.98. C19H16FNO5. Вычислено, %: С 63.86; Н 4.51; N 3.92. М 357.34.
Пример 3. N-[4-(Тиазол-2-ил)аминосульфонилфенил]амид 2-гидрокси-4-оксо-4-(4-этоксифенил)-2-бутеновой кислоты (III). К 2.55 (0.01 моль) 2-(4-аминобензолсульфамидо)тиазола, растворенного при нагревании в 10 мл ледяной уксусной кислоты, добавляли 2.50 г (0.01 моль) метилового эфира 4-этоксибензоилпировиноградной кислоты и 0.82 г (0.01 моль) безводного ацетата натрия, растворенных в 15 мл ледяной уксусной кислоты. Реакционную смесь кипятили в течение 20 минут. Выпавший при охлаждении осадок отфильтровывали и перекристаллизовывали из диоксана. Выход 3.84 г (81%), т. пл. 219-221°C. ИК спектр,ν, см-1: 3344 (2NH), 3100 (OH), 1704 (CONH), 1610 (С=O), 1380, 1152 (SO2). Спектр ЯМР 1Н, δ, м. д., (DMSO-d6): 1.36 т (3Н, CH3CH2O), 4.16 к (2Н, CH3CH2O), 4.58 с (2Н, COCH2CO), 6.82, 6.83 д (1Н, С5Нтиаз., J=4.60 Гц), 7.09, 7.11 д (2Н, Н-3, Н-5 аром., J=8.95 Гц), 7.16 с (1H, CH=), 7.25, 7.26 д (1H, С4Нтиаз., J=4.60 Гц), 7.79, 7.81 д (2Н, Н-2, Н-6 аром., J=8.80 Гц), 7.98, 7.99 д (2Н, Н-3, Н-5 аром., J=8.80 Гц), 8.06, 8.08 д (2Н, Н-2, Н-6 аром., J=8.95 Гц), 10.90 с (1Н, CONHC6H4), 12.72 с (1Н, SO2NH). Масс-спектр: m/z 472 (1%) [М-Н]+, m/z 121 (59.76%) [EtOC6H4]+, m/z 149 (98.30%) [EtOC6H4CO]+, m/z 156 (40.24%) [H2NC6H4SO2]+, m/z 191 (100%) [EtOC6H4COCH=C(OH)]+, m/z 218 (12.51%) [M-H2NC6H4SO2NHC3H2NS]+, m/z 255 (38.54%) [H2NC6H4SO2NHC3H2NS]+. Найдено, %: С 53.14, 53.39; H 3.98, 4.11; N 8.78, 8.95; S 13.63, 13.45. C21H19N3O6S2. Вычислено, %: С 53.27; H 4.04; N 8.87; S 13.54. М 473.53.
ЛИТЕРАТУРА
[1] Андрейчиков Ю.С., Милютин А.В., Крылова И.В., Сараево Р.Ф., Дормидонтова Е.В., Дровосекова М.П., Назметдинов Ф.Я., Колла В.Э. // Хим.-фарм. журн. 1990. Т. 24. №7. С. 33.
[2] Андрейчиков Ю.С., Налимова Ю.А., Тендрякова С.П., Виленчик Я.М. // ЖОрХ. 1978. Т. 14. Вып. 1. С. 160.
[3] Козлов А.П., Сажнев С.С., Козлова Г.А., Андрейчиков Ю.С. // ЖОрХ. 1996. Т. 32. Вып. 10. С. 1573.