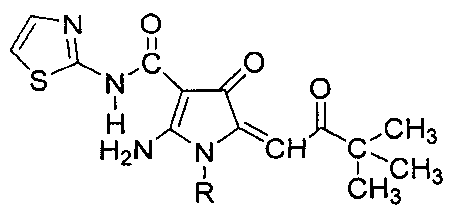
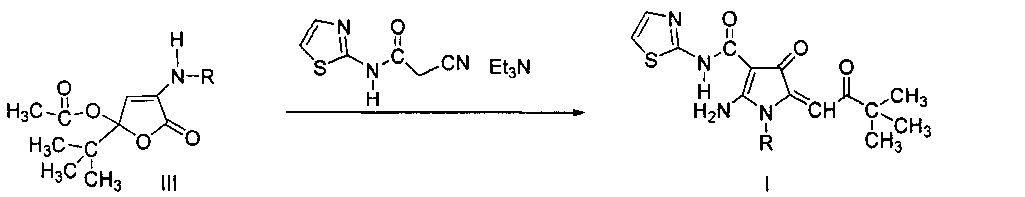
Результат интеллектуальной деятельности: 2-АМИНО-1-АРИЛ-5-(3,3-ДИМЕТИЛ-2-ОКСОБУТИЛИДЕН)-4-ОКСО-N-(ТИАЗОЛ-5-ИЛ)-4,5-ДИГИДРО-1Н-ПИРРОЛ-3-КАРБОКСАМИДЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ И АНТИРАДИКАЛЬНУЮ АКТИВНОСТЬ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ
Вид РИД
Изобретение
Изобретение относится к области медицины и может быть использовано для лечения или предупреждения роста опухолевых клеток.
Заявлены соединения формулы (I), имеющие структуру, родственную определенным природным и синтетическим аминопирролам, а также способ получения упомянутых соединений и фармацевтическая композиция на их основе.
В настоящее время имеются единичные исследования по изучению противоопухолевой активности у прототипов - 4-пивалоилзамещенных-2-пирролонов (Зыкова С.С., Козьминых В.О., Игидов Н.М. 2002. Синтез и фармакологическая активность 3-гидрокси-1,5-диарил-4-пивалоил-2,5-дигидро-2-пирролонов. Хим-фарм. журнал. 36(4): 23-26).
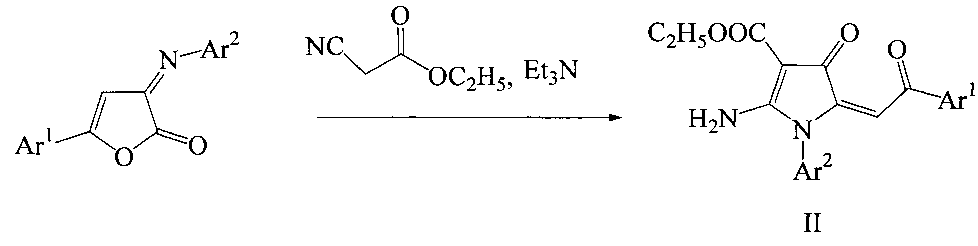
Известны ближайшие структурные аналоги заявляемых соединений, получаемые взаимодействием 5-арил-3-арилимино-3H-фуран-2-онов с этиловым эфиром циануксусной кислоты в присутствии триэтиламина, но их биологическая активность не изучалась [Харитонова С.С., Игидов Н.М., Захматов А.В., Рубцов А.Е. Химия иминофуранов VIII. Рециклизация 5-арил-3-арилимино-3H-фуран-2-онов под действием производных цианоуксусной кислоты // Журн. орган, химии. 2013. Т. 49. - Вып. 2. - С. 252-261].
Синтез ближайших структурных аналогов осуществляется по следующей схеме [Харитонова С.С., Игидов Н.М., Захматов А.В., Рубцов А.Е. Химия иминофуранов VIII*. Рециклизация 5-арил-3-арилимино-3Н- фуран-2-онов под действием производных цианоуксусной кислоты // Журн. орган, химии. 2013. Т. 49. - Вып. 2. - С. 252-261]:
Известны производные паклитаксела:
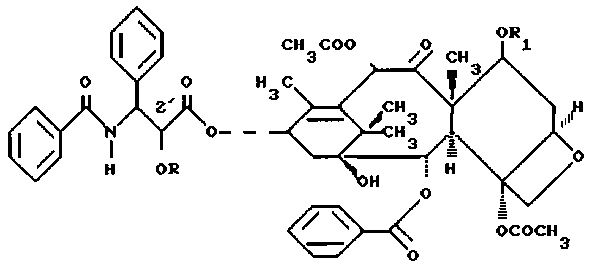
Известна фармацевтическая композиция (Таксол), обладающая противоопухолевой активностью, включающая активное вещество и фармацевтически приемлемый носитель (Кремофор), отличающаяся тем, что в качестве активного вещества содержит производное паклитаксела общей формулы I, указанной выше, в количестве 0,01-2500,0 мг (патент РФ №2059631, МПК C07D 305/14, A61K 31/195, опубл. 10.05.1996), ближайшие по технической сущности и принятые за прототипы.
Задачей предлагаемого изобретения является разработка способа получения не описанных ранее {2-амино-1-арил-5-(3,3-диметил-2-оксобутилиден)-4-оксо-4,5-дигидро-1H-пиррол-3-ил]-N-(тиазол-5-ил)карбоксамидов (Ia, б), проявляющих противоопухолевую и антирадикальную активность и обладающих более низкой токсичностью, чем противоопухолевый лекарственный препарат - Таксол.
Задачей изобретения является обеспечение соединений, обладающих повышенной противоопухолевой и антирадикальной активностью, а также пониженной токсичностью.
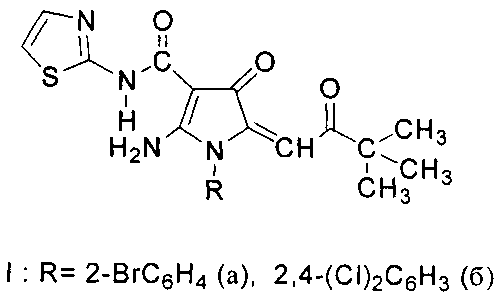
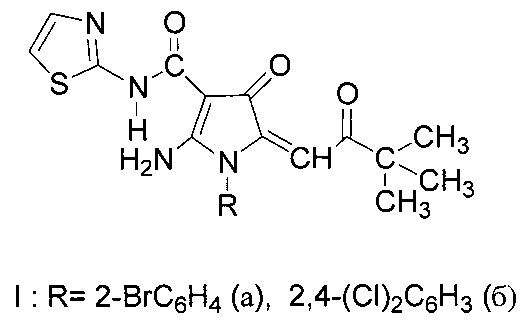
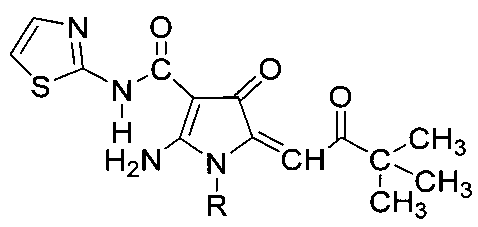
Заявлено 2-амино-1-арил-5-(3,3-диметил-2-оксобутилиден)-4-оксо-N-(тиазол-5-ил)-4,5-дигидро-1H-пиррол-3-карбоксамиды общей формулы Ia, б
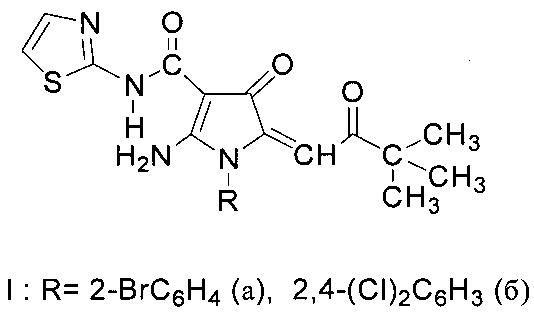
где R = 2-бромфенил(Ia); или 2,4-дихлорфенил (Iб), или его фармацевтические приемлемые соли, которые включают нетоксичные органические или неорганические соли, в частности гидрохлориды, сульфаты, гидросульфаты, нитраты, фосфаты, лактаты, ацетаты, цитраты, бензоаты, сукцинаты, тартраты и т.п. Предпочтительно, такие соли представляют собой гидрохлориды. Под термином "арил" подразумевается ароматическая моно- или полициклическая группа, предпочтительно моно- или бициклическая группа С6-С10, предпочтительно фенил или нафтил позволяют решить вышеуказанную задачу.
Также заявлен способ получения 2-амино-1-арил-5-(3,3-диметил-2-оксобутилиден)-4-оксо-N-(тиазол-5-ил)-4,5-дигидро-1H-пиррол-3-карбоксамидов общей формулы Ia, б
при котором 2-трет-бутил-4-(арил-амино)-2,5-дигидро-5-оксофуран-2-илацетата (III) и 0.42 г (0.0025 моль) 2-циано-N-(тиазол-2-ил)ацетамида в количестве 0.90-092 г (0.0025 моль) растворяют при нагревании в 90 мл бензола, при дальнейшем добавлении 0.25-0.42 г (0.0025-0.005 моль) триэтиламина и кипячении в течение 20-25 минут, выпавший осадок отфильтровывают и перекристаллизовывают из растворителя.
В качестве растворителя применяют бензол или этанол.
Отфильтрованный и перекристаллизованный осадок является получаемым соединением Ia или Iб.
Также заявлена фармацевтическая композиция, обладающая противоопухолевой и антирадикальной активностью, содержащая фармацевтически приемлемый наполнитель и активный ингредиент, в которой новым является то, что в качестве активного ингредиента она содержит соединение, имеющее общую формулу Ia или Iб.
Изобретение относится к производным пиррола, а именно к новым 2-амино-1-арил-5-(3,3-диметил-2-оксобутилиден)-4-оксо-N-(тиазол-5-ил)-4,5-дигидро-1H-пиррол-3-карбоксамидам формулы (Ia, б):
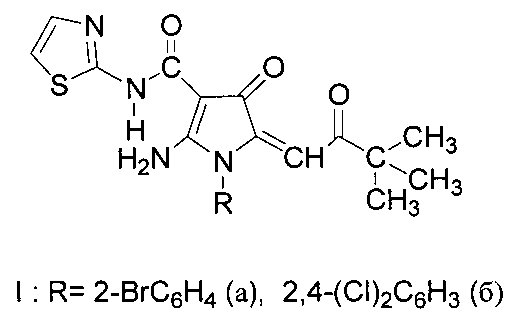
Заявляемые соединения Ia, б представляют собой слегка желтоватого цвета кристаллические вещества, растворимые в диметилсульфоксиде (ДМСО), диметилформамиде, трудно растворимые в бензоле, толуоле, не растворимые в гексане и в воде.
Соединения Ia и Iб проявляют выраженную антиоксидантную и противоопухолевую активность, превосходя препарат сравнения тролокс (антиоксидант) и Таксол (противоопухолевое средство) при более низкой токсичности и могут найти применение в медицине в качестве лекарственных препаратов.
Поставленная задача достигается взаимодействием 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов (III) с 2-циано-N-(тиазол-2-ил)ацетамидом в присутствии триэтиламина в среде бензола по схеме:
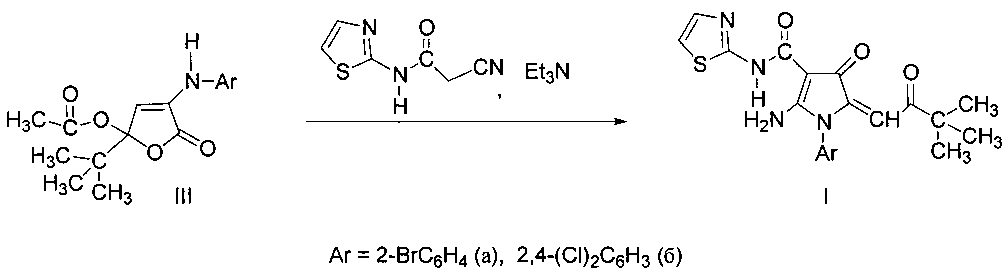
Синтез соединений-предшественников 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов (III) описан ранее [Тюнева А.В., Игидов Н.М., Корягина Н.Н., Бородин А.Ю., Захматов А.В., Макаров А.С., Токсарова Ю.С., Рубцов А.Е. Химия иминофуранов. VII. Внутримолекулярная циклизация 2-N-арилзамещенных производных 4-арил-4-оксобут-2-еновых и 2-амино-5,5-диметил-4-оксогекс-2-еновых кислот // Журн. орган, химии. 2011. Т. 46. Вып. 2. с. 258-264].
Техническим результатом является наличие противоопухолевой и антирадикальной активности соединений, а также наличие низкой токсичности.
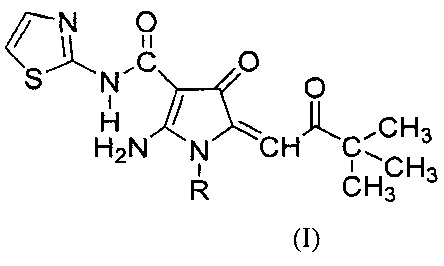
Технический результат достигается обеспечением соединения общей формулы I:
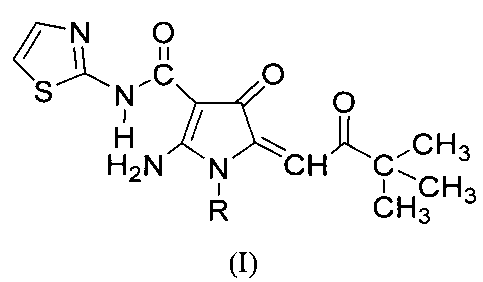
где R представляет собой С6-С10 арил, необязательно замещенный одним или более атомами галогена, или его фармацевтические приемлемые соли.
R представляет собой фенил или нафтил.
Фенил замещен одним или более атомами галогена.
Фенил замещен одним или двумя атомами брома.
Фенил замещен одним или двумя атомами хлора.
Технический результат также достигается способом получения соединения общей формулы I:
где R представляет собой С6-С10 арил, необязательно замещенный одним или более атомами галогена, или его фармацевтически приемлемые соли, который включает взаимодействие 4-R-амино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетата (III) и 2-циано-N-(тиазол-2-ил)ацетамида в присутствии триэтиламина, согласно следующей схеме:
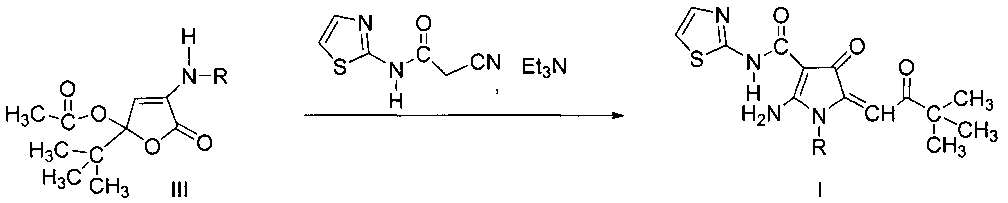
4R-амино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетат (III) и 2-циано-N-(тиазол-2-ил)ацетамид берут в эквимольном количестве.
Триэтиламин берут в количестве от эквимольного до двухкратного избытка по отношению к 2-циано-N-(тиазол-2-ил)ацетамиду и 4R-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетату.
Взаимодействие осуществляют в среде бензола.
Образовавшийся продукт соединения формулы (1) выпадает в виде осадка.
Осадок перекристаллизовывают.
Технический результат также достигается обеспечением фармацевтической композиции, обладающей противоопухолевой и антирадикальной активностью, содержащей фармацевтически приемлемый наполнитель и активный ингредиент в фармацевтически активном количестве, причем в качестве активного ингредиента содержит соединение, имеющее общую формулу I, или его фармацевтически приемлемые соли.
Технический результат также достигается применением соединения для получения лекарственных препаратов для лечения онкологических заболеваний.
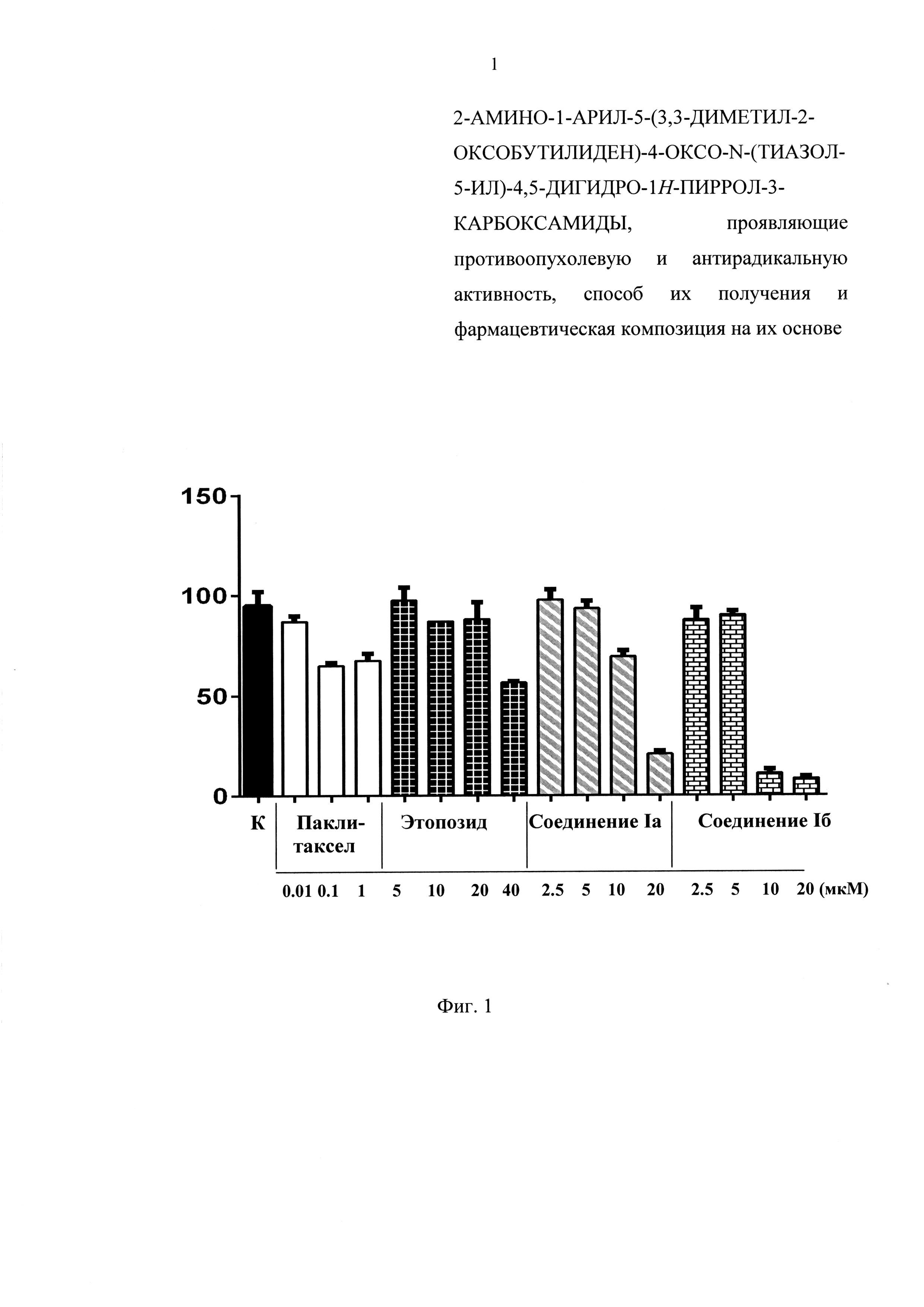
Противоопухолевая активность соединений представлена на фигурах 1 и 2.
На фиг. 1 представлен график, на котором показана противоопухолевая активность соединений Ia, Iб и препаратов сравнения - паклитаксела и этопозида - по отношению к клеткам остеосаркомы человека U2 OS (48 часов инкубации с препаратами), где по оси ординат - количество жизнеспособных клеток (в %) от контроля "К", по оси абсцисс - концентрация исследуемых соединений и препаратов сравнения паклитаксела и этопозида (в мкМ).
На фиг. 2 показано дозозависимое накопление клеток в М-фазе клеточного цикла (увеличение клеток округлой формы) после 24-часовой инкубации нормальных (фибробласты BJ) и опухолевых клеточных линий (HeLa и U2 OS) с соединением Ia.
Примеры предпочтительного осуществления изобретения.
Пример 1. Получение заявляемого соединения (Ia):
0.92 г (0.0025 моль) 2-трет-бутил-4-(2-бромфениламино)-2,5-дигидро-5-оксофуран-2-илацетата (III) и 0.42 г (0.0025 моль) 2-циано-N-(тиазол-2-ил)ацетамида растворяли при нагревании в 90 мл бензола, добавляли 0.25 г (0.0025 моль) триэтиламина, кипятили в течение 20 минут. Выпавший осадок отфильтровывали и перекристаллизовывали из бензола. Получали 0.66 г (64%) кристаллического вещества (II) с Тпл 173-174°С. C20H19BrN4O3S. ИК-спектр, ν/см-1, вазелиновое масло: 3305 (NH), 1660 (С=O), 1623, 1543 (С=O, С=С). Спектр ЯМР 1Н, δ, м.д.: 0.89 с (9Н, (СН3)3С), 1.10 с (9Н, (СН3)3С), 5.53 с (1Н, СН), 6.55 с (1Н, СН), 7.20-7.91 м (6Н, C6H4, C3H2NS), 8.49 с (1Н, NH), 8.79c (1H, NH), 11.33 c (1H, NH).
Пример 2. Получение заявляемого соединения (Iб):
0.90 г (0.0025 моль) 2-трет-бутил-4-(2,4-дихлорфениламино)-2,5-дигидро-5-оксофуран-2-илацетата (III) и 0.42 г (0.0025 моль) 2-циано-N-(тиазол-2-ил)ацетамида растворяли при нагревании в 90 мл бензола, добавляли 0.42 г (0.005 моль) триэтиламина, кипятили в течение 25 минут. Выпавший осадок отфильтровывали и перекристаллизовывали из этанола. Подбор растворителя осуществляют эмпирическим путем.
Получали 0.90 г (75%) кристаллического вещества (Iб) с Тпл 270-271°С. C20H18Cl2N4O3S. ИК-спектр, ν/см-1, вазелиновое масло: 3319 (NH), 1655 (С=O), 1621, 1536 (С=O, С=С). Спектр ЯМР 1Н, δ, м.д.: 0.92 с (9Н, (СН3)3С), 1.09 с (9Н, (СН3)3С), 5.67 с (1Н, СН), 6.47 с (1Н, СН), 7.07-7.85 м (5Н, С6Н3, C3H2NS), 8.44 уш. с (1Н, NH), 8.69 уш. с (1Н, NH), 11.18 уш. с (1Н, NH).
Полученные соединения (Ia, б) представляют собой слегка желтоватого цвета кристаллические вещества, растворимые в ДМСО, диметилформамиде, трудно растворимые в бензоле, толуоле, не растворимые в гексане и в воде.
Пример 3. Острую токсичность при внутрибрюшинном введении определяли на белых нелинейных мышах-самцах массой 18-22 г. Описываемые соединения Ia и Iб и препарат сравнения (Таксол) вводили в брюшную полость в виде взвеси в 2%-ной крахмальной слизи из расчета 0,1 мл на 10 г массы животного в возрастающих дозах. Результаты обрабатывали по Прозоровскому с вычислением средней смертельной дозы (ЛД50) при Р<0,05 (таблица 1).

Пример 4. Соединения Ia и Iб исследовали на наличие антирадикальной активности.
Для определения антирадикальной активности использовали реакцию со стабильным свободным радикалом дифенилпикрилгидразилом (ДФПГ) (производство Sigma-Aldrich). Концентрация ДФПГ в 95% этаноле составила 6,5×10-5 М. В качестве эталона сравнения использовался тролокс (выпускается фирмой Sigma-Aldrich под названием Trolox).
Реакционная смесь, которая состоит из 3 мл 0,3 мМ раствора ДФПГ, 1 мл буферного раствора ТРИС-HCl с pH=7,4 и 1×10-5 М соединения по изобретению или тролокса, растворенных в ДМСО, инкубируется при стандартных температурных условиях (Т=298К) в течение 30 минут. Затем при длине волны 517 нм в кюветах с толщиной слоя 0,5 см определяют оптическую плотность реакционной смеси на фотоэлектроколориметре КФК-3-01. Ингибирующий эффект представляет собой убыль радикалов ДФПГ (Q), которую рассчитывают по формуле:
Q=100(D0-Dx)/D0
где D0 - оптическая плотность контрольного раствора ДФПГ, Dx - оптическая плотность раствора ДФПГ в присутствии исследуемого вещества, либо раствора эталона сравнения. Полученные измерения обрабатывали по стандартной методике с использованием критерия Стьюдента (доверительная вероятность составляла 0,95). Каждый результат (таблица 2) представляет собой среднее значение ± стандартная ошибка среднего.
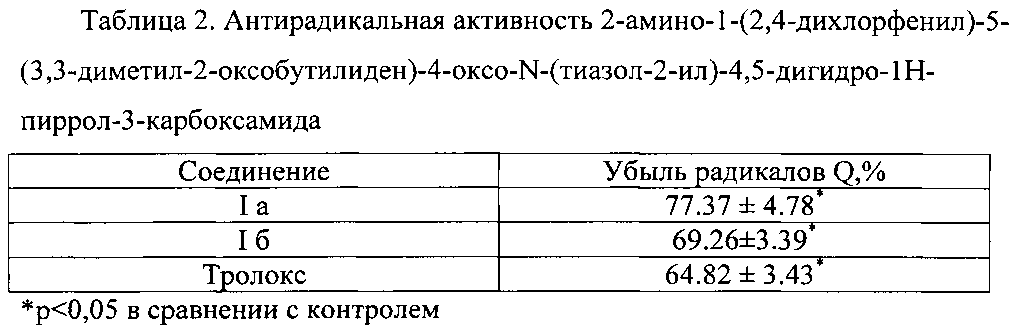
Антирадикальная активность 2-амино-1-(2,4-дихлорфенил)-5-(3,3-диметил-2-оксобутилиден)-4-оксо-N-(тиазол-2-ил)-4,5-дигидро-1H-пиррол-3-карбоксамида (Iб) превышает способность к связыванию радикалов у тролокса.
Пример 5. Противоопухолевая активность соединений Ia и Iб.
Противоопухолевая активность соединений Ia, Iб и препаратов сравнения - паклитаксела и этопозида по отношению к клеткам остеосаркомы человека U2 OS (48 часов инкубации с препаратами) показана на графике на фиг. 1, где по оси ординат - количество жизнеспособных клеток (в %) от контроля "К", по оси абсцисс - концентрация исследуемых соединений и препаратов сравнения Таксола и этопозида (в мкМ).
Одним из механизмов выявленного противоопухолевого эффекта у исследуемых соединений может являться нарушение в регуляции клеточного цикла опухолевых клеток, а именно блокада клеток в М-фазе клеточного цикла. В пользу этого свидетельствует значительное и дозозависимое накопление клеток округлой формы после их инкубации с вышеуказанными соединениями Ia и Iб. Обнаруженный нами эффект был значительно более выражен в опухолевых клетках: линии U2 OS (остеосаркома), HeLa S3 (аденокарцинома шейки матки), H1299 (немелкоклеточный рак легкого) по сравнению с нормальными клетками (например, фибробласты) (см. фиг. 2).
Таким образом, результаты свидетельствуют о том, что заявляемые соединения (Ia, б) проявляют выраженную дозозависимую противоопухолевую активность in vitro, являются малотоксичными по сравнению с прототипом Таксолом и ингибитором топоизомеразы II типа - этопозидом.
Таким образом, 2-амино-1-арил-5-(3,3-диметил-2-оксобутилиден)-4-оксо-N-(тиазол-2-ил)-4,5-дигидро-1H-пиррол-3-карбоксамиды проявляют более выраженное антирадикальное и противоопухолевого действие при пониженной токсичности, превосходя некоторые из препаратов сравнения по показателю активности. Следовательно, заявляемые соединения (Ia, б) и их аналоги могут найти применение в медицине в качестве антиоксидантных и противоопухолевых лекарственных средств.