Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ 4-ЗАМЕЩЕННЫХ ТИОМОРФОЛИНОВ
Вид РИД
Изобретение
Предлагаемое изобретение относится к области органической химии, в частности к способу получения 4-замещенных тиоморфолинов общей формулы (I):
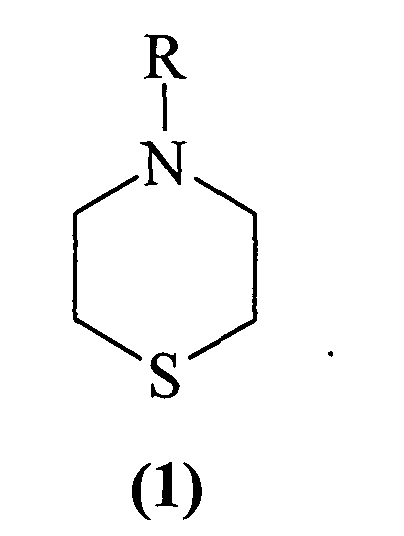
где R=СН3(СН2)2, C6H5, о-, р-СН3С6Н4, C4H4OH, СН3СО.
N-замещенные тиоморфолины могут представлять интерес как фармацевтические средства с анальгезирующей активностью [Патент РФ, №2101284 С2, Ацусуке Терада, Иосио Иизука, Казуюки Вати, Кендзи Фудзибаяси], с антагонистической активностью по отношению к тахикининовым рецепторам [Патент РФ, №237905 С2, Такахаси Масами, Яманака Такеси, Мияки Цутому], как высокоэффективные сорбенты тяжелых металлов для очистки сточных вод, экстрагенты для разделения редких, благородных и драгоценных металлов [Б.А. Трофимов, С.И. Амосова. Дивинилсульфид и его производные. Новосибирск: Наука, 1983; А.В. Свиридова, Е.Н. Прилежаева, Успехи химии, 1974, Т.43, №3, С.519].
Известные способы получения 4-замещенных тиоморфолинов базируются на реакциях тиоморфолина с различными электрофилами.
Так, взаимодействие 2-(трет-бутоксикарбониламино-)пропилового эфира метансульфоновой кислоты с 4-тиоморфолином в присутствии карбоната калия в ацетонитриле при 50°С приводит к образованию (S)-1-метил-2-тиоморфолин-4-ил-этиламина (2) [By Chen, Li et al. From U. S. Pat. Appl. Publ., 20100152203, 17 Jun 2010] по схеме:
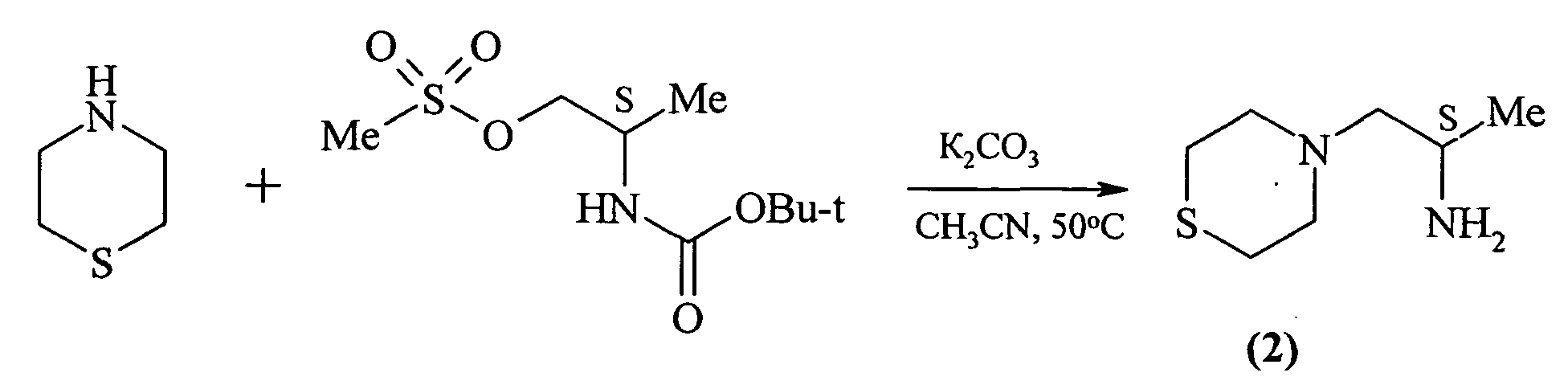
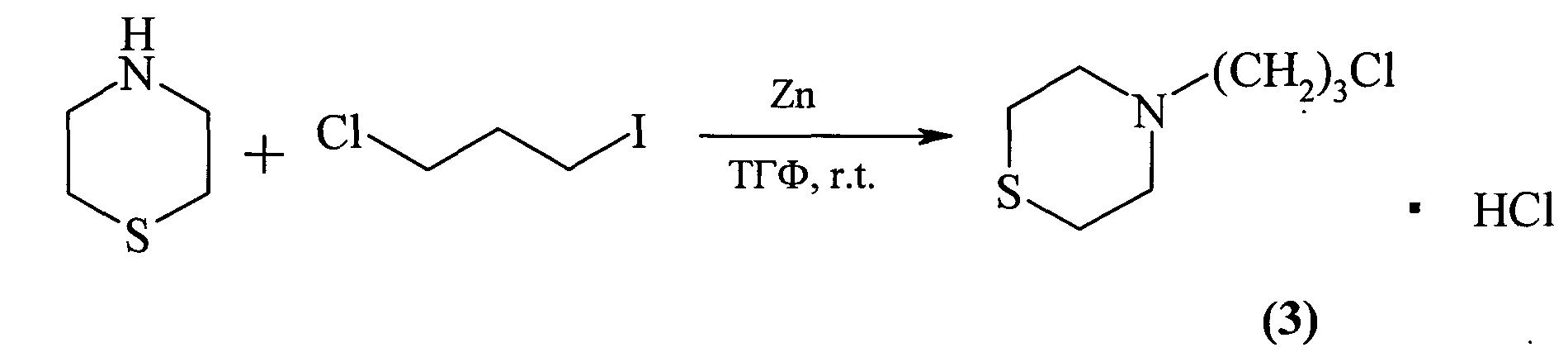
Известен способ [By Vennerstrom, Jonathan L. et al. From PCT Int. Appl., 2009058859, 07 May 2009] получения 4-(3-хлорпропил)-тиоморфолин гидрохлорида (3) взаимодейсвием тиоморфолина с 1-хлор-3-йодпропаном в сухом ТГФ в присутствии порошкообразного Zn при комнатной температуре с выходом 19% по схеме:
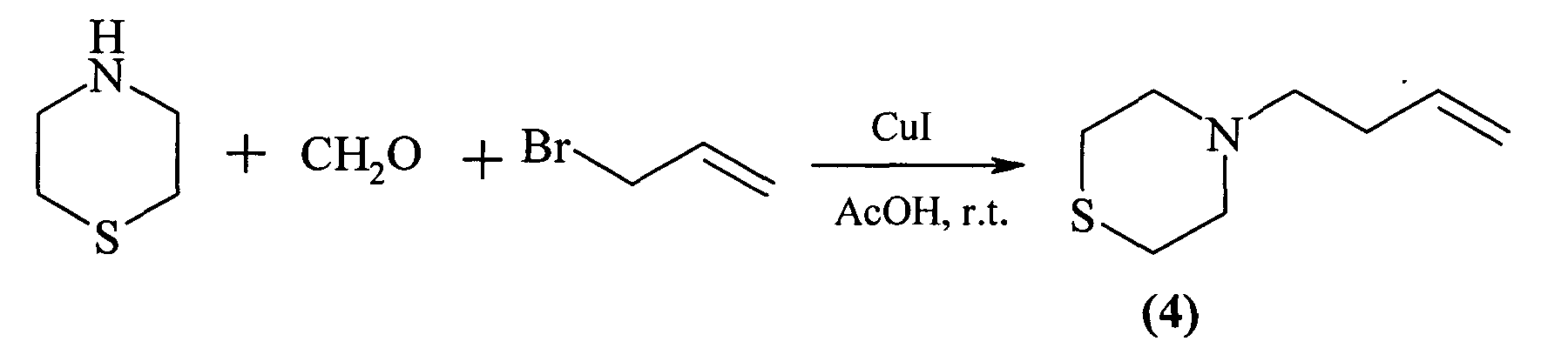
Известен способ [By Estevam, Idalia H.S. and Bieber, Lothar W., Tetrahedron Letters, 44 (4), 667-670, 2003] получения 4-(3-бутенил)-тиоморфолина (4) взаимодействием 4-тиоморфолина с формальдегидом и бромпропеном в уксусной кислоте в присутствии йодида меди при комнатной температуре по схеме:
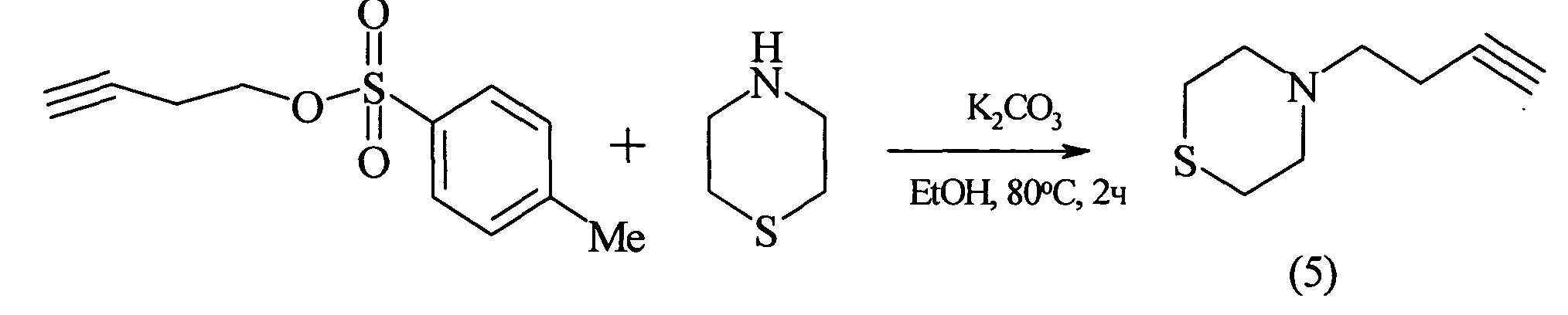
Известен способ [By Apodaka, Richard et al, From U.S. Pat. Appl. PubL, 20040002604, 01 Jan 2004] получения 4-(3-бутинил)-тиоморфолина (5) взаимодействием тиоморфолина с 3-бутин-1-ил-4-толуилсульфонатом в этаноле в присутствии карбоната калия при 80°С в течение 2 ч по схеме:
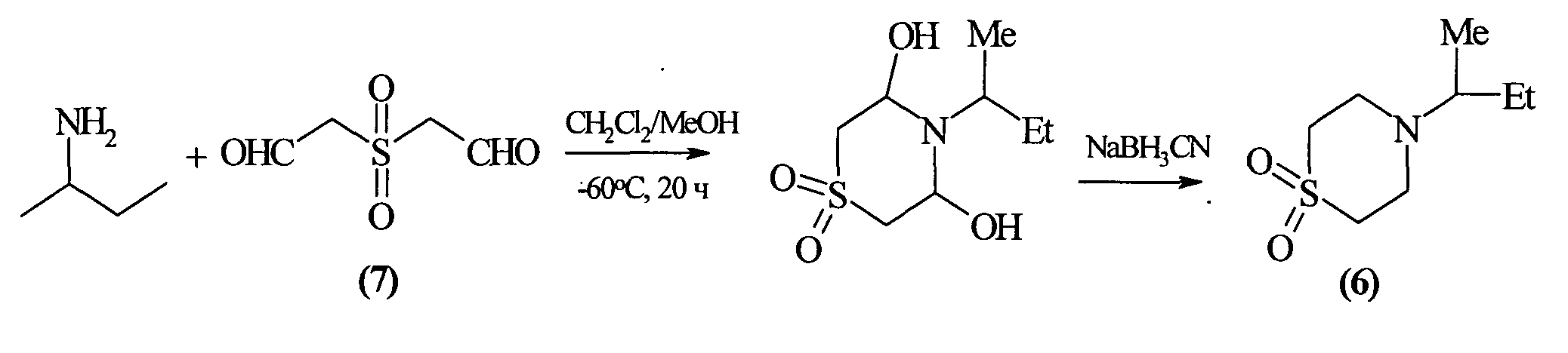
Известен способ [By Baxter, Ellen W. and Reitz, Alien B. From Organic Reactions (Hoboken, NJ, United States), 59, No pp. Given, 2002] получения 4-(1-метилпропил)-тиоморфолин-диоксида (6) взаимодействием 2-амино-бутана с сульфоксидсодержащим диальдегидом (7) в смеси растворителей CH2Cl2:МеОН (4:1) при температуре -60°С с последующим восстановлением цианборгидридом натрия по схеме. Выход продукта (6) составляет 26%:
Известным способом не могут быть получены 4-замещенные тиоморфолины общей формулы (1).
Таким образом, в литературе отсутствуют сведения по получению 4-замещенных тиоморфолинов общей формулы (1).
Предлагается новый способ селективного получения 4-замещенных тиоморфолинов общей формулы (1).
Сущность способа заключается во взаимодействии дивинилсульфида с аминосубстратом R-NH2 (пропиламин, анилин, о-, p-толуидин, моноэтаноламин, ацетамид) в присутствии катализатора PdCl2-CF3COOH-Ph3P, взятыми в мольном соотношении дивинилсульфид:аминосубстрат (пропиламин, анилин, о-, p-толуидин, моноэтаноламин, ацетамид): PdCl2:CF3COOH:Ph3P=10:10:(0.3-0.7):(1.5-3.5):(0.3-0.7), предпочтительно 10:10:0.5:2.5:0.5 в толуоле в качестве растворителя, при температуре 55-65°С и атмосферном давлении в течение 38-42 ч, предпочтительно 40 ч. Выход 4-замещенных тиоморфолинов общей формулы (1) составляет 50-78%. Реакция протекает по схеме:
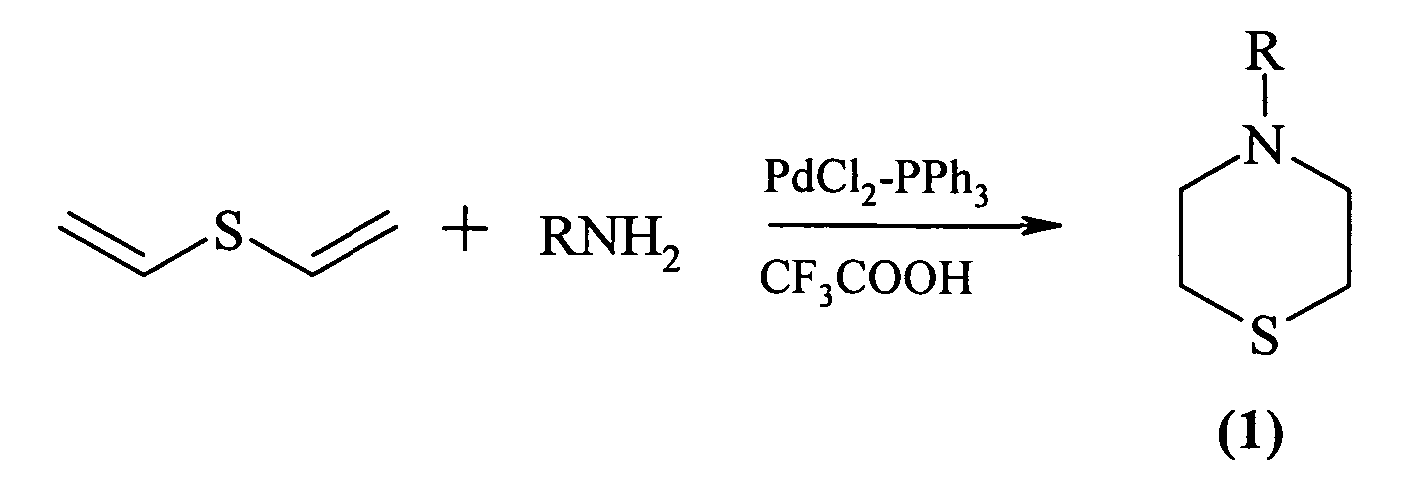
где R=СН3(СН2)2, С6Н5, о-, p-СН3С6Н4, С2Н4ОН, СН3СО.
4-Замещенные тиоморфолины общей формулы (1) образуются только лишь с участием дивинилсульфида и аминосубстрата (пропиламин, анилин, о-, p-толуидин, моноэтаноламин, ацетамид), взятыми в стехиометрическом соотношении 1:1. При другом соотношении исходных реагентов снижается выход 4-замещенных тиоморфолинов общей формулы (1). В присутствии других катализаторов (NiCl2, CoCl2, FeCl3, ZrCl4), а также в их отсутствие целевые продукты общей формулы (1) не образуются.
Реакции проводили при температуре 55-65°С. При температуре ниже 55°С (например, 40°С) снижается скорость реакции, и уменьшается выход продукта (1). При температуре выше 65°С (например, 100°С) снижается селективность реакции и увеличиваются энергозатраты. Опыты проводили в толуоле, т.к. в указанном растворителе хорошо растворяются исходные реагенты и целевые продукты (1).
Существенные отличия предлагаемого способа
В предлагаемом способе в качестве исходных реагентов применяются дивинилсульфид и аминосубстраты (пропиламин, анилин, о-, р-толуидин, моноэтаноламин, ацетамид), а в качестве катализатора PdCl2-CF3COOH-PPh3. Способ позволяет селективно получать 4-замещенные тиоморфолины общей формулы (1). В известных способах в качестве исходных реагентов применяются тиоморфолин или сульфоксидсодержащий диальдегид, а в качестве катализатора CuI, К2СО3 или Zn.
Способ поясняется примерами
Пример 1. В сосуд Шлейка, установленный на магнитной мешалке, в атмосфере аргона при комнатной температуре (~20°С) помещают 5 мл толуола, 0.09 г (0.5 ммоль) PdCl2, 0.3 мл (2.5 ммоль) CF3COOH и 0.13 г (0.5 ммоль) PPh3, перемешивают в течение 30 мин, добавляют 0.9 мл (10 ммоль) дивинилсульфида и 0.6 мл (10 ммоль) пропиламина, перемешивают при температуре 60°С в течение 40 ч. Из реакционной массы выделяют 4-(пропил)-тиоморфолин (1а) с выходом 64%. Другие примеры, подтверждающие способ, приведены в табл.1.
|
Все опыты проводили в толуоле. ТСХ осуществляли на пластинах ″Sorbfie″ в системе С6Н6-CHCl3-EtOAc-МеОН, 2:3:2:1.
Физико-химические и спектральные характеристики полученных соединений:
4-(Пропил)-тиоморфолин (1a)
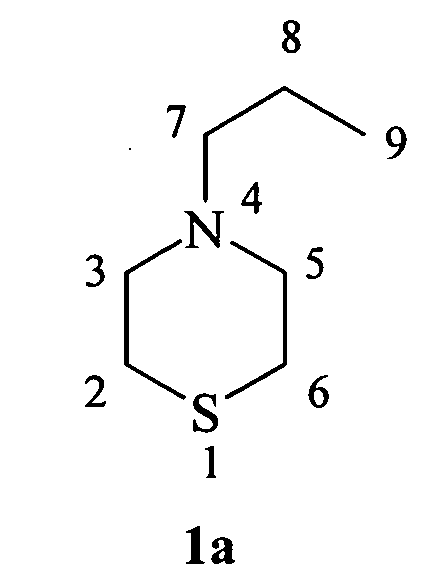
Масло желтого цвета. Rf=0,65, nD=1.5650
ИК-спектр, ν, см-1: 690, 720, 1098, 1120, 1380, 1469, 1475, 3428.
ЯМР 1Н (δ, м.д. J, Гц,): 0.91 (т, 3Н,, СН3, J=6.8); 1.36 (м, 2Н, СН2 (8)); 2.40 (т, 2Н, СН2 (7), J=5.4); 2.57 (д, 4Н, СН2 (2, 6). J=9.4); 3.24 (д, 4Н, СН2 (3, 5), J=7.6);
ЯМР 13С (δ, м.д.): 13.92 (С9); 20.57 (С8); 27.76 (С2,6); 29.70 (С7); 54.33 (С3,5).
Масс-спектр, m/z 144 (10) [М-Н]+, m/z 130 (87) [М-СН3]+, m/z 116 (55) [М-СН3СН2]+, m/z 102 (34) [М-СН2СН2СН3]+, m/z 85 (14) [М-CH2SCH2]+, m/z 60 (74) [CH2SCH2]+, m/z 43 (100) [C3H7]+. C7H15NS. Мтеор=145,27.
4-(-Фенил)-тиоморфолин (1b)
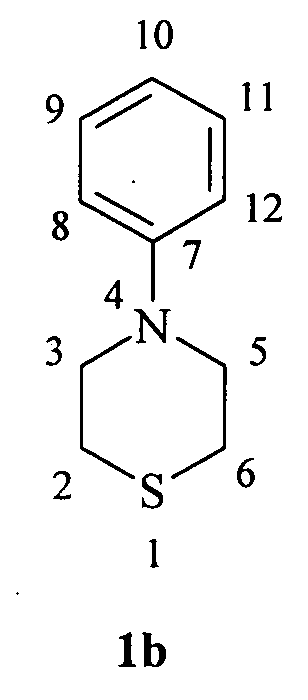
Масло желтого цвета. Rf=0.71, nD=1.6452
ИК-спектр, ν, см-1: 690, 750, 1105, 1180, 1495, 1639.
ЯМР 1Н (δ, м.д.б J, Гц,): 2.58 (уш.с, 4Н, СН2 (2, 6)); 3.26 (д, 4Н, СН2 (3, 5), J=10); 6.36 (1Н, CHAr,); 6.76 (2Н, CHAr,); 7.22 (2Н, CHAr,).
ЯМР 13С (δ, м.д.): 27.84 (С2,6); 54.44 (С3,5); 115.02, 129.88, 130.52, 149.06 (CAr).
Масс-спектр, m/z 178 (32) [М-Н]+, m/z 119 (100) [М-CH2NC6H5CH2]+, m/z 102 (55) [М-NCH2CH2SCH2CH2]+, m/z 11 (55) [М-C6H4]+, m/z 60 (84) [CH2SCH2]+. C10H13NS. Мтеор=179,28.
4-(о-Толуидин)-тиоморфолин (1c)
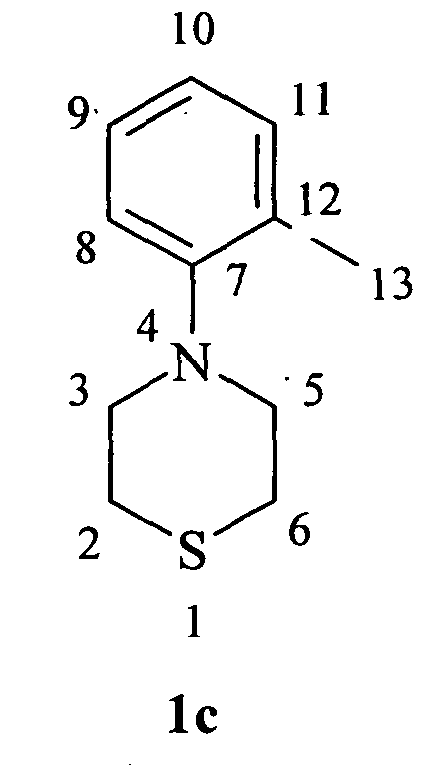
Масло желтого цвета. Rf=0,70, nD=1.6615
ИК-спектр, ν, см-1: 690, 750, 1105, 1180, 1479, 1495, 1639.
ЯМР 1Н (δ, м.д., J, Гц,) 2.17 (с, 3Н,, СН3 (13)); 2.58 (с, 4Н, СН2 (2, 6)); 3.26 (уш.с, 4Н, СН2 (3, 5)); 6.60 (1Н, CHAr,); 6.98 (1Н, CHAr,); 7.27 (1Н, CHAr,); 7.38 (1H, CHAr,).
Спектр ЯМР 13С (δ, м.д.): 16.45 (СН3); 29.79 (С2,6); 55.16 (С3,5); 120.39, 124.63, 128.81, 133.12, 135.06, 152.02 (CAr).
Масс-спектр, m/z 192 (6) [М-Н]+ 178 (23) [М-СН3]+, m/z 105 (51) [М-CH2CH2SCH2CH2]+, m/z 91 (100) [М-CH2CH2SCH2CH2N]+, m/z 81 (55) [М-CH3C6H4N]+. C11H15NS. Мтеор=193,31.
4-(р-Толуидин)-тиоморфолин (1d)
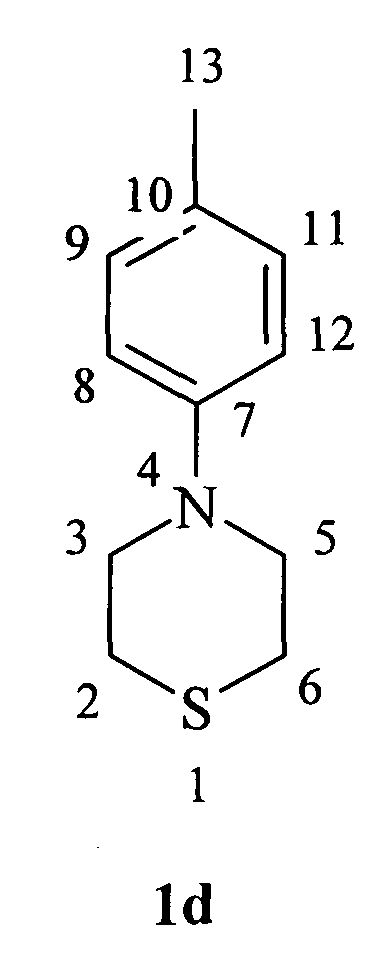
Масло желтого цвета. Rf=0,69, nD=1.6303
ИК-спектр, ν, см-1: 690, 750, 1100, 1380, 1479, 1739.
ЯМР 1Н (δ, м.д., J, Гц,) 2.16 (с, 3Н,, СН3 (13)); 2.56 (т, 4Н, СН2 (2, 6)); 3.24 (т, 4Н, СН2 (3, 5)); 6.60 (д, 1Н, CHAr,); 6.98 (д, 1Н, CHAr,); 7.30 (т, 1Н, CHAr,); 7.31 (д, 1H CHAr,).
Спектр ЯМР 13С (δ, м.д.): 16.45 (СН3); 29.79 (С2,6); 55.16 (С3,5); 119.89-151.92 (CAr).
Масс-спектр, m/z 192 (10) [М-Н]+ 178 (23) [М-СН3]+, m/z 105 (51) [М-CH2CH2SCH2CH2]+, m/z 91 (100) [М-CH2CH2SCH2CH2N]+, m/z 81 (55) [М-CH3C6H4N]+. C11H15NS. Мтеор=193,31.
2-(Тиоморфолин-4-ил)этанол (1e)
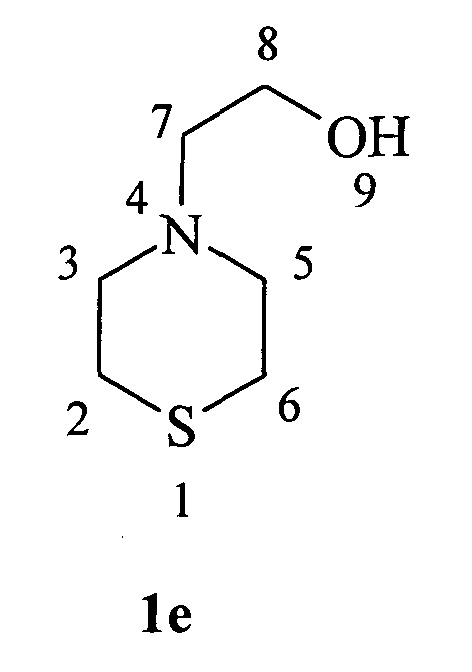
Масло желтого цвета. Rf=0,70. nD=1.5601
ИК-спектр, см-1: 695, 744, 998, 1300, 1112, 1290, 1253, 1352, 3338.
Спектр ЯМР 1Н (δ, м.д., J, Гц, 20°С): 2,0 (уш.с, 2Н, СН2 (6)); 2,079 (уш.с, 2Н, СН2 (2)); 2,58 (уш.с, 2Н, СН2 (5)); 2,64 (уш.с, 2Н, СН2 (3)); 3,45 (уш.с, 2Н, СН2 (7)); 3,79 (уш.с, 2Н, СН2 (8)).
Спектр ЯМР 13С (δ, м.д.): 27.31 (С2,6); 54.53 (С3,5); 56.06 (С7); 60.15 (С8).
Масс-спектр, m/z 146 (15) [М-Н]+, m/z 101 (38) [М-СН2СН2ОН]+, m/z 31 (100) [М-CH2CH2SCH2CH2NCH2]+, m/z 45 (25) [М-CH2CH2SCH2CH2N]+, 115 (21) [М-СН2ОН]. C6H13NSO. Мтеор=147,24
4-(Ацил)-тиоморфолин (1f)
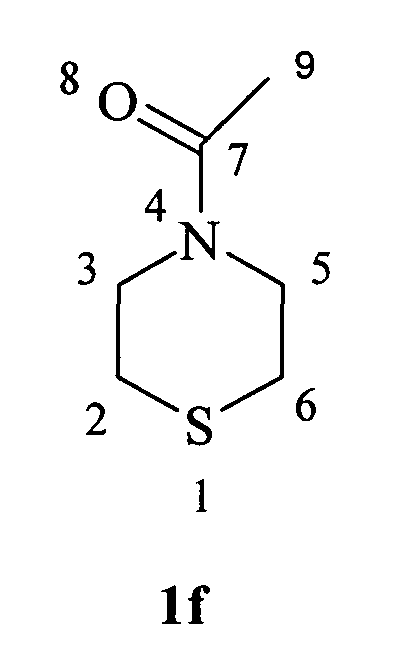
Масло желтого цвета. Rf=0,67, nD=1.5803
ИК-спектр, см-1: 695, 744, 1020, 1200, 1339, 1290,1700, 1745, 1405.
ЯМР 1Н (δ, м.д., J, Гц,) 2.06 (с, 3Н,, СН3 (9)); 2.83 (с, 4Н, СН2 (2, 6)); 3.72 (m, 4Н, СН2 (3,5), J=8.4).
Спектр ЯМР 13С (δ, м.д.): 21.92 (СН3); 28.04 (С2,6); 47.80 (С3); 51.03 (С5) 169.06 (С7).
Масс-спектр, m/z 144 (17) [М-Н]+ , m/z 130 (42) [М-СН3]+, m/z 102 (100) [М-СН3СО] +, m/z 98 (25) [М-CH2CH2SCH2CH2]+, m/z 47 (37) [М-CH2NCOCH3]+, m/z 43 (17) [M-NCH2CH2SCH2CH2]+. C6H11NSO. Mтеор=145,22.
Способ получения 4-замещенных тиоморфолинов общей формулы (I): где R=СН(СН), СН, о-, p-СНСН, СНОН, СНСО,отличающийся тем, что дивинилсульфид подвергается взаимодействию с аминосубстратом R-NH [R = указанные выше] в присутствии катализатора РdСl-СFСООН-РРh при мольном соотношении дивинилсульфид:аминосубстрат:РdСl:СFСООН:РРh=10:10:(0.3-0.7):(1.5-3.5):(0.3-0.7), при 55-65°С и атмосферном давлении в течение 38-42 ч.