Результат интеллектуальной деятельности: Гидрохлорид 1,7,7-триметилбицикло[2.2.1]гептан-2-ил 3-(пиперидин-1-ил)пропионат, используемый в качестве ингибитора вируса Эбола
Вид РИД
Изобретение
Изобретение относится к химии и медицине, а именно к лекарственным средствам, конкретно, к соединению формулы I:
у которого выявлена биологическая активность, заключающаяся в ингибировании репродукции вируса Эбола. Данное соединение I может использоваться в качестве ингибитора репродукции вируса Эбола и может быть применено в медицине, вирусологии и фармакологии.
Вирусная геморрагическая лихорадка Эбола - острое заболевание, сопровождающееся высокими уровнями заболеваемости и летальности. Возбудителем лихорадки Эбола как и родственной лихорадки Марбург, является РНК-содержащий вирус, принадлежащий к семейству филовирусов (Flaviviridae). Первая официально зарегистрированная вспышка лихорадки Эбола произошла в 1976 году в Заире (в настоящее время Демократическая Республика Конго) в районе реки Эбола. На протяжении 40 лет в странах Центральной Африки происходили спорадические вспышки данного заболевания, которые удавалось оперативно ликвидировать, однако в 2014-2015 годах в западной Африке вспышка Эбола оказалась на порядок более масштабной и сложной. В ходе ее ликвидации были задействованы усилия множества стран мира (Shoman, Н., Karafillakis, Е., Rawaf, S. The link between the West African Ebola outbreak and health systems in Guinea, Liberia and Sierra Leone: a systematic review. Globalizationand health, 2017 13(1), 1). Основной проблемой в борьбе с филовирусными лихорадками является полное отсутствие зарегистрированных вакцин и профилактических препаратов против данных заболеваний. Большие надежды возлагались на препараты, включающие моноклональные антитела, однако испытания коктейля моноклональных антител ZMapp показали ограниченность этого подхода (Liu, G., Wong, G., Su, S., Bi, Y., Plummer, F., Gao, G.F., Qiu, X. Clinical Evaluation of Ebola Virus Disease Therapeutics. Trends in molecular medicine, 201723, 9, 820-830). Альтернативой иммунотерапии, уже доказавшей свою эффективность на ряде вирусов (вирус гриппа, вирус гепатита С), являются малые органические соединения, способные блокировать жизненно важные этапы репродукции вируса.
В настоящее время большинство исследований, посвященных поиску антивирусных соединений, сконцентрировано на ингибиторах специфического фермента РНК содержащих вирусов РНК-зависимой РНК-полимеразы. Репликация, которую осуществляет этот фермент, является важнейшим этапом жизненного цикла вируса, однако его наступление означает, что вирус уже проник в клетку. С целью минимизировать воздействие вируса на организм, желательно, что бы он был заблокирован на этапе проникновения.
Филовирусы и, в частности, вирус Эбола, содержат на своей поверхности единственный гликопротеин - GP, обеспечивающий проникновения патогена в клетку. Этот белок является подходящей мишенью, поскольку, как и РНК-зависимая РНК-полимераза, отсутствует в клетках млекопитающих. Несмотря на то, что все вспышки лихорадки Эбола в 20-ом веке удавалось оперативно ликвидировать, вспышка этой болезни в Западной Африке в 2014-2015 годах свидетельствует о значительной недооценке ее эпидемического потенциала и необходимости увеличения усилий, направленных на поиск антивирусных соединений.
Известно новое применение известного лекарственного средства тейкопланина против вируса Эбола (заявка США №20180353568, МПК А61Р 31/14, опубл. 13.12.2018 г.). Тейкопланин является антибиотиком гликопептидной структуры, демонстрирующим in vitro бактерицидную активность в отношении анаэробных и аэробных грамположительных микроорганизмов. При помощи псевдовирусной системы выявлена антивирусная активность тейкопланина, способного подавлять проникновение вируса Эбола в клетки. Тейкопланин ингибирует белок оболочки GP вируса Эбола и особенно может ингибировать белок оболочки этого вируса штамма типа Заир.
Однако активность этого соединения не подтверждена в экспериментах с натуральным вирусом. Кроме того, описан ряд побочных эффектов возникающих при приеме этого вещества человеком.
Наиболее близким к заявляемому соединению прототипом, является сертралин II. Сертралин известен как антидепрессант из группы селективных ингибиторов обратного захвата серотонина.
При этом обнаружено, что данное соединение блокирует инфицирование клеток вирусом Эбола и активно на ранних этапах репродукции вируса (Jingshan Ren, Yuguang Zhao, Elizabeth E. Fry, David I. Stuart Target Identificationand Mode of Action of Four Chemically Divergent Drug sagainst Ebola virus Infection J. Med. Chem. 2018, 61, 724-733).
Недостатком известного соединения является невысокая противовирусная активность.
Задачей изобретения является расширение нового класса эффективных ингибиторов репродукции вируса Эбола.
Технический результат: повышение эффективности подавления репродукции вируса Эбола и расширение ассортимента ингибиторов репродукции данного вируса.
Поставленная задача решается новым соединением формулы I, обладающим выраженными свойствами ингибиторов репродукции вируса Эбола.
Соединение формулы I, после проведения углубленных фармакологических исследований, может использоваться, как в чистом виде, так и в качестве компонента новых низкотоксичных высокоэффективных против вируса Эбола лекарственных форм.
Исследования биологической активности I, проведенные с использованием псевдовирусных систем и вируса Эбола штамм Заир, показали высокую эффективность данного агента как ингибитора репродукции вируса.
Синтез соединения проводили по схеме 1. Ход реакций отслеживали отбором проб и анализом хромато-масс спектров. На первой стадии проводили взаимодействие природного (-)-борнеола с хлорангидридом 2-хлорпропионовой кислоты с образованием соответствующего 3-хлорпропионата III. Дальнейшая реакция последнего с пиперидином приводит к промежуточному свободному основанию IV, взаимодействием которого с соляной кислотой в эфире получается целевая соль I.
Спектральные исследования выполнены в Химическом Сервисном Центре коллективного пользования СО РАН. Величины удельного вращения определяли на спектрометре PolAAr 3005. Спектры ЯМР 1Н и 13С регистрировали на спектрометрах Bruker AV-400 (1Н: 400.13 МГц, 13С: 100.61 МГц), DRX-500 (1Н: 500.13 МГц, 13С: 125.76 МГц) и AV-600 (1Н: 600.30 МГц, 13С: 150.95 МГц). В качестве внутреннего стандарта использовали остаточные сигналы растворителя - хлороформа (1Н 7.24, 13С 76.90 м.д.). Отнесение сигналов в спектрах ЯМР проводилось с привлечение стандартных одномерных и двумерных экспериментов. Нумерация атомов в соединениях дана для отнесения сигналов в спектрах ЯМР и не совпадает с нумерацией атомов в номенклатурном названии. Хромато-масс-спектры записывали на газовом хроматографе Agilent 7890 А с квадрупольным масс-спектрометром Agilent 5975С в качестве детектора, кварцевая колонка НР-5MS 300000.25 мм, газ-носитель - гелий. Удельное вращение выражено в (град⋅мл)⋅(г⋅дм)-1, концентрация раствора (г)⋅(100 мл)-1. Растворители перед использованием сушились и перегонялись.
Изобретение иллюстрируется следующими примерами.
Пример 1.
1,7,7-Триметилбицикло[2.2.1]гептан-2-ил-3-хлорпропионат III.
К раствору 3-хлорпропановой кислоты в CH2Cl2 добавили избыток (COCl)2 и каплю ДМФА. Реакционную смесь перемешивали при комнатной температуре в течение 4 ч. в атмосфере Ar. Избыток (COCl)2 удалили на ротационном испарителе, полученный хлорангидрид использовали свежеприготовленный. Далее к раствору (-)-борнеола 0.03 моль и Et3N 0.03 моль в 20 мл сухого CH2Cl2 в атмосфере Ar прибавляли 0.03 моль свежеприготовленного хлорангидрида 3-хлорпропановой кислоты. Реакционную смесь перемешивали и оставили на 24 ч при 23-25°С. Осадок гидрохлорида триэтиламина отфильтровывали, в фильтрат добавляли CH2Cl2, промывали насыщенный NaCl, сушили безводным Na2SO4. Осушитель отфильтровали, растворитель упарили. Выход 70%.
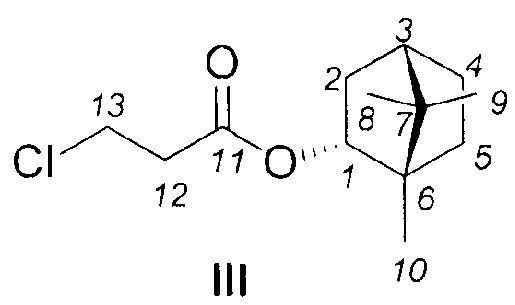
ЯМР 1Н (400 МГц, CDCl3, δ, м.д.): 0.80 (3Н, с, Ме-9), 0.84 (3Н, с, Ме-10), 0.87 (3Н, с, Ме-8), 0.97 (1Н, дд, 2J=13.7, J2н, 1к=3.5, Н-2эндо), 1.16-1.33 (2Н, м, Н-4эндо, Н-5экзо), 1.65 (1Н, дд, J3, 2к=J3, 4к=4.6, Н-3), 1.67-1.77 (1Н, м, Н-4экзо), 1.89 (1Н, ддд, 2J=12.9, J5н, 4н=9.3, J5н, 4к=4.4, Н-5эндо), 2.33 (1Н, м, Н-2экзо), 2.77 (2Н, т, J=6.6 Гц, Н-12), 3.74 (2Н, т, J=6.6 Гц, Н-13), 4.91 (1Н, ддд, J1к, 2к=10.0, J1к, 2н=3.5, J1к, 5к=2.2, Н-1экзо). ЯМР 13С (125 МГц, CDCl3, δ, м.д.): 170.40 с (С-11), 80.50 д (С-1), 48.69 с (С-6), 47.69 с (С-7), 44.71 д (С-3), 39.18 д (С-13), 37.80 д (С-12), 36.54 т (С-2), 27.85 т (С-4), 26.97 т (С-5), 19.55 к (Ме-9), 18.69 к (Ме-10), 13.34 к (Ме-8).  (CHCl3, с-0.7). Найдено: m/z 244.1225 [М]+ C13H21O2Cl. Вычислено: М=244.1222.
(CHCl3, с-0.7). Найдено: m/z 244.1225 [М]+ C13H21O2Cl. Вычислено: М=244.1222.
Пример 2.
1,7,7-Триметилбицикло[2.2.1]гептан-2-ил-3-(пиперидин-1-ил)пропионат IV.
Смесь 1 экв 1,7,7-триметилбицикло[2.2.1]гептан-2-ил 3-хлорпропионата III, 1.1 экв пиперидина и 1 экв Et3N в 15 мл МеОН перемешивали при комнатной температуре в течение суток, затем растворитель упарили. К сухому остатку добавили 20 мл EtOAc и промыли насыщенным раствором NaCl, водный слой еще раз экстрагировали EtOAc. Объединенный органический слой сушили безводным Na2SO4 и упарили. Остаток хроматографировали на SiO2, используя в качестве элюента гексан/этилацетат (100:0→0:100) + метанол (1%). Выход 74%.
ЯМР 1Н (400 МГц, CDCl3, δ, м.д): 0.79 (3Н, с, Ме-10), 0.83 (3Н, с, Ме-8), 0.86 (3Н, с, Ме-9), 0.94 (1H, дд, 2J=13.7, J2н, 1к=3.5, Н-2эндо), 1.15-1.30 (2Н, м, Н-4эндо, Н-5экзо), 1.33-1.43 (2Н, м, Н-16), 1.49-1.57 (4Н, м, 2Н-15, 2Н-17), 1.63 (1Н, дд, J3, 2к=J3, 4к=4.6, Н-3), 1.65-1.76 (1H, м, Н-4экзо), 1.85-1.94 (1Н, ддд, 2J-12.9, J5н, 4н=9.3, J5н, 4к=4.4, Н-5эндо), 2.30 (1Н, м, Н-2экзо), 2.31-2.42 (4Н, уш. сиг, 2Н-14, 2Н-18), 2.43-2.53 (2Н, м, Н-12), 2.57-2.66 (2Н, м, Н-13), 4.86 (1Н, ддд, J1к, 2к=10.0, J1к, 2н=3.5, J1к, 5к=2.2, Н-1экзо). ЯМР 13C (125 МГц, CDCl3, δ, м.д.): 172.62 с (С-11), 79.28 д (С-1), 54.02 т (С-13), 53.78 т (С-14, С-18), 48.32 с (С-6), 47.32 с (С-7), 44.73 д (С-3), 36.21 т (С-2), 32.33 т (С-12), 27.57 т (С-4), 26.66 т (С-5), 25.52 т (С-15, С-17), 23.87 т (С-16), 19.23 к (Ме-9), 18.38 к (Ме-10), 13.01 к (Ме-8).  (CHCl3, с=0.8). Найдено: m/z 293.2356 [M]+ C18H31O2N. Вычислено: М=293.2349.
(CHCl3, с=0.8). Найдено: m/z 293.2356 [M]+ C18H31O2N. Вычислено: М=293.2349.
Пример 3.
Гидрохлорид 1,7,7-Триметилбицикло[2.2.1]гептан-2-ил-3-(пиперидин-1-ил)пропионат I.
К раствору 1,7,7-Триметилбицикло[2.2.1] гептан-2-ил-3-(пиперидин-1-ил)пропионата IV в гексане добавляли насыщенный раствор HCl в эфире при перемешивании и охлаждении на ледяной бане до прекращения образования осадка. Реакционную смесь выдерживали при охлаждении 20 мин, отфильтровали, промыли охлажденным гексаном. Осадок сушили до постоянного веса, выход количественный.
ЯМР 1H (400 МГц, CDCl3, δ, м.д): 0.75 (3Н, с, Ме-10), 0.81 (3Н, с, Ме-8), 0.83 (3Н, с, Ме-9), 0.89 (1Н, дд, 2J=13.7, J2н, 1к=3.5, Н-2эндо), 1.12-1.29 (2Н, м, Н-4эндо, Н-5экзо), 1.32-1.44 (1Н, м, Н-16а), 1.63 (1Н, дд, J3, 2к=J3, 4к=4.6, Н-3), 1.65-1.73 (1Н, м, Н-4экзо), 1.76-1.89 (4Н, m, Н-5эндо, Н-16э, Н-15а, Н-17а), 2.14-2.33 (3Н, м, Н-2экзо, Н-15э, Н-17э), 2.57-2.69 (2Н, м, Н-12), 3.05-3.12 (2Н, м, Н-14а, Н-18а), 3.18-3.26 (2Н, м, Н-14э, Н-18э), 3.42-3.51 (2Н, m, Н-13), 4.79-4.85 (1Н, m, Н-1экзо). ЯМР 13С (125 МГц, CDCl3, δ, м.д.): 170.37 с (С-11), 81.24 д (С-1), 53.78 и 53.29 т (С-14, С-18), 52.17 т (С-13), 48.56 с (С-6), 47.66 с (С-7), 44.54 д (С-3), 36.41 т (С-2), 28.92 т (С-12), 27.72 т (С-4), 26.76 т (С-5), 22.36 т (С-15, С-17), 21.79 т (С-16), 19.44 к (Ме-9), 18.58 к (Ме-10), 13.33 к (Ме-8). Элементный анализ: рассчитано - С - 65.53; Н - 9.78; Cl - 10.75; N - 4.25; измерено - С - 65.58; Н - 9.67; Cl - 10.72; N - 4.31.
Пример 4.
Определение цитотоксичности соединений на клетках линии 293FT
Стоковые растворы соединений в ДМСО (в концентрации 100 мМ) добавлялись в ростовую среду к клеткам-мишеням линии 293FT в различных концентрациях - от 10 мкМ до 500 мкМ - на 48 ч. По окончании инкубации клеток с веществами, к культурам клеток добавляли тетразолиевый краситель МТТ (3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-тетразолиум бромид) до рабочей концентрации 0.5 мг/мл и инкубировали в течение 4 часов. Образующийся осадок формазана растворяли добавлением в ростовую среду 10% раствора додецилсульфата натрия с 0.01 М соляной кислотой. Количество формазана (пропорциональное количеству жизнеспособных клеток) определяли спектрофотометрически, измеряя абсорбцию при длине волны света 570 нм. Процент жизнеспособных клеток в культурах, содержащих разные концентрации исследуемого вещества I, определяли по отношению к контролю (который представлял из себя культуру клеток 293FT, инкубируемую в ростовой среде с ДМСО в отсутствие соединений), пользуясь формулой
% жизнеспособных клеток [I] = ОП [I]/ОП[ДМСО].
За величину CD50 (50% цитотоксическая концентрация) принимали концентрацию вещества, при которой выживало 50% клеток по сравнению с контролем.
Пример 5.
Определение противовирусного действия соединения I в отношении вируса Эбола штамм Заир in vitro на культуре клеток Vero.
В работе был использован вирус Эбола штам Заир, полученный из Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ БВ «Вектор» Роспотребнадзора в виде культуральной жидкости (титр вируса 4,5 lgTCD50/ml).
Определение эффективных (IC50) концентраций соединений было проведено в тесте снижения цитопатического действия вируса Эбола на клетки в трех повторах. Метод основан на способности жизнеспособных клеток поглощать и накапливать суправитальный краситель нейтральный красный. Культура клеток Vero была выращена в 96 - луночных культуральных планшетах с конфлюэнтностью не менее 90%. Готовили последовательные понижающиеся трехкратные разведения соединений, начиная с концентрации 100 мкг/мл. В эксперименте использовали вирус Эбола множественностью заражения 0,01 (эквивалентно дозе 100 TCD50 на лунку).
Определение ингибирующей активности и токсической концентрации соединений проводили одновременно. Для этого в культуральный планшет с монослоем клеток вносили разведения соединений, затем вносили поддерживающую среду без вируса (для определения токсической концентрации соединений) и жидкость содержащую вирус (для определения ингибирующей активности соединений). Культуральные планшеты инкубировали при 37°С в течение 7 суток, затем окрашивали нейтральным красным. Учет результатов проводили на планшетном анализаторе (ThermoScientificMultiskanFC), обработку данных осуществляли при помощи программы SOFTmax PRO 4.0 с использованием 4-х параметрического метода анализа. Для всех исследованных соединений определены 50% токсическая концентрация (CD50) и концентрации 50% ингибирования (IC50) В дальнейшем, для каждого соединения рассчитывался индекс селективности (SI) отношение токсичности соединения и ингибирующей активности против вируса Эбола (CD50/IC50) (табл. 1).
Пример 6.
Определение острой токсичности соединения I
Исследования острой токсичности соединения I выполняли на аутбредных мышах ICR массой 22-25 грамм. Каждая группа состояла из 2 животных. Исследуемое вещество в дозах 1.08 г/кг, 0.44 г/кг, 0.27 г/кг, 0.14 г/кг вводили в объеме 0,25 мл внутрижелудочно однократно в виде суспензии. Суспензию готовили на 10% водном растворе DMSO, начальная концентрация соединения была выбрана по принципу образование жидкости, которая способна проходить через отверстие желудочного зонда. После введения суспензий соединения за животными наблюдали в течение 7 дней. Гибели животных в течение всего периода наблюдения не было зарегистрировано. Таким образом, результаты исследования свидетельствуют о том, что соединение не токсично для взрослых мышей при внутрижелудочном введении (LD50 более 1 г/кг).
Таким образом, в результате представленной работы, было показано, что заявляемое соединение I обладает по сравнению с соединением-прототипом более высокой противовирусной активностью в отношении вируса Эбола штамм Заир.
![Гидрохлорид 1,7,7-триметилбицикло[2.2.1]гептан-2-ил 3-(пиперидин-1-ил)пропионат, используемый в качестве ингибитора вируса Эбола](https://fips.edrid.ru/images/rid/2e/78/30/512ab59b05ca84a071aa03d89950729c.jpg)
![Гидрохлорид 1,7,7-триметилбицикло[2.2.1]гептан-2-ил 3-(пиперидин-1-ил)пропионат, используемый в качестве ингибитора вируса Эбола](https://fips.edrid.ru/images/rid/2e/78/30/8e0fceeafed7dff536997638c7d7b8d4.jpg)

