Результат интеллектуальной деятельности: Способ хроматографического разделения гидрокортизона ацетата, кортизона ацетата, метилпарагидроксибензоата, пропилпарагидроксибензоата методом обращенно-фазовой высокоэффективной жидкостной хроматографии
Вид РИД
Изобретение
Изобретение относится к области хроматографии и может быть использовано в фармацевтической промышленности для контроля качества лекарственных препаратов (мазь, крем), содержащих в качестве активного вещества гидрокортизона ацетат, а в качестве консервантов метилпарагидроксибензоат и пропилпарагидроксибензоат, по показателям нормативной документации: «Родственные соединения» или «Посторонние примеси». Данный способ позволяет определять родственные соединения или посторонние примеси гидрокортизона ацетата (кортизон ацетат, единичные неидентифицированные примеси), которые могут в процессе хранения или исследования стабильности образовываться в мазях и кремах, содержащих гидрокортизон ацетат и консерванты. Хроматографическое разделение осуществляется методом обращенно-фазовой высокоэффективной жидкостной хроматографии (ОФ ВЭЖХ) на колонках, заполненных октадецисилилсиликагелем, например Zorbax Eclipse XDB С18, а в качестве подвижной фазы используется смесь метанол для жидкостной хроматографии - ацетонитрил для хроматографии - вода (200:240:560 об/об/об). Способ позволяет обеспечить высокую степень разделения заявленных веществ.
Гидрокортизон в мягкой лекарственной форме давно известен и применяется в медицинской практике более 20 лет. Активным действующим веществом мази является полусинтетический глюкокортикостероид гидрокортизон ацетат. При нанесении мази на кожу гидрокортизон угнетает высвобождение биологически активных веществ, ответственных за развитие воспалительных и аллергических процессов (простагландинов и цитокинов) из клеток крови. Под действием гидрокортизона уменьшаются воспалительные клеточные инфильтраты, тормозится миграция лейкоцитов и лимфоцитов в область воспаления. При применении в виде коротких курсов лечения на ограниченных участках кожи не вызывает подавления гипоталамо-гипофизарно-надпочечниковой системы. Применяется мазь гидрокортизон в составе комплексного лечения воспалительных и аллергических заболеваний кожи - атопического дерматита (в том числе нейродермита), экземы, простого и аллергического дерматита, псориаза, фотодерматозов, зуда различного происхождения, укусов насекомых, красного плоского лишая. Для детей мазь применяется с осторожностью.
В настоящее время в Российской Федерации перед лабораториями, занимающимися контролем качества лекарственных средств, стоит задача обязательного контроля родственных соединений или посторонних примесей в препаратах, и гидрокортизон не является исключением.
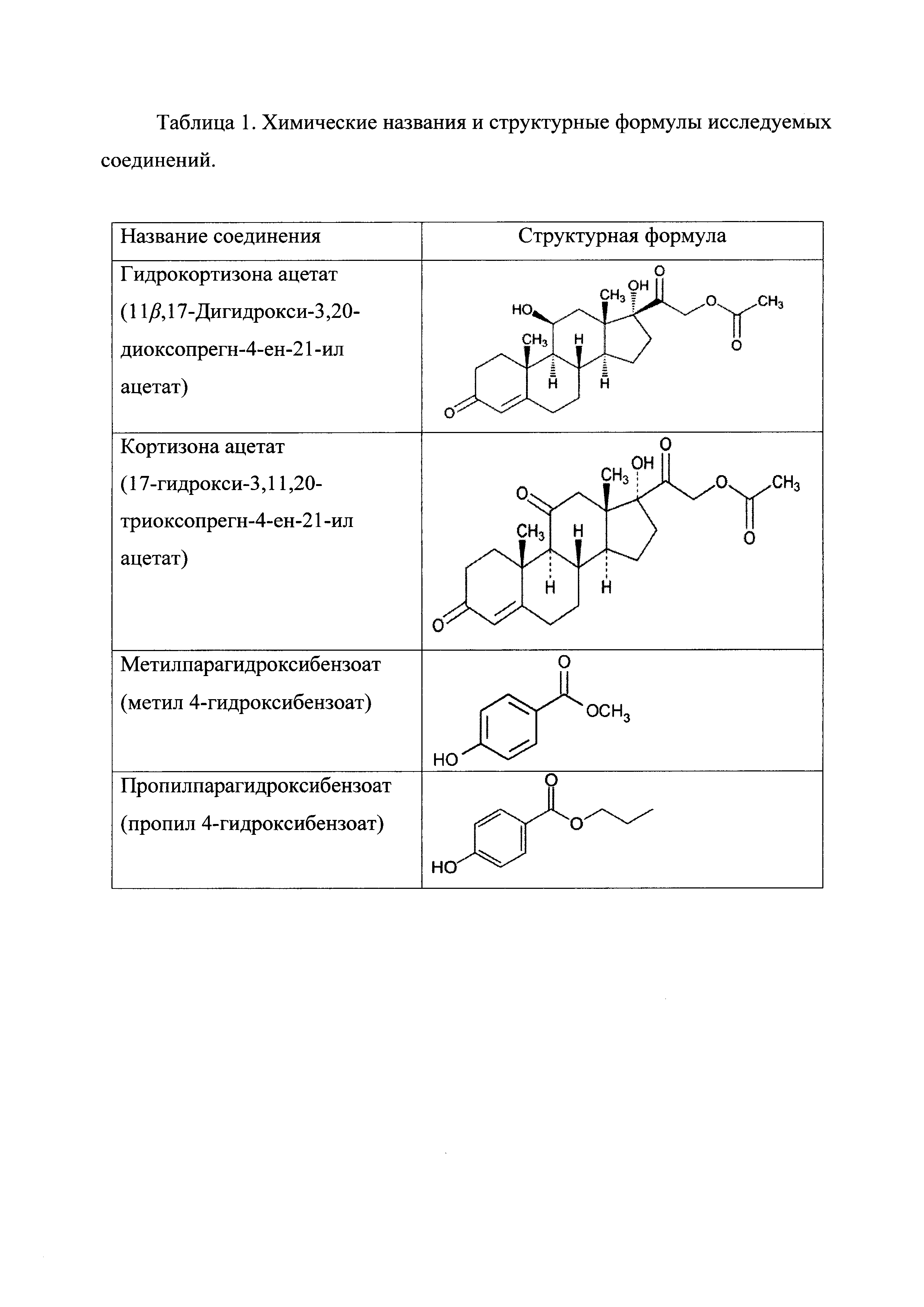
Из уровня техники известно о существовании фармакопейных монографий на гидрокортизона ацетат мазь и крем. Данные препараты описаны в ведущих фармакопеях мира Британской и Американской, но, к сожалению, разделы «Родственные соединения» или «Посторонние примеси» в них отсутствуют, что не дает возможности производителям контролировать данный показатель в препаратах гидрокортизона ацетата. Активная фармацевтическая субстанция (АФС) гидрокортизона ацетат, на основе которой изготавливаются гидрокортизона ацетат мази и кремы, описана во многих фармакопеях: Американской (The United States Pharmacopeia (USP) and the National Formulary (NF) (USP 39 NF 34, Official Monographs, Hydrocortisone Acetate, p. 4224-4225), Европейской (European Pharmacopeia - 8th Edition, volume 2, Hydrocortisone Acetate, p. 2444-2446), Белорусской (Государственная Фармакопея Республики Беларусь 2009, том III, Гидрокортизона ацетат, стр. 229-231), Казахской (Государственная Фармакопея Республики Казахстан 2009, том II, Гидрокортизона ацетат, стр. 178-180). В данных фармакопеях описан показатель «Родственные примеси» или «Сопутствующие примеси», но методики и подвижные фазы, применяемые для АФС (ацетонитрил для хроматографии - вода (400:600)), оказались полностью непригодными для применения их к готовой лекарственной форме (ГЛФ) мази или крему. Дело в том, что в состав данных мазей или кремов входят антибактериальные и противогрибковые агенты (консерванты) метилпарагидроксибензоат и пропилпарагидроксибензоат. Эти консерванты обладают синергетическим эффектом и, как правило, используются вместе, чтобы максимально эффективно обеспечить качество препарата по микробиологическим показателям. Молекула пропилпарагид-роксибензоата, не смотря на различное химическое строение (таблица 1) с молекулой гидрокортизона ацетата, обладает одинаковыми с ней сорбционными свойствами, что в условиях методик на АФС выражается в виде совпадения времен удерживания на хроматограмме испытуемого раствора и отсутствием разделения между этими пиками.
Таким образом, проблема заключается в невозможности разделения пиков гидрокортизона ацетата и пропилпарагидроксибензоата в условиях, описанных в методике по показателю «Родственные соединения» или «Посторонние примеси» в АФС. Консерванты в препаратах определяются количественно, и при использовании подвижной фазы с кислотой (муравьиная кислота (99,7%) : ацетонитрил для хроматографии : тетрагидрофуран : вода (2,3:200:265:535)) разделение пиков метилпарагидроксибензоата, гидрокортизона ацетата и пропилпарагидроксибензоата происходит хорошо, но возникает вторая проблема: пик гидрокортизона ацетата не разделяется с примесью кортизоном ацетататом. Подводя итог вышесказанному, из предшествующего уровня техники не удалось выявить способов, позволяющих разделить четыре пика: гидрокортизон ацетат, кортизон ацетат, метилпарагидроксибензоат и пропилпарагидроксибензоат. Существует необходимость исследования и разработки способов хроматографического разделения данных пиков, так как это необходимо для разработки методик контроля качества ГЛФ.
Задачей настоящего изобретения является разработка хроматографического способа разделения четырех составляющих: гидрокортизон ацетат, кортизон ацетат, метилпарагидроксибензоат и пропилпарагидроксибензоат.
Авторы данного изобретения установили, что, добавляя в подвижную фазу второй органический модификатор (метанол для жидкостной хроматографии в количестве, сопоставимом с количеством ацетонитрила для хроматографии): метанол для жидкостной хроматографии - ацетонитрил для хроматографии - вода (200:240:560 об/об/об), удалось разделить все четыре компонента и предложили способ хроматографического разделения.
Подвижная фаза. Смешивают метанол для жидкостной хроматографии, ацетонитрил для хроматографии и воду в объемном соотношении 200:240:560, перемешивают, фильтруют через мембранный фильтр из регенерированной целлюлозы с размером пор 0,45 мкм и дегазируют любым удобным способом.
Раствор используют свежеприготовленным.
Растворитель. Смешивают ацетонитрил для хроматографии, тетрагидрофуран и воду в объемном соотношении 20:20:60. Раствор используют свежеприготовленным.
Испытуемый раствор. Около 500 мг (точная навеска) мази или крема помещают в коническую колбу вместимостью 50 мл, прибавляют 10,0 мл растворителя, перемешивают при нагревании на водяной бане, охлаждают раствор до комнатной температуры и фильтруют через бумажный фильтр «синяя лента», отбрасывая первые 2 мл фильтрата. Полученный раствор фильтруют через мембранный фильтр из регенерированной целлюлозы с размером пор 0,45 мкм, отбрасывая первые 2 мл фильтрата (концентрация гидрокортизона ацетата 0,5 мг/мл).
Раствор используют свежеприготовленным.
Раствор «плацебо». 495 мг смеси вспомогательных веществ, входящих в состав мази или крема в соответствующих пропорциях, помещают в коническую колбу вместимостью 50 мл, прибавляют 10,0 мл растворителя, перемешивают при нагревании на водяной бане, охлаждают раствор до комнатной температуры и фильтруют через бумажный фильтр «синяя лента», отбрасывая первые 2 мл фильтрата. Полученный раствор фильтруют через мембранный фильтр из регенерированной целлюлозы с размером пор 0,45 мкм, отбрасывая первые 2 мл фильтрата.
Раствор используют свежеприготовленным.
Раствор сравнения гидрокортизона ацетата. Около 10,0 мг (точная навеска) стандартного образца гидрокортизона ацетата (USP RS, BP CRS, ЕР CRS) помещают в мерную колбу вместимостью 100 мл, прибавляют 50 мл растворителя, обрабатывают ультразвуком в течение 10 мин, охлаждают раствор до комнатной температуры, доводят объем раствора растворителем до метки и перемешивают.
1,0 мл полученного раствора помещают в мерную колбу вместимостью 10 мл, доводят объем раствора растворителем до метки и перешивают (концентрация гидрокортизона ацетата 0,01 мг/мл).
Раствор используют свежеприготовленным.
Раствор для проверки чувствительности хроматографической системы. 5,0 мл раствора сравнения гидрокортизона ацетата помещают в мерную колбу вместимостью 200 мл, доводят объем раствора растворителем до метки и перемешивают (концентрация гидрокортизона ацетата 0,00025 мг/мл).
Раствор используют свежеприготовленным.
Исходный раствор кортизона ацетата. 10,0 мг стандартного образца кортизона ацетата (USP RS, ЕР CRS, BP CRS) помещают в мерную колбу вместимостью 100 мл, прибавляют 50 мл растворителя, обрабатывают ультразвуком в течение 10 мин, охлаждают раствор до комнатной температуры, доводят объем раствора растворителем до метки и перемешивают.
Раствор используют свежеприготовленным.
Исходный раствор метилпарагидроксибензоата. 8,0 мг стандартного образца метилпарагидроксибензоата (ЕР CRS) или стандартного образца метилпарабена (USP RS) помещают в мерную колбу вместимостью 20 мл, прибавляют 10 мл растворителя, обрабатывают ультразвуком в течение 5 мин, доводят объем раствора растворителем до метки и перемешивают.
Раствор используют свежеприготовленным.
Исходный раствор пропилпарагидроксибензоата. 10,0 мг стандартного образца пропилпарагидроксибензоата (ЕР CRS) или стандартного образца пропилпарабена (USP RS) помещают в мерную колбу вместимостью 100 мл, прибавляют 50 мл растворителя, обрабатывают ультразвуком в течение 5 мин, доводят объем раствора растворителем до метки и перемешивают.
Раствор используют свежеприготовленным.
Раствор для проверки пригодности хроматографической системы. 5,0 мг стандартного образца гидрокортизона ацетата (USP RS, BP CRS, ЕР CRS) помещают в мерную колбу вместимостью 10 мл, прибавляют 1,0 мл исходного раствора кортизона ацетата, 1,0 мл исходного раствора метилпарагидроксибензоатата и 1,0 мл исходного раствора пропилпарагидроксибензоатата, обрабатывают ультразвуком в течение 10 мин, охлаждают раствор до комнатной температуры, доводят объем раствора растворителем до метки и перемешивают (концентрация гидрокортизона ацетата 0,5 мг/мл, кортизона ацетата 0,01 мг/мл, метилпарагидроксибензоата 0,04 мг/мл, пропилпарагидроксибензоата 0,01 мг/мл).
Раствор используют свежеприготовленным.
Хроматографические условия:
- колонка: 250×4,6 мм, размер частиц 5 мкм, заполненная сорбентом силикагель октадецилсилильный, например Zorbax Eclipse XDB С18 или аналогичная, для которой выполняются условия пригодности хроматографической системы,
- скорость потока: 1,2 мл/мин,
- температура колонки: 30°С,
- детектор: УФ, 254 нм,
- объем пробы: 10 мкл.
Подвижная фаза: метанол для жидкостной хроматографии - ацетонитрил для хроматографии - вода (200:240:560).
Время хроматографирования испытуемого раствора не менее 2,5 времени удерживания пика гидрокортизона ацетата.
Время удерживания пика гидрокортизона ацетата около 21 мин.
Предложенные условия являются предпочтительными, но при необходимости могут быть изменены для обеспечения пригодности хроматографической системы.
Допускается незначительно изменять содержание метанола для жидкостной хроматографии в подвижной фазе, для достижения требуемого разрешения между пиками пропилпарагидроксибензоата и гидрокортизона ацетата, и между пиками гидрокортизона ацетата и кортизона ацетата.
По 10 мкл раствора для проверки чувствительности хроматографической системы, раствора для проверки пригодности хроматографической системы, раствора сравнения гидрокортизона ацетата (получая не менее трех хроматограмм), растворителя, раствора «плацебо» и испытуемого раствора хроматографируют на жидкостном хроматографе с УФ-спектрофотометрическим детектором.
Проверка пригодности хроматографической системы.
Хроматографическая система считается пригодной, если на хроматограмме раствора сравнения гидрокортизона ацетата:
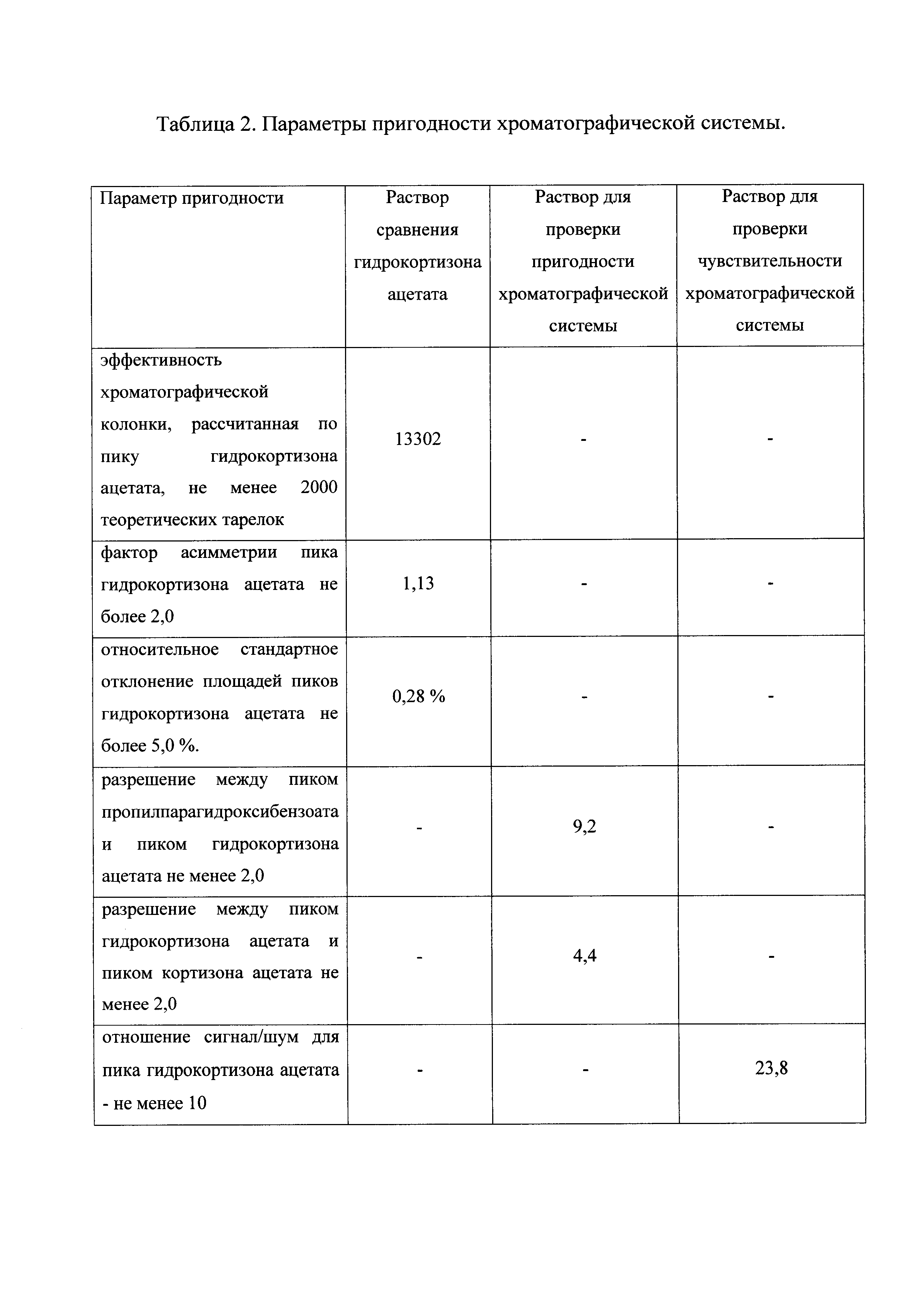
- эффективность хроматографической колонки, рассчитанная по пику гидрокортизона ацетата, не менее 2000 теоретических тарелок,
- фактор асимметрии пика гидрокортизона ацетата не более 2,0.
- относительное стандартное отклонение площадей пиков гидрокортизона ацетата не более 5,0%.
На хроматограмме раствора для проверки пригодности хроматографической системы:
- разрешение между пиком пропилпарагидроксибензоата и пиком гидрокортизона ацетата не менее 2,0,
- разрешение между пиком гидрокортизона ацетата и пиком кортизона ацетата не менее 2,0,
На хроматограмме раствора для проверки чувствительности хроматографической системы: отношение сигнал/шум для пика гидрокортизона ацетата - не менее 10.
Содержание любой единичной примеси в препарате в процентах (X) вычисляют по формуле:
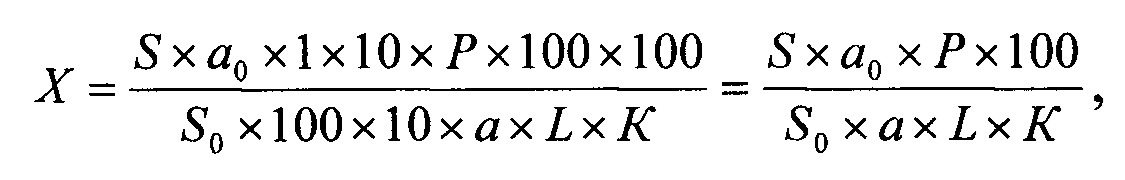
где
S - площадь пика любой единичной примеси на хроматограмме испытуемого раствора,
S0 - площадь пика гидрокортизона ацетата на хроматограмме раствора сравнения гидрокортизона ацетата,
а0 - навеска стандартного образца гидрокортизона ацетата, в миллиграммах,
а - навеска препарата, в миллиграммах,
Р - содержание гидрокортизона ацетата в стандартном образце в миллиграммах на миллиграмм (USP RS), в процентах (BP CRS, ЕР CRS),
К - коэффициент учета выражения концентрации основного вещества в стандартном образце гидрокортизона ацетата (k=1 для USP RS k=100 для BP CRS, ЕР CRS),
L - заявленное содержание гидрокортизона ацетата в препарате в процентах.
Сумму примесей в процентах рассчитывают путем сложения содержания любых единичных примесей.
При расчете не учитывают пики, относящиеся к растворителю, пики «плацебо», (включая пик метилпарагидроксибензоата с относительным временем удерживания около 0,24 относительно пика гидрокортизона ацетата, пропилпарагидроксибензоата с относительным временем удерживания около 0,73 относительно пика гидрокортизона ацетата, а также пики с площадью, равной или менее площади пика гидрокортизона ацетата на хроматограмме раствора для проверки чувствительности хроматографической системы (0,05% и менее 0,05%)).
Нормы.
Любая единичная примесь - не более 2,0%, сумма примесей - не более 4,0%.
Используя данный способ, удалось разделить все интересующие пики и рассчитать содержание родственных соединений в препарате.
Параметры пригодности хроматографической системы удовлетворяют заявленным требованиям и приведены в таблице 2.
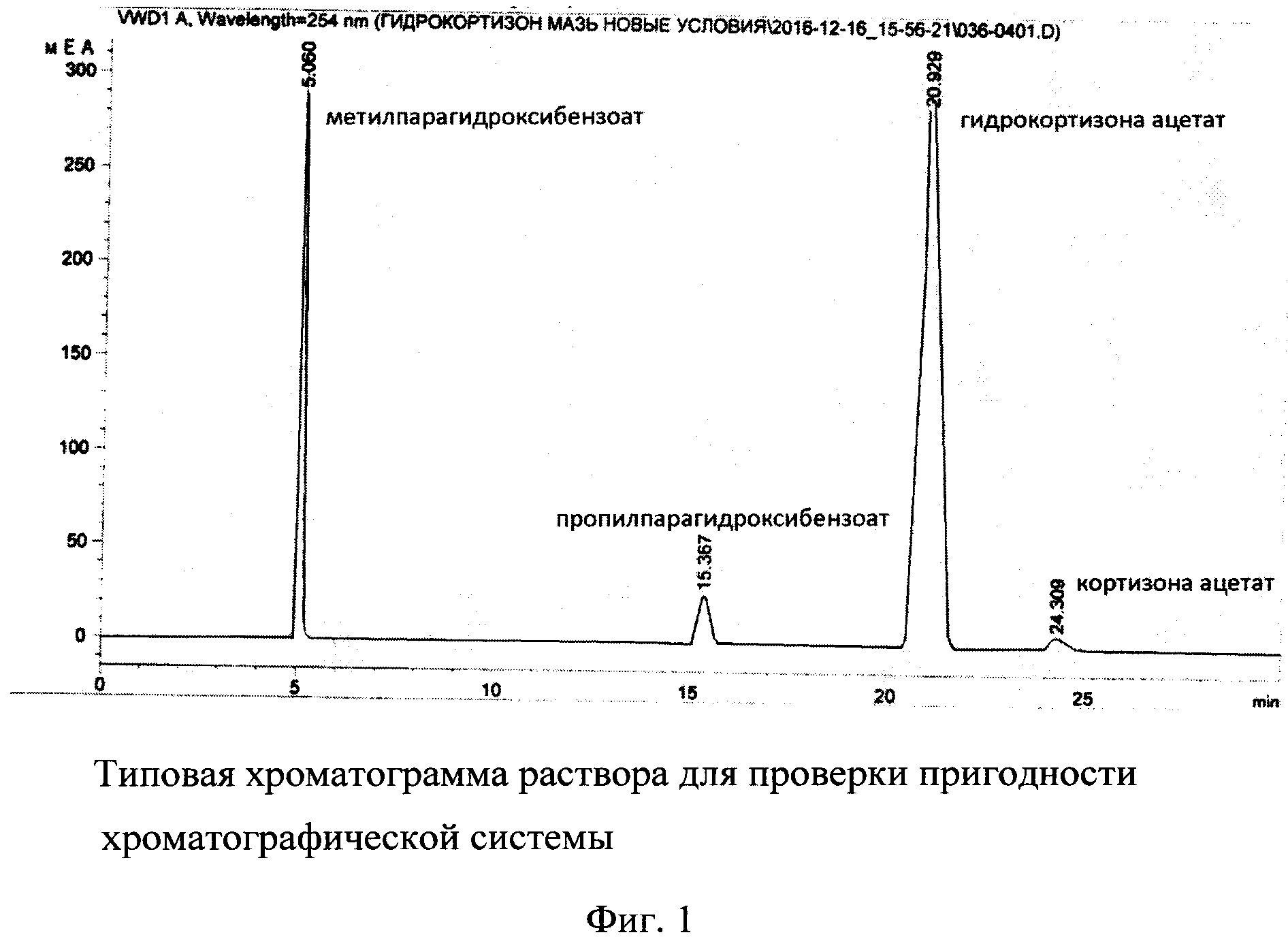
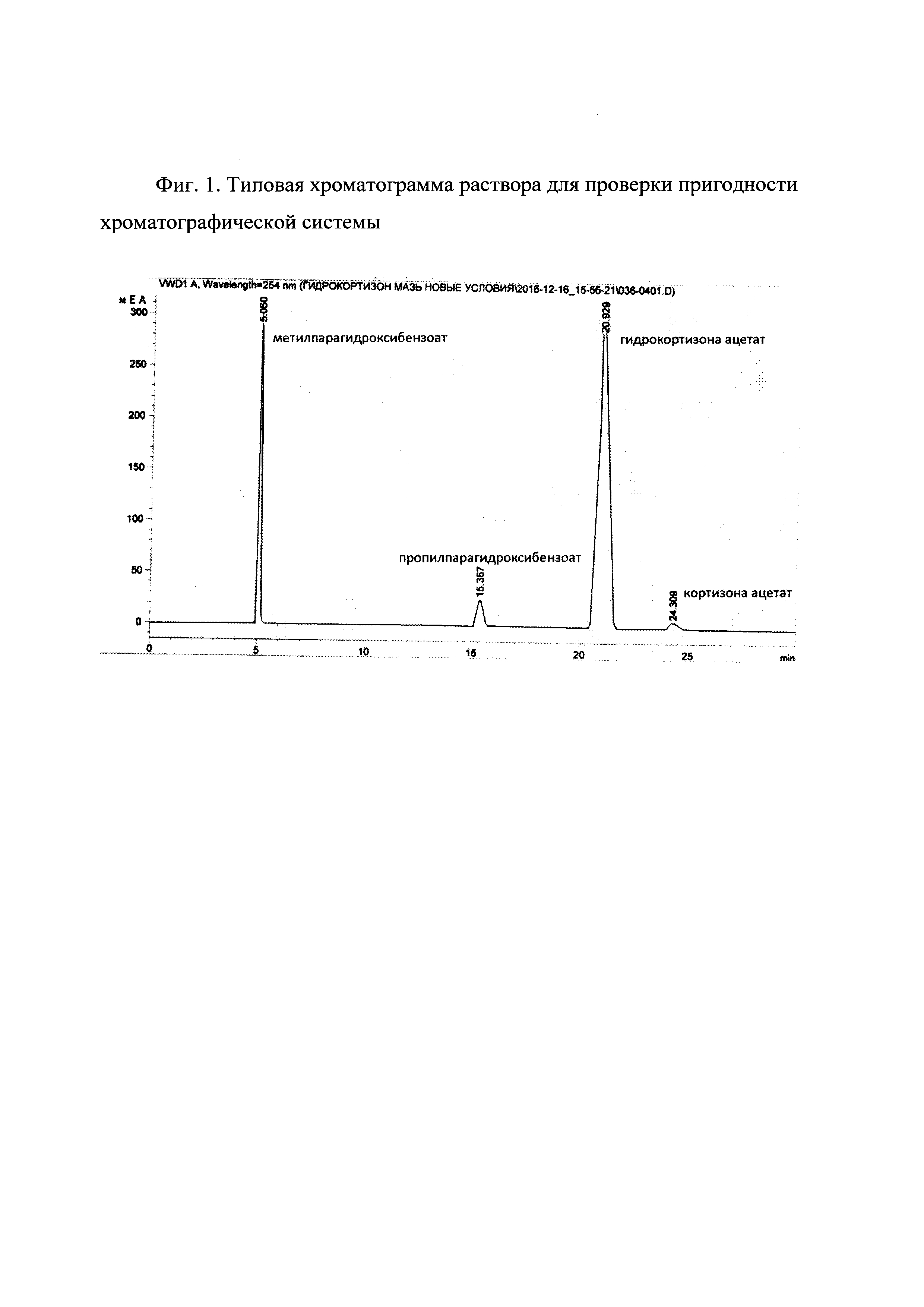
Типовая хроматограмма раствора для проверки пригодности хроматографической системы представлена на Фиг. 1.
Как видно на представленной хроматограмме (Фиг. 1), пики всех четырех компонентов раствора для проверки пригодности хроматографической системы хорошо разделяются.
Таким образом, экспериментальным путем были подобраны оптимальные условия хроматографического разделения гидрокортизона ацетата, кортизона ацетата, метилпарагидроксибензоата, пропилпарагидроксибензоата методом обращенно-фазовой высокоэффективной жидкостной хроматографии. Предложенный способ удовлетворяет стандартным требованиям проверки пригодности хроматографической системы и позволяет разделить пики анализируемых веществ в гидрокортизоне креме или мази.