Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ МЕТИЛДОПЫ В ПЛАЗМЕ КРОВИ ЧЕЛОВЕКА
Вид РИД
Изобретение
Изобретение относится к фармации, а именно к фармацевтической химии.
Метилдопа - это антигипертензивное средство центрального действия. Согласно международным и отечественным рекомендациям данный препарат является препаратом первой линии для лечения гипертонии беременных. Его применение направлено на предупреждение развития сердечно-сосудистых осложнений и улучшение ближайшего и отдаленного прогноза со стороны матери и будущего ребенка. Создание воспроизведенного препарата метилдопы может сделать данное лекарственное средство более доступным по цене для пациентов. Для подтверждения биоэквивалентности оригинального лекарственного препарата и дженерика требуются надежные методики количественного определения лекарственных веществ в плазме крови. Согласно требованиям международной нормативной документации предел количественного определения биоаналитических методик должен составлять не более 5% от максимальной концентрации лекарственного вещества в плазме крови (Cmax). Для лаборатории, которая проводит данные исследования, также важна высокая производительность процесса подготовки проб и аналитических процедур. В связи с этим большое значение имеет разработка новых точных и объективных методик, обеспечивающих высокую чувствительность при минимальной пробоподготовке.
Известен способ количественного определения метилдопы в плазме крови человека, заключающийся в том, что к плазме крови пациента добавляют раствор внутреннего стандарта фенилдопы, проводят жидкостно-жидкостную экстракцию дихлорметаном и измеряют концентрацию в диапазоне от 0,02 до 5 мкг/мл метилдопы методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием по калибровочному графику (Olivera С.Н., Barrientos-Astigarraga R.E., Sucupira M.et al., Journal of Chromatography B, 768, pp. 341-348, 2002). Однако данный способ имеет ряд недостатков: длительная пробоподготовка за счет использования жидкостно-жидкостной экстакции, низкая точность.
Наиболее близким аналогом (прототипом) предлагаемого решения является способ, заключающийся в том, что плазму крови, полученную от пациента, подвергают депротеинизации метанолом, затем после центрифугирования в надосадочной жидкости проводят измерение концентрации метилдопы в диапазоне от 0,32 до 20 мкг/мл методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием при следующих условиях хроматографического разделения и ионизации (Vlase L., Mihu D., Рора D.S. et al., Studia UBB chemia, 58, pp. 31-41, 2013):
Колонка: Zorbax SB-C18 (150×4,6 мм, 5 мкм)
Подвижная фаза: ацетонитрил и раствор муравьиной кислоты 0,2% в объемном соотношении 98:2 соответственно
Температура термостата: 40°С
Скорость потока: 0,8 мл/мин.
Способ ионизации: электрораспыление, полярность: положительная
Расчет концентрации проводят по калибровочному графику.
Однако данный способ имеет ряд недостатков: низкая чувствительность и точность.
Цель предлагаемого способа - повышение точности и объективности количественного определения метилдопы в плазме крови.
Поставленная цель достигается тем, что для депротеинизации плазмы применяют раствор дейтерированного внутреннего стандарта метилдопы в метаноле, хроматографическое разделение компонентов матрицы проводят с использованием двух хроматографических колонок Phenomenex Lima Phenyl-Hexyl (50×3,0 мм, 5 мкм) и Phenomenex Synergi Fusion - RP 80A (150×4,6 мм, 4 мкм), а электрораспылительную ионизацию осуществляют одновременно с химической ионизацией при атмосферном давлении.
Новизна способа заключается в депротеинизации плазмы раствором дейтерированного внутреннего стандарта метилдопы в метаноле, хроматографическом разделении компонентов матрицы с использованием двух хроматографических колонок Phenomenex Luna Phenyl-Hexyl (50×3,0 мм, 5 мкм) и Phenomenex Synergi Fusion - RP 80A (150×4,6 мм, 4 мкм) и использовании электрораспылительной ионизации одновременно с химической ионизацией при атмосферном давлении.
Технические решения, имеющие признаки, совпадающие с отличительными признаками предлагаемого нами способа, не выявлены, что позволяет сделать вывод о соответствии предлагаемого способа критерию «изобретательский уровень».
Предлагаемый способ осуществляется следующим образом: из плазмы крови отбирают аликвоту объемом 100 мкл, переносят ее в пробирку, добавляют 400 мкл раствора внутреннего стандарта дейтерированной метилдопы в концентрации 0,125 мкг/мл, затем пробирку закрывают, полученную смесь перемешивают на вортексе в течение 30 с при частоте около 2400 мин-1, подвергают центрифугированию в течение 10 мин при 3500 об/мин и температуре +4°С. Затем проводят хромато-масс-спектрометрическое определение при следующих условиях:
Колонка №1: Phenomenex Luna Phenyl-Hexyl, 50×3,0 мм, 5 мкм;
Колонка №2: Phenomenex Synergi Fusion - RP 80A, 150×4,6 мм, 4 мкм;
Температура термостата: 25°С;
Объем вводимой пробы: 8 мкл;
Подвижная фаза: метанол, деионизированная вода и формиатный буферный раствор в концентрации 80 ммоль/л в объемном соотношении 4:4:2 соответственно;
Скорость потока насоса А: до 1,25 мин анализа - 0,4 мл/мин, с 1,25 мин по 4,25 мин - 1,0 мл/мин, с 4,25 мин до конца анализа (8 мин) - 0,4 мл/мин;
Скорость потока насоса В: 0,4 мл/мин;
Положения шестипортового крана: до 0,75 мин поток элюента с колонки №1 направляется на слив, с 0,75 мин до 1,05 мин поток элюента с колонки №1 направляется на колонку №2, с 1,05 мин до конца анализа поток элюента с колонки №1 направляется на слив, с колонки №2 - в масс-спектрометрический детектор;
Способ ионизации: химическая ионизация при атмосферном давлении одновременно с электрораспылительной, полярность: положительная.
Для детекции аналита и внутреннего стандарта были подобраны следующие параметры масс-спектрометрического детектора:
Поток распыляющего газа: 3 л/мин;
Поток нагревающего газа: 5 л/мин;
Поток осушающего газа: 15 л/мин;
Напряжение электроспрея: 4000 Вт;
Температура интерфейса: 350°С;
Температура нагревательного блока: 300°С;
Температура линии десольватации: 250°С;
Давление газа в ячейке соударений: 270 кПа;
Режим детектирования метилдопы: MRM - m/z - 211,95→138,90;
Режим детектирования внутреннего стандарта: MRM - m/z - 214,95→169,00.
Данные параметры индивидуальны для каждой модели масс-спектрометрического детектора.
Расчет концентрации метилдопы проводят путем сравнения соотношения площадей пиков метилдопы и дейтерированного внутреннего стандарта метилдопы со значениями данных соотношений в калибровочной зависимости, которая построена предварительно перед проведением анализа на модельных смесях в диапазоне от 0,020 до 3 мкг/мл, и если полученное соотношение площадей пиков укладывается в диапазон значений соотношений калибровочной зависимости, то концентрация метилдопы в плазме рассчитывается по линейному уравнению данной зависимости
x=(y-b)/а,
где x - измеренная концентрация метилдопы в плазме;
y - соотношение площадей пиков "аналит-внутренний стандарт";
a - наклон калибровочной кривой;
b - свободный член.
В рамках апробации способа проводилось определение концентрации метилдопы при исследовании биоэквивалентности препаратов таблеток "Метилдопа" в дозировке 250 мг (ЗАО «Р-Фарм», Россия, серия 20614) и таблеток "Допегит", содержащих метилдопу в дозировке 250 мг (ОАО "Фармацевтический завод ЭГИС", Венгрия, серии D358N1014 и A358N0813) на 24 испытуемых.
В процессе разработки способа была проведена его валидация на модельных смесях по показателям селективность, нижний предел количественного определения, линейность калибровочных кривых, внутрисерийная и межсерийная прецизионность и точность, эффект переноса предыдущей пробы, степень извлечения, тест на разведение образца, оценка эффекта матрицы, стабильность согласно руководству ЕМЕА (Guideline on bioanalytical method validation, EMEA, 192217, 2009) и руководству по экспертизе лекарственных средств (А.Н. Миронов (ред.), Руководство по экспертизе лекарственных средств, т. 1, Москва, 2013). Данный способ соответствует всем установленным требованиям.
В рамках валидации проводилась оценка показателей «калибровочная кривая» и «нижний предел количественного определения» путем анализа модельных смесей плазмы, содержащей метилдопу, на 8 уровнях концентраций в диапазоне от 0,02 до 3 мкг/мл. Для приготовления данных модельных смесей к 950 мкл плазмы добавляли 50 мкл стандартного раствора метилдопы в ацетонитриле. Концентрации стандартных растворов представлены в таблице 1:
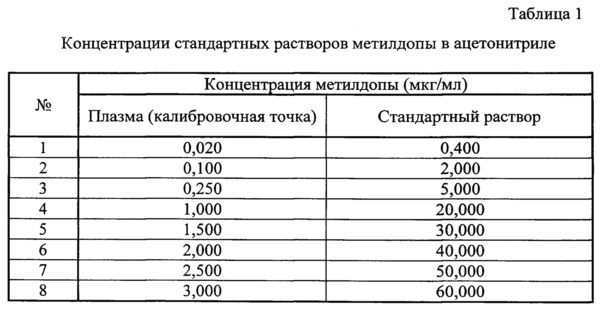
Каждую пробу анализировали 6 раз: измеряли соотношение площадей пиков «аналит / внутренний стандарт». По средним значениям данных соотношений был построен калибровочный график, уравнение которого: x=(y-0,0514)/1,4679, где y - соотношение площадей пиков «аналит-внутренний стандарт», x - измеренная концентрация метилдопы в плазме. По данному уравнению рассчитывались концентрации данных градуировочных образцов: значения не менее 75% концентраций должны быть в пределах ±15% от номинальных значений (для нижнего предела количественного определения в пределах ±20%), коэффициент вариации (CV) не должен превышать 15% (для нижнего предела количественного определения - 20%). Полученные результаты представлены в таблице 2.
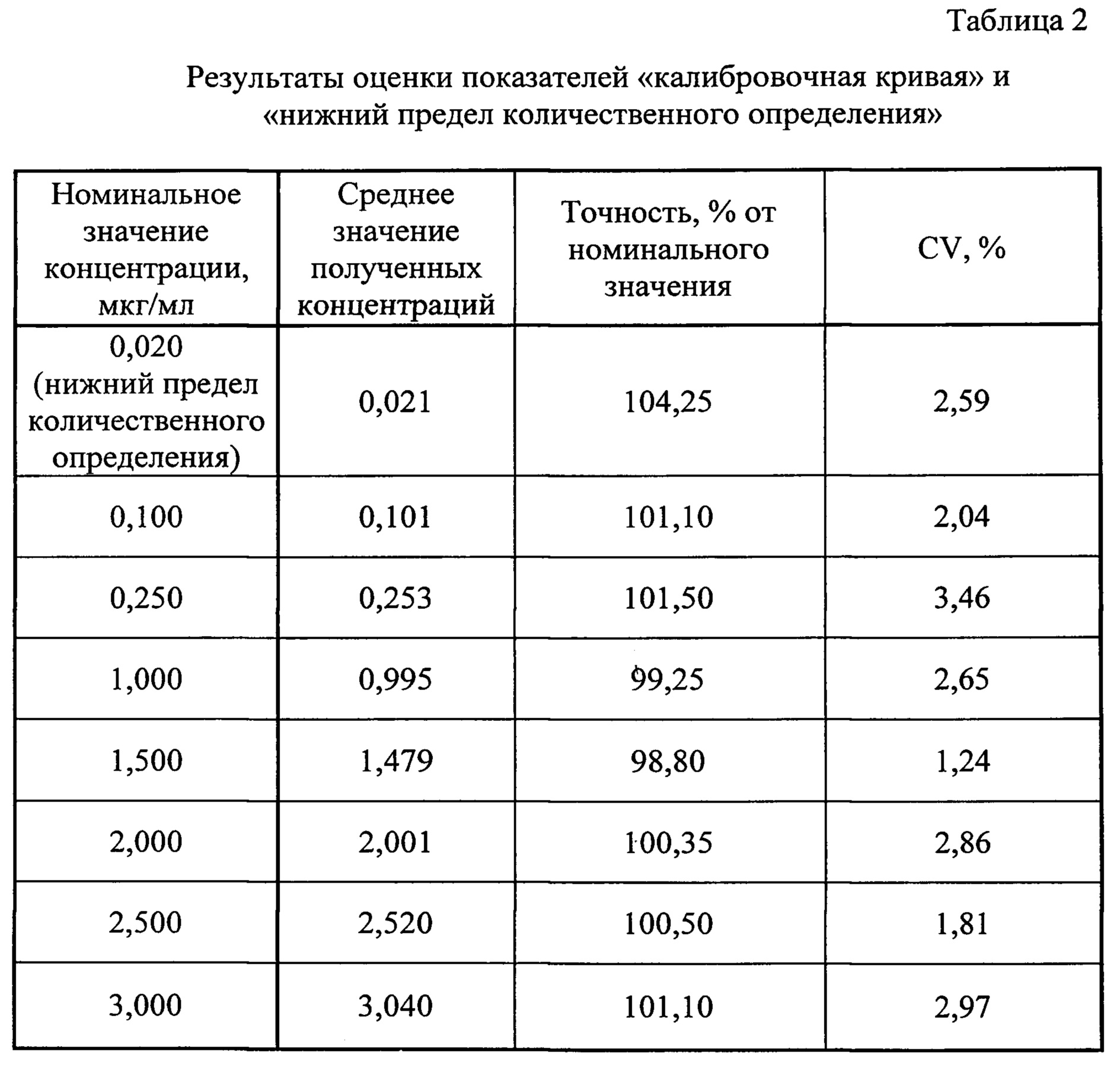
Из данных, приведенных в таблицы 2, видно, что способ соответствует критериям приемлемости по показателям «калибровочная кривая» и «нижний предел количественного определения».
Оценка внутрисерийной и межсерийной точности и прецизионности способа оценивалась на 6 уровнях концентрации: 0,02, 0,06, 0,30, 1,20, 2,40, 3,00 мкг/мл. Для приготовления данных модельных смесей к 950 мкл плазмы добавляли 50 мкл стандартного раствора метилдопы в ацетонитриле. Концентрации стандартных растворов представлены в таблице 3.
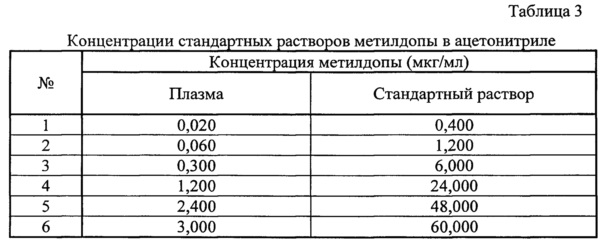
При выполнении оценки межсерийной прецизионности и точности результаты тестов, проведенных в разные дни разными лаборантами, сравниваются между собой. Прецизионность метода выражалась коэффициентами вариации. Точность оценивалась путем соотношения значения, полученного по результатам измерения, и номинального значения. Расчет концентраций выполнялся по калибровочному графику, уравнение которого: x=(y-0,0514)/1,4679, где y - соотношение площадей пиков «аналит - внутренний стандарт», x - измеренная концентрация метилдопы в плазме. Значения измеренных концентраций должны быть в пределах ±15% от номинальных значений (для нижнего предела количественного определения в пределах ±20%), коэффициент вариации (CV) не должен превышать 15% (для нижнего предела количественного определения - 20%). Полученные результаты представлены в таблице 4.
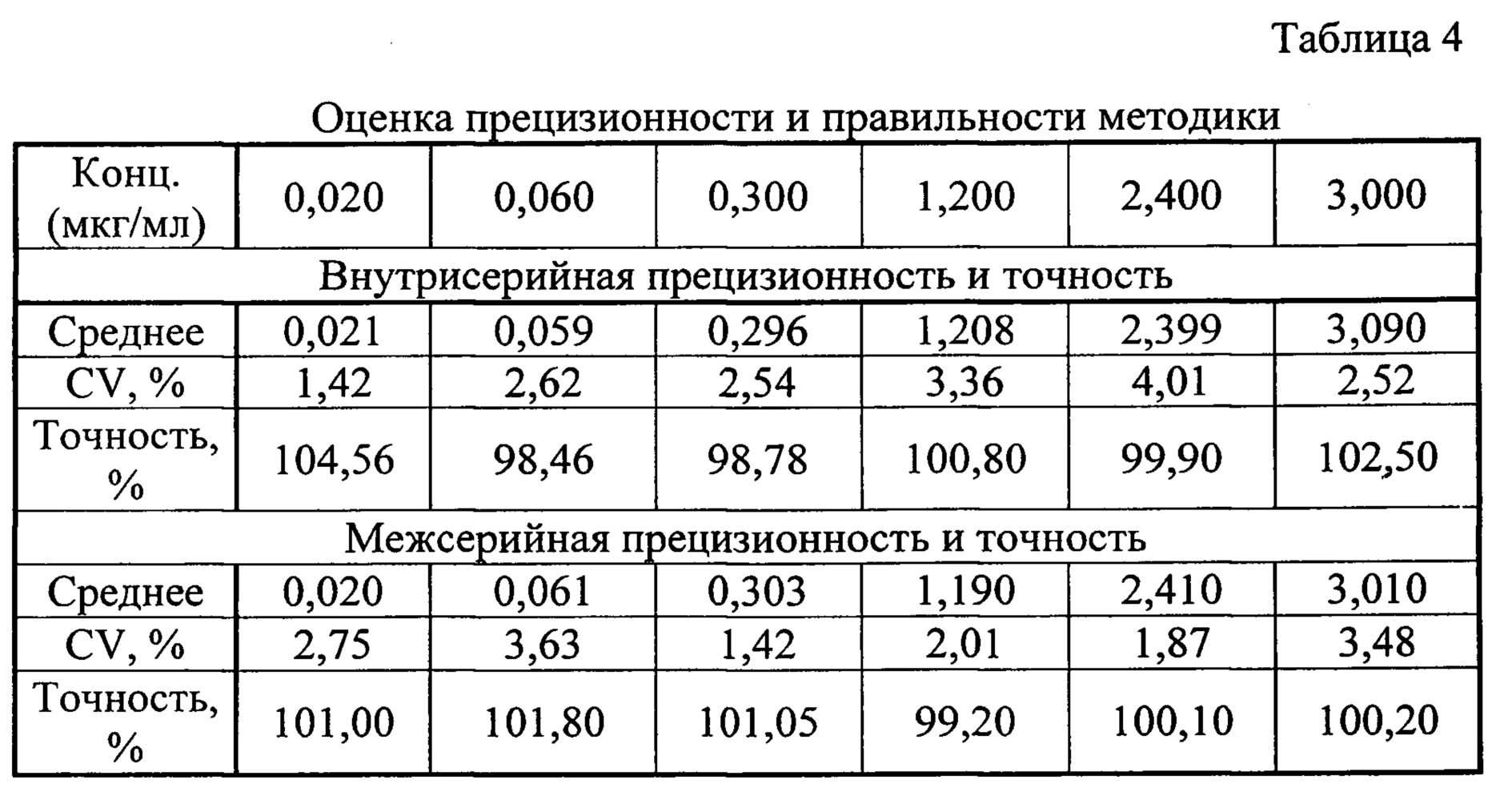
Из данных, приведенных в таблице 4, видно, что способ соответствует критериям приемлемости по показателям внутрисерийная и межсерийная прецизионность и точность.
Предлагаемый способ иллюстрируется следующими примерами использования.
Пример 1. Испытуемый М., 25 лет, принял 1 таблетку "Допегит", содержащую метилдопу в дозировке 250 мг. Затем у него проводился забор крови из вены предплечья через установленный катетер через 5 мин, 15 мин, 30 мин, 45 мин, 1 ч, 1 ч 15 мин, 1 ч 30 мин, 1 ч 45 мин, 2 ч, 2 ч 15 мин, 2 ч 30 мин, 3 ч, 4 ч, 6 ч, 9 ч, 12 ч, 18 ч, 24 ч после приема лекарственного препарата. После отбора крови пробирки направляли на центрифугирование для отделения плазмы. Затем из данных образцов отбирали аликвоту объемом 100 мкл, переносили ее в пробирку, добавляли 400 мкл раствора внутреннего стандарта дейтерированной метилдопы в концентрации 0,125 мкг/мл, затем пробирку закрывали, полученную смесь перемешивали на вортексе в течение 30 с при частоте около 2400 мин-1, подвергали центрифугированию в течение 10 мин при 3500 об/мин и температуре +4°С. Хромато-масс-спектрометрическое определение концентрации метилдопы в надосадочной жидкости проводили с применением двух хроматографических колонок Phenomenex Luna Phenyl-Hexyl (50×3,0 мм, 5 мкм) и Phenomenex Synergi Fusion - RP 80A (150×4,6 мм, 4 мкм) и использовании электрораспылительной ионизации одновременно с химической ионизацией при атмосферном давлении. Для расчета концентрации метилдопы применялся калибровочный график, уравнение которого: х=(у+0,021)/1,3512, где y - соотношение площадей пиков «аналит - внутренний стандарт», x - измеренная концентрация метилдопы в плазме. Полученные значения концентраций представлены в таблице 5.
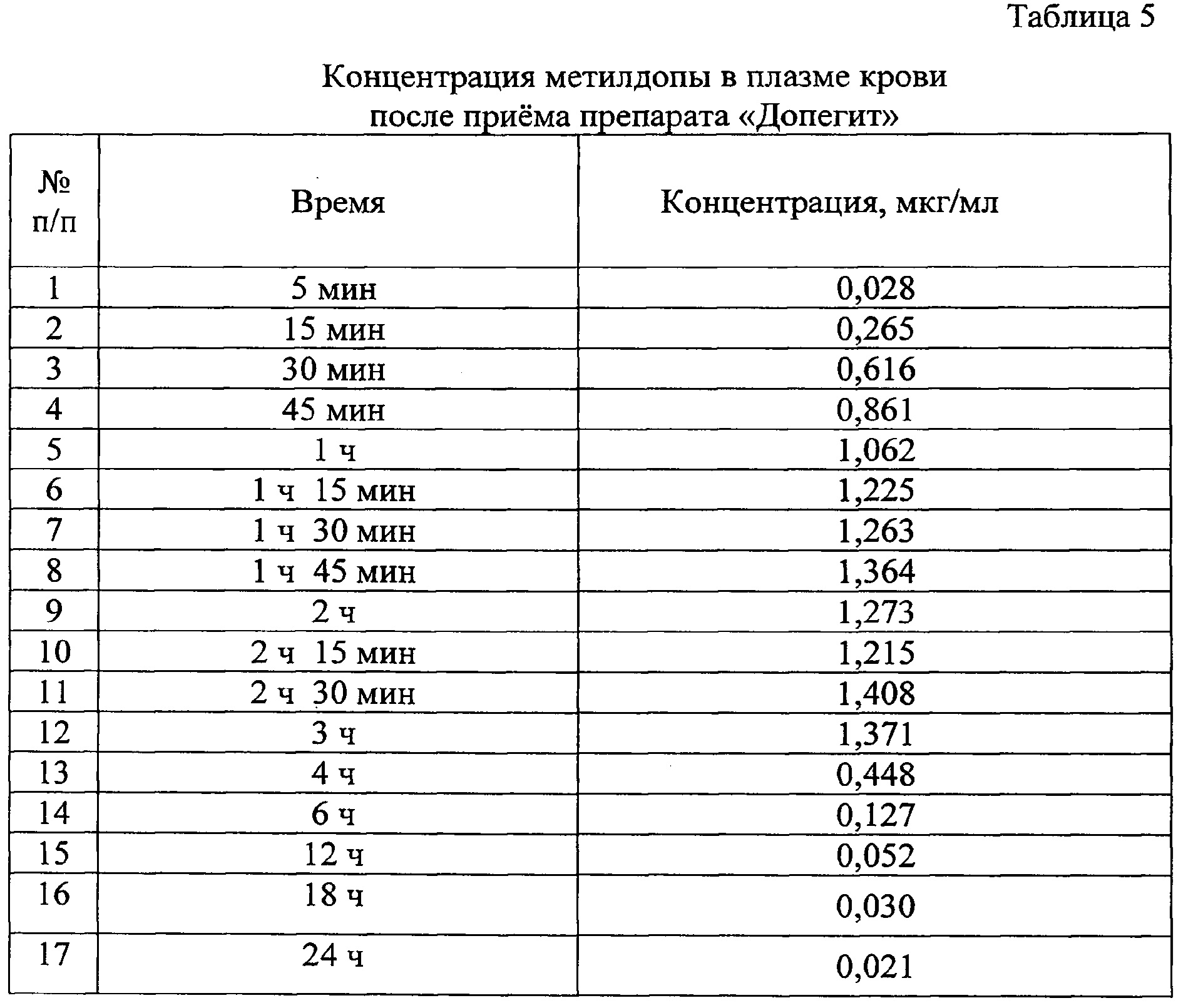
Часть результатов определения концентраций метилдопы в плазме была подтверждена с помощью способа-прототипа (Vlase L., Mihu D., Рора D.S. et al., Studia UBB chemia, 58, pp. 31-41, 2013). Так концентрация метилдопы через 1 час после отбора составила 1,040 мкг/мл - расхождение составило 2,11%, через 4 часа - 0,460 мкг/мл - расхождение составило 2,6%, что укладывается в допустимый диапазон точности: ±15% от измеренной концентрации.
Таким образом, разработанный способ позволяет измерить концентрацию метилдопы в плазме крови пациента в диапазоне от 0,02 до 3 мкг/мл.
Предлагаемый способ применен для определения концентрации метилдопы в плазме крови в лаборатории ООО "Квинта-Аналитика Ярославль".
Способ определения концентрации метилдопы в плазме крови человека, заключающийся в том, что из плазмы отбирают аликвоту, подвергают ее депротеинизации, полученную смесь центрифугируют, в надосадочной жидкости измеряют концентрацию метилдопы методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием в диапазоне от 0,020 до 3 мкг/мл по калибровочному графику, отличающийся тем, что для депротеинизации применяют раствор дейтерированного внутреннего стандарта метилдопы в метаноле, хроматографическое разделение компонентов матрицы проводят с использованием двух хроматографических колонок Phenomenex Luna Phenyl-Hexyl (50×3,0 мм, 5 мкм) и Phenomenex Synergi Fusion - RP 80A (150×4,6 мм, 4 мкм), а электрораспылительную ионизацию осуществляют одновременно с химической ионизацией при атмосферном давлении.
