Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ (1S,4R)-1-ИЗОПРОПИЛ-4-МЕТИЛ-10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ
Вид РИД
Изобретение
Предлагаемое изобретение относится к области органической химии, конкретно, к способу получения (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов (1):
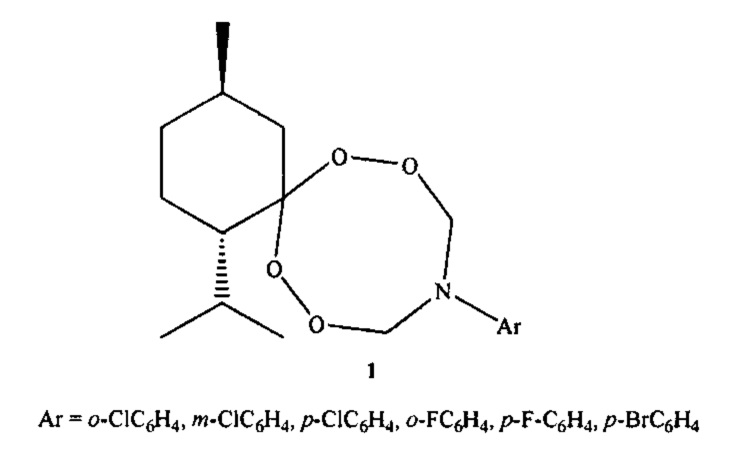
N-Содержащие тетраоксаны применяются в медицине в качестве препаратов, обладающих противомалярийной (Opsenica I., Opsenica D., Lanteri C.A., Anova L., Milhous W.K., Smith K.S., Solaja B.A. // J. Med. Chem. - 2008. - Vol. 51. - p.2261-2266), противоопухолевой и антигельминтной активностью (Vennerstrom J.L., Arbe-Barnes S., Brun R., Chavman S.A., Chiv F.C.K. // Nature. - 2004. - Vol. 430. - p.900-904).
Известен способ получения 1,2,4-диоксазолидинов формулы 3а-с с выходом 60-80% окислением раствора соответствующих иминов 2а-с в смеси петролейного эфира и бензола кислородом воздуха при -15-20°С.(Hawkins, Е.G.Е. // J. Chem. Soc. (С). - 1971. - Р. 160-166) по схеме:
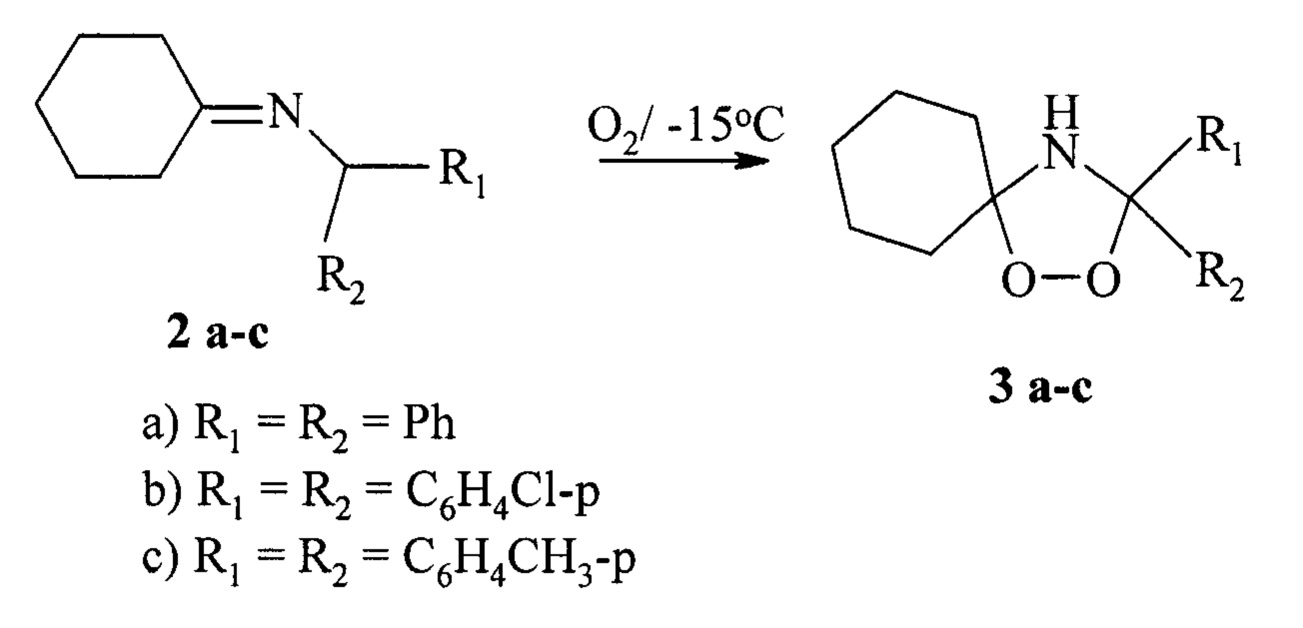
Известным способом не могут быть получены (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы общей формулы (1).
Известен способ получения бициклических 1,2,4-диоксазолидинов формулы 5 окислением озоном производных индена 4а-е в присутствии первичных аминов при -70°С (Y. Ushigoe, S. Satake, A. Masuyama, M. Nojima, K.J. McCullough // J. Chem. Soc, Perkin Trans. 1. - 1997. - P. 1939-1942).
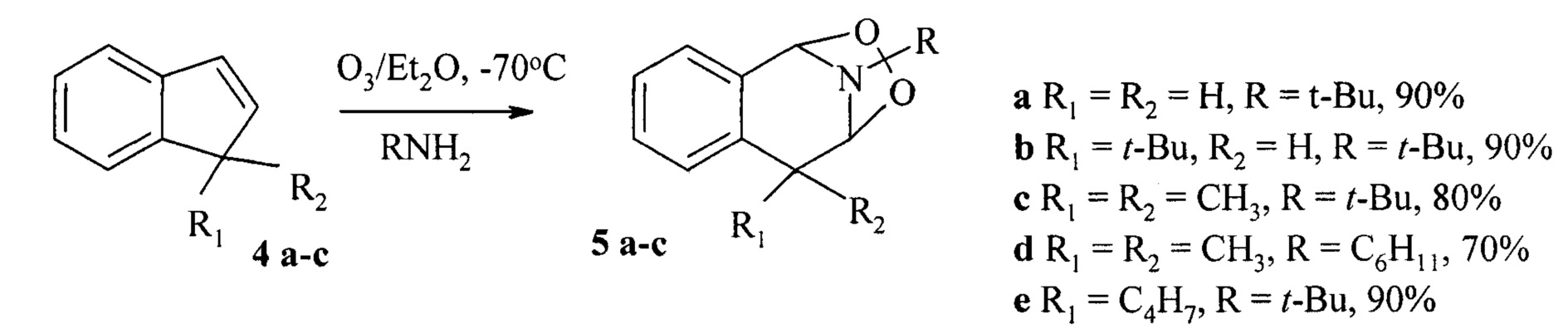
Известным способом не могут быть получены ((1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы общей формулы (1).
Известен способ получения 1,2,4- диоксазолидин-3,5-диона формулы 7 - перспективного соединения с точки зрения промышленного применения в качестве инициатора свободно-радикальной полимеризации (Hagemann, Н. // Angew. Chem., Int. Ed. - 1981. - V. 20. - №9. - P. 784). Реакцию проводили действием Н2О2 в щелочных условиях на N-метилиминодикарбонилдихлорид 6.
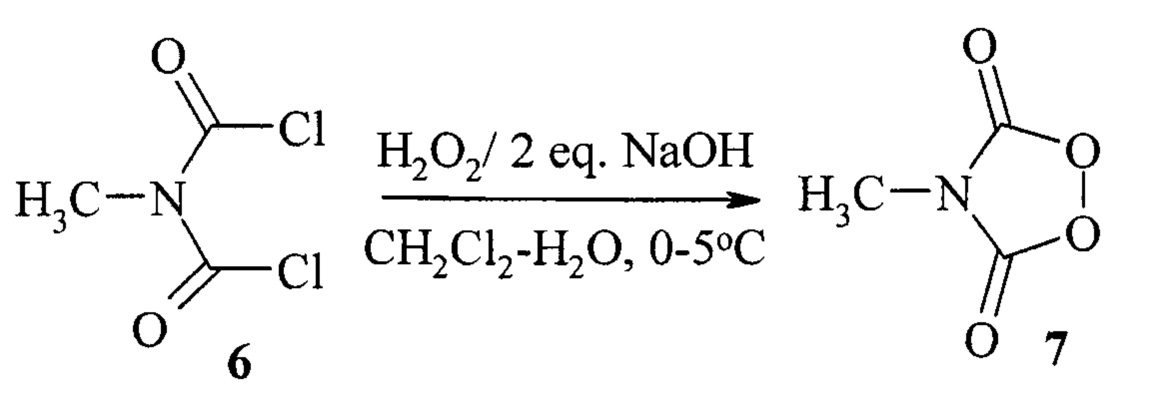
Известным способом не могут быть получены (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы общей формулы (1).
Известен способ получения N-арил-тетраоксазаспироалканов формулы (9) реакцией пентаоксаспироалканов (8) с ариламинами под действием катализатора Sm(NO3)⋅6Н2O (Makhmudiyarova, N.N., Khatmullina, G.M., Rakhimov, R.Sh., Meshcheryakova, E.S., Ibragimov, A.G., Dzhemilev, U.M. Tetrahedron. - 2016. - 72, p. 3277-3281)
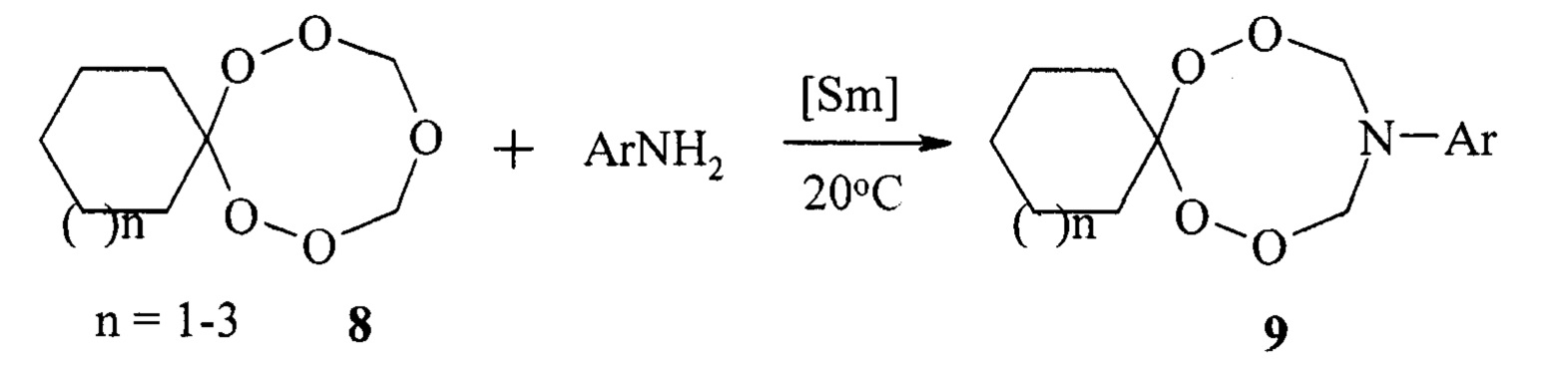
Известным способом не могут быть получены (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов формулы (1).
Предлагается новый способ селективного получения (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов общей формулы (1).
Сущность способа заключается во взаимодействии 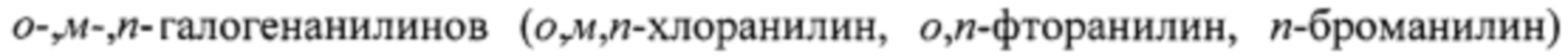 с (1S, 4R)-1 -изопропил-4-метил-7,8,10,12,13 -пентаоксаспиро[5.7]тридеканом в присутствии катализатора HfCl4, взятыми в мольном соотношении галогенанилин: (1S,4R)-1-изопропил-4-метил-7,8,10,12,13- пентаоксаспиро[5.7]тридекан: НfCl4=10:(10-12):(0.5-0.7), предпочтительно 10:11:0.5, при комнатной температуре (20°С) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч. Выход (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов (1) составляет 79-89%. Реакция протекает по схеме:
с (1S, 4R)-1 -изопропил-4-метил-7,8,10,12,13 -пентаоксаспиро[5.7]тридеканом в присутствии катализатора HfCl4, взятыми в мольном соотношении галогенанилин: (1S,4R)-1-изопропил-4-метил-7,8,10,12,13- пентаоксаспиро[5.7]тридекан: НfCl4=10:(10-12):(0.5-0.7), предпочтительно 10:11:0.5, при комнатной температуре (20°С) и атмосферном давлении в тетрагидрофуране в качестве растворителя в течение 4-6 ч. Выход (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов (1) составляет 79-89%. Реакция протекает по схеме: 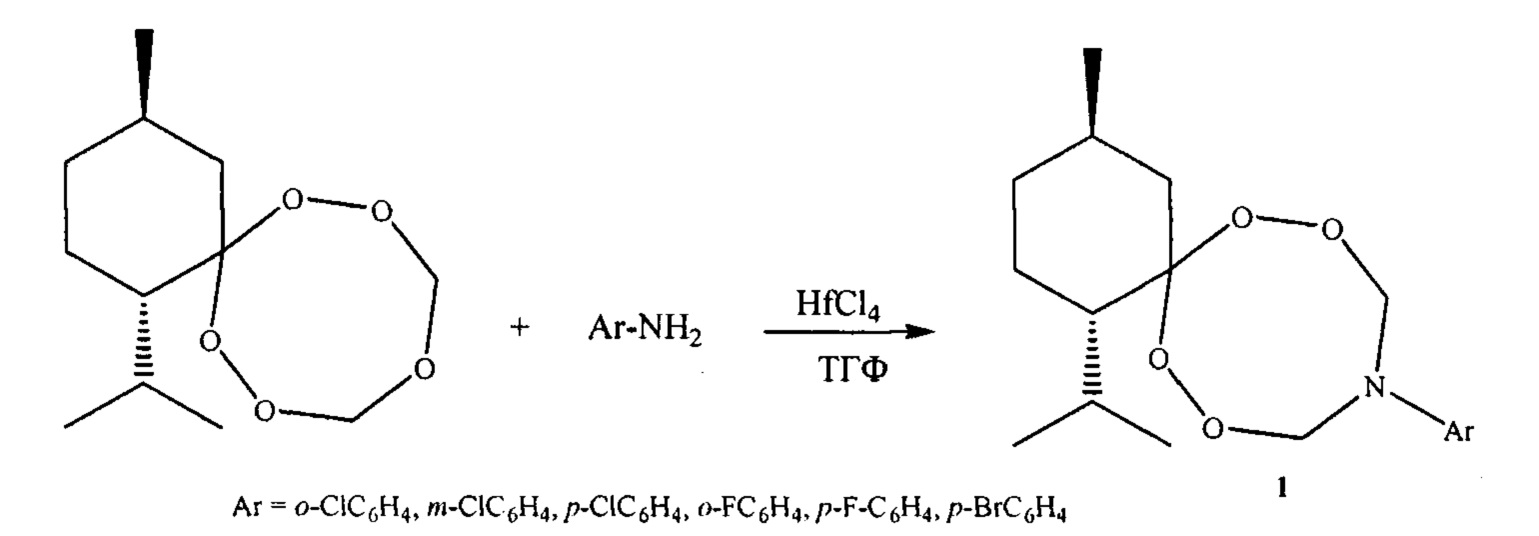
(1S,4R)-1 -изопропил-4-метил-10-арил-7,8,12,13 -тетраокса-10-азаспиро[5.7]тридеканы (1) образуются только лишь с участием 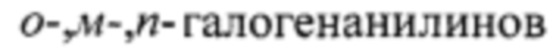 и (1S,4R)-1-изопропил-4-метил-7,8,10,12,13-пентаоксаспиро[5.7]тридеканом. В присутствии других соединений первичных аминов (например, алкиламины, гетариламины) целевые продукты (1) не образуются. Без катализатора реакция не идет.
и (1S,4R)-1-изопропил-4-метил-7,8,10,12,13-пентаоксаспиро[5.7]тридеканом. В присутствии других соединений первичных аминов (например, алкиламины, гетариламины) целевые продукты (1) не образуются. Без катализатора реакция не идет.
Проведение указанной реакции в присутствии катализатора HfCl4 больше 7 мол.% не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора HfCl4 менее 3 мол.% снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°С. При температуре выше 20°С (например, 60°С) снижается селективность реакции, и увеличиваются энергозатраты, а при температуре ниже 20°С (например, -10°С) снижается скорость реакции. Опыты проводили в тетрагидрофуране, т.к. в нем хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа:
В известном способе реакция идет с участием в качестве одного из исходных реагентов пентаоксаспироалкана и катализатора Sm(NO3)3⋅6H2O. Известный способ не позволяет получать (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы (1).
В предлагаемом способе в качестве исходных реагентов применяются (1S,4R)-1-изопропил-4-метил-7,8,10,12,13 -пентаоксаспиро[5.7]тридекан и HfCl4 в качестве катализатора. В отличие от известных способов, предлагаемый способ позволяет синтезировать индивидуальные (1S,4R)-1-изопропил-4-метил-10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы. (1).
Способ поясняется следующими примерами:
Синтез исходного (1S,4R)-1-изопропил-4-метил-7,8,10,12,13-пентаоксаспиро[5.7]тридекана. В сосуд Шленка, установленный на магнитной мешалке, при температуре ~20°С помещают 5 мл тетрагидрофурана, 1.46 мл (20 ммоль) водного раствора (37%) формальдегида и 2.04 г (10 ммоль) 1(2S,5R)-1,1-дигидроперокси-2-изопропил-5-метилциклогексан (D. Azarifar, Z. Najminejad, К. Khosravi. Synthetic Commun. 2013, 43, 826-836), затем добавляют 0.16 г (0.5 ммоль) НfCl4. Реакционную смесь перемешивают при температуре ~20°С в течение 5 ч, выделяют (1S,4R)-1-изопропил-4-метил-7,8,10,12,13-пентаоксаспиро[5.7]тридекан с выходом 75%.
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 5 мл тетрагидрофурана, 0.016 г (0.5 ммоль) HfCl4, 1.27 г (10 ммоль) о-хлоранилина, 2.04 г (11 ммоль) (1S,4R)-1-изопропил-4-метил-7,8,10,12,13-пентаоксаспиро[5.7]тридекана. Реакционную смесь перемешивают при комнатной температуре (-20°С) в течение 5 ч. Из реакционной массы выделяют (1S,4R)-1-изопропил-4-метил-10-(о-хлорфенил)-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекан с выходом 84%. Другие примеры, подтверждающие способ, приведены в табл. 1.
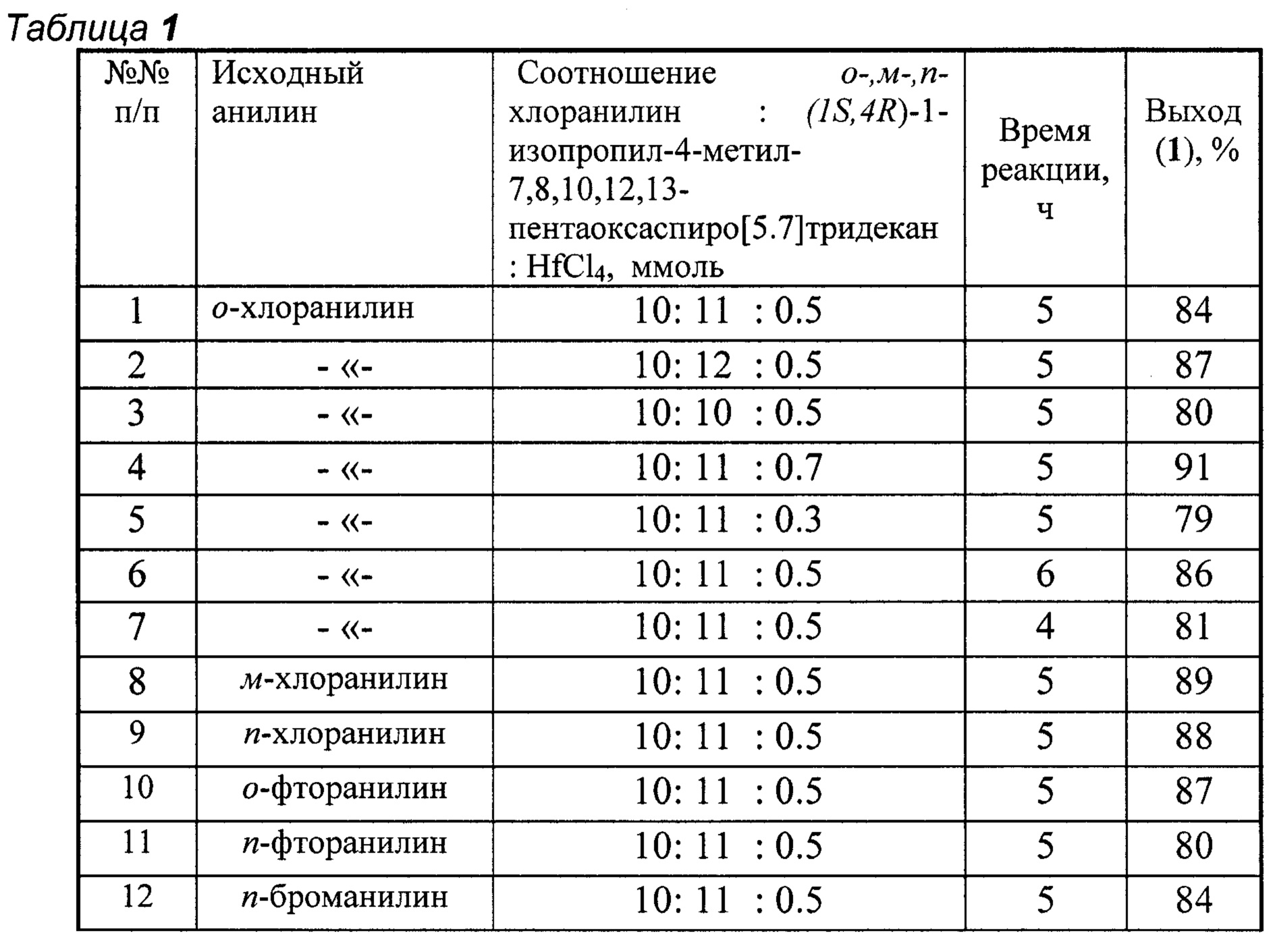
Все опыты проводили в тетрагидрофуране при комнатной температуре (~20°С).
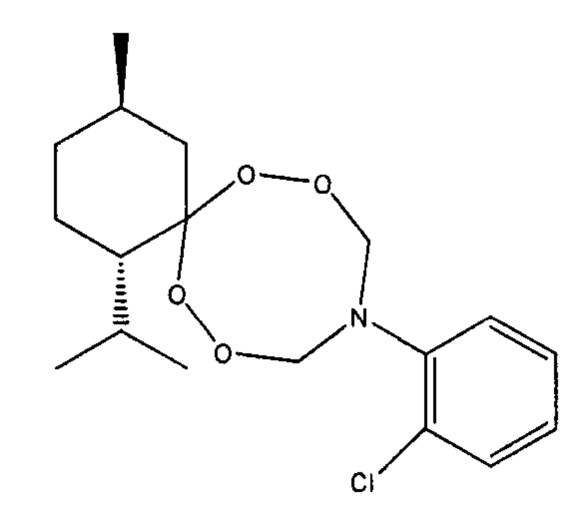
Спектральные характеристики (1S,4R)-10-(2-хлорофенил)-1-изопропил-4-метил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: δН (400 MHz, DMSO-d6, 25°С) 0.80-0.84 (m, 3Н, Н3С), 0.94-0.97 (m, 6Н, Н3С), 1.45-1.50 и 1.59-1.62 (m, 2Н, Н2С), 2.21-2.24 (m, 1Н, НС), 1.72-1.74 (m, 1Н, НС), 1.79-1.81 (m, 2Н, Н2С), 2.98-3.00 и 1.13-1.18 (m, 2Н, Н2С), 1.54-1.59 (m, 1Н, НС), 5.12-5.27 и 5.42-5.53 (m, 4Н, OH2CN), 6.72-6.75 (m, 1Н, НС), 6.92-6.95 (m, 1Н, НС), 7.13-7.17 (m, 1Н, НС), 7.27-7.30 (m, 1Н, НС); δС (100 MHz, CDCl3, 25°С) 18.74 (СН3), 21.59 (СН3), 22.95 и 23.35 (СН2), 24.84 (СН), 28.68 (СН), 34.59 (СН2), 38.83 (СН2), 50.38 (СН), 90.27 (OCH2N), 112.74 (С), 113.14 (Аr), 119.26 (Аr), 127.59 (Аr), 129.31 (Аr), 130.55 (Аr), 141.85 (Аr).
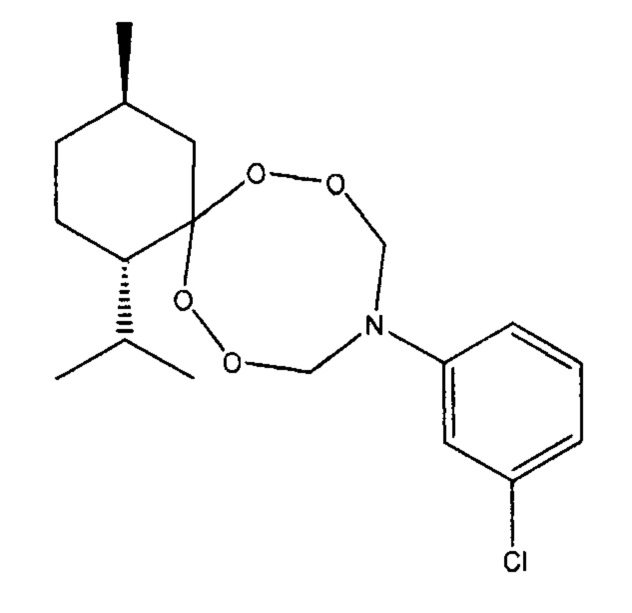
Спектральные характеристики (1S,4R)-10-(3-хлорофенил)-1-изопропил-4-метил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: δН (400 MHz, DMSO-d6, 25°С) 0.84-0.85 (m, 3Н, Н3С), 0.88-0.92 (m, 6Н, Н3С), 1.40-1.45 и 1.56-1.59 (m, 2Н, Н2С), 2.14-2.19 (m, 1Н, НС), 1.65-1.67 (m, 1Н, НС), 1.74-1.76 (m, 2Н, Н2С), 2.64-2.67 и 1.00-1.06 (m, 2Н, Н2С), 1.54-1.59 (m, 1Н, НС), 5.37-5.43 и 5.56-5.67 (m, 4Н, OH2CN), 6.95-6.97 (m, 1Н, НС), 7.09-7.10 (m, 1Н, НС), 7.00-7.02 (m, 1Н, НС), 7.21-7.24 (m, 1Н, НС); δС (100 MHz, CDCl3, 25°С) 19.36 (СН3), 21.90 (СН3), 23.10 и 23.42 (СН2), 24.74 (СН), 28.38 (СН), 34.48 (СН2), 39.27 (СН2), 51.82 (СН), 88.39 (OCH2N), 113.26 (С), 116.77 (Аr), 118.98 (Аr), 122.43 (Аr), 130.29 (Аr), 135.04 (Аr), 147.67 (Аr).
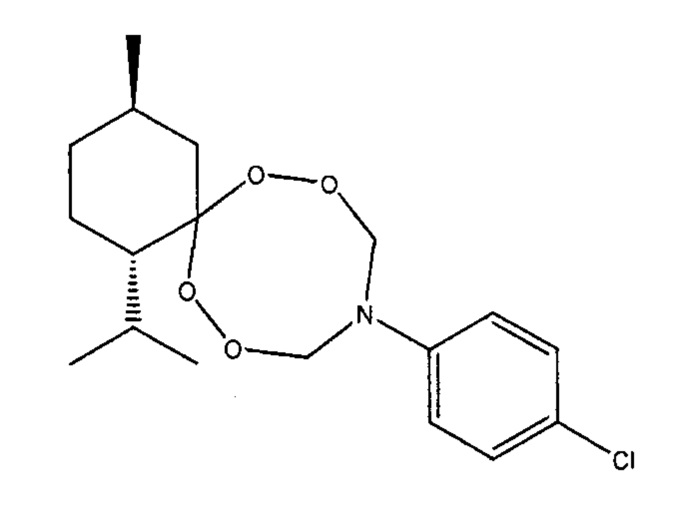
Спектральные характеристики (1S,4R)-10-(4-хлорофенил)-1-изопропил-4-метил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: δН (400 MHz, DMSO-d6, 25°С) 0.81-0.84 (m, 3Н, Н3С), 0.90-0.95 (m, 6Н, Н3С), 1.40-1.43 и 1.51-1.52 (m, 2Н, Н2С), 2.16-2.18 (m, 1Н, НС), 1.57-1.60 (m, 1Н, НС), 1.74-1.77 (m, 2Н, Н2С), 2.64-2.67 и 1.00-1.10 (m, 2Н, Н2С), 1.54-1.59 (m, 1H, НС), 5.39-5.43 и 5.57-5.65 (m, 4Н, OH2CN), 7.02-7.04 (m, 2Н, НС), 7.27-7.28 (m, 2Н, НС); δС (100 MHz, CDCl3, 25°С) 19.36 (СН3), 21.34 (СН3), 23.07 и 23.41 (СН2), 24.74 (СН), 28.40 (СН), 34.48 (СН2), 39.22 (СН2), 51.82 (СН), 88.80 (OCH2N), 114.02 (С), 120.25 (Аr), 127.74 (Аr), 129.28 (Аr), 144.94 (Аr).
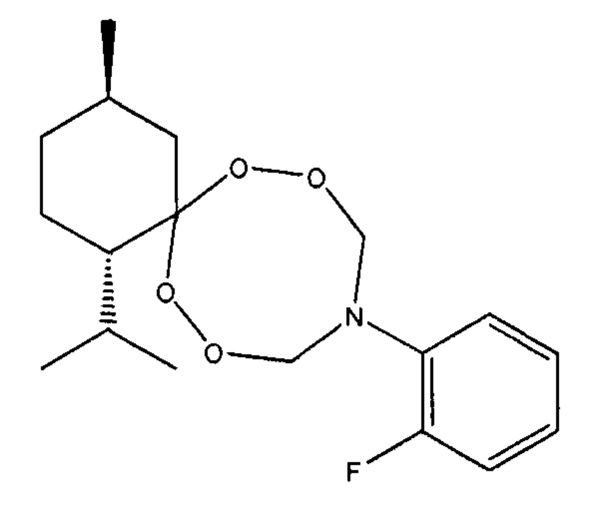
Спектральные характеристики (1S,4R)-10-(2-фторфенил)-1 -изопропил-4-метил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: δН (400 MHz, DMSO-d6, 25°С) 0.85-0.87 (m, 3Н, Н3С), 0.88-0.96 (m, 6Н, Н3С), 1.43-1.46 и 1.56-1.59 (m, 2Н, Н2С), 2.19-2.22 (m, 1Н, НС), 1.68-1.69 (m, 1Н, НС), 1.77-1.80 (m, 2Н, Н2С), 2.88-2.91 и 0.99-1.00 (m, 2Н, Н2С), 1.52-1.54 (m, 1Н, НС), 5.27-5.30 и 5.46-5.60 (m, 4Н, OH2CN), 6.87-6.92 (m, 1Н, НС), 6.95-6.99 (m, 1Н, НС), 7.11-7.14 (m, 1Н, НС), 7.35-7.39 (m, 1H, НС); δС (100 MHz, CDCl3, 25°С) 19.95 (СН3), 22.03 (СН3), 23.01 и 23.04 (СН2), 24.80 (СН), 28.46 (СН), 34.55 (СН2), 39.37 (СН2), 51.87 (СН), 90.32 (OCH2N), 113.80 (С), 123.31 (d, J=6 Hz) (Аr), 115.88 (d, J=6 Hz) (Ar), 124.51 (d, J=26 Hz) (Ar), 121.28 (Ar), 136.47 (Ar), 158.77 (Ar).
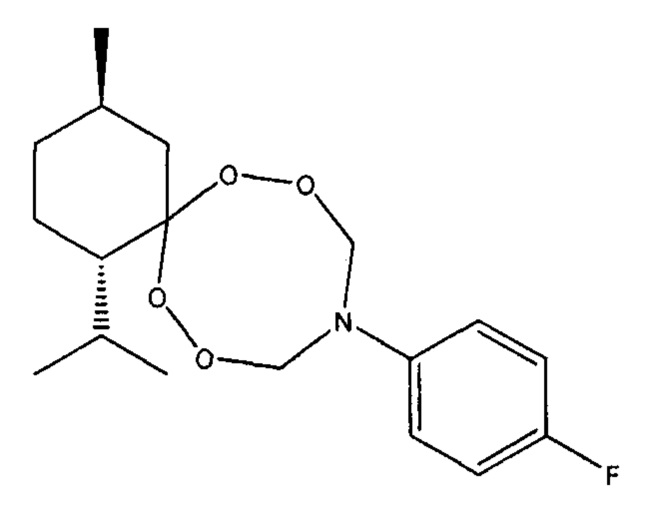
Спектральные характеристики (1S,4R)-10-(4-фторфенил)-1-изопропил-4-метил-7,8,12,13-тетраокса- 10-азаспиро[5.7]тридекана: δН (400 MHz, DMSO-d6, 25°С) 0.82-0.87 (m, 3Н, Н3С), 0.89-0.94 (m, 6Н, Н3С), 1.41-1.46 и 1.57-1.60 (m, 2Н, Н2С), 2.17-2.20 (m, 1Н, НС), 1.65-1.66 (m, 1Н, НС), 1.75-1.77 (m, 2Н, Н2С), 2.72-2.74 и 1.02-1.07 (m, 2Н, Н2С), 1.52-1.54 (m, 1Н, НС), 5.41-5.44 и 5.53-5.60 (m, 4Н, OH2CN), 7.00-7.03 (m, 2Н, НС), 7.07-7.09 (m, 2Н, НС); δС (100 MHz, CDCl3, 25°С) 19.37 (СН3), 21.26 (СН3), 23.06 и 23.41 (СН2), 24.76 (СН), 28.41 (СН), 34.50 (СН2), 39.28 (СН2), 51.77 (СН), 89.46 (OCH2N), 113.88 (С), 115.86 (d, J=17 Hz) (Ar), 121.17 (d, J=7 Hz) (Ar), 142.92 (Ar), 158.77 (d, J=191 Hz) (Ar).
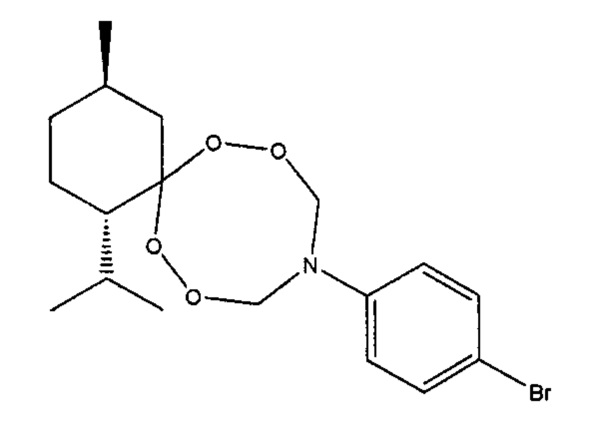
Спектральные характеристики (1S,4R)-10-(4-бромфенил)-1-изопропил-4-метил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: δН (400 MHz, DMSO-d6, 25°С) 0.82-0.83 (m, 3Н, Н3С), 0.86-0.93 (m, 6Н, Н3С), 1.37-1.44 и 1.55-1.58 (m, 2Н, Н2С), 2.15-2.28 (m, 1Н, НС), 1.60-1.64 (m, 1H, НС), 1.73-1.75 (m, 2Н, Н2С), 2.63-2.66 и 0.97-1.04 (m, 2Н, Н2С), 1.50-1.53 (m, 1Н, НС), 5.37-5.42 и 5.56-5.64 (m, 4Н, OH2CN), 6.71-7.95 (m, 2Н, НС), 7.40-7.42 (m, 2Н, НС); δС (100 MHz, CDCl3, 25°С) 19.37 (СН3), 21.96 (СН3), 23.07 и 23.42 (СН2), 24.73 (СН), 28.39 (СН), 34.48 (СН2), 39.22 (СН2), 51.82 (СН), 88.66 (OCH2N), 114.02 (С), 120.55 (Аr), 132.22 (Аr), 145.53 (Аr).
![СПОСОБ ПОЛУЧЕНИЯ (1S,4R)-1-ИЗОПРОПИЛ-4-МЕТИЛ-10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ](https://fips.edrid.ru/images/rid/e1/5b/e9/7aa2a37caa940c6933f6326696cdc1ad.jpg)
![СПОСОБ ПОЛУЧЕНИЯ (1S,4R)-1-ИЗОПРОПИЛ-4-МЕТИЛ-10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ](https://fips.edrid.ru/images/rid/e1/5b/e9/2d04797b81ee387735a3bc77139b0031.jpg)
![СПОСОБ ПОЛУЧЕНИЯ (1S,4R)-1-ИЗОПРОПИЛ-4-МЕТИЛ-10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ](https://fips.edrid.ru/images/rid/e1/5b/e9/061f301ca1c67d1de5634502ac57c984.jpg)
![СПОСОБ ПОЛУЧЕНИЯ (1S,4R)-1-ИЗОПРОПИЛ-4-МЕТИЛ-10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ](https://fips.edrid.ru/images/rid/e1/5b/e9/97687ba83a385da3c25ced8f5b94386d.jpg)
![СПОСОБ ПОЛУЧЕНИЯ (1S,4R)-1-ИЗОПРОПИЛ-4-МЕТИЛ-10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ](https://fips.edrid.ru/images/rid/e1/5b/e9/7ffd7a255c4b32c216f469b53f448817.jpg)

