Результат интеллектуальной деятельности: СПОСОБ КОМБИНИРОВАННОЙ ЗАЩИТЫ МИОКАРДА И УСТРОЙСТВО ДЛЯ ВЫПОЛНЕНИЯ КРОВЯНОЙ ХОЛОДОВОЙ КАРДИОПЛЕГИИ ПРИ ОПЕРАЦИЯХ НА СЕРДЦЕ У НОВОРОЖДЕННЫХ И ДЕТЕЙ ГРУДНОГО ВОЗРАСТА
Вид РИД
Изобретение
Изобретение относится к области хирургии, в частности к кардиохирургии и может быть использовано при операциях на сердце у новорожденных и детей грудного возраста.
Известны способы защиты миокарда при операциях на сердце у детей такие как фармакохолодовая кристаллоидная кардиоплегия и кровяная холодовая кардиоплегия [Аверина Т.Б. и соавт., 2007; Бокерия Л.А. и соавт., 2003; Allen B.S. et al., 2001; Amark K. et al., 2005; Buckberg G.D., 1995; Kotani Y. et al., 2013; Matte G.S., del Nido P.J., 2012; O'Brien J.D. et al., 2013].
Для выполнения кардиоплегии используются различные устройства, в основе которых лежит методика смешивания 4 частей оксигенированной крови из артериальной магистрали и 1 части кардиоплегического раствора с последующим охлаждением до 4°С и подачей в коронарное русло сеансами с определенной скоростью [Buckberg G.D., 1995]. Основным недостатком этих устройств является суммарный большой объем заполнения как теплообменного устройства, так и вспомогательных магистралей.
Недостатками применения указанных способов у новорожденных и детей грудного возраста является выраженные метаболические нарушения, нагрузка организма ребенка ионами К+, приводящая к гиперкалиемии и опасным нарушениям ритма после снятия зажима с аорты.
Цель изобретения - обеспечение адекватной защиты миокарда при оперативных вмешательствах у новорожденных и детей грудного возраста, нивелирование метаболических и электролитных нарушений при выполнении кардиоплегии.
Цель достигается тем, что для защиты миокарда при операциях на сердце у новорожденных и детей грудного возраста непосредственно перед операцией из официнальных препаратов изготавливают три кардиоплегических раствора, которые потом вводят в коронарное русло в 3 этапа; при этом на 1 этапе (индукция в кардиоплегию) в корень аорты шприцом вводят раствор до момента асистолии, содержащий: маннит 12 мг/мл, магния сульфат 8 мг/мл, натрия гидрокарбонат 5,6 мг/мл, лидокаин 0,48 мг/мл, калия хлорид 2,8 мг/мл в объеме 10 мл/кг с температурой +4°С; затем на 2 этапе (поддержание индукции кровяной кардиоплегией) вводят раствор, содержащий натрия гидрокарбонат 2,6 мг/мл, калия хлорид 3,52 мг/мл, смешанный с оксигенированной кровью в соотношении 1:4, длительность сеанса 2 минуты с температурой конечного раствора +4°С; на 3 этапе (поддержание кардиоплегии) вводят раствор с содержанием натрия гидрокарбоната 2,5 мг/мл, калия хлорида 2 мг/мл, при этом скорость подачи раствора составляет 5% от основной скорости потока, температура раствора +4°С, длительность сеанса кардиоплегии 1 мин. Соотношение кровь/кристаллоид - 4:1, а сеанс кардиоплегии выполняют каждые 20 мин. Для осуществления способа используют устройство, которое включает теплообменник; оксигенатор и сосуд с кристаллоидным кардиоплегическим раствором, связанные магистралями для подачи в теплообменник, роликовый насос, приборы для регистрации температуры и давления.
Поэтапное введение растворов при кардиоплегии обусловлено тем, что сначала требуется быстрая остановка сердца и применяется кристаллоиддный кардиоплегический раствор в основе которого высокая концентрация магния и лидокаина. Также в кардиоплегии используется магний и калий для уравнивания разности потенциала на мембранах кардиомиоцитов, бикарбонат натрия в качестве буфера, маннит в качестве буфера, а также лидокаин для блокады быстрых натриевых каналов. Учитывая незрелость системы Т-трубочек и особенности обмена кальция в миокарде новорожденных, в составе кардиоплегии препараты кальция не использовались. Использование магния и лидокаина позволяет снизить содержание калия. Лидокаин посредством его блокирующего действия на быстрые натриевые каналы предотвращает микрофибрилляцию, которая не видна на ЭКГ.
Модификация существующей системы для кардиоплегии заключается в исключении из системы отдельных элементов, сокращении общей длины магистралей. Внесение изменений в конструкцию позволило дать применяемым элементам двойное функциональное назначение и выполнить двукратную редукцию заполняемого объема.
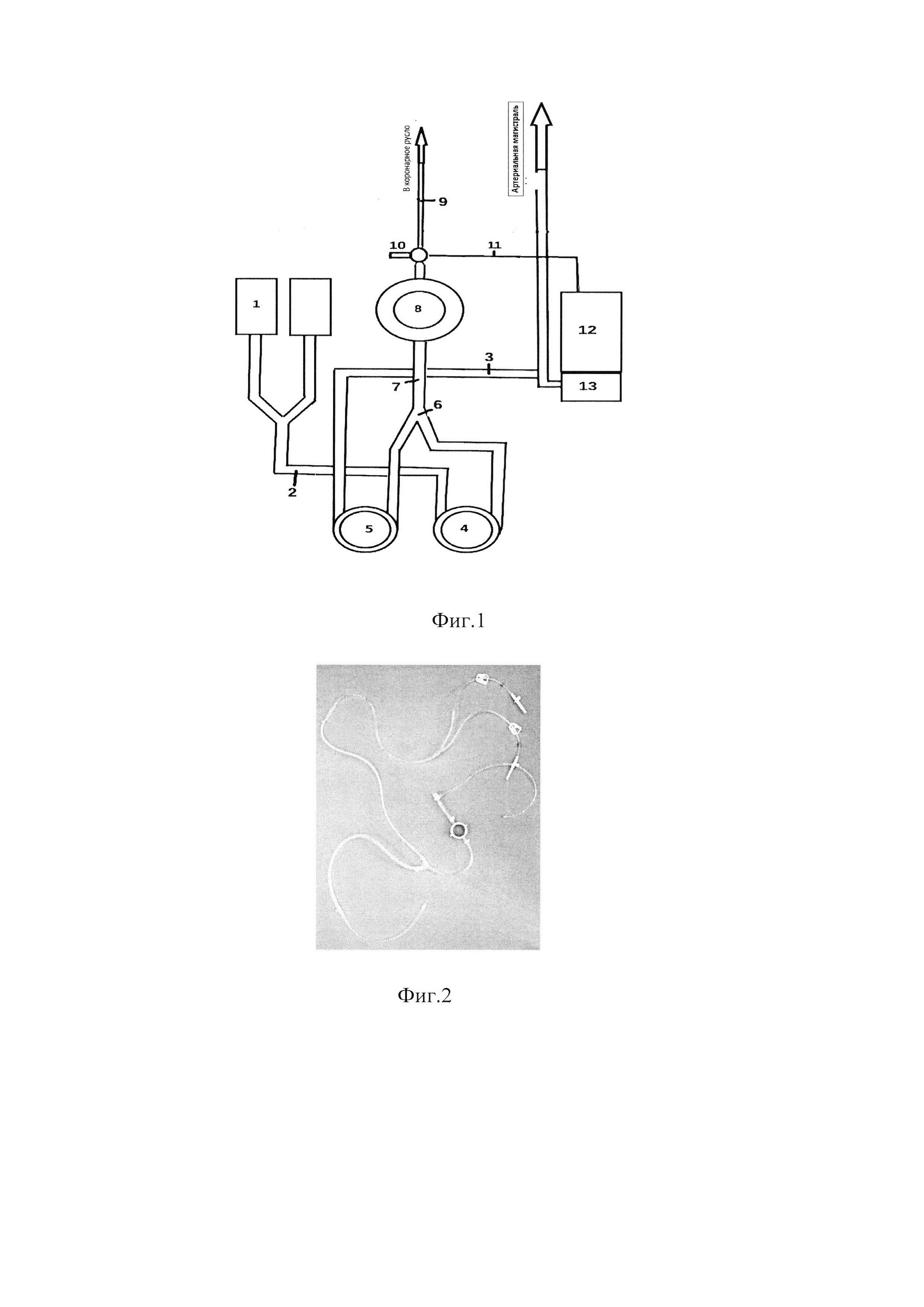
Изобретение поясняется фиг. 1, на которой показана схема устройства для выполнения холодовой кровяной кардиоплегии; а также фиг. 2, на которой изображена система для кровяной кардиоплегии.
Для осуществления этого способа защиты миокарда используют устройство для выполнения кровяной фармакохолодовой кардиоплегии у новорожденных и детей грудного возраста, в целях снижения общего объема заполнения и суммарного объема кардиоплегического раствора, которое включает в себя (Фиг. 1): 1 - кардиоплегический раствор, 2 - магистраль забора кардиоплегического раствора, 3 - магистраль забора оксигенированной крови, 4 - насос регулировки подачи кардиоплегического раствора, 5 - насос регулировки забора оксигенированной крови, 6 - коннектор-тройник, 7 - магистраль доставки раствора в теплообменное устройство, 8 - теплообменное устройство, 9 - линия доставки конечной смеси, 10 - трехходовый краник, 11 - магистраль отвода воздуха/линия измерения давления, 12 - кардиотомный резервуар, 13 - оксигенатор.
Конструкция существующей кардиоплегической системы была модифицирована. Исключены из контура циркуляции системы подачи кардиоплегии отдельные элементы, сокращена общая длина магистралей. Внесение изменений в конструкцию позволило дать некоторым элементам двойное функциональное назначение и вдвое снизить объем заполнения.
Интраоперационное выполнение защиты миокарда осуществляется в 3 основных этапа. На каждом из этапов применяется определенный вид кардиоплегии с использованием предназначенного для него кардиоплегическим раствором:
1. Индукция асистолии кристаллоидом.
2. Поддержание индукции кристаллоидом с кровяной кардиоплегией.
3. Поддержание кардиоплегии кристаллоидом с кровяной кардиоплегией.
1 Этап - Индукция асистолии кристаллоидом. Осуществляется после пережатия аорты путем введения шприцом 50 мл в корень аорты кристаллоидного индукционного раствора №1 в объеме 10 мл/кг с температурой +4°С до момента асистолии. Индукционный раствор №1 готовится непосредственно перед операцией из официнальных компонентов на основе изотонического раствора натрия хлорида с конечной концентрацией следующих ингредиентов: маннита 12 мг/мл, магния сульфата 8 мг/мл, натрия гидрокарбоната 5,6 мг/мл, лидокаина 0,48 мг/мл, калия хлорида 2,8 мг/мл.
2 Этап - Поддержание индукции кровяной кардиоплегией. Выполняется введением кардиоплегического раствора №2 смешанного с оксигенированной кровью в корень аорты. Для этого кровь забирается насосом из кардиотомного резервуара (12), далее при помощи коннектора-тройника (6) смешивается с кристаллоидным раствором (1), подача которого регулируется насосным сегментом (4); полученная смесь крови и кристаллоида подается в теплообменное устройство (8), а затем в кардиоплегические канюли (9) - Фиг. 1. В теплообменнике устанавливается температура, обеспечивающая охлаждение конечной смеси до +4°С. Раствор №2 (для поддержания индукции) готовится непосредственно перед операцией на основе изотонического раствора натрия хлорида с конечной концентрацией следующих ингредиентов: натрия гидрокарбоната 2,6 мг/мл, калия хлорида 3,52 мг/мл. Соотношение производительности насосных сегментов (4,5 - на Фиг. 1) для подачи крови и кристаллоида устанавливается как 4:1 (4 объема крови, 1 объем кристаллоидного кардиоплегического раствора). Введение кардиоплегического раствора осуществляется в корень аорты, сразу же после наложения зажима на аорту под давлением 100 мм рт.ст. Скорость подачи раствора регулируется кардиоплегическими насосами и составляет 5% от основной скорости потока. Длительность поддержания индукции составляет 2 минуты.
3 Этап - Поддержание кардиоплегии. Выполняется каждые 20 мин. Введение кардиоплегического раствора осуществляется по той же методике, как при поддержании индукции, используется раствор, приготовленный перед применением с содержанием натрия гидрокарбоната 2,5 мг/мл, калия хлорида 2 мг/мл. Скорость подачи раствора - 5% от основной скорости потока. Температура раствора +4°С. Длительность сеанса кардиоплегии составляет 1 мин. Соотношение кровь/кристаллоид - 4:1.
Предлагаемый способ был использован при операциях на сердце у 100 детей с врожденными пороками сердца. Мы провели сравнительный анализ использования данного способа защиты миокарда - группа №2 с раствором «Дель-Нидо»- группа №1 (Рефортан - 500 мл; KCl 4% - 20 мл; сода 4% - 13 мл; маннит 15% - 10 мл; лидокаин 1% - 6,5 мл; магний 25% - 5 мл; глюкоза 40% - 2,5 мл).
Объем заполнения контура аппарата искусственного кровообращения в первой группе составил 451±16 мл, во второй группе 352±12 мл, что в первую очередь связано с уменьшенным объемом заполнения кардиоплегического контура предлагаемого нами и применяемого у пациентов 2 группы. За счет более высокой концентрации ионов магния индукционный раствор №1 обеспечивает остановку сердца в течение 2 секунд через асистолию. Развития фибрилляции на этапе индукции кардиоплегии при применении предлагаемой методики зарегистрировано не было.
За 10 минут до отключения искусственного кровообращения у всех пациентов были взяты контрольные лабораторные данные. В обеих группах полученные показатели оставались в пределах нормы. Однако при анализе полученных результатов было отмечено значительное снижение уровня калия с одновременным повышением гемоглобина во 2 группе, по сравнению с аналогичными показателями в 1 группе. Так во второй группе перед отключением искусственного кровообращения тенденции к гиперкалиемии не наблюдалось, в то время, как при применении технологии Дель-Нидо концентрация К+ в плазме наблюдалась намного выше (3,7 ммоль/л и 4,8 ммоль/л соответственно, р=0,001). Наиболее вероятно, это связано с меньшей степенью гемодилюции и рециркуляции меньших объемов кристаллоида у пациентов 2 группы.
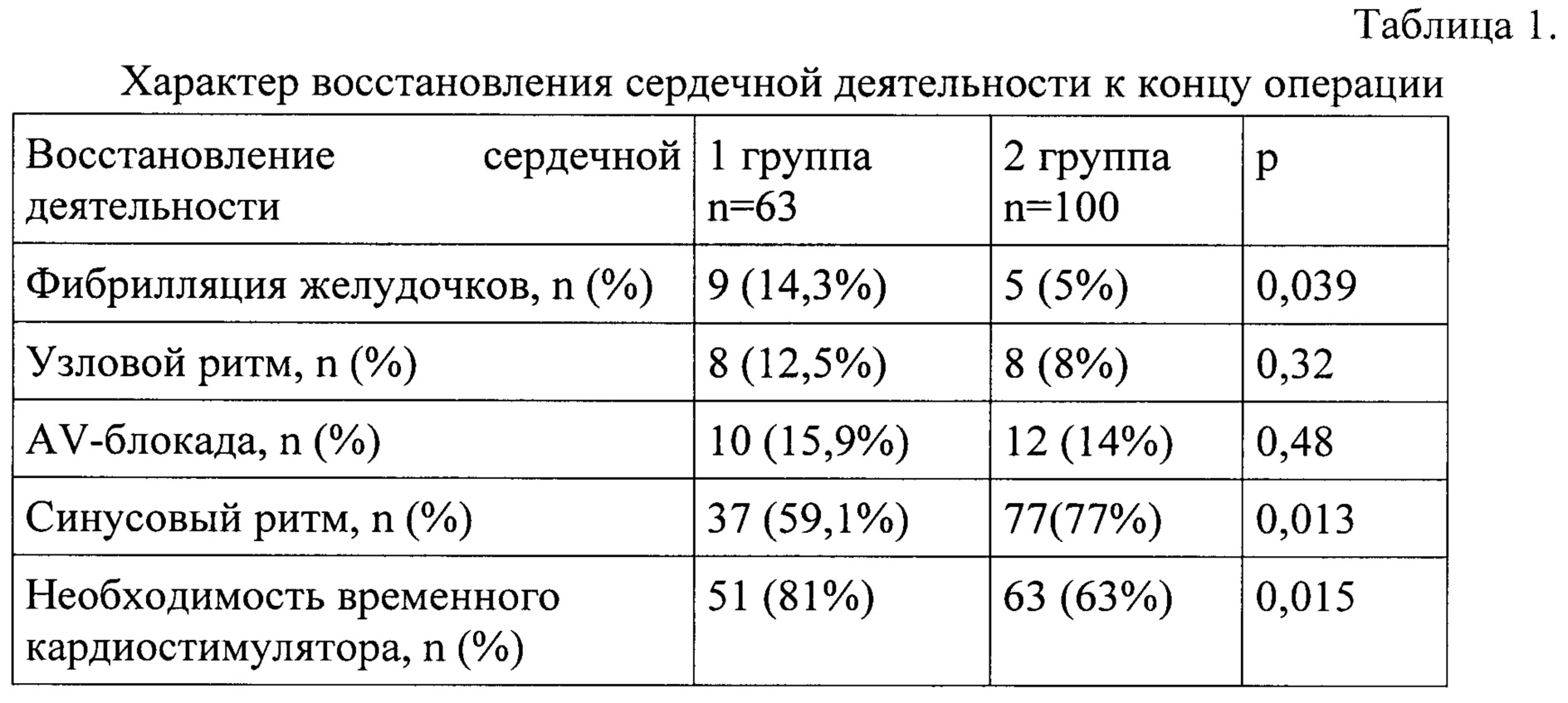
При исследовании характера восстановления сердечного ритма отмечалось снижение количества эпизодов возникновения фибрилляции желудочков после снятия зажима с аорты среди пациентов 2 группы (таблица 1). Помимо этого, во 2 группе устойчивый синусовый ритм к концу операции отмечался в 77% случаев, а частота использования временной электрокардиостимуляции снизилась до 63%.
В ближайшем постперфузионном периоде допамин не использовался. При необходимости инотропная поддержка проводилась адреналином в дозировке 0,01-0,05 мкг/кг/мин. У некоторых больных для стабилизации гемодинамики требовалась дополнительная вазопрессорная поддержка норадреналином в дозе 0,01-0,05 мкг/кг/мин. Степень инотропной и вазопрессорной терапии по завершению операции у пациентов двух групп существенно отличалась. Так среди пациентов второй группы 6 пациентам (6%) не потребовалось какой-либо инотропной терапии, а потребность в высоких дозах адреналина в сочетании с норадреналином была существенно ниже.
Сократительная способность миокарда в ближайшем послеоперационном периоде оценивалась при помощи трансторакальной эхокардиографии с вычислением основных гемодинамических показателей. Так фракция выброса левого желудочка у пациентов первой группы составила 53±9 (ДИ: 50-55; мин 23; максимум 68), у пациентов второй группы 54±8 (ДИ: 53-56; мин 23; максимум 76). Сердечный индекс (СИ, л/мин/м2) в первой группе 2,0±0,3 (ДИ: 1,9-2,1; мин 1,3; максимум 2,7), во второй 2,5±0,2 (ДИ: 2,4-2,6; мин 1,9; максимум 2,9). Индекс доставки кислорода (IDO2, мл/мин/м2) в первой группе 331±21 (ДИ: 325-336; мин 295; максимум 383), во второй 419±14 (ДИ: 416-421; мин 384; максимум 453). В результате основные гемодинамические показатели среди пациентов 2 группы оказались выше. Данная тенденция свидетельствует о лучшей сократительной способности миокарда в послеоперационном периоде.
При оценке результатов лечения пациентов были проанализированы осложнения и показатели, приведенные в таблице 2.
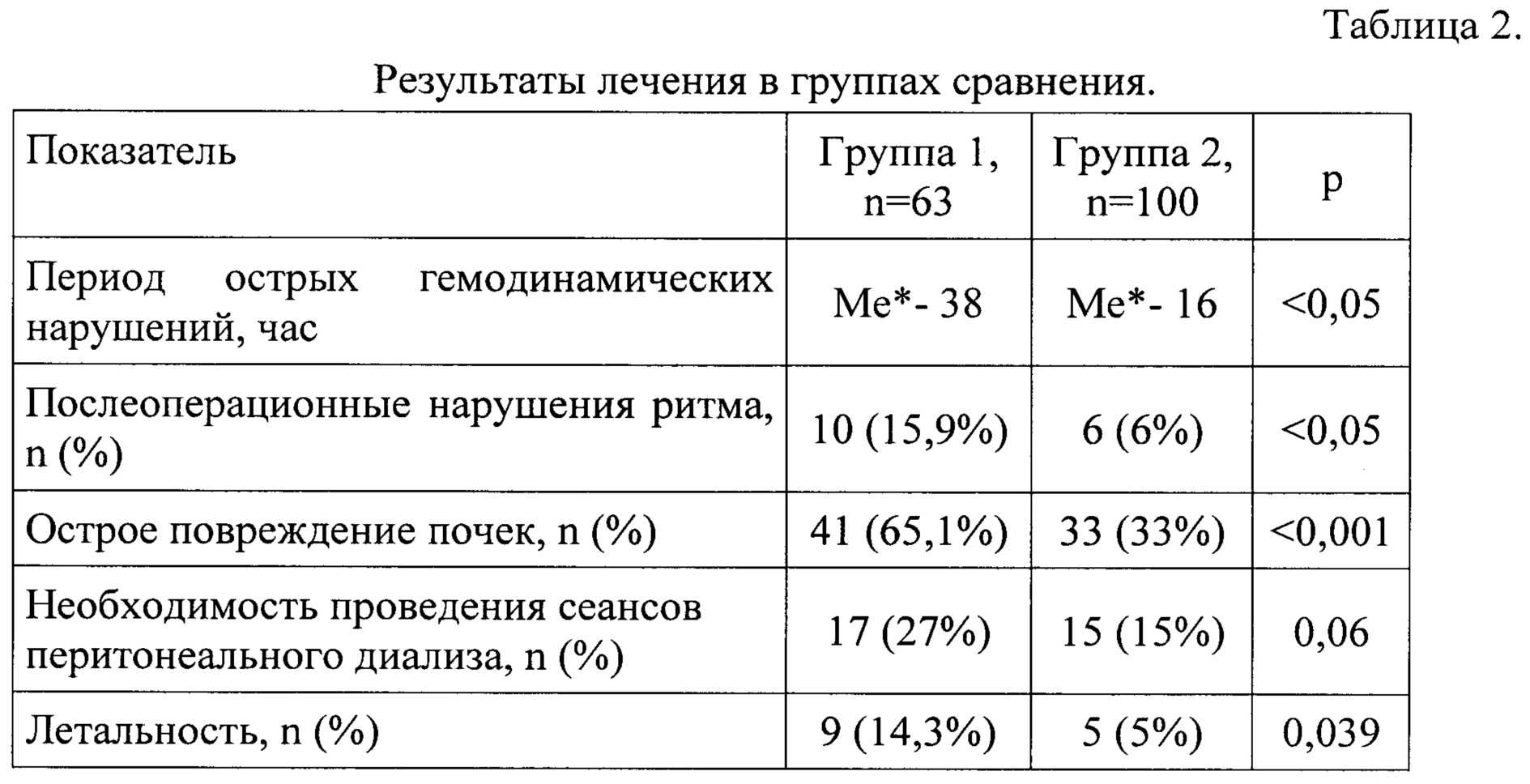
*Ме - медиана
Более высокую летальность в 1 группе нельзя объяснить только различиями в кардиоплегии. Из 14 летальных исходов 11 (78,6%) имели эпизоды гипоперфузии до операции. Среди пациентов первой группы 22 (34,9%) перенесли транспортировку из других стационаров, сопровождавшуюся эпизодами гипоперфузии с повышением лактата. Такую транспортировку перенесли лишь 15 (15%) пациентов второй группы. Относительный риск развития летального исхода увеличивается в 2,5 раза при транспортировке с эпизодами гипоперфузии до операции.
Таким образом, в исследовании показано, что восстановление сердечной деятельности во второй группе было более благоприятным, чем в первой. Это подтверждается наблюдением, что восстановление синусового ритма во второй группе было у 77% пациентов, по сравнению с 59,1% пациентов первой группы (р=0,013) и отражалось в меньшей частоте применения кардиостимуляции (81% против 63%), р=0,015). Так же спонтанное восстановление сердечного ритма во второй группе составило 95% в то время как в первой группе в 14,3%) происходило через фибрилляцию желудочков (р=0,039).
Во второй группе перед отключением искусственного кровообращения тенденции к гиперкалиемии не наблюдалось (3,7 ммоль/л), в то время, как при применении технологии Дель-Нидо концентрация К в плазме наблюдалась выше 4,8 ммоль/л соответственно (р=0,001). Это достигалось применяемой техникой комбинированной кровяной холодовой кардиоплегии и использованием контура с уменьшеным объемом заполнения.
Объемное соотношение кровь : кристаллоид 4:1 вместо 1:4 (у пациентов 1 группы) связано с несколькими особенностями. Из-за наличия в растворе большего количества форменных клеточных элементов, кровяная кардиоплегия обеспечивает более высокую доставку кислорода и онкотическое давление для предотвращения отека кардиомиоцитов. Таким образом, в период пережатия аорты, кардиоплегия обеспечивает остановку сердца в среде, обогащенной кислородом, с минимальной потерей АТФ митохондриями. Благодаря нормальной концентрации в крови естественных буферов создается нормальное онкотическое давление кардиоплегического раствора. Наличие естественных акцепторов свободных радикалов в крови помогает предотвратить реперфузионное повреждение, к которому неонатальный миокард особенно чувствителен. Таким образом, использование большего объема крови в качестве основы кардиоплегического раствора приводит к эффективной доставке кислорода и энергетических субстратов, снижению степени реперфузионного повреждения, естественной буферности кардиоплегического раствора и антиоксидантной защиты. Более высокие концентрации гемоглобина в ходе выполнения кардиоплегии дали предпосылки для лучшего сохранения функции миокарда после перенесенного этапа пережатия аорты. Получены лучшие значения в послеоперационном периоде показателей во второй группе, интегрально отражающих функциональные показатели левого желудочка, скорость системного потока крови и доставку кислорода. Также отмечено снижение частоты острого повреждения почек у пациентов 2 группы (33% против 65%, р<0,001). Как следствие этого отсутствие капиллярной утечки и быстрая экстубация существенно изменяют характер течения послеоперационного периода. Уменьшилась частота применения почечнозаместительной терапии (27% и 15%, в 1 и 2 группах соответственно, р=0,06). Косвенным подтверждением более благоприятного течения послеоперационного периода является частота применения инотропной поддержки (12,7% против 4%, р=0,038).
Необходимость поиска технических решений для доставки кардиоплегии определяется физиологическими и техническими особенностями осуществления искусственного кровообращения у детей. Объем заполнения кардиоплегического устройства при работе с новорожденными или маловесными детьми влияет на количество применяемых компонентов крови и развитие системного воспалительного ответа. Во второй группе конструкция существующей кардиоплегической системы была модифицирована. Исключены из системы подачи кардиоплегии отдельные элементы, сокращена общая длинна магистралей. Внесение изменений в конструкцию позволило дать применяемым элементам двойное функциональное назначение и выполнить двукратную редукцию заполняемого объема. Применение предлагаемой конструкции кардиоплегического устройства существенно уменьшает рециркуляциию высококалиевого индукционного раствора, позволяет выполнять многократные повторные сеансы кардиоплегии без метаболических и электролитных нарушений, уменьшает гемодиллюцию и поддерживает достаточный уровень гемоглобина во время искусственного кровообращения.
Все вышеизложенные эффекты способствуют быстрому восстановлению функции миокарда после его гибернации, уменьшению проявлений реперфузионного и аритмического синдромов, благоприятному течению раннего послеоперационного периода, восстановлению функций почек.
Представленная методика сохраняет все свойства кровяной фармакохолодовой кардиоплегии. Оптимизированный состав кардиоплегического раствора и конструктивные изменения, внесенные в устройство, позволяют избегать неблагоприятных побочных эффектов данного метода защиты миокарда (гиперкалиемия, электролитные и метаболические расстройства, снижение сократительной функции миокарда, нарушения ритма сердца), обеспечивая безопасность оперативных вмешательств на сердце, проводимых в условиях искусственного кровообращения у новорожденных и детей грудного возраста.
Использование модифицированной методики комбинированной кристаллоидно-кровяной холодовой кардиоплегии с уменьшенным объемом заполнения системы доставки для хирургической коррекции врожденных пороков сердца у новорожденных, а также детей раннего и старшего возраста является эффективным вариантом интраоперационной защиты миокарда, увеличивает сердечный индекс в послеоперационном периоде с 2,0±0,3 до 2,5±0,2 (р=0,003) и улучшает индекс доставки кислорода с 331±21 до 419±14 (<0,0001), уменьшает частоту острого повреждения почек с 65,1% до 33% и уменьшает относительный риск развития острого повреждения почек в 1,9 раза.