Результат интеллектуальной деятельности: Субстрат для культивирования ксилотрофных базидиомицетов и способ его получения с использованием методов химической модификации лигноцеллюлозного сырья
Вид РИД
Изобретение
Изобретение относится к биотехнологии. Изобретение может быть использовано для получения плодовых тел съедобных, лекарственно-съедобных и лекарственных грибов, а также для производства субстрата для получения плодовых тел съедобных, лекарственно-съедобных и лекарственных грибов.
Известен субстрат (патент РФ №2436283) для выращивания плодовых тел грибов состоящий из березовых опилок 96%, гипса 1% и мела 3%. Недостатком данного субстрата является использование в качестве основы только березовых опилок, т.к. это сильно ограничивает сырьевую базу производства. К тому же в описании изобретения отсутствует источник азота и урожайность плодовых тел будет сильно зависеть от времени заготовки и свежести опила.
Известен субстрат для получения плодовых тел Ganoderma lucidum состоящий из гидролизованной разбавленной соляной кислотой ржаной соломы - 55%; дубовых опилок - 25%; ржаных отрубей - 10%; кукурузной муки - 8%; мела химически осажденного - 1%; гипса природного - 1% описанный в патенте РФ №2453105. Указанный субстрат готовят путем предварительного гидролиза ржаной соломы 0,5-1% раствором соляной кислоты, а затем смешивания гидролизованной ржаной соломы, дубовых опилок с питательными веществами - отрубями ржаными, кукурузной мукой, мелом химически осажденным, гипсом природным. Недостатком данного метода является длительность процесса кислотного гидролиза (2 ч), а также использование ценного сырья - дубовых опилок, которые находят свое применение для получения композитных строительных материалов, копчения деликатесных пищевых продуктов и др. К тому же, кислотный гидролиз, описанный в патенте РФ №2453105 приводит к увеличению доли свободных моно- и олигосахаров, что приводит к высокому риску контаминации плесневыми грибами, дрожжами и бактериями.
Наиболее близким к заявленному изобретению является способ получения субстрата (патент РФ 2140145 С1) для выращивания съедобных грибов, включающий измельчение растительного сырья, увлажнение его и стерилизацию, отличающийся тем, что увлажнение сырья осуществляют раствором уксусной кислоты для одновременного осуществления гидролиза сырья, где в качестве растительного сырья используют смесь соломы злаковых культур и отходы хвойных пород в количестве, соответственно равном 35-60 и 40-65 мас. %, а концентрация уксусной кислоты 1,5-2%.
Недостатком такого метода является повышенное содержание свободных Сахаров, которые образуются в процессе частичного гидролиза растительного сырья, что приводит к значительному повышению риска контаминации.
Заявляемый способ получения субстратов для культивирования ксилотрофных базидиомицетов с использованием методов кислотной модификации лигноцеллюлозного сырья и субстраты, полученные предлагаемым способом, включает этап модификации лигноцеллюлозных отходов сельского хозяйства и лесопереработки кислотами. Для этого в кислотоустойчивые емкости, футерованных фторопластом, загружают лигноцеллюлозное сырье (моно- или многокомпонентное) и добавляют раствор кислот в концентрации 0,5-5%. Предобработку осуществляют при температуре 80-135°C, соотношении сырья к раствору кислоты от 1:2 до 1:8 и длительности процесса 0,5-1 ч. После завершения процесса полученную пульпу промывают 1-4 объемами воды для удаления сахаров и смолистых веществ, а также остатков непрореагировавшей кислоты. Далее вносят дополнительный источник азота, а также мел и известь. Кислотная предобработка снижает количество Сахаров в субстрате, увеличивает содержание лигнина, делая такой субстрат селективным для ксилотрофных грибов «белой гнили», в том числе съедобных, лекарственно-съедобных и лекарственных.
Для предобработки лигноцеллюлозного сырья можно использовать как органические, так и минеральные кислоты.
Предлагаемый субстрат может содержать лигноцеллюлозное сырье из перечня, включающего отходы деревоперерабатывающей промышленности и сельского хозяйства, такие как опилки лиственных пород деревьев, опилки хвойных пород деревьев, кора, листья, хвоя, солома злаков, кукурузная кочерыжка, костра льна, рисовая шелуха и др. Настоящий перечень не ограничивает виды лигноцеллюлозного сырья, которые можно использовать в заявленном способе.
Предлагаемый субстрат может содержать источник азота, выбранный из пшеничных, ржаных или овсяных отрубей, кукурузной, соевой или рыбной муки, разными по источнику получения жмыхами и жомами. Настоящий перечень не ограничивает виды источников азота, которые можно использовать в заявленном способе.
Заявляемый способ предназначен для культивирования лекарственных и съедобных ксилотрофных грибов из перечня, включающего следующие виды: Agrocybe aegerita, Flammulina velutipes, Ganoderma lucidum, Grifola frondosa, Hericium erinaceus, Hypsizygus marmoreus, H. ulmarius, Lentinus edodes, Pholiota nameko, Pleurotus citrinopileatus, P. eringii, P. djamor, P. ostreatus, P. pulmonarius, P. sajor-caju, Trametes versicolor. Настоящий перечень не ограничивает виды ксилотрофных грибов, которые можно использовать в заявленном способе.
Пример 1
Предобработку производили в стерилизующем автоклаве. Для этого в хемостойкие емкости загружали лигноцеллюлозное сырье, смачивали советующим раствором минеральной или органической кислоты согласно таблице 1 и нагревали до соответствующей температуры в течении 1 часа. Содержание целлюлозы, гемицеллюлоз и лигнина определяли методами, описанными в NREL LAB-002, LAB-003.
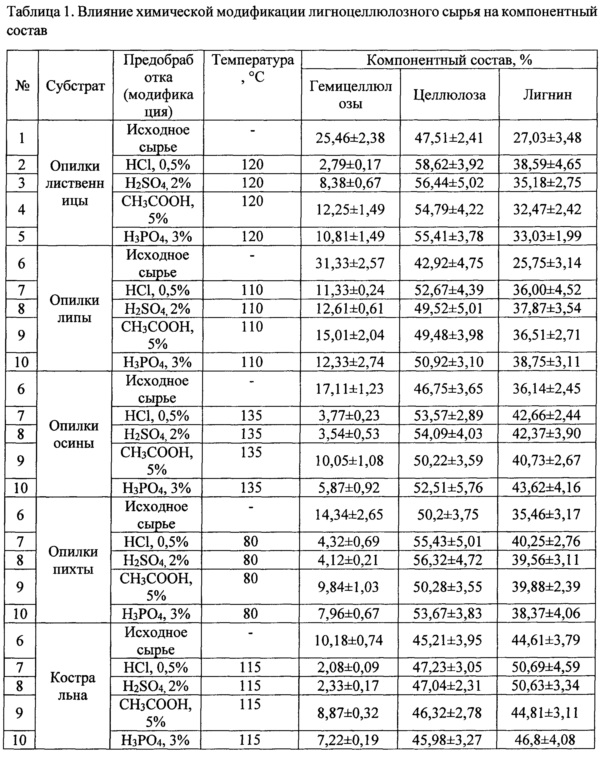
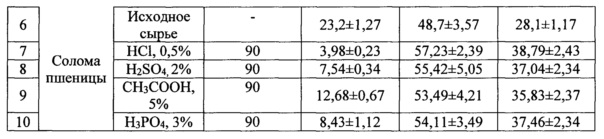
Проведение кислотной предобработки способствовало удалению легкогидролизуемых полисахаридов (гемицеллюлоз и аморфную часть целлюлозы), частично разрушило межмолекулярные связи между молекулами лигнина и целлюлозы.
Пример 2
Скорость освоения модифицированных субстратов определяли следующим методом: в чашки Петри помещали смесь лигноцеллюлозного субстрата, отрубей пшеницы и мела взятых в соотношении 7,8:2:0,2, увлажняли до 80% водой и стерилизовали. Засев культурой гриба проводили с использованием агаровых блоков с культурой гриба размером 2*2*2 мм. Размер колонии гриба измеряли на 8 сутки.
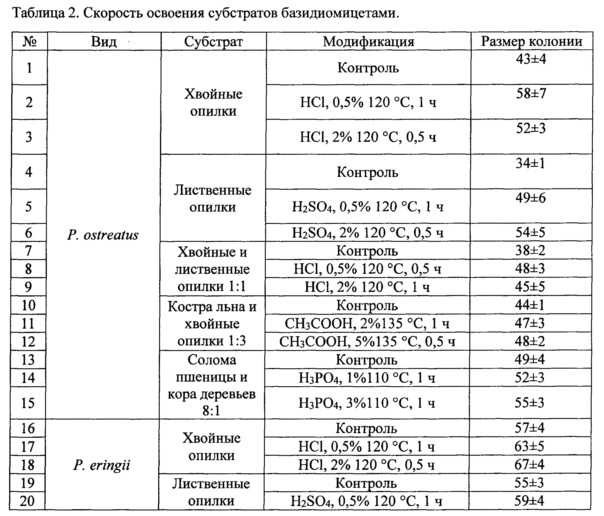
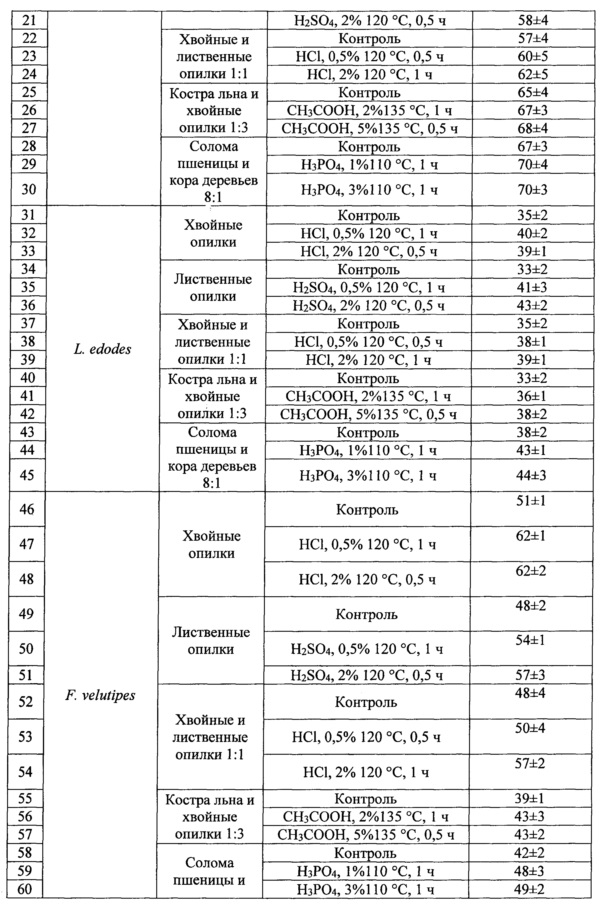
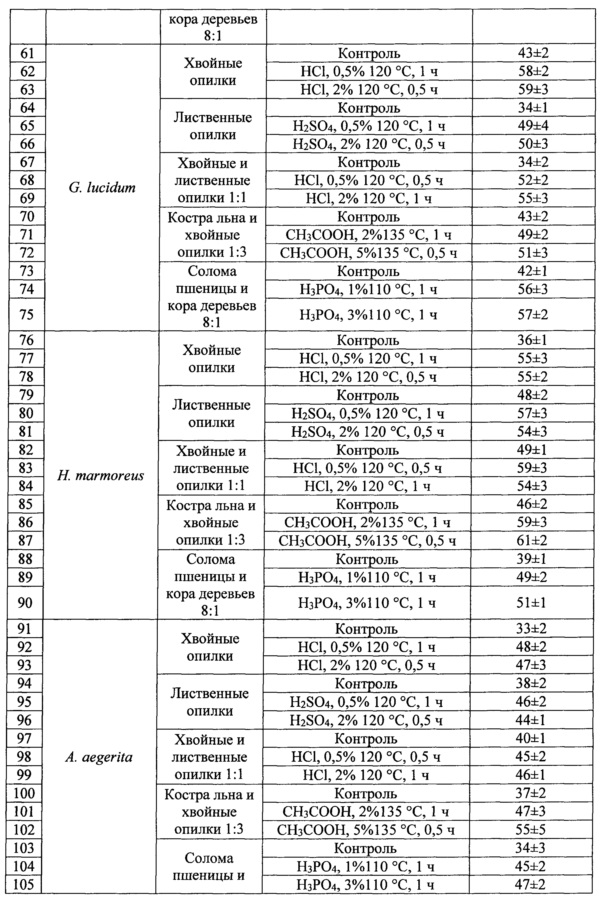
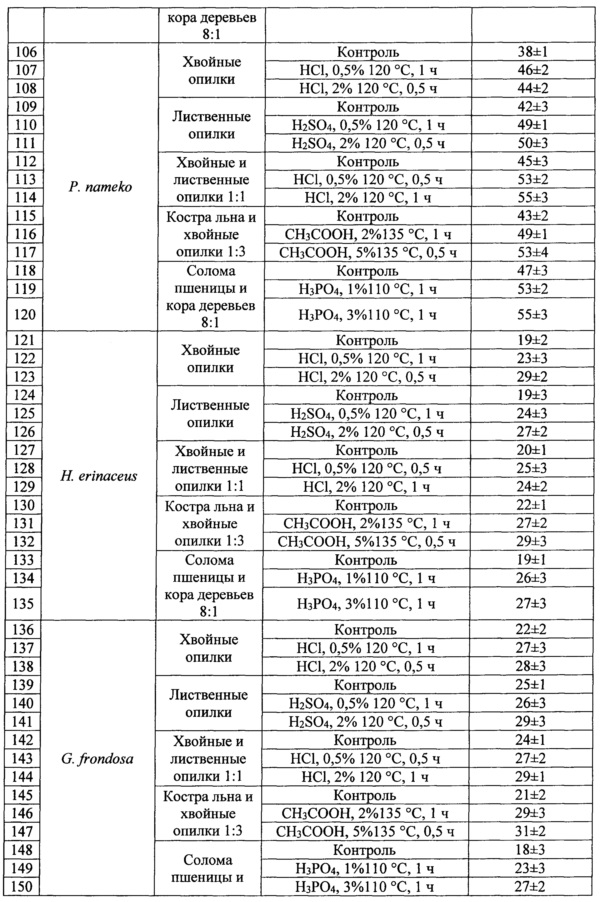
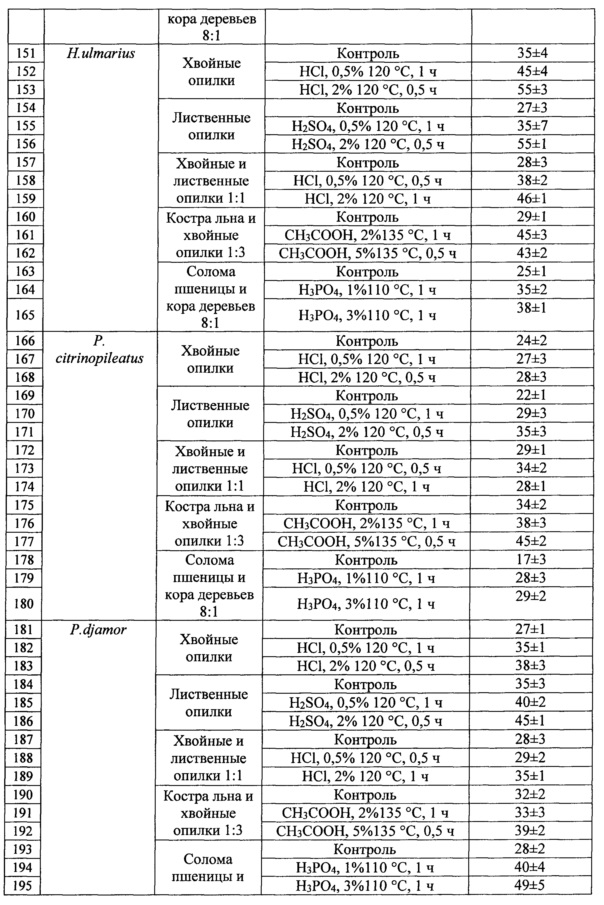
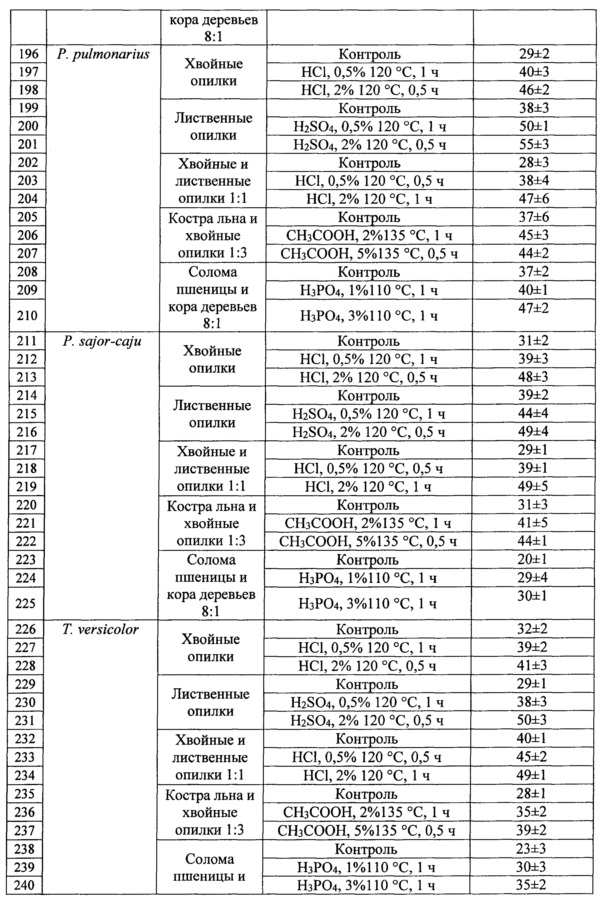

Кислотная модификация лигноцеллюлозного сырья привела к увеличению скорости роста ксилотрофных базидиомицетов на 20-50%, что позволило существенно сократить время освоения блоков грибом при культивировании. Увеличение скорости роста не только сокращает врем технологических циклов, но и снижает вероятность контаминации другими микроорганизмами - конкурентов за субстрат.
Пример 3
Получение субстратов для твердофазного культивирования.
Субстрат 1. Хвойные и лиственные опилки в соотношении 2:1 помещали в хемостойкие емкости и смешивали с раствором соляной кислоты с концентрацией 1,5% в соотношении 1:2 и помещали в автоклав. Время обработки 0,5 час, температура 135°C. Сырье охлаждали до комнатной температуры, переносили на фильтр и промывали однократно водой и давали стечь избытку влаги. В полученную основу вносили 15% масс. отрубей пшеницы, 2% мела и тщательно перемешивали. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и пастеризовали.
Субстрат 2. Кора деревьев и солома пшеницы в соотношении 1:4 помещали в хемостойкие емкости и смешивали с раствором серной кислоты концентрацией 2% в соотношении 1:3 и помещали в автоклав. Время обработки 1 час, температура 121°C. Сырье охлаждали до комнатной температуры, переносили на фильтр и промывали однократно водой и давали стечь избытку влаги. В полученную основу вносили 10% масс, отрубей ржи, 2% мела и тщательно перемешивали. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и пастеризовали.
Субстрат 3. Хвоя и костру льна в соотношении 1:8 помещали в хемостойкие емкости и смешивали с раствором фосфорной кислоты с концентрацией 2,5% в соотношении 1:4 и помещали в автоклав. Время обработки 1 час, температура 135°C. Сырье охлаждали до комнатной температуры, переносили на фильтр и промывали однократно водой и давали стечь избытку влаги. В полученную основу вносили 20% масс. кукурузной муки, 2% мела и тщательно перемешивали. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и пастеризовали.
Субстрат 4. Кукурузную кочерыжку и хвойные опилки в соотношении 1:5 помещали в хемостойкие емкости и смешивали с раствором уксусной кислоты с концентрацией 5% соотношением 1:6 и помещали в автоклав. Время обработки 0,5 час, температура 110°C. Сырье охлаждали до комнатной температуры, переносили на фильтр и промывали однократно водой и давали стечь избытку влаги. В полученную основу вносили 10% масс, рыбной муки, 2% мела и тщательно перемешивали. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и стерилизовали.
Субстрат 5. Костру льна и лиственные опилки в соотношении 1:6 помещали в хемостойкие емкости и смешивали с раствором соляной кислоты с концентрацией 2% в соотношении 1:8 и помещали в автоклав. Время обработки 0,5 час, температура 121°C. Сырье охлаждали до комнатной температуры, переносили на фильтр и промывали однократно водой и давали стечь избытку влаги. В полученную основу вносили 20% масс. жмыха подсолнечника, 2% мела и тщательно перемешивали. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и стерилизовали.
Субстрат 6. Солому пшеницы и кору деревьев в соотношении 4:1 помещали в хемостойкие емкости и смешивали с раствором соляной кислоты с концентрацией 1,5% в соотношении 1:8 и помещали в автоклав. Время обработки 1 час, температура 80°C. Сырье охлаждали до комнатной температуры, переносили на фильтр и промывали однократно водой и давали стечь избытку влаги. В полученную основу вносили 20% масс, свекловичного жома, 2% мела и тщательно перемешивали. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и стерилизовали.
Пример 4
Культивирование P. ostreatus, G. lucidum, Н. erinaceus на субстратах, полученных по примеру 3. В качестве контроля выступал следующий субстрат: лиственные опилки 80%, 20% масс. отрубей пшеницы, 2% мела и тщательно перемешивали и смачивали водой до 80% влажности. Полученный субстрат расфасовывали по мешкам из полипропилена с вклеенными фильтрами и пастеризовали.
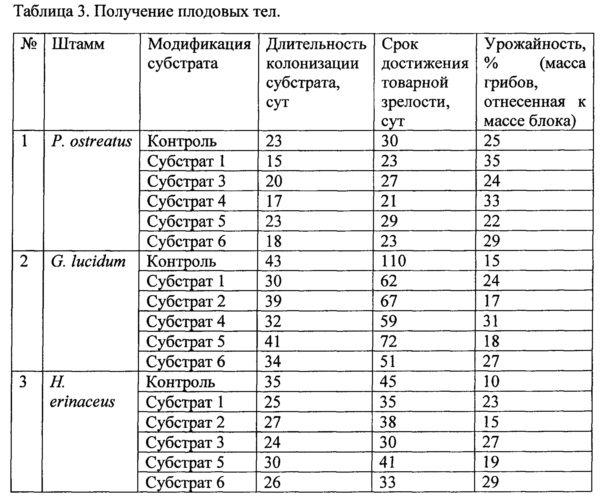
Из результатов, приведенных в примерах, следует, что поставленная техническая задача решена - созданы селективные условия для развития съедобных и лекарственных ксилотрофных грибов «белой гнили» за счет повышения содержания лигнина в субстрате, что обеспечило увеличение скорости освоения субстрата, сокращение срока достижения плодовыми телами товарной зрелости и повышение урожайности.

