Результат интеллектуальной деятельности: Способ количественного определения фенола в биологических лекарственных препаратах методом газожидкостной хроматографии
Вид РИД
Изобретение
Изобретение относится к области фармации, в частности к лабораторной экспертизе биологических лекарственных препаратов (далее - БЛП), а именно к количественному определению примесей и вспомогательных веществ, содержащихся в БЛП.
Известен способ определения фенола в аллергенах [1], состоящий в определении фенола при помощи спектрофотометрии. Способ основан на способности фенола поглощать ультрафиолетовое излучение при длине волны 269 нм.
К недостаткам этого способа следует отнести необходимость пробоподготовки (разведение образца), относительную точность и специфичность, поскольку все органические соединения, имеющие в своей структуре ароматическое бензольное кольцо, обладают способностью поглощать излучение в ультрафиолетовой области, в частности, при длине волны 269 нм. Данный способ можно считать специфичным, только допуская, что испытуемый образец не содержит подобных веществ.
Также известен способ количественного определения фенола в крови [2], заключающийся в экстракции фенола из крови и последующем определении его с помощью метода газожидкостной хроматографии (далее - ГЖХ).
К недостаткам этого способа следует отнести необходимость пробоподготовки (экстракция фенола и разведение образца), а также ограниченную область применения: способ разработан для определения содержания фенола в крови и не пригоден для определения содержания фенола в БЛП ввиду различий состава образцов и диапазона концентраций фенола.
Также известен способ, применяемый для определения фенола в иммунных сыворотках и вакцинах [3], состоящий в определении фенола колориметрически. Способ основан на образовании антипиринового красителя при реакции 4-аминоантипирина с фенолами в щелочной среде в присутствии окислителя (феррицианида калия) и последующем измерении интенсивности окраски в анализируемом образце.
К недостаткам этого способа следует отнести необходимость пробоподготовки (разведение образца), длительность, необходимость использования дополнительных реагентов, а также относительную точность и специфичность способа: реакцию с 4-аминоантипирином дают все вещества, относящиеся к классу фенолов.
В качестве прототипа выбран способ количественного определения фенола спектрофотометрическим методом в иммунобиологических лекарственных препаратах [4].
К недостаткам этого способа следует отнести необходимость пробоподготовки (предварительного разведения препаратов в 100 раз), в результате которой концентрация фенола в испытуемом образце соответствует диапазону аналитической области способа. А также относительную точность и специфичность, поскольку все органические соединения, имеющие в своей структуре ароматическое бензольное кольцо, обладают способностью поглощать излучение в ультрафиолетовой области, в частности, при длине волны 269 нм. Данный способ можно считать специфичным, только допуская, что испытуемый образец не содержит подобных веществ.
Техническим результатом изобретения является повышение специфичности и точности количественного определения фенола в БЛП методом ГЖХ.
В данном тексте под терминами специфичность и точность [5, 6] подразумевается следующее.
Специфичность - это способность аналитической методики однозначно оценивать определяемое вещество в присутствии сопутствующих компонентов.
Для описания точности метода измерений используют два термина: «правильность» и «прецизионность». Термин «правильность» характеризует степень близости среднего арифметического значения результатов измерений к истинному или принятому опорному значению, термин «прецизионность» -степень близости результатов измерений друг к другу.
Определение правильности методики непосредственно связано с оценкой линейности. Линейность методики - это наличие линейной зависимости аналитического сигнала от концентрации или количества определяемого вещества в анализируемой пробе в пределах аналитической области. Аналитическая область - это интервал между верхним и нижним значениями аналитических характеристик определяемого компонента в объекте анализа. Для представления прецизионности используют результаты, полученные в условиях «повторяемости (сходимости)» и в условиях «воспроизводимости».
Поставленная задача решается благодаря:
- расширению спектра аналитического оборудования;
- подбору хроматографической колонки, позволяющей обеспечить эффективное отделение фенола от веществ, входящих в состав образца;
- подбору условий ГЖХ: режима подачи несущего газа (гелия); скорости потока несущего газа (гелия); условий деления потока несущего газа (гелия), температуры инжектора, температуры термостата хроматографической колонки; температуры детектора, позволяющих обеспечить эффективное отделение фенола от веществ, входящих в состав образца;
- подбору линейной области концентраций фенола, соответствующей содержанию фенола в БЛП;
- исключению этапа пробоподготовки (разведения образца);
- выбору внутреннего стандарта, позволяющего контролировать эффективность хроматографического разделения.
В заявляемом изобретении способ количественного определения фенола в БЛП осуществляется методом ГЖХ.
Способ количественного определения фенола в БЛП методом ГЖХ реализуется следующим образом.
В качестве внутреннего стандарта используют раствор 2-феноксиэтанола в абсолютном этаноле, концентрацией 5 мг/мл.
В качестве рабочего раствора фенола используют раствор фенола в этаноле концентрацией 5 мг/мл.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл:
0,2 мл рабочего раствора фенола помещают в виалу №1, объемом 1,5 мл для хроматографирования, добавляют воду 0,8 мл, добавляют 0,5 мл внутреннего стандарта, перемешивают. Полученный раствор представляет собой стандартный раствор с концентрацией фенола 1 мг/мл, содержащий внутренний стандарт.
0,6 мл рабочего раствора фенола помещают в виалу №2, объемом 1,5 мл для хроматографирования, добавляют воду 0,4 мл, добавляют 0,5 мл внутреннего стандарта, перемешивают. Полученный раствор представляет собой стандартный раствор с концентрацией фенола 3 мг/мл, содержащий внутренний стандарт.
1,0 мл рабочего раствора фенола помещают в виалу №3, объемом 1,5 мл для хроматографирования, добавляют 0,5 мл внутреннего стандарта, перемешивают. Полученный раствор представляет собой стандартный раствор с концентрацией фенола 5 мг/мл, содержащий внутренний стандарт.
Исследуемый образец: 1,0 мл образца БЛП, содержащий фенол в концентрации 1,5-4 мг/мл, без предварительного разведения, вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Последовательность ввода образцов соответствует номеру виалы.
Оптимальные условия ГЖХ были подобраны для колонки DB-WAX (размер 30 м × 0,25 мм × 0,25 мкм) фирмы Agilent Technologies; температура инжектора 250°С; деление потока 40:1; объем пробы 0,5 мкл; газ-носитель гелий; режим постоянное давление; скорость потока 1,4 мл/мин; температурный профиль печи: начальная температура 160°С, выдержка 3 мин, градиент 40°С/мин до температуры 200°С выдержка 0,6 мин, градиент 40°С/мин до температуры 220°С; время анализа 7,133 мин; пламенно-ионизационный детектор, температура детектора 250°С.
Критерии пригодности хроматографической системы, установленные в процессе валидации способа:
- число теоретических тарелок не менее 180000;
- разрешение пиков фенола и внутреннего стандарта не менее 15;
- коэффициент асимметрии пика фенола от 0,8 до 1,2;
- время удерживания пика фенола около 5,0 мин;
- время удерживания внутреннего стандарта около 6,0 мин.
Расчет производят относительно внутреннего стандарта, переводя величину полученного аналитического сигнала в относительные единицы.
Оценку результатов производят, используя график регрессионной зависимости относительных площадей пика фенола от концентрации фенола в стандартных растворах.
Существенные отличительные признаки заявляемого изобретения:
1. Повышение специфичности способа за счет подбора хроматографической колонки и условий газохроматографического разделения, позволяющих обеспечить эффективное отделение фенола от веществ, входящих в состав образца.
2. Повышение точности (правильности и прецизионности) способа за счет:
- исключения этапа пробоподготовки;
- проведения анализа с использованием линейной области способа, соответствующей концентрации фенола в БЛП;
- использования внутреннего стандарта, позволяющего контролировать эффективность газохроматографического разделения и проводить расчет в относительных единицах.
3. Расширение спектра аналитического оборудования пригодного для количественного определения фенола в БЛП.
Краткое описание чертежей и иных материалов (Приложения 1-5):
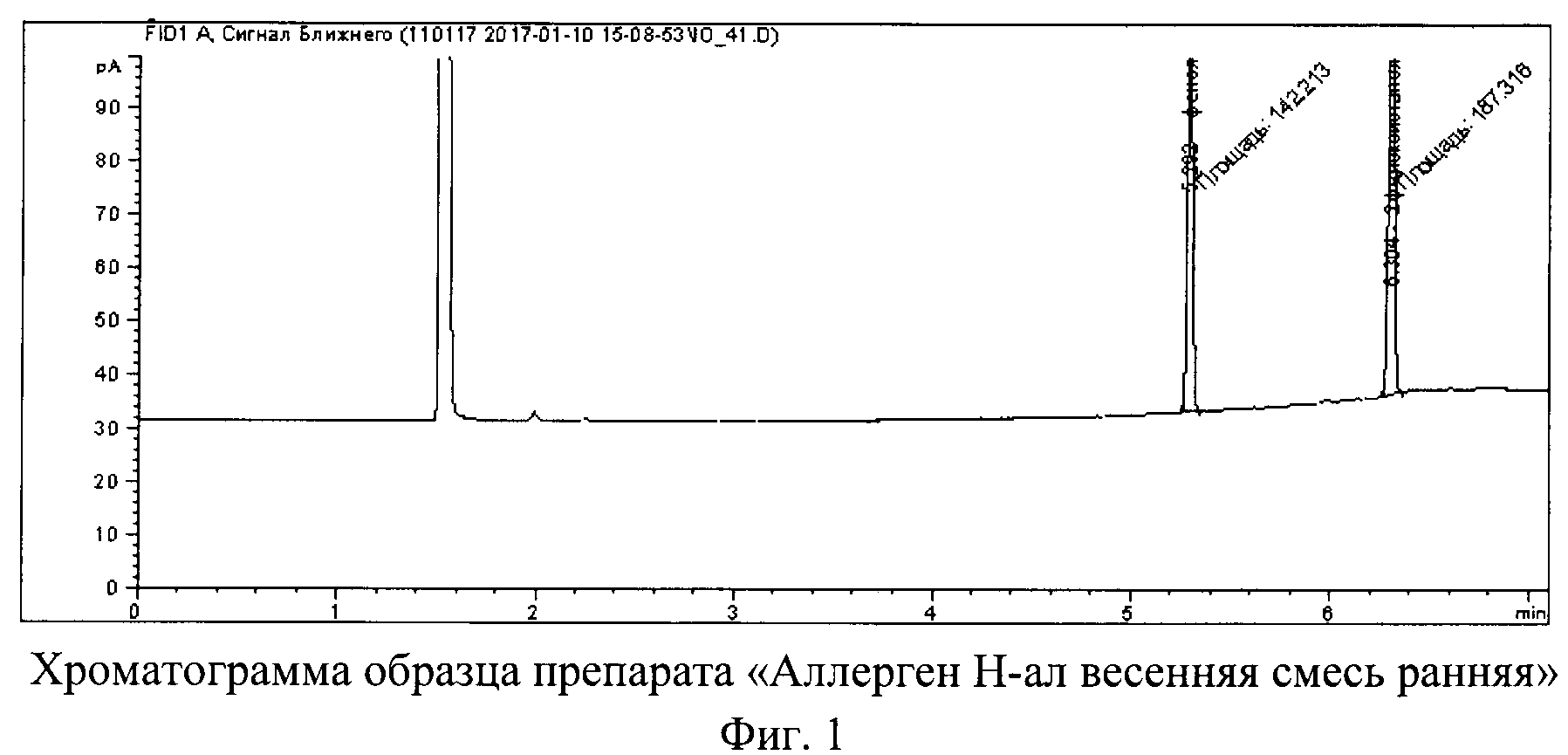
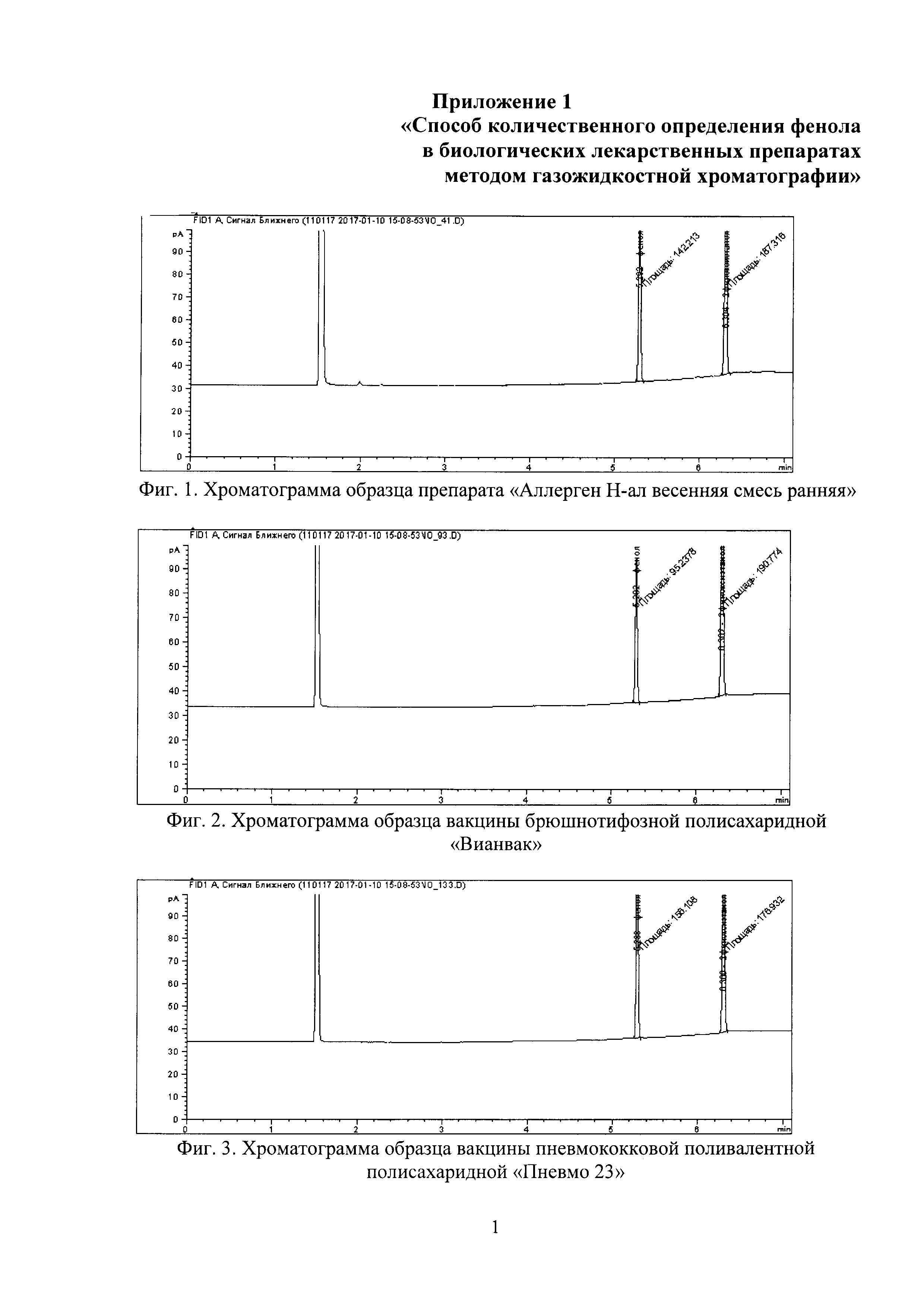
Фиг. 1. Хроматограмма образца препарата «Аллерген Н-ал весенняя смесь ранняя». На хроматограмме обозначены пики фенола (время удерживания 5,202 мин и площадь пика 142,213) и 2-феноксиэтанола (время удерживания 6,304 мин и площадь пика 187,318).
Фиг. 2. Хроматограмма образца вакцины брюшнотифозной полисахаридной «Вианвак». На хроматограмме обозначены пики фенола (время удерживания 5,202 мин и площадь пика 95,2378) и 2-феноксиэтанола (время удерживания 6,302 мин и площадь пика 190,774).
Фиг. 3. Хроматограмма образца вакцины пневмококковой поливалентной полисахаридной «Пневмо 23». На хроматограмме обозначены пики фенола (время удерживания 5,200 мин и площадь пика 156,108) и 2-феноксиэтанола (время удерживания 6,304 мин и площадь пика 176,932).
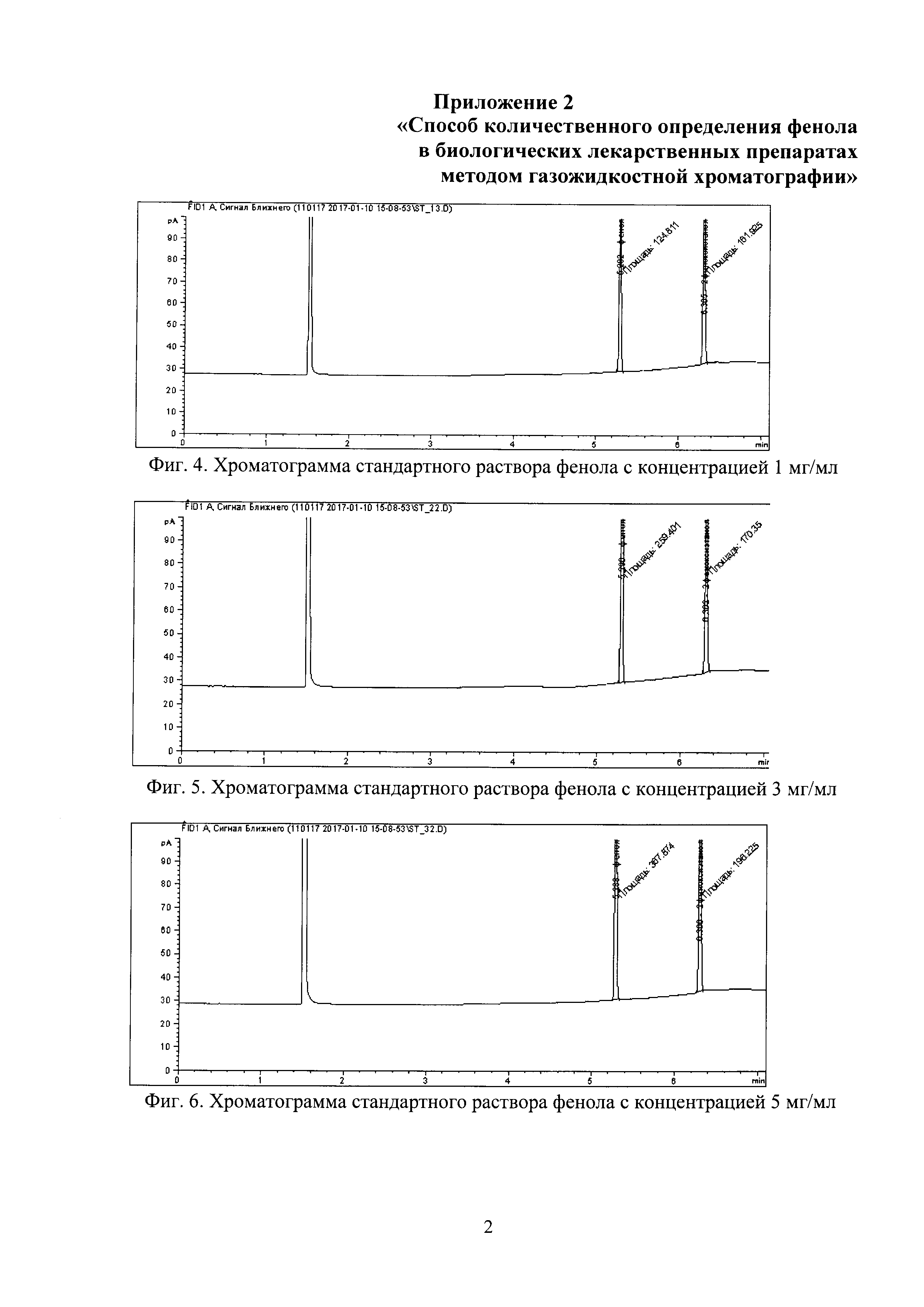
Фиг. 4. Хроматограмма стандартного раствора фенола с концентрацией 1 мг/мл. На хроматограмме обозначены пики фенола (время удерживания 5,202 мин и площадь пика 124,811) и 2-феноксиэтанола (время удерживания 6,305 мин и площадь пика 181,925).
Фиг. 5. Хроматограмма стандартного раствора фенола с концентрацией 3 мг/мл. На хроматограмме обозначены пики фенола (время удерживания 5,200 мин и площадь пика 259,401) и 2-феноксиэтанола (время удерживания 6,302 мин и площадь пика 170,32).
Фиг. 6. Хроматограмма стандартного раствора фенола с концентрацией 5 мг/мл. На хроматограмме обозначены пики фенола (время удерживания 5,200 мин и площадь пика 367,874) и 2-феноксиэтанола (время удерживания 6,300 мин и площадь пика 196,225).
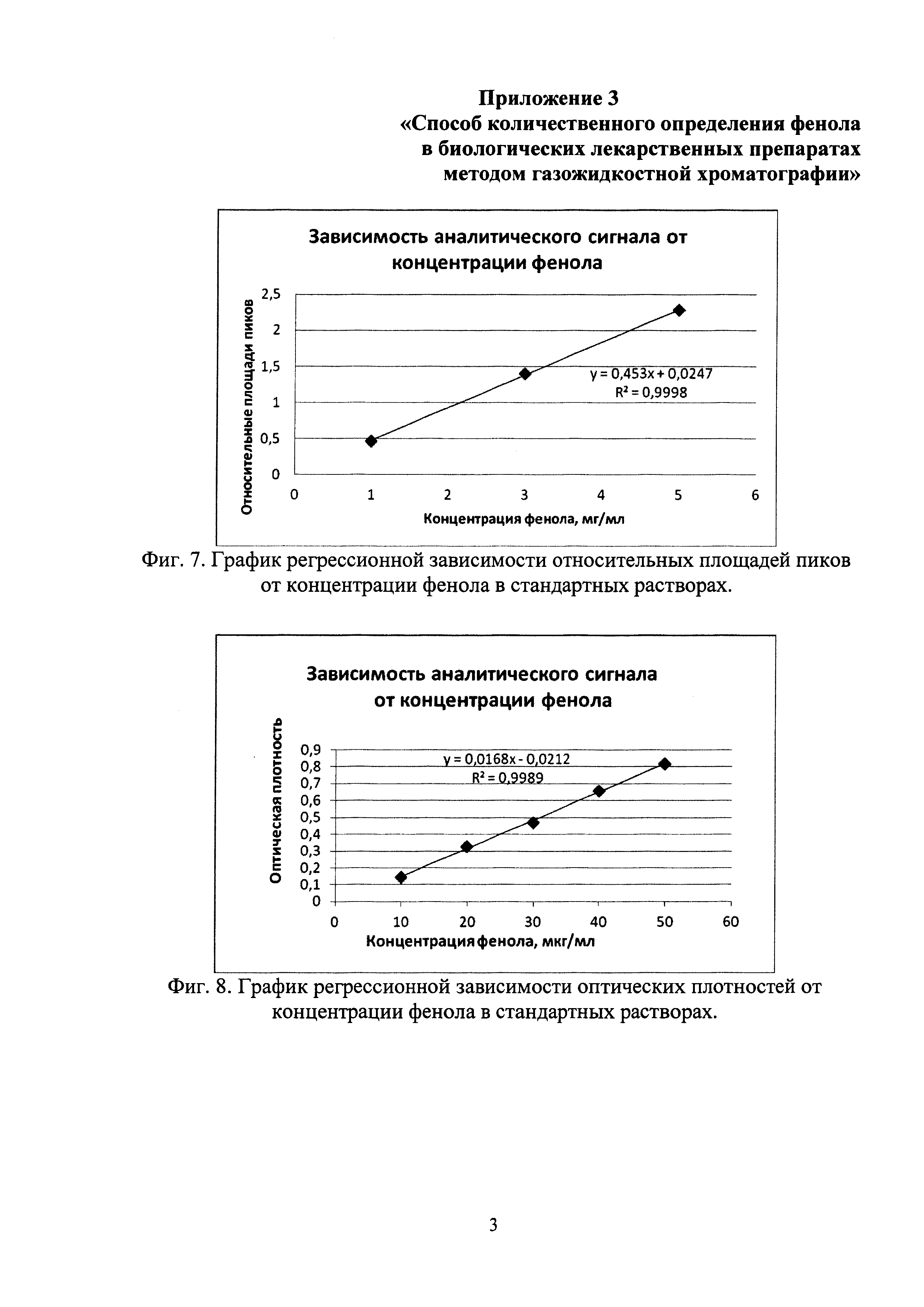
Фиг. 7. График регрессионной зависимости относительных площадей пиков от концентрации фенола в стандартных растворах. На рисунке представлен калибровочный график, полученный при воспроизведении заявляемого способа и отражающий зависимость отношения площади пика фенола к площади пика внутреннего стандарта от концентрации фенола в стандартном растворе.
Фиг. 8. График регрессионной зависимости оптических плотностей от концентрации фенола в стандартных растворах. На рисунке представлен калибровочный график, полученный при воспроизведении способа прототипа и отражающий зависимость оптической плотности от концентрации фенола в стандартном растворе.
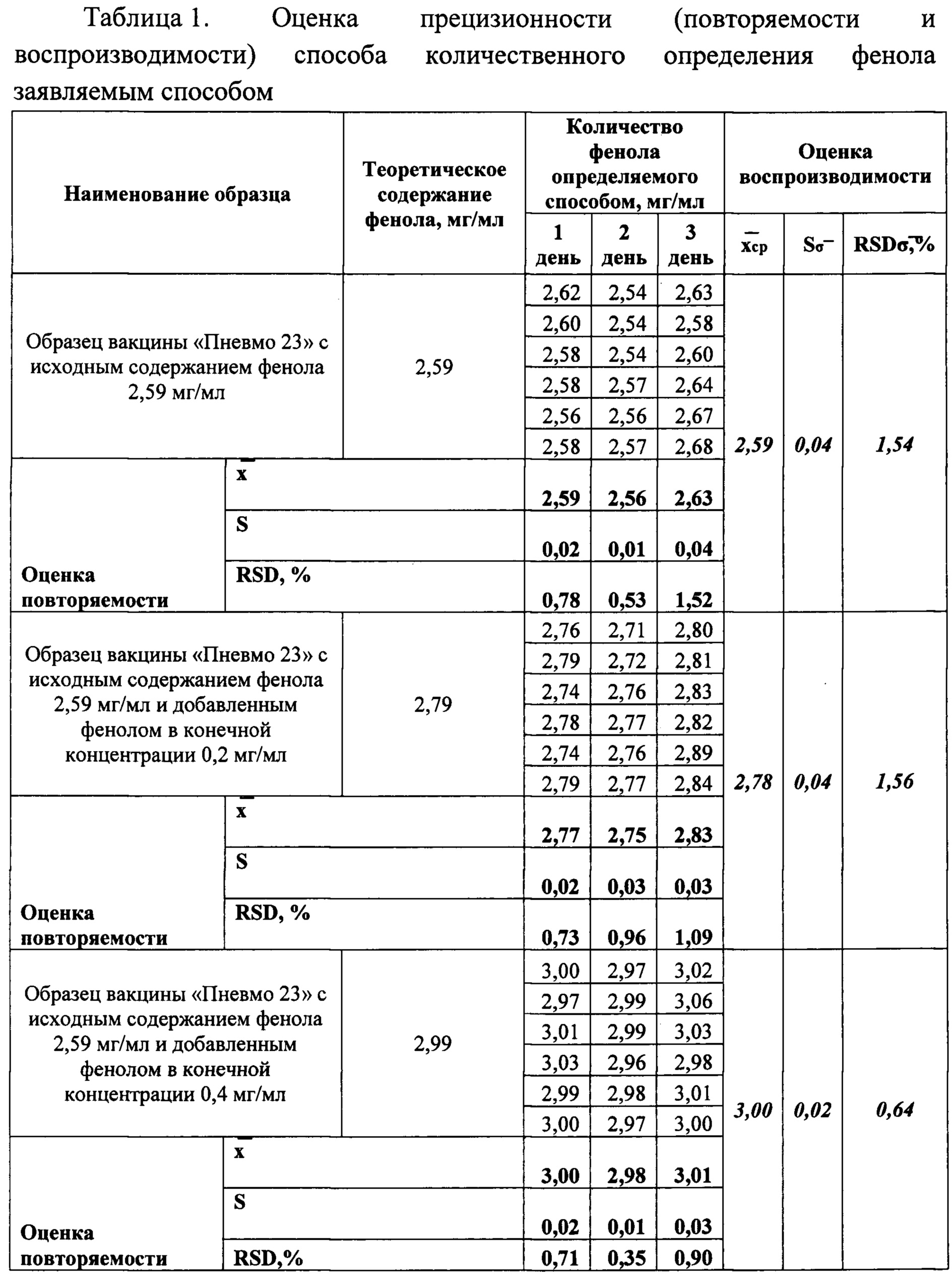
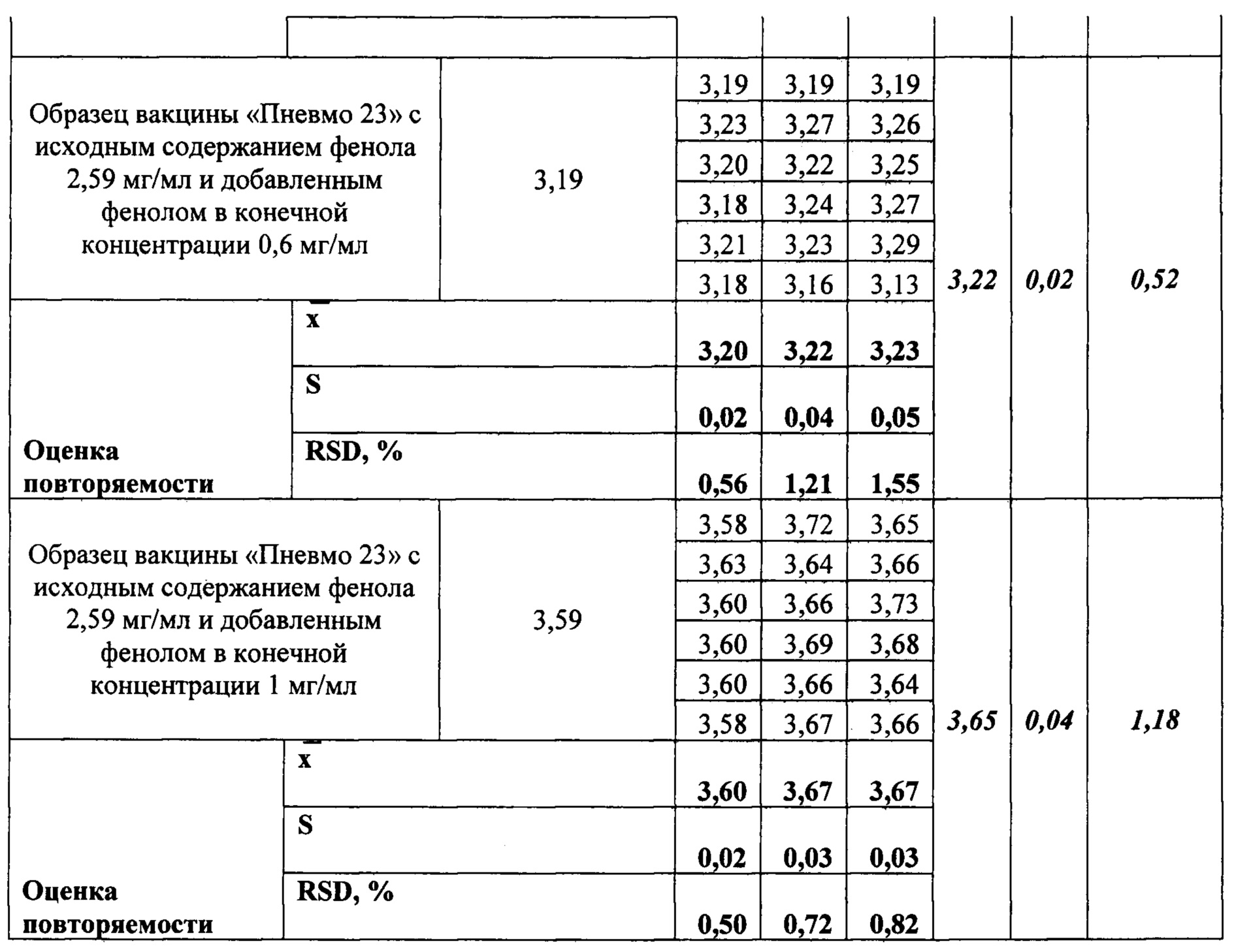
Таблица 1. Оценка прецизионности (повторяемости и воспроизводимости) способа количественного определения фенола заявляемым способом. Исследование проводили с применением метода добавок.
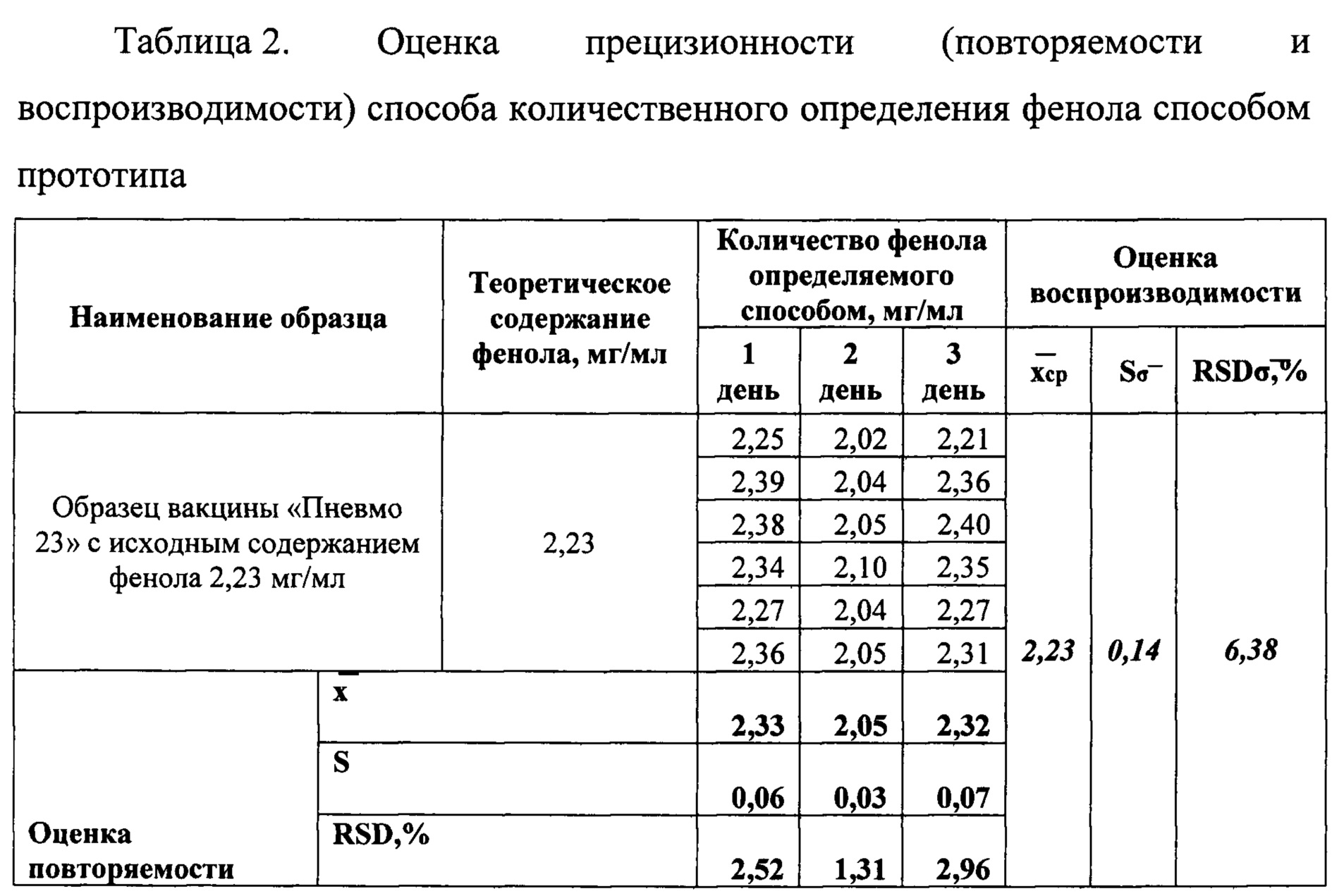
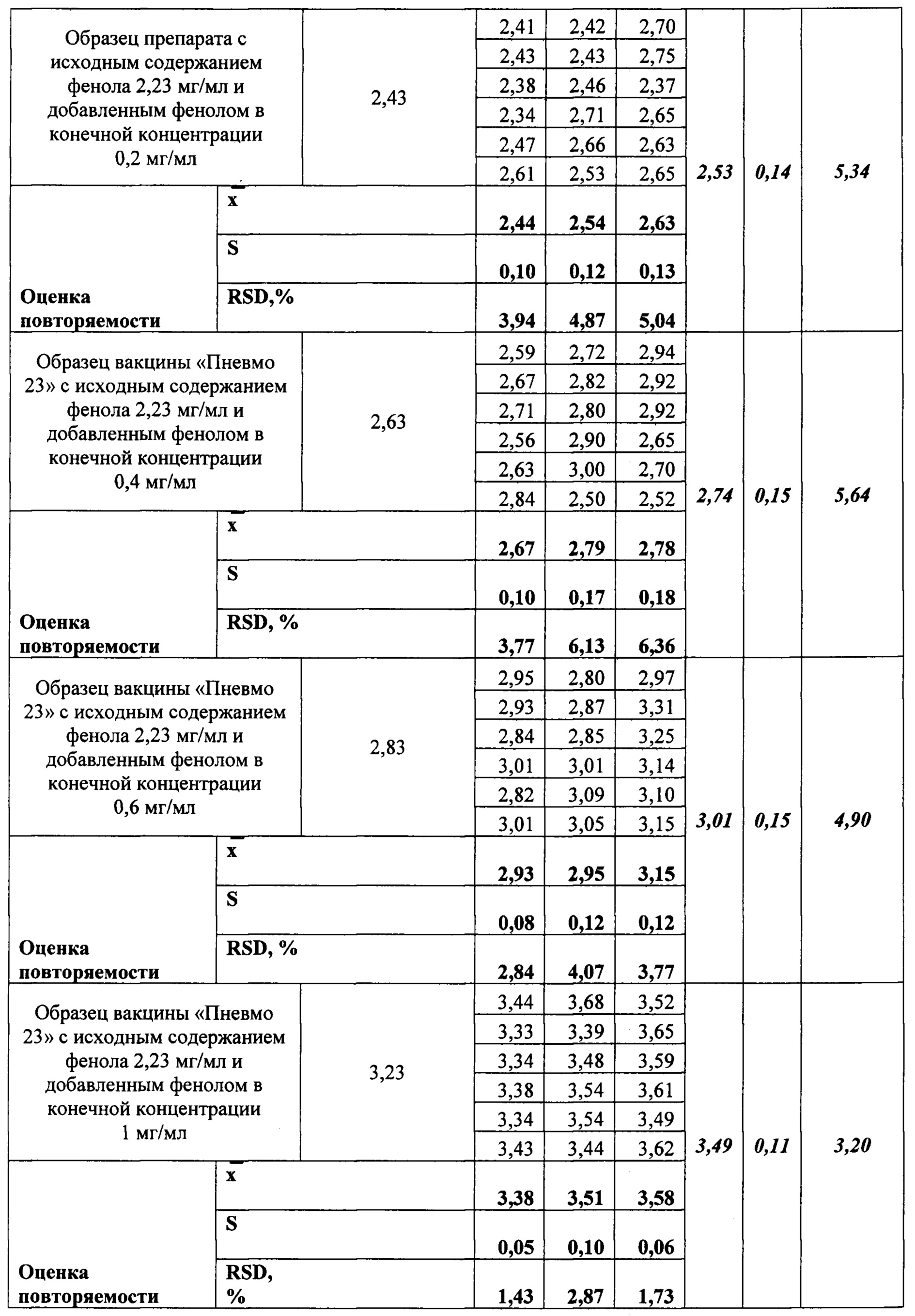
Таблица 2. Оценка прецизионности (повторяемости и воспроизводимости) способа количественного определения фенола способом прототипа. Исследование проводили с применением метода добавок.
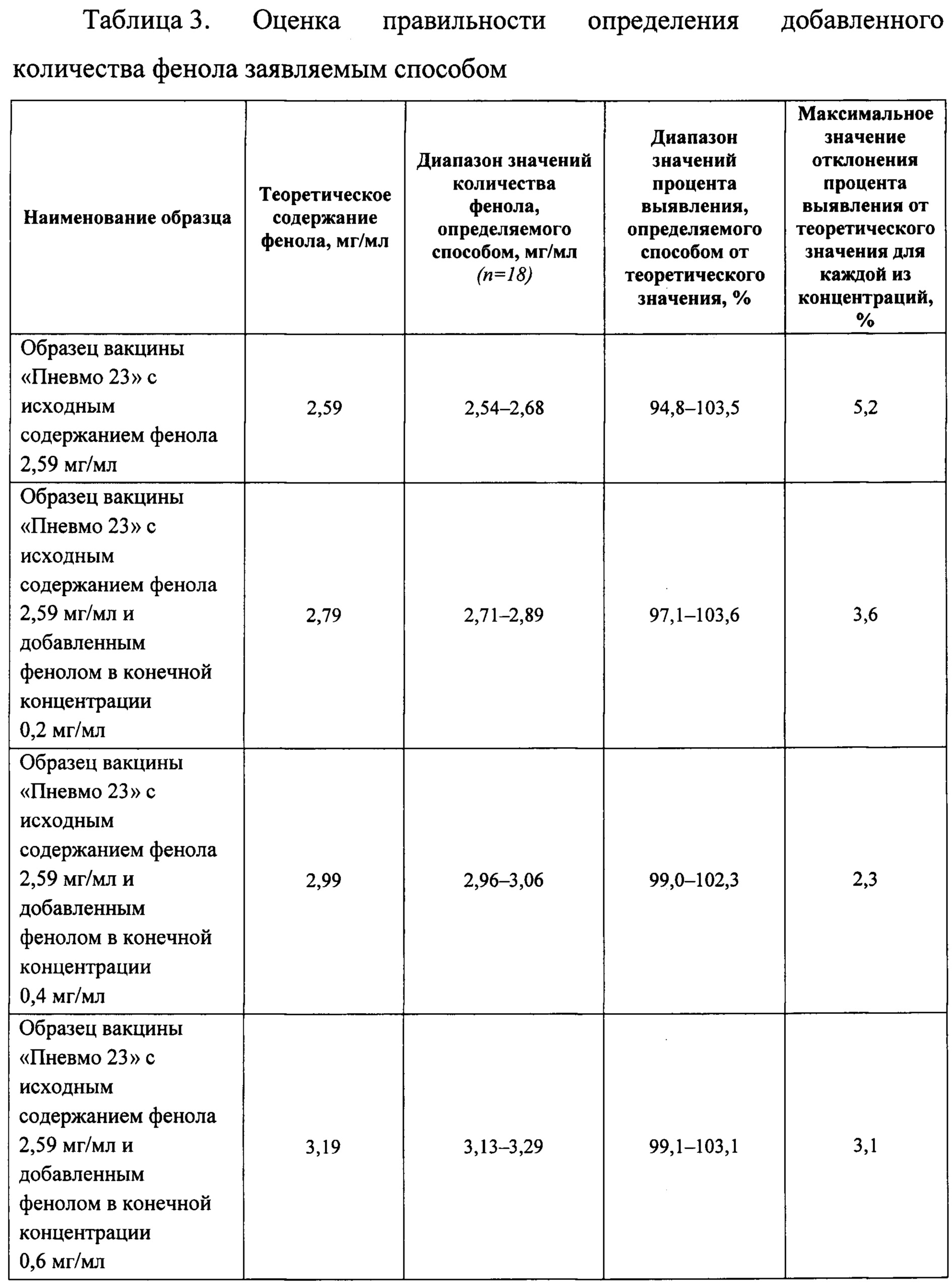
Таблица 3. Оценка правильности способа количественного определения фенола заявляемым способом. Исследование проводили с применением метода добавок.
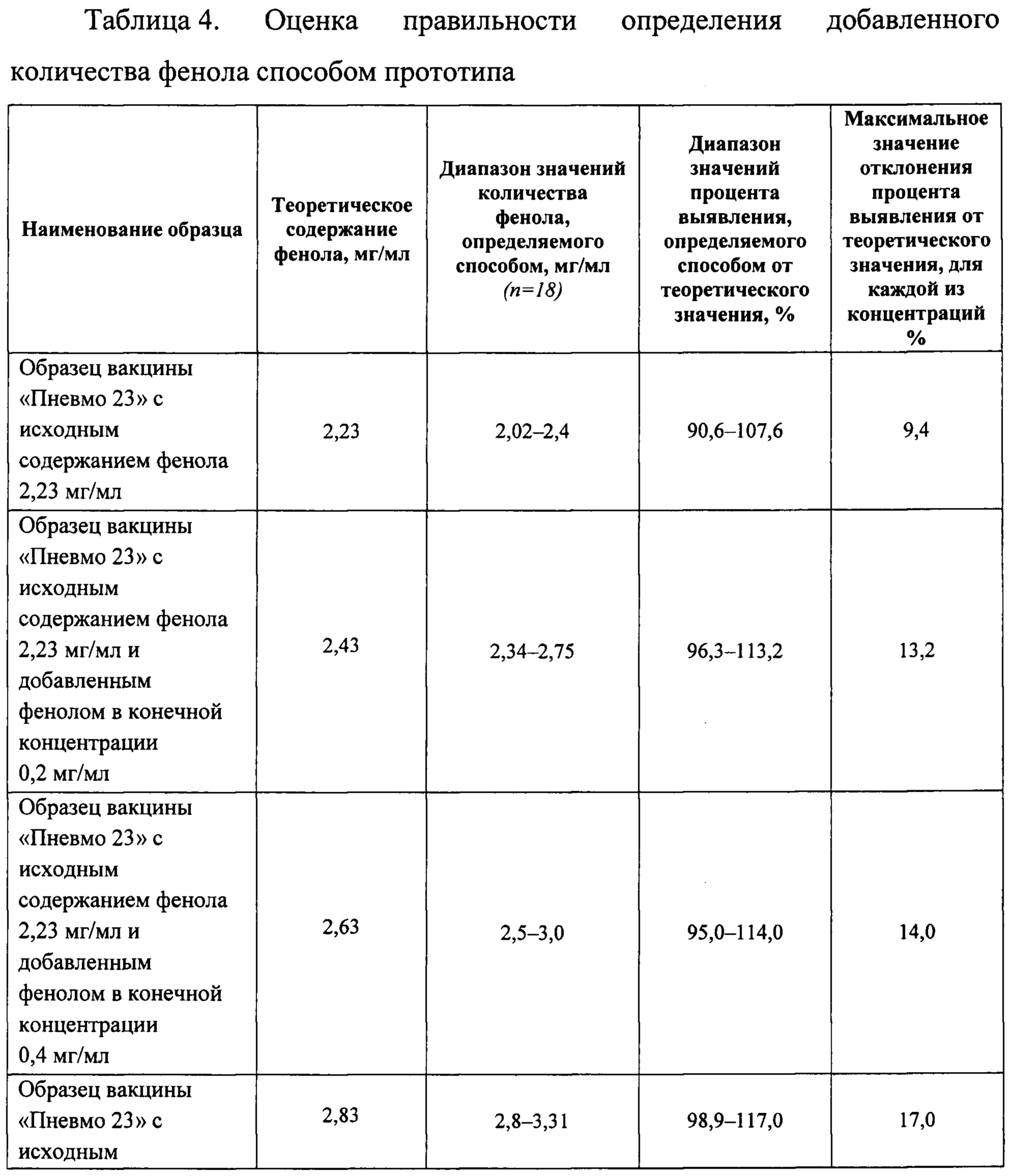
Таблица 4. Оценка правильности способа количественного определения фенола способом прототипа. Исследование проводили с применением метода добавок.
Возможность применения заявляемого изобретения показана следующими примерами:
Пример 1. Определение фенола в препарате «Аллерген Н-ал весенняя смесь ранняя», производство «Севафарма» а.о., Чешская республика (Фиг. 1) заявляемым способом.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл проводят в соответствии с описанием изобретения.
Исследуемый образец: 1,0 мл препарата «Аллерген Н-ал весенняя смесь ранняя», без предварительного разведения, вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Последовательность ввода образцов соответствует номеру виалы.
Подтверждение критериев пригодности хроматографической системы:
- коэффициент асимметрии пика 0,96;
- число теоретических тарелок 205260;
- разрешение пика 21,3.
Результат: содержание фенола в препарате 1,87 мг/мл. Данный пример показывает возможность использования заявляемого способа для определения фенола в указанном препарате.
Пример 2. Определение фенола в вакцине брюшнотифозной полисахаридной «Вианвак», производства «Гритвак», Россия (Фиг. 2) заявляемым способом.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл проводят в соответствии с описанием изобретения.
Исследуемый образец: 1,0 мл вакцины брюшнотифозной полисахаридной «Вианвак» без предварительного разведения вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Подтверждение критериев пригодности хроматографической системы:
- коэффициент асимметрии пика 0,98;
- число теоретических тарелок 232452;
- разрешение пика 22,26.
Результат: содержание фенола в препарате 1,29 мг/мл. Данный пример показывает возможность использования заявляемого способа для определения фенола в указанной вакцине.
Пример 3. Определение фенола в вакцине пневмококковой поливалентной полисахаридной «Пневмо 23», производства «Санофи Пастер», Франция. (Фиг. 3) заявляемым способом.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл проводят в соответствии с описанием изобретения.
Исследуемый образец: 1,0 мл вакцины пневмококковой поливалентной полисахаридной «Пневмо 23» без предварительного разведения вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Подтверждение критериев пригодности хроматографической системы:
- коэффициент асимметрии пика 0,95;
- число теоретических тарелок 232233;
- разрешение пика 21,95.
Результат: содержание фенола в препарате 2,06 мг/мл. Данный пример показывает возможность использования заявляемого способа для определения фенола в указанной вакцине.
Пример 4. Сравнение специфичности способов определения фенола.
В качестве образцов использованы препараты, отличные по составу (Примеры 1-3).

Данный пример показывает, что определение фенола заявляемым способом обладает большей специфичностью за счет возможности разделения компонентов исследуемого образца с последующей идентификацией пика фенола и его количественного определения.
Пример 5. Сравнение линейности способов определения фенола.

Данный пример показывает, что:
1. Аналитическая область заявляемого способа, охватывающая диапазон концентраций допустимого содержания фенола в препаратах БЛП, позволяет исключить стадию пробоподготовки (предварительное разведение образца), что повышает точность количественного определения за счет отсутствия дополнительного источника систематической и/или случайной ошибки определения.
2. Коэффициент детерминации, характеризующий линейность заявляемого способа, ближе к 1, что позволяет сделать вывод о большей точности значений, вычисленных с применением уравнения регрессионной зависимости заявляемого способа.
Пример 6. Сравнение прецизионности (повторяемости и воспроизводимости) способов определения фенола.
Для подтверждения прецизионности (повторяемости и воспроизводимости) заявляемого способа были проведены три независимых серии испытаний исходного образца вакцины пневмококковой поливалентной полисахаридной «Пневмо 23» с исходным содержанием фенола 2,59 мг/мл и 2,23 мг/мл и образцов с добавлением известного количества фенола. Каждый образец готовился в шести повторностях. Результаты определения повторяемости и воспроизводимости способа приведены в Таблице 1 (Приложение 4).
Для сравнительной оценки прецизионности соответствующее количество образцов и измерений было сделано с применением спектрофотометрического способа. Результаты приведены в Таблице 2 (Приложение 4).
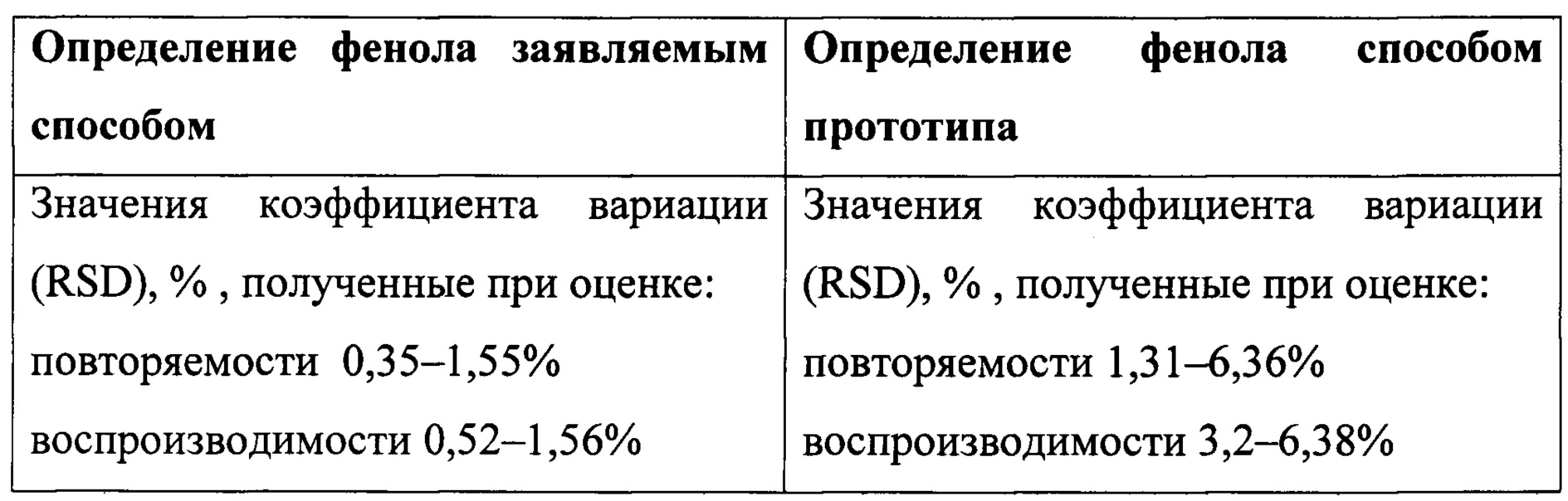
Данный пример показывает, что прецизионность заявляемого способа, характеристикой которой являются величины коэффициентов вариации значений, полученных в условиях повторяемости и воспроизводимости, выше, чем прецизионность способа-прототипа.
Пример 7. Сравнение правильности способов определения фенола.
Правильность способа подтверждают с помощью метода добавок. Вычисляют процент выявления фенола в образце относительно теоретического (истинного) значения. За теоретическое значение принимают сумму исходного количества фенола в препарате и количества фенола внесенного в препарат (добавленного). В качестве образцов использовали вакцину пневмококковую поливалентную полисахаридную «Пневмо 23» с исходным содержанием фенола 2,59 мг/мл и 2,23 мг/мл. Рассчитывали диапазоны значений процентов выявления для каждой из взятых концентраций. Максимальный диапазон значений процентов выявления определяли с учетом наименьшего и наибольшего из всех полученных значений. Результаты приведены в Таблицах 3 и 4 (Приложение 5).
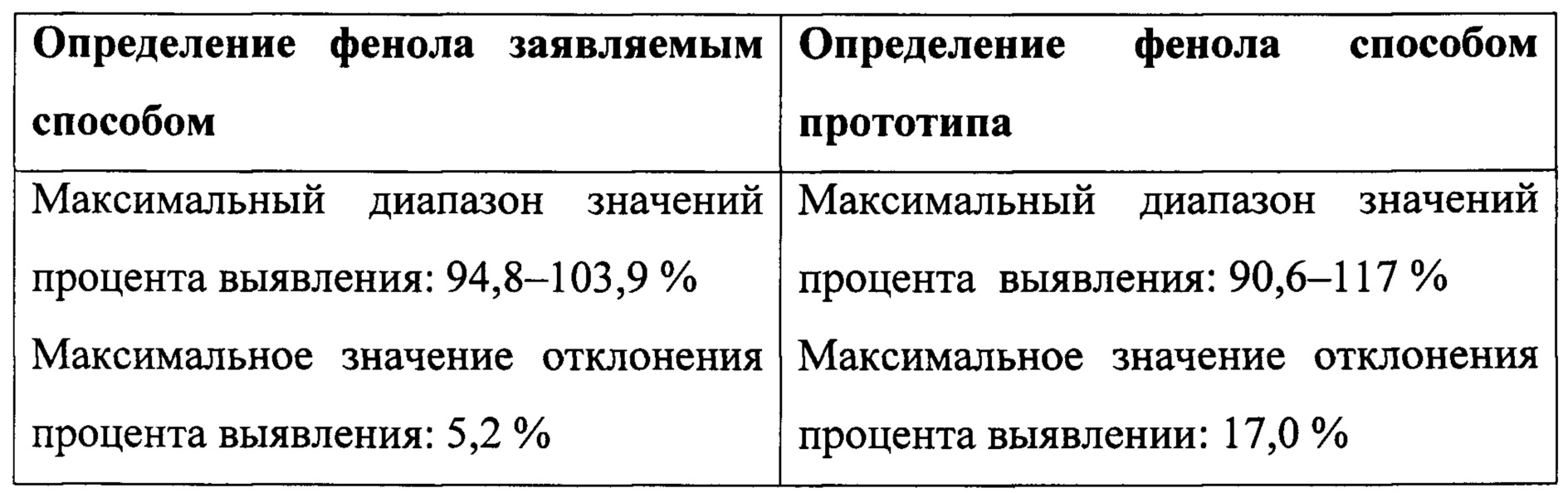
Данный пример показывает, что правильность заявляемого способа определения фенола выше, чем правильность способа прототипа, поскольку максимальное значение отклонения процента выявления определяемого количества фенола от теоретического (истинного) более чем в 3 раза меньше максимального значения отклонения процента выявления способа прототипа.
Источники информации
1. Способ определения фенола в аллергенах (SU, патент 989410, 1983).
2. Способ количественного определения фенола в крови (RU, патент 2188416,2002).
3. European Pharmacopoeia 9.2. Phenol in immunosera and vaccines 01/2008:20515 [Электронный ресурс] http://online6.edqm.eu/ep902/
4. Государственная фармакопея РФ. ГФ XIV. ОФС.1.7.2.0028.15 Количественное определение фенола спектрофотометрическим методом в иммунобиологических лекарственных препаратах [Электронный ресурс] http://femb.ru/femb/pharmacopea.php
5. ГОСТ ИСО 5725-2002 Точность (правильность и прецизионность) методов и результатов измерений.
6. Государственная фармакопея РФ. ГФ XIV. ОФС.1.1.0012.15 Валидация аналитических методик [Электронный ресурс] http://femb.ru/femb/pharmacopea.php
Приложение 4 к заявке на изобретение «Способ количественного определения фенола в биологических лекарственных препаратах методом газожидкостной хроматографии»
Приложение 5 к заявке на изобретение
«Способ количественного определения фенола в биологических лекарственных препаратах методом газожидкостной хроматографии»