Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ КОКЛЮШНОГО КОМПОНЕНТА КОМПЛЕКСНЫХ ВАКЦИН
Вид РИД
Изобретение
Способ получения коклюшного компонента комплексных вакцин
Изобретение относится к биотехнологии, в частности к способам прогнозирования иммуногенной активности коклюшного компонента комплексных вакцин.
Известен способ отбора и проверки иммуногенной активности колоний производственных штаммов коклюшных бактерий [1].
Способ включает следующие этапы: отбор колоний по морфологическим свойствам и определение поверхностных агглютиногенов 1, 2 и 3 (агг) с помощью реакции агглютинации адсорбированными типоспецифическими сыворотками к агглютиногенам 1, 2 и 3 при селекции штамма. Отбирают колонии, выросшие на плотной среде Борде-Жангу или казеино-угольном агаре (КУА) с 10% крови. Колонии коклюшных бактерий мелкие, диаметром от 0, 5 до 1,0 мм, выпуклые, круглые, с ровными краями, серого цвета, блестящие (в виде «жемчужин»), полупрозрачные, окруженные нерезко ограниченной зоной гемолиза. Если требованиям типичных колоний соответствуют менее 80% выросших колоний, то необходимо провести селекцию штамма, заключающуюся в повторном посеве культуры типичных колоний на среду Борде-Жангу или КУА. После отбора выросших колоний определяют поверхностные агглютиногены 1, 2 и 3 с помощью реакции агглютинации адсорбированными типоспецифическими сыворотками. Критерием оценки уровня иммуногенной активности испытуемого коклюшного компонента является количественное содержание в нем агглютиногенов, выявляемое адсорбированными сыворотками в титре не ниже 1:1280.
Общим с заявляемым способом являются следующие этапы: выращивание коклюшных бактерий на плотной среде Борде-Жангу или КУА, определение количественного содержания агглютиногенов в коклюшном компоненте на этапе селекции штамма.
К недостаткам ближайшего аналога (прототипа) следует отнести то, что отбор клеток только по морфологическим свойствам не всегда гарантирует получение культуры с высоким содержанием в клетках агглютиногенов 1, 2 и 3, присущих штамму В. pertussis, при этом критерий «титр 1:1280» не обеспечивает высокую и стабильную иммуногенную активность коклюшного компонента.
В связи с этим задачей данного изобретения является увеличение иммуногенной активности штаммов коклюшных бактерий и получение коклюшного компонента комбинированных вакцин, сохраняющего нормируемые показатели.
Данный технический результат достигается благодаря тому, что в заявленном способе получения коклюшного компонента комплексных вакцин предусмотрено следующее отличие - количественное содержание агглютиногенов в коклюшном компоненте комбинированных вакцин должно выявляться адсорбированными сыворотками в титре не менее 1:3200.
Сущность предложенного способа заключается в следующем. Способ получения коклюшного компонента комплексных вакцин, включающий следующие стадии: посев культуры В. pertussis на плотные питательные среды Борде-Жангу или казеино-угольный агар (КУА) с 10% крови, отбор по морфологическим признакам выросших колоний, пересев отобранных колоний на сектора чашки Петри, приготовление двукратных разведений сыворотки, стандартизацию коклюшной суспензии по оптическому стандарту мутности до концентрации 10 ME на 1 мл суспензии, внесение в разведенные сыворотки равного объема стандартизованной микробной взвеси, определение количественного содержания агглютиногенов в приготовленных коклюшных суспензиях с помощью реакции агглютинации адсорбированными типоспецифическими сыворотками, отбор коклюшных суспензий производят при условии выявления агглютиногенов 1, 2, 3 в титре не менее 1:3200.
Поставленная задача решается благодаря тому, что в способе получения коклюшного компонента комплексных вакцин, включающем отбор колоний В. pertussis по морфологическим свойствам, получение коклюшных суспензий с последующим определением в них поверхностных агглютиногенов 1, 2 и 3 с помощью реакции агглютинации адсорбированными типоспецифическими сыворотками, предусмотрены следующие отличия: для получения высокой иммуногенной активности коклюшного компонента комплексных вакцин агглютиногены должны выявляться адсорбированными сыворотками в титре не менее 1:3200.
Между совокупностью существенных признаков заявляемого способа и достигаемым техническим результатом существует причинно-следственная связь, а именно: повышение показателя количественного содержания агглютиногенов 1, 2 и 3 до содержания, выявляемого адсорбированными сыворотками в титре не менее 1:3200, гарантирует получение популяции коклюшных бактерий с высокой иммуногенной активностью.
Получение коклюшного компонента комплексных вакцин
Исследованиями показано, что агглютиногены участвуют в формировании противококлюшного иммунитета [2, 3]. В связи с этим в требованиях к коклюшной вакцине эксперты ВОЗ рекомендуют определять наличие агглютиногенов 1, 2 и 3 [3] в коклюшной вакцине. Критерии количественного содержания агглютиногенов в рекомендациях ВОЗ не указаны.
Уровень экспрессии коклюшными бактериями агглютиногенов 1, 2 и 3, определяемых адсорбированными типоспецифическими сыворотками в титре не менее 1:3200, обеспечивает высокую иммуногенную (протективную) активность коклюшного компонента комплексных вакцин.
Обоснованность выбора данного критерия подтверждается результатами лабораторной оценки иммуногенной активности в опыте экспериментального менингоэнцефалита, выражаемой в международных единицах (МЕ/мл) (пример, табл.1), а также выявлением корреляции между количественным содержанием агглютиногенов 1, 2 и 3 в коклюшном компоненте и его иммуногенной активностью (табл.5).
Критерии минимального содержания иммуногенной активности не менее 8 МЕ/мл коклюшной вакцины были установлены в международных исследованиях, проведенных в Британии [4] в 1956 году, которые коррелировали с профилактической эффективностью вакцины.
При условии содержания всех присущих штамму В. pertussis агглютиногенов в реакции агглютинации (РА) в титре менее 1:3200 необходимо провести селекцию, которая заключается в многократном (при низком уровне агглютиногенов) пересеве и отборе изолированных колоний штамма В. pertussis по количественному содержанию агглютиногенов 1, 2 и 3. Многократный отбор обусловлен гетерогенностью клеточной популяции по этому показателю, что согласуется с данными других исследователей [5, 6].
Отобранную по количественному содержанию агглютиногенов (в РА титр агглютиногенов 1:3200 и более) культуру выращивают на поверхности плотной питательной среды и лиофильно высушивают. Приготовленную лиофильно высушенную коклюшную культуру, содержащую высокий уровень агглютиногенов, хранят в ампулах или во флаконах под вакуумом при температуре минус 20°С (музейные штаммы) или (4±2)°С (посевные культуры); последние используют для приготовления коклюшного компонента комплексных вакцин.
Краткое описание чертежей
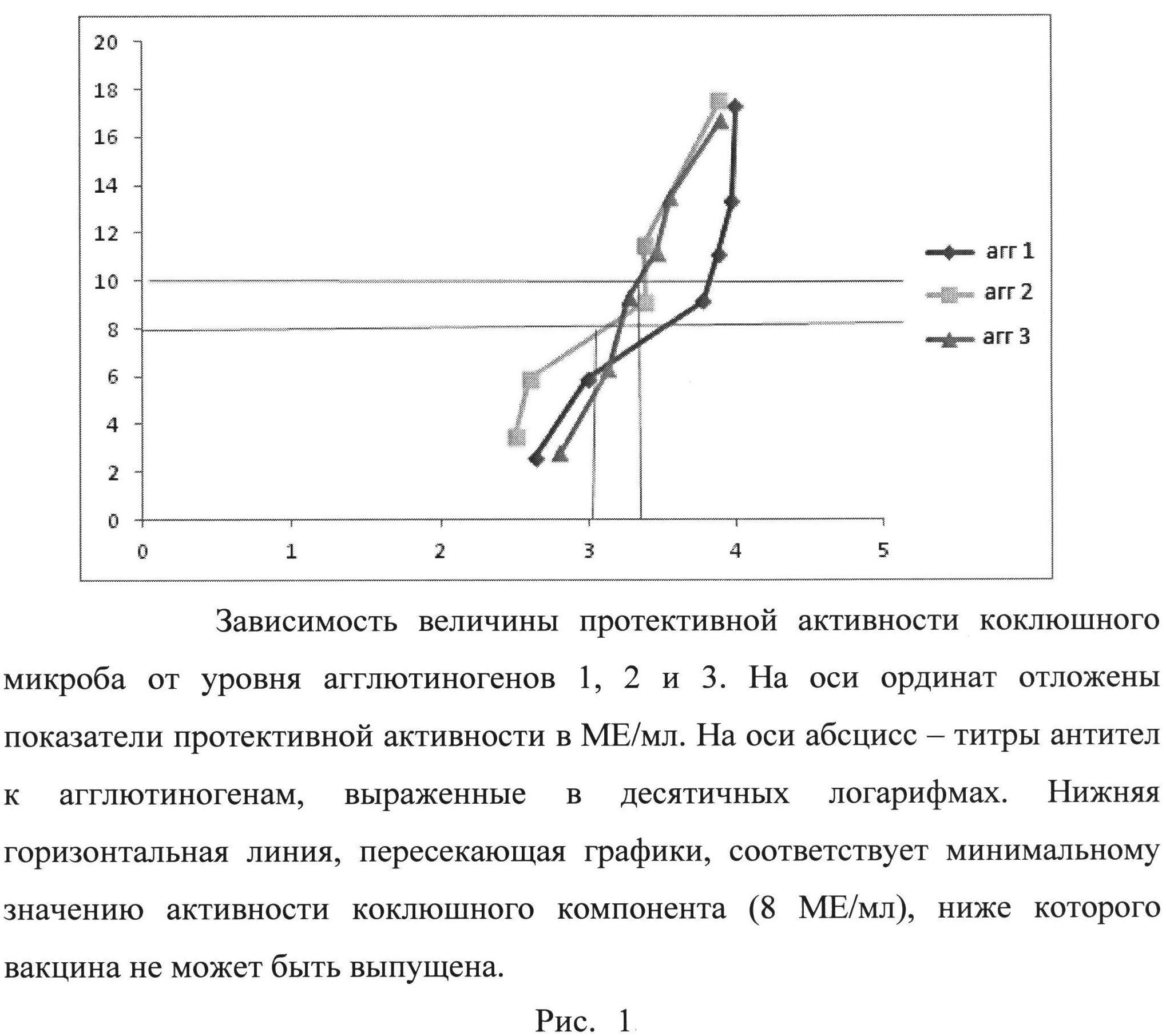
На рис. 1 показана зависимость величины протективной активности коклюшного микроба от уровня агглютиногенов 1, 2 и 3.
В таблице 1 представлена характеристика штаммов В. pertussis по количественному содержанию агглютиногенов и иммуногенной (протективной) активности.
В таблице 2 представлены данные о гетерогенности культуры коклюшных бактерий разных штаммов в отобранных единичных колониях, характерных I фазе (рост на плотной среде Борде-Жангу).
В таблице 3 приведено содержание агглютиногенов 1, 2 и 3 в производственных штаммах до и после проведенной селекции.
В таблице 4 приведены сведения, иллюстрирующие взаимосвязь между количественным содержанием в клетках коклюшных бактерий агглютиногенов 1, 2 и 3 и протективной активностью коклюшных бактерий.
В таблице 5 представлены титры антител к агглютиногенам 1, 2 и 3 коклюшного микроба в группах, сформированных по показателям иммуногенной (протективной) активности штаммов коклюшных бактерий, и соответствующая им протективная активность.
Возможность осуществления заявляемого изобретения показана следующим примером.
Пример. Увеличение иммуногенной активности штаммов коклюшных бактерий достигают посредством селекции отдельных колоний.
Необходимость селекции обусловлена тем, что коклюшная культура обладает значительной гетерогенностью. В таблице 2 представлены данные по содержанию агглютиногенов разными колониями производственных штаммов коклюшных бактерий, что демонстрирует гетерогенность выросшей культуры. Результаты, полученные в реакциях агглютинации на стекле и в более точной развернутой реакции в пробирках, имеют обозначения * и ** соответственно. Представленные данные демонстрируют, что изученные колонии различных штаммов коклюшной бактериальной клетки имеют на своей поверхности разное содержание агглютиногенов. Из 10-12 отобранных колоний можно выделить как колонии, экспрессирующие высокий уровень агглютиногенов, так и колонии с низким их содержанием. Только отбор клеток, экспрессирующих высокий уровень поверхностных агглютиногенов 1, 2 и 3, позволит получить высокоиммуногенную коклюшную суспензию.
Для получения коклюшной культуры, содержащей высокий уровень агглютиногенов, проводили селекцию отдельных колоний культуры первого пассажа по культуральным свойствам. С этой целью под микроскопом-лупой отбирали 10-15 типичных колоний (I фазы). Каждую колонию засевали на сектор чашки Петри со средой Борде-Жангу с 30% крови (6 секторов на 1 чашке). Чашки с культурой помещали в термостат при температуре (35,5±0,5)°С на 44-48 ч. Через 44-48 ч определяли активность выросшей культуры в развернутой реакции агглютинации с адсорбированными типоспецифическими сыворотками к агглютиногенам 1, 2, 3. Отбирали культуру, которая показала значения содержания агглютиногенов 1:3200 и выше, наращивали биомассу посредством посева на питательную среду; смытую культуру использовали для лиофильного высушивания. В случае если культура коклюшных бактерий агглютинировалась сывороткой в более низких разведениях (титр в РА менее 1:3200), то процедуру селекции необходимо повторить. Результаты проведенной селекции культуры представлены в таблице 3. Таблица демонстрирует значительное, более чем в 10 раз, увеличение содержания агглютиногенов для штамма №703. Для других штаммов также получен значительный прирост содержания агглютиногенов.
Изучение типоспецифического состава штаммов и иммуногенной активности вакцин проходило не одновременно, а на протяжении нескольких лет, в течение которых были использованы разные по активности адсорбированные сыворотки к агглютиногенам 1, 2 и 3 и разные лабораторные животные для оценки иммуногенной активности вакцин. Показатели парной ранговой корреляции свидетельствуют о наличии достаточно высокой связи между количественным содержанием агглютиногенов 1, 2 и 3 и иммуногенной активностью штаммов В. pertussis (табл.4).
Выбор величины критерия титр агглютиногенов 1:3200 (по РА), который мы предлагаем для оценки иммуногенной активности коклюшной суспензии, был сделан на основе материалов, представленных в таблице 5 и на рисунке 1. В таблицу 5 вошли данные, которые были объединены в группы, сформированные по показателям иммуногенной активности штаммов коклюшных бактерий. В первую группу были включены суспензии, защитная активность которых колебалась от 2,0 до 4,0 МЗЕ, во вторую от 4,1 до 6,0 МЗЕ и т.д. Из графика, представленного на рис. 1, видно, что при содержании всех агглютиногенов, выявляемых соответствующими адсорбированными сыворотками в разведении 1:1280 (lg 3,1) и выше, коклюшная суспензия по защитной активности (8 МЕ/мл) гарантированно соответствовала требованиям ВОЗ. В коклюшной суспензии с более выраженными иммуногенными свойствами (10 МЕ/мл и более) агглютиногены 1, 2 и 3 обнаружены в титре 1:3200 (lg 3,5) и выше. Выпуск вакцины на нижнем допустимом пределе протективной активности (8 МЕ/мл) и соответствующем ему уровне агглютиногенов (1:1280) не всегда гарантирует получение стабильного по этому показателю препарата на протяжении срока годности 2,5 г.
Для постановки реакции агглютинации используют коммерческий набор сывороток диагностических коклюшных к агглютиногенам 1, 2, 3 адсорбированных. В ампулу с сухими адсорбированными типоспецифическими сыворотками к агглютиногенам 1,2,3 добавляют 1,0 мл 0,9% раствора натрия хлорида, рН 7,1±0,2, для получения разведения 1:10 (с учетом исходного разведения сыворотки при адсорбции в 5 раз). Содержимое ампулы несколько раз перемешивают пипеткой до однородного состояния.
Для постановки развернутой РА готовят двукратные разведения сыворотки от 1:10 до 1:20480 на 0,9% растворе натрия хлорида рН 7,1±0,2.
В ряд пробирок, за исключением первой, вносят 0,5 мл 0,9% раствора натрия хлорида рН 7,1±0,2. Затем в первую и вторую пробирки вносят по 0,5 мл разведения сыворотки 1:10. После тщательного перемешивания содержимого второй пробирки 0,5 мл полученного разведения 1:20 из второй пробирки переносят в третью, где получают разведение 1:40, из третьей в четвертую и т.д. Из последней пробирки ряда, содержащей предельное разведение сыворотки, 0,5 мл жидкости удаляют для сохранения общего объема.
В ряд агглютинационных пробирок с двукратными разведениями сыворотки в объеме 0,5 мл вносят равный объем микробной взвеси с мутностью 10 международных оптических единиц (ME). Предварительно проводят стандартизацию коклюшной суспензии по оптическому стандарту мутности, устанавливая концентрацию 10 ME в 1 мл суспензии. При
постановке реакции проводят контроль сыворотки и антигена в тех же объемах на отсутствие спонтанной агглютинации:
-сыворотка в разведении 1:10 с 0,9% раствором натрия хлорида рН 7,1±0,2;
- микробная взвесь с 0,9% раствором натрия хлорида рН 7,1±0,2. Содержимое пробирок перемешивают путем встряхивания штатива.
Затем штатив помещают на 2 ч в термостат при температуре (36±1)°С, после чего оставляют на 18-20 ч при температуре (5±3)°С.
Результаты реакции агглютинации учитывают визуально до встряхивания пробирок, а затем для более точного учета - в агглютиноскопе при осторожном встряхивании осадка путем медленного наклона пробирки.
Учет реакции:
++++ - полная агглютинация: большой плотный осадок, четко виден зонтик, полное просветление надосадочной жидкости; после легкого встряхивания - крупные хлопья в прозрачной надосадочной жидкости;
+++ - осадок большой, рыхлый, надосадочная жидкость еще прозрачна, слегка опалесцирует; после легкого встряхивания - средние хлопья в слегка опалесцирующей надосадочной жидкости;
++ - мелкие, нестойкие хлопья, осадок небольшой, рыхлый, надосадочная жидкость непрозрачна; после легкого встряхивания - мелкие, нестойкие хлопья;
+ - следы агглютинации: в центре небольшой осадок, надосадочная жидкость непрозрачная;
- - отрицательная реакция: осадка нет или небольшой компактный осадок в центре дна пробирки, взвесь равномерно мутная.
Титром считают последнее разведение сыворотки, дающее агглютинацию на три креста.
В таблице 1 приведены данные по содержанию в производственных штаммах агглютиногенов, определенных в реакции агглютинации, и показатели иммуногенной активности вакцин, приготовленных из них. Штаммы, уровень агглютиногенов которых выявлялся сывороткой в низких титрах (менее 1:1280), обладали иммуногенной активностью, не удовлетворяющей нормативным требованиям (менее 8 МЕ/мл). Коклюшные бактерии стабильно проявляли высокую активность (10 МЕ/мл и более) при условии, если агглютиногены выявлялись сыворотками в титре 1:3200 и выше. В случае выявления у одного и того же штамма как высокого, так и низкого уровня разных агглютиногенов, вакцина, приготовленная из него, может в ряде случаев удовлетворять нормативным требованиям на протяжении не более 1,5 лет (например, штаммы №298, 345); при потере штаммом одного или нескольких присущих ему агглютиногенов (например, штамм №38) иммуногенная активность вакцины может не удовлетворять нормативным требованиям при выпуске.
Литература
1. МУК 4.2.2317-08. Отбор, проверка и хранение производственных штаммов коклюшных, паракоклюшных и бронхисептикозных бактерий. М., 2009.
2. WHO, Technical Report Series 800, Fortieth Report, 1990.
3. WHO, Technical Report Series, No 941, 2007. Annex 6. Recommendations for whole-cell pertussis vaccine.
4. Medical Research council. Vaccination against whooping-cough: Relation between protection in children and result of laboratory tests. // Brit. med. J., - 1956, - V 2, - No 4990, - P. 454-462.
5. Cameron J. Variation in Bordetella pertussis // J. Path. Bact. - 1967. - №94. - P. 367.
6. Standbridge T.N., Preston N.W. Variation of serotype in strains of Bordetella pertussis. // J. Hyg. Camb. - 1974. - No 73. - P. 305.
|
|
|
|
|