Результат интеллектуальной деятельности: ОФТАЛЬМОЛОГИЧЕСКИЕ КОМПОЗИЦИИ С УЛУЧШЕННОЙ ЗАЩИТОЙ ОТ ОБЕЗВОЖИВАНИЯ И УДЕРЖИВАНИЕМ
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
Настоящая заявка испрашивает приоритет согласно §119 раздела 35 Свода законов США на основании предварительной заявки на патент США № 61/642901, поданной 4 мая 2012 г., содержание которой полностью включено в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к композициям искусственных слез и композициям для доставки офтальмологических лекарственных средств, и более конкретно к композициям, содержащим галактоманнан, такой как гуар, гиалуроновую кислоту и цис-диол.
УРОВЕНЬ ТЕХНИКИ
Офтальмологические композиции для местного применения, в частности композиции искусственных слез, содержат соединения, которые смазывают и защищают поверхность глаза. В случае расстройств, связанных с сухостью глаз, композиции искусственных слез могут предотвратить такие симптомы, как боль и дискомфорт, и могут предотвратить биоадгезию и повреждение тканей, вызванное трением. Доступно большое количество потенциальных соединений, которые являются подходящими в качестве смазывающих материалов и средств для защиты поверхности глаза. Например, некоторые продукты искусственных слез, имеющиеся в продаже, содержат натуральные полимеры, такие как галактоманнаны. Другие смазывающие агенты и средства для защиты поверхности глаза включают, например, карбоксиметилцеллюлозу, глюкоманнан, глицерин и гидроксипропилметилцеллюлозу.
Как отмечено выше, в офтальмологических композициях, описанных ранее, используют соединения галактоманнана, такие как гуар. В патенте США № 6403609 автора Asgharian с названием изобретения «Офтальмологические композиции, содержащие полимеры галактоманнана и борат» (“Ophthalmic compositions containing galactomannan polymers and borate”) описаны такие системы, и содержание указанного патента полностью включено в настоящую заявку посредством ссылки.
Несмотря на то, что существующие композиции искусственных слез имеют некоторый успех, проблемы в лечении сухости глаза, тем не менее, остаются. Наряду с тем, что применение заменителей слез является временно эффективным, в целом необходимо повторное применение во время бодрствования пациента. Пациентам нередко приходится наносить раствор искусственных слез от десяти до двадцати раз в течение дня. Это действие является не только обременительным и трудоемким, но также потенциально очень дорогим. Проходящие симптомы сухости глаза, связанные с рефракционной хирургией, как сообщалось, в некоторых случаях длятся от шести недель до шести месяцев или более после операции.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к офтальмологическим композициям от сухости глаз, содержащим гуар и гиалуроновую кислоту. В композициях также присутствует цис-диол, такой как сорбитол или пропиленгликоль. В некоторых вариантах реализации настоящего изобретения в композиции также присутствует соединение бората. Композиции согласно настоящему изобретению обеспечивают улучшенные характеристики защиты от обезвоживания и характеристики удерживания. Композиции согласно настоящему изобретению также подходят в качестве носителя для доставки лекарственных средств при применении офтальмологических терапевтических средств.
Авторами настоящего изобретения обнаружено, что сочетание гуара и гиалуроновой кислоты демонстрирует синергетический эффект в отношении защиты от обезвоживания и удерживания на поверхности глаза по сравнению с композициями, содержащими только один из указанных полимеров.
Более того, композиции согласно настоящему изобретению продемонстрировали улучшенную стабильность при воздействии повышенных температур, таких как температуры, которые встречаются в ходе процессов стерилизации, таких как автоклавирование.
В вышеизложенном кратком описании широко описаны признаки и технические преимущества некоторых вариантов реализации настоящего изобретения. Дополнительные признаки и технические преимущества описаны в подробном описании изобретения, которое следует далее.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Более полное понимание настоящего изобретения и его преимуществ может быть получено, ссылаясь на следующее описание, которое следует рассматривать совместно с приложенными чертежами, на которых одинаковые ссылочные номера обозначают одинаковые признаки и где:
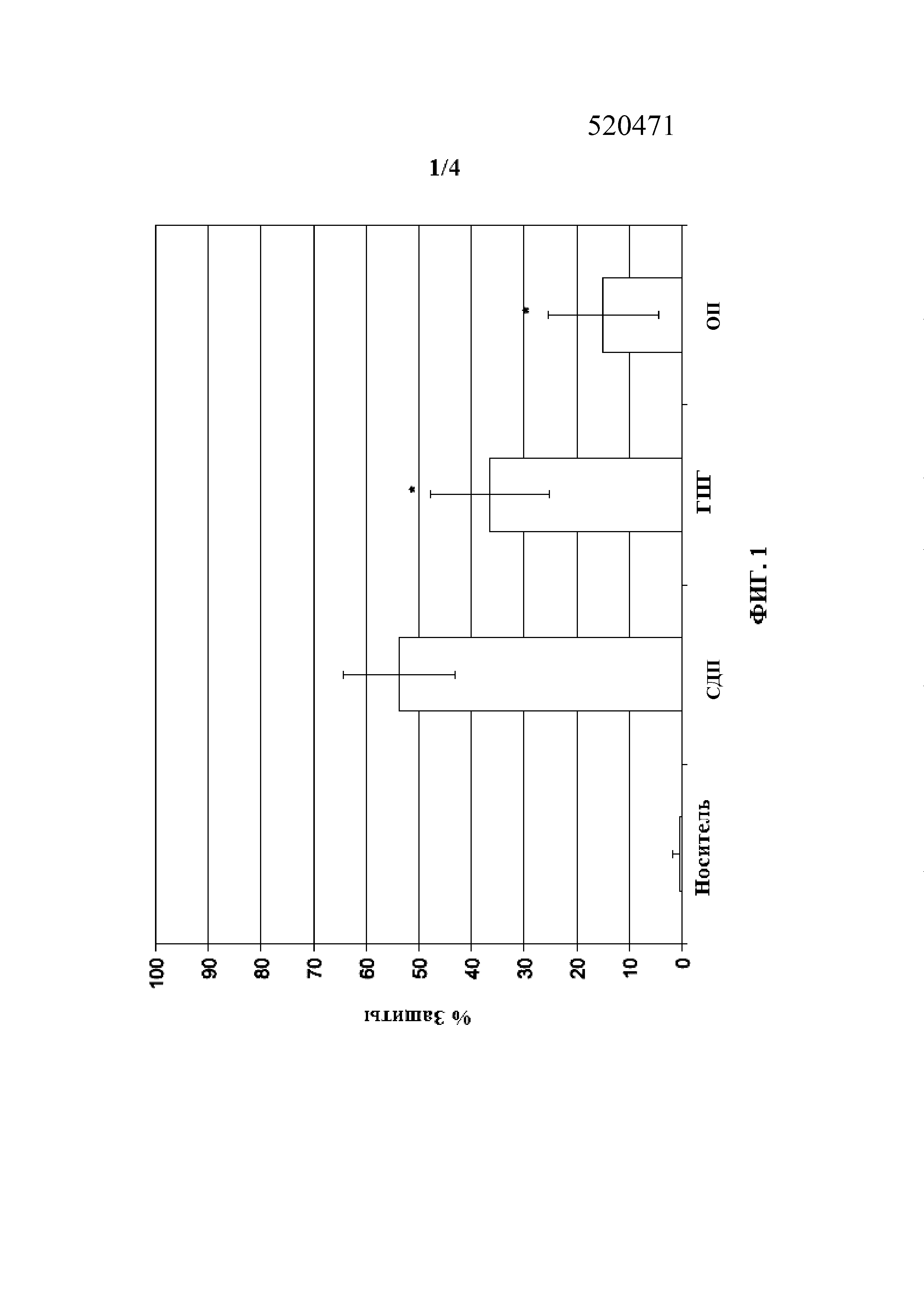
на Фиг. 1 представлена гистограмма сравнения характеристики обезвоживания композиции, содержащей как гидроксипропилгуар, так и гиалуроновую кислоту, с композициями, содержащими или гидроксипропилгуар, или гиалуроновую кислоту;
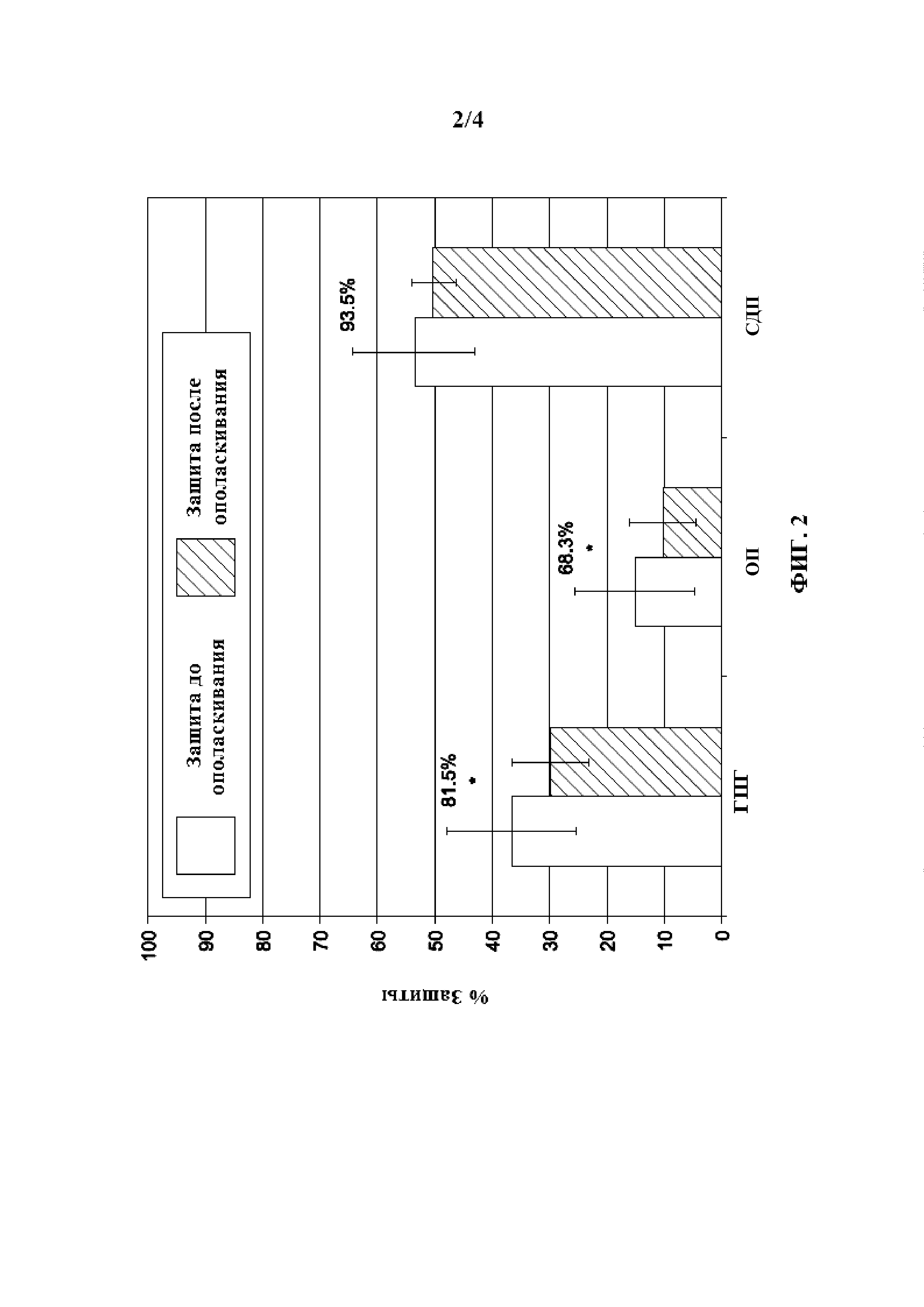
на Фиг. 2 представлена гистограмма сравнения характеристики удерживания композиции, содержащей гидроксипропилгуар и гиалуроновую кислоту, с композициями, содержащими только гидроксипропилгуар или гиалуроновую кислоту;
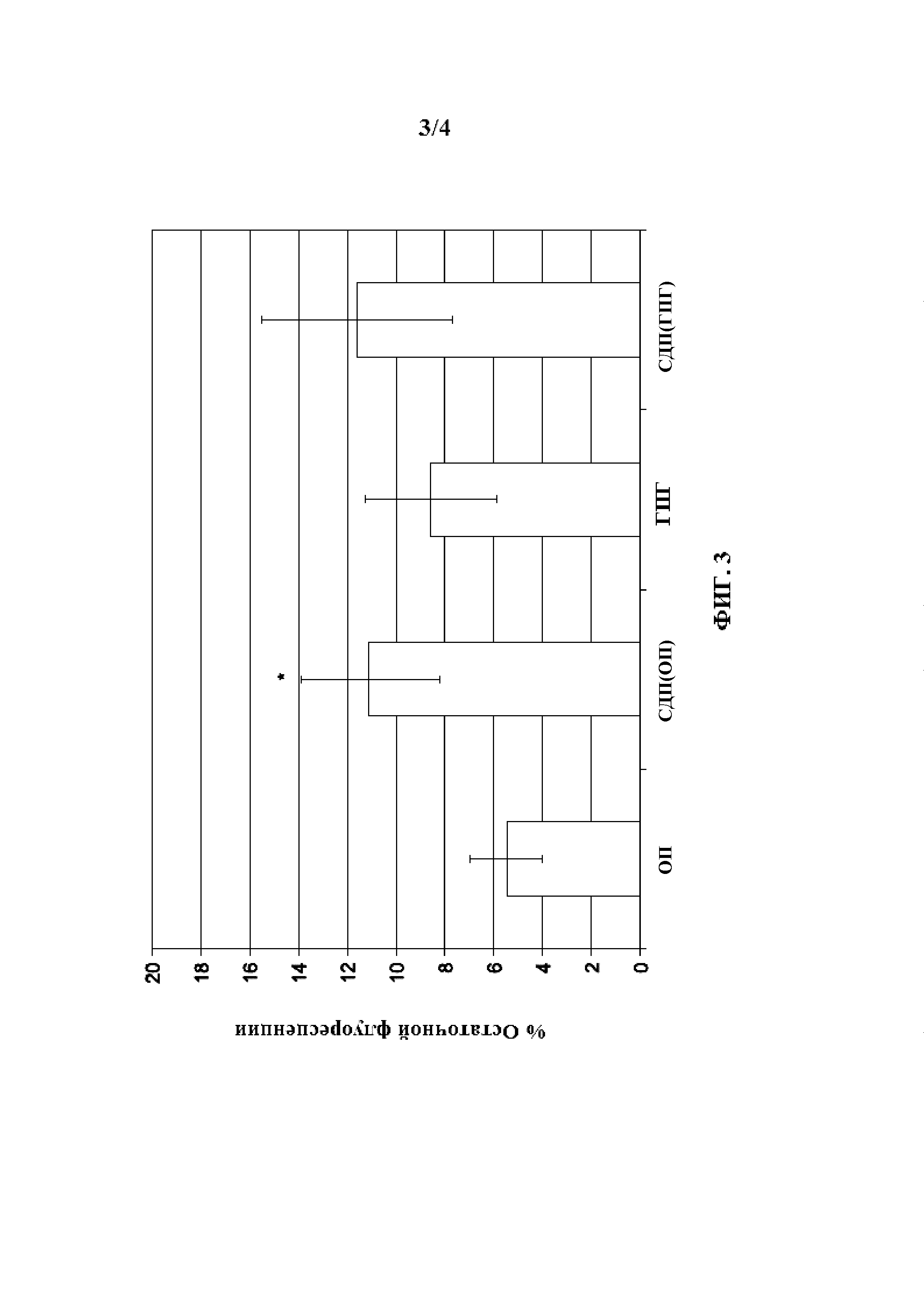
на Фиг. 3 представлена гистограмма сравнения удерживания флуоресцентно-меченых полимерных композиций и
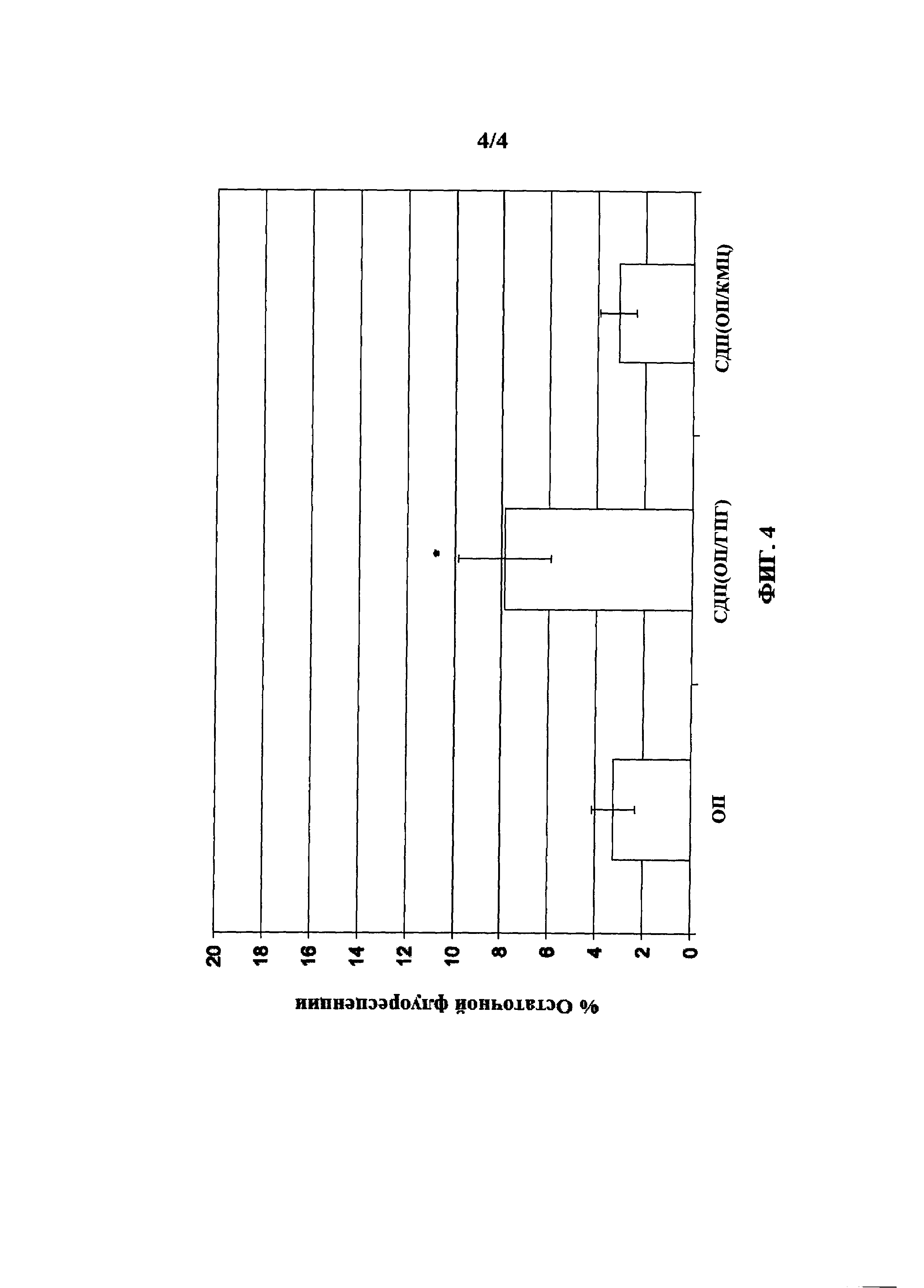
на Фиг. 4 представлена гистограмма сравнения удерживания композиции, содержащей гидроксипропилгуар/гиалуроновую кислоту, с композицией, содержащей гиалуроновую кислоту/карбоксиметилцеллюлозу.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Композиции согласно настоящему изобретению содержат галактоманнан, такой как гуар, гиалуроновую кислоту и цис-диол. Типы галактоманнанов, которые можно применять в настоящем изобретении, обычно получают из гуаровой камеди, камеди рожкового дерева и камеди тары. В настоящем документе термин «галактоманнан» относится к полисахаридам, полученным из вышеуказанных природных камедей или аналогичных природных или синтетических камедей, которые содержат остатки маннозы или галактозы или обе указанные группы в качестве основных структурных компонентов. Предпочтительные галактоманнаны согласно настоящему изобретению состоят из линейных цепочек (1- 4)-β-D-маннопиранозильных фрагментов и α-D-галактопиранозильных фрагментов, соединенных (1-6)-связями. В предпочтительных галактоманнанах отношение D-галактозы к D-маннозе варьируется, но обычно составляет от примерно 1:2 до 1:4. Галактоманнаны, имеющие соотношение D-галактоза:D-манноза примерно 1:2, являются наиболее предпочтительными. Кроме того, в определение «галактоманнан» также включены другие химически модифицированные вариации полисахаридов. Например, в галактоманнанах согласно настоящему изобретению можно произвести гидроксиэтил, гидроксипропил и карбоксиметилгидроксипропил замещения. Неионные вариации галактоманнанов, такие как вариации, содержащие алкокси и алкил (С1-С6) группы, являются особенно предпочтительными, когда необходимо получение мягкого геля (например, гидроксипропилзамещение). Заместители в гидроксильных положениях, не являющихся цис-положениями, являются наиболее предпочтительными. Примером неионного замещения в галактоманнане согласно настоящему изобретению является гидроксипропилгуар с молярным замещением примерно 0,4. В галактоманнанах также можно произвести анионные замещения. Анионное замещение является особенно предпочтительным, когда необходимо получение сильно реагирующих гелей. Галактоманнан, как правило, присутствует в композиции согласно настоящему изобретению в концентрации от примерно 0,025 до примерно 0,8 мас./об.%, предпочтительно от примерно 0,1 мас./об.% до примерно 0,2 мас./об.%, и более предпочтительно от примерно 0,17 до примерно 0,18 мас./об.%. Согласно одному варианту реализации настоящего изобретения, гидроксипропилгуар присутствует в концентрации примерно 0,175 мас./об.%. Предпочтительные галактоманнаны согласно настоящему изобретению представляют собой гуар и гидроксипропилгуар. Гидроксипропилгуар является особенно предпочтительным.
Гликозаминогликаны, такие как гиалуроновая кислота, представляют собой отрицательно заряженные молекулы. Гиалуроновая кислота представляет собой несульфатированный гликозаминогликан, состоящий из повторяющихся дисахаридных фрагментов N-ацетилглюкозамина (GlcNAc) и глюкуроновой кислоты (GlcUA), соединенных между собой с помощью чередующихся бета-1,4, и бета-1,3 гликозидных связей. Гиалуроновая кислота также известна как гиалуронан, гиалуронат или ГК (HA). В настоящем документе термин «гиалуроновая кислота» также включает солевые формы гиалуроновой кислоты, такие как гиалуронат натрия. Композиции согласно настоящему изобретению включают от примерно 0,05 до примерно 0,5 мас./об.% гиалуроновой кислоты. Согласно предпочтительному варианту реализации настоящего изобретения, гиалуроновая кислота присутствует в концентрации от примерно 0,1 до примерно 0,2 мас./об.% и более предпочтительно в концентрации от примерно 0,13 до 0,17 мас./об.%. Согласно одному варианту реализации настоящего изобретения, гиалуронат натрия присутствует в концентрации примерно 0,15 мас./об.%. Предпочтительной гиалуроновой кислотой является гиалуронат натрия. Молекулярная масса гиалуроновой кислоты, применяемой в композициях согласно настоящему изобретению, может варьироваться, но, как правило, составляет от 0,5 до 2,0 кДа. Согласно одному варианту реализации настоящего изобретения, гиалуроновая кислота имеет молекулярную массу от 900000 до 1 кДа. Согласно другому варианту реализации настоящего изобретения, гиалуроновая кислота имеет молекулярную массу от 1,9 до 2,0 кДа.
Цис-диольные соединения, которые можно применять согласно вариантам реализации настоящего изобретения, включают, но не ограничиваются ими, гидрофильные углеводы, такие как сорбитол или маннитол, которые содержат цис-диольные группы (гидроксильные группы, присоединенные к соседним атомам углерода). Предпочтительные цис-диольные соединения согласно настоящему изобретению включают полиэтиленгликоли, полипропиленгликоли и блок-сополимеры полиэтиленоксида-полибутиленоксида. Особенно предпочтительными цис-диольными соединениями являются сорбитол и маннитол. Цис-диольные соединения присутствуют в композициях согласно настоящему изобретению в концентрациях от примерно 0,5 до 5,0 мас./об.% и предпочтительно присутствуют в концентрации от примерно 1,0 до 2,0 мас./об.%. Согласно одному варианту реализации настоящего изобретения, сорбитол присутствует в концентрации примерно 1,4%. В целом, молекулярная масса таких цис-диольных соединений находится в диапазоне от 400 г/моль до 5000000 г/моль.
При условии наличия в композиции согласно настоящему изобретению, борат, как правило, присутствует в концентрации от примерно 0,1 до примерно 1,8 мас./об.%. Согласно предпочтительному варианту реализации настоящего изобретения, борат присутствует в концентрации от 0,3 до 0,4 мас./об.%. Согласно одному варианту реализации настоящего изобретения, борная кислота присутствует в концентрации примерно 0,35 мас./об.%. В настоящем документе термин «борат» относится ко всем фармацевтически приемлемым формам боратов, включая, но не ограничиваясь ими, борную кислоту и бораты щелочных металлов, такие как борат натрия и борат калия. Борная кислота является предпочтительным боратом, применяемым согласно вариантам реализации настоящего изобретения.
Композиции согласно настоящему изобретению могут необязательно содержать одно или более дополнительных вспомогательных веществ и/или один или более дополнительных активных ингредиентов. Вспомогательные вещества, обычно применяемые в фармацевтических композициях, включают, но не ограничиваются ими, смягчающие агенты, агенты, регулирующие тоничность, консерванты, хелатирующие агенты, буферные агенты и поверхностно-активные вещества. Другие вспомогательные вещества включают солюбилизирующие агенты, стабилизирующие агенты, агенты, усиливающие комфорт, полимеры, смягчающие вещества, рН-регулирующие агенты и/или смазывающие вещества. В композициях согласно настоящему изобретению можно применять любое из множества вспомогательных веществ, включая воду, смеси воды и смешиваемых с водой растворителей, таких как С1-С7-алканолы, растительные масла или минеральные масла, содержащие от 0,5 до 5% нетоксичных полимеров, растворимых в воде, природные продукты, такие как альгинаты, пектины, трагакантовая камедь, камедь карайи, ксантановая камедь, каррагенин, агар и аравийская камедь, производные крахмала, такие как ацетат крахмала и гидроксипропилкрахмал, а также другие синтетические продукты, такие как поливиниловый спирт, поливинилпирролидон, поливинилметиловый эфир, полиэтиленоксид, предпочтительно поперечно-сшитая полиакриловая кислота и смеси этих продуктов.
Смягчающие агенты, применяемые согласно вариантам реализации настоящего изобретения, включают, но не ограничиваются ими, глицерин, поливинилпирролидон, полиэтиленоксид, полиэтиленгликоль, пропиленгликоль и полиакриловую кислоту. Особенно предпочтительными смягчающими агентами являются пропиленгликоль и полиэтиленгликоль 400.
Подходящие агенты, регулирующие тоничность, включают, но не ограничиваются ими, маннитол, хлорид натрия, глицерин и им подобные. Подходящие буферные агенты включают, но не ограничиваются ими, фосфаты, ацетаты и им подобные, и аминоспирты, такие как 2-амино-2-метил-1-пропанол (AMP). Подходящие поверхностно-активные вещества включают, но не ограничиваются ими, ионные и неионные поверхностно-активные вещества, в то время как предпочтительными являются неионные поверхностно-активные вещества, RLM-100, POE 20 цетилстеариловые эфиры, такие как Procol® CS20, и полоксамеры, такие как Pluronic® F68.
Композиции, приведенные в настоящем документе, могут содержать один или более консервантов. Примеры таких консервантов включают сложный эфир п-гидроксибензойной кислоты, перборат натрия, хлорит натрия, спирты, такие как хлорбутанол, бензиловый спирт или фенилэтанол, производные гуанидина, такие как полигексаметиленбигуанид, перборат натрия, поликватерниум-1 или сорбиновую кислоту. Согласно некоторым вариантам реализации настоящего изобретения, композиция может быть консервированной сама по себе, таким образом, необходимости в применении консерванта нет.
Композиции согласно настоящему изобретению представляют собой офтальмологически подходящие композиции для применения для глаз пациента. Термин "водный" обычно обозначает водную композицию, в которой вспомогательное вещество составляет >50%, более предпочтительно >75%, в частности >90%, от массы воды. Эти капли можно наносить из ампулы с однократной дозой, которая предпочтительно может быть стерильной и, таким образом, делает бактериостатические компоненты композиции ненужными. Кроме того, капли можно наносить из многодозовой бутылки, которая предпочтительно может содержать устройство, которое извлекает любой консервант из композиции при нанесении, такие устройства известны в данной области.
Композиции согласно настоящему изобретению предпочтительно являются изотоническими или незначительно гипотоническими в целях борьбы с любой гипертоничностью слез, вызванной испарением и/или болезнью. Агент, регулирующий тоничность, может потребоваться для доведения осмоляльности композиции до уровня примерно или около 210-320 миллиосмолей на килограмм (мОсм/кг). Композиции согласно настоящему изобретению в целом имеют осмоляльность в интервале 220-320 мОсм/кг и предпочтительно имеют осмоляльность в интервале 235-300 мОсм/кг. Офтальмологические композиции в целом готовят в виде стерильных водных растворов.
Композиции согласно настоящему изобретению также можно применять для введения фармацевтически активных соединений для лечения, например, глазных болезней, таких как глаукома, дегенерация желтого пятна и глазная инфекция. Такие соединения включают, но не ограничиваются ими, терапевтические средства для лечения глаукомы, обезболивающие, противовоспалительные и противоаллергические лекарственные средства и противомикробные средства. Более конкретные примеры фармацевтически активных соединений включают бетаксолол, тимолол, пилокарпин, ингибиторы карбоангидразы и простагландины; дофаминергические антагонисты; послеоперационные противогипертензивные средства, такие как парааминоклонидин (Апраклонидин); противоинфекционные средства, такие как ципрофлоксацин, моксифлоксацин и тобрамицин; нестероидные и стероидные противовоспалительные средства, такие как напроксен, диклофенак, непафенак, супрофен, кеторолак, тетрагидрокортизол и дексаметазон; терапевтические средства для лечения сухости глаз, такие как ингибиторы PDE4; и противоаллергические лекарственные средства, такие как ингибиторы H1/H4, ингибиторы H4 и олопатадин.
Также предполагают, что концентрации ингредиентов, содержащихся в композиции согласно настоящему изобретению, могут варьироваться. Обычному специалисту в данной области будет понятно, что эти концентрации могут варьироваться в зависимости от добавления, замещения и/или удаления ингредиентов из данной композиции.
Предпочтительные композиции получают с применением буферной системы, которая поддерживает рН композиции от примерно 6,5 до примерно 8,0. Предпочтительными композициями для местного применения (в частности, офтальмологическими композициями для местного применения, как отмечено выше) являются композиции, которые имеют физиологическое значение рН, соответствующее ткани, на которую композиция будет применена или распределена.
Согласно конкретным вариантам реализации, композицию согласно настоящему изобретению вводят один раз в день. Однако эти композиции могут быть также приготовлены для введения с любой частотой, в том числе один раз в неделю, один раз каждые 5 дней, один раз каждые 3 дня, один раз каждые 2 дня, два раза в день, три раза в день, четыре раза в день, пять раз в день, шесть раз в день, восемь раз в день, каждый час или с большей частотой. Такую частоту дозирования также поддерживают в течение различной продолжительности времени в зависимости от схемы приема терапевтических средств. Продолжительность конкретной схемы приема терапевтических средств может варьироваться от однократного дозирования до схемы приема, которая длится в течение нескольких месяцев или лет. Специалисту в данной области техники хорошо известно определение схемы приема терапевтических средств для конкретного симптома.
Следующие примеры представлены, чтобы дополнительно проиллюстрировать выбранные варианты реализации настоящего изобретения.
ПРИМЕР 1
|
ПРИМЕР 2
Композиции согласно настоящему изобретению, содержащие гуар и гиалуронат, автоклавировали при стандартных условиях. Как показано ниже в Таблице 1, композиция, содержащая сорбитол, имеет стабилизированную молекулярную массу по сравнению с композицией, которая не содержит сорбитол.
|
ПРИМЕР 3
Способность композиций согласно настоящему изобретению защищать эпителиальные клетки человека от стресса из-за обезвоживания оценивали следующим образом. Человеческие трансформированные эпителиальные клетки роговицы высевали в количестве 0,09×106 клеток/мл на 48-луночные планшеты с коллагеновым покрытием (BD Biosciences #35-4505) и выращивали до смыкания монослоя на среде EpiLife (Invitrogen #MEPI500CA), дополненной добавкой для роста роговицы человека (HCGS Invitrogen #S0095), в течение 48 часов. Клетки обрабатывали испытуемыми растворами в течение 30 минут при 37°С, затем однократно ополаскивали (250 мкл) средой без добавки. Все растворы осторожно удаляли и клетки подвергали обезвоживанию при 45% влажности, 37°С в течение 30 минут в камере для обезвоживания (Caron Environmental Chamber 6010 Series). Жизнеспособность клеток определяли, применяя MTS-тест (Promega #G5421) для расчета % защиты относительно контрольной среды. Оценку удерживания раствора на поверхности клеток проводили посредством измененного вышеуказанного эксперимента обезвоживания, в котором выполняли пять «ополаскиваний средой» после 30-минутной инкубации исследуемого раствора. Среди тестируемых растворов присутствовали композиция, содержащая гидроксипропилгуар (ГПГ), композиция, содержащая гиалуроновую кислоту (ГК), и композиция согласно настоящему изобретению, содержащая как гидроксипропилгуар, так и гиалуроновую кислоту (ГПГ/ГК).
Как показано на Фиг. 1 и в Таблицах 2 и 3 ниже, композиция c двумя полимерами (DPS composition) показала значительно большую защиту от обезвоживания, чем раствор ГПГ или раствор ГК. Как показано на Фиг. 2 и в Таблице 3, раствор ГПГ/ГК также продемонстрировал большее удерживание на эпителиальной поверхности, чем раствор ГПГ или раствор ГК. Синергетический эффект был отмечен по отношению к защите от обезвоживания и поведению при удерживании на поверхности раствора ГПГ/ГК.
|
|
Среднее время удерживания композиции согласно настоящему изобретению сравнивали с ее отдельными компонентами. Вкратце, декстран, меченный флуоресцеином, с молекулярной массой приблизительно 70 кДа (Molecular Probes, Eugene, Орегон) добавляли к каждому испытуемому составу в концентрации 0,1 мас./об.%. Для мониторинга ослабления сигнала, соответствующего удалению составов, применяли сканирующий флуорофотометр (Ocumetrics, Mountain View, Калифорния). Как показано на Фиг. 3 и в Таблице 4 ниже, индивидуальное флуоресцентное мечение полимерных компонентов раствора ГПГ/ГК демонстрирует увеличение количества полимера, связанного с эпителиальной поверхностью, когда полимеры гидроксипропилгуар и гиалуроновую кислоту применяли в сочетании. На Фиг. 4 и в Таблице 5 показано, что этот эффект улучшенного удерживания не был отмечен в составе с двумя полимерами, содержащими гиалуроновую кислоту и карбоксиметилцеллюлозу (ГК/КМЦ).
|
|
Как показано в Таблице 6, в которой представлены данные по сравнению свойств защиты от обезвоживания и защиты посредством удерживания композиций для сухости глаз, имеющихся в продаже, содержащих гиалуроновую кислоту, композиция, содержащая ГПГ/ГК, продемонстрировала значительно большую защиту от обезвоживания и защиту посредством удерживания относительно протестированных ГК-содержащих продуктов, имеющихся в продаже в данный момент.
|
В Таблице 7 представлены результаты исследования дозозависимого эффекта гиалуроновой кислоты, в котором сравнивали защиту от обезвоживания композиций с гиалуроновой кислотой индивидуально с композициями, содержащими гиалуроновую кислоту и гидроксипропилгуар.
|
Настоящее изобретение и его варианты реализации подробно описаны. Однако не предполагается, что содержание настоящего изобретения ограничено конкретными вариантами реализации любого процесса, производства, композиции согласно изобретению, соединений, средств, способов и/или этапов, приведенных в настоящем описании. В раскрытых материалах могут быть сделаны различные модификации, замены и вариации, не выходя за рамки сущности и/или существенных характеристик настоящего изобретения. Соответственно, средний специалист в данной области легко поймет из описания, что более поздние модификации, замены и/или вариации, выполняющие по существу ту же самую функцию или достигающие по существу того же результата, что и варианты реализации, описанные в настоящем документе, можно использовать в соответствии с такими родственными вариантами реализации настоящего изобретения. Таким образом, предполагается, что следующая далее формула изобретения охватывает в пределах ее объема модификации, замены и вариации процессов, производств, композиций согласно изобретению, соединений, средств, способов и/или стадий, раскрытых в настоящем документе.