Результат интеллектуальной деятельности: ЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ ГЕМИНА С АНТИМИКРОБНЫМИ СВОЙСТВАМИ И СПОСОБ ЕГО СИНТЕЗА
Вид РИД
Изобретение
Область техники
Изобретение относится к области биоорганической химии и направлено на получение нового производного гемина и создание нового антибактериального средства и композиций на его основе.
Уровень техники
Одной из глобальных проблем современной медицины является повышение резистентности микроорганизмов к используемым в настоящее время антибиотикам. Это явление представляет серьезную угрозу для здоровья населения, так как скорость приобретения микроорганизмами устойчивости приближается к скорости выхода на рынок новых антибиотиков. Так, согласно данным ВОЗ за 2014 год, число смертей от инфекционных заболеваний продолжает расти [Shankar P.R., Balasubramanium R. Antimicrobial Resistance: Global Report on Surveillance // Australasian Medical Journal., 2014, V. 7(5), p. 238-239.]. Рост устойчивости бактерий к антибактериальным препаратам в первую очередь является результатом злоупотребления антибиотиками в клинической практике и их чрезмерного использования. Проблема осложняется появлением полирезистентных бактерий и их способностью распространять эти свойства на другие бактерии посредством горизонтального переноса генов [Al-Bahry Saif N., Mahmoud I.Y., Paulson J.R., Al-Musharafi S.K. Antibiotic resistant bacteria in terrestrial and aquatic environments: A review // The international Arabic journal of antimicrobial agents, 2014, V.4(3), p. 1-11]. Вследствие этого поиск новых эффективных антисептических и терапевтических средств с антимикробными свойствами, а также развитие методов их синтеза является актуальной задачей для биологов и химиков.
Ранее предпринимались попытки модификации молекулы гемина путем его конъюгации с аминокислотами, пептидами и их производными, а также биогенными аминами, с целью создания биологически активных производных. В результате модификации карбоксильных групп гемина путем получения соответствующих амидов были синтезированы и исследованы производные гемина (ПГ) общей формулы (II),
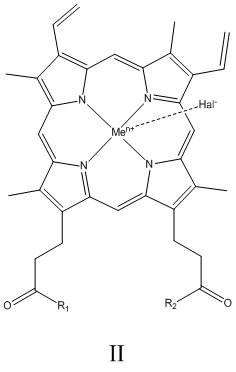
где R1 и R2, одинаковые или различные, представляли собой –ОН, или остаток аминокислоты, или пептида, или биогенного амина, причем R1 и R2 не могут одновременно обозначать -ОН. Men+ представляет собой Fe2+ или Fe3+; Hal‐ представляет собой F‐, Cl‐, Br‐ или I‐ [патент RU№2250906, опубликованный 27.04.2005]. Для этих производных были выявлены разные виды биологической активности, включая антибактериальную (WO 2013/073998 A2), нуклеазную (RU №2404191), пероксидазную, каталитическую (RU№2404191) и вирулицидную (RU №2404191).
В ранее опубликованных работах описаны производные полиамина - спермина, который содержит в своем составе две первичные и вторичные аминогруппы. Из-за присутствия в молекулах полиаминов этих аминогрупп в синтезах обычно используют селективные их защиты [Miller K.A., Suresh Kumar E.V.K., Wood S.J. Lipopolysaccharide Sequestrants: Structural Correlates of Activity and Toxicity in Novel Acylhomospermines // J. Med. Chem., 2005, V.48, p. 2589-2599; Petukhov IA, Maslov MA, Morozova NG Russ., Synthesis of polycationic lipids based on cholesterol and spermine // Chem. Bull. Int.Ed., 2010, V.59 (1), p. 260-268]. Так, известно производное холестерина, модифицированное остатком полиамина, а также другие конъюгаты - конъюгат спермина с холестерином и липоспермидин, но не производные норспермидина, в том числе циклические производные порфиринов и полиаминов неизвестны [Petukhov I.A., Maslov M.A., Morozova NG Russ., Synthesis of polycationic lipids based on cholesterol and spermine // Chem. Bull. Int.Ed., 2010, V.59 (1), p. 260-268; Andrew J. Geall and Ian S. Blagbrough Homologation of Polyamines in the Synthesis of Lipo-Spermine Conjugates and related Lipoplexes // Tetrahedron Letters, V. 39, 1998, p. 443-446].
Сущность изобретения
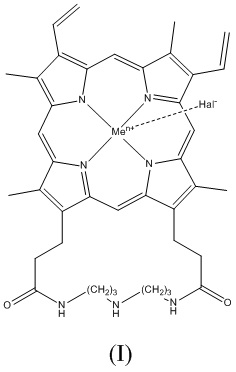
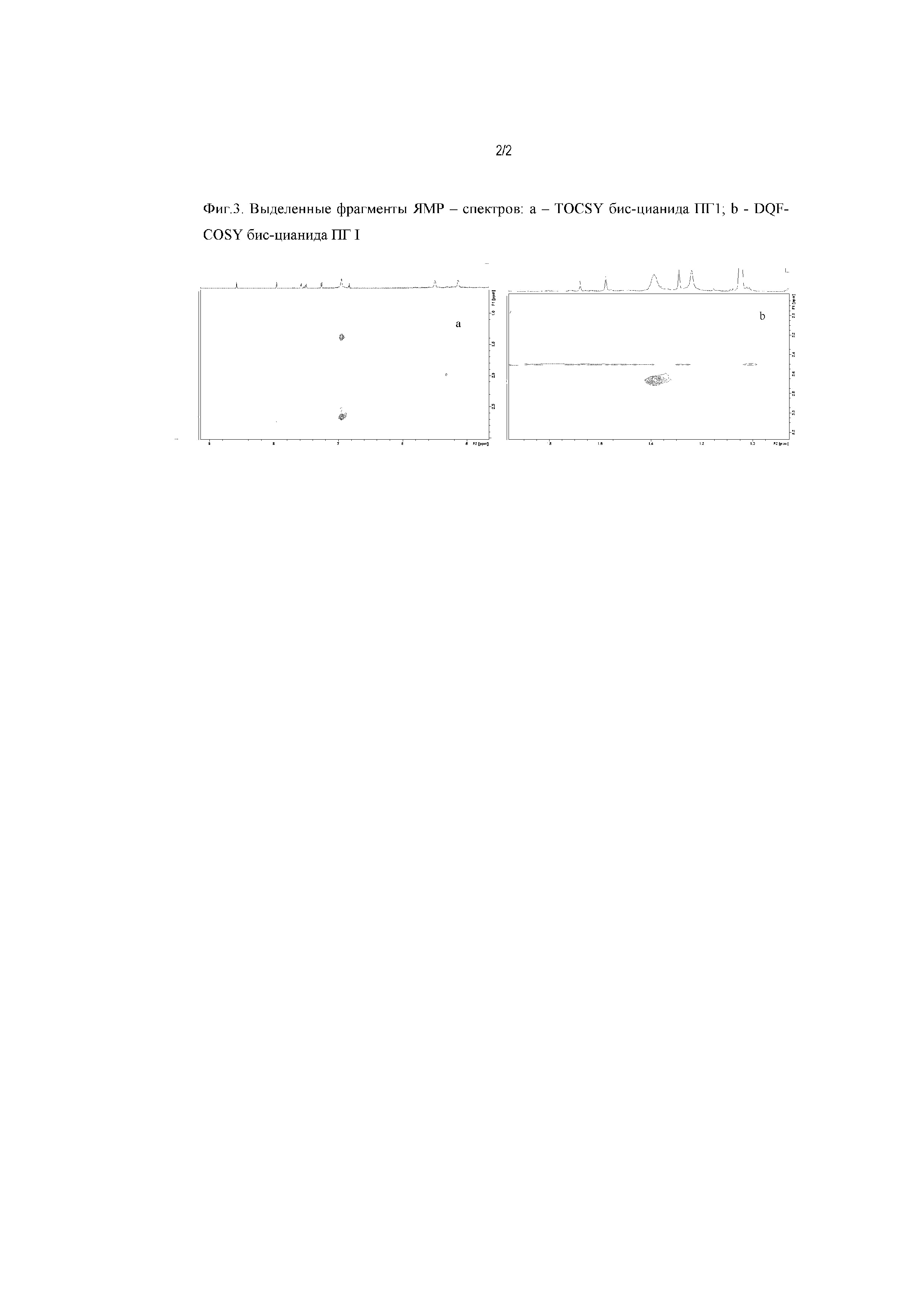
Настоящее изобретение относится к новому циклическому производному гемина, модифицированного остатком полиамина общей формулы (I):
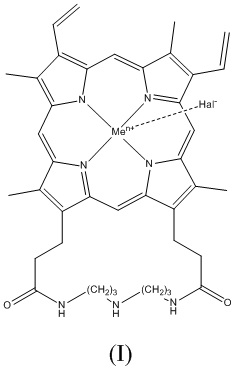 ,
,
где Men+ представляет собой Fe2+ или Fe3+; Hal‐ представляет собой F‐, Cl‐, Br‐ или I‐, или его фармацевтически приемлемым солям.
Кроме того, изобретение относится к способу получения соединения формулы (I) и фармацевтической композиции на основе указанного соединения, а также к антибактериальному и/или антисептическому и дезинфицирующему средству на основе соединения формулы (I). Изобретение также относится к применению соединения формулы (I) и способу лечения бактериальных заболеваний с использованием соединения формулы (I).
Краткое описание чертежей
На Фиг.1 изображен 1Н ЯМР-спектр ПГ (I) (700 MHz, d6-DMSO при 303 К): а - высокоспиновое состояние; b - бис-цианидное низкоспиновое состояние. Факт образования амидных связей карбоксильных групп гемина с первичными аминогруппами норспермидина был подтвержден методом ЯМР. Все ЯМР-эксперименты были проведены в d6-DMSO, концентрация ПГ (I) составляла 2 мг/мл. Низкоспиновое состояние иона железа в молекуле было получено добавлением к пробе KCN до концентрации 100мМ. В 1Н - ЯМР-спектре ПГ (I), находящееся в низкоспиновом состоянии (Фиг.1, b), наблюдались сигналы в области от -4 до 0, 6-15 ppm, относящиеся к отдельным группам гемового остава, а также норспермидиновому заместителю. В 1Н - ЯМР-спектре высокоспинового состояния ПГ (I) (фиг 1, а) вышеупомянутые сигналы отсутствуют.
На Фиг.2 изображен Двумерный ЯМР-спектр 1H/15N - HSQC бис-цианидного производного ПГ (I). В двумерном спектре 1H/15N - HSQC наблюдался лишь один сигнал, соответствующий NH - группе норспермидина, находящейся рядом с карбоксильной CO - группой.
На Фиг.3 изображены выделенные фрагменты ЯМР-спектров: а - TOCSY бис-цианида ПГ1; b - DQF-COSY бис-цианида ПГ I. В двумерном спектре TOCSY ПГ (I) наблюдаются кросс-пики с сигнала 6.95 pmm, соответствующего протону при атоме азота, на протоны с химическим сдвигом 1.38 и 2.66 ppm (фиг. 3, a). В двумерном спектре DQF - COSY наблюдаются кросс-пики с сигнала при 6.95 - на сигнал 2.66 ppm (фиг.к 3, b). Это означает, что протоны с химическим сдвигом 2.66 ppm находятся на соседних с атомом азота С-атомах, а протон с химическим сдвигом 1.38 находится на соседнем с ним С-атоме. Это подтверждается наличием кросс-пиков с химическим сдвигом 2.66 и 1.38 ppm друг на друга в спектре DQF-COSY (фиг.3, b). Таким образом можно заключить, что сигнал с химическим сдвигом 2.66 относится к протонам при атомах углерода 4 и/или 2, а 1.38 - к протонам при атоме углерода 3 норспермидина (III)
Подробное описание изобретения
Авторы настоящего изобретения синтезировали новое оригинальное циклическое норспермидиновое производное гемина (ПГ), соответствующее формуле (I):
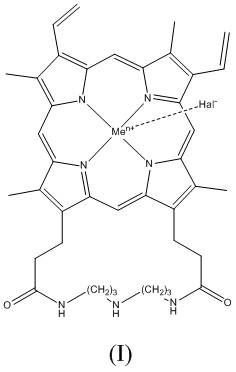 ,
,
где Men+ представляет собой Fe2+ или Fe3+; Hal- представляет собой F-, Cl-, Br- или I-, или его фармацевтически приемлемым солям.
Синтез соединения (I) осуществлялся новым способом - без использования селективных защитных групп по амино- и иминофункциям норспермидина. Норспермидин - биогенный амин, который образуется в результате жизнедеятельности бактерий и участвует в процессе спонтанного разрушения биопленок [Kolodkin-Gal I., Cao S., Chai L., Böttcher T., Kolter R., Clardy J., Losick R. A self-produced trigger for biofilm disassembly that targets exopolysaccharide// Cell, 2012, 149, p 684-692] и соответствует формуле:
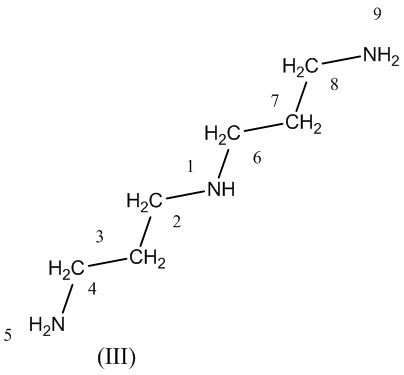
В отличие от ранее описанных соединений ПГ соединение формулы (I) обладает неизменной одинаковой активностью против целого ряда бактерий, резистентных к современным антибиотикам. При этом токсичность данного соединения отсутствовала вплоть до концентрации 256 мкг/мл, которая превышает минимальные подавляющие и бактерицидные концентрации (МПК, МБК) против ряда резистентных бактерий в 4-8 раз.
Соединение формулы (I) может быть использовано в виде солей с фармацевтически приемлемыми кислотами, например молочной, винной, лимонной, хлористоводородной и др. Соли ПГ (I) по вторичной аминогруппе получают путем добавления раствора фармацевтически приемлемой кислоты в воде, органическом растворителе или их смеси к ПГ с последующим удалением в вакууме.
Заявляемое, представленное выше, соединение формулы (I), проявляет активность против резистентных бактерий, в частности таких как грамположительные бактерии рода Staphylococcus, Enterococcus, более конкретно, бактерий Enterococcus faecalis, St. aureus, St. aureus, St. haemolyticus, St. haemolyticus, а также чувствительного штамма St. aureus.
Указанное выше соединение и/или его фармацевтически приемлемая соль могут быть использованы в качестве активного ингредиента в фармацевтической композиции (например, в твердой, полутвердой или жидкой форме) в смеси с органическим или неорганическим носителем или наполнителем. Активный ингредиент может быть включен в композицию вместе с обычно используемыми нетоксичными, фармацевтически приемлемыми носителями, пригодными для изготовления растворов, таблеток, пилюль, капсул, суппозиториев, эмульсий, суспензий, спреев, капель, мазей и любых других лекарственных форм. В качестве носителей могут быть использованы вода, глюкоза, лактоза, аравийская камедь, желатин, крахмал, триксилит магния, тальк, кукурузный крахмал, мочевина, полиэтиленгликоль и другие носители, пригодные для изготовления твердых, мягких или жидких препаратов. При этом в качестве добавок могут быть использованы стабилизаторы, загустители, красители и отдушки. Соединение вводят в композицию в эффективном количестве, достаточном для получения антибактериального действия. При изготовлении разовой лекарственной формы количество активного ингредиента, используемого в комбинации с носителем, может варьировать в зависимости от реципиента, подвергающегося лечению, от конкретного способа введения лекарственного средства.
Так, например, при использовании соединения настоящего изобретения в виде раствора для инъекций, содержание действующего начала в нем составляет 0,001-1 мас.%. В качестве разбавителя вещества могут быть использованы 0,9% раствор натрия хлорида, дистиллированная вода, раствор новокаина для инъекций, раствор Рингера, раствор глюкозы, в том числе возможно с добавками, такими как 2- гидроксипропил-β-циклодекстрин и плюроники, например, F-127.
При использовании соединения формулы (I) в виде таблеток и суппозиториев количество вещества составляет 1,0-100,0 мг на единичную дозированную форму. Для таблеток и суппозиториев в качестве фармацевтического наполнителя используют любую фармацевтически пригодную основу.
Далее, изобретение относится к антимикробному, в том числе антибактериальному, средству на основе указанного выше соединения формулы (I), и соответствующим фармацевтическим, антисептическим и/или дезинфицирующим композициям.
Изобретение также относится к способу лечения заболеваний, вызываемых указанными выше бактериями, включающему введение нуждающемуся в этом пациенту указанного выше соединения формулы (I) или фармацевтической композиции на его основе.
Способ лечения предназначен для пациентов-млекопитающих, в том числе людей. Рекомендуемые дозы соединения формулы (I) составляют 0,01-10 мг/кг. Поскольку соединение формулы (I) обладает антибактериальной активностью, оно может также использоваться в качестве или в составе антисептического и/или дезинфицирующего средств. Такие средства могут быть изготовлены, например, в виде растворов с использованием различных растворителей, таких как вода и низшие спирты (например, 1-пропанол или 2-пропанол), в том числе с добавками, такими как 2- гидроксипропил-β-циклодекстрин и плюроники, например, F-127.
Еще один аспект изобретения относится к способу получения описанного выше нового соединения формулы (I).
Соединение формулы (I) получают путем взаимодействия, активированного по карбоксильным группам производного гемина с незащищенным по амино- и иминогруппам полиамином-норспермидином. Ранее в синтезах с использованием полиаминов их селективно защищали по амино- и иминофункциям трифторацетильными и бензилоксикарбонильними группами, которые в конце синтеза удаляли [Miller K.A., Suresh Kumar E.V.K., Wood S.J. Lipopolysaccharide sequestrants: structural correlates of activity and toxicity in novel acylhomospermines//J. Med. Chem., 2005, 48, p 2589-2599. Petukhov IA, Maslov M.A., Morozova N.G. Synthesis of polycationic lipids based on cholesterol and spermine // Russ. Chem. Bull. Int. Ed., 2010, 59, p 260-268]. Таким образом, известный способ существенно более длителен и трудоемок. В соответствии с предлагаемым способом для предотвращения образования побочных продуктов аминокомпонент добавляли к разбавленному раствору активированного эфира порционно, что неожиданно привело к одностадийному получению ПГ, соответствующему структуре (I). Структура полученного продукта подтверждена физико-химическими методами, в том числе ЯМР, а индивидуальность - методом ВЭЖХ.
Еще в одном аспекте изобретение относится к применению вышеуказанных соединений формулы (I) или фармацевтических композиций, их содержащих, для лечения заболеваний, вызываемых бактериями.
Еще в одном аспекте изобретение относится к применению вышеуказанных соединений формулы (I) или фармацевтических композиций, их содержащих, для получения лекарственного средства для лечения заболеваний, вызываемых бактериями.
Производное гемина, предложенное в настоящем изобретении, обладает практически одинаковой антибактериальной активностью в отношении резистентных к современным антибиотикам штаммов, при отсутствии токсичности вплоть до концентрации 250 мкг/мл.
Таким образом, предлагается новое эффективное антибактериальное средство на основе природных соединений - гемина и норспермидина. Преимуществом заявляемого действующего вещества (I) является биосовместимость, биодеградируемость, практически одинаковая активность в отношении целого ряда резистентных к современным антибиотикам штаммов бактерий, отсутствие токсичности вплоть до 256 мкг/мл, а также простой одностадийный способ получения.
Изобретение далее иллюстрируется с помощью примеров, которые не предназначены для ограничения его объема.
Список сокращений
Hem - остаток гемина
ИК - инфракрасная спектроскопия
МПК - минимальная подавляющая концентрация
МБК - минимальная бактерицидная концентрация
ВЭЖХ -высокоэффективная жидкостная хроматография
ТСХ - тонкослойная хроматография
DMFA - N,N'-диметилформамид
DMSO - диметилсульфоксид
MeOH - метиловый спирт
Все величины, выраженные в процентах, относятся к процентам по массе, если не указано иначе.
Примеры
В работе использовали бис-(3-аминопропил)-амин (норспермидин) -фирмы «Aldrich» (Германия). DCC, Hemin (≥90%) («Sigma Aldrich», США), HONSu («Fluka», Швейцария). Все растворители безводные. Протекание реакций и индивидуальность полученного соединения проверяли методом ТСХ на пластинах Kieselgel 60 F254 (Merck, Германия) в системе растворителей: хлороформ - метанол - уксусная кислота - вода (5:4:1:1) (1) и хлороформ - метанол (9:1) (2).
Аналитическую ВЭЖХ осуществляли в условиях (3) на хроматографе Knauer pump 64 (Knauer, Германия), колонка (4.6×150 мм), обращенная фаза Luna С18 (2), 100 А, средний размер частиц сорбента 5 микрон, в градиенте ацетонитрила от 5 до 100% в 0.1% водном растворе TFA, скорость потока 1 мл/мин, детекция при 400 нм.
Колоночную хроматографию соединений проводили на силикагеле Kieselgel 60 F254 (Merck, Германия), сефадексе LH-20 (Pharmacia, Швеция).
Масс-спектры высокого разрешения получали на время-пролетном масс-спектрометре «Ultraflex» (Bruker, Германия) методом матриксной лазерно-десорбционной ионизации (TOF MALDI), в качестве матрицы использовалась 2,5-дигидроксибензойная кислота.
Электронные спектры регистрировали на спектрофотометре Helios Alpha (Thermo Electron, США). ИК-спектры регистрировали на Фурье-спектрометре EQUINOX-55 фирмы Bruker (Германия).
Все ЯМР-спектры были сняты в d6-DMSO, концентрация (ПГ 1) составляла 2 мг/мл. ЯМР-спектры были сняты на спектрометре Bruker Avance 700 MHz, снабженном импульсным градиентным датчиком тройного резонанса (H/C/N) (Brucer, Германия). Низкоспиновое состояние иона железа в молекуле получено добавлением к пробе KCN до концентрации 100 мМ. Спектроскопию ЯМР осуществляли при 3030К.
Пример 1
6,7-цикло- [бис-(3'-амидопропил) амин] протогемин (IX) (ПГ I)
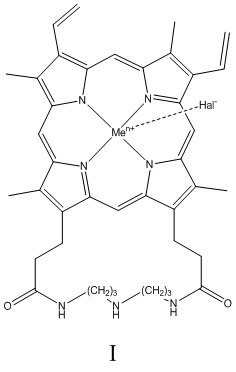
К 200 мг (0.24 ммоль) Hem(ONSu)2 в 20 мл DMFA прибавляли постепенно по 300 мкл через каждые 10 мин раствора 34 мкл (0.24 ммоль) норспермидина в 3 мл DMFA при интенсивном перемешивании при комнатной температуре. Оставляли реакционную смесь на 16 часов. Ход реакции контролировали ТСХ в условиях (1,2). Растворитель удаляли в вакууме. Вещество растворяли в 4 мл MeOH и подкисляли 400 мкл (0.48 ммоль) HCl в MeOH. При этом наблюдалось изменение цвета раствора на бордовый. Растворитель удаляли в вакууме, остаток очищали колоночной хроматографией на силикагеле (2.2×40.0 см). Элюировали 150 мл смеси хлороформ:метанол:уксусная кислота:вода 5:4:1:1. Растворитель из фракции, содержащей целевое вещество, удаляли в вакууме. Дополнительную очистку вещества проводили гель-хроматографией на колонке с LH-20, элюируя метанолом. Продукт анализировали методом ВЭЖХ в условиях (3). Время выхода индивидуального продукта при ВЭЖХ 32.1 мин. Вещество растворимо в воде, метаноле при концентрации 10-3М. Выход целевого вещества 35мг (21%). Rf 0.68 (1). Масс-спектр, (MALDI): m/z [M-Cl-]+ 711.017 (Вычислено 711.680). ИК-Фурье спектр, ν, см-1, таблетка KBr: 1647 (амид I), 1568 (амид II). Электронный спектр, DMSO, λmax, нм, (ε×10-3): 400 (74.0), 503 (2.79), 603 (1.56).
В 1Н - ЯМР-спектре наблюдались следующие сигналы (химический сдвиг, число протонов, элемент структуры): 6.95, 2H, при N5 и N9 норспермидина; 5.19, 2Н, 5.58, 2Н, CH2 группы пропионовокислого остатка гемина, находящиеся вблизи порфиринового кольца; 2.68, 8Н, CH2 групп 4, 2, 6, 8 норспермидина; 1.38, 4H, CH2 групп 3, 7 групп норспермидина; 2.59, 2Н, dd, винил Hβ; 2.31, 2Н, dd, винил Hβ. Сигналы протонов при парах атомов углерода 4 и 2, 6 и 8 норспермидина имеют одинаковый 1Н химический сдвиг (2.68 ppm), и ему по количеству соответствуют 8 протонов.
Таким образом, по совокупности данных ЯМР-спектроскопии, в ПГ 1 остаток норспермидина ковалентно присоединен к пропионовокислым остаткам гемина посредством двух первичных аминогрупп.
Пример 2
Определение минимальной подавляющей концентрации и минимальной бактерицидной концентрации (МПК, МБК) ПГ для различных резистентных штаммов бактерий
Исследованные резистентные бактериальные штаммы
Грамположительные:
Enterococcus faecalis 560,
Staphylococcus aureus 700699,
Staphylococcus aureus 3798,
Staphylococcus haemolyticus 585,
Staphylococcus haemolyticus 1025,
Staphylococcus aureus 10,
Бактериальный инокулюм был постоянным и составлял 5×105 КОЕ/мл.
Штаммы были предоставлены коллекцией Научно-исследовательского института по изысканию новых антибиотиков им. Г. Ф. Гаузе РАМН.
Определение минимальной подавляющей концентрации (МПК) проводили по методике, описанной в публикации [Okorochenkov S.A., Zheltukhina G.A., Mirchink EP Synthesis, anti-mrsa, and anti-vre activity of hemin conjugates with amino acids and branched peptides//Chem. Bio.l Drug. Des., 2013, 82, p. 410-417; National Committee for Clinical Laboratory Standards. (2000) Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria That Grow Aerobically, 5th edn. 17 (2). Approve Standard M7-A5. Wayne, PA: NCCLS].
Стоковый раствор соединения (I) готовили в воде.
За МПК - минимальную подавляющую концентрацию принимали последнее разведение испытуемых препаратов с подавлением роста бактериальной культуры. Минимальную бактерицидную концентрацию (МБК) определяли путем нанесения бульонной культуры из лунок, предшествующих МПК, в которых четко фиксируется ингибирование роста бактерий, на чашки со средой, не содержащей антибиотика. Инкубацию проводили в термостате при 36°C в течение 24 ч. Затем отмечали наименьшую концентрацию вещества в лунке, высев из которой не дал роста. Эту концентрацию принимали за минимальную бактерицидную - МБК.
Полученные результаты представлены в Таблице 1
Таблица 1. Определение антибактериальной активности (МПК, МБК) соединения (I)
|
Новое соединение показало практически одинаковую активность в отношении всех исследованных резистентных к современным антибиотикам штаммов. МПК, как правило, не превышала 32 мкг/мл, а МБК - 64 мкг/мл.
Пример 3
Токсичность нового производного гемина (I)
Для исследования использовали свежую кровь здоровых доноров. Концентрацию лейкоцитов и эритроцитов определяли в камере Горяева. Мертвые и живые клетки после инкубации с ПГ (I) определяли флуоресцентной спектроскопией с применением пропидий - иодида и Hoechst 33342, анализ проводился с использованием микроскопа [Okorochenkov SA, Zheltukhina GA, Mirchink EP Synthesis, anti-mrsa, and anti-vre activity of hemin conjugates with amino acids and branched peptides//Chem. Bio.l Drug. Des., 2013, 82, p. 410-417]. Соединение (I) практически не токсично; гибель лейкоцитов человека не превышала 3% процентов вплоть до 250 мкг/мл. Данное производное гемина (I) не вызывает выхода гемоглобина из эритроцитов крови человека вплоть до 250 мкг/мл.
Пример 4
Примеры лекарственных форм
А. Желатиновые капсулы
Состав вводимого в капсулу порошка:
Соединение, соответствующее общей формуле (I) 1-80 мг
Оксид магния 50 мг
Крахмал 100-200 мг
Указанные выше ингредиенты смешивают и смесь вводят в твердые желатиновые
капсулы в количестве 151-300 мг.
Б. Таблетированная форма
Таблетированную форму получают, используя приведенные ниже ингредиенты:
Соединение, соответствующее общей формуле (I) 1-80 мг
Крахмал картофельный 100 мг
Поливинилпирролидон 10 мг
Магния стеарат 2 мг
Лактоза 48-82 мг
Аэросил 5 мг
Компоненты смешивают и прессуют для образования таблеток массой 170-250 мг каждая.
В. Раствор для инъекций
В качестве растворителя при приготовлении раствора для инъекций могут быть
использованы: 0,9% раствор натрия хлорида, дистиллированную воду, раствор
новокаина, в том числе возможно с добавками 2- гидроксипропил-β-циклодекстрина и плюроников, например, F-127.
Форма выпуска - ампулы, флаконы, шприц-тюбики,
Состав раствора для инъекций:
Соединение, соответствующее общей формуле (I) 0,1-20 мг
Вода дистиллированная 1-2 мл, в том числе возможно с добавками 2- гидроксипропил-β-циклодекстрина и плюроников, например, F-127.
Возможно изготовление различных лекарственных форм для инъекций - стерильных
растворов, стерильных порошков и таблеток.
Примеры композиций для дезинфицирующих и антисептических средств
Г. Соединение, соответствующее общей формуле I 0,001-1%
1-пропанол 30-40%
2-пропанол 10-70%
вода дистиллированная 10-60%
Д. Соединения, соответствующие общей формуле I 0,001-1%
Четвертичное аммониевое основание (или их смесь) 2-10%
Вода дистиллированная до 100%
Е. Соединения, соответствующие общей формуле I 0,001-1%
Диметилсульфоксид (DMSO) 1-20%
или полиэтиленгликоль (PEG) М.М. 200-12000 1-20%
вода дистиллированная до 100%
Ж. Соединения, соответствующие общей формуле I 0,001-1%
Смесь спиртов, DMSO, PEG, ПАВ, 2- гидроксипропил-β-циклодекстрин, плюроники, например, F-127.
в различных сочетаниях и соотношениях 1-80%
вода дистиллированная до 100%
З. Соединения, соответствующие общей формуле 0,001-1%
вода дистиллированная до 100%
Таким образом, производное гемина общей формулы (I) обладает антибактериальной активностью, в том числе в отношении патогенного для человека S. Aureus и его резистентных штаммов. Преимуществами заявленного соединения (I) являются природное происхождение входящих в его состав компонентов, простой и экономичный способ получения, практически одинаковая активность против ряда бактерий, резистентных к современным антибиотикам, и практически полное отсутствие токсичности к клеткам крови человека.
Эффективность соединения, соответствующего общей формуле I, подтверждает его пригодность для промышленного применения в составе дезинфицирующих, антисептических и терапевтических средств с антибактериальным и антисептическим действием.