Результат интеллектуальной деятельности: Способ получения 2-[(оксифенил)метил]бутан-1,4-диолов
Вид РИД
Изобретение
Изобретение относится к способу получения β-замещенных 1,4-бутандиолов, конкретно к способу получения 2-[(оксифенил)метил]бутан-1,4-диолов общей формулы (1a-d):
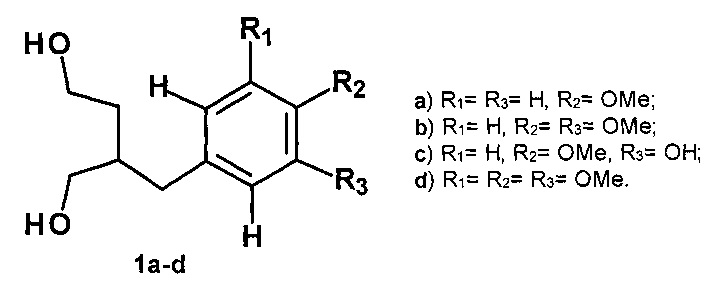
Разработанный способ открывает новый путь к получению практически важных 2-бензилзамещенных 1,4-бутандиолов, используемых при синтезе γ-бутиролактонов, лигнанов ([1] Dhal R., Landais Y., Lebrun A., Robin J.-P., Tetrahedron, 1994, V. 50, №4, P. 1153-1164; [2] Ward R.S. Recent advances in the chemistry of lignans. В книге: Studies in Natural Products Chemistry (Ed. by Atta-ur-Rahman), 2000, V. 24, Part E, P.739-798; [3] Ito ML, Shiibashi A., Ikariya Т., Chem. Commun., 2011, V. 47, P. 2134-2136), а также 3-(арилметил)-пирролидинов ([4] патент ЕР 562185 A1).
Известен способ ([5] Shao L., Miyata Sh., Muramatsu H., Kawano H., Ishii Y., Saburi M, Uchida Y., J. Chem. Soc. Perkin Trans. 1990. - V. 1. - P. 1441-1445) получения 2-[(оксифенил)метил]бутан-1,4-диолов с выходом 80-85% путем восстановления бензилзамещенных янтарных кислот с помощью LiAlH4 в ТГФ при кипячении в атмосфере азота в течение 1 ч по схеме:
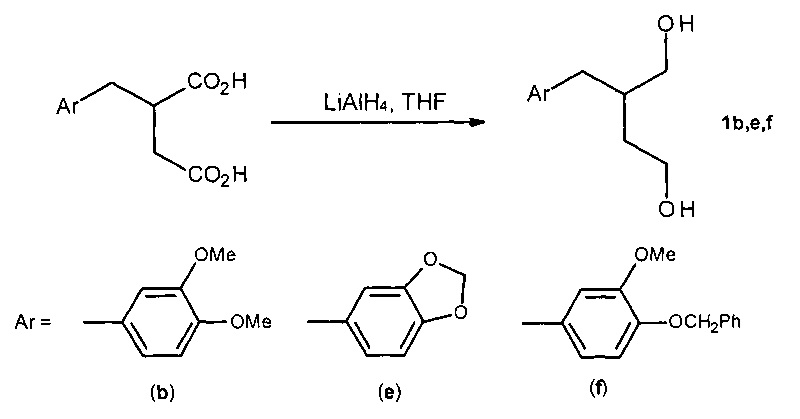
К недостаткам метода следует отнести использование в качестве исходных соединений труднодоступных бензилзамещенных янтарных кислот.
Известен способ ([6] Ito М., Ootsuka Т., Watari R., Shiibashi A., Himizu A., Ikariya Т., J. Am. Chem. Soc, 2011, V. 133, P. 4240-4242, патенты WO 2010/004883 A1, EP 2298723 A1) получения 2-фенил-1,4-бутандиола в реакции гидрирования 3-фенилтетрагидрофуран-2-она с помощью молекулярного водорода при давлении 5 МПа в присутствии KOtBU и катализатора Cp*RuCl(N-*C2-N) в изопропиловом спирте при температуре 100°C в течение 12-15 ч:
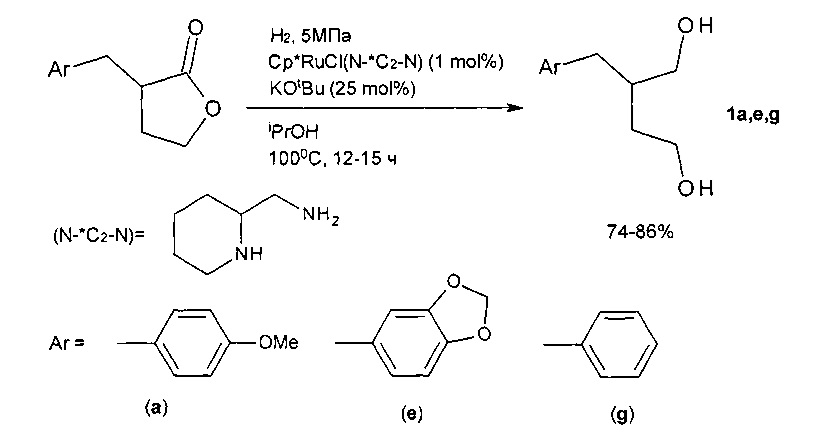
В качестве недостатков следует отметить необходимость проведения реакции при высоком давлении и температуре, а также использование дорогостоящего рутениевого катализатора и труднодоступных бензилзамещенных γ-бутиролактонов.
Известен способ ([7] Kamlage S., Sefkow М., Zimmermann N., Peter M.G., Synlett, 2002, No. 1, P. 77-80) синтеза 2-[(оксифенил)метил]бутан-1,4-диолов 1d,e,g-k путем восстановления 2-бензил-1,4-бутендиолов с помощью Н2 при давлении 100 бар с конверсией субстрата 100% в присутствии 3-5 мол. % Ir(I)-фосфиноксазолиновых катализаторов в течение 2 ч по схеме:
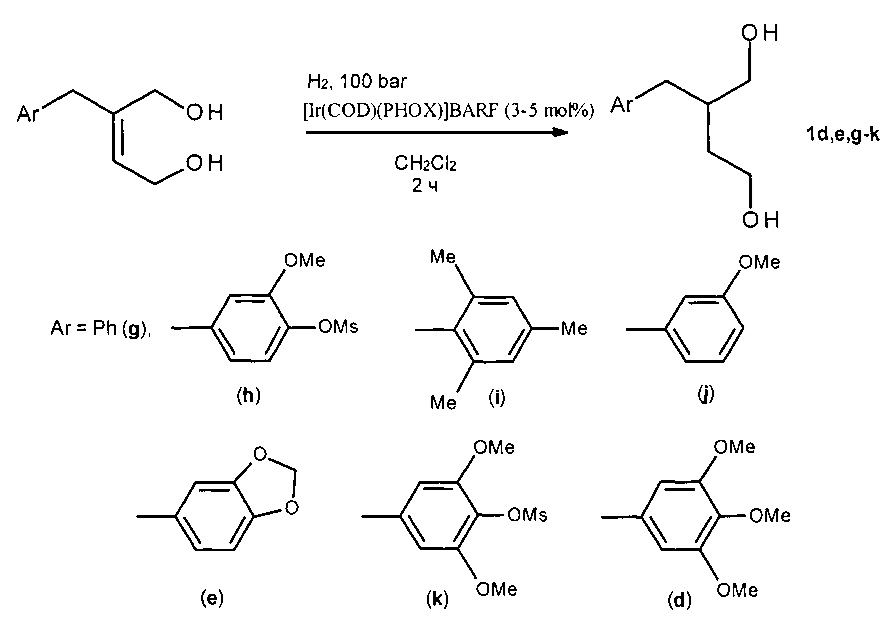
К недостаткам метода следует отнести использование труднодоступных 2-бензилбут-2-ен-1,4-диолов в качестве исходных соединений, применение дорогостоящего катализатора на основе иридия и проведение реакции при высоком давлении.
Наиболее близким к изобретению является способ ([8] Джемилев У.М., Ибрагимов А.Г., Золотарев А.П., Муслухов P.P., Толстиков Г.А., Изв. АН СССР, Сер. хим. - 1990. - №10. - С. 2831-2841) получения 2-бензил-1,4- диола (1g) в реакции AlEt3 с аллилбензолом в присутствии катализатора Cp2ZrCl2, взятых в мольном соотношении алкен: AlEt3:Cp2ZrCl2=100:120:2, за 10 ч при комнатной температуре с последующим окислением реакционной массы сухим воздухом и гидролизом водным раствором NaOH:
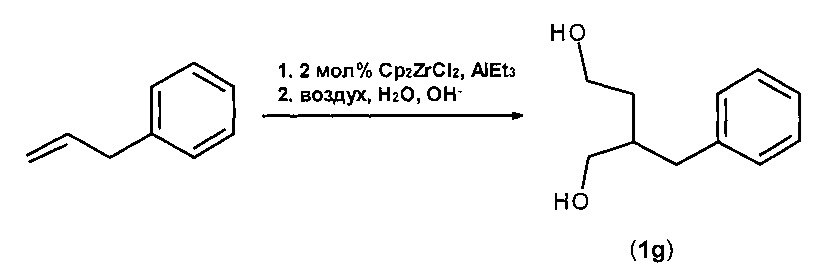
Известный способ не позволяет получать 2-[(оксифенил)метил]бутан-1,4-диолы (1a-d) с достаточным выходом.
Таким образом, в литературе отсутствуют сведения по однореакторному синтезу 2-[(оксифенил)метил]бутан-1,4-диолов (1a-d) из замещенных аллилбензолов, а имеющийся метод приводит к низкому выходу целевых продуктов.
Задачей изобретения является разработка однореакторного способа получения 2-[(оксифенил)метил]бутан-1,4-диолов (1a-d) в реакции замещенных аллилбензолов с триэтилалюминием (AlEt3) в присутствии катализатора Cp2ZrCl2 с последующим окислением реакционной массы сухим O2 и гидролизом с помощью HCl.
Сущность способа заключается во взаимодействии замещенных аллилбензолов (аллиланизола, 4-аллил-1,2-диметоксибензола, 4-аллил-2-метоксифенола (евгенола), 5-аллил-1,2,3-триметоксибензола) с триэтилалюминием (AlEt3) в присутствии катализатора Cp2ZrCl2, взятых в мольном соотношении алкен:AlEt3:[Zr]=50:(150-180):(1-2) в атмосфере аргона при комнатной температуре (~22°C) и атмосферном давлении в толуоле в течение 16 ч с последующим окислением сухим O2 и гидролизом с помощью 10% раствора HCl. Выход целевого продукта (la-d) составляет 60-65%. Реакция проходит по схеме:
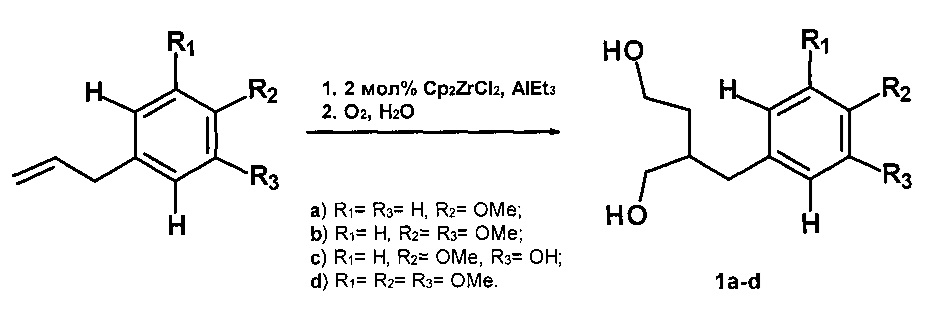
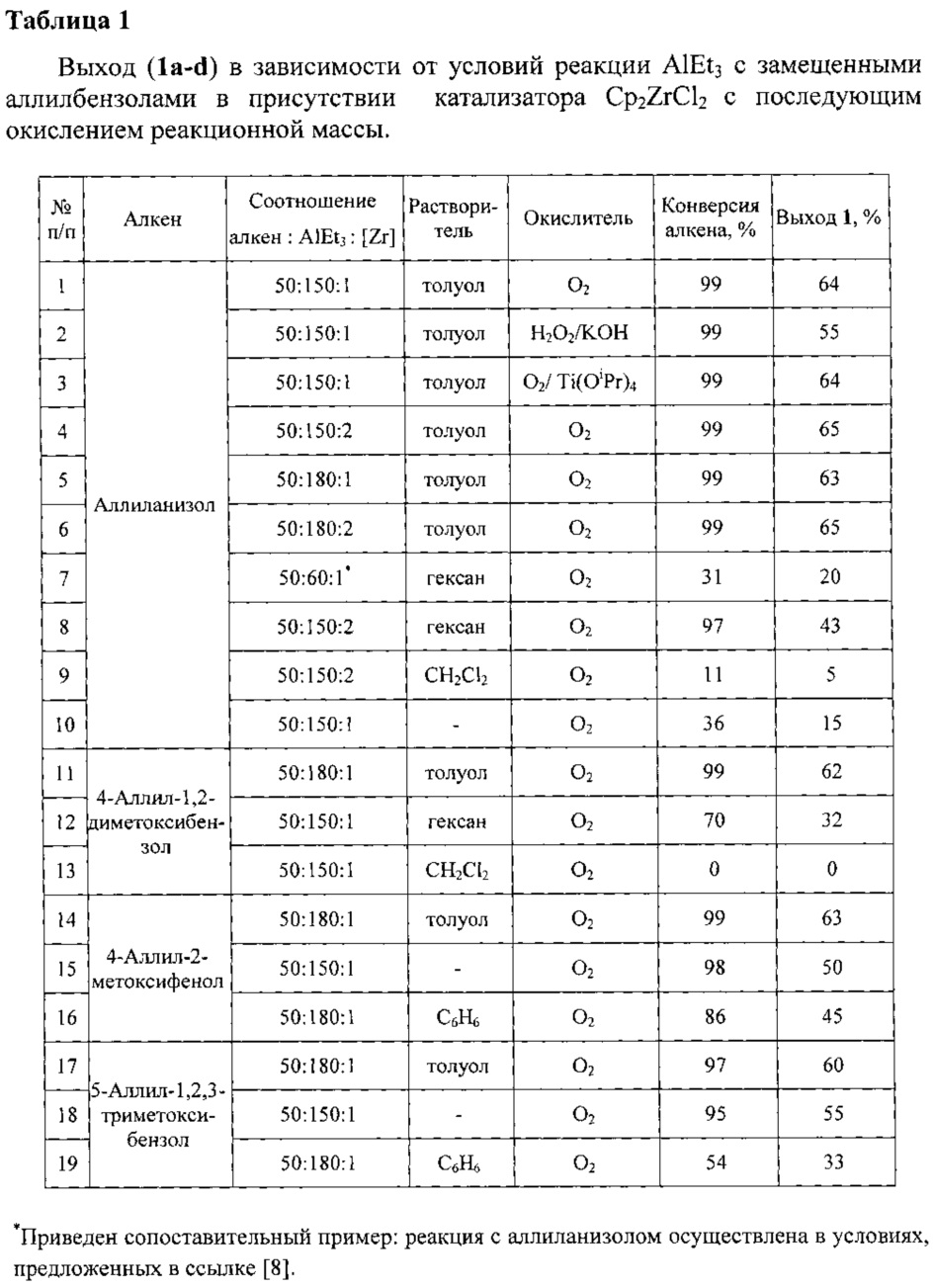
2-Бензил-1,4-бутандиолы (1a-d) образуются в результате двухстадийного синтеза без выделения промежуточных продуктов. На первой стадии используются кислородсодержащие аллилбензолы, AlEt3 и Cp2ZrCl2 в качестве катализатора. На второй стадии применяется газообразный кислород. В присутствии других алюминийорганических соединений (например, AlMe3, AlBui3, Et2AlCl) целевые продукты (la-d) не образуются. Использование других комплексов переходных металлов в качестве катализаторов, например ZrCl4, Zr(acac)4, Cp2TiCl2, Pd(acac)2, Ni(acac)2, не приводит к образованию 2-бензил-1,4-бутандиолов (1a-d). Применение других окислителей, например H2O2 в КОН, приводит к снижению выхода (1a-d) (Таблица 1). Повышение температуры реакции окисления до 40°C или добавление каталитических количеств Ti(OiPr)4 в ходе окисления не приводит к существенному увеличению выхода (1a-d).
Реакцию проводили при перемешивании на магнитной мешалке, при температуре ~22°C. При температуре выше 40°C возрастает скорость протекания побочных реакций. Понижение температуры снижает выход (1а-d), а также увеличивает время реакции.
Проведение реакции в присутствии катализатора Cp2ZrCl2 больше 4 мол. % по отношению к олефину не приводит к существенному увеличению выхода целевого продукта (1a-d). Уменьшение концентрации катализатора менее 2 мол. % вызывает снижение скорости реакции и выхода спиртов (1а-d).
Изменение соотношения исходных реагентов в сторону уменьшения исходной концентрации AlEt3 приводит к снижению скорости реакции и выхода целевого продукта (1a-d). Увеличение исходной концентрации AlEt3 не приводит к значительному увеличению выхода (1a-d).
Существенные отличия предлагаемого способа:
1. Предлагаемый способ основывается на использовании в качестве исходных реагентов замещенных аллилбензолов (аллиланизола, 4-аллил-1,2-диметоксибензола, 4-аллил-2-метоксифенола (евгенола), 5-аллил-1,2,3-триметоксибензола). Реакция проходит в толуоле. В известном способе используется незамещенный аллилбензол. Реакция походит без растворителя.
2. В предлагаемом способе применяется сухой O2, а гидролиз проходит с использованием 10% раствора HCl. В известном способе на стадии окисления используется сухой воздух, а реакционная масса гидролизуется с помощью водного раствора NaOH.
3. В предлагаемом способе используется мольное соотношение исходных реагентов алкен:AlEt3:[Zr]=50:(150-180):(1-2), тогда как в известных способах соотношение алкен:AlEt3:[Zr] составляет 100:120:2.
Предлагаемый способ обладает следующими преимуществами:
1. Способ обеспечивает получение целевых продуктов - 2-[(оксифенил)метил]бутан-1,4-диолов с выходом 60-65%).
Способ поясняется следующим примером:
Общая методика. В стеклянный реактор объемом 10 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 0.06-0.12 ммоль катализатора Cp2ZrCl2, 3 ммоль замещенного аллилбензола и 9-10.8 ммоль AlEt3 (25% раствор в толуоле). Реакцию проводят при температуре 20-22°C при непрерывном перемешивании в течение 16 часов. Колбу охлаждают до 0°C и барботируют сухой O2 в течение 2 ч. Реакционную массу затем перемешивают в атмосфере кислорода еще в течение 24 ч. Полученную смесь гидролизуют 10%-ым раствором HCl. Продукт экстрагируют диэтиловым эфиром. Органический слой сушат над Na2SO4. Полученные спирты выделяют при помощи колоночной хроматографии на силикагеле. Выход 1a-d составляет 60-65%.
Пример 1. В стеклянный реактор объемом 10 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 35 мг (0.12 ммоль) катализатора Cp2ZrCl2, 0.46 мл аллиланизола и 5.8 мл AlEt3 (25% раствор в толуоле). Реакцию проводят при температуре 20-22°C при непрерывном перемешивании в течение 16 часов. Колбу охлаждают до 0°C и барботируют сухой O2 в течение 2 ч. Реакционную массу затем перемешивают в атмосфере кислорода еще в течение 24 ч. Полученную смесь гидролизуют 10%-ым раствором HCl. Продукт экстрагируют диэтиловым эфиром. Органический слой сушат над Na2S04. Продукт выделяют при помощи колоночной хроматографии на силикагеле. Получают спирт 1а с выходом 65% (Табл. 1, №4).
Примеры 2, 3 и 4 для 4-аллил-1,2-диметоксибензола, 4-аллил-2-метоксифенола и 5-аллил-1,2,3-триметоксибензола выполнены аналогично примеру 1. Результаты приведены в таблице 1: №№11, 14 и 17.
Спектральные характеристики 1a-d.
2-[(4-Метоксифенил)метил]бутан-1,4-диол (1а). ЯМР 1H (400.13 МГц, CDCl3) δН 1.49-1.61 (м, CHCHHO, 1Н), 1.61-1.72 (м, CHCHHO, 1H), 1.84-1.97 (м, CH, 1Н), 2.47 (дд, 2J=13.6 Гц, 3J=Гц, CHHPh, 1Н), 2.59 (дд, 2J=13.6 Гц, 3J=Гц, CHHPh, 1Н), 3.42 (дд, 2J=10.8 Гц, 3J=7.2 Гц, OCHHCH, 1Н), 3.52-3.64 (м, OCHHCHCH2CHHO, 2Н), 3.65-3.75 (м, CH2CHHO, 1Н), 3.78 (с, ОСН3, 3Н), 6.82 (д, 3J=8.4 Гц, Ph, 2Н), 7.08 (д, 3J=8.4 Гц, Ph, 2Н). ЯМР 13С (100.62 МГц, CDCl3) δС 35.2 (С3), 37.2 (С5), 41.4 (С2), 55.2 (ОСН3), 60.8 (С4), 65.4 (С1), 113.8, 130.0, 132.4, 157.8 (Ph).
2-[(3,4-Диметоксифенил)метил]бутан-1,4-диол (1b). ЯМР 1Н (400.13 МГц, CDCl3) δН 1.52-1.64 (м, CHCHH, 1Н), 1.66-1.76 (м, CHCHH, 1Н), 1.90-2.00 (м, CH, 1Н), 2.49 (дд, 2J=14.0 Гц, 3J=7.60 Гц, CHHPh, 1Н), 2.61 (дд, 2J=14.0 Гц, 3J=6.4 Гц, CHHPh, 1H), 3.47 (дд, 2J=10.8 Гц, 3J=6.8 Гц, OCHHCH, 1Н), 3.58-3.68 (м, OCHHCHCH2CHHO, 2Н), 3.72-3.80 (м, CH2CHHO, 1Н), 3.85 (с, ОСН3, 3Н), 3.86 (с, ОСН3, 3Н), 6.67-6.73 (м, Ph, 2Н), 6.78 (д, 3J=8.8 Гц, Ph, 1Н). ЯМР 13С (100.62 МГц, CDCl3) δС 35.3 (С3), 37.9 (С5), 41.3 (С2), 55.86 (OCH3), 55.91 (OCH3), 61.0 (С4), 65.5 (С1), 111.2, 112.3, 121.1, 132.9, 147.3, 148.8 (Ph).
2-[(3-Гидрокси-4-метокси-фенил)метил]бутан-1,4-диол (1с). ЯМР 1Н (400.13 МГц, CDCl3) δН 1.56-1.68 (м, CHCHH, 1Н), 1.69-1.80 (м, CHCHH, 1Н), 1.93-2.03 (м, CH, 1Н), 2.51 (дд, 2J=14.0 Гц, 3J=6.8 Гц, CHHPh, 1Н), 2.63 (дд, 2J=14.0 Гц, 3J=7.6 Гц, CHHPh, 1Н), 3.53 (дд, 2J=11.2 Гц, 3J=7.2 Гц, OCHHCH, 1Н), 3.52-3.64 (м, OCHHCHCH2CHHO, 2Н), 3.77-3.86 (м, CH2CHHO, 1H), 3.90 (с, OCH3, 3Н), 6.68 (д, 3J=7.8 Гц, Ph, 1Н), 6.70 (с, Ph, 1Н), 6.85 (д, 3J=7.8 Гц, Ph, 1Н). ЯМР 13С (100.62 МГц, CDCl3) δС 35.2 (С3), 38.0 (С5), 41.4 (С2), 55.9 (OCH3), 61.2 (С4), 65.6 (С1), 111.5, 114.4, 121.7, 132.1, 143.9, 146.4 (Ph).
2-[(3,4,5-Триметоксифенил)метил]бутан-1,4-диол (1d). ЯМР 1Н (400.13 МГц, CDCl3) δН 1.57-1.70 (м, CHCHH, 1Н), 1.71-1.83 (м, CHCHH, 1Н), 1.95-2.08 (м, CH, 1Н), 2.53 (дд, 2J=10.6 Гц, 3J=7.6 Гц, CHHPh, 1Н), 2.65 (дд, 2J=10.6 Гц, 3J=7.4 Гц, CHHPh, 1Н), 3.55 (дд, 2J=10.6 Гц, 3J=4.8 Гц, OCHHCH, 1Н), 3.66-3.73 (м, OCHHCH, 1Н, 2Н), 3.66-3.75 (м, CH2CHHO, 1Н), 3.79-3.82 (м, CH2CHHO, 1Н), 3.87 (с, ОСН3, 6Н), 3.85 (с, ОСН3, 3Н), 6.41 (с, Ph, 2Н). ЯМР 13С (100.62 МГц, CDCl3) δС 35.3 (С3), 38.7 (С5), 41.2 (С2), 56.1 (ОСН3), 60.9 (С4), 61.2 (OCH3), 65.6 (С1), 106.0, 136.1, 153.1 (Ph).
![Способ получения 2-[(оксифенил)метил]бутан-1,4-диолов](https://fips.edrid.ru/images/rid/e6/d2/24/47c36850ae4ed0b751cdbc28dffc3908.jpg)
![Способ получения 2-[(оксифенил)метил]бутан-1,4-диолов](https://fips.edrid.ru/images/rid/e6/d2/24/6c2504866a416306c72ede419594707d.jpg)

