Результат интеллектуальной деятельности: ИНЪЕКЦИОННЫЙ ИЛИ ИНФУЗИОННЫЙ РАСТВОР L-АРГИНИНИЕВОЙ СОЛИ 5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-а]ПИРИМИДИН-7-ОНА МОНОГИДРАТА ДЛЯ ТЕРАПИИ ГРИППА И ДРУГИХ ВИРУСНЫХ ИНФЕКЦИЙ
Вид РИД
Изобретение
Изобретение относится к разработке новых инъекционных или инфузионных растворов противовирусного соединения L-аргининиевой соли 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-она моногидрата (НТП) для терапии вирусных инфекций.
Триазолопиримидины были синтезированы в качестве близких к триазоло-триазинам соединений, многие из которых проявляют широкий спектр противовирусной активности [Т.П. Кофман, Т.А. Уварова, Г.Ю. Карцева, Т.Л. Успенская 6-Нитро- и 6-бромпроизводные 4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин-7-она, Журнал органической химии, 1997, т. 33, вып. 12, с. 1784-1793]. Соединения - натриевая соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-он, дигидрат [Чупахин О.Н., Русинов В.Л., Уломский Е.Н., Чарушин В.Н., Петров А.Ю., Киселев О.И. Натриевая соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-она, дигидрат. Патент РФ 2 330036 от 27.07.2008], L-аргининиевая соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-она, моногидрат [Чупахин О.Н., Чарушин В.Н., Русинов В.Л., Уломский Е.Н., Котовская С.К., Киселев О.И., Деева Э.Г. Саватеев К.В., Борисов С.С., 5-Метил-6-нитро-7-оксо-1,2,4-триазоло[1,5-а]пиримидинида L-аргининия, моногидрат, Положительное решение о выдаче патента от 20.06.2014 по заявке 2013116765 от 15.04.2013]. Триазолопиримидины отличаются от известного препарата Триазавирин - представителя триазолотриазинов, как по способу синтеза, так и по нескольким ключевым элементам структуры, обладают рядом преимуществ в физико-химических свойствах, проявляют широкий спектр противовирусной активности. Более того, данные соединения ближе к природным азотистым основаниям в силу включения в структуру пиримидинового цикла вместо триазинового.
В отличие от натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она (Триазавирина) [Чупахин О.Н., Русинов В.Л., Уломский Е.Н., Чарушин В.Н., Петров А.Ю., Киселев О.И. Натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат, обладающая противовирусным действием, Патент РФ 2294936 от 10.03.2007], L-аргининиевая соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-он, моногидрат [Чупахин О.Н., Чарушин В.Н., Русинов В.Л., Уломский Е.Н., Котовская С.К., Киселев О.И., Деева Э.Г. Саватеев К.В., Борисов С.С., 5-Метил-6-нитро-7-оксо-1,2,4-триазоло[1,5-а]пиримидинида L-аргининия, моногидрат, Положительное решение о выдаче патента от 20.06.2014 по заявке 2013116765 от 15.04.2013] (НТП) лишен S-метильной группы в 1,2,4-триазольном цикле, но при этом сохраняет нитро-группу в пиримидиновом цикле (аналоге 1,2,4-триазинового кольца). Это делает соединение более стабильным и не подверженным окислению по одному из боковых заместителей. При этом сохраняется основная структура соединения, включая реакционно активную нитро-группу.
Соединения на основе азолоазинов, проявляющие противовирусную активность, слабо растворимы в воде. Поэтому при решении задачи получения лекарственных форм в виде инъекционных или инфузионных растворов необходимо повысить растворимость и биодоступность избранных для этих целей препаратов.
Использование солей НТП на основе аргинина, кроме повышения растворимости [Киселев О.И., Чупахин О.Н., Русинов В.Л., с соавт. Инъекционный и инфузионный раствор триазавирина для лечения вирусных инфекций. Заявка на патент РФ, 2013146452/15(072136) от 16.10.2013] преследует дополнительную цель - совершенствование фармакологических свойств данного противовирусного средства в форме инъекционного или инфузионного раствора. В частности, дополнительным свойством L-аргинина является его способность к участию в качестве субстрата NO-синтетазы как донора NO, что необходимо для усиления противобактериальной защиты, сопутствующей вирусным инфекциям и повышение растворимости [Чупахин О.Н., Чарушин В.Н., Русинов В.Л., Уломский Е.Н., Котовская С.К., Киселев О.И., Деева Э.Г., Саватеев К.В. 5-Метил-6-нитро-7-оксо-1,2,4-триазоло[1,5-а]пиримидинид L-аргининия моногидрат, per. №2013116765 от 15.04.2013; Sasaki S., Miura Т., Nishikawa S., et al. Protective Role of Nitric Oxide in Staphylococcus aureus Infection in Mice. Infection and Immunity. 1998, Vol. 66, p. 1017-1022; Bogdan C. Nitric oxide and the immune response. Nature Immunology 2001, Vol. 2, p. 907-916].
Сравнение структуры Триазавирина и НТП представлено на ФИГ. 1.
Известно, что нитрогруппа в гетероциклических соединениях проявляет фармакологическую активность в отношении важных для клеток и вирусов функциональных лекарственных мишеней [Hoffstrom B.G., Kaplan A., Letso R., Schmid R.S., Turmel G.J., Lo D.C., Stockwell B.R. Inhibitors of protein disulfide isomerase suppress apoptosis induced by misfolded proteins. Nature Chemical Biology, 6, 900-906, (2010), doi: 10.1038/nchembio.467; Gallina A., Hanley T.M., Mandel R., Trahey M., Broder C.C, Viglianti G.A., Ryser H. J.-P. Prevent HIV-1 Entry Receptor-bound Glycoprotein 120 and Prevent Cleavage of Disulfide Bonds in Inhibitors of Protein-Disulfide Isomerase. doi: 10.1074/jbc.M204547200 originally published online September 5, 2002. J. Biol. Chem. 2002, 277: 50579-50588]. Поэтому ее сохранение в структуре НТП имеет принципиальное значение.
Известен инфузионный и инъекционный раствор противовирусного препарата широкого спектра действия Триазавирина, описанный в заявке на патент [Киселев О.И., Чупахин О.Н., Русинов В.Л., с соавт. Инъекционный и инфузионный раствор триазавирина для лечения вирусных инфекций. Заявка на патент РФ, 2013146452/15(072136) от 16.10.2013], в котором впервые для данного класса соединений были разработаны инъекционные и инфузионные растворы для лечения тяжелых форм вирусных инфекций.
Известны также инфузионные и инъекционные растворы препаратов Тамифлю (Осельтамивир) и Перамивира [http://www.biocryst.com/peramivir]. Характерной особенностью препаратов из группы нейраминидазных ингибиторов является снижение их терапевтической эффективности при лечении гриппозной пневмонии, сопровождающейся развитием легочного дистресс синдрома [Short K.R.,Veldhuis Kroeze E.J.B., Fouchier R.A.M., Prof Kuiken T. Pathogenesis of influenza-induced acute respiratory distress syndrome. The Lancet Infectious Diseases, Volume 14, Pages 57-69, January 2014. doi: 10.1016/S1473-3099(13)70286-XCite or Link Using DOI; Nakajima N., Sato Y., Katano H. et al. Histopathological and immunohistochemical findings of 20 autopsy cases with 2009 H1N1 virus infection. Modern Pathology (2012) 25, 1-13; doi: 10.1038/modpathol.2011.125; published online 26 August 2011]. Это может быть связано с усилением метаболизма лекарственных препаратов при высоком уровне активных форм кислорода. Генерирование реакционно активных форм кислорода (от синглетного кислорода до гидроксония и пероксинитрита) сопровождает процессы легочной гипоксии при дыхательной недостаточности и дистресс синдроме. С другой стороны, сам по себе механизм действия ингибиторов нейраминидазы недостаточно совершенен. Фактически, ингибиторы нейраминидазы блокируют почкование зрелых вирусных частиц, нарушая их освобождение от клеток, то есть, иными словами, диссеминацию вирусной инфекции, что уже не имеет принципиального значения при таких тяжелых осложнениях, как легочный дистресс-синдром, отек легких или сепсис.
Известно, что патогенные вирусы гриппа с высокой тропностью к легким вызывают альвеолит, то есть дисперсное мелкоочаговой поражение легочной ткани [Jakab GJ, Astry CL, Warr GA. Alveolitis induced by influenza virus. Am Rev Respir Dis. 1983 Oct; 128(4): 730-9; Jeffery K. Taubenberger J.K., Morens D.M. The Pathology of Influenza Virus Infections. Annu Rev Pathol. 2008; 3: 499-522]. Поэтому бессмысленно рассчитывать на то, что блокада освобождения почкующегося на пневмоцитах вируса приведет к остановке внутритканевого распространения инфекции. Таким образом, на поздних стадиях инфекции, когда произошла диссеминация вируса в органах и тканях, и, в первую очередь, в легких, блокада почкования вируса ингибиторами нейраминидазы уже не приводит к ожидаемым терапевтическим результатам [Киселев О.И. Химиотерапия и химиопрепараты против гриппа. СПб. Изд. «Росток». 2012. С. 269]. Конструктивное несовершенство, начиная с замысла создания ингибиторов нейраминидазы, постепенно осознается в мировой литературе и поэтому предпринимаются попытки создания комплексных препаратов, до известной степени исключающие недостатки этих препаратов [Zasloff М., Formulations comprising aminosterols. US 8623416 В2]. Аминостероиды в сочетании с Тамифлю используются для снижения деструктивных процессов в легочной ткани. В цитируемом патенте отмечается, что данная группа средств может снижать неблагоприятное действие противовирусного препарата на состояние легочной ткани.
Вместе с тем, концепция комплексной терапии гриппа значительно шире. Эта идеология является основой российской практики лечения гриппа [Киселев О.И. Химиотерапия и химиопрепараты против гриппа. СПб. Изд. «Росток». 2012].
Возрастающий интерес к инъекционным и инфузионным растворам противогриппозных препаратов относится к периоду пандемии «свиного» гриппа A(H1N1), когда в ускоренном режиме был создан внутривенный препарат Перамивир [http://www.biocryst.com/peramivir; Goldbach Р., Grassmann О., Sauer I. Polymorphic forms of oseltamivir phosphate. US Patent, 8,334,319 B2. 2012; Zasloff M., Formulations comprising aminosterols. US 8623416 B2; Babu Y.S., Chand P., Arnold S., Kilpatrick J.M. Intramuscular antiviral treatments. Patent Application Publication (10) Pub. No.: US 2011/0015264 A1; Hilfinge J., Amidon G. Prodrugs of neuraminidase inhibitors. WO 2009129305 A2; Kohno S. Kida H., Mizuguchi M., Shimada J. for the S-021812 Clinical Study Group. Efficacy and Safety of Intravenous Peramivir for Treatment of Seasonal Influenza Virus Infection. Antimicrob. Agents Chemother. 2010, p. 4568-4574 Vol. 54, No. 11].
Перамивир применяется в виде раствора NaCl в концентрации 0,9 или 0,45% без сопутствующих дополнительных компонентов [Kohno S., Kida Н., Mizuguchi М., et al. Efficacy and Safety of Intravenous Peramivir for Treatment of Seasonal Influenza Virus Infection. Antimicrob. Agents & Chemother. 2010, Vol. 54, p. 4568-4574; Louie JK, Yang S, Yen C, Acosta M, Schechter R, et al. (2012) Use of Intravenous Peramivir for Treatment of Severe Influenza A(H1N1)pdm09. PLoS ONE 7(6): e40261. doi: 10.1371/journal.pone.0040261].
Учитывая повышение уровня угрозы распространения новых штаммов патогенных вирусов гриппа и, в первую очередь, вируса A(H7N9), проводятся исследования по изучению эффективности внутривенных лекарственных форм Перамивира. Полученные результаты позволяют рекомендовать данный препарат для терапии тяжелых случаев гриппа, вызванных вирусом A(H7N9) [http://www.chinanews.com/jk/2013/04-06/4705205.shtml].
Однако при этом остаются все вышеуказанные издержки использования такого терапевтического подхода, если учитывать, что наиболее тяжелым осложнением этого вида гриппа является тяжелый острый респираторный дистресс синдром.
Ранее установлено, что L-аргининиевая соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-она моногидрат обладает широким спектром противовирусной активности.
Инъекционные формы противовирусных препаратов позволяют решать несколько задач:
- собственно антивирусной терапии,
- сочетание со средствами системной противовоспалительной терапии,
- проблемы дезинтоксикации при гриппе и других инфекциях.
Изобретение направлено на разработку лекарственной композиции инъекционной или инфузионной форм препаратов НТП, обеспечивающей повышение терапевтической эффективности при лечении гриппозной пневмонии и осложненных форм гриппа за счет высокой метаболической стабильности и биодоступности соединения при ограничении объемов вводимой жидкости в организм пациента. Также расширен спектр фармакологической активности НТП.
Задачи изобретения решаются следующим образом:
- использованием противовирусного соединения L-аргининиевой соли 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-он, моногидрат (НТП) с высокой по сравнению с триазавирином растворимостью и высокой биодоступностью и отсутствием легко окисляемых заместителей и, в частности, S-метильной группы во втором положении триазольного цикла;
- введением в виде компонентов, образующих соли с НТП дополнительных соединений, обеспечивающих расширение спектра фармакологической активности НТП;
L-аргининиевая соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-он, моногидрат (НТП) отличается от Триазавирина более высокой растворимостью, что позволяет готовить растворы с концентраций до 8 и более процентов. В связи с этим при их применении возможно снижение количества вводимой больному гриппом жидкости при состояниях, угрожающих развитием отека легких.
Инъекционный и инфузионный растворы согласно изобретению содержат биологически активное вещество L-аргининиевую соль 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-она, моногидрат (НТП) [Чупахин О.Н., Чарушин В.Н., Русинов В.Л., Уломский Е.Н., Котовская С.К., Киселев О.И., Деева Э.Г. Саватеев К.В., Борисов С.С., 5-Метил-6-нитро-7-оксо-1,2,4-триазоло[1,5-а]пиримидинида L-аргининия, моногидрат, Положительное решение о выдаче патента от 20.06.2014 по заявке 2013116765 от 15.04.2013].
В композицию могут вводиться дополнительные вещества, например вспомогательное вещество - восстановленный глутатион (трипептид Глу-Цис-Гли) в количестве 2,0% и карнозин в количестве 2,0%.
В случае тяжелого течения вирусной инфекции, вызванной патогенным гриппом и осложненной развитием «цитокинового шторма», необходимо использование антиоксидантов (аскорбиновая кислота, сульфитные соединения, L-цистеин, N-ацетилцистеин, тиодипропионовая кислота, тиомолочная кислота, монотиоглицерин, пропилгаллат и др.). В отдельных случаях существует необходимость в добавлении к растворам, согласно изобретению, местноанестезирующих веществ, как, например, прокаингидрохлорид, лидокаингидрохлорид, а также антиконвульсантов, ингибиторов Nf-kB, фактора некроза опухолей, эндотелиальных и сосудистых проекторов [Short К., Veldhuis Kroeze E.J.B., Fouchier R.A.M., Kuiken Т. Pathogenesis of influenza-induced acute respiratory distress syndrome. Lancet.com.infection. 2014, Vol. 14 p. 57-69]. Возможна комбинация с кислотами, например янтарной кислотой, сахарами, включая глюкозу, маннозу, спирты, например маннит или сорбит. Для ускорения растворения раствор нагревают на водяной бане до 50-60°C. Сразу после получения соли в композицию при перемешивании до или после охлаждения растворяют остальные составные части или в нее вносят. После добавления остального количества растворителя композицию стерилизуют фильтрованием через бактериальный фильтр и/или нагреванием.
Изобретение реализуется следующим образом.
Пример 1. Получение растворов L-аргининиевой соли 5-метил-6-нитро-1,2,4-триазоло[1,5-а]пиримидин-7-она, моногидрат (НТП)
В приготовлении инъекционных и инфузионных растворов руководствовались следующими условиями.
1. Определением порога растворимости для достижения оптимальной концентрации инъекционного и инфузионного раствора.
2. Определением условий повышения растворимости, биодоступности и метаболической стабильности.
3. Достижением условия сочетания с другими субстанциями, требующимися для повышения терапевтической противовирусной эффективности препарата НТП.
Исследование растворимости НТП было проведено следующим способом. Во взвешенный стакан объемом 250 мл поместили якорь магнитной мешалки, 100 г воды (по весу), 8 г препарата и перемешивали 8 ч при комнатной температуре. Предел измерения весов составил 0,2 г. После перемешивания смесь отфильтровали в приборе, состоящем из взвешенной круглодонной колбы объемом 250 мл, перехода с отводом и взвешенной воронки со шлифом. После фильтрования взвесили по отдельности фильтрат и влажный осадок. Осадок оставили сушиться, фильтрат упарили из колбы полностью на ротационном испарителе при остаточном давлении в приборе 10÷15 мм рт.ст., температуре в бане 40÷50°C и также оставили сушиться в течение ночи при комнатной температуре. Установлено, что масса раствора перед упариванием составила 106,2 г, масса сухого препарата - 6,2 г. таким образом, растворимость НТП в воде составила около 6,0% [Киселев О.И., Чупахин О.Н., Русинов В.Л. и др. Инъекционный и инфузионный раствор триазавирина для лечения вирусных инфекций. Заявка №2013146452/15(072136) от 16.10.2013].
Пример 2. Исследование токсичности растворов НТП при внутривенном введении
В опытах на кроликах и грызунах исследована острая токсичность образцов субстанции НТП [Чупахин О.Н., Чарушин В.Н., Русинов В.Л., Уломский Е.Н., Котовская С.К., Киселев О.И., Деева Э.Г. Саватеев К.В., Борисов С.С., 5-Метил-6-нитро-7-оксо-1,2,4-триазоло[1,5-а]пиримидинида L-аргининия, моногидрат, Положительное решение о выдаче патента от 20.06.2014 по заявке 2013116765 от 15.04.2013], синтезированной в институте органического синтеза УрО РАН.
По данным исследования острой и хронической токсичности НТП на грызунах средняя смертельная доза НТП при внутрибрюшинном введении крысам составляет >5000 мг/кг. При пероральном введении НТП крысам внутрь животные переносили препарат в дозах до 40000 мг/кг без каких либо видимых признаков интоксикации. По данным исследований, проведенных в ЗАО «Санкт-Петербургский институт Фармации», при пероральном введении крысам ЛД50 составила более 40000 мг/кг.

Установлено, что характер токсического действия аналогичен в исследованиях на мышах и крысах, т.е. токсические изменения в органах и тканях практически отсутствовали.
В экспериментах установить значения ЛД50 оказалось невозможным в связи с отсутствием гибели животных в экспериментальных группах при обоих путях введения. Следовательно, по показателям острой токсичности субстанцию НТП можно отнести к VI классу относительно безвредных веществ по классификации Hodge и Sterner [Hodge Н. et al., 1975].
В острых экспериментах на кроликах проведено изучение токсичности и переносимости субстанции НТП при внутривенном пути введения. Растворы НТП, так же как и Триазавирина, для внутривенного введения готовили с использованием биполярного растворителя диметилсульфоксида (ДМСО) и 0,9% раствора хлорида натрия, подогретого до температуры 38-39°. Необходимость использования ДМСО обусловлена ограничением растворимости НТП, как и большинства представителей соединений триазоло-триазинового и триазоло-пиримидинового ряда. Так, при комнатной температуре растворимость НТП в воде составляет 8%.
Изучение острой токсичности НТП при внутривенном способе введении проведено на кроликах с массой тела от 2,5 кг до 3,5 кг, содержащихся в виварии НИИ гриппа. НТП вводили в возрастающих дозировках от 700 мг/кг до 1500 мг/кг. Гибели животных при этом не наблюдалось. В соответствии с установленными нормами в экспериментах НТП вводили внутривенно как струйным, так и капельным способом в объеме 100 мл, что в 5 раз превышает рекомендуемый объем. При этом удавалось ввести дозу 1500 мг/кг. Наблюдение за животными в течение недели не позволило выявить изменений в их поведении, интенсивности и характере двигательной активности, координации движений, потреблении корма и воды.
НТП так же как и препарата Триазавирин [Киселев О.И., Чупахин О.Н., Русинов В.Л. и др. Инъекционный и инфузионный раствор триазавирина для лечения вирусных инфекций. Заявка №2013146452/15(072136) от 16.10.2013] может быть отнесен к практически нетоксичным соединениям и характеризуется более высокой растворимостью, что позволяет готовить более концентрированные инъекционные и инфузионные растворы препарата и, следовательно, избегать излишнего введения жидкости.
Инъекционная (инфузионная) лекарственная форма препарата НТП должна соответствовать концентрации раствора субстанции не менее 0,5%, который в определенном объеме введения обеспечит его эффективную концентрацию в крови, а именно 0,5-10 мкг/мл, предпочтительно 2-4 мкг/мл. При тяжелом течение гриппа можно увеличивать дозу и достигать концентрации препарата до 20 мкг/мл.
Диапазон эффективных доз для человека при парентеральном способе введения составляет 5,0-25 мг/кг. Поэтому оптимальной формой выпуска для инфузионных растворов НТП являются флаконы по 50-100 мл с содержанием субстанции НТП до 500 мг/флакон или 5-10 мг/мл. Для лечения клинически тяжелых форм гриппа с развитием гриппозной пневмонии и угрозой отека легких рекомендуется введение препарата до 3 раз в день по 1 флакону с дозой по 500 мг на одно внутривенное введение. Для инъекций можно рекомендовать растворы 5-10 мл с концентрацией от 20 до 50 мг.
Как уже указывалось, для лечения гриппа в период пандемии 2009/11, вызванной «свиным» штаммом вируса A(H1N1) в США был зарегистрирован инъекционный и инфузионный препарат Перамивир (http://www.biocryst.com/peramivir). Препарат используется в водном растворе в дозах от 6 до 10 мг/кг и выпускается в виде порошка во флаконах по 300 или 600 мг для растворения в растворе хлорида натрия 0,9 или 0,45%. Практика применения показала, что оптимальной скоростью введения является 40 мг/мин. НТП также хорошо растворим в физиологических растворах хлорида натрия. Вместе с тем, более адекватно в этом случае в относительно небольших объемах использовать Мексидол, который может быть совместим с инфузиями НТП и служить дополнительным средством дезинтоксикации путем снижения уровня генерирования свободных радикалов кислорода [Kalyanaraman В. Teaching the basics of redox biology to medical and graduate students: Oxidants, antioxidants and disease mechanisms. Redox Biology. 2013, Vol. 1, p. 244-257, Zimniak P. Relationship of electrophilic stress to aging. Free Radical Biology and Medicine. 2011, Vol. 51, p. 1087-1105].
Однако наиболее оптимальным является сочетание НТП с известными антиоксидантами и препаратами, восстанавливающими и стабилизирующими окислительно-восстановительный потенциал инфицированных клеток. Поэтому в нижеприведенных примерах предлагаются композиции инфузионных растворов НТП, основанные на этих выводах и известных рекомендациях по терапии неотложных состояний в инфекционных клиниках [http://www.drrobertamorgan.com/intravenous-therapies-and-infections.htm].
Пример 3. Состав инъекционных или инфузионных растворов препарата
Ниже приводятся композиции инъекционных и инфузионных растворов, содержащих в качестве основного противовирусного компонента НТП. Выбор композиций осуществлялся на основании следующих принципов.
1. Водно-солевые композиции, обеспечивающие поддержание водно-солевого баланса и не интерферирующие с действием НТП.
2. Растворы, содержащие восстановленный Глутатион - трипептид Глу-Цис-Гли, являющийся основным компонентом редокс-системы клеток. Глутатион в сочетании с карнозином [Koen R., Yamamoto Y., Cundy K.C., Ames B.N. Antioxidant activity of carnosine, homocarnosine, and anserine present in muscle and brain. Proc. NatI. Acad. Sci. USA. 1988, Vol. 85, pp. 3175-3179] является активным протектором в отношении деструктивного действия активных форм кислорода, что обеспечивает защиту тканей от окислительного стресса [Bae O.-N., Serfozo K., Baek S.-H., et. al. Safety and Efficacy Evaluation of Carnosine, an Endogenous Neuroprotective Agent for Ischemic Stroke. Stroke. 2013; 44: 205-212; Ditte Z., Ditte P., Labudova M., Simko V., et al. Carnosine inhibits carbonic anhydrase IX-mediated extracellular acidosis and suppresses growth of HeLa tumor xenografts. BMC Cancer. 2014 May 22; 14: 358. doi: 10.1186/1471-2407-14-358], сопутствующего воспалительным процессам. Карнозин в условиях гипоксии значительно повышает уровень экспрессии гена HIF-lα - фактора, индуцированного гипоксией, обеспечивая протективный эффект в условиях ацидоза и недостатка кислорода. К этому следует добавить, что Глутатион является участником реакций с белками, известными как S-глутатионирование, играющих важную роль в регуляции функций ферментов и контроле вирусной репродукции [Palamara А.Т., Brandi G., Rossi L. New synthetic glutathione derivatives with increased antiviral activities. Antivir. Chem. Chemother. 2004 Mar; 15(2): 83-91.; Ma H-C, Liu Y, Wang C., Strauss M., Rehage N., et al. (2014) An Interaction between Glutathione and the Capsid Is Required for the Morphogenesis of C-Cluster Enteroviruses. PLoS Pathog 10(4): e1004052. doi: 10.1371/journal.ppat. 1004052].
Для исследования противовирусной активности использовали различные композиции НТП с соединениями, разрешенными для клинического применения и способными усилить общий и специфический терапевтический эффект противовирусного препарата.
Композиции имели следующий состав:
1. НТП - 500 мг, Натрия хлорид - 900 мг, Вода д/инъек. до 100 мл, pH 5,5-7,2.
2. НТП- 500 мг, Глюконолактон - 2000 мг, Глутаминовая кислота - 2000 мг, Карнозин - 2000 мг, Сульфит натрия - 100 мг, Вода д/инъек. до 100 мл, pH 5,2-6,5.
3. НТП - 500 мг, Глутатион (восстан.) - 2000 мг, Карнозин - 2000 мг, Вода д/инъек. до 100 мл, pH 6,8-7,25.
Исследование противовирусной активности полученных препаратов проводили на стандартной модели смертельной гриппозной инфекции на мышах, используя адаптированный к мышам штамм вируса гриппа A/Aichi/2/68 A(H3N2) [Киселев О.И., Чупахин О.Н., Русинов В.Л., Чарушин В.Н., Деева Э.Г. Коньюгаты 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4I′)-она с глютатионом и другими пептидами, обладающие противовирусной активностью. Патент на изобретение RUS 2516936 27.04.2012]. Белых беспородных мышей заражали 1- или 10 - кратной смертельной дозой вируса, препарат вводили одновременно с заражением и эффект защиты определяли по числу выживших мышей, получавших препарат. Данные защитного эффекта представлены в таблице 2.
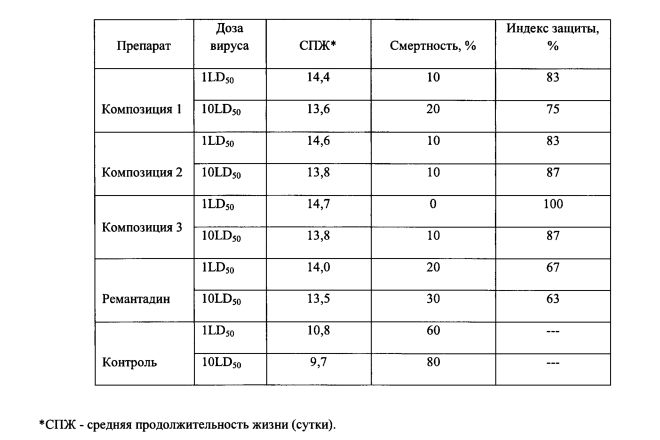
Таким образом, все композиции проявили высокий уровень противовирусной активности в отношении ремантадин-чувствительного штамма вируса гриппа A/Aichi/2/68 A(H3N2). В зависимости от динамики инфекционного процесса могут осуществляться назначения тех или иных композиций растворов НТП. Глутатионовая и Карнозиновая композиции (2 и 3) имеют преференции при тяжелых состояниях, связанных с нарушением окислительно-восстановительного баланса.
Из приведенных составов композиций следует, что количественное содержание компонентов соответствует заявленному содержанию в формуле изобретения.
![ИНЪЕКЦИОННЫЙ ИЛИ ИНФУЗИОННЫЙ РАСТВОР L-АРГИНИНИЕВОЙ СОЛИ 5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-а]ПИРИМИДИН-7-ОНА МОНОГИДРАТА ДЛЯ ТЕРАПИИ ГРИППА И ДРУГИХ ВИРУСНЫХ ИНФЕКЦИЙ](https://fips.edrid.ru/images/rid/25/95/80/1fa11cc71e3183f9e8d7f40a9260055f.png)

