Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-(2-АЦИЛВИНИЛ)ИНДОЛОВ
Вид РИД
Изобретение
Изобретение относится к области органической химии - синтезу гетероциклических соединений - производных 2-(2-ацилвинил)индола, представляющих интерес в качестве исходных соединений для синтеза веществ фармацевтического назначения.
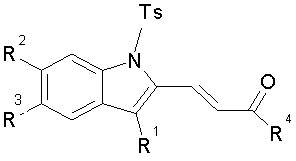
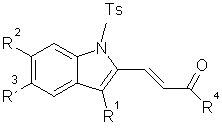
Изобретение относится к разработке способа получения производных 2-(2-ацилвинил)индола общей формулы Ia-к, которые являются привлекательными объектами для медицинской химии. Данные соединения могут быть успешно использованы в синтезе аналогов алкалоидов флиндерола А-С, обладающих ярко выраженной противомалярийной активностью [D.Н. Dethe, R.D. Erande, A. Ranjan, J. Org. Chem., 2013, 78, 10106-10120] и гиполипидемического препарата флувастатина [J.Т. Zacharia, Т. Tanaka, М. Hayashi, J. Org. Chem., 2010, 75, 7514-7518].
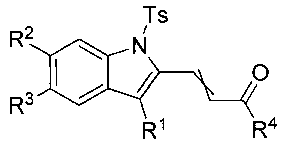
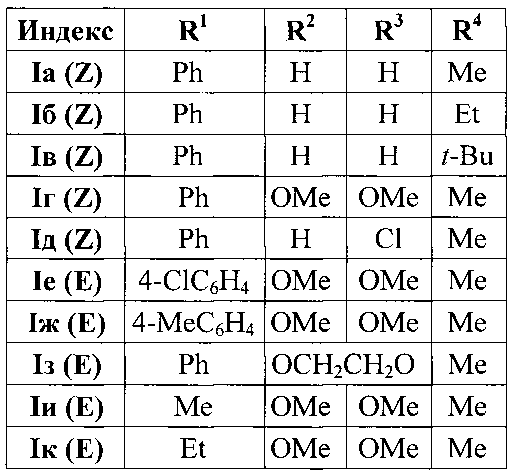
В литературе описано несколько подходов к синтезу замещенных 2-ацилвинилиндолов, однако большинство из них основаны на модификации соединений, содержащих готовый индольный фрагмент. Наиболее распространенным подходом к получению халконов индольного ряда является реакция Виттига. Так, например, взаимодействие 3-метил-1Н-индол-1-фенилсульфонил-2-карбальдегида и 1-(трифенилфосфоранилиден)-2-пропанона в кипящем ТГФ приводит к 2-(2-ацилвинил)индолу [А.К. Mohanakrishnan, Р.С. Srinivasan, J. Org. Chem., 1995, 60, 1939-1946]. Другим методом синтеза 2-(2-ацилвинил)индолов является альдольная конденсация 5-хлор-1H-индол-2-карбальдегида и ацетона в спирте, катализируемая водной щелочью [J. Zhou, G. Geng, J.Н. Wu, Invest New Drugs, 2010, 28, 291-298]. Кроме этого в литературе описана реакция алкенилирования 1-(пиридин-2-илсульфонил)-1H-индола пент-1-ен-3-оном, катализируемая трифторацетатом палладия в уксусной кислоте [Z. - L. Yan, W. - L. Chen, Y. - R. Gao, S. Mao, Y. - L. Zhang, Y. - Q. Wang, Adv. Synth. Catal., 2014, 356, 1085-1092]. Другой пример алкенилирования основан на родий катализируемом взаимодействии 2-(1H-индол-1-ил)фенола и бут-3-ен-2-она при нагревании в диметилацетамиде [C. - Y. Tang, Y. Tao, X. - Y. Wu, F. Shaa, Adv. Synth. Catal., 2014, 356, 609-615]. К недостаткам перечисленных методов можно отнести обязательное присутствие направляющей группы для селективного алкенилирования, дороговизну используемых катализаторов, низкие выходы, а также труднодоступность исходных соединений.
Помимо перечисленных методов синтеза 2-(2-ацилвинил)индолов, использующих субстраты с уже готовым индольным каркасом, в литературе описаны примеры синтеза, основанные на одновременном построении индольного фрагмента и введении алкен-2-онового заместителя во 2-ое положение ядра. Один из таких подходов основан на one-pot реакции рециклизации замещенных 2-тозиламинобензилфуранов, образующихся в результате алкилирования N-тозилфурфуриламина производными 2-тозил-аминобензилового спирта [Uchuskin М.G., Molodtsova N.V., Lysenko S.А., Strel'nikov V.N., Trushkov I.V., Butin A.V., Eur. J. Org. Chem. 2014, 2508-2515, Учускин М.Г., Лысенко C.A., Молодцова H.B., Трушков И.В., Бутин А.В., патент РФ №2488581]. Однако данный метод позволяет получать лишь индолы, имеющие 2-ацетилвинильный заместитель во втором положении с выходами 30-71%, кроме того, эта реакция приводит к формированию преимущественно E-изомера, что накладывает определенные ограничения на ее использование.
В основу другого метода положен термолиз легкодоступных 2-азидобензилфуранов в высококипящих растворителях [Abaev V.Т., Plieva А.Т., Chalikidi P.N., Uchuskin М.G., Trushkov I.V., Butin А.V., Org. Lett., 2014, 16, 4150-4153; Сердюк О.В., Плиева А.Т., Учускин М.Г., Трушков И.В., Бутин А.В., Абаев В.Т. Патент РФ №2495027]. Хотя данный метод и позволяет варьировать заместители у атома С(2) ацилвинильного заместителя, применение данной реакции для синтеза целевых индольных производных в большинстве случаев приводит к смеси Z- и E-изомеров, что ограничивает область применения этого метода.
В основе заявляемого метода лежит описанная ранее реакция окисления 4-(5-метилфуран-2-ил)бутан-2-онов N-бромсукцинимидом в водном ТГФ в присутствии Cu(ОАс)2 и уксусной кислоты с образованием 4-(5-метилфуран-2-ил)бут-3-ен-2-онов [Yu Н., Zhong W., Не Т., Gu W., Yin В. Tetrahedron Lett. 2013, 54, 1256-1260].
Задача изобретения - разработка нового эффективного метода получения производных 2-(2-ацилвинил)индолов Ia-к, позволяющего расширить номенклатуру потенциально физиологически активных веществ и представляющих интерес в качестве легкодоступных исходных соединений для синтеза биологически активных соединений.
Техническим результатом является создание простого и эффективного метода синтеза 2-(2-ацилвинил)индолов, позволяющего стереоселективно получать целевые продукты с высоким выходом, а также варьировать заместители в индольном ядре, равно как и природу ацилвинильного фрагмента, что, в конечном счете, позволяет преодолеть ряд ограничений и недостатков существующих методов.
Технический результат достигается в результате последовательной обработки доступных 2-тозиламинобензилфуранов [А.V. Butin, S.К. Smirnov, Т.A. Stroganova, W. Benderb, G.D. Krapivin, Tetrahedron, 2007, 63, 474-491] м-хлорпербензойной кислотой, а затем трифторуксусной кислотой в дихлорметане.
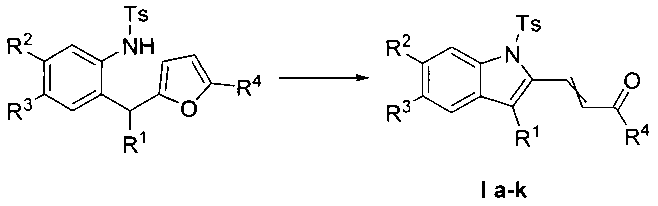
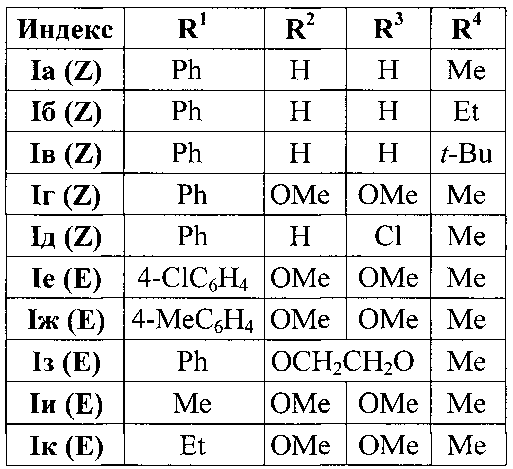
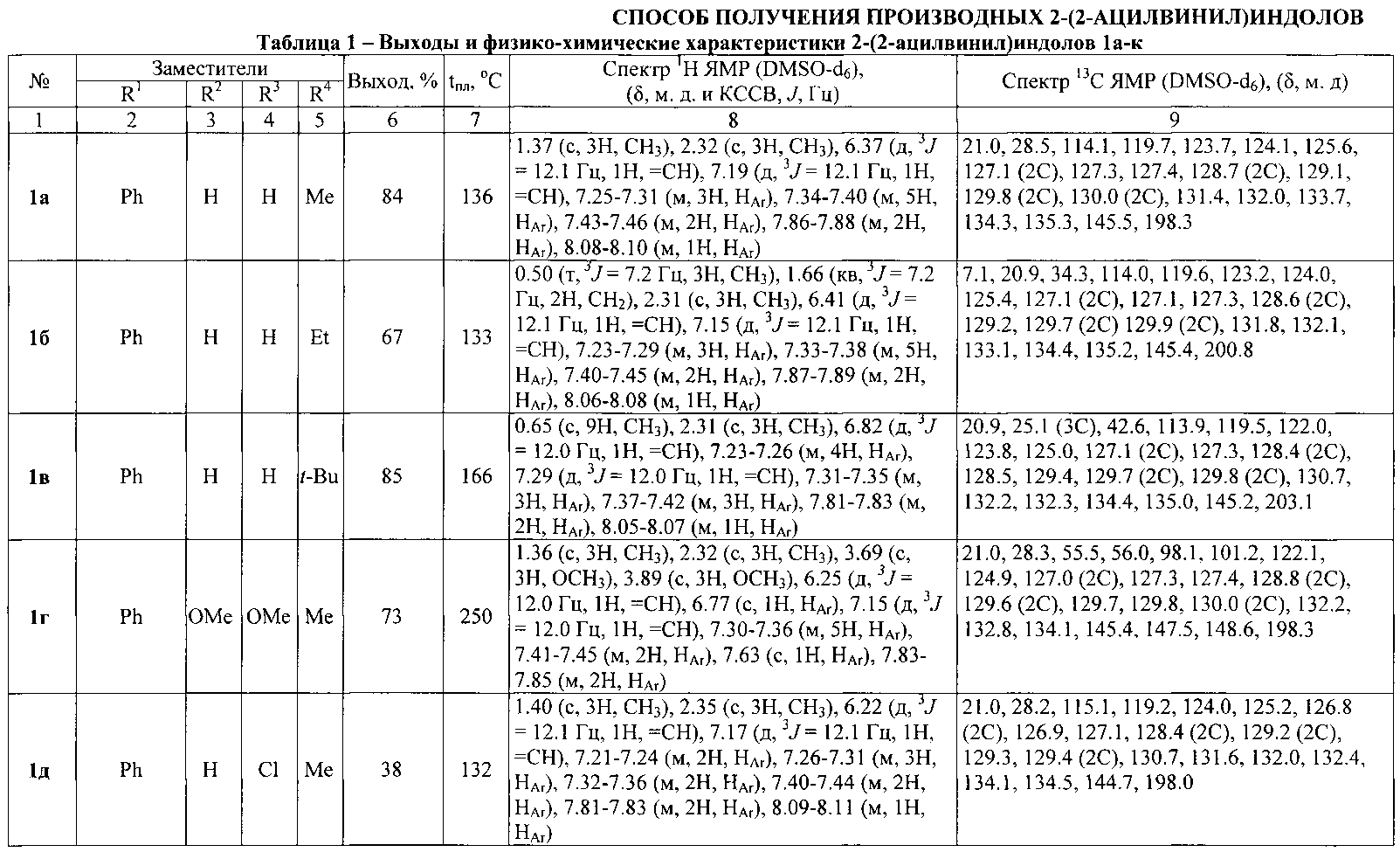
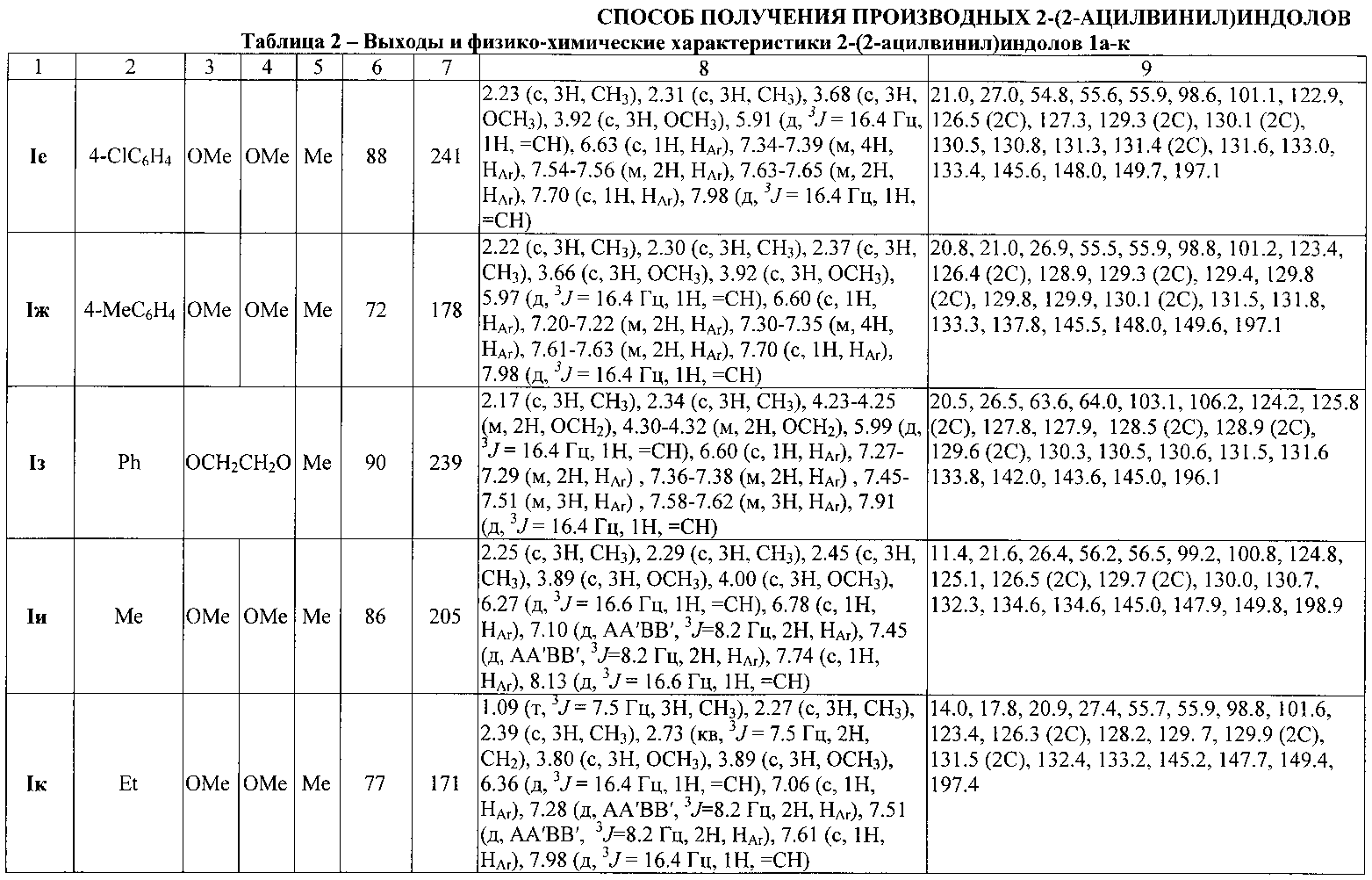
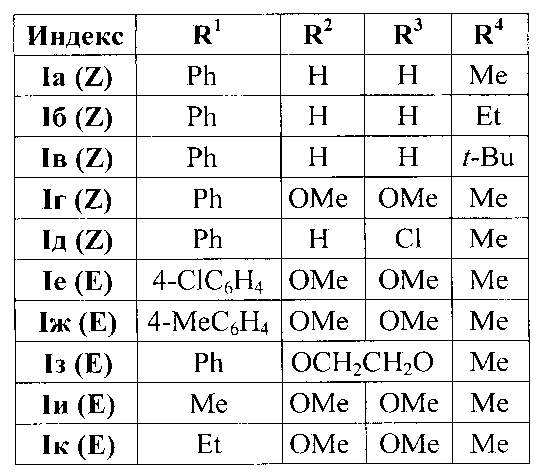
Выходы продуктов реакции, температуры плавления, данные элементного анализа, и спектральные характеристики 2-(2-ацилвинил)индолов Ia-к приведены в таблице 1 (приложение к заявке).
Полученный технический результат позволяет получать желаемые продукты Ia-к с высокими выходами, в виде индивидуальных Z- или Е-стереоизомеров. Помимо этого, метод имеет более широкую область применения, что выражается в большом наборе субстратов, которые могут быть использованы для синтеза различных замещенных 2-(2-ацилвинил)индолов, являющихся потенциально биологически активными соединениями.
Совокупность существенных признаков, изложенных в формуле изобретения, позволяет достичь желаемого технического результата.
Примеры осуществления заявляемого способа получения (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-она 1а.
Пример 1.
Смесь 0.209 г 2-метил-5-[2-(N-тозиламино)бензгидрил]фурана (0.5 ммоль) и 0.104 г мета-хлорпербензойной кислоты (0.6 ммоль) растворяют в 2 мл безводного дихлорметана и перемешивают на магнитной мешалке при 0°С в течение 1 часа. Выпавшую мета-хлорбензойную кислоту отфильтровывают, промывают холодным безводным дихлорметаном (2×2 мл), добавляют к фильтрату 8 мкл трифторуксусной кислоты (0.1 ммоль) и перемешивают при комнатной температуре в течение 20 часов (контроль ТСХ). По окончании реакции к реакционной смеси добавляют 0.055 г NaHCO3 (0.65 ммоль), перемешивают 5 мин при кипячении, растворитель удаляют при пониженном давлении. Целевой (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-он очищают методом колоночной хроматографии на силикагеле марки КСК (производства ООО Сорбполимер) фракция 5-40 мкм, элюент - хлористый метилен:петролейный эфир (1:5). Выход 88% (0.183 г).
Rf=0,46 (этилацетат/петролейный эфир 1:2)
Тпл.=136°С
Спектр 1Н ЯМР (DMSO-d6), (δ, м. д. и КССВ, J, Гц): 1.37 (с, 3Н, СН3), 2.32 (с, 3Н, СН3), 6.37 (д, 3J=12.1 Гц, 1H, =СН), 7.19 (д, 3J=12.1 Гц, 1Н, =СН), 7.25-7.31 (м, 3Н, НАr), 7.34-7.40 (м, 5Н, НАr), 7.43-7.46 (м, 2Н, НАr), 7.86-7.88 (м, 2Н, НАr), 8.08-8.10 (м, 1Н, НАr)
Спектр 13С ЯМР (DMSO-d6), (δ, м. д.): 21.0, 28.5, 114.1, 119.7, 123.7, 124.1, 125.6, 127.1 (2С), 127.3, 127.4, 128.7 (2С), 129.1, 129.8 (2С), 130.0 (2С), 131.4, 132.0, 133.7, 134.3, 135.3, 145.5, 198.3.
Пример 2.
Смесь 0.209 г 2-метил-5-[2-(N-тозиламино)бензгидрил]фурана (0.5 ммоль) и 0.104 г мета-хлорпербензойной кислоты (0.6 ммоль) растворяют в 2 мл безводного дихлорметана и перемешивают на магнитной мешалке при 0°С в течение 1 часа. Выпавшую мета-хлорбензойную кислоту отфильтровывают, промывают холодным безводным дихлорметаном (2×2 мл), добавляют к фильтрату 4 мкл трифторуксусной кислоты (0.05 ммоль) и перемешивают при комнатной температуре в течение 20 часов (контроль ТСХ). По окончании реакции к реакционной смеси добавляют 0.055 г NaHCO3 (0.65 ммоль), перемешивают 5 мин при кипячении, растворитель удаляют при пониженном давлении. Целевой (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-он очищают методом колоночной хроматографии на силикагеле марки КСК (производства ООО Сорбполимер) фракция 5-40 мкм, элюент - хлористый метилен:петролейный эфир (1:5). Выход 88% (0.184 г).
Пример 3.
Смесь 0.209 г 2-метил-5-[2-(N-тозиламино)бензгидрил]фурана (0.5 ммоль) и 0.104 г мета-хлорпербензойной кислоты (0.6 ммоль) растворяют в 2 мл безводного дихлорметана и перемешивают на магнитной мешалке при 0°С в течение 1 часа. Выпавшую мета-хлорбензойную кислоту отфильтровывают, промывают холодным безводным дихлорметаном (2×2 мл), добавляют к фильтрату 2 мкл трифторуксусной кислоты (0.025 ммоль) и перемешивают при комнатной температуре в течение 20 часов (контроль ТСХ). По окончании реакции к реакционной смеси добавляют 0.055 г NaHCO3 (0.65 ммоль), перемешивают 5 мин при кипячении, растворитель удаляют при пониженном давлении. Целевой (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-он очищают методом колоночной хроматографии на силикагеле марки КСК (производства ООО Сорбполимер) фракция 5-40 мкм, элюент - хлористый метилен:петролейный эфир (1:5). Выход 82% (0.170 г).
Пример 4.
Смесь 0.209 г 2-метил-5-[2-(N-тозиламино)бензгидрил]фурана (0.5 ммоль) и 0.104 г мета-хлорпербензойной кислоты (0.6 ммоль) растворяют в 2 мл безводного дихлорметана и перемешивают на магнитной мешалке при 0°С в течение 1 часа. Выпавшую мета-хлорбензойную кислоту отфильтровывают, промывают холодным безводным дихлорметаном (2×2 мл), добавляют к фильтрату 3 мкл уксусной кислоты (0.05 ммоль) и перемешивают при комнатной температуре в течение 20 часов (контроль ТСХ). По окончании реакции к реакционной смеси добавляют 0.055 г NaHCO3 (0.65 ммоль), перемешивают 5 мин при кипячении, растворитель удаляют при пониженном давлении. Целевой (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-он очищают методом колоночной хроматографии на силикагеле марки КСК (производства ООО Сорбполимер) фракция 5-40 мкм, элюент - хлористый метилен:петролейный эфир (1:5). Выход 60% (0.124 г).
Пример 5.
Смесь 0.209 г 2-метил-5-[2-N-тозиламино)бензгидрил]фурана (0.5 ммоль) и 0.104 г мета-хлорпербензойной кислоты (0.6 ммоль) растворяют в 2 мл безводного дихлорметана и перемешивают на магнитной мешалке при 0°С в течение 1 часа. Выпавшую мета-хлорбензойную кислоту отфильтровывают, промывают холодным безводным дихлорметаном (2×2 мл). Смесь перемешивают при комнатной температуре в течение 20 часов (контроль ТСХ). По окончании реакции к реакционной смеси добавляют 0.055 г NaHCO3 (0.65 ммоль), перемешивают 5 мин при кипячении, растворитель удаляют при пониженном давлении. Целевой (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-он очищают методом колоночной хроматографии на силикагеле марки КСК (производства ООО Сорбполимер) фракция 5-40 мкм, элюент - хлористый метилен:петролейный эфир (1:5). Выход 13% (0.026 г).
Пример 6.
Смесь 0.209 г 2-метил-5-[2-(N-тозиламино)бензгидрил]фурана (0.5 ммоль) и 0.104 мг мета-хлорпербензойной кислоты (0.6 ммоль) растворяют в 2 мл безводного дихлорметана и перемешивают на магнитной мешалке при 0°С в течение 1 часа. Выпавшую мета-хлорбензойную кислоту отфильтровывают, промывают холодным безводным дихлорметаном (2×2 мл), добавляют к фильтрату 87 мкл диизопропилэтиламина (0.5 ммоль) и перемешивают при комнатной температуре в течение 20 часов (контроль ТСХ). По окончании реакции к реакционной смеси добавляют 0.055 г NaHCO3 (0.65 ммоль), перемешивают 5 мин при кипячении, растворитель удаляют при пониженном давлении. Целевой (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-он очищают методом колоночной хроматографии на силикагеле марки КСК (производства ООО Сорбполимер) фракция 5-40 мкм, элюент - хлористый метилен:петролейный эфир (1:5). Выход 14% (0.029 г).
В таблице 2 приведены данные о влиянии условий проведения реакции на выход (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-она (примеры 1-6).
Как видно из таблицы 2, результат, а именно, получение (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-она, может быть достигнут при использовании трифторуксусной кислоты в качестве катализатора. Оптимальным количеством используемой кислоты является 10 мольных %. Снижение количества кислоты приводит к снижению выхода соответствующего продукта, тогда как ее увеличение не приводит к заметному увеличению выхода соответствующего продукта. Присутствие кислоты является необходимым фактором для осуществления превращения. Использование основания в качестве катализатора не позволяет получить продукт с высоким выходом.
Таблица X - Влияние реакционных условий на выход (Z)-4-{3-фенил-1-[(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-она 1а.

Методом 1 получен ряд производных [(4-метилфенил)сульфонил]-1H-индол-2-ил}бут-3-ен-2-онов 1а-к с выходами 38-90%.