Результат интеллектуальной деятельности: КЛЕТОЧНАЯ ЛИНИЯ ВЕРЕТЕНОКЛЕТОЧНОЙ САРКОМЫ МЫШИ 164 MSar FE
Вид РИД
Изобретение
Изобретение относится к области биотехнологии. Полученная новая клеточная линия веретеноклеточной саркомы мыши 164 MSar FE обладает стабильными морфологическими и культуральными характеристиками. Данная клеточная линия может использоваться в экспериментальной онкологии для создания перевивной модели саркомы мягких тканей мыши, пригодна для лабораторных исследований с целью разработки диагностических наборов и тест-систем для определения активности фармацевтических препаратов. Клеточная линия депонирована в Специализированной коллекции культур клеток позвоночных Российской коллекции клеточных культур под регистрационным номером РККК (П) 803 Д.
Саркомы мягких тканей (СМТ) являются редкими и гетерогенными мезенхимальными злокачественными новообразованиями, насчитывающими более чем 100 гистологических подтипов. В России ежегодно регистрируется около 10000 новых случаев возникновения СМТ, что составляет 1% всех злокачественных новообразований [Бенберин В.В., Байзаков Б.Т., Шаназаров Н.А., Зинченко СВ. Саркомы мягких тканей - современный взгляд на проблему // Вестник Авиценны.- 2019. - Т. 21(2):291-7. http://dx.doi.org/10.25 005/2074-0581-2019-21-2-291-297]. Заболеваемость составляет 30 случаев на 1000000 населения, при этом в детском возрасте частота выше и составляет 6,5%, занимая 5 место по заболеваемости и смертности. СМТ часто характеризуются агрессивным течением и метастатическим процессом. Долгое время единственным способом лечения больных с саркомами мягких тканей являлся хирургический метод, который остается наиболее часто применяемым и сегодня. Прогресс химиотерапии и иммунотерапии несколько увеличил выживаемость пациентов с СМТ, однако, несмотря на проводимое лечение, около 80% рецидивов (как местных, так и отдаленных метастазов) возникает в первые два года после основного этапа лечения первичной опухоли [Bourcier К., Le Cesne A., Tselikas L., Adam J., Mir O., Honore C, de Baere T. Basic Knowledge in Soft Tissue Sarcoma // Cardiovasc Intervent Radiol. - 2019. - Vol. 42(9):1255-1261. doi:10.1007/s00270-019-02259-w].
Можно констатировать, что на современном этапе развития онкологии саркомы мягких тканей представляют собой плохо изученную группу злокачественных новообразований человека. Лечение этой патологии, безусловно, требует мультидисциплинарного подхода. Совершенствование имеющихся подходов к лечению СМТ и разработка новых требует применения модельных систем в контексте предклинических испытаний. Создание животных моделей, позволяющих вести экспериментальную работу in vivo, является важной составляющей этих исследований, так как развитие онкологии невозможно без постановки экспериментов, проведение которых на человеке недопустимо. Выбор для исследования подходящей модели имеет исключительно важное значение, потому что полученные на ней данные можно переносить в клинику, если модель в определенной степени адекватна опухоли человека.
Среди моделей опухолей, используемых в онкологии, наиболее многочисленную группу составляют перевиваемые опухоли, которые обладают рядом преимуществ перед химически индуцированными: отсутствие канцерогена - фактора риска для других животных и персонала, и его воздействия на поведение самой опухоли. Кроме того, можно получать в короткие сроки запланированное для исследований количество опухолей, что делает возможным постановку эксперимента с большим числом сравниваемых групп животных, при этом получаются более воспроизводимые и статистически достоверные результаты, причем на общем меньшем числе животных.
Перевиваемые саркомы мягких тканей мышей немногочисленны; наиболее известна саркома S3 7, впервые использованная в 30-х годах 20-го века [Hewitt Н. Studies of the Quantitative Transplantation of Mouse Sarcoma // Br J Cancer. - 1953. - 7(3), 367-383. doi: 10.1038/bjc.l953.35] и до сих пор активно использующаяся отечественными исследователями в качестве экспериментальной модели [Петриев В.М., Тищенко В.К., Сморызанова О.А., Михайловская А.А., Больбит Н.М., Дуфлот В.Р., Гайворонский А.В., Морозова Н.Б., Якубовская Р.И. Новый радиофармпрепарат на основе термочувствительного полимера и 153Sm для локальной радионуклидной терапии солидных опухолей // Радиация и риск (Бюллетень НРЭР). - 2018. -№1 - С. 66-76. doi: 10.21870/0131-3878-2018-27-1-66-76; Шульгина О.Г., Бахтин А.В., Селютина О.Н., Златник Е.Ю., Закора Г.И., Сидоренко И.П., Сустретов В.А. Влияние функционализированных углеродных нанотрубок на жизнеспособность опухолевых клеток in vitro и in vivo // Современные проблемы науки и образования. - 2015. - №3. https://science-education.ru/ru/article/view?id=19714].
К недостаткам данной модели можно отнести возможность культивирования только в асцитической жидкости живых животных (поддержки только в виде штамма), поскольку при культивировании in vitro изменяется морфология клеток и замедляется рост [Lasnitzki I. The behaviour of ascites tumour cells in vitro and in vivo. Br J Cancer. 1953 Jun;7(2):238-49. doi: 10.1038/bjc.l953.22. PMID: 13081904; PMCID: PMC2007889.], а также тот факт, что в опухолевые клетках данного штамма персистируют онковирусы [Bather R. Observations on murine monocytic leukaemia induced by a virus isolated from S37 sarcoma. Br J Cancer. 1961 Mar; 15(1):114-9. doi: 10.1038/bjc.l961.12. PMID: 13687745; PMCID: РМС2071118]. Таким образом, экспериментальная модель на основе штамма S3 7 in vivo соответствует лишь небольшой части сарком мягких тканей человека, вызываемых вирусами; кроме того, затруднена стандартизация штаммов из различных источников.
Техническим результатом изобретения является расширение арсенала клеточных линий опухолевых клеток лабораторных животных, используемых для моделирования опухолевого процесса с целью изучения закономерностей роста сарком мягких тканей в экспериментальных условиях. Кроме того, полученная новая клеточная линия может использоваться для тестирования активности различных фармацевтических препаратов, создания диагностических наборов и тест-систем для разработки новых терапевтических подходов и лекарственных средств.
Указанный технический результат достигается тем, что получена новая клеточная линия 164 MSar FE из опухолевого образца саркомы мягких тканей мыши, индуцированной бензо(а)пиреном. Полученная клеточная линия 164 MSar FE обладает стабильными культуральными и морфологическими характеристиками и хранится в Специализированной коллекции культур клеток позвоночных Российской коллекции клеточных культур под регистрационным номером РККК (П) 803Д.
Клеточная линия выделена из индуцированной бензо(а)пиреном ветереноклеточной саркомы мягких тканей мыши Balb/c. Материал получен при хирургическом удалении опухолевого узла.
Получение клеточной линии 164 MSar FE осуществлено следующим образом.
Опухолевая ткань получена хирургическим путем. Измельченные стерильным скальпелем образцы опухоли (1-3 мм2) подвергали механической дезагрегации в автоматическом режиме, помещая их на стерильные ножи, в течение 30 с - 1 мин. Полученную суспензию клеток пропускали последовательно через стерильные нейлоновые фильтры 100 мкм, 70 мкм, 50 мкм, суспендировали в полной среде и переносили в культуральную посуду, в которой осуществляли культивирование в течение длительного времени. Стабильно растущая клеточная линия была получена на 100 пассаже.
Морфологические признаки клеточной линии 164 MSar FE характеризуются следующим образом.
Культура представлена клетками преимущественно веретеновидной формы, среди которых встречаются клетки округлой формы меньшего размера. При формировании конфлюэнтного монослоя наблюдается тенденция к образованию радиальных скоплений.
Культуральные свойства клеточной линии 164 MSar FE представлены следующим образом.
Клеточная линия культивируется в питательной среде DMEM/F12 с добавлением 20% эмбриональной телячьей сыворотки, глутамина, инсулина (5 мкг/мл), трансферрина (5 мкг/мл), селена (5 нг/мл), пенициллина (100 ед/мл), стрептомицина (100 мкг/мл). Культивирование осуществляется при 37°С, 5% СО2, 100% влажности. Культура имеет адгезионный монослойный тип роста. Во флаконы объемом 25 см2 в 5 мл среды засевают 1×106 клеток. Пересев 1 раз в неделю в соотношении 1:2 с использованием равных объемов 0,25% раствора трипсина и 0,02% раствора версена.
Видовая принадлежность клеточной линии 164 MSar FE подтверждена с помощью кариологического анализа. Клетки опухоли мыши.
Кариологический анализ выявил высокую гетерогенность клеточной культуры: клеточная популяция распадается на 4 клона, также выявляются одиночные кариотипы:
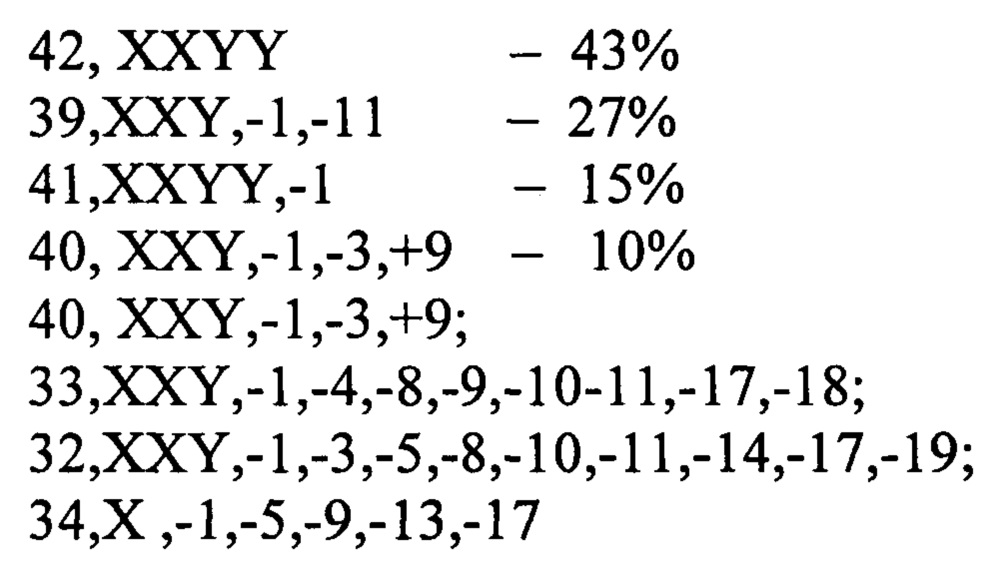
Условия криоконсервации следующие.
Для длительного хранения клетки консервируют путем замораживания в жидком азоте. Криосреда: DMEM/F12 50%, эмбриональная телячья сыворотка 40%, DMSO 10%; 3×106 клеток/мл на ампулу. Клетки клеточной линии ресуспендируют в среде для замораживания. Режим замораживания: жидкий азот, снижение температуры на 1°С в минуту до -25°С, затем быстрое замораживание до минус 70°С. Хранение в жидком азоте при температуре -196°С. Размораживание быстрое, при 37°С. Клетки разводят в 10 мл бессывороточной среды и осаждают центрифугированием, ресуспендируют в 5 мл той же среды, содержащей 20% эмбриональной телячьей сыворотки, и переносят в культуральный флакон объемом 25 см2. Жизнеспособность клеток оценивают по включению трепанового синего. Жизнеспособность клеток после криоконсервации составляет 87%.
Контаминация исследована следующим образом.
При длительном наблюдении бактерии и грибы в культуре не обнаружены. Методом ПЦР с использованием тест системы Мусо Real-Time (Евроген, Россия) были проведены исследования на наличие ДНК микроорганизмов класса Mollicutes, в т.ч. наиболее часто встречающихся в лабораторных условиях контаминантов клеточных культур: Mycoplasma orale, М. arginini, М. fermentans, М. hominis, М. hyorhinis, М. gallisepticum, М. genitalium, М. penetrans, М. pneumonia, М. salivarium и Acholeplasma laidlawii. Тест на микоплазму отрицателен.
Использование клеточной линии 164 MSar FE представлено следующими примерами.
Пример 1. Использование клеточной линии 164 MSar FE для создания модели перевивной саркомы мыши
1. Клеточную линию 164 MSar FE культивировали в пластиковых флаконах в полной питательной среде DMEM/F12 с добавлением 20% эмбриональной сыворотки крупного рогатого скота, глутамина, инсулина (5 мкг/мл), трансферрина (5 мкг/мл), селена (5 нг/мл), пенициллина (100 ед/мл), стрептомицина (100 мкг/мл). Культивирование осуществляли при 37°С, 5% СO2, 100% влажности в СО2-инкубаторе «Heracel» (Termo Electron LTD GmbH, Германия).
2. Сорока пяти мышам-самкам линии BALB/C в возрасте 3 месяцев инокулировали клеточную линию 164 MSar FE (72 пассаж) подкожно в правый бок в количестве 0,15 мл (3,2 × 106 клеток/мышь). Получена 100% перевиваемость клеточной культуры.
3. По достижении опухолью размера от 0,17 до 0,85 см3 (18-21 день от перевивки культуры) животные были рандомизированы в группы по 15 особей: контроль, терапия доксорубицином в дозе 4 мг/кг, однократно внутрибрюшинно, терапия циклофосфамидом в дозе 300 мг/кг однократно внутрибрюшинно.
4. Через 21 день от начала терапии были получено 81% торможение роста перевиваемой саркомы 164 MSar FE при воздействии циклофосфамида и 79% торможение при воздействии доксорубицина, что подтверждает чувствительность модели к данным препаратам.
Преимущество модели веретеноклеточной саркомы мыши, ведущей свое происхождение от саркомы, индуцированной бенз(а)пиреном, заключается в том, что опухоль достигает размера, пригодного для тестирования противоопухолевых препаратов, в течение нескольких недель (в отличие от исходной индуцированной саркомы, для которой этот срок составляет 4-6 месяцев). В то же время, разработанная модель сохраняет гистологическое строение исходной саркомы и обладает сходными иммуногистохимическими характеристиками. Данная модель позволяет изучать in vivo особенности изменения микроокружения злокачественного новообразования в процессе лекарственной терапии, а также чувствительность опухоли к новым видам лекарственного воздействия.
Пример 2. Использование клеточной линии 164 Msar FE для создания модельной системы, позволяющей оценить чувствительность опухолевых клеток к цитостатикам
1. Клеточную линию 164 Msar FE культивировали, как описано выше. При достижении конфлюэнтного монослоя клетки снимали с субстрата с помощью равновесной смеси 0,25% раствора трипсина и 0,02% раствора версена.
2. Клетки отмывали дважды в полной культуральной среде, производили подсчет клеток и оценку их жизнеспособности.
3. Получали сфероиды линии 164 Msar FE методом предельных разведений. Для этого планшету с низкоадгезивной поверхностью лунок (BD Bioscience, США) помещали клетки в стартовой концентрации 104 кл/лунка в полной питательной среде и культивировали в течение 5-7 дней.
6. Для оценки химиочувствительности сфероиды линии 164 Msar FE помещали в 96-луночные планшеты (BD Bioscience, США) в 100 мкл раствора исследуемых химиопрепаратов.
7. В качестве химиотерапевтических агентов использовали ифосфамид, доксорубицин, дакарбазин. Добавляли химиотерапевтические агенты в конечной концентрации, соответствующей 10% пика концентрации в плазме крови больного (Salmon S.E., 1981)., с учетом различий в метаболизме мыши и человека. Продолжительность инкубации с химиотерапевтическими агентами соответствовала периоду полувыведения препарата из циркуляции.
8. В качестве положительного контроля использовали сфероиды линии 164 Msar FE без воздействия.
9. Сфероиды культивировали в экспериментально системе в течение 24 ч, затем подвергали ферментативной диссоциации, окрашивали DAPI и анализировали с помощью проточного цитофлуориметра.
10. Обнаружили, что что клетки сфероидов линии 164 Msar FE чувствительны к доксорубицину согласно данным анализа на проточном цитофлуориметре. При воздействии доксорубицина в концентрации, эквивалентной терапевтической, жизнеспособность клеток 164 Msar FE составила 38,6%, циклофосфамида - 75,6% и их комбинации - 48,6%.
Новая клеточная линия веретеноклеточной саркомы мыши 164 MSar FE расширяет арсенал клеточных линий опухолевых клеток лабораторных животных, используемых для моделирования опухолевого процесса с целью изучения закономерностей роста сарком мягких тканей в экспериментальных условиях, может использоваться для тестирования активности различных фармацевтических препаратов, создания диагностических наборов и тест-систем для разработки новых терапевтических подходов и лекарственных средств.
Клеточная линия веретеноклеточной саркомы мыши 164 Msar FE, используемая для создания перевивной модели саркомы мягких тканей мыши и тестирования противоопухолевых препаратов, хранится в Специализированной коллекции культур клеток позвоночных Российской коллекции клеточных культур под регистрационным номером РККК (П) 803Д.
