Результат интеллектуальной деятельности: СПОСОБ ДВУХЭТАПНОЙ БИОИНЖЕНЕРНОЙ РЕКОНСТРУКЦИИ ВЕРХНИХ ПИЩЕВАРИТЕЛЬНЫХ ПУТЕЙ
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к онкологии, в частности для устранения дефектов верхних отделов пищеварительного тракта, после удаления местно-распространенных опухолей.
Известен способ фарингопластики в условиях дефицита пластического материала, при котором пластику гортаноглотки и шейного отдела пищевода, мягких тканей шеи осуществляют с помощью висцерального тонкокишечно-брыжеечного трансплантата (RU 2427339 C1). Пластику гортаноглотки и шейного отдела пищевода осуществляют с помощью единого висцерального тонкокишечно-брыжеечного трансплантата с сохранением брыжейки в полном объеме. Анастомозируют питающие трансплантат сосуды с сосудами шеи. Кишечный фрагмент лоскута укладывают в позиции гортаноглотки так, чтобы его противобрыжеечный край располагался относительно средней линии шеи по другую сторону от зоны микрососудистых анастомозов. Формируют дистальный анастомоз между кишечной трубкой аутотрансплантата и шейным отделом пищевода. «Г-образно» складывают оральный фрагмент кишки, используя ее естественные изгибы так, чтобы длина горизонтально расположенной части кишечного фрагмента соответствовала величине диаметра просвета ротоглотки. Накладывают фиксирующий шов между углом кишечного фрагмента и прилежащей стенкой ротоглотки. Клинообразно иссекают фрагмент стенки кишечной составляющей аутотрансплантата по его противобрыжеечному краю в зоне оростомы. Формируют проксимальный анастомоз между кишечной трубкой и ротоглоткой. Затем брыжеечным фрагментом лоскута изолируют линии швов в области органных и микрососудистых анастомозов. Фрагментами брыжейки, прилежащими к ротоглотке, укрывают проксимальный анастомоз с кишкой и микрососудистые анастомозы. Оставшейся прядью брыжейки изолируют зону пищеводно-кишечного соустья и средостение. Использование данного изобретения позволяет восстановить целостность органов проксимального отдела пищеварительного тракта.
Однако использование данного способа фарингопластики возможно только у соматически сохранных пациентов, ограничено сопутствующей патологией донорских органов и ранее произведенными вмешательствами на органах брюшной полости, возможно только в специализированных центрах при наличии оборудования и персонала, владеющего знаниями и практическими навыками микрохирургических операций.
Известен способ восстановления тканей орофарингеальной области префабрицированными аутотрансплантатами у онкологических больных (Ребрикова И.В. / восстановление тканей орофарингеальной области префабрицированными аутотрансплантатами у онкологических больных // Экспериментально-клиническое исследование. // Автореферат диссертации на соискание ученой степени к.м.н., 2015). Реконструкцию тканей орофарингеальной области осуществляют префабрицированными лоскутами с восстановлением слизистой оболочки и мягкотканого компонента, а также функционально достаточного объема и формы органа. Производят забор микрографтов слизистой оболочки твердого неба в пределах слизистого слоя размерами 1-3 мм, которые отмывают в физиологическом растворе. Далее после осуществления операционного доступа согласно разметке на площади, соответствующей размеру дефекта слизистой оболочки, на фасцию мышцы имплантируют и фиксируют микрографты слизистой оболочки, которые укрывают резорбируемой викриловой сеткой с фиксируют ее по периметру. Далее трансплантат изолируют стерильной полиэтиленовой пленкой, которую фиксируют по периметру. Рану послойно ушивают наглухо с оставлением силиконового дренажа. При выполнении реконструктивного этапа перемещенными префабрицированными лоскутами после осуществления операционного доступа и после удаления полиэтиленовой пленки, во всех случаях в зоне ранее произведенной имплантации микрографтов слизистой оболочки выявляли вновь образованную ткань на фасции мышцы. Соответственно размеру дефекта формировали мышечный лоскут с предварительно имплантированной слизистой, в ряде случаев из волокон большой грудной мышцы на питающих торако-акромиальных сосудах, в ряде случаев из волокон широчайшей мышцы спины на питающих торако-дорзальных сосудах. Сформированный префабрицированный мышечный лоскут перемещали на область дефекта. Восстановление слизистой оболочки осуществляли префабрицированным фрагментом лоскута, мягкотканый дефект орофарингеальной зоны замещали мышечной порцией лоскута.
Однако известный способ префабрикации лоскутов при орофарингопластики является достаточно трудоемким и результат зависит от качества его выполнения.
В качестве прототипа выбран способ реконструкции верхних дыхательных путей с использованием тканевого эквивалента у онкологических больных (Батухтина Е.В. / Реконструкция верхних дыхательных путей с использованием тканевого эквивалента у онкологических больных. Клинико-экспериментальное исследование // Автореферат диссертации на соискание ученой степени к.м.н., 2006). Реконструкцию верхних пищеварительных путей осуществляют в два этапа. На первом этапе выполняют префабрикацию лоскута путем имплантации аллогенного тканевого эквивалента слизистой оболочки на волокна большой грудной мышцы. Реконструктивный этап осуществляют в сроки от 7 суток до 30 дней после имплантации тканевого эквивалента. Восстановление мягкотканого дефекта фарингеальной зоны осуществляют мышечной порцией лоскута, слизистую оболочку восстанавливают тканевым эквивалентом. Лоскут послойно фиксируют по периметру дефекта узловыми швами. Тканевая культура, включающая коллагеновый гель, аллогенную клеточную культуру фибробластов и эпидермальных кератиноцитов, являясь эквивалентом слизистой оболочки и закрывая ее дефект, оказывает непосредственное влияние на заживление и эпителизацию раны. Преимуществом методики является то, что реконструкцию верхних пищеварительных путей осуществляют с восстановлением всех составляющих элементов органа, включая мышечный каркас, эпителиальную выстилку, а также функционально достаточного объема и формы органа.
Однако, известный способ имеет ряд недостатков, таких как: применение тканевого эквивалента изготовленного на подложке из коллагенового геля связано с техническими трудностями, обусловленными тем, что гель, как основа трансплантируемого эквивалента не имеет плотной структуры, требует для своей фиксации дополнительно вносимой викриловой сетчатой структуры, его технически сложно переносить на мышцу, сложно крепить к подлежащим тканям, в результате чего увеличивается риск смещения и нарушения целостности трансплантируемой конструкции. Применение в качестве клеточной составляющей донорских (аллогенных) клеток снижает эффективность приживления тканевого эквивалента в организме реципиента, и в данном случае трансплантат выполняет роль временно выстраивающегося эпителиального покрытия, которое в течение нескольких недель элиминируется, стимулируя миграцию собственных клеток пациентов область дефекта. Данный механизм у больных с ослабленной в результате противоопухолевого лечения динамикой пролиферации, миграции и регенерации собственных тканей может не давать эффекта и снижать процент успешности применения трансплантата. Кроме этого, фибробласты, которые входят в состав аллогенного тканевого эквивалента, могут способствовать контракции и развитию грануляций, что при устранении дефектов глотки и пищевода повышает риск таких осложнений, как образование стриктур и к стенозам просвета.
Техническим результатом предложенного изобретения является разработка способа реконструкции верхних пищеварительных путей, с использованием перемещенного пекторального лоскута и аутологичного тканевого эквивалента слизистой оболочки.
Тканевой эквивалент слизистой оболочки представляет собой слой собственных эпителиальных клеток пациента (кератиноцитов кожи или клеток букального эпителия) помещенных на биосовместимую эластичную тонкую пленку, состоящую из комплекса пептидов и/или гиалуроновой кислоты.
Технический результат достигается тем, что также как и в известном способе на первом этапе выполняют префабрикацию лоскута путем имплантации тканевого эквивалента на фасцию большой грудной мышцы, на втором этапе выполняют фарингопластику перемещенным пекторальным префабрицированным лоскутом с восстановлением внутренней выстилки верхних пищеварительных путей.
Особенностью заявляемого способа является то, что из фрагментов эпителиальной ткани пациента, полученную путем биопсии фрагмента кожи размером 1×1 см или слизистой оболочки полости рта размером 0,5×0,5 см, выделяют «in vitro» эпителиальные клетки и культивируют их для увеличения клеточной массы, затем выращенные клетки переносят на поверхность биосовместимой матрицы и формируют эпителиальный слой, созданный, таким образом аутологичный тканевый эквивалент слизистой оболочки, имплантируют на фасцию большой грудной мышцы клеточным слоем вверх и фиксируют нитью, затем мышцу с закрепленным на ней тканевым эквивалентом изолируют пленкой, рану послойно ушивают, а созданный аутологичный тканевый эквивалент оставляют на мышце пациента на 3-4 недели, и когда на фасции сформируется слизистая оболочка, выполняют отсроченную фарингопластику: производят разрез кожи в левой субмаммарой области, кожно-жировые лоскуты мобилизуют и разводят, кожно-жировой лоскут отсепаровывают от большой грудной мышцы, пленку удаляют и формируют мышечный лоскут с включением большой грудной мышцы на торакоакромиальных сосудах, далее производят разрез, окаймляющий фарингостому на границе кожи и слизистой, при этом края кожи и слизистой мобилизуют, а сформированный префабрицированный мышечный лоскут перемещают на область дефекта, далее префабрицированный фрагмент лоскута сшивают по периметру с краями слизистой оболочки фарингостомы отдельными узловыми швами, мышечной порцией лоскута дополнительно укрывают швы по периметру фарингостомы, мягкие ткани шеи восстанавливают мышечной порцией перемещенного лоскута и фиксируют отдельными узловыми швами, рану шеи ушивают с оставлением силиконового дренажа в подлоскутном пространстве слева, после чего донорскую рану послойно ушивают с оставлением двух силиконовых дренажей.
В заявленном способе тканевой эквивалент, в отличие от прототипа, не содержит фибробластов, что предотвращает развитие грануляций и стенозов. Аутологичные эпителиальные клетки, в отличие от аллогенных, не элиминируются после трансплантации, а встраиваются в подлежащие ткани с последующим формированием эпителиальной выстилки на фасции мышцы на необходимой для устранения дефекта слизистой оболочки площади, что сокращает время восстановления органа после реконструкции. Отличием от прототипа является то, что созданный тканевой эквивалент на основе биосовместимой матрицы состоит из комплекса пептидов и/или гиалуроновой кислоты, т.к. формируется на поверхности мышечной ткани и базальной мембраны покровных тканей и обладает эластичностью, механической прочностью, что упрощает его трансплантацию на мышцу.
Изобретение поясняется подробным описанием, клиническим примером и иллюстрациями, на которых изображено:
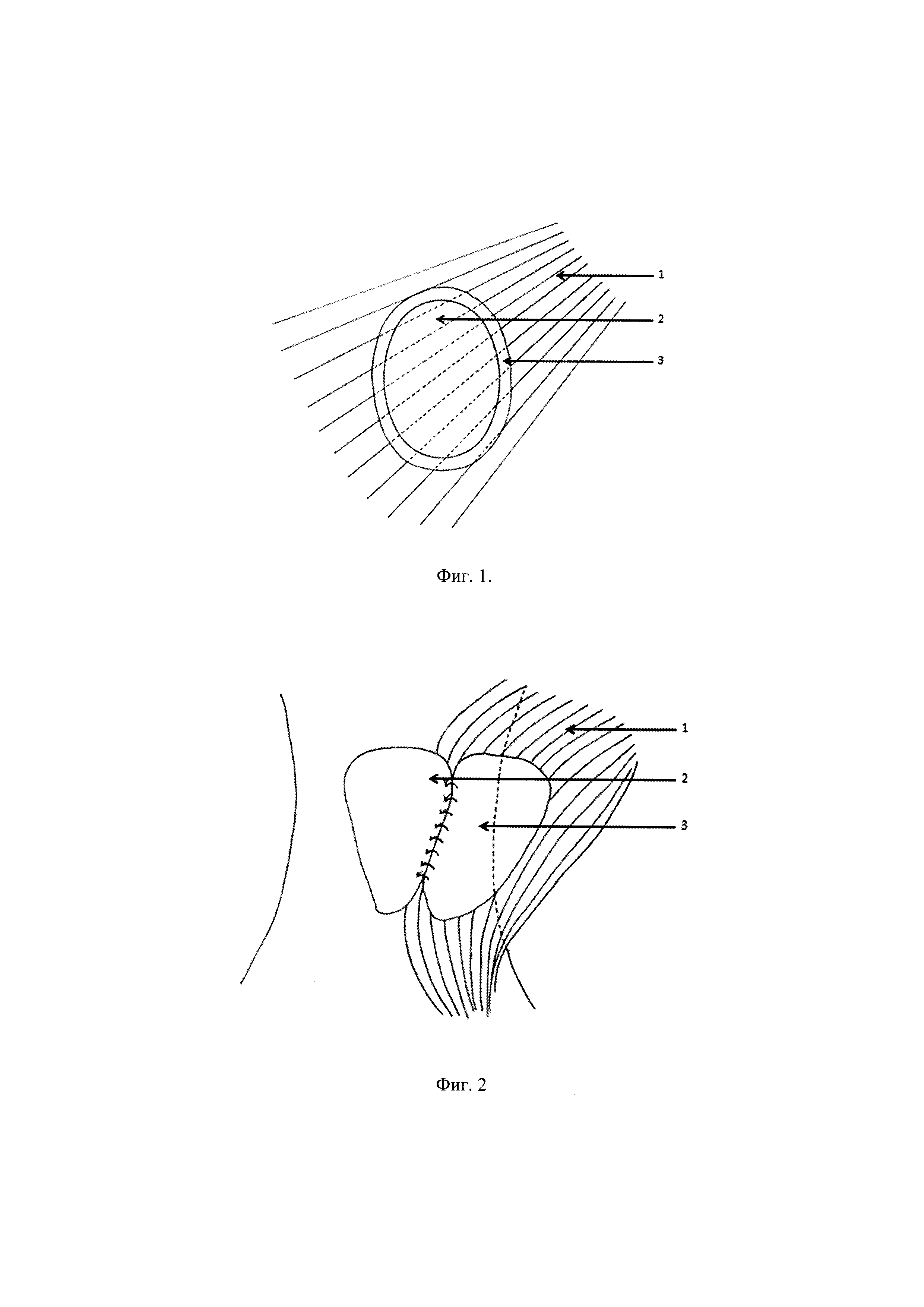
Фиг. 1 - Схема префабрикации биоинженерного лоскута; 1 - волокна большой грудной мышцы, 2 - тканевой эквивалент слизистой оболочки, 3 - пленка;
Фиг. 2 - Схема фарингопластики перемещенным префабрицированным пекторальным лоскутом: 1 - волокна большой грудной мышцы, 2 - фарингостома, 3 - префабрицированный фрагмент лоскута (область ранее имплантированного тканевого эквивалента);
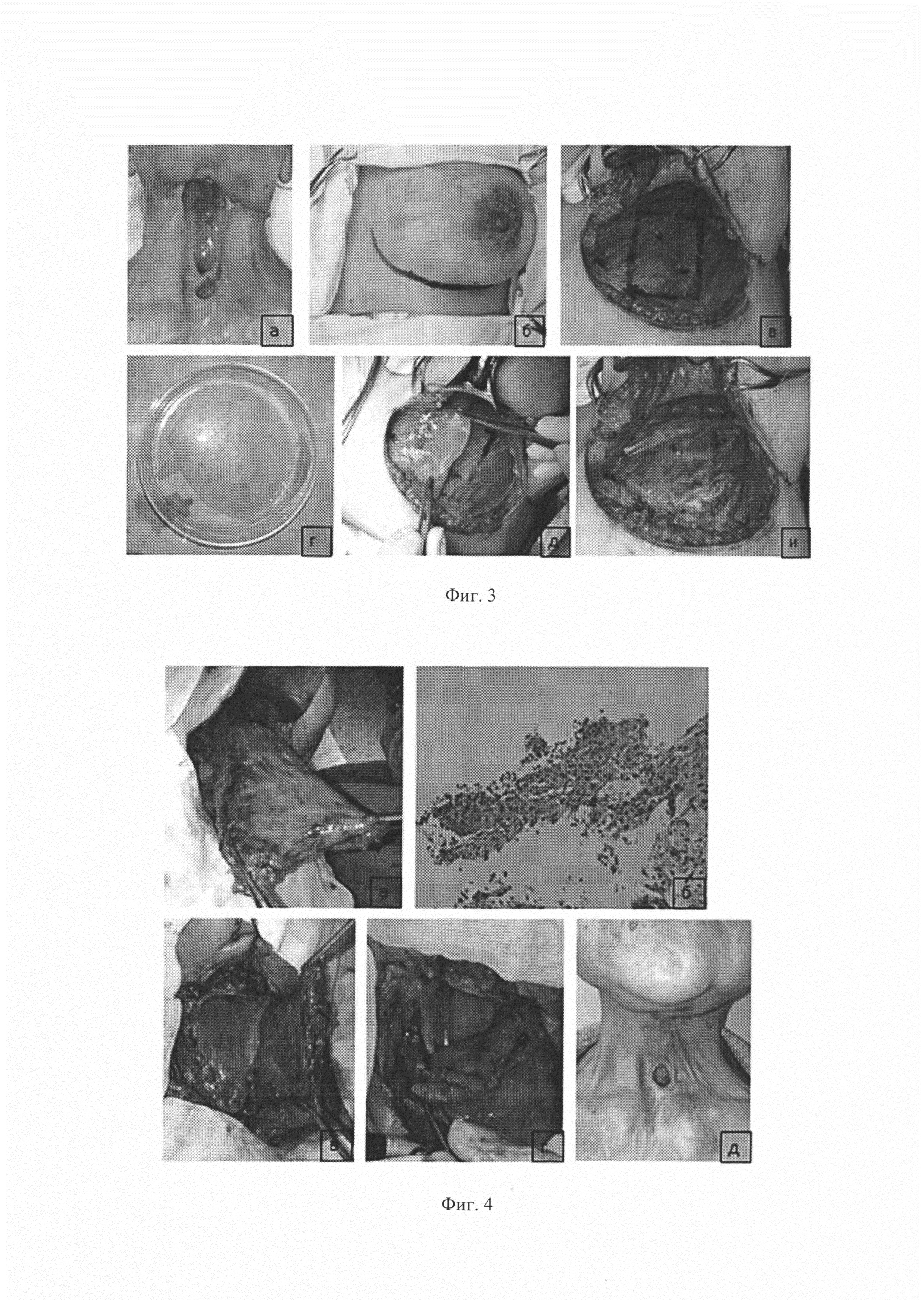
Фиг. 3 - Префабрикация биоинженерного пекторального лоскута: а) фарингостома, б) разметка доступа в субмаммарной области, в) - разметка области имплантации тканевого эквивалента на фасцию большой грудной мышцы, г) - тканевой эквивалент слизистой оболочки, д) - имплантация тканевого эквивалента слизистой оболочки на фасцию большой грудной мышцы, е) изоляция имплантированного тканевого эквивалента пленкой.
Фиг. 4 - Фарингопластика: а) сформированный префабрицированный биоинженерный пекторальный лоскут, б) - гистологическое исследование биопсийного материала префабрицированного фрагмента лоскута, окраска Гематоксилин и Эозин, ув х 200, в), г) - этапы фарингопластики, д) - окончательный вид раны шеи.
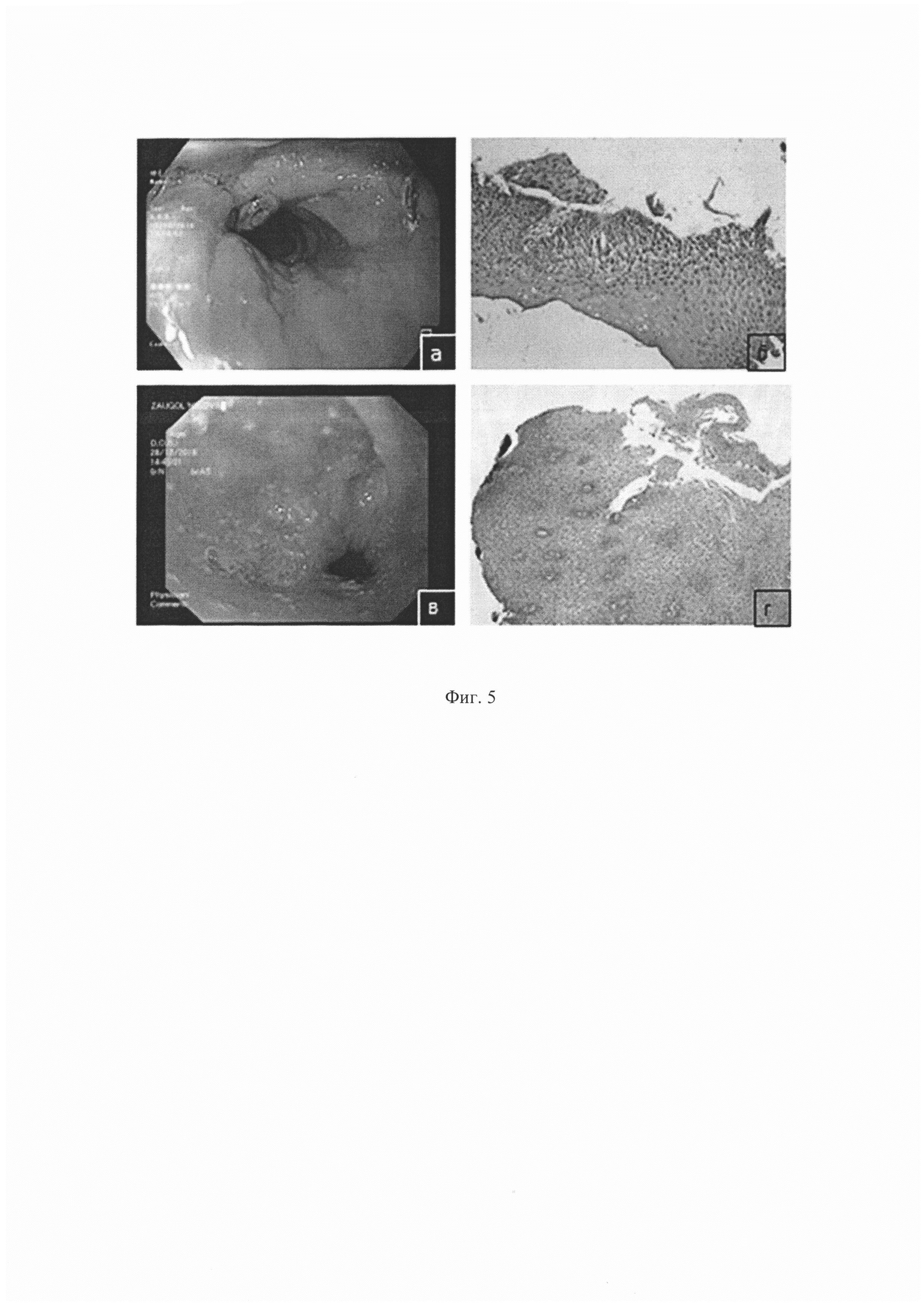
Фиг. 5 - а) - вид глотки при видеофарингоэзофагоскопии через 1,5 месяца, б) - гистологическое исследование биопсийного материала префабрицированного фрагмента лоскута, окраска Гематоксилин и Эозин, ув х 100, в) - вид глотки при видеофарингоэзофагоскопии через 5 месяцев, б) - гистологическое исследование биопсийного материала префабрицированного фрагмента лоскута, окраска Гематоксилин и Эозин, ув х 100.
Способ осуществляют следующим образом.
Под местной анестезией выполняют резекцию фрагмента эпителиальной ткани пациента (возможно использование биоптата слизистой ротовой полости или эпидермиса кожи пациента) размерами 1×1 см с последующим ушиванием раны. В лабораторных условиях «in vitro» из полученного фрагмента выполняют выделение эпителиальных клеток их культивируют для увеличения клеточной массы, необходимом для закрытия дефекта верхних пищеварительных путей у пациента. Затем выращенные клетки переносят на поверхность биосовместимой матрицы, сформированной по форме и размеру в соответствии с дефектом верхних пищеварительных путей у пациента, где клетки формируют эпителиальный слой. Далее, созданного таким образом эквивалент слизистой, переносят на мышцу и выполняют этап префабрикации лоскута.
I этап реконструкции: префабрикация лоскута (фиг. 1).
Производят разрез в субмаммарной складке. Кожно-жировой лоскут над большой грудной мышцей мобилизуют .На фасцию большой грудной мышцы слева имплантируют тканевой эквивалент слизистой оболочки, фиксируют по периметру нитью - монокрил №4. Сверху тканевой эквивалент изолируют полиэтиленовой пленкой, фиксированной по периметру нитью - пролен №3. Выполняют послойное ушивание раны с оставлением силиконового дренажа. Спирт, ас. повязка.
II этап реконструкции: отсроченная фарингопластика (фиг. 2).
Выполняют через 3-4 недели после префабрикации. Под ЭТН произведен разрез кожи в левой субмаммарой области. Кожно-жировые лоскуты мобилизуют, разводят. Кожно-жировой лоскут отсепаровывают от большой грудной мышцы. Пленку удаляют. Производят оценку области имплантации тканевого эквивалента. В большинстве случаев выявляется разрастание ткани в виде отдельных фрагментов на гладком блестящем слое. Формируют мышечный лоскут с включением большой грудной мышцы на торакоакромиальных сосудах. Далее производят разрез, окаймляющий фарингостому на границе кожи и слизистой. Края кожи и слизистой мобилизуют. Сформированный префабрицированный мышечный лоскут перемещают на область дефекта. Префабрицированный фрагмент лоскута (область ранее имплантированного тканевого эквивалента) сшивают по периметру с краями слизистой оболочки фарингостомы отдельными узловыми швами. Мышечной порцией лоскута дополнительно укрывают швы по периметру фарингостомы. Мягкие ткани шеи восстанавливают мышечной порцией перемещенного лоскута, который фиксируют отдельными узловыми швами. Рану шеи ушивают с оставлением силиконового дренажа в подлоскутном пространстве слева. Донорскую рану ушивают послойно наглухо с оставлением 2х силиконовых дренажей. Переинтубация на трахеостомическую трубку.
Клинический пример.
Пациентка З., 59 лет. Клинический диагноз: рак гортани IVA ст. ypT3N2cM0. Комбинированное лечение (хирургическое лечение (ларингэктомия с резекцией гортаноглотки и мягких тканей шеи, лимфаденэктомия на шее справа) 17.10.2017 г., (лимфаденэктомия на шее слева) 23.11.2017., лучевая терапия СОД 50 Гр 02-03.2018 г.). Фарингостома. Трахеостома. Гастростома. Без рецидива и метастазов (С 32).
Сопутствующий диагноз: ЖКБ, холецистэктомия в 2009 г.
При осмотре: при осмотре конфигурация шеи изменена за счет проведенного ранее хирургического лечения. Гортань с передними отделами гортаноглотки, мягкими тканями шеи удалены ранее. Имеется фарингостома с сохраненной задней стенкой гортаноглотки (фиг 3а). Фарингостома сформирована удовлетоврительно, слизистая оболочка розовая, визуально и пальпатороно без опухолевой патологии. В нижней трети шеи - трахеостома диаметром 1,5 см, слизистая розовая, визуально и пальпаторно без опухолевой патологии. В области шеи справа и слева гиперемия кожных покровов от уровня нижней челюсти до уровня ключиц, отек мягких тканей (постлучевые реакции). На фоне послеоперационных рубцов и отека пальпаторно и визуально опухолевой патологии не определяется. Питание через гастростому.
По данным комплексного обследования данных за рецидив и метастазирование не получено.
Учитывая перенесенные ранее операции, в том числе лимфаденэктомии на шее справа и слева, невозможность выполнить микрохирургическую реконструкцию, принято решение о выполнении пациентке реконструкции по описанной методике.
Под местной анестезией раствором новокаина 0,5% выполнена биопсия кожи затылочной области размерами 1×1 см. Фрагмент кожи помещен в стерильных условиях в среду. Выполнено выделение, культивирование эпидермальных кератиноцитов «in vitro». Выполнена посадка и культивирование клеток на носителе G-derm, площадь носителя соответствует дефекту слизистой оболочки глотки (фиг. 3г).
Выполнен I этап реконструкции - префабрикация лоскута.
Ход операции: под ЭТН произведен разрез в субмаммарной складке (фиг. 3б). Кожно-жировой лоскут над большой грудной мышцей мобилизован (фиг. 3в). На фасцию большой грудной мышцы слева имплантирован тканевой эквивалент слизистой оболочки, фиксирован по периметру нитью - монокрил №4 (фиг. 3д). Сверху тканевой эквивалент изолирован полиэтиленовой пленкой, фиксированной по периметру нитью - пролен №3 (фиг. 3и). Выполнено послойное ушивание раны с оставлением силиконового дренажа. Спиртовая асептическая повязка.
Через 4 недели после префабрикации выполнен II этап реконструкции - отсроченная фарингопластика.
Ход операции: под ЭТН произведен разрез кожи в левой субмаммарой области. Кожно-жировые лоскуты мобилизованы, разведены. Кожно-жировой лоскут отсепарован от большой грудной мышцы. Пленка удалена. Выявлено разрастание ткани в виде отдельных фрагментов на гладком блестящем слое. Выполнена биопсия этой ткани, при гистологическом исследовании выявлен многослойный плоский эпителий (фиг. 4б). Сформирован мышечный лоскут с включением большой грудной мышцы слева на левых торакоакромиальных сосуда (фиг. 4а). Далее произведен разрез, окаймляющий фарингостому на границе кожи и слизистой. Края кожи и слизистой мобилизованы. Сформированный префабрицированный мышечный пекторальный лоскут перемещен на область дефекта (фиг. 4в). Префабрицированный фрагмент лоскута фиксировали по периметру с краями слизистой оболочки фарингостомы отдельными узловыми швами (фиг. 4г). Мышечной порцией лоскута дополнительно укрыт шов по периметру фарингостомы. Мягкие ткани шеи восстановлены мышечной порцией перемещенного лоскута, который фиксирован отдельными узловыми швами. Рана шеи ушита с оставлением силиконового дренажа в подлоскутном пространстве слева. Донорская рана ушита послойно наглухо с оставлением двух силиконовых дренажей. Наложена асептическая повязка. Переинтубация на трахеостомическую трубку.
В послеоперационном периоде выявлено развитие слюнного свища в верхней трети шеи слева на 7-е сутки, который самостоятельно закрылся на 14 сутки. Лоскут был жизнеспособный во всех отделах, адаптирован удовлетворительно. Донорская рана заживала первичным натяжением. В результате проведенной операции был устранен дефект глотки с восстановлением слизистой оболочки, мягких тканей перемещенным префабрицированным пекторальным биоинженерным лоскутом с восстановлением слизистой оболочки глотки тканевым эквивалентом слизистой оболочки, мягких тканей - пекторальным лоскутом.
Питание через рот восстановлено через 4 недели в полном объеме.
Через 4 месяца выполнена редукция избыточной порции пекторального лоскута в области прохождения сосудистой ножки, трахеопищеводное шунтирование с установкой голосового протеза (фиг. 4д). Пациентке восстановлена голосовая функция.
Область имплантации тканевого эквивалента через 4 недели имела вид розовой гладкой блестящей ткани, сходной визуально с окружающей слизистой оболочкой, визуализируется шовный материал (фиг. 5а). Выполнялась биопсия префабрицированного фрагмента трансплантата, при морфологическом исследовании биопсийного материала выявлен многослойный плоский неороговевающий эпителий (фиг. 5б).
Область имплантации тканевого эквивалента через 6 месяцев имела вид розовой гладкой блестящей ткани, сходной визуально с окружающей слизистой оболочкой (фиг. 5в). Выполнялась биопсия префабрицированного фрагмента трансплантата, при морфологическом исследовании биопсийного материала выявлен многослойный плоский неороговевающий эпителий (фиг. 5г).
Таким образом, предлагаемый способ может быть использован для устранения дефектов после удаления местно-распространенных опухолей с восстановлением эпителиальной выстилки, мягких тканей шеи.
Способ имеет социальный и медицинский эффект и позволяет:
- отсроченно устранить дефект верхних пищеварительных путей биоинженерным префабрицированным пекторальным лоскутом с восстановлением эпителиальной выстилки и мягких тканей;
- получить слизистую оболочку на фасции мышцы за счет имплантации аутологичного тканевого эквивалента слизистой оболочки;
- широко использовать метод в практике, т.к. тканевой эквивалент сформирован из аутологичных клеток;
- получить аутологичный тканевой эквивалент слизистой оболочки с эпителиальными аутологичными клетками на биосовместимом носителе с имитацией структуры базальной мембраны покровных тканей.
Способ двухэтапной биоинженерной реконструкции верхних пищеварительных путей, заключающийся в том, что на первом этапе выполняют префабрикацию лоскута путем имплантации тканевого эквивалента на фасцию большой грудной мышцы, на втором этапе выполняют фарингопластику перемещенным пекторальным префабрицированным лоскутом с восстановлением внутренней выстилки верхних пищеварительных путей, отличающийся тем, что из фрагментов эпителиальной ткани пациента, полученную путем биопсии фрагмента кожи размером 1×1 см или слизистой оболочки полости рта размером 0,5×0,5 см, выделяют «in vitro» эпителиальные клетки и культивируют их для увеличения клеточной массы, затем выращенные клетки переносят на поверхность биосовместимой матрицы и формируют эпителиальный слой, созданный таким образом аутологичный тканевый эквивалент слизистой оболочки имплантируют на фасцию большой грудной мышцы клеточным слоем вверх и фиксируют нитью, затем мышцу с закрепленным на ней тканевым эквивалентом изолируют пленкой, рану послойно ушивают, аутологичный тканевый эквивалент оставляют на мышце на 3-4 недели, и когда на фасции сформируется слизистая оболочка, выполняют отсроченную фарингопластику: производят разрез кожи в субмаммарой области, кожно-жировые лоскуты мобилизуют и разводят, кожно-жировой лоскут отсепаровывают от большой грудной мышцы, пленку удаляют и формируют мышечный лоскут с включением большой грудной мышцы на торакоакромиальных сосудах, далее производят разрез, окаймляющий фарингостому на границе кожи и слизистой, при этом края кожи и слизистой мобилизуют, а сформированный префабрицированный мышечный лоскут перемещают на область дефекта, далее префабрицированный фрагмент лоскута сшивают по периметру с краями слизистой оболочки фарингостомы отдельными узловыми швами, мышечной порцией лоскута дополнительно укрывают швы по периметру фарингостомы, мягкие ткани шеи восстанавливают мышечной порцией перемещенного лоскута и фиксируют отдельными узловыми швами, рану шеи ушивают с оставлением силиконового дренажа в подлоскутном пространстве слева, после чего донорскую рану послойно ушивают с оставлением двух силиконовых дренажей.