Результат интеллектуальной деятельности: СПОСОБ ЛЕЧЕНИЯ ПОРАЖЕНИЯ НЕРВНОЙ СИСТЕМЫ С ПОМОЩЬЮ РЕКОМБИНАНТНОЙ ГЛУТАМАТОКСАЛОАЦЕТАТТРАНСАМИНАЗЫ
Вид РИД
Изобретение
Область техники
Изобретение относится к области медицины, а именно к способу лечения поражений нейронов лекарственным средством, содержащим в своем составе рекомбинантную глутаматоксалоацетаттрансаминазу. Лекарственное средство действует в каскадах повреждения клеток головного мозга, вызванных различными причинами, где существенную роль играет внутриклеточный глутамат. Высвобождаясь из первоначально поврежденных клеток в межклеточное пространство, глутамат вызывает повреждение окружающих здоровых клеток, что приводит к их гибели и новому поступлению глутамата в окружающую тканью. Мишенью лекарственного средства является глутамат периферической крови. Глутаматоксалоацетаттрансаминаза превращает глутамат в нетоксичные кетоглутарат и аспартат. Механизм действия лекарственного средства заключается в трансаминировании глутамата периферической крови, приводящем к устранению избыточного токсического глутамата в ткани головного мозга и снижению объема поврежденной нервной ткани при ишемическом инсульте. Основное фармакологическое действие лекарственного средства - нейропротекторное.
Уровень техники
Сосудистые заболевания головного мозга и связанные с ним дегенеративно-дистрофические процессы сохраняют лидирующие позиции по уровню инвалидизации лиц пожилого и старческого возраста. До настоящего времени не разработано эффективных консервативных методов лечения и профилактики указанных серьезных заболеваний. Вместе с тем, установлена прямая зависимость между уровнем глутаминовой кислоты в экстрацеллюлярной жидкости тканей головного мозга и инсультом.
Недостаток питательных веществ в клетках нервной системы приводит к деполяризации мембраны нейронов и последующему массивному выбросу глутамата во внеклеточное пространство, что, в свою очередь, приводит к резкому нарушению работы глутаматных транспортеров, вызывая эксайтотоксическое действие и гибель нейронов.
Боковой амиотрофический склероз является смертельным заболеванием, характеризующимся поражением верхних и нижних мотонейронов. Симптомы ALS могут быть различными: бульбарный паралич, дизартрия, дисфагия, паралич дыхательных мышц и др. Несмотря на то, что причины, вызывающие данное заболевание для подавляющего числа пациентов, не могут быть установлены, в развитие бокового амиотрофическго склероза немалую роль играет эксайтотоксический глутамат.
Единственным лекарственным средством, применяемым для терапии бокового амиотрофическиого склероза, в настоящее время является рилузол. Данный препарат снижает глутаматный эксайтотоксичекий эффект, однако обладает эффективностью только в течение нескольких месяцев (Expert Opinion on Emerging Drugs (2011), vol. 16(2), p. 537-558). Поэтому задача эффективного и длительного лечения бокового амитрофического склероза остается актуальной задачей.
Глутаматоксалоацетаттрансаминаза снижает уровень глутамата в крови и в головном мозге. Изменение уровня глутамата прерывает «глутаматный эксайтотоксичекий каскад» и уменьшает объем повреждения нервной ткани (Neurochemical Research (2012), vol. 37(10), p. 2198-2205; J Biol Chem. (1999), vol. 274(45), p. 31891-31895; Journal of Biological Chemistry (2009), vol. 158(1), p. 301-308; Analytical Biochemistry (1966), vol. 15(3), p. 487-497). Причем низкая токсичность данного фермента и высокая активность позволяет эффективно элиминировать избыточный глутамат в течение длительного времени.
Из уровня техники известен способ лечения поражений нервной системы при избытке глутамата препаратом, содержащим доминирующий белковый экстракт из ткани плаценты, обладающий, соответственно, ферментативной активностью (патент РФ №2405560, опубл. 10.12.2010). Задачей указанного технического решения является получение эффективного средства, нормализующего функции нервной системы, высокой чистоты приемлемым в промышленном масштабе способом. Терапевтический эффект достигается посредством введения препарата, содержащего в том числе глутаматоксалоацетаттрансаминазу, в организм человека в виде назальных капельных вливаний (по 1 капле в каждую ноздрю), ежедневно, на протяжении 12-14 дней, хотя возможно и внутривенное или интралюмбарное введение препарата с соответствующим перерасчетом дозировок.
Из уровня техники известен способ лечения поражений нервной системы при избытке глутамата препаратом, являющимся биологически активным комплексом из головного мозга эмбрионов копытных сельскохозяйственных животных для фармацевтического производства препаратов, стимулирующих физиологическую и репаративную регенерацию нервной ткани, для применения в производстве лекарственных препаратов при заболеваниях центральной и периферической нервной системы (патент РФ №2428196, опубл. 10.09.2011). В описании изобретения указано на возможность применения данного комплекса, обладающего ферментативной активностью, с целью репаративно-регенеративного действия на нервную ткань. Рекомендуемый способ применения биологически активного белково-полипептидного комплекса в клинике - внутривенный или эндолюмбальный, терапевтическая доза (ТД) для человека, в том числе для ребенка, составляет 0,05 мг/кг/сутки.
Известен способ лечения острого нарушения мозгового кровообращения ишемического и геморрагического характера, заключающийся во введении фармкомпозиции, содержащей в качестве биологически активного вещества белково-полипептидный комплекс, полученный из быстрозамороженного эмбрионального мозга сельскохозяйственных копытных животных с определенным сроком гестации (патент РФ №2477637, 24.12.2010). Белково-полипептидный комплекс может быть использован посредством подкожного, внутримышечного или внутривенного введения 1-2 раза в сутки в дозе 0,1-0,8 мг/сут по 1-4 мл 0,1% раствора или интраназального введения 0,1% раствора по 0,2-0,4 мл в каждый носовой ход утром и днем в течение 7-14 суток с повтором курса через 5-14 дней. При тяжелых инсультах рекомендовано применение комплекса в суточной дозе до 0,6 мг, при состоянии пациентов крайней степени тяжести с выраженным нарушением сознания - до 0,8 мг в сутки или интратекальное введение 0,4 мг препарата 1 раз в 2-4 дня, при отсутствии абсолютных противопоказаний к люмбальной пункции. Способ оказывает благоприятное действие на выраженность и темпы восстановительных процессов, способствует ускорению регресса общемозговых и очаговых нарушений.
Из уровня техники известен белково-полипептидный комплекс (БПК), обладающий антигипоксическим, тканеспецифическим репаративным действием на центральную и периферическую нервную систему, получаемый из экстрагированного гомогената нервной ткани эмбрионов копытных сельскохозяйственных животных с определенным сроком гестации (патент РФ №2485132, 20.06.2013). БПК используют в качестве активного действующего компонента в фармацевтических композициях, предназначенных для получения лечебных средств. Изобретения позволяют получать препараты, обладающие высокой биологической активностью и предназначенные для лечения заболеваний центральной и периферической нервной системы, гипоксических состояний. Рекомендовано внутривенное введение фармкомпозиции БПНК в количестве 2 мл при концентрации 0,1 мг/мл. При этом терапевтическая доза (ТД) для человека, в том числе для ребенка, может составлять 0,05 мг/кг/сутки.
Недостатком вышеперечисленных решений является ограниченное время применения препаратов (7-14 дней), которое не позволяет проводить терапию хронических заболеваний, таких как боковой амиотрофический склероз. Помимо этого, применяемые для лечения препараты характеризуются нестабильностью состава, т.к. для их получения используется сырье животного происхождения.
Наиболее близким к заявляемому изобретению является WO 2016157190 A1, где описан способ получения и применение рекомбинантной глутаматоксалоацетаттрансаминазы человека для лечения различных заболеваний нервной системы. Однако в данном изобретении не приводится конкретного способа введения, концентрации препарата и схемы лечения, не показано достижение терапевтического эффекта для лечения хронических заболеваний, таких как боковой амиотрофический склероз.
Раскрытие изобретения
Проблемой, решаемой изобретением, является разработка эффективной схемы лечения бокового амиотрофического склероза с использованием рекомбинантной глутаматоксалоацетаттрансаминазы человека.
Техническим результатом является выявление максимально выраженного терапевтического эффекта при лечении бокового амиотрофического склероза за счет использования комплексной схемы, включающей подкожное введение лекарственного препарата, содержащего рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента на фоне приема оксалоацетата в виде биологически активной добавки перорально. Такая схема позволяет на протяжении длительного времени проводить поддерживающую терапию с наиболее выраженным эффектом снижения уровня глутамата и проявлений заболевания.
Поставленная задача решается введением лекарственного препарата, содержащего рекомбинантную глутаматоксалоацетаттрансаминазу человека, следующего состава:

Поставленная задача решается указанным лекарственным препаратом, путем подкожного введения из расчета 4,38 ЕД/кг, а затем ежедневно в дозе 1,14 ЕД/кг, но не более 36 введений на фоне приема оксалоацетата перорально в виде биологически активной добавки в количестве 100 мг в день.
Краткое описание чертежей
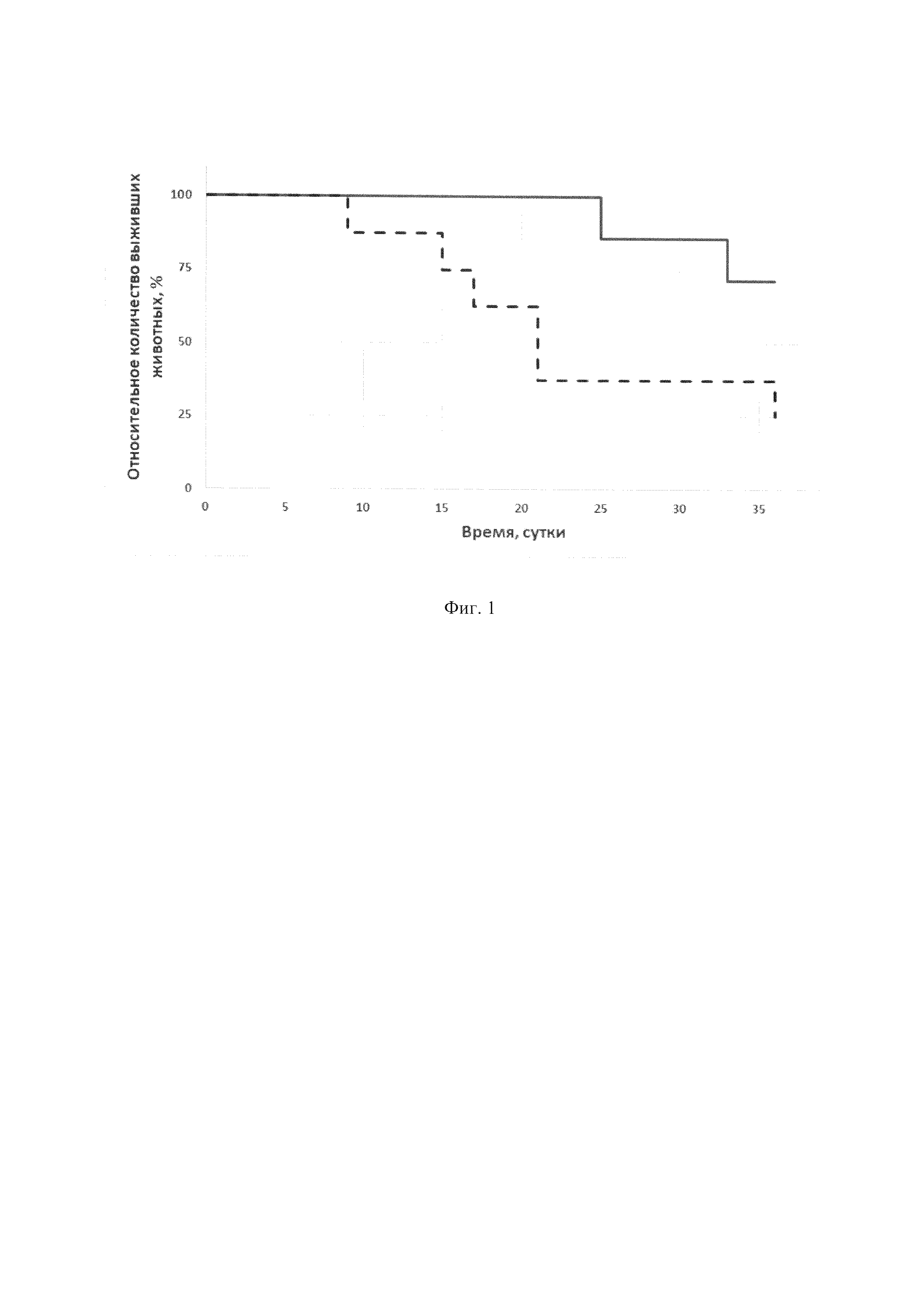
На фиг. 1 представлена кривая выживаемости животных Гехана. Сплошная линия - животные опытной группы, пунктирная линия - негативный контроль (животные, не получавшие лечения).
Осуществление изобретения
Получение лекарственного препарата
Рекомбинантная глутаматоксалоацетаттрансаминаза человека может быть получена способом, описанным в WO 2016157190 A1.
Для осуществления изобретения последовательность глутаматоксалоацетаттрансаминазы человека синтезировали методом твердофазного синтеза (Genescript, USA, https://www.genscript.com/express_gene_synthesis.html) клонировали по сайтам рестрикции NdeI и XhoI в плазмиду pET22b с использованием стандартных методов молекулярной биологии известных из научно-технической литературы (Molecular Cloning: A Laboratory Manual (Third Edition) By Joseph Sambrook, Peter MacCallum, David Russell).
Полученную плазмиду, содержащую ген глутаматоксалоацетаттрансаминазы человека, трансформировали в клетки E. coli штамма BL21(DE3)Rosetta2pLysS (cat # 70956, Merck, USA) методом кальциево-фосфатной трансформации (Molecular Cloning: A Laboratory Manual (Third Edition) By Joseph Sambrook, Peter MacCallum, David Russell).
Проводили аналитическую экспрессию целевого белка с использованием химического индуктора ИПТГ (изопропил-β-D-тиогалактопиранозид). Для этого колонии E.coli, несущие ген целевого белка, выращивали на жидкой питательной среде LB с ампициллином в пробирках в течение 15±2 часов при температуре 37°С при постоянном покачивании в качалке. Далее добавляли 0.5 мл полученной клеточной суспензии в колбы объемом 250 мл, содержащие 50 мл жидкой среды LB с ампициллином. Растили при температуре 37°С при постоянном покачивании до оптической плотности 0.5-0.1 (OD540). Затем добавляли химический индуктор ИПТГ до конечной концентрации 1 мМ и наращивали далее в течение 3 часов при температуре 30°С при постоянном покачивании. Биомассу собирали центрифугированием в пластиковых пробирках на 50 мл (15 минут, 3000 g).
Проводили электрофоретический анализ полученного клеточного белка в полиакриламидном геле в денатурирующих условиях. Для этого к аликвоте клеток 10 мг добавляли 40 мкл воды, перемешивали на встряхивателе и добавляли 40 мкл 2х буфера для образцов для белкового денатурирующего электрофореза. Образец прогревали при 95°С в течение 4 минут и наносили на денатурирующий гель с концентрацией акриламида 12%. После проведения электрофоретического разделения гель промывали дистиллированной водой, после чего окрашивали краской, содержащей краситель Кумасси. Избыток краски отмывали раствором, содержащим этанол и уксусную кислоту.
Анализ наличия целевого белка проводили визуально, сравнивая набор клеточных белков в неиндуцированных клетках и клетках, индуцированных ИПТГ. Для определения молекулярной массы полученного целевого белка использовали набор белков с известными молекулярными весами (PageRuler™ Prestained Protein Ladder, 10 to 180 kDa, ThermoFisher, USA).
Проводили анализ количества целевого белка по отношению к общему клеточному белку. Для этого гель сканировали на сканере Epson 1660 Photo. Полученное изображение обрабатывали с помощью программы Onedscan.
Результаты экспрессии показали высокий уровень синтеза целевого белка, содержание целевого белка составило не менее 43% от общего клеточного белка (в отличие от аналогов, характеризующихся содержанием целевого белка, в среднем 20-25%).
Для очистки белка клетки центрифугировали 15 мин при 3000 g, осадок обрабатывали ультразвуком на Sonics Vibra Cell (USA), полученную суспензию центрифугировали 20 мин при 18000 g и собирали супернатант.
Затем проводили диафильтрацию. Для этого в ячейку на приборе Vivacell 70 (мембрана 10 кДа, регенерированная целлюлоза) заполняли полученным супернатантом (180 мл) и концентрировали данный раствор, под давлением стерильного азота доводя объем раствора до 4 мл. Далее проводили замену буфера, путем добавления к концентрированному раствору белка 66 мл буферного раствора (20 мМ трис(гидроксиметил)аминометана, 20 мМ натрия хлорида, рН 7.5±0.1) и повторного концентрирования полученной смеси до объема 4 мл. Эту процедуру повторяли трижды. Полученный в итоге раствор белка в буфере сливали, а мембрану из регенерированной целлюлозы дважды промывали 4-5 мл буферным раствором (20 мМ трис(гидроксиметил)аминометана, 20 мМ натрия хлорида, рН 7.5±0.1), промывные воды объединяли с концентрированным раствором белка.
Затем проводили очистку методом анионообменной хроматографии на колонке Tricom 10/300 объемом 23,5 мл (сорбент Capto Q, размер частиц 90 мкм, длина колонки 30 см). Перед началом очистки систему Акт A Pure подготавливали следующим образом: промывали все каналы водой, затем пропускали через колонку два эквивалентных объема водного раствора гидроксида натрия с концентрацией 0,5 М, затем промывали водой до рН=9 и далее буферным раствором А для анионобменной хроматографии (20 мМ трис(гидроксиметил)аминометана, рН 7.5±0.1) до достижения рН элюата 7.5. Уравновешивали колонку путем пропускания 4 эквивалентных объемов колонки (ECV) буферного раствора А для анионобменной хроматографии со скоростью 4 мл/мин.
Наносили полученный раствор белка на колонку с помощью насоса со скоростью 4 мл/мин. Затем промывали колонку путем пропуска эквивалентных объемов буферного раствора А со скоростью 5 мл/мин и собирают все выходящие фракции.
После промывания буферным раствором А для анионобменной хроматографии начинали элюирование:
Ступень 1: градиент от О до 30% буферного раствора Б (20 мМ трис(гидроксиметил)аминометана, 500 мМ натрия хлорида, рН 7.5±0.1) на протяжении 5 ECV и далее промывка 30% буферным раствором Б на протяжении 5 ECV;
Ступень 2: градиент от 30 до 42% буферного раствора Б на протяжении 5 ECV и далее промывка 42% буферным раствором Б на протяжении 4 ECV;
Ступень 3: градиент от 42 до 55% буферного раствора Б на протяжении 5 ECV и далее промывка 55% буферным раствором Б на протяжении 10 ECV;
Ступень 4: градиент от 55 до 75% буферного раствора Б на протяжении 10 ECV;
Ступень 5: градиент от 75 до 100% буферного раствора Б на протяжении 5 ECV.
Собирали фракции на отрезке градиента 42-55% буферного раствора Б и определяли содержание белка по методу ВСА. Чистоту белка определяли ВЭЖХ методом RP-HPLC и гель-электрофорезом. Для этого проводили электрофоретический анализ полученного белка в полиакриламидном геле в денатурирующих условиях. Для этого к аликвоте белка 10 мкг (40 мкл) добавляли 20 мкл 2х буфера для образцов для белкового денатурирующего электрофореза. Образец прогревали при 95°С в течение 4 минут и наносили на денатурирующий гель с концентрацией акриламида 12%. После проведения электрофоретического разделения гель промывали дистиллированной водой, после чего окрашивали краской, содержащей краситель Кумасси. Избыток краски отмывали раствором, содержащим этанол и уксусную кислоту. Чистота полученного белка составила 90%.
Определение активности полученного белка проводили на биохимическом анализаторе Konelab 500 с использованием набора для определения активности аспартатаминотрансферазы DiaSys ASAT (GOT) FS (IFCC mod) в автоматическом режиме определения в соответствии с инструкцией производителя.
Фракции, содержащие целевой продукт, первоначально концентрировали с использованием прибора Millipore Labscale (мембрана 10 кДа, регенерированная целлюлоза) доводя объем раствора до 40-50 мл, систему дважды промывали водой очищенной (15 мл), промывные воды объединяли с концентрированным раствором белка. Затем концентрирование продолжали на приборе Vivacell 70 (мембрана 10 кДа, регенерированная целлюлоза) доводя объем раствора до 10 мл. Далее проводили замену буфера, путем добавления к концентрированному раствору белка 60 мл буферного раствора для формуляции (48 мМ фосфатный буфер рН раствора до 7.4±0.1) и повторного концентрирования полученной смеси до объема 4 мл. Эту процедуру повторяли трижды. Полученный в итоге раствор белка в буфере сливали в стерильную полипропиленовую емкость, а мембрану из регенерированной целлюлозы дважды промывали 4-5 мл буферного раствора для формуляции, промывные воды объединяли с концентрированным раствором белка.
Измеряли концентрацию очищенного белка с помощью Nanodrop и/или спектрофотометра на длинах волн 280-320 нм (для расчета используют коэффициент экстинкции 1,39 для раствора с концентрацией 1 мг/мл). Финальная концентрация раствора белка составляла 4 мг/мл.
Затем в емкость с раствором белка помещали стерильный якорь магнитной мешалки, а также на каждые 1,25 мл раствора белка добавляют 0,75 мл 10%-го раствора человеческого сывороточного альбумина и 1 мл раствора для криопротекции (500 мг/мл сахарозы, 24 мг/мл натрия хлорида). Все тщательно перемешивали в течение 15 минут на магнитной мешалке.
Полученную композицию разливали по флаконам объемом 6 мл по 3 мл на флакон, замораживали и подвергали лиофильной сушке в течение 51 часа.
Оксалоацетат получали методом растворения содержимого капсулы биологически-активной добавки Oxaloacetate (Fractal Health, США), 100 мг.
Модель бокового амиотрофического склероза
При разработке способа лечения использовали модель бокового амиотрофического склероза, в которой нейротоксиканты вводили в интратекальное пространство нелинейным самцам крыс весом 350-400 г длительное время. Регистрировали количество выживших животных, динамику двигательной активности, морфологическую картину срезов головного мозга для оценки нейропротекторного эффекта препаратов.
Распределение по группам и состав экспериментальных групп
Животные были распределены по группам случайным образом, разброс по массе тела для животных каждого вида составил не более±10% от среднего значения. Экспериментальные группы содержали количество животных, достаточное для полноценной регистрации изученных эффектов препаратов и статистической обработки полученных данных.
Схема введения лекарственного препарата.
Во флакон с препаратом медленно вводили с помощью стерильных шприца и иглы 5 мл воды для инъекций. Затем содержимое флакона осторожно взбалтывали до растворения лиофилизата. Введение лекарственного препарата осуществляли подкожно за сутки до имплантации минипомпы в дозе 27,0 ЕД/кг, а затем ежедневно в одно и то же время (около 18:00) осуществляли подкожное введение лекарственного препарата в дозе 7,0 ЕД/кг в течение 14 суток (или в течение 36 суток другой когорте животных).
Контрольным животным вводили соответствующие объемы 0,9% раствора хлорида натрия для инъекций и глутаминовую кислоту (Sigma Aldrich, чистота >98%) в дозе 0,015 мкг/кг в 0,9% растворе натрия хлорида для инъекций в объеме 0,5 мл болюсно. Для морфологического исследования использовали часть животных (по 6 животных в каждой группе) через 7 суток после установки минипомпы и введения лекарственного препарата.
Длительность введения одной дозы при этом составляла не менее 1 и не более 3 мин.
Оксалоацетат давался животным в питьевой воде в концентрации 0,2 М/л весь этот период наблюдения с питьевой водой. Регистрируемые параметры.
Проводили измерение концентрации глутаминовой кислоты в крови флюориметрическим методом, описанным в литературе (Analytical Biochemistry (1966), vol. 15(3), p. 487-497) с предварительной депротеинизацией образца: к образцу крови объемом 200 мкл для депротеинизации добавлялись 0,2 мл ледяной 1 М хлорной кислоты и затем смесь центрифугировалась при 10000 об./мин в течение 10 мин при температуре 4°С. Собиралась надосадочная жидкость, ее рН доводили до значения 7,2 с помощью 2 М карбоната калия и образец хранили при температуре -70°С для последующего энзиматического определения концентрации глутамата с использованием флюориметра при длине волны активации 350 нм и длине волны регистрации 460 нм. Показатели, подлежащие регистрации: содержание глутаминовой кислоты в крови - исходное и через 1, 2, 4, 6 и 24 часа после введения фармакологического агента.
Проводили оценку выживаемости в течение 36 дней после имплантации минипомпы с нейротоксикантами, двигательных нарушений в тесте «Ротарод» (установка Ugo Basile, Италия), объема поражения спинного мозга, а также гистологическое исследование.
При изучении влияния лекарственного препарата и оксалоацетата на продолжительность жизни животных на модели бокового амиотрофического склероза использовали анализ кривых выживаемости (критерий Гехана с поправкой Йейтса). При изучении различий признаков до и после введения веществ применяли критерий Уилкоксона при 5% уровне значимости. В расчетно-аналитическом разделе работы применяли пакетом программ по статистике BIOSTAT и SPSS (версия 9.2).
Хирургические манипуляции.
Половозрелую особь (использовали нелинейных крыс-самцов) с исходным весом 350-400 г наркотизировали внутрибрюшинным введением 50 мг/кг тиопентал-натрия («Тиопентал-натрий», Россия). После наступления стадии хирургического наркоза животное помещали на подогреваемую хирургическую площадку в положении на животе, фиксировали. Шерсть над пятым поясничным позвонком выбривали. В стерильных условиях производили рассечение кожи, ретракцию паравертебральных мышц. Пластинка пятого поясничного позвонка скусывалась микрокусачками под операционным микроскопом, обнажая участок твердой мозговой оболочки 2-3 мм в диаметре. В области тазового отдела позвоночника подкожно животному формировался карман, в который помещалась осмотическая минипомпа «ALZET model 2001» (1 мкл/ч, производства «Alza Scientific Products» США). Инфузионный конец минипомпы был обращен в сторону окна в позвоночнике. После этого твердую мозговую оболочку вскрывали, в сформированное отверстие вводили инфузионный катетер минипомпы на расстояние 1-1,5 см от места разреза оболочки. Катетер фиксировали нейлоновой нитью к оболочке, добавляли каплю хирургического адгезива. Рану послойно ушивали. Приготовление осмотической минипомпы осуществляли заранее. Для этого нейротоксины, вызывающие дегенерацию мотонейронов - каиновую кислоту (0,375 мМ) и циклотиазид (0,375 мМ) «Sigma-Aldrich», Германия) - растворяли в среде следующего состава: 122 мМ NaCl, 3,1 мМ КС1, 5 мМ NaHCO3, 0,4 мМ КН2РС4, 1,3 мМ CaCl2, 1,0 мМ MgSO4, и 10 мМ глюкозы, рН 7,4). 200 мкл полученного раствора нейротоксикантов помещали в минипомпу, которую инкубировали при 37°С в растворе хлорида натрия для инъекций на протяжении как минимум 6 часов перед имплантацией животному.
Гистологическое исследование. После эвтаназии спинной мозг извлекали на уровне L1-L5 и, используя микротом, приготавливали серию срезов толщиной 6 мкм с последующим проведением соответствующей гистологической проводки. Срезы окрашивали по Нисслю в модификации Бельшовского.
Было показано, что при ежедневном подкожном курсовом введении лекарственного препарата в стартовой дозе 27 ЕД/кг и поддерживающей ежедневной дозе 7,0 ЕД/кг в течение 36 суток (в том числе в комбинации с оксалоацетатом, поступающего экспериментальным животным с питьевой водой) установлено, что лекарственный препарат, содержащий рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента в комбинации с оксалоацетатом эффективно снижает уровень глутаминовой кислоты. Результаты представлены в таблице 1.
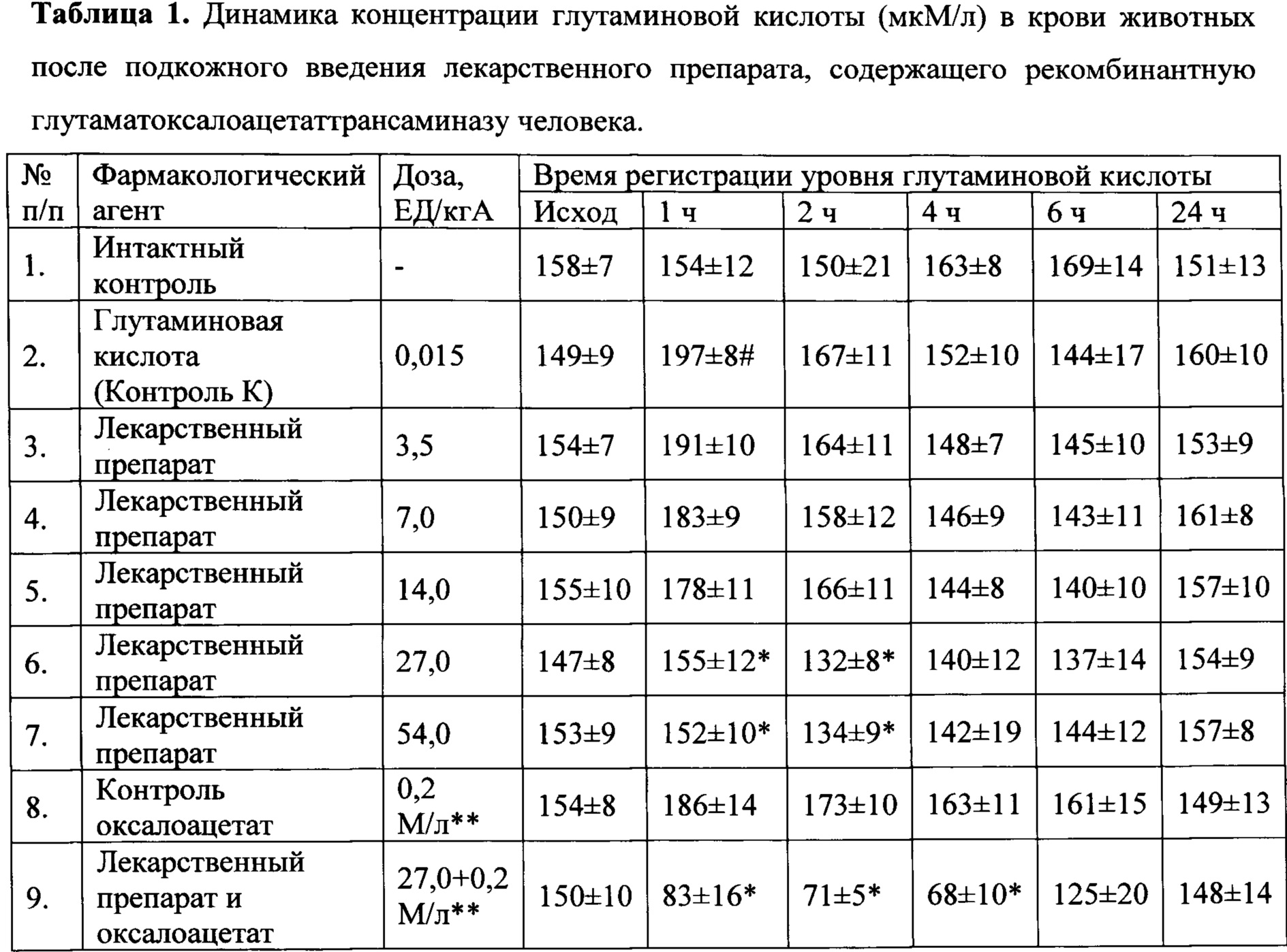
Примечание: # - различия при сравнении с интактным контролем статистически значимы при p<0,05 (одномерный дисперсионный анализ, критерий Даннета); * - различия при сравнении с контролем К статистически значимы при p<0,05 (одномерный дисперсионный анализ, критерий Даннета); А - мг/кг для OA и глутаминовой кислоты; ** - в питьевой воде.
Были проведены исследования терапевтической эффективности заявляемой схемы лечения в широком диапазоне интервалов значений. При подкожном введении лекарственного препарата, содержащий рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента, в диапазоне доз от 3,5 ЕД/кг до 14,0 ЕД/кг не наблюдали значимого эффекта по снижению уровня глутаминовой кислоты. В дозе 27,0 ЕД/кг лекарственный препарат снижал концентрацию медиатора эксайтотоксичности через 1 ч после подкожного введения. Увеличение дозы до 54,0 ЕД/кг не приводило к усилению эффекта.
Оксалоацетат при концентрации 0,2 М/л в питьевой воде не приводил к снижению уровня глутаминовой кислоты ни в одной временной точке. Однако, введение лекарственного препарата в дозе 27,0 ЕД/кг в сочетании с введением приемом оксалоацетата в концентрации 0,2 М/л в питьевой воде приводило к наиболее выраженному снижению уровня глутаминовой кислоты, продолжительностью более 4 часов (время наблюдения).
На модели бокового амиотрофического склероза было показано, что лекарственный препарат, содержащий рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента, на фоне приема оксалоацетата сдерживает вызываемую нейротоксикантами глутамат-опосредованную экайтотоксичность, что проявляется в сохранении площади моторных зон и их клеточного состава в передних рогах спинного мозга на уровне формирования патологического процесса, замедлении формирования моторного дефицита и увеличении продолжительности жизни экспериментальных животных.
С учетом соответствующих коэффициентов пересчета, данная доза была преобразована в эквивалентную дозу для человека и составила 4,38 ЕД/кг при начальном введении и 1,14 ЕД/кг при ежедневном поддерживающем введении на фоне приема оксалоацетата в виде биологически активной добавки в количестве 100 мг в день.
Настоящее изобретение поясняется конкретными примерами.
Пример 1. Влияние введения лекарственного препарата, содержащего рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента и оксалоацетата на динамику двигательной функции у животных на фоне формирующегося бокового амиотрофического склероза.
Оценку двигательных нарушений в течение 14 дней после имплантации минипомпы с нейротоксикантами на фоне введения лекарственного препарата и оксалоацетата проводили в тесте «Ротарод» (установка Ugo Basile, Италия).
Результаты представлены в Таблице 2.

Примечание: # - различия при сравнении с показателем на 4-е сут статистически значимы при p<0,05 (критерий Уилкоксона); * - различия статистически достоверны при сравнении с контролем при p<0,05 (одномерный дисперсионный анализ, критерий Стьюдента)
В контрольной группе животных с имплантированной минипомпой, получающих физиологический раствор подкожно и питьевую воду без добавления OA, отмечено проградиентное угнетение двигательной функции, показатель которой к 14-м суткам наблюдения принимает значения 25% от величины, зарегистрированной на 4-е сутки после операции.
Назначение животным с формирующимся БАС комбинированного лечения, включающего подкожное введение лекарственного препарата, содержащего рекомбинантную глутаматоксалоацетаттрансаминазу человека, в стартовой дозе 27,0 ЕД/кг с последующим ежесуточным введением фермента в дозе 7,0 ЕД/кг на фоне получения животными оксалоацетата с питьевой водой в концентрации 0,2 М, приводит к сохранению двигательной функции на протяжении 14 суток наблюдения, при этом на 7 сутки фиксировали активацию моторной функции до 116 с в среднем (Таблица 2).
Пример 2. Влияние введения лекарственного препарата, содержащего рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента и оксалоацетата на площади моторных зон спинного мозга и сохранных мотонейронов у животных на фоне формирующегося бокового амиотрофического склероза.
Оценку объема поражения спинного мозга в течение 14 дней после имплантации минипомпы с нейротоксикантами на фоне введения лекарственного препарата и оксалоацетата проводили с помощью гистологического исследования.
Результаты представлены в Таблице 3.


Примечание: * - различия статистически достоверны при сравнении с соответствующим контролем при p<0,05 (одномерный дисперсионный анализ, критерий Стьюдента)
При проведении морфологического исследования были изучены срезы спинного мозга, выполненные на уровне поясничных позвонков, и окрашенные по Нисслю в модификации Бельшовского (Таблица 3).
Комбинированное топическое воздействие на спинной мозг животных каионовой кислотой и циклотиазидом приводит к 14 суткам эксперимента к сужению площади моторных зон передних рогов спинного мозга на уровне поясничных позвонков наряду с их клеточным запустеванием в результате токсической гибели мотонейронов.
Комбинированное фармакологическое воздействие, включающее подкожное введение лекарственного препарата в стартовой дозе 27,0 ЕД/кг с последующим ежесуточным введением лекарственного препарата в дозе 7,0 ЕД/кг на фоне получения животными оксалоацетата с питьевой водой в концентрации 0,2 М, статистически значимо сдерживает развитие и глубину нейродегенеративного процесса в паренхиме спинного мозга.
Пример 3. Влияние введения лекарственного препарата, содержащего рекомбинантную глутаматоксалоацетаттрансаминазу человека в качестве активного компонента и оксалоацетата на выживаемость животных на фоне формирующегося бокового амиотрофического склероза.
Оценку выживаемости проводили при однократном введении лекарственного препарата до имплантации минипомпы с нейротоксикантами в дозе 27,0 ЕД/кг, а затем ежедневно в одно и то же время осуществляли подкожное введение лекарственного препарата в дозе 7,0 ЕД/кг в течение 36 суток.
Результаты исследования представлены на фиг 1.
Как видно из представленных данных, гибель животных в контрольной группе начиналась на 9 сутки опыта и затем прогрессивно нарастала: к концу периода наблюдения из 8 контрольных (не леченных) животных в живых осталось лишь два.
В опытной группе, получавших лекарственный препарат на фоне приема оксалоацетата с питьевой водой, гибель животных начиналась только на 25 сутки. Снижалось и количество погибших крыс: за 36-суточный период в опытной группе наблюдения - выжили 5 животных из 7 принимавших участие в наблюдении.