Результат интеллектуальной деятельности: Питательная среда для консервации и транспортировки клеток для дальнейшего цитологического и иммуноцитохимического исследования
Вид РИД
Изобретение
Изобретение относится к составам для консервации живых клеток и представляет собой питательную среду для накопления, сохранения, промывания и транспортировки образца клеточного материала, изъятого у пациента, на период до проведения последующего цитологического и/или иммуноцитохимического анализа.
В современных условиях развития цитологической диагностики и внедрения дополнительных уточняющих метолов диагностики (иммуноцитохимия, ПЦР) существует потребность в хранении и транспортировке клеточного материала. В средах, применяемых на данный момент, основным консервирующим раствором являются производные спиртов (этиловый, изопропиловый) или альдегидов (формальдегид), которые по своей природе вызывают денатурацию белков, приводя к морфологическим изменениям (сморщиванию) и нарушению антигенного состава клеток. Данный факт и побудил к созданию питательной среды, где консервантом является азид натрия, действием которого является нарушение клеточного дыхания (ингибирование фосфорилирующего окисления, подавляя сопряжённый с фосфорилированием перенос электронов в интактных митохондриях), не нарушая антигенного состава клеток, подавляя при этом рост и размножение микроорганизмов.
Известна питательная среда, защищённая патентом РФ № 2435842, C12N 1/20, C12R 1/32, опубл.10.12.2011 г., содержащая дрожжевую воду, гидролизат говяжьего мяса, натрия хлорид, глюкозу, глицерин, цитрат натрия, метабисульфит натрия и дистиллированную воду. Изобретение позволяет обеспечить оптимальные условия для роста, размножения бруцеллезного микроба при транспортировке питательной среды на любые расстояния.
Известному раствору присущи недостатки: отсутствует возможность анализа образцов опухолевой ткани, крови, лимфоузлов, слизистой и др.; гидролизат говяжьего мяса не обладает эффективностью в отношении улучшения цитологического исследования.
Известна также среда для установления присутствия и(или) вида микроорганизма; использование селективных сред для испытания антибиотиков или бактерицидов; составы, содержащие химический индикатор для этих целей, описанные в патенте РФ № 2529711 С12 Q1/04, C12N 1/20, опубл.27.09.2014 г.
По известному способу определяют чувствительность бактерий, вызывающих кишечные инфекции, к комплексным антибактериальным препаратам. Проводят разведение антибактериальных препаратов в концентрации 10 мкг/мл в питательной среде с рН 7,2-7,6. Подготовленную взвесь бактерий вносят в лунки, содержащие приготовленные разведения. Вносят индикатор – 0,5% раствор бромкрезолового пурпурного в количестве 10 мкл. Инкубируют в течение 3-4 ч. Проводят визуальную оценку роста бактерий и оценку окраски среды в лунке при достижении рН 5,2-6,8 среды. Делают вывод о чувствительности бактерий к комплексным антибактериальным препаратам по наличию или отсутствию роста бактерий и изменению окраски среды с красной на желтую. Чувствительными считают бактерии, у которых отсутствует рост и изменение цвета питательной среды с антибактериальными препаратами. Устойчивыми считаются бактерии, у которых наблюдается рост и изменение цвета среды с антибактериальными препаратами.
Недостатками известной среды являются отсутствие возможности анализа образцов опухолевой ткани, крови, лимфоузлов, слизистой и др. и то, что антибактериальные компоненты, входящие в состав среды, не имеют положительного влияния на выполнение цитологических исследований.
Наиболее близкой к заявляемому изобретению, выбранной в качестве прототипа, является питательная среда накопления образца клеток для последующего цитологического и/или иммуноцитохимического анализа, защищенная патентом РФ № 2246110, G01N 33/48, G01N 33/53, A01N 1/02, опубл.10.02.2005 г. Среда представляет собой раствор Хенкса, содержащий соли NaCl, KCl, CaCl2 безводный, MgSO4·6H2O, MgCl2·6H2O, Na2HPO4·2H2O, KH2PO4, NaHCO3 и глюкозу и дополнительно включает 10% раствор альбумина и полиглюкин (декстран 60000) при следующем соотношении: 10% раствор альбумина, раствор Хенкса, полиглюкин = 1:1:1.
Недостатком известной среды является недостаточный срок сохранения и транспортировки образца клеточного материала (в течение до 48 часов), а также необходимость ее хранения в условиях заморозки и наличие соответствующего низкотемпературного оборудования.
Техническая проблема, решаемая предлагаемым изобретением, – создание питательной среды, способствующей сохранению морфологических свойств клеточного состава, с упрощенными условиями хранения и длительными сроками хранения и транспортировки.
Технический результат от использования изобретения заключается в повышении длительности сохранения и транспортировки образца клеточного материала и упрощении условий хранения среды.
Указанный технический результат достигается тем, что питательная среда для транспортировки клеток для дальнейшего цитологического и иммуноцитохимического исследования, содержащая стерильный 10% раствор альбумина человека, дополнительно включает раствор среднемолекулярной фракции частично гидролизованного декстрана в изотоническом растворе натрия хлорида и раствор азида натрия при следующем соотношении компонентов, мас.%:
стерильный 10 % раствор альбумина человека – 33,0-33,3
раствор среднемолекулярной фракции частично гидролизованного декстрана – 33,0-33,3
натрий хлорид – 33,32-33,94
раствор азида натрия – 0,06- 0,08.
Заявляемый состав питательной среды накопления образца клеток является оптимальным с точки зрения получения наилучших результатов цитологических и иммуноцитохимических (ИЦХ) исследований.
Альбумин способствует созданию и поддержанию исследуемого клеточного образца в состоянии суспензии – коллоидного состояния, близкого к естественному. Меньшее количество альбумина приводит к уменьшению размеров и искажению формы помещенных туда клеток, а большее количество приводит к набуханию клеток, вплоть до их лизиса.
Раствор среднемолекулярной фракции частично гидролизованного декстрана в изотоническом растворе натрия хлорида обеспечивает необходимое питание и поддержание жизнеспособности живых клеток в изъятом у пациента образце ткани.
При меньшем количестве его происходит набухание и лизис клеток, при большем количестве – искажение клеток в виде сморщивания.
Азид натрия (NaN3) – это бесцветная соль азотистоводородной кислоты. В растворе азида натрия практически все биологические объекты сохраняют исходный цвет, форму и размер. При этом диапазон рабочих концентраций азида натрия варьирует от 0,5% до 0,05 %. При высоких концентрациях есть данные об эффективном консервировании биологических образцов тканей. Однако при концентрации 0,5% наблюдается деградация биологического материала на молекулярном уровне. Были проведены исследования по влиянию разных концентраций азида натрия на реакцию с антигеном (РА), наличия сопутствующей микрофлоры (МФ), состояния мембраны и органелл клеток (https://monographies.ru/en/book/section?id=4951).
Данные сведены в таблицу 1.
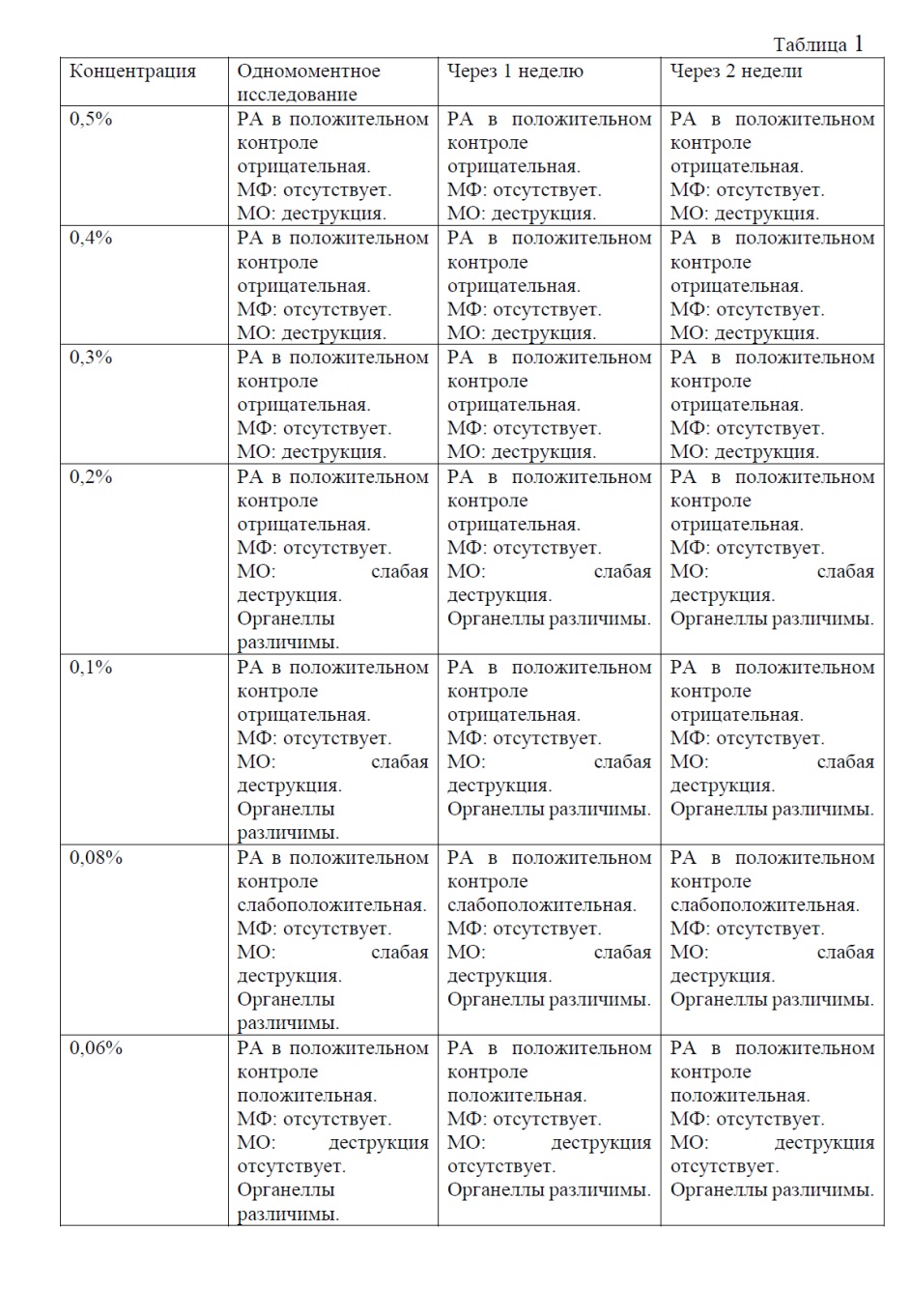
Полученные результаты свидетельствуют о том, что при концентрации азида натрия 0,06-0,08% не наблюдалось изменений структуры мембраны и органелл клеток, не были обнаружены признаки наличия микрофлоры, а также не проявлялось негативное влияние азида натрия на способность антител специфически взаимодействовать с исследуемым антигеном.
Все используемые составляющие заявляемой среды выпускаются отечественной промышленностью:
стерильный 10% раствор альбумина человека – ГУЗ Нижегородская областная станция переливания крови им. Н.Я.Климова;
раствор среднемолекулярной фракции частично гидролизованного декстрана – ООО «Биосинтез»;
натрий хлорид – ООО «Биосинтез»;
раствор азида натрия – ООО «Биолайн».
Для приготовления заявляемого состава, перечисленные выше компоненты смешивают в указанной пропорции. Хранят питательную среду в холодильниках при температуре +4-+8°С.
Используют питательную среду следующим образом. Производят отбор образца исследуемых тканей, например пунктата щитовидной железы, протыкают крышку пробирки после взятия материала, промывают питательной средой иголку путем всасывания внутрь шприца питательной среды, и весь материал окажется в пробирке.
Транспортировка и хранение образца живой ткани, помещенного в заявляемую питательную среду, может быть осуществлена при температуре окружающей среды в течение до 10 суток.
Заявляемая среда может быть использована для анализа образцов опухолевой ткани, крови, лимфоузлов, слизистой и др.
Пример использования питательной среды для иммуноцитохимического анализа:
Осадок клеток вносят в пробирку с питательной средой путем прокалывания крышки и помещения внутрь пробирки материала (клеток, взятых от пациента). Затем пробирку центрифугируют до формирования осадка, открывают не позднее чем через 10 суток (в зависимости от потребности специалиста).
Подготовленный осадок клеток вносят на предметное стекло и высушивают при комнатной температуре.
На осадок клеток на стекле (далее образец) наносят по 50 мкл раствора 3% перекиси водорода на 10 минут.
Промывают препараты в двух порциях буферного раствора, по 2 минуты в каждом.
Важно! С этого этапа нельзя допустить высыхания препарата до окончания реакции. При необходимости нахождение в буфере возможно дольше указанного времени
На образец клеток наносят по 50 мкл протеин-блока на 10 минут.
Промывают препараты в двух порциях буферного раствора, по 2 минуты в каждом.
На образец наносят 30 мкл первичных антител. Время инкубации 30 минут при комнатной температуре.
Промывают препараты в двух порциях буферного раствора, по 2 минуты в каждом.
На образец наносят по 30 мкл вторично-меченных антител. Время инкубации 20 минут при комнатной температуре.
Промывают препараты в двух порциях буферного раствора, по 2 минуты в каждом.
Подготавливают рабочий раствор диаминобензидина (ДАБ) растворив рабочим раствором растворителя в соотношении 1:1.
На образец наносят 30 мкл раствора ДАБ на 3-5 минут.
Промывают препараты в трех порциях воды, по 2 минуты в двух и 10 минут в третьей.
На образец наносят 30 мкл раствора гематоксилина Майера на 1 минуту.
Промывают препараты в воде, высушивают и микроскопируют.
Изобретение поясняется клиническими примерами и иллюстрациями, на которых изображено:
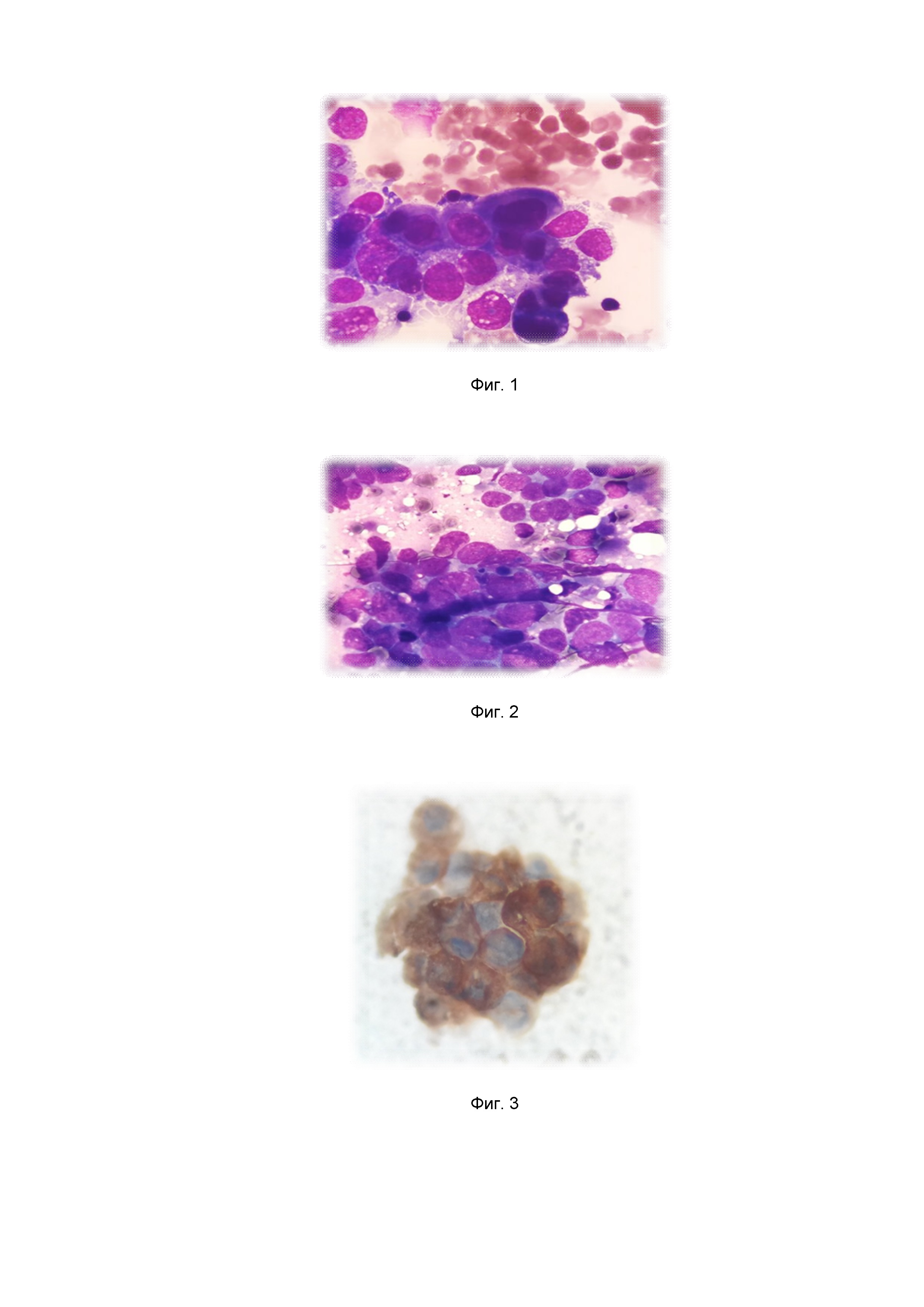
На фиг.1 – Цитологический препарат сразу после забора материала (к примеру 1);
На фиг. 2 – Цитологический препарат через 10 суток в заявляемой питательной среде. (к примеру 1);
На фиг.3 – Иммуноцитохимическое исследование материала после хранения в заявляемой питательной среде (антитело NCAM (CD 56)) (к примеру 1);
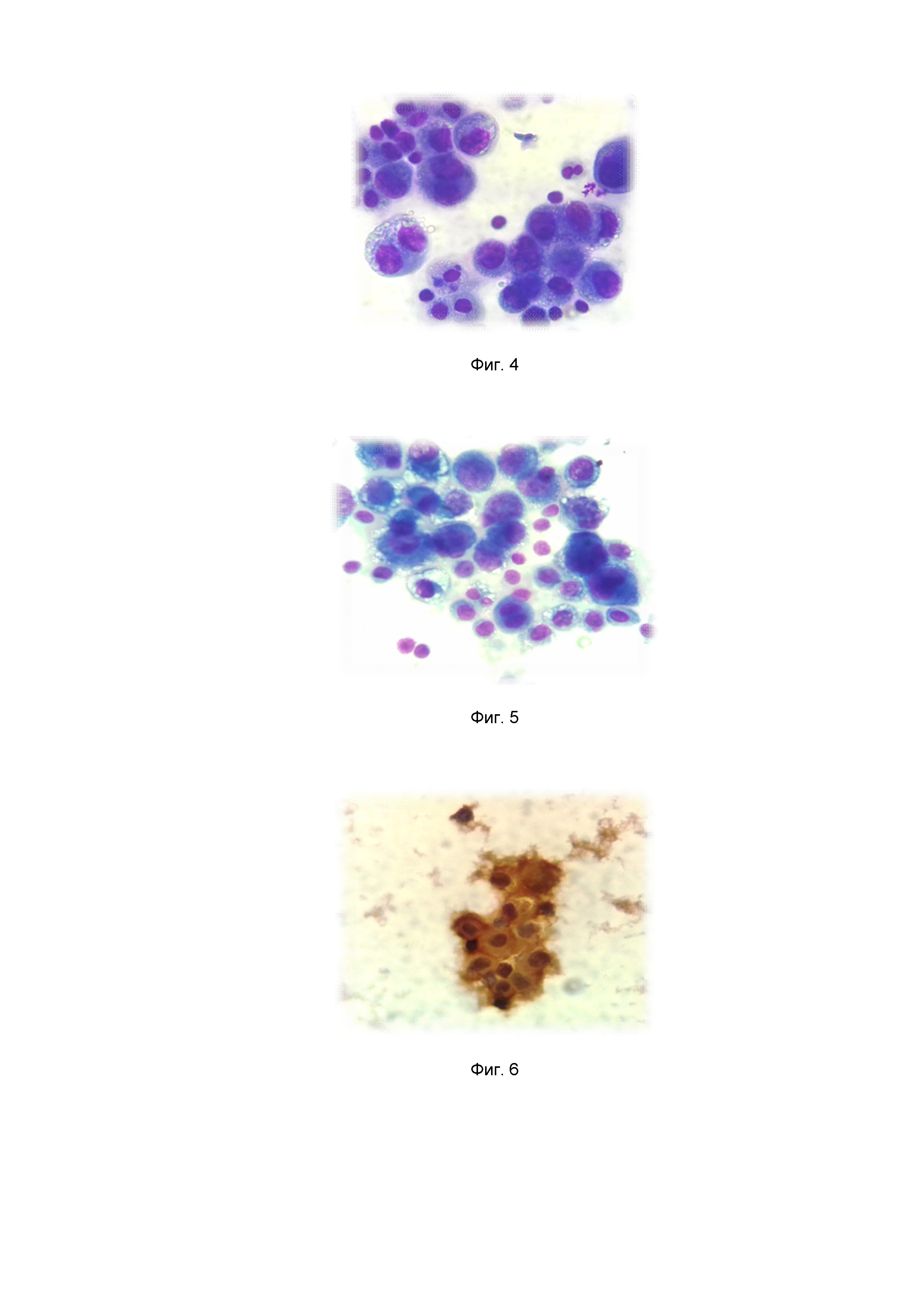
На фиг. 4 – Цитологический препарат сразу после забора материала (к примеру 2);
На фиг. 5 – Цитологический препарат через 10 суток в заявляемой питательной среде. (к примеру 2);
На фиг.6 – Иммуноцитохимическое исследование материала после хранения в заявляемой питательной среде (антитело NCAM (CD 56)) (к примеру 2).
Пример 1.
Пациент Х, 48 лет с диагнозом объемное образование верхней доли левого легкого находился на лечении в диагностическом отделении Областного туберкулезного диспансера. Во время срочного интраоперационного цитологического исследования (26.09.18г. 11:30) выдано заключение: «цитологическая картина злокачественного новообразования. Низкодифференцированная аденокарцинома с элементами мелкоклеточной дифференцировки.». Для уточнения гистологического типа опухоли методом иммуноцитохимического исследования взят соскоб стерильным скальпелем с разреза удаленной опухоли (26.09.2018 г 12:00) и помещен в питательную среду, содержащую стерильный 10 % раствор альбумина человека 33,3 мас.%, раствор среднемолекулярной фракции частично гидролизованного декстрана 33,3 мас.% в изотоническом растворе натрия хлорида 33,32 мас.% и раствор азида натрия 0,08 мас.%. Материал направлен на иммуноцитохимическое исследование и доставлен в ПАО Областной клинической больницы 27.09.2019 в 10:00 (спустя 22 часа от момента забора) с промежуточным хранением при температуре +4°С. Иммуноцитохимическое исследование проведено 28.09.2018 в 13:00 (спустя 49 часов от момента забора материала). Исследование проведено согласно методике, описанной выше. Результат исследования подтвердил диагноз: Мелкоклеточный рак верхней доли левого легкого. Таким образом, установлено, что хранение исследуемого препарата, содержащего опухолевые клетки, в заявляемой питательной среде в течение 49 часов, не искажает иммунных и морфологических качеств клеток и не влияет на результаты иммуноцитохимического анализа.
Пример 2.
Пациентка 58 лет. С диагнозом «Асцит» доставлена в приемное отделение хирургического стационара с целью лапароцентеза. В процессе манипуляции удалено 1,5 л жидкости, материал отправлен на цитологическое исследование 13.05.2018 г 15:00. При исследовании выдано цитологическое заключение: «Цитологическая картина специфического экссудата. Аденокарцинома.». Для определения первичной локализации опухоли оставшийся клеточный осадок помещен в питательную среду, содержащую стерильный 10% раствор альбумина человека 33,0 мас.% раствор среднемолекулярной фракции частично гидролизованного декстрана 33,0 мас.% в изотоническом растворе натрия хлорида 33,94 мас.% и раствор азида натрия 0,06 мас.% 13.05.2018 в 16:30 и оставлен при температуре +4°С с целью иммуноцитохимического исследования. 24.05.2018 в 8:00 (спустя 232 часа от момента забора) материал направлен в ПАО областной больницы для дальнейшего исследования. Иммуноцитохимическое исследование проведено 24.05.208 в 17:30 (спустя 233,5 часа от момента забора материала). Исследование проведено согласно методике описанной выше. Результат исследования подтвердил диагноз: «Серозная аденокарцинома яичника». Таким образом, установлено, что хранение и транспортировка исследуемого препарата, содержащего опухолевые клетки, в заявляемой питательной среде в течение 233,5 часа, не искажает иммунных и морфологических качеств клеток и не влияет на результаты иммуноцитохимического анализа.
Таким образом, предлагаемая питательная среда по сравнению с прототипом имеет следующие преимущества:
- более длительный срок хранения с материалом (до 233,5 часов), что создает условия для транспортировки биоматериала в лабораторию от места забора (при необходимости транспортировки из отдаленных районов в центральные лаборатории);
- более простой способ хранения (отсутствие необходимости хранения в условиях заморозки и наличия соответствующего низкотемпературного оборудования).
Кроме того, использование азида натрия в качестве консерванта не изменяет органолептических свойств питательной среды (отсутствие запаха) и питательная среда способствует сохранению морфологических свойств клеточного состава аналогичных на момент забора материала.