Результат интеллектуальной деятельности: СПОСОБ ИММУНОТЕРАПИИ РАКОВЫХ ЗАБОЛЕВАНИЙ
Вид РИД
Изобретение
Изобретение относится к области медицины, в частности к онкологии, и может быть использовано для лечения пациентов с диагнозом лейкоз.
Известен способ иммунотерапии опухолей, заключающийся в приеме пациентом экзомсодержащего препарата per os (патент: RU 2593003 С2, опубл. 27.07.2016, МПК A61K 35/54, А61Р 35/00, А61Р 37/00).
Одним из основных недостатков данного способа является его недостаточная специфичность, обусловленная тем, что экзосомы для препарата получают от клеточной линии, а не от культуры опухолевых клеток, полученных от пациента. Клеточные линии даже лейкозов не отражают объективно фенотипические особенности конкретной опухоли, имеющей место у пациента, также не учитывают мутационные процессы, способствующие доминированию определенного клона или клонов и приобретению опухолью резистентностью к терапевтическим препаратам. Данный метод имеет определенные ограничения, связанные с состоянием иммунной системы на момент введения препарата, т.к. принцип его действия заключается в попытке запустить специфическое звено иммунитета против опухоли посредством представления опухолевых антигенов иммунокомпетентным клеткам. Однако данный метод не предлагает никаких средств по восстановлению состояния иммунной системы, которая на момент введения препарата, как правила, угнетена химиотерапией и, помимо того, подавляется самими опухолевыми факторами, и может не иметь достаточно ресурсов для реализации противоопухолевого иммунного ответа.
Техническим результатом, достигаемым при реализации настоящего способа, является возможность лечения пациентов с диагнозом лейкоз.
Указанный технический результат достигается тем, что при реализации способа иммунотерапии раковых заболеваний, согласно настоящему изобретению, для пациентов с диагнозом лейкоз получают 5 мл образца костного мозга от здорового донора, затем выделяют из него мононуклеарные клетки, далее культивируют их в полной культуральной среде следующего состава: среда DMEM/F12 1:1 с HEPES с добавлением 2 ммоль/мл или 3,65 мг/10 мл L-глутамина, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 10% эмбриональной сыворотки, в условиях Т=37°С и 5% CO2 в течение 48-72 часов, затем выделяют из полученной культуральной среды экзосомосодержащий осадок, растворяют его в фосфатно-солевом буфере в соотношение 1:5-1:20, и далее полученный раствор назначается per os (перорально, внутрь, через рот) пациенту с диагнозом лейкоз, а именно 1 раз в три дня после еды в утренние часы, при этом число курсов приема составляет 3 или 5.
Забор материала от здорового донора позволяет получить экзосомы, несущие в себе информацию о сигнальных путях и уровнях экспрессии рецепторов и сигнальных молекул, характерных для здоровой костномозговой ткани. Последующий прием подобных экзосом реципиентом с опухолевым поражением костного мозга способствует восстановлению сигналлинга между клетками и внутри клеток, характерного для непораженных клеток костного мозга, запуску процессов репрограммирования в уже трансформированных клетках костного мозга с последующим приобретением ими фенотипа здоровых клеток. Культивирование осуществляется в среде описанного состава, т.к. она обеспечивает необходимые для жизнедеятельности клеток вещества и стерильность получаемого материала. Период культивирования обусловлен особенностями роста клеточных культур, 48 часов необходимы для приживания культуры в культуральном флаконе, после 72 часов значительно меняются фенотипические и функциональные характеристики клеток, в связи с чем наиболее оптимальным временным периодом для забора экзосом являются первые 48 часов, но не более 72 часов.
Соотношение экзосомосодержащего осадка к фосфатно-солевому буферу 1:5-1:20 позволяет максимально эффективно собрать экзосомы, не допустив при этом чрезмерного растворения и потери части материала.
Предпочтительно выделение мононуклеарных клеток осуществлять путем смешивания образца костного мозга от здорового донора с раствором Хэнкса 1:1 или с полной культуральной средой следующего состава: среда DMEM/F12 1:1 с HEPES с добавлением 2 ммоль/мл или 3,65 мг/10 мл L-глутамина, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 10% эмбриональной сыворотки, затем полученную смесь наслаивают на раствор фиколла-урографина плотностью 1,077 г/см3 в соотношении 1:3-1:4, затем проводят центрифугирование при 1500 об/мин в течение 20 минут, собирают интерфазное кольцо, содержащее мононуклеарные клетки, которое смешивают с раствором Хэнкса в соотношении 1:10-1:20, центрифугируют при 1500 об/мин в течение 3 минут, собирают образовавшийся осадок, который 2-3 раза подвергают смешению с раствором Хэнкса в соотношении 1:10 с последующим центрифугированием при 1500 об/мин в течение 3 минут после каждого смешения, с получением на выходе осадка с монуклеарными клетками.
Метод выделения мононуклеарных клеток наслоением на фиколл является стандартной процедурой получения клеточной культуры без эритроцитов, он удобен и не требует выраженных финансовых и временных затрат. Культивирование осуществляется в среде описанного состава, т.к. она обеспечивает необходимые для жизнедеятельности клеток вещества и стерильность получаемого материала. Период культивирования обусловлен особенностями роста клеточных культур, 48 часов необходимы для приживания культуры в культуральном флаконе, после 72 часов значительно меняются фенотипические и функциональные характеристики клеток, в связи с чем наиболее оптимальным временным периодом для забора экзосом являются первые 48 часов, но не более 72 часов. Обозначенные соотношения растворов, используемые на этапах выделения клеток и последующей отмывки, обеспечивают необходимые оптимальные условия для проведения описанных процессов: разбавление полученной клеточной массы в 2 раза обеспечивает формирование интерфазного кольца с четким его отделением от осевших эритроцитов; если не проводить разведения полученного объема ткани, то в процессе выделения интерфазное кольцо может быть неотделимо от эритроцитарной массы, при разведении более чем в 2 раза повысится число циклов выделения клеток при отсутствии повышения эффективности процесса. Полученный раствор наслаивается на фиколл в соотношении 1:3-1:4, т.к. именно при таком соотношении плотности фиколла достаточно для поддержания интерфазного кольца и одновременно отделения его от эритроцитарной массы; при увеличениисоотношения есть вероятность получить слишком высокий эритроцитарный столбик, выходящий за границы фиколльной фазы, что может привести к потерям выделяемых клеток и их смешиванию с эритроцитами, которые являются артефактами в получаемой культуре. Уменьшение соотношения приведет к необходимости проведения дополнительных циклов выделения и расходу реагентов при отсутствии повышения эффективности.
Предпочтительно выделение из полученной культуральной среды экзосомосодержащего осадка осуществлять путем дифференциального центрифугирования, а именно: центрифугируют полученную культуральную среду при 3000 об/мин в течение 10 мин., затем собирают образовавшийся супернатант далее проводят центрифугирование при 10000 об/мин в течение 30 минут, затем отбирают образовавшийся супернатант и проводят ультрацентрифугирование при 100000 об/мин в течение 2-х часов, далее отделяют образовавшийся осадок.
Ультрацентрифугирование было выбрано в качестве метода выделения экзосом в связи с его более высокой эффективностью в сравнении с коммерческими наборами по данным опубликованных работ [Methods Mol Biol. 2015; 1295:179-209. doi: 10.1007/978-l-4939-2550-6_15. A protocol for exosome isolation and characterization: evaluation of ultracentrifugation, density-gradient separation, and immunoafflnity capture methods. Greening DW, Xu R] и по данным собственных исследований.
Примеры реализации заявленного способа:
Мужчина 53 лет, диагноз типичный хронический миелолейкоз (определяется филадельфийская хромосома) с апреля 2018 года, курит (со слова пациента, стаж 30 лет, не более 5 сигарет в день), в анамнезе язвенная болезнь двенадцатиперстной кишки (1995 год), аппендэктомия (1985 год), в остальном анамнез без особенностей. В общем анализе крови от мая 2018 года СОЭ увеличена до 32 мм/ч, сдвиг лейкоцитарной формулы влево с повышением лейкоцитов до 13*109/мл и увеличением количества базофилов до 4%, общий анализ мочи от мая 2018 года без особенностей, биохимический анализ крови от мая 2018 года без особенностей, по данным УЗИ увеличение селезенки до 12 см*7 см*5 см. В миелограмме от апреля 2018 года увеличение бластов до 5%. Пациенту провели 3 курса (продолжительность одного курса составляет 3 недели) терапии препаратом из модифицирующих экзосом per os. Режим приема препарат был следующий: 1 раз в три дня после еды в утренние часы в концентрации 20 млн экзосом/25 мл. По завершении курса в конце июля повторно были проведены лабораторные и инструментальные исследования с выявлением следующей динамики: СОЭ снизилась до 25 мм/ч, лейкоцитоз снизился до 10*109/мл, базофилы до 3%. По данным УЗИ сохраняется увеличение селезенки до тех же цифр (12 см*7 см*5 см). В миелограмме наблюдается снижение бластов до 3-4%.
Девушка 18 лет, диагноз В-клеточный острый лимфобластный лейкоз с декабря 2017 года, в анамнезе аллопеция на нервной почве (2014 год, в связи с разводом родителей), в остальном анамнез без особенностей. В общем анализе крови от февраля 2018 года эозинофилы 0%, определяются бластные формы до 6%, в миелограмме лимфобласты до 20%, CD19+, CD22+ и CD34+. Пациентке провели 5 курсов (продолжительность одного курса составляет 3 недели) терапии препаратом из модифицирующих экзосом per os. Режим приема препарат был следующий: 1 раз в три дня после еды в утренние часы в концентрации 20 млн экзосом/25 мл. По завершении курса определялась следующая динамика показателей лабораторных методов исследования: снижение бластных форм в общем анализе крови до 2%, в миелограмме снижение бластных форм до 9% при сохранении фенотипа.
Алгоритм заявленного способа:
Отбирают шприцем (5 мл) образец костного мозга от здорового донора, затем выделяют из него мононуклеарные клетки, путем смешивания образца 1:1 костного мозга от здорового донора с полной культуральной средой следующего состава: среда DMEM/F12 1:1 с HEPES (SigmaAldrich, Швейцария) с добавлением 2 ммоль/мл или 3,65 мг/10 мл (лиофилизат) L-глутамина (Панэко, Россия), 100 ед./мл пенициллина (Панэко, Россия), 100 мкг/мл стрептомицина (Панэко, Россия), 10% эмбриональной сыворотки (SigmaAldrich, Швейцария), затем полученную смесь наслаивают на раствор фиколла-урографина (Панэко, Россия) плотностью 1,077 г/см3 в соотношении 1:4, затем проводят центрифугирование (Jouan SA, Франция) при 1500 об/мин в течение 20 минут, собирают интерфазное кольцо, содержащее мононуклеарные клетки, которое смешивают с раствором Хэнкса (ThermoFisher, USA) в соотношении 1:10, центрифугируют (Jouan SA, Франция) при 1500 об/мин в течение 3 минут, собирают образовавшийся осадок, который 3 раза подвергают смешению с раствором Хэнкса (ThermoFisher, USA) в соотношении 1:10 с последующим центрифугированием (Jouan SA, Франция) при 1500 об/мин в течение 3 минут после каждого смешения, с получением на выходе осадка с монуклеарными клетками.
Полученный осадок с мононуклеарными клетками культивируют в полной культуральной среде следующего состава: среда DMEM/F12 1:1 с HEPES (SigmaAldrich, Швейцария) с добавлением 2 ммоль/мл (лиофилизата) L-глутамина (Панэко, Россия), 100 ед./мл пенициллина (Панэко, Россия), 100 мкг/мл стрептомицина (Панэко, Россия), 10% эмбриональной сыворотки (SigmaAldrich, Швейцария), в условиях Т=37°С и 5% CO2 (инкубатор Binder, Германия) в течение 72 часов, затем выделяют из полученной культуральной среды экзосомосодержащий осадок путем дифференциального центрифугирования (581 Or, Eppendorf, Германия), а именно: центрифугируют полученную культуральную среду при 3000 об/мин в течение 10 мин., затем собирают образовавшийся супернатант далее проводят центрифугирование при 10000 об/мин в течение 30 минут, затем отбирают образовавшийся супернатант и проводят ультрацентрифугирование при 100000 об/мин (Beckman Coulter, USA) в течение 2-х часов, далее отделяют образовавшийся осадок, растворяют его в фосфатно-солевом буфере (SigmaAldrich, Швейцария) в соотношение 1:5-1:20, и далее полученный раствор вводят per os пациенту с диагнозом лейкоз.
Эффективность применяемого способа возможно оценить по данным показателей лабораторных и инструментальных методов исследования, в частности, по данным цитометрического исследования клеток костного мозга (по изменениям в процентных соотношениях различных пулов клеток и по проценту содержания бластных клеток) и по данным цитологического исследования клеток периферической крови.
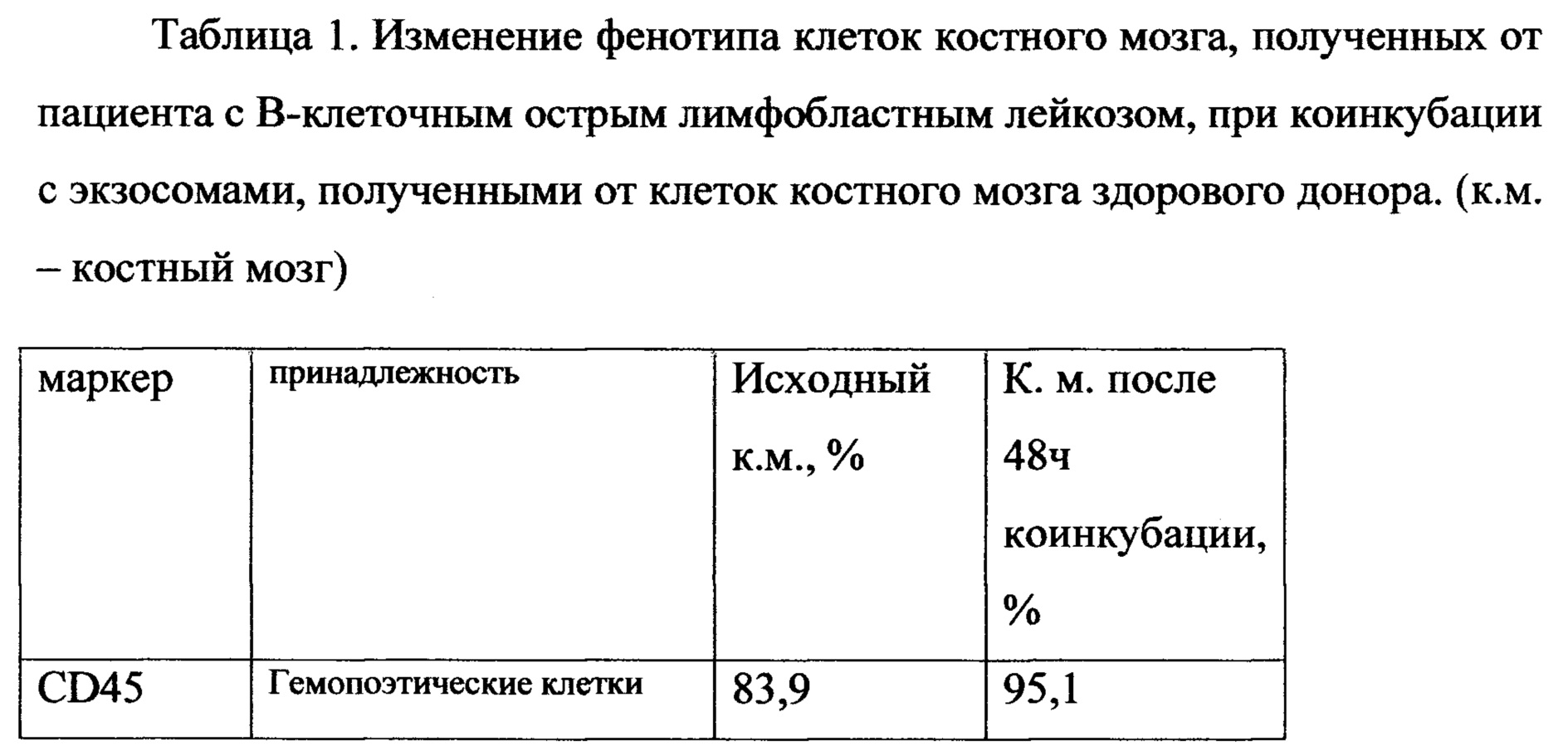
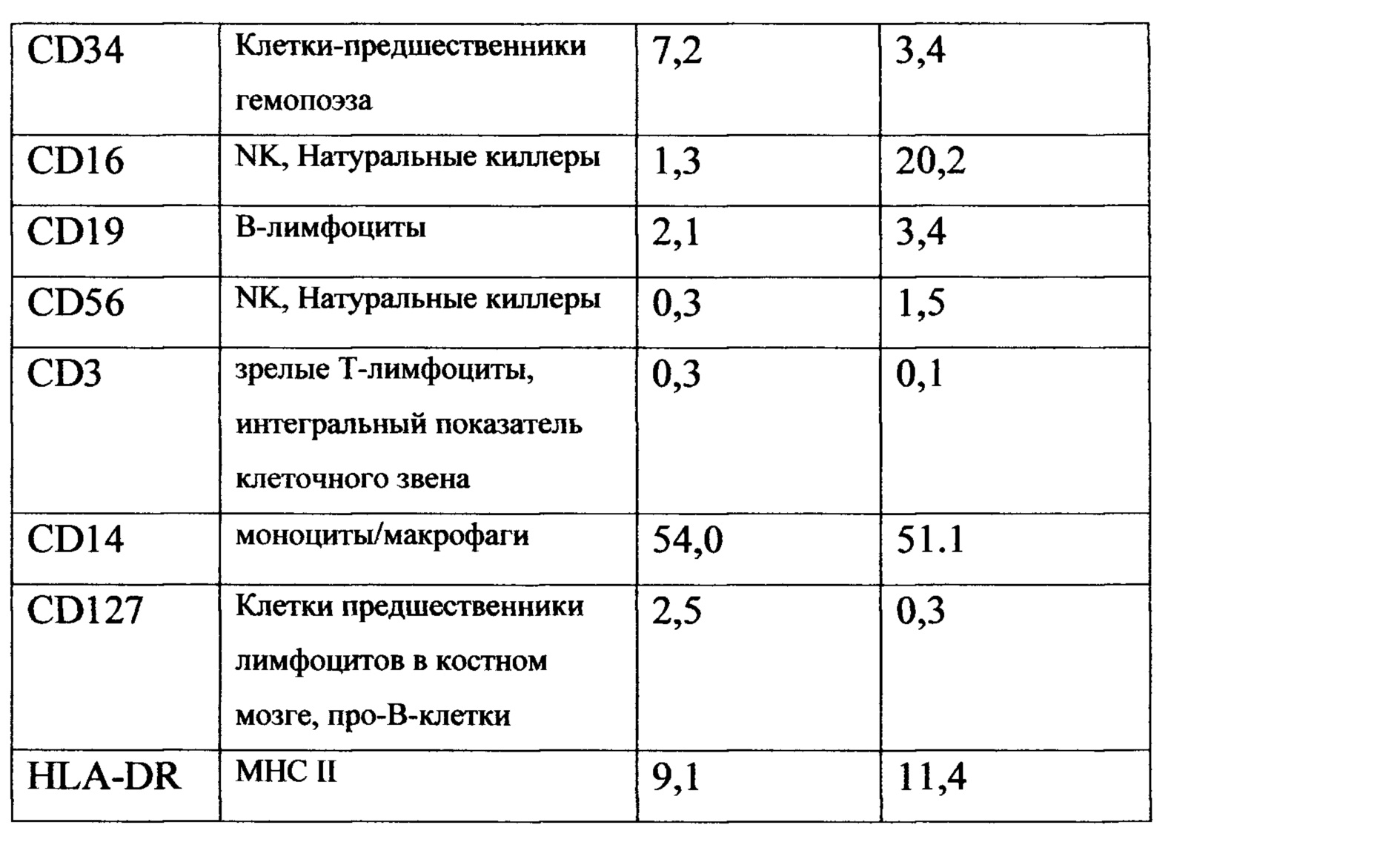
В таблице номер 1 представлены данные по изменению количественного соотношения различных пулов клеток, из которого следует, что при коинкубации экзосом из клеток костного мозга здорового донора (фиг. 1) с клеточной культурой (фиг. 2), полученной от пациента с диагнозом острый В-клеточный лимфобластный лейкоз увеличивается пул зрелых предшественников и уменьшается количество CD34+ клеток. Полученные данные свидетельствуют также о стимулировании неспецифического иммунитета за счета роста числа макрофагов и NK клеток, также о стимулировании специфического звена иммунитета (повышение HLA-DR+ и HLA-DR/127+ клеток) и гемопоэза.
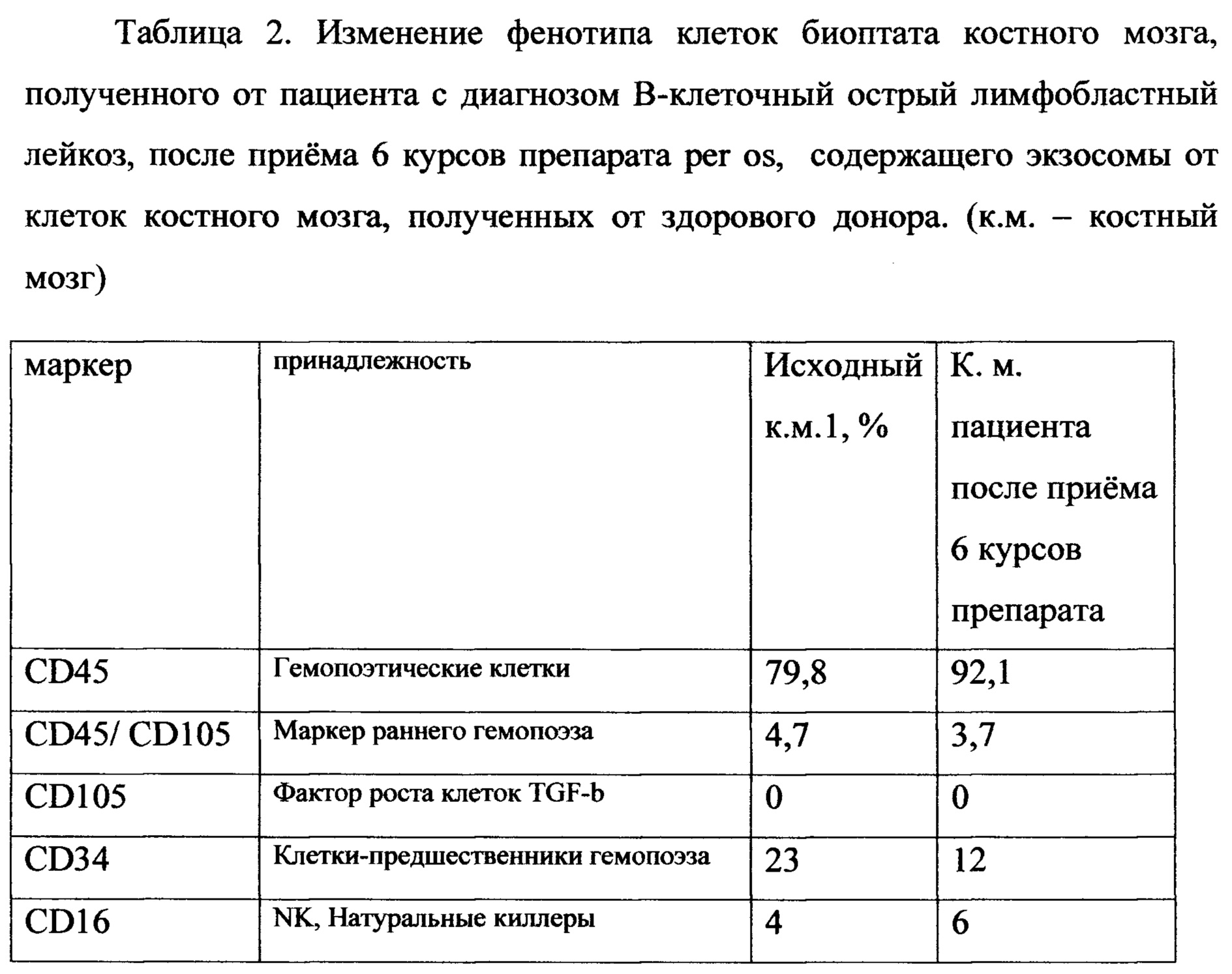
В таблице номер 2 представлены данные по изменению соотношения пулов клеток костного мозга пациента с острым В-клеточным лимфобластным лейкозом после приема 6 курсов препарата, содержащего экзосомы, полученные от клеток костного мозга здорового донора (фиг. 3). После проведения курса терапии уменьшается количество CD34+ клеток с 25% до 12%, т.е. значительно снижается пул бластных клеток.

На фигуре 1 представлена клеточная культура из клеток костного мозга здорового донора.
На фигуре 2 представлена клеточная культура от костного мозга пациента с диагнозом В-клеточный острый лимфобластный лейкоз
На фигуре 3 представлены клетки костного мозга пациента с диагнозом острый В-клеточный лимфобластный лейкоз (до и после соответственное) приема пациентом 6 курсов препарата, содержащего экзосомы от клеток костного мозга здорового донора.
Способ иммунотерапии раковых заболеваний, характеризующийся тем, что для пациентов с диагнозом лейкоз получают 5 мл костного мозга от здорового донора, затем выделяют из него мононуклеарные клетки путем смешивания образца костного мозга от здорового донора с раствором Хэнкса 1:1 или с полной культуральной средой следующего состава: среда DMEM/F12 1:1 с HEPES с добавлением 2 ммоль/мл или 3,65 мг/ 10 мл L-глутамина, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 10% эмбриональной сыворотки, затем полученную смесь наслаивают на раствор фиколла-урографина плотностью 1,077 г/см в соотношении 1:3-1:4, затем проводят центрифугирование при 1500 об/мин в течение 20 минут, собирают интерфазное кольцо, содержащее мононуклеарные клетки, которое смешивают с раствором Хэнкса в соотношении 1:10-1:20, центрифугируют при 1500 об/мин в течение 3 минут, собирают образовавшийся осадок, который 2-3 раза подвергают смешению с раствором Хэнкса в соотношении 1:10 с последующим центрифугированием при 1500 об/мин в течение 3 минут после каждого смешения, с получением на выходе осадка с монуклеарными клетками, далее культивируют полученные монуклеарные клетки в полной культуральной среде следующего состава: среда DMEM/F12 1:1 с HEPES с добавлением 2 ммоль/мл или 3,65 мг/10 мл L-глутамина, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 10% эмбриональной сыворотки, в условиях Т=37°С и 5% CO в течение 48-72 часов, затем выделяют из полученной культуральной среды экзосомосодержащий осадок путем дифференциального центрифугирования, а именно: центрифугируют полученную культуральную среду при 3000 об/мин в течение 10 мин, затем собирают образовавшийся супернатант, далее проводят центрифугирование при 10000 об/мин в течение 30 минут, затем отбирают образовавшийся супернатант и проводят ультрацентрифугирование при 100000 об/мин в течение 2-х часов, далее отделяют образовавшийся осадок, затем образовавшийся осадок растворяют в фосфатно-солевом буфере в соотношении 1:5-1:20 и далее полученный раствор вводят per os пациенту с диагнозом лейкоз 1 раз в три дня после еды в утренние часы, при этом число курсов приема составляет 3 или 5.


