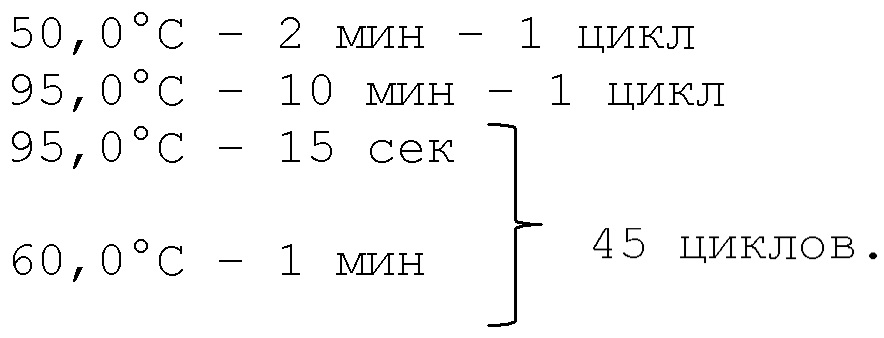Результат интеллектуальной деятельности: Способ прогнозирования выживаемости больных светлоклеточным почечно-клеточным раком
Вид РИД
Изобретение
Область техники
Заявляемое изобретение относится к области биомедицины, конкретно к онкологии, способам прогнозирования исхода заболевания у больных раком почки и может быть использовано для определения подходов к лечению, оптимальных сроков динамического наблюдения за больными и объема обследования.
Рак почки занимает третье место по частоте среди онкоурологических заболеваний. Наиболее частым типом рака почки (70-80%) является светлоклеточный почечно-клеточный рак. Важную роль в выборе тактики лечения больных светлоклеточным почечно-клеточным раком (скПКР) играют факторы прогноза. Однако особенностью протекания этого заболевания является непредсказуемость развития, что затрудняет выбор тактики лечения. Для повышения эффективности лечения необходимы методы, позволяющие прогнозировать развитие заболевания, особенно выживаемость больных. Существующие способы и методы такого прогноза не обладают достаточными характеристиками для надежного прогнозирования.
Уровень техники
Известен способ прогнозирования развития гематогенных метастазов после комбинированного лечения при раке почки путем исследования пациента, отличающееся тем, что в ткани опухоли определяют тотальную активность протеасом, экспрессию NF-kB р50, HIF-1α содержание сосудистого эндотелиального фактора роста VEGF и рассчитывают дискриминантные функции Y1, Y2 по уравнениям:
Y1=-3,2+0,026·Х1+0,03·Х2-0,02·Х3+0,34·Х4+0,3·Х5
Y2=-33,3-0,01·Х1+0,11·Х2-1,2·Х3+1,57·Х4+1,8·Х5,
где X1 - тотальная активность протеасом ·10-3 МЕ/мг белка;
Х2 - содержание VEGF, пг/мг белка;
Х3 - экспрессия HIF-1α, УЕ/мг белка в лунке;
Х4 - экспрессия NF-κВ р50, УЕ/мг белка в лунке;
Х5 - коэффициент NF-κВ р65/50;
и при Y1>Y2 прогнозируют отсутствие, а при Y1<Y2 прогнозируют развитие гематогенных метастазов.
Информативность данных критериев обоснована наличием связи экспрессии NF-кВ p50, HIF-1α и VEGF с возникновением гематогенных метастазов рака почки, полученное при исследовании 65 больных почечноклеточным раком (RU 2528100).
Известен способ прогнозирования исхода заболевания у больных метастатическим раком почки, при котором проводят морфологическое и иммуногистохимическое исследование операционного материала, отличающийся тем, что определяют уровень экспрессии транскрипционного фактора HIF-1α и сосудистого эндотелиального фактора роста VEGF и при уровне HIF-1α более 6,35 УЕ/мг белка в лунке и VEGF более 32 пг/мг белка прогнозируют благоприятный исход заболевания, а при уровне HIF-1α менее 6,35 УЕ/мг белка в лунке и VEGF менее 32 пг/мг белка прогнозируют неблагоприятный исход заболевания (RU 2589286)
Известен способ прогнозирование возможного исхода заболевания у больных с метастатическим светлоклеточным раком почек после нефрэктомии или резекции почки. Для этого проводят морфологическое и иммуногистохимическое исследование операционного материала. Определяют уровень пролиферативной активности опухоли по экспрессии антигена Ki-67 и экспрессию онкогена мутантного типа p53. Гистологическую степень злокачественности опухоли определяют по значению среднего диаметра ядер опухолевых клеток, наличию или отсутствию ядрышек в ядрах опухолевых клеток. Прогноз онкологической выживаемости рассчитывают по формуле
УМБП=1,83Х1+1,45Х2+1,18Х3,
где УМБП - морфо-биомолекулярный показатель;
X1 - гистологическая степень злокачественности опухоли;
Х2 - уровень экспрессии Ki-67;
Х3 - уровень экспрессии p53.
и при значении умбп≤6,29 прогноз онкологической выживаемости больных скПКР расценивают как благоприятный, при умбп=6,82-8,92 - как относительно благоприятный, при умбп=9,19-11,55 как относительно неблагоприятный, при умбп>11,55 - как неблагоприятный. (RU №2438127, прототип).
Недостатками перечисленных известных способов являются сложность, низкие чувствительность и специфичность, применимость только при метастатическом раке почки, а также длительность исследований и низкая точность прогнозирования выживаемости больных скПКР.
Техническая проблема, разрешаемая созданием заявляемого изобретения – необходимость разработки более точных маркеров и способов оперативного прогноза. Разрешение этой проблемы позволит прогнозировать выживаемость конкретного больного и, таким образом, персонализировать лечение, расширить арсенал клинически удобных, требующих очень малого количества (менее 1 мкг) мРНК, что дает возможность использовать заявляемый способ для анализа уровня экспрессии мРНК генов в образцах малого размера, для эффективного способа прогнозирования выживаемости больных скПКР на основе найденной группы генов - CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2 – путем выявления уровня экспрессии мРНК нескольких их этих генов или их комбинаций.
Технический результат при использовании заявляемого способа, обеспечивающий разрешение указанной проблемы заключается в расширении возможностей его применения для прогнозирования выживаемости и обоснованного выбора тактики лечения больных скПКР на разных стадиях развития благодаря повышению чувствительности, специфичности и достоверности результатов прогнозирования, упрощению технологии, сокращению длительности процедур и, тем самым, в увеличению производительности и эффективности исследований.
Сущность изобретения состоит в том, что способ прогнозирования выживаемости больных светлоклеточным почечно-клеточным раком (скПКР) предусматривает получение образцов из опухолевой и нормальной ткани почки, выделение из них мРНК, выполнение обратной транскрипции мРНК и полимеразной цепной реакции в реальном времени (ПЦР-РВ) с продуктами обратной транскрипции с помощью наборов праймеров, специфичных к продуктам обратной транскрипции мРНК генов, для измерения уровня экспрессии мРНК, на основании которого делают прогноз выживаемости больных скПКР путем сравнения уровня экспрессии мРНК генов из группы CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2 в образцах из опухолевой ткани с уровнем экспрессии тех же генов в образцах из нормальной ткани, соотнесенных с уровнями экспрессии мРНК эндогенного контрольного гена, исходя из того, что:
- в том случае, если значения уровня экспрессии мРНК образцов опухолевой ткани не менее трех генов из группы CA9, VWF, BHLHE41, EGLN3 и PLIN2 превышают уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а также в том случае, если значения уровня экспрессии мРНК образцов опухолевой ткани не менее двух генов из группы CA9, VWF, BHLHE41, EGLN3 и PLIN2 превышают уровень экспрессии мРНК тех же генов в образцах нормальной ткани и, одновременно, значение уровня экспрессии мРНК гена BAP1 ниже уровня экспрессии мРНК этого гена в образцах нормальной ткани, результаты проведенных измерений свидетельствуют в каждом из этих случаев, о благоприятном прогнозе 3,5-летней выживаемости больных с момента постановки диагноза.
Предпочтительно, в качестве мРНК эндогенного контрольного гена используют мРНК гена из группы: GAPDH и ACTB, а прогноз признают благоприятным в том случае, если значения уровня экспрессии мРНК образцов опухолевой ткани генов, выбранных для анализа из группы CA9, VWF, BHLHE41, EGLN3 и PLIN2 превышают, по меньшей мере, в 3,3; 2; 2; 3,5 и 1,5 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а также в том случае, если значение уровня экспрессии мРНК выбранного для анализа гена BAP1 ниже, по меньшей мере, в 2,5 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани.
Предпочтительно, выделение мРНК образцов из опухолевой и нормальной ткани почки проводят путем лизиса образцов в растворе гуанидинтиоционата, сорбции мРНК на колонках, отмывках мРНК в спиртовых растворах и элюции мРНК.
Предпочтительно, наличие и качество выделенной мРНК проверяют с помощью электрофореза в 1,8% агарозном геле при постоянной силе тока 130 мА в течение 30 мин, а оценку полученных электрофорезом фрагментов проводят на трансиллюминаторе в ультрафиолетовом свете.
Предпочтительно, https://ru.wikipedia.org/wiki/%D0%90%D0%BC%D0%BF%D0%BB%D0%B8%D1%84%D0%B8%D0%BA%D0%B0%D1%86%D0%B8%D1%8F_%28%D0%BC%D0%BE%D0%BB%D0%B5%D0%BA%D1%83%D0%BB%D1%8F%D1%80%D0%BD%D0%B0%D1%8F_%D0%B1%D0%B8%D0%BE%D0%BB%D0%BE%D0%B3%D0%B8%D1%8F%29 - cite_note-1амплификацию при полимеразной цепной реакции (ПЦР-РВ) проводят в режиме реального времени в термоциклере в следующих режимах:

причем в диапазоне температуры 60,0°С – 95,0°С производят снятие кривой плавления путем наблюдения интенсивности флуоресценции продуктов ПЦР (ампликонов) при ступенчатом изменении температуры с шагом в 1°С.
Предпочтительно, перед проведением реакции обратной транскрипции выравнивают концентрации мРНК в контрольных и экспериментальных образцах из опухолевой и нормальной ткани почки, смешивают водный раствор мРНК (0,3 – 1,5 мкг) с гексапраймером Random 6 и реакционной смесью, включающей: буфер 5x, MgCl2 – 25mM, dNTP – 10 mM, а обратную транскрипцию вышеупомянутой смеси проводят в термоциклере в следующих режимах: 250С – 10 мин. , 420С – 1час, 700С – 10мин.
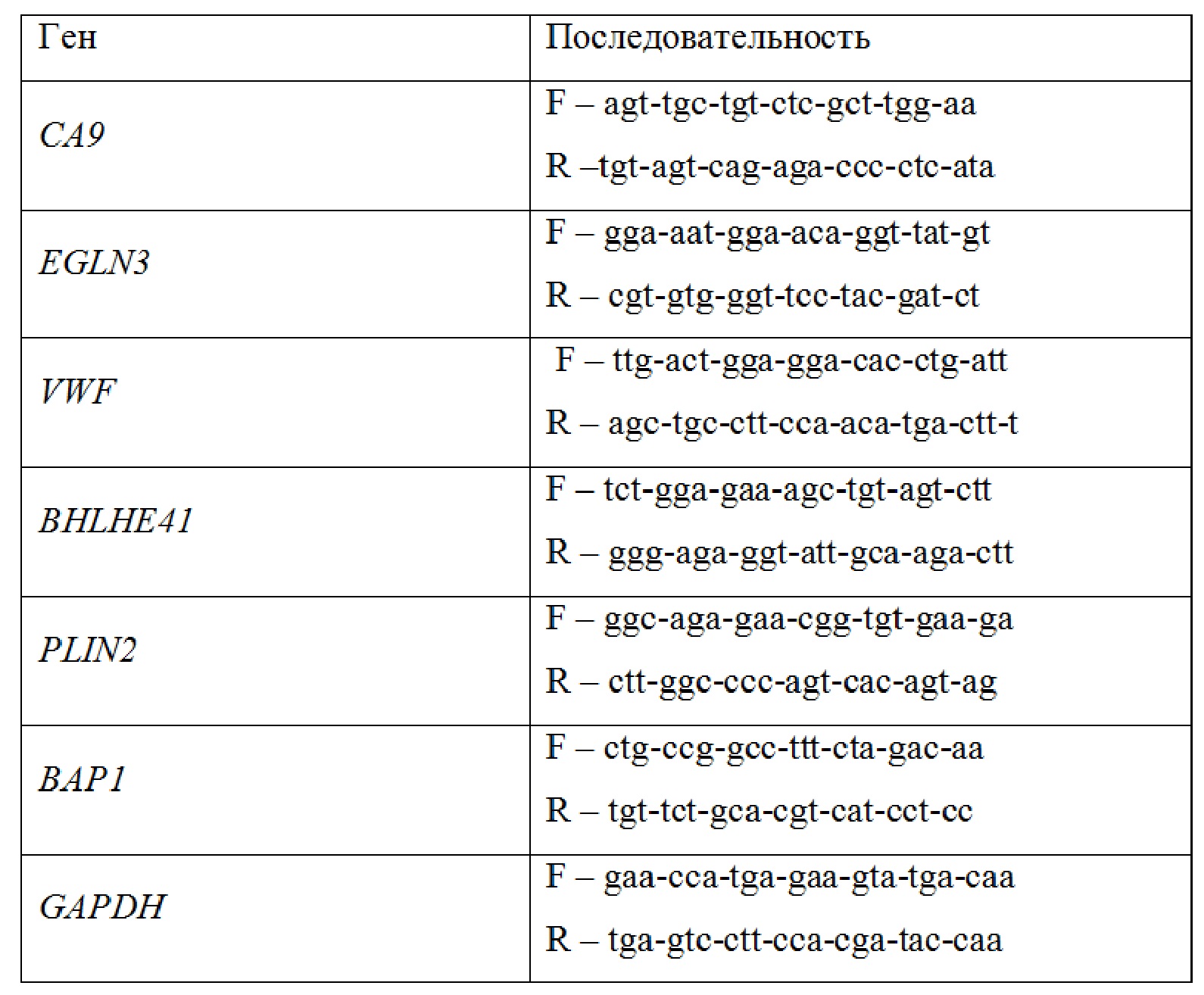
В частных случаях реализации способа определяют уровень экспрессии мРНК генов с использованием красителя Eva Green, для чего для каждого исследуемого гена конструируют олигонуклеотидные F - прямой праймер и R - обратный праймер следующей структуры и состава
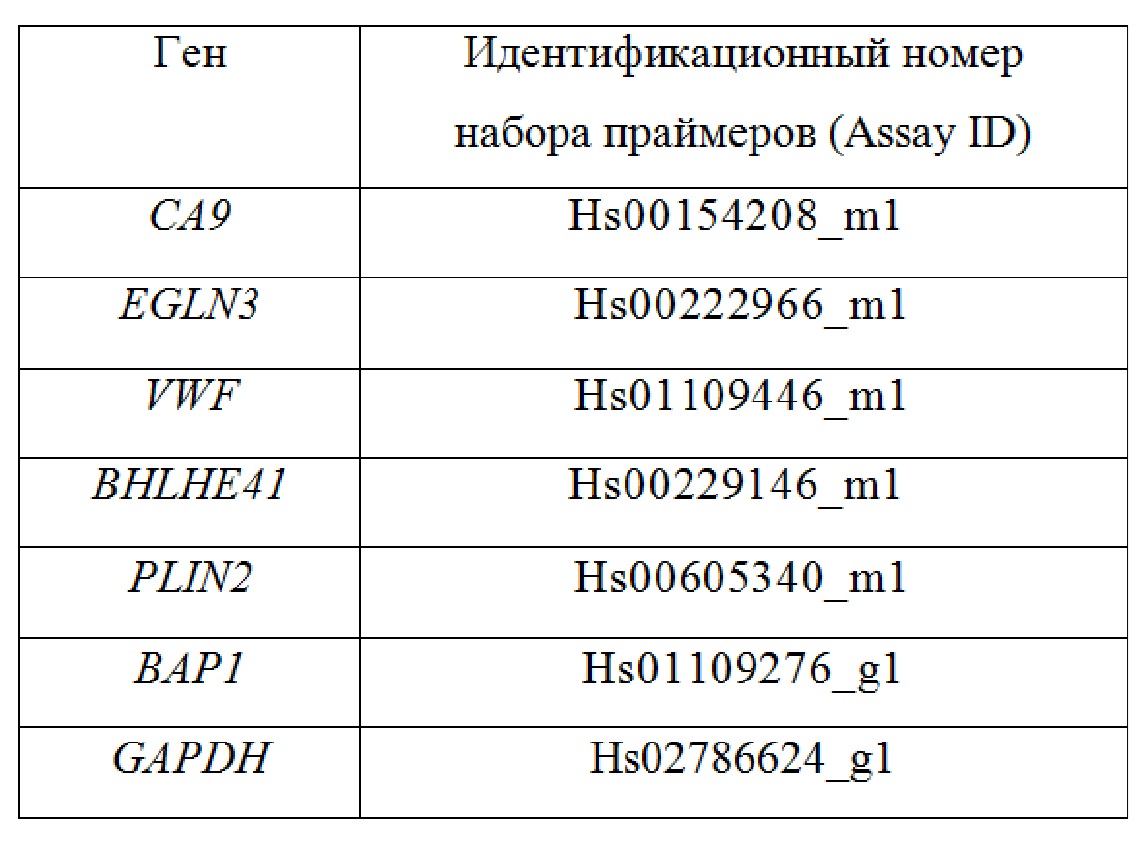
В иных частных случаях реализации определяют уровень экспрессии генов с использованием наборов праймеров TaqMan® Gene Expression Assay, в следующих сочетаниях указанных наборов и генов.
При этом для каждого исследуемого образца из опухолевой и нормальной ткани почки, составляют смесь общим объемом 20 мкл, содержащую: 1мкл. набора праймеров TaqMan® Gene Expression Assay, 10 мкл. набора TaqMan® Gene Expression Master Mix, 1,6 мкл. комплементарной ДНК (1 мкл.), 7,4 мкл. деионизированной воды, которую встряхивают на вортексе и центрифугируют в течение 5 сек., а ПЦР-РВ проводят на приборе Step One Plus в следующих режимах:

Настоящее изобретение основано на том, что обнаружено и подтверждено наличие ассоциации уровней экспрессии группы генов с прожитием более и менее 3,5 лет. Анализ уровней экспрессии матричной РНК (мРНК) 200 генов в опухолях скПКР и нормальной ткани того же органа позволил выявить 4 гена, связанных с выживаемостью больных раком почки: CA9, VWF, BHLHE41 и EGLN3. Было выяснено, все эти гены прямо регулируются транскрипционным фактором HIF1α. Дополнительно на связь экспрессии с выживаемостью были проанализированы шесть генов, 4 регулируемых транскрипционным фактором HIF2α: PLIN2, CCND1, MMP1, SK1 и два гена, связанных с выживаемостью больных скПКР по данным литературы: MKI67, BAP1. Надежную ассоциацию с выживаемостью продемонстрировали гены BAP1 и PLIN2.
В результате сформирован набор (панель) генов для прогнозирования выживаемости на основе измерения уровня экспрессии мРНК в опухолевых образцах и образцах нормальной ткани одного и того же органа, включающий гены CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2.
Реализация изобретения
Способ прогнозирования выживаемости больных светлоклеточным почечно-клеточным раком (скПКР) реализуется следующим образом.
Использование настоящего изобретения предусматривает измерение уровня экспрессии мРНК генов в опухоли относительно нормальной (гистологически не измененной) ткани почки.
Способ предусматривает следующие основные процедуры: выделение мРНК из операционного материала опухолевой и нормальной ткани почки; обратная транскрипция мРНК; полимеразная цепная реакция в реальном времени (ПЦР-РВ) с продуктами обратной транскрипции, оценка качества проведенной ПЦР-РВ, анализ полученных данных, определение качества и измерение концентрации водного раствора суммарной мРНК;
Выделение мРНК.
Выделение мРНК из материала выполняется с помощью, например, набора RNeasy Mini Kit (QIAGEN, США) согласно инструкции к набору. Метод основан на лизисе образцов в растворе гуанидинтиоционата, сорбции мРНК на колонках, отмывках мРНК в спиртовых растворах и элюции РНК.
Наличие и качество мРНК проверяется с помощью, например, электрофореза в 1,8% агарозном геле. Электрофорез проводится, например, в горизонтальном аппарате для электрофореза SUB CELL 96 BIO-RAD производства США при постоянной силе тока 130 мА в течение 30 мин. Оценка полученных фрагментов может быть проведена на трансиллюминаторе Whatman-Biometra TL-3 в ультрафиолетовом свете. К качественным относятся образцы с четкими полосами 18S и 28S РНК на картине электрофореза без видимой примеси ДНК.
Концентрация водного раствора мРНК определяется, например, на спектрофотометре Nanodrop 1000 (Thermo Scientific, США) согласно инструкции к прибору.
В случае определения уровня экспрессии с использованием красителя Eva Green реакцию обратной транскрипции проводили с использованием набора ImProm-II™ Reverse Transcription System (США) в соответствии с инструкцией производителя. Перед проведением реакции обратной транскрипции концентрации мРНК выравнивали в контрольных и экспериментальных образцах. Далее водный раствор РНК (0,3 – 1,5 мкг) смешивали с гексапраймером Random 6 и реакционной смесью (буфер 5x, MgCl2 – 25mM, dNTP – 10 mM, обратная транскриптаза) вышеупомянутого набора и проводили реакцию в термоциклере (ЗАО НПФ ДНК - Технология, Россия). С заданной программой 250С – 10 мин., 420С – 1час, 700С – 10мин.
Для анализа с помощью красителя Eva Green были сконструированы олигонуклеотидные праймеры для полимеразной цепной реакции в реальном времени (ПЦР-РВ) следующей структуры и состава (таблица 1).

Предпочтительно, для подготовки каждого исследуемого образца, составляется смесь общим объемом 25 мкл, содержащую: по 0,25 мкМ каждого оригинального олигонуклеотида (праймера); по 200 мкМ каждого нуклеозидтрифосфата; 1,0 единица активности taq – полимеразы (СибЭнзим, Россия); буфер для ПЦР (670 мМ трис pH 8,8, 166 мМ сульфата аммония, 20 мМ MgCl2 и 0,1% Tween 20); интеркалирующий краситель SYBR Green1 0,1 мкл (100x), затем полученную смесь встряхивают на вортексе и центрифугируют в течение 5 сек., а амплификацию проводят в термоциклере в режиме:

причем в диапазоне температуры 60,0°С – 95,0°С производят снятие кривой плавления ПЦР продуктов с шагом в 1°С.
В случае определения уровня экспрессии с использованием наборов TaqMan все процедуры проводятся в соответствии с инструкцией производителя.
Определение уровней экспрессии мРНК методом TaqMan проводится с использованием наборов TaqMan® Gene Expression Assay фирмы Applied Biosystems, США. Перечень наборов TaqMan приведен в таблице 2.
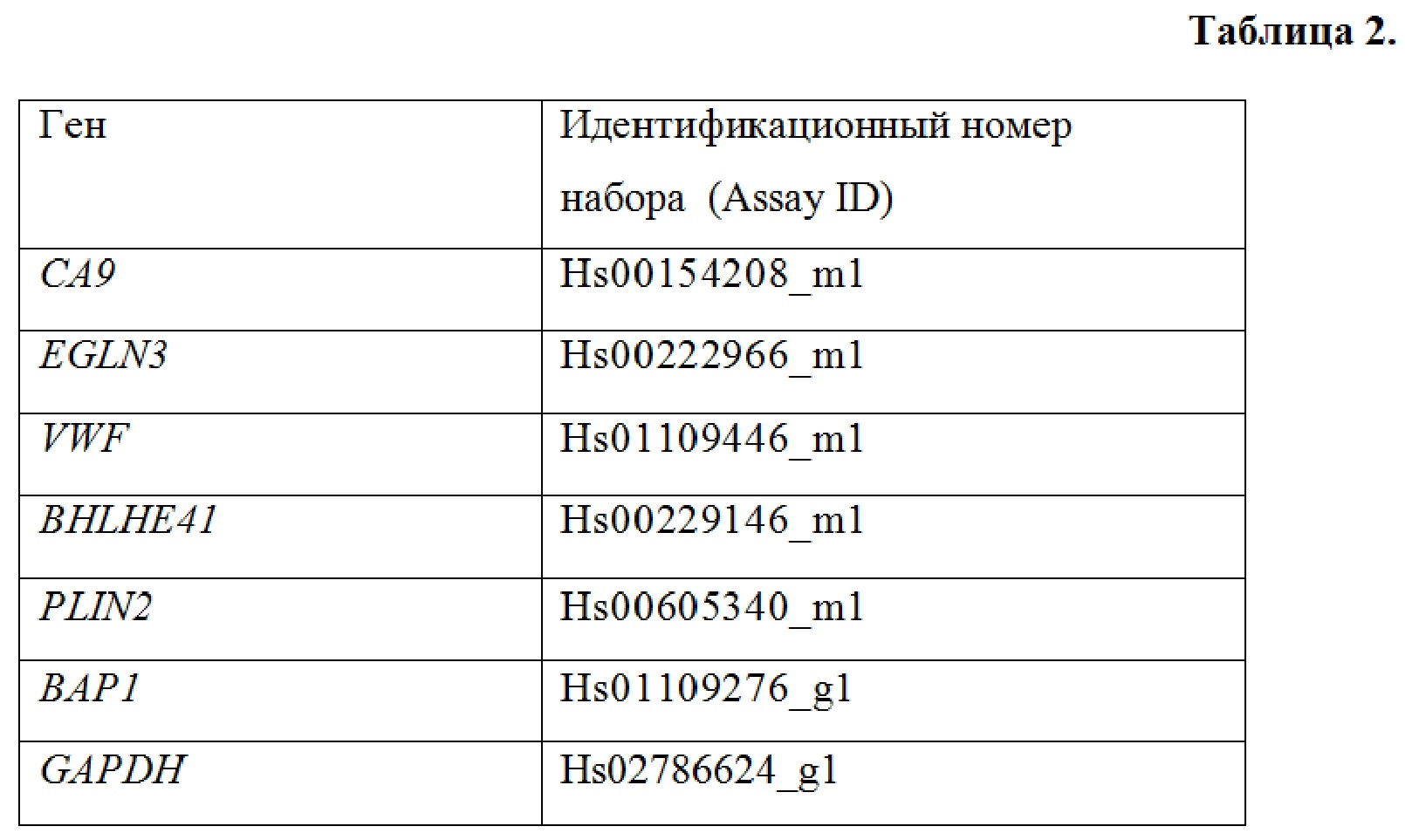
Для каждого образца, составляют смесь общим объемом 20 мкл, содержавшую: 1мкл TaqMan® Gene Expression Assay, 10 мкл TaqMan ® Gene Expression Master Mix, 1,6 мкл комплементарной ДНК (1-100 нг), 7,4 мкл деионизированной воды. Полученную смесь встряхивали на вортексе и центрифугировали в течение 5 сек. ПЦР-РВ проводили на приборе Step One Plus (Applied Biosystems, США) в следующем режиме:
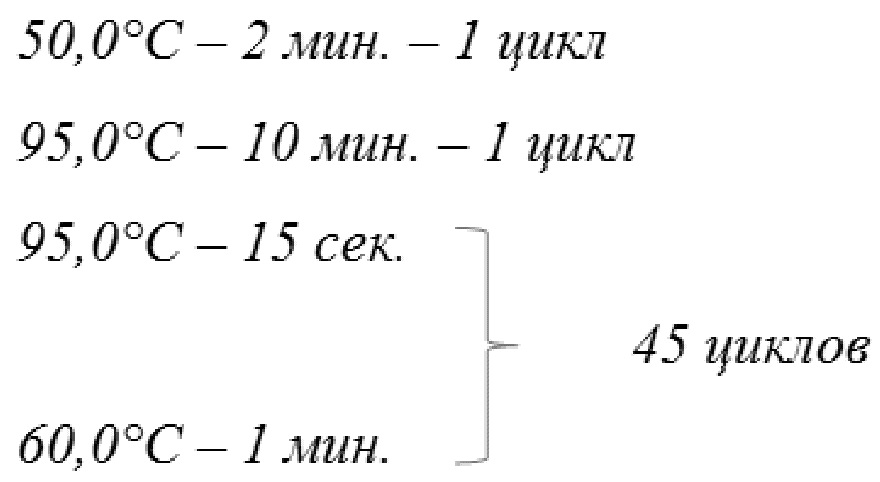
Выполняется ПЦР-РВ для определения уровня экспрессии мРНК каждого гена, выбранного из группы CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2, как для образцов опухолевой ткани, так и для образцов нормальной ткани. В каждом эксперименте предусмотрен негативный контроль (ПЦР-смесь без матрицы - кДНК).
В качестве эндогенных контролей используются гены GAPDH и ACTB.
При анализе результатов данные, полученные относительно эндогенного контрольного гена GAPDH или ACTB, являлись сопоставимыми (эквивалентными). Указанные гены используются в качестве контрольных, так как экспрессируются в исследуемых клетках и тканях независимо от статуса заболевания на примерно одинаковом уровне (то есть, количества мРНК этих генов примерно одинаковы) в образцах опухоли и в нормальной ткани. Их применение позволяет нормировать суммарное количество РНК. В результатах (примерах 1-5) представлены данные относительно гена GAPDH или ACTB. Результаты сравнения уровня экспрессии мРНК генов (генов-маркеров) из группы CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2 в образцах из опухолевой ткани с уровнем экспрессии тех же генов в образцах из нормальной ткани, соотнесенных с уровнями экспрессии мРНК эндогенного контрольного гена, выражают как отношение экспрессии мРНК гена-маркера относительно экспрессии мРНК эндогенного контрольного гена в образце опухоли к такому же соотношению в образце нормальной ткани.
Относительные количества мРНК в опухолевой и нормальной ткани, соотнесенные с уровнями мРНК эндогенного контрольного гена, вычисляются с помощью программного обеспечения Step One Software. В результате получают значения изменения экспрессии в опухолевой ткани относительно нормальной (RQ). Уровень снижения мРНК равен 1/RQ и показывает, во сколько раз содержание мРНК гена снижено в опухоли по сравнению с нормальными тканями, уровень повышения мРНК равен RQ и показывает, во сколько раз содержание мРНК гена повышено в опухоли по сравнению с нормальными тканями.
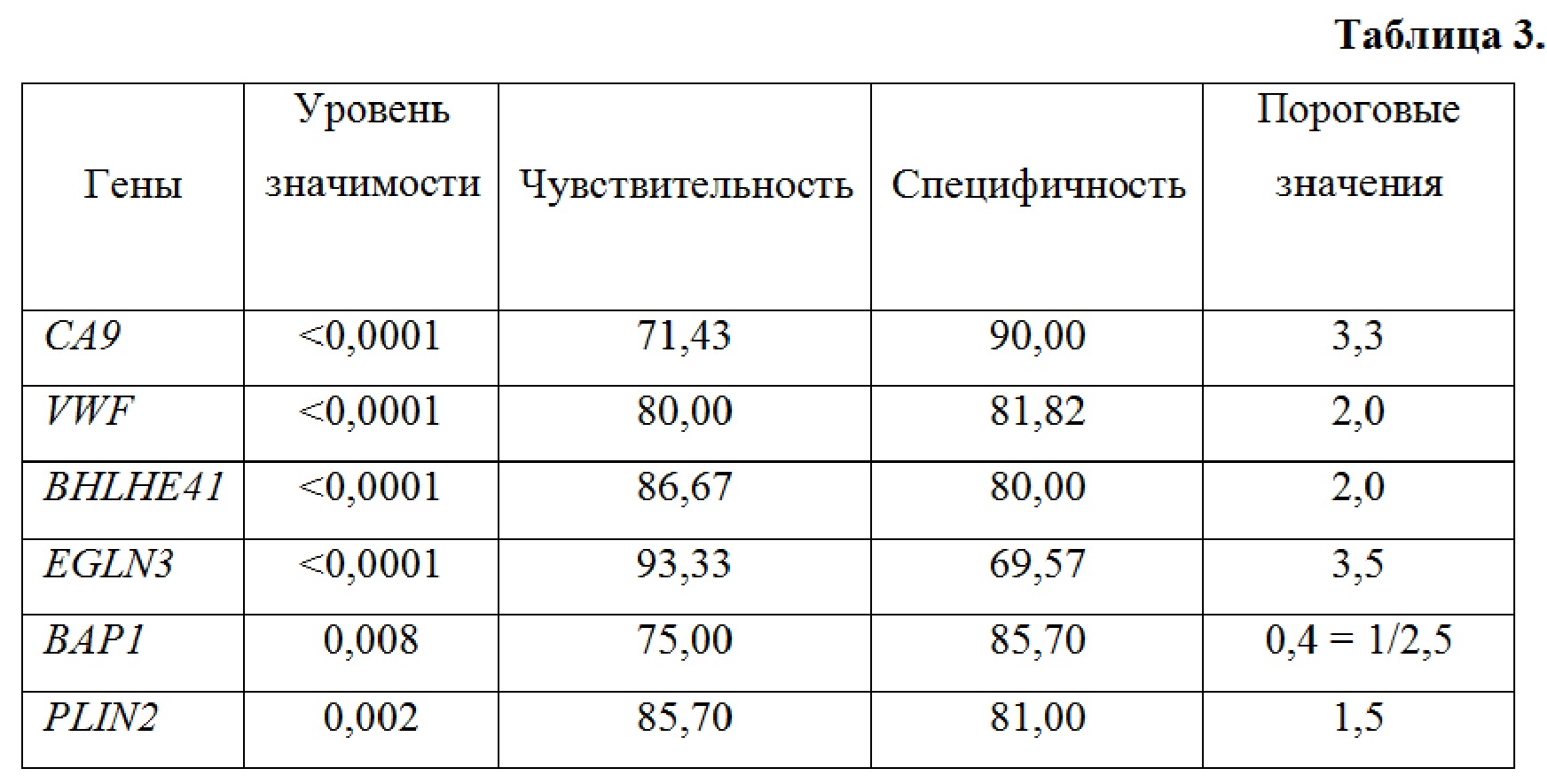
Больных разделили на две группы: с длительностью жизни больше 3,5 лет (благоприятный прогноз) и менее 3,5 лет (неблагоприятный прогноз) с момента постановки диагноза. Для выявления статистически значимых различий в уровнях экспрессии генов в группах больных с разной продолжительностью жизни применили ROC-анализ. Полученные данные, показывающие связь экспрессии генов с выживаемостью: ROC анализ, представлены в таблице 3.
Основой ROC-анализа является построение ROC-кривой, которая отражает зависимость доли правильно классифицированных положительных результатов от доли ложноположительных результатов. Такие кривые называют Receiver Operating Characteristic curve — «операционные характеристические кривые наблюдателя», или, сокращенно, ROC-curve (ROC-кривые), а действия, выполняемые для их построения и расчетов значимости различий, значений чувствительности и специфичности — ROC-анализом.
Как следует из данных в табл. 2, все 6 генов - CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2 - имеют статистически значимые отличия по уровню экспрессии между группами больных скПКР с разной длительностью жизни. Значения уровня экспрессии этих генов, превышающие определенный критерий отсечения (или находящиеся ниже в случае гена BAP1), свидетельствуют о благоприятном прогнозе 3,5-летней выживаемости. Чувствительность определения выживаемости с помощью экспрессии этих генов находится в интервале 71% - 93%, специфичность - в интервале 70% - 90%. То есть, эти показатели достаточно высокие. Полученные значения площади под кривой AUC показывают, гены CA9, VWF, BHLHE41 и EGLN3 являются отличными классификаторами, а гены BAP1 и PLIN2 - хорошие классификаторы больных скПКР по прогнозируемой продолжительности жизни.
При этом выявление уровня экспрессии генов CA9, VWF, BHLHE41, EGLN3, и PLIN2 выше критерия отсечения в пораженной раком ткани человека, по сравнению со здоровой тканью почки (или ниже в случае гена BAP1) служит прогностическим признаком выживаемости больных скПКР. Заявленный способ прогнозирования выживаемости больных скПКР позволяет на основе уровня экспрессии генов или их комбинаций с высокой специфичностью и чувствительностью прогнозировать выживаемость больных скПКР.
Процедура реализации способа прогнозирования выживаемости больных светлоклеточным почечно-клеточным раком состоит в том, что у обследуемых лиц берут образцы пораженной раком ткани почки и нормальной ткани того же органа, производят выделение и очистку РНК из взятых образцов и производят методом ПЦР в реальном времени анализ уровня экспрессии РНК с применением праймеров, специфичных к продуктам обратной транскрипции РНК генов, прогнозируют выживаемость больных скПКР по уровню экспрессии в раковой опухоли относительно нормальной ткани какого-либо гена из группы генов: CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2 или их комбинаций.
Анализ связи уровня экспрессии мРНК набора указанных 6 генов с выживаемостью больных скПКР может быть осуществлен рядом методов. В частности была проведена оценка значимости различий кривых выживаемости, построенных по Каплан-Мейеру. Программное обеспечение позволяет построить кривые выживаемости больных, характеризующиеся разным уровнем экспрессии генов – выше или ниже критерия отсечения, определенного при ROC – анализе. Статистическую значимость различий кривых выживаемости при разном уровне экспрессии генов оценивали с помощью лог-ранк теста.
Результаты сравнения кривых выживаемости с помощью лог-ранк теста представлены в таблице 4.
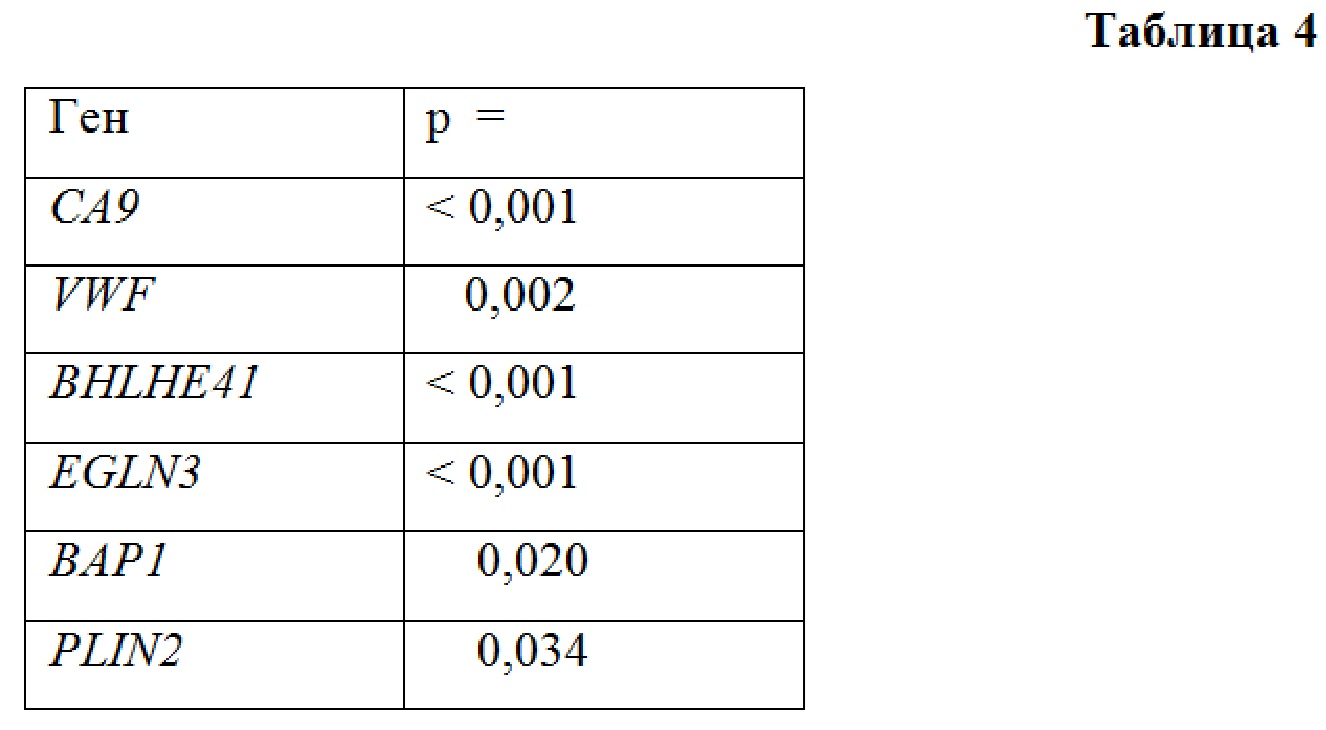
Для увеличения надежности результатов было использовано несколько статистических критериев. Результаты, полученные с помощью точного критерия Фишера, представлены в таблице 5. Пороговые значения уровней экспрессии, использованные при этой статистической обработке, были определены при ROC-анализе.
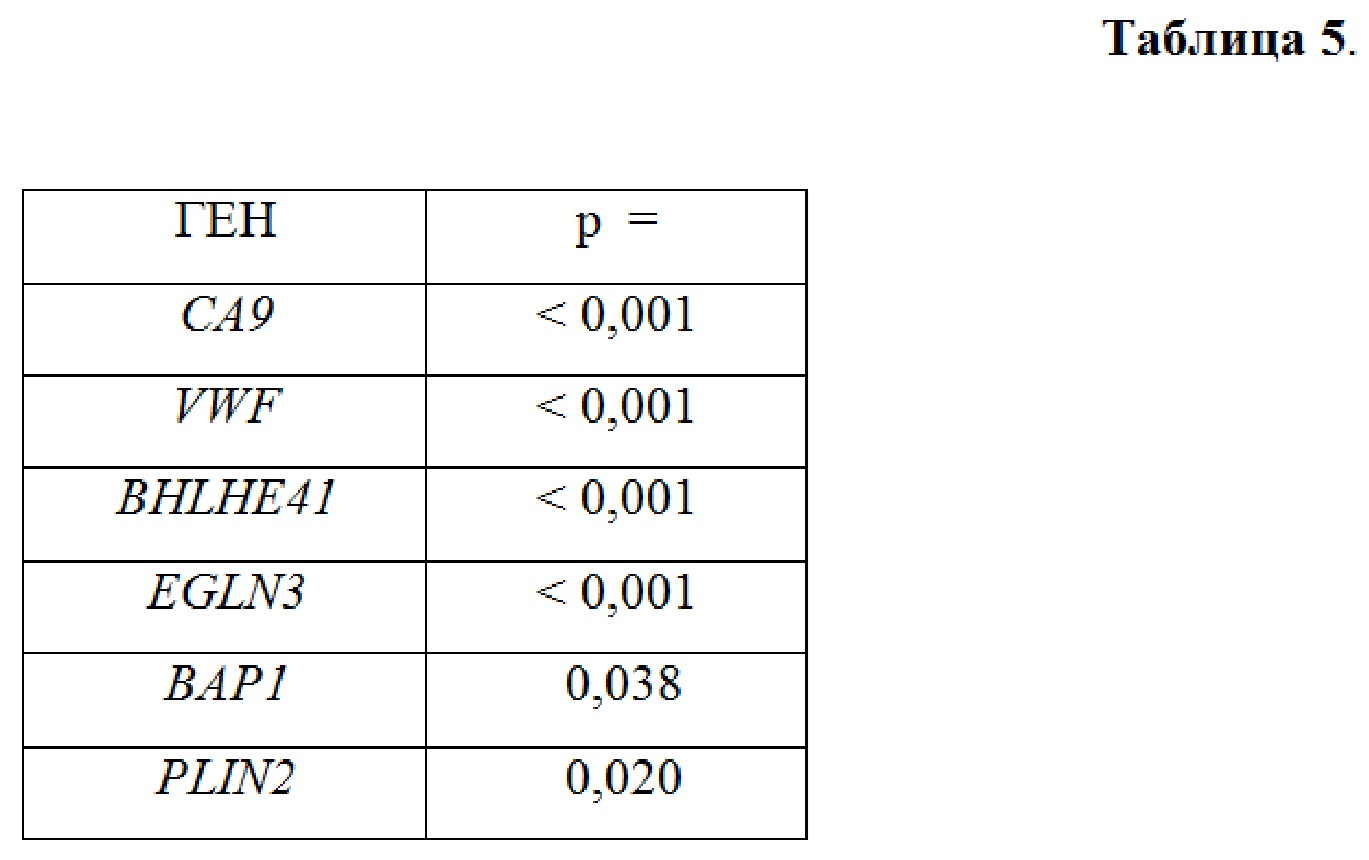
Как видно из данных в табл. 5, значимо связанной с выживаемостью оказалась экспрессия тех же генов, которые были выявлены при ROC-анализе и тесте лог-ранк (таблицы 3 и 4).
Показатели общей выживаемости оказались существенно выше у больных с повышенной экспрессией генов CA9, VWF, BHLHE41, EGLN3, PLIN2 и с пониженной экспрессией гена BAP1 в опухоли, по сравнению с пациентами, у которых экспрессия этих генов снижена или повышена в случае гена BAP1 (в среднем доля проживших более 3,5 лет различается почти в 5 раз в связи с уровнем экспрессии).
Повышение экспрессии генов CA9, VWF, BHLHE41, EGLN3, PLIN2 и понижение экспрессии гена BAP1 является благоприятным прогностическим фактором для срока жизни больных, а снижение экспрессии этих генов или повышение в случае гена BAP1 – неблагоприятным.
Указанные гены с высокими значениями чувствительности и специфичности могут выступать в качестве маркеров 3,5-летней выживаемости. Для улучшения показателей чувствительности и специфичности выявленных маркеров, а также увеличения надежности показателей, применили анализ с использованием одновременно нескольких генов. При этом получили несколько панелей маркеров 3,5-летней выживаемости. В зависимости от задачи анализа можно использовать различные панели.
Для подтверждения справедливости изложенного выше способа проведены исследования, конкретные результаты которых приведены в частных примерах 1-5, следующим образом.
Получали образцы опухолевой и нормальной ткани почки больных светлоклеточным почечно-клеточным раком (скПКР), в которых исследована экспрессия мРНК генов из группы CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2, соотнесенная с уровнями экспрессии мРНК эндогенного контрольного гена (GAPDH или ACTB). Использование указанных эндогенных контрольных генов обеспечивает точность и высокое разрешение при количественном определении данных экспрессии мРНК генов из группы CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2.
ПЦР-РВ для определения уровня экспрессии мРНК каждого гена, выбранного из группы CA9, VWF, BHLHE41, EGLN3, BAP1 и PLIN2, как для образцов опухолевой ткани, так и для образцов нормальной ткани осуществляли в трех повторностях (троекратно).
Из указанных образцов выделена мРНК путем лизиса образцов в растворе гуанидинтиоционата, сорбции мРНК на колонках, отмывках мРНК в спиртовых растворах и элюции мРНК. Наличие и качество выделенной мРНК проверены с помощью электрофореза в 1,8% агарозном геле при постоянной силе тока 130 мА в течение 30 мин, а оценка полученных электрофорезом фрагментов проведена на трансиллюминаторе в ультрафиолетовом свете. Перед проведением реакции обратной транскрипции выравнивали концентрации мРНК в контрольных и экспериментальных образцах из опухолевой и нормальной ткани почки, смешивали водный раствор мРНК (0,3 – 1,5 мкг) с гексапраймером Random 6 и реакционной смесью, включающей: буфер 5x, MgCl2 – 25mM, dNTP – 10 mM. Обратную транскрипцию вышеупомянутой смеси проводили в термоциклере в следующих режимах: 250С – 10 мин., 420С – 1час, 700С – 10мин.
В случаях (примеры 1,2) определения уровеня экспрессии мРНК генов с использованием красителя Eva Green, для каждого исследуемого гена были сконструированы и использованы олигонуклеотидные F – прямой праймер и R – обратный праймер приведенные выше в таблице 1.
Амплификацию при полимеразной цепной реакции (ПЦР-РВ) проводили в режиме реального времени в термоциклере в следующих режимах:

причем в диапазоне температуры 60,0°С – 95,0°С производили снятие кривой плавления путем наблюдения интенсивности флуоресценции продуктов ПЦР (ампликонов) при ступенчатом изменении температуры с шагом в 1°С.
В других случаях (примеры 3,4,5) реализацию способа для определения уровня экспрессии мРНК генов производили с использованием набора праймеров TaqMan® указанных выше в таблице 2.
Для каждого исследуемого образца из опухолевой и нормальной ткани почки, составляют смесь общим объемом 20 мкл, содержащую: 1мкл. набора праймеров TaqMan® Gene Expression Assay, 10 мкл. набора TaqMan® Gene Expression Master Mix, 1,6 мкл. комплементарной ДНК (1 мкл), 7,4 мкл. деионизированной воды, которую встряхивают на вортексе и центрифугируют в течение 5 сек., а ПЦР-РВ проводят на приборе Step One Plus в следующих режимах:
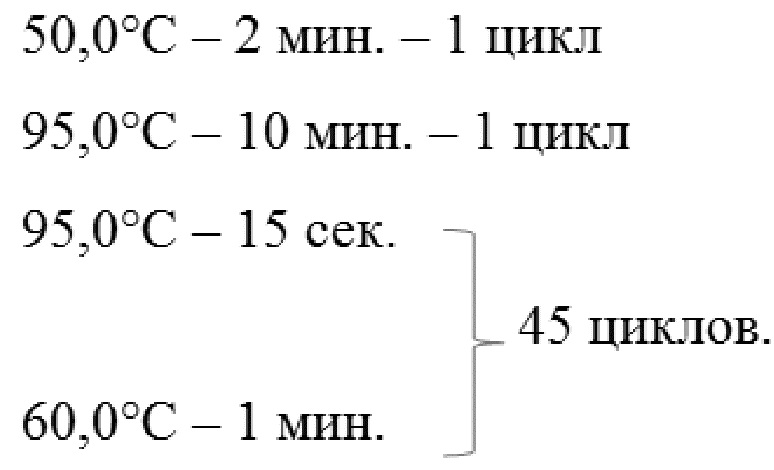
Измененные значения экспрессии мРНК генов выражаются в относительных единицах - экспрессия в опухоли относительно нормальной ткани. Меняться может от долей единицы до сотен значений; но больше 200 - 300, как правило, не бывает.
В любом случае с использованием красителя Eva Green или набора праймеров TaqMan®, для определения связи экспрессии генов с выживаемостью использовали панель из пяти генов VWF, EGLN3, BHLHE41, PLIN2 и BAP1. Прогноз 3,5-летней выживаемости считали в целом благоприятным, если значения уровня экспрессии мРНК образцов опухолевой ткани не менее трех генов из группы VWF, BHLHE41, EGLN3 и PLIN2 превышают уровень экспрессии мРНК тех же генов в образцах нормальной ткани не менее, чем в 1,5 раза, а также в том случае, если значения уровня экспрессии мРНК образцов опухолевой ткани не менее двух генов из группы VWF, BHLHE41, EGLN3 и PLIN2 превышают уровень экспрессии мРНК тех же генов в образцах нормальной ткани и, одновременно, значение уровня экспрессии мРНК гена BAP1 меньше не менее, чем в 2,0 раза, уровня экспрессии мРНК этого гена в образцах нормальной ткани, в каждом из этих случаев. При этом в качестве мРНК эндогенного контрольного гена использовали мРНК гена из группы: GAPDH и ACTB, а прогноз признавали наиболее благоприятным в том случае, если значения уровня экспрессии мРНК образцов опухолевой ткани генов из группы VWF, BHLHE41, EGLN3 и PLIN2 превышают в 2; 2; 3,5 и 1,5 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше в 2,5 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани.
Был применен следующий принцип (схема, или формула): если положительный результат демонстрирует 0 или 1 ген – плохой прогноз; 2 гена – серая зона (дать ответ не представляется возможным); 3 – 5 генов – хорошая выживаемость.
Изложенный подход обеспечивает оптимальное сочетание надежности результата, чувствительности и специфичности метода. Если положительный сигнал дают хотя бы три гена, вероятность ошибочного суждения о результате мала и может быть оценена, на основании показателей чувствительности и специфичности для отдельных генов панели, как не превышающая 0,008.
Применение описанного способа прогнозирования к 149 больным скПКР (примеры 1-5) позволило правильно определить прогноз выживаемости среди 132 больных.
Пример 1.
Описанным образом получены образцы опухолевой и нормальной ткани почки 34 больных (включая 12 женщин и 22 мужчин в возрасте от 17 до 68 лет) больных светлоклеточным почечно-клеточным раком (скПКР) на разных стадиях развития (от ранней до стадии метастазирования), в которых исследована экспрессия мРНК трех из указанной выше группы генов.
А именно, для определения прогноза выживаемости указанных больных использовали панель из трех генов VWF, EGLN3, и BAP1.
У 22 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов VWF, EGLN3 и превышают не менее чем в 2; 3,5 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше не менее чем в 2,5 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани хотя бы у двух генов из указанных трех. У 21 больных из данной группы наблюдениями подтвержден прогноз не менее 3,5 года выживаемости с даты постановки диагноза
У 8 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов VWF, EGLN3 превышают в 1,1-1,4; 1,6-1,8 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше в 2,0 – 2,1 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани. У 6 больных из данной группы наблюдениями подтвержден прогноз менее 3,5 года выживаемости со времени постановки диагноза
У 4 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов VWF, EGLN3 превышают в 2,0 -2,1; 1,6-1,8 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше в 2,5 – 2,6 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани. У 2 больных из данной группы наблюдениями установлено менее 3,5 года выживаемости со времени постановки диагноза, у 2 больных – более 3,5 года выживаемости с даты постановки диагноза.
Пример 2.
Описанным образом получены образцы опухолевой и нормальной ткани почки 28 больных (включая 11 женщин и 17 мужчин в возрасте от 19 до 66 лет) больных светлоклеточным почечно-клеточным раком (скПКР) на разных стадиях развития (от ранней до стадии метастазирования), в которых исследована экспрессия мРНК четырех из указанной выше группы генов.
А именно, для определения прогноза выживаемости указанных больных использовали панель из четырех генов EGLN3, BHLHE41, PLIN2 и BAP1
У 19 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2 и превышают не менее чем в 3,6; 2,1; 2,2 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше не менее чем в 2,6 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани хотя бы у двух генов из указанных четырех. У 18 больных из данной группы наблюдениями подтвержден прогноз не менее 3,5 года выживаемости с даты постановки диагноза
У 7 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2 превышают в 1,2-1,5; 1,3-1,8; 1,9-3,0 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше в 1,9 – 2,1 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани. У 6 больных из данной группы наблюдениями подтвержден прогноз менее 3,5 года выживаемости со времени постановки диагноза
У 2 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2 превышают в 2,0 -2,1; 1,6-1,8; 3,1-3,2 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше в 2,6 – 2,7 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани. У 1 больного из данной группы наблюдениями установлено менее 3,5 года выживаемости со времени постановки диагноза, у 1 больного – более 3,5 года выживаемости с даты постановки диагноза.
Пример 3.
Описанным образом получены образцы опухолевой и нормальной ткани почки 29 больных (включая 10 женщин и 19 мужчин в возрасте от 20 до 66 лет) больных светлоклеточным почечно-клеточным раком (скПКР) на разных стадиях развития (от ранней до стадии метастазирования), в которых исследована экспрессия мРНК четырех из указанной выше группы генов.
А именно, для определения прогноза выживаемости указанных больных использовали панель из четырех генов EGLN3, BHLHE41, PLIN2 и VWF,
У 20 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2, VWF и превышают не менее чем в 3,5; 2,1; 1,6; 2,1 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани хотя бы у двух генов из указанных четырех. У 19 больных из данной группы наблюдениями подтвержден прогноз не менее 3,5 года выживаемости со времени постановки диагноза
У 7 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2, VWF превышают в 1,4-1,6; 1,3-1,8; 1,6-2,0; 2,1-2,3 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани. У 6 больных из данной группы наблюдениями подтвержден прогноз менее 3,5 года выживаемости с даты постановки диагноза
У 2 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2, VWF превышают в 2,0 -2,1; 1,6-1,8; 1,6-2,2; 2,1-2,5 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани. У 1 больного из данной группы наблюдениями установлено менее 3,5 года выживаемости со времени постановки диагноза, у 1 больного – более 3,5 года выживаемости с даты постановки диагноза.
Пример 4.
Описанным образом получены образцы опухолевой и нормальной ткани почки 27 больных (включая 10 женщин и 17 мужчин в возрасте от 22 до 70 лет) больных светлоклеточным почечно-клеточным раком (скПКР) на разных стадиях развития (от ранней до стадии метастазирования), в которых исследована экспрессия мРНК четырех из указанной выше группы генов.
А именно, для определения прогноза выживаемости указанных больных использовали панель из четырех генов EGLN3, BHLHE41, PLIN2 и CA9.
У 18 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2, CA9 и превышают не менее чем в 3,5; 2,1; 1,6; 3,3 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани хотя бы у двух генов из указанных четырех. У 17 больных из данной группы наблюдениями подтвержден прогноз не менее 3,5 года выживаемости со времени постановки диагноза
У 7 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2, CA9 превышают в 1,5-1,8; 1,4-1,7; 1,2-1,4; 2,9-3,3 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани. У 6 больных из данной группы наблюдениями подтвержден прогноз менее 3,5 года выживаемости с даты постановки диагноза
У 2 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов EGLN3, BHLHE41, PLIN2, CA9 превышают в 2,0 -2,1; 1,6-1,8; 1,3-1,6; 2,1-2,5 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани. У 1 больного из данной группы наблюдениями установлено менее 3,5 года выживаемости со времени постановки диагноза, у 1 больного – более 3,5 года выживаемости со времени постановки диагноза.
Пример 5.
Описанным образом получены образцы опухолевой и нормальной ткани почки 31 больного (включая 12 женщин и 19 мужчин в возрасте от 22 до 71 года) больных светлоклеточным почечно-клеточным раком (скПКР) на разных стадиях развития (от ранней до стадии метастазирования), в которых исследована экспрессия мРНК четырех из указанной выше группы генов.
А именно, для определения прогноза выживаемости указанных больных использовали панель из шести генов СА9, VWF, EGLN3, BHLHE41, PLIN2 и BAP1.
У 20 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов СА9, VWF, EGLN3, BHLHE41, PLIN2 и превышают не менее чем в 3,3; 2,1; 3,5; 2,1; 1,6 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше не менее чем в 2,5 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани хотя бы у трех генов из указанных шести. У 18 больных из данной группы наблюдениями подтвержден прогноз не менее 3,5 года выживаемости со времени постановки диагноза
У 9 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов СА9, VWF, EGLN3, BHLHE41, PLIN2 превышают в 2,5-2,8; 1,5-1,7; 2,3-3,4; 0,9-1,3 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше не более чем в 1,5-1,8 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани хотя бы у трех генов из указанных шести. У 7 больных из данной группы наблюдениями подтвержден прогноз менее 3,5 года выживаемости с даты постановки диагноза
У 2 больных значения уровня экспрессии мРНК образцов опухолевой ткани генов СА9, VWF, EGLN3, BHLHE41, PLIN2 превышают в 2,3 -2,5; 1,5-1,8; 3,3-3,6; 1,1-1,5 раза, соответственно, уровень экспрессии мРНК тех же генов в образцах нормальной ткани, а значение уровня экспрессии мРНК гена BAP1 меньше не более чем в 1,7-1,9 раза уровня экспрессии мРНК этого гена в образцах нормальной ткани. У 1 больного из данной группы наблюдениями установлено менее 3,5 года выживаемости со времени постановки диагноза, у 1 больного – более 3,5 года выживаемости со времени постановки диагноза.
Приведенными примерами подтверждено, что примененный подход обеспечивает наиболее эффективное сочетание надежности результата, чувствительности и специфичности метода. Только единичные ответы были ложноположительными, или ложноотрицательными и три были определены, как относящиеся к серой зоне и нуждающиеся в дальнейших исследованиях.
Как показали исследования, если положительный сигнал дают хотя бы три гена, вероятность ошибочного суждения о результате мала и может быть оценена, на основании показателей чувствительности и специфичности для отдельных генов панели, как не превышающая 0,008. Чувствительность и специфичность способа составили 83,3%. Без учета серой зоны чувствительность и специфичность составляют 92,5%.
Использование предлагаемого способа на разных стадиях развития скПКР позволяет оперативно и с минимальной трудоемкостью сделать достоверный прогноз выживаемости для большинства больных скПКР. В результате обеспечено увеличение производительности и эффективности исследований для прогнозирования выживаемости и обоснованного выбора тактики лечения больных светлоклеточным почечно-клеточным раком.