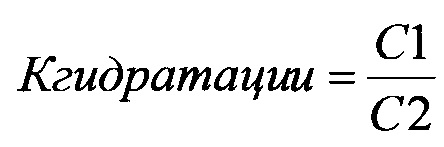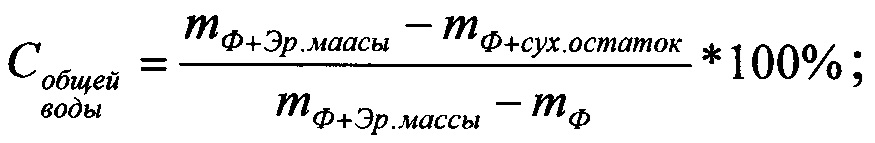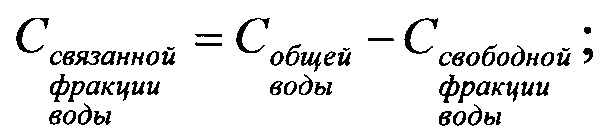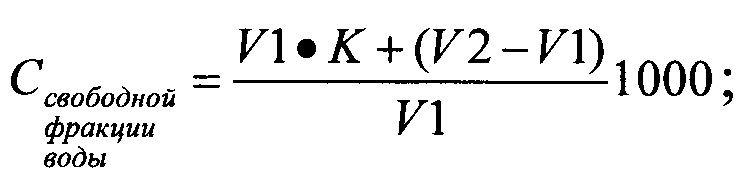Результат интеллектуальной деятельности: Способ прогнозирования развития отека легких у пациентов с инфарктом миокарда
Вид РИД
Изобретение
Изобретение относится к медицине и может быть использовано в кардиологии.
Известен способ прогнозирования развития осложнений у больных инфарктом миокарда путем подсчета лейкоцитарной формулы в окрашенных мазках крови и по соотношению гранулоцитов и агранулоцитов судят о реактивности организма. При величине этого соотношения более 4,0 прогнозируют развитие осложнений течения инфаркта миокарда в виде развития отека легких, кардиогенного шока или летального исхода. Но данный способ трудоемкий, требует специальных красителей и время для окрашивания форменных элементов крови. Кроме того, он неспецифичен и не позволяет начать превентивное лечение для предупреждения развития конкретного осложнения. (Справочник лабораторные методы исследования в клинике. Под редакцией профессора В.В. Меньшикова, Москва «Медицина» 1987, С. 106-107, 111-112, 124).
Известен способ прогнозирования осложнений при остром инфаркте миокарда, заключающийся в том, что у пациента в первый день течения острого инфаркта миокарда берут кровь, затем выделяют из нее тромбоциты, к которым добавляют антиген из некротической кардиальной ткани, а после проведения реакции тромболизиса оценивают величину повреждения тромбоцитов. Если эта величина выше 14%, то риск развития осложнений считается высоким. Однако данный метод сложен для применения, особенно в условиях неотложной помощи: для выделения тромбоцитов в нативном виде необходимы дорогостоящие оборудование и реактивы, этот процесс занимает продолжительное время; для получения антигена из некротизированной кардиальной ткани также требуется сложное оборудование, подготовленный специалист, а для постановки дальнейшей реакции тромболизиса требуются стандартизированные условия и дополнительное время. (Патент №1388807 СССР, МПК G01N 33/49 (Способ прогнозирования осложнений при остром инфаркте миокарда)/ М.М. Миррахимов и др.; заявитель и патентообладатель Киргизский научно-исследовательский, институт кардиологии; заявка №3734043 от 27.04.1984; опубликовано 15.04.1988. Бюл. №14).
Известно, что водой представлена основная составляющая часть всех систем живых организмов, в том числе человека. Все физико-химические реакции обмена веществ происходят только в водной среде. По своей структуре она неоднородна и выделяют свободную и связанную фракции воды. Их выделяют не только из-за различий в физико-химических свойствах, но и из-за разных физиологических функций. (Аксенов С.И. Связанная вода в дисперсных системах // Состояние воды в биологических системах. - 1980. - №57. - С. 46-74.; Бычков С.М., Кузьмина С.А.; Действие протеогликанов на эритроциты в циркулирующей крови // Бюллетень экспериментальной биологии и медицины. 1993. - №3. с. 240-242. Горизонтов П.Д., Белоусов О.И., Федотова М.И. Стресс и система крови. М.: Медицина, 1983. - 239 с.). Количество структурированной фракции воды имеет большое значение функционирование молекул биологически активных веществ, в том числе изменяя конфигурацию белков и упорядочивая их третичную и четвертичную структуры (Жуковский А.Л., Ровнов Н.В., Сорвин С.В., Петров Л.Н., Вукс Е.М. Изменение конформации белков в водных растворах гетерофункциональных неэлектролитов // Биофизика. - 1999. - Т. 44, вып. 3. - С. 407-411).
Одним из механизмов ответной реакции организма на внешнее воздействие является феномен адаптивной стабилизации структур. В основе этого процесса лежит механизм накопления белков семейства HSP70, то есть белков теплового шока. Эти белки обладают уникальной способностью дезагрегировать или ренатурировать поврежденные клеточные структуры. В случае длительного или чрезвычайно сильного воздействия повреждающего фактора содержание стресс-белков снижается (Меерсон Ф.З. «Защита сердца от ишемических повреждений: роль стресс-лимитирующих систем и стабилизации структур миокарда», «Российский кардиологический журнал», 2001, №5(31), с. 49-59). Изменения соотношений свободной и связанной фракций воды в компонентах крови являются отражением процессов, происходящих в клетках органов и межклеточной среде в результате патологического процесса.
Способ основан на свойстве воды увеличиваться в объеме при замораживании (кристаллизации) и различных свойствах свободной и связанной фракций воды в этом процессе. Свободная фракция воды кристаллизуется при температуре несколько ниже 0°С, а связанная с биомакромолекулами фракция воды начинает кристаллизоваться при температуре ниже -20°С.
Технический результат предлагаемого изобретения состоит в прогнозировании развития отека легких у больных инфарктом миокарда.
Сущность предлагаемого способа заключается в том, что с помощью определения содержания связанной воды в эритроцитарной массе крови пациента и расчета Кгидратации эритроцитарной массы прогнозируют развитие отека легких у пациентов с острым инфарктом миокарда.
Способ осуществляется следующим образом.
В эритроцитарной массе определяют содержание свободной и связанной воды дилатометрическим способом в модификации Н.Ф. Фаращука (авт. св. №1544381). В основе этого способа лежит свойство кристаллизации воды, которое сопровождается увеличением ее объема. В биологических жидкостях вода представлена свободной и связанной фракциями. При замораживании свободная фракция переходит в кристаллическое состояние при температуре несколько ниже 0°С, в то время как связанная фракция кристаллизуется при температуре ниже -20°С. Это свойство позволяет рассчитать и оценить объем каждой из водных фракций. Для осуществления способа необходим следующий комплект оборудования: центрифуга, морозильная камера, сушильный шкаф, аналитические весы, микроскоп медицинский учебный МИКМЕД-5У, дилатометрическое устройство для измерения объема жидкости до вымораживания и после него, устройство для отбора проб жидких тканей, описанное в патенте №1710000.
У пациентов с острым инфарктом миокарда с подозрением на развивающийся отек легких при поступлении производят забор 4 мл венозной крови в сухую стеклянную пробирку с 2 каплями раствора гепарина. Полученную кровь центрифугируют до отделения плазмы эритроцитарной массы. После этого с помощью автоматизированной пипетки удаляют отделившуюся плазму от эритроцитарной массы, которую с помощью устройства для взятия проб биологических жидкостей набирают в капилляр. В результате возвратно-поступательного перемещения ролика вдоль эластичной трубки, закрепленной в донной части кожуха эритроцитарная масса заполняет капилляр. Используют капилляр Панченко, потому что его деления через 1 мм совпадают с таковыми в отсчетной шкале микроскопа, что позволяет с точностью до 0,05 мм регистрировать объем жидкости. Эритроцитарную массу набирают до уровня высоты столба 90-92 мм, чтобы увеличенный в процессе кристаллизации воды объем жидкости оставался в пределах шкалы. Капилляр с образцами компонентов крови закрепляют в металлическом держателе и зажимают винтом на верхней площадке. После этого через отверстие в винте пропускают металлический зонд, имеющий строго поперечный нижний срез, не достигая уровня биологических жидкостей. С помощью микроскопа медицинского учебного МИКМЕД-5У регистрируют исходный объем жидкости. После этого дилатометрическое устройство в собранном виде погружают в морозильную камеру с постоянной температурой -10°С на 20 минут. Затем устройство вынимают и с помощью металлического зонда, продвигаемого в капилляр до упора, фиксируют объем эритроцитарной массы после замерзания (кристаллизации) свободной фракции воды и регистрируют его при помощи микроскоп медицинского учебного МИКМЕД-5У. Взвешивают кусочек металлической фольги размером 3 см*3 см. После этого зонд извлекают из капилляра, который освобождают из держателя, а эритроцитарную массу выливают на предварительно взвешенный кусочек металлической фольги, взвешивают на любых аналитических весах с точностью до 0,0001 г и высушивают в сушильном шкафу при 100°С в течение 40 минут с последующей регистрацией массы сухого остатка.
Содержание общей воды рассчитывают по формуле:
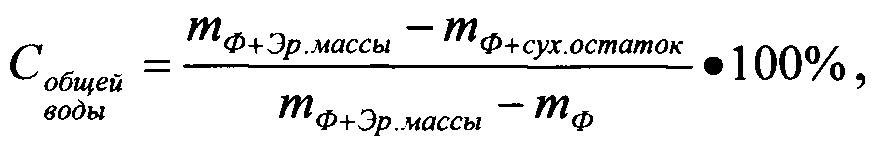
mф+Эр.массы - масса взвешенного кусочка металлической фольги и эритроцитарной массы,
m Ф+сух.остаток - масса взвешенного кусочка металлической фольги и сухого остатка,
mф - масса взвешенного кусочка металлической фольги.
Содержание свободной фракции воды рассчитывают по формуле:
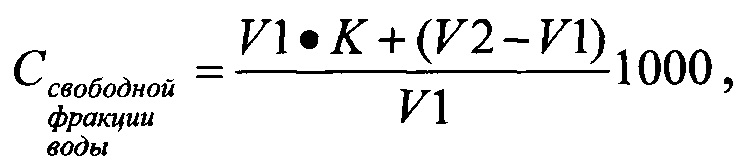
V1 - исходный объем жидкости;
V2 - объем жидкости после кристаллизации свободной фракции воды;
K - коэффициент сжатия эритроцитарной массы при охлаждении от комнатной температуры до температуры кристаллизации (0°С), установленный опытным путем.
Содержание связанной фракции воды рассчитывают по формуле;
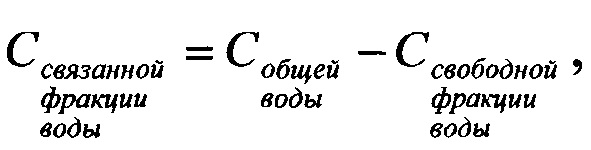
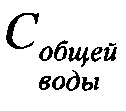 - содержание общей воды,
- содержание общей воды,
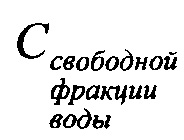 - содержание свободной фракции воды.
- содержание свободной фракции воды.
Рассчитывают коэффициент гидратации эритроцитарной массы по следующей формуле:
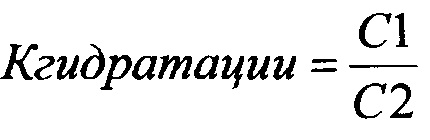 , где С1 - содержание связанной фракции воды, С2 - содержание свободной фракции воды.
, где С1 - содержание связанной фракции воды, С2 - содержание свободной фракции воды.
И делают вывод: если у пациентов с острым инфарктом миокарда содержание связанной фракции воды ≤22,12%, а Кгидратации ≤0,55, то прогнозируют развитие отека легких в течение первых суток; если у пациентов с инфарктом миокарда определяют содержание связанной фракции воды от 25,8% до 27,8%, а Кгидратации от 0,68 до 0,74, то прогнозируют неосложненное течение инфаркта миокарда.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1.
Пациентка С., 68 лет, поступила в клинику 17.07.2018 г. с жалобами на интенсивную боль в области сердца с иррадиацией в левое плечо, шею, на чувство нехватки воздуха, усиливающееся в положении лежа, выраженную общую слабость.
В анамнезе: артериальная гипертензия, постоянно принимает лозартан 50 мг 2 раза в день, бисопролол 2,5 мг утром и кардиомагнил 75 мг на ночь. Вышеописанные жалобы раньше не беспокоили и возникли около 14 часов назад,, самостоятельно принимала НПВС, корвалол,, валидол, глицин - без улучшения, вызвала СМП. Была оказана медицинская помощь и пациентка доставлена в клинику.
Объективно: Рост: 168 см, вес: 74 кг, ИМТ=26,22 кг/м2. АД=135/80 мм рт. ст., ЧСС=84 в мин, ЧДД=18-20 в мин. SpO2=98-99%. Кожные покровы телесные, умеренной влажности. Периферических отеков не выявлено. Дыхание над всей поверхностью легких везикулярное, несколько ослаблено в нижних отделах, хрипов нет. Тоны сердца ритмичные, приглушены. Живот мягкий, безболезненный при пальпации. Стул и диурез в норме.
Изменений в общем анализе крови и общем анализе мочи не выявлено.
Биохимический анализ крови: АЛТ=62 ЕД/л, АСТ=108 ЕД/л, ЛДГ=800, КФК=2418 ЕД/л, КФК-МВ=132 ЕД/л, холестерин=9,2 ммоль/л, креатинин=87 мкмоль/л, мочевина=5,2 ммоль/л, общий белок=73 г/л, глюкоза крови=7,1 ммоль/л.
Рентген органов грудной клетки - без видимой инфильтрации. Корни легких несколько расширены.
Электрокардиограмма: ритм синусовый, ЧСС=80 в мин, э.о.с. не отклонена. Динамика течения острого передне-бокового инфаркта миокарда левого желудочка с элевацией сегмента ST. Патологический зубец QV2-V5.
У пациентки взята венозная кровь для исследования. Выявлены следующие изменения:


Полученные данные расценивают как критерий высокого риска развития острой левожелудочковой недостаточности в виде отека легких.
В течение 1,5 часов пребывания в стационаре у пациентки развился альвеолярный отек легких, который был купирован. На фоне проводимой терапии состояние пациентки улучшилось и она выписана для дальнейшего амбулаторного наблюдения.
Пример 2.
Пациент Т., 54 года, поступил в клинику 4.09.2018 г. с жалобами на интенсивную боль за грудиной с иррадиацией в эпигастральную область, на чувство нехватки воздуха, выраженную общую слабость.
В анамнезе: эпизодически отмечал повышение артериального давления до 160/90 мм рт. ст. на фоне эмоционального и физического стресса, принимал каптоприл (обычное артериальное давление 135-140/85 мм рт. ст.). Вышеописанные жалобы возникли около 10 часов назад, самостоятельно принимал валидол, наружно - диклофенак - без улучшения, вызвал СМП. Была оказана медицинская помощь. Пациент доставлен в клинику.
Объективно: Рост: 189 см, вес: 106 кг, ИМТ=29,67 кг/м2. АД=145/90 мм рт. ст., ЧСС=58 в мин, ЧДД=18-20 в мин. SpO2=98%. Кожные покровы телесные, умеренной влажности. Периферических отеков не выявлено. Дыхание над всей поверхностью легких везикулярное, ослаблено в нижних отделах, хрипов нет. Тоны сердца ритмичные, приглушены. Живот мягкий, безболезненный при пальпации. Стул и диурез в норме.
Изменений в общем анализе крови и общем анализе мочи не выявлено.
Биохимический анализ крови: АЛТ=56 ЕД/л, АСТ=112 ЕД/л, ЛДГ=643, КФК=2128 ЕД/л, КФК-МВ=116 ЕД/л, холестерин=8,7 ммоль/л, креатинин=82 мкмоль/л, мочевина=5,8 ммоль/л, общий белок=84 г/л, глюкоза крови=6,9 ммоль/л.
Рентген органов грудной клетки - без видимой инфильтрации. Корни легких расширены. Тень сердца - расширено влево.
Электрокардиограмма: синусовая брадикардия, ЧСС=56-58 в мин, э.о.с. отклонена влево. Динамика течения острого нижнего инфаркта миокарда левого желудочка. Патологический зубец Q в III и aVF.
У пациента взята венозная кровь для исследования. Выявлены следующие изменения:
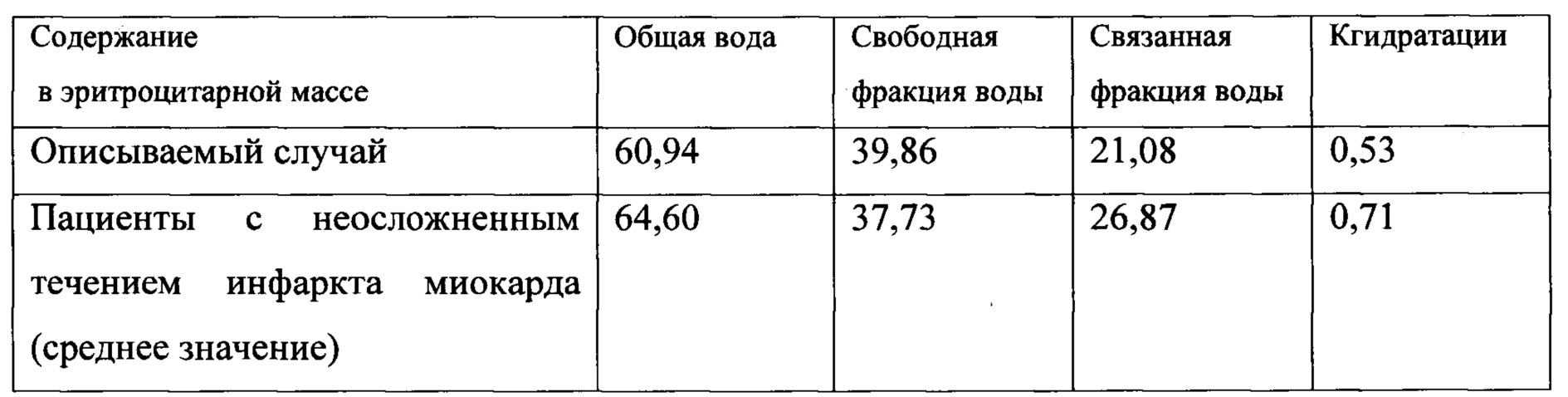
Полученные данные расценивают как критерий высокого риска развития острой левожелудочковой недостаточности в виде отека легких.
Через 11 часов 45 минут пребывания в стационаре у пациента развился альвеолярный отек легких, который был успешно купирован. На фоне проводимой терапии состояние пациента улучшилось и он выписан под наблюдение кардиолога по месту жительства.
Пример 3.
Пациент М., 59 лет, поступил в клинику 2.09.2018 г. с жалобами на интенсивную давящую боль за грудиной с иррадиацией в шею, нижнюю челюсть, на чувство нехватки воздуха, усиливающееся в положении лежа, выраженную общую слабость.
В анамнезе: артериальная гипертензия, периодически при высоком артериальном давлении принимает капотен, лизиноприл. За медицинской помощью не обращался.
Накануне пациент отмечает интенсивный физический труд («копал картофель»). Вышеописанные жалобы раньше не беспокоили и возникли около 17 часов назад, самостоятельно принимал валидол, настойку валерианы, пустырника, боярышника - без значительного улучшения, родственники вызвали СМП. Была оказана медицинская помощь и пациент доставлен в клинику.
Объективно: Рост: 179 см, вес: 94 кг, ИМТ=29,34 кг/м2. АД=150/90 мм рт. ст., ЧСС=96 в мин, ЧДД=18-20 в мин. SpO2=98-99%. Кожные покровы телесные, умеренной влажности. Периферических отеков не выявлено. Дыхание над всей поверхностью легких везикулярное, хрипов нет. Тоны сердца ритмичные, приглушены. Живот мягкий, безболезненный при пальпации. Стул и диурез в норме.
Изменений в общем анализе крови и общем анализе мочи не выявлено.
Биохимический анализ крови: АЛТ=56 ЕД/л, АСТ=102 ЕД/л, ЛДГ=853, КФК=2326 ЕД/л, КФК-МВ=118 ЕД/л, холестерин=7,4 ммоль/л, креатинин=76 мкмоль/л, мочевина=4,2 ммоль/л, общий белок=81 г/л, глюкоза крови=6,9 ммоль/л.
Рентген органов грудной клетки - без видимой инфильтрации. Корни легких несколько расширены.
Электрокардиограмма: синусовая тахикардия, ЧСС=96 в мин, э.о.с. не отклонена. Динамика течения острого передне-перегородочного инфаркта миокарда левого желудочка. Патологический зубец QV1-V4.
У пациента взята венозная кровь для исследования. Выявлены следующие изменения:
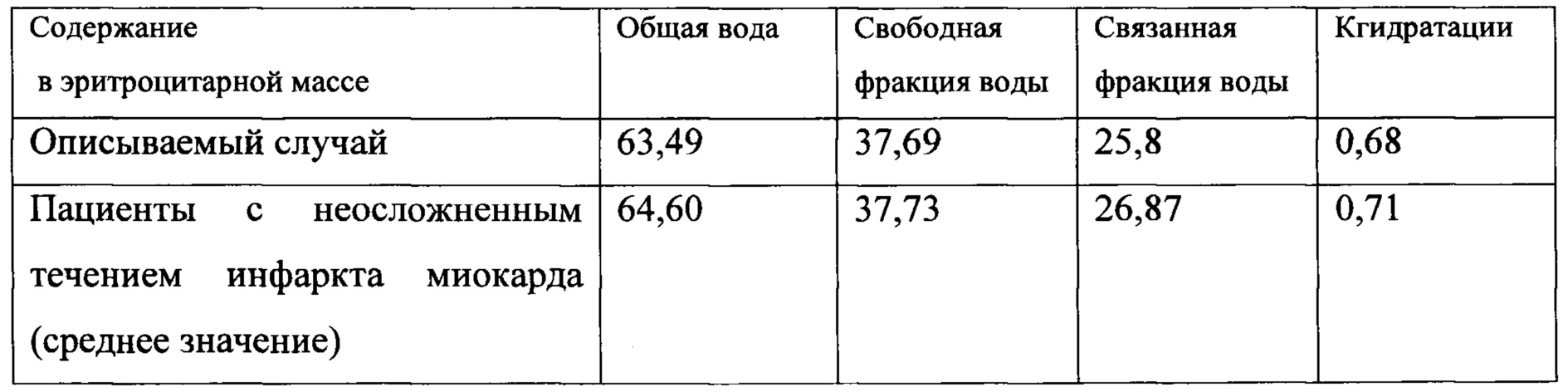
Полученные данные свидетельствуют об адекватной активизации адаптационных механизмов у данного пациента и низком риске развития отека легких.
В течение 14 койко-дней пребывания в стационаре на фоне проводимой терапии состояние пациента улучшилось и он выписан для дальнейшего амбулаторного наблюдения.
Пример 4.
Пациент Ф., 48 лет, поступил в клинику 12.08.2018 г. с жалобами на жгучую боль за грудиной без иррадиации, на чувство нехватки воздуха, выраженную общую слабость, потливость.
В анамнезе: редко отмечал повышение артериального давления до 150/80 мм рт. ст.на фоне эмоционального стресса, принимал но-шпу (обычное артериальное давление 115-120/80 мм рт. ст.).
Вышеописанные жалобы возникли около 18 часов назад, самостоятельно принимал но-шпу, нитроглицерин - с непродолжительным улучшением, Самостоятельно обратился в клинику.
Объективно: Рост: 182 см, вес: 92 кг, ИМТ=27,77 кг/м2. АД=140/85 мм рт. ст., ЧСС=88 в мин, ЧДД=18-20 в мин. SpO2=98%. Ттела=36,8°С. Кожные покровы телесные, влажные. Периферических отеков не выявлено. Дыхание над всей поверхностью легких везикулярное, хрипов нет. Тоны сердца ритмичные, приглушены. Живот мягкий, безболезненный при пальпации. Стул и диурез в норме.
Изменений в общем анализе крови и общем анализе мочи не выявлено.
Биохимический анализ крови: АЛТ=51 ЕД/л, АСТ=98 ЕД/л, ЛДГ=759, КФК=2054 ЕД/л, КФК-МВ=83 ЕД/л, холестерин=8,9 ммоль/л, креатинин=76 мкмоль/л, мочевина=5,1 ммоль/л, общий белок=77 г/л, глюкоза крови=6,2 ммоль/л.
Рентген органов грудной клетки - без видимой инфильтрации.
Электрокардиограмма: ритм синусовый, ЧСС=80-88 в мин, э.о.с. отклонена влево. Динамика течения острого субэндокардиального повреждения миокарда в области передней стенки левого желудочка.
У пациента взята венозная кровь для исследования. Выявлены следующие изменения:
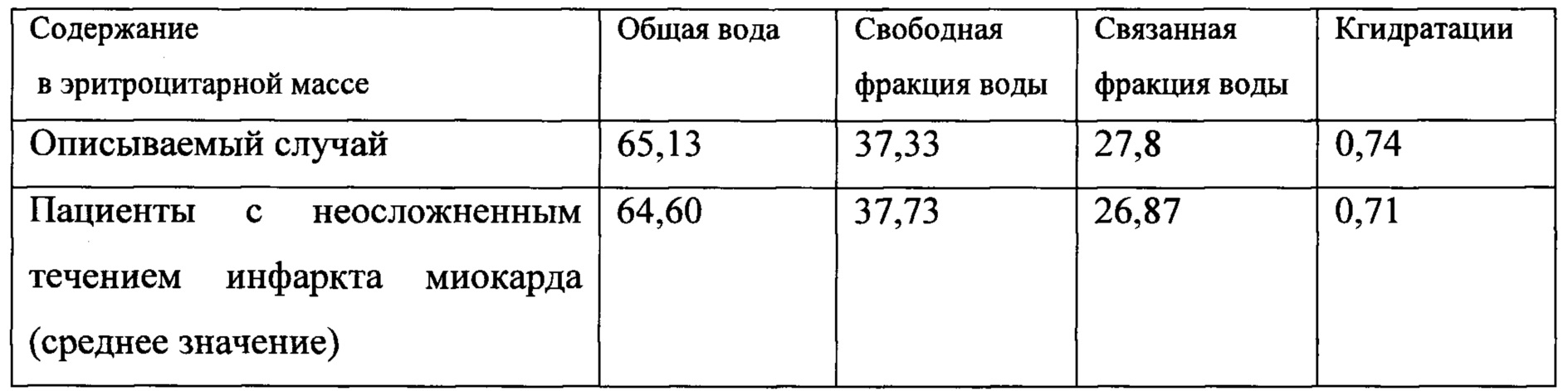
Полученные данные свидетельствуют об адекватной активизации адаптационных механизмов у данного пациента и низком риске развития отека легких.
В результате проводимой терапии состояние пациента улучшилось и на 13-е сутки он выписан под наблюдение кардиолога по месту жительства.
Представленные примеры иллюстрируют возможность прогнозировать развитие отека легких у пациентов с инфарктом миокарда по изменению содержания связанной фракции воды в эритроцитарной массе и Кгидратации. Увеличение количества связанной фракции воды отражает адаптационную стабилизацию тканевых структур в ответ на развитие повреждения кардиомиоцитов и общую стрессорную реакцию организма при развитии инфаркта миокарда. В то же время значительное снижение связанной фракции воды у пациентов с развившейся острой левожелудочковой недостаточностью в виде отека легких свидетельствует об истощении компенсаторных механизмов организма и о необходимости активного вмешательства для их восстановления.
Предлагаемый способ впервые позволяет прогнозировать у пациентов с острым инфарктом миокарда развитие острой левожелудочковой недостаточности в виде отека легких, отличается простотой выполнения, в то же время обладает высокой точностью, быстротой получения результатов, их достоверностью, позволяет вовремя начать проведение превентивной терапии для предупреждения развития отека легких у пациентов с инфарктом миокарда. Кроме того, для выполнения данного способа необходимо элементарное лабораторное оборудование, которое используется многократно, не требуются дорогостоящие реактивы, что является экономически выгодным.