Результат интеллектуальной деятельности: Способ получения ди-N,N'-оксидов динитрилов 2,4,6-триалкилбензол-1,3-дикарбоновых кислот
Вид РИД
Изобретение
Изобретение относится к химии высокомолекулярных соединений, в частности к диоксидам орто- замещенных ароматических динитрилов, используемых в качестве низкотемпературных отвердителей каучуков.
N,N'-диоксиды динитрилов 2,4,6-триалкилбензол-1,3-дикарбоновых кислот являются представителями наиболее стабильных ароматических нитрилоксидов. Стабильными их делает наличие электронодонорных алкильных заместителей в молекуле в орто-положении к нитрильным группам. Из них практическое применение получили динитрилоксиды, полученные на основе триметилбензола (мезитилена) и триэтилбензола. Они представляют собой твердые кристаллические вещества, обладающие повышенной химической стабильностью, в том числе, и к реакциям димеризации. Использование ароматических динитрилоксидов в качестве сшивающих агентов непредельных полимеров основано на реакции 1,3-диполярного присоединения их к соединениям, имеющим кратные связи:
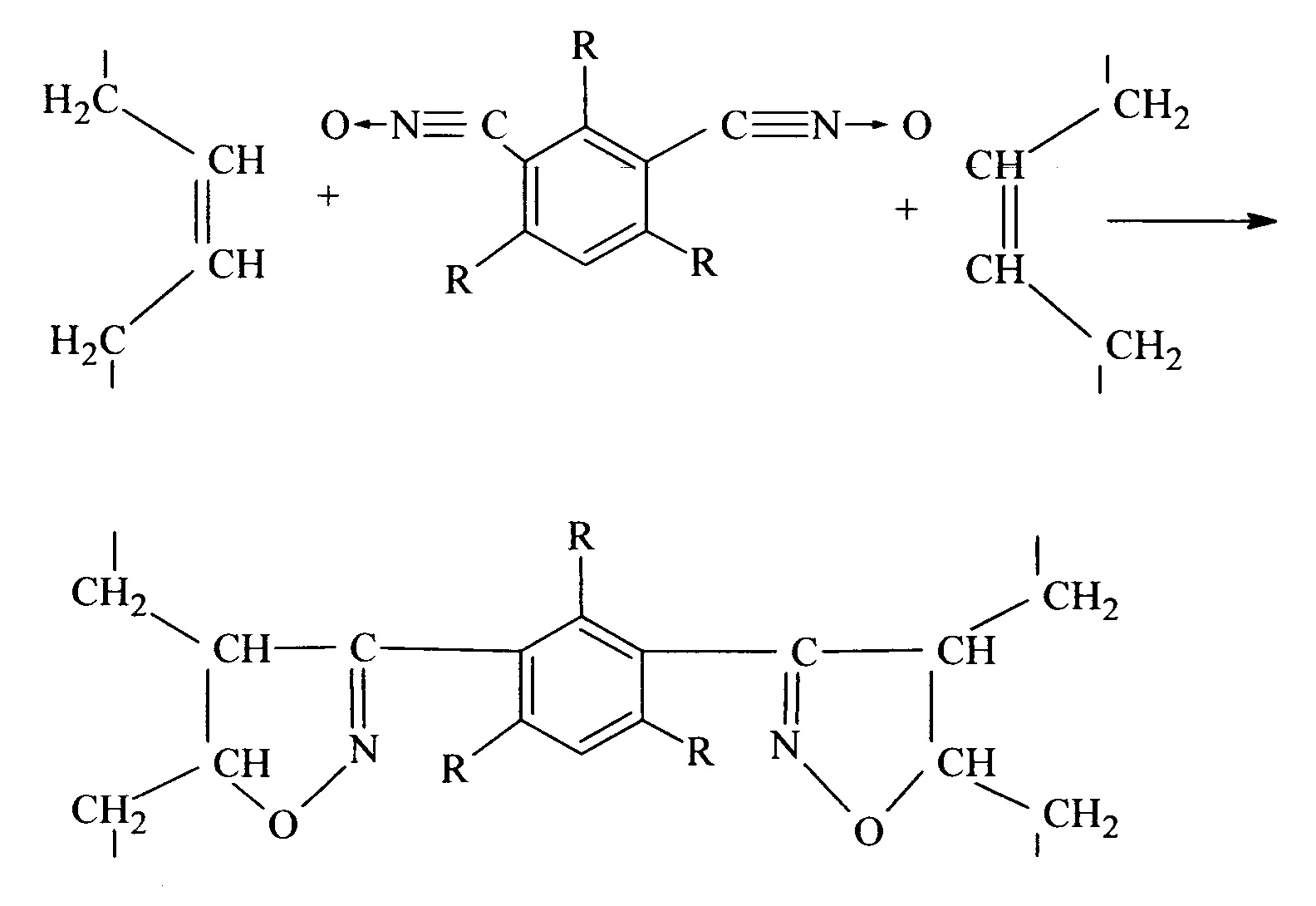
Первое сообщение об использовании полифункциональных нитрилоксидов в качестве сшивающих агентов для ненасыщенных полимеров появилось в американском патенте в 1968 году [1]. В связи с тем, что авторы работали с нестабильными нитрилоксидами и сшитые эластомеры из диеновых каучуков оказались жесткими, эти исследования не получили дальнейшего развития.
Практическое развитие химия стабильных ароматических нитрилоксидов получила благодаря работам советских ученых, которые исследовали бифункциональные, в частности, мезитилен- и триэтилбензолдинитрилоксиды в качестве низкотемпературных вулканизирующих агентов каучуков и композиций на их основе [2-8].
Предшественниками стабильных ароматических динитрилоксидов являются оксимы соответствующих альдегидов.
Основной реакцией получения ароматических нитрилоксидов является реакция дегидрогенизации соответствующих альдоксимов:
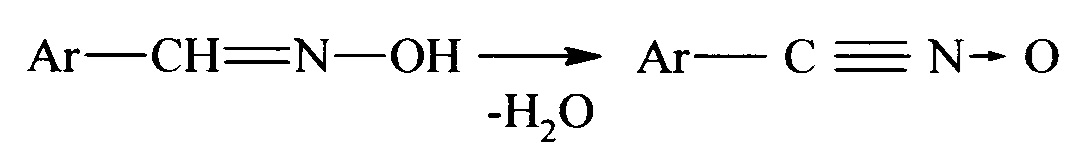
Варианты этой реакции описаны в обзоре [9]. Практическое значение приобрели два способа получения нитрилоксидов:
окислительное галоидирование соответствующих оксимов с промежуточным образованием гидроксииминоилгалогенидов с последующей обработкой основаниями
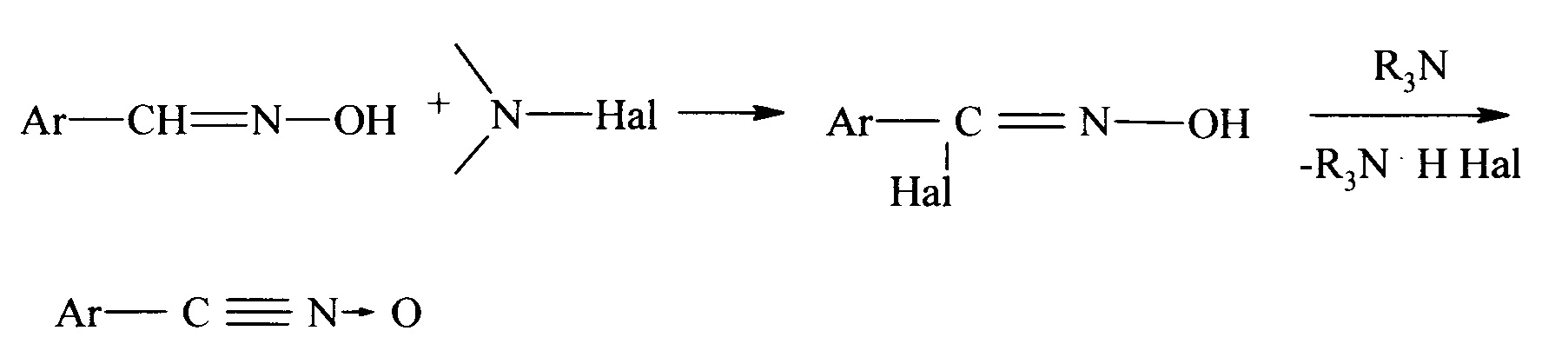
и окисление и дегидрогалоидирование оксимов щелочными растворами гипогалогенитов в одну стадию [10-13]
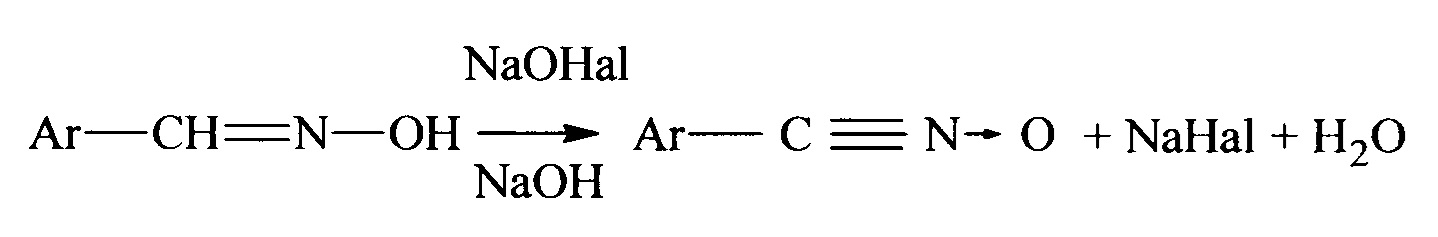
Классический синтез орто-замещенных диальдоксимов может быть представлен следующей схемой:
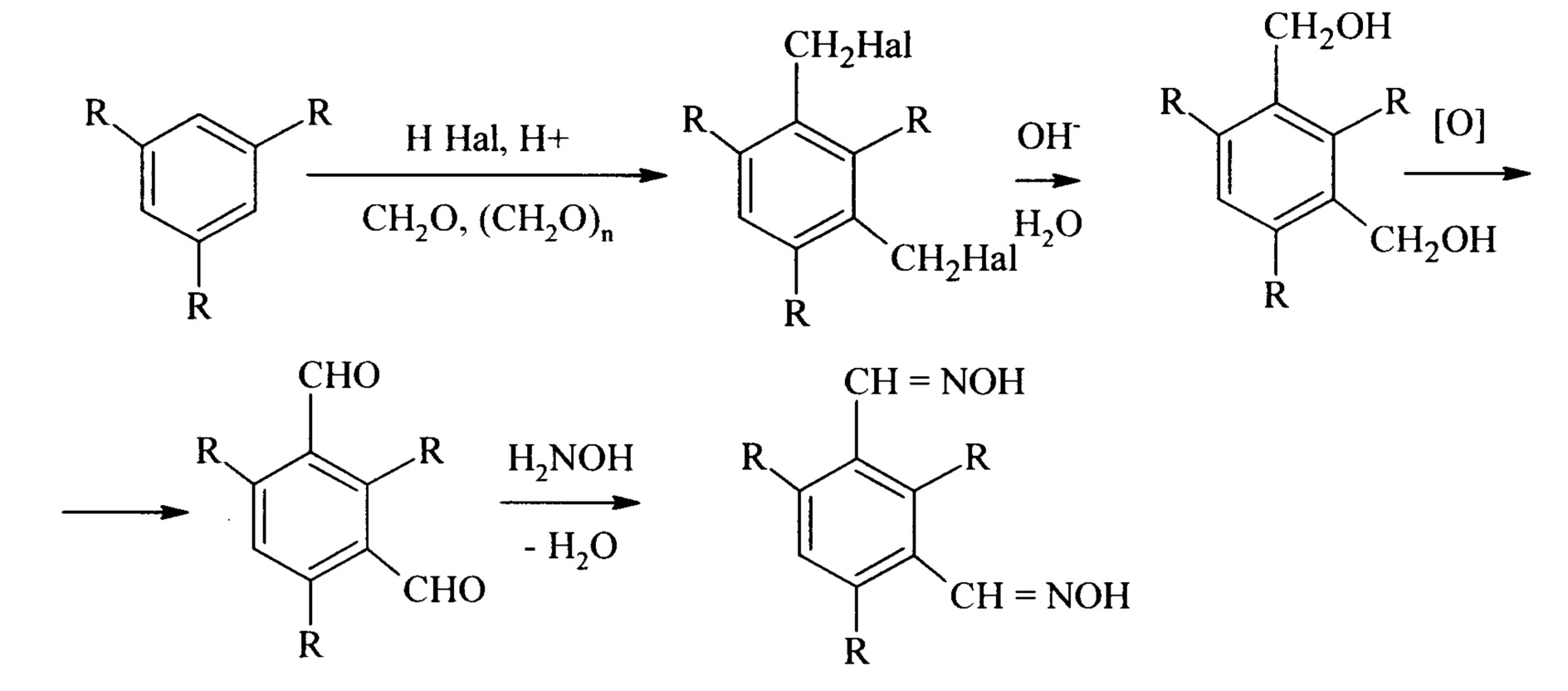
Первая стадия галоидметилирования с использованием хлористого или бромистого водорода и формальдегида или его полимерных форм является общей для получения диметил-, триметил-, диэтил- и триэтилбензолальдоксимов и диальдоксимов. Гидролиз галоидметильных производных и окисление образующихся спиртов до альдегидов также считают классическими реакциями [14-16].
Известны также публикации [17-19] по получению альдегидов другими методами, в которых окислению или формилированию подвергаются непосредственно галоидметильные производные алкилбензолов.
В практическом плане интерес представляют два способа получения замещенных ароматических альдегидов:
1. Окисление соответствующих спиртов хромовым ангидридом [16, 19, 20];
2. Окисление галоидметильных замещенных бензолов калиевой или натриевой солями нитроалканов [13].
Стадия получения альдоксимов взаимодействием альдегидов с гидроксиламином является общеизвестной и ее применение в синтезе замещенных ароматических альдоксимов не вызывает затруднений. Реакцию проводят с водным раствором гидроксиламина или его солей.
Получение ароматических нитрилоксидов из соответствующих альдоксимов в ранних публикациях [5, 10, 11, 12, 18] предусматривало взаимодействие последних с галоидсукцинимидами в органических средах с промежуточным образованием гидроксииминоилгалогенидов с последующей обработкой их основаниями. О высокой избирательности реакции галогидрирования ароматических альдоксимов соответствующими галоидсукцинимидами сообщалось в работах [11, 12].
В первой работе сообщалось о получении 2,4,6-триметилизофтало-бис-нитрилоксида (мезитилендинитрилоксида) с выходом 81% галоидированием диальдоксима N-бромсукцинимидом с последующей обработкой триэтиламином. После перекристаллизации из этилацетата температура плавления нитрилоксида составила 138-139°С.
Во второй работе описан синтез промежуточного 2,4,6-триметил-бензогидроксиминоилхлорида с выходом 92% взаимодействием мезитиленальдоксима с N-хлорсукцинимидом в диметилформамиде. Мезитиленнитрилоксид получен после обработки хлорида триэтиламином в эфире, выход 95%.
Тем не менее, в последующих технологических разработках по получению замещенных арилдинитрилоксидов использовался, главным образом, метод окислительного хлорирования альдоксимов растворами гипохлоритов [13, 14].
Однако, как выяснилось, окисление гипохлоритами в щелочной среде не позволяет получать целевой продукт высокого качества.
Так в патенте [13] динитрилоксид мезитилена получали окислением диальдоксима водным раствором гипохлорита натрия (концентрация около 5%). Выход динитрилоксида составил 87%, содержание основного вещества не приводится. Мы воспроизвели по опубликованной методике [13] получение мезитилендинитрилоксида с использованием гипохлорита натрия из мезитилендиальдоксима высокого качества (98-100%) и получили мезитилендинитрилоксид с содержанием основного веществ на уровне 90-92% по данным метода ВЭЖХ. По-видимому, при синтезе мезитилендинитрилоксида окислением гипохлоритом натрия в щелочной среде протекает побочная реакция с участием промежуточного мезитиленгидроксиминоилхлорида с образованием продуктов димеризации и полимеризации. В отчете [Т.К. Гончаров, Е.П. Игнатьева, А.В. Набатова. Очистка N-динитрилоксидов. Институт проблем химической физики РАН (Черноголовка)] приведены методы очистки промышленных партий мезитилендинитрилоксида с использованием препаративной колоночной хроматографии и перекристаллизации из гексана и этилацетата. При этом качество образцов удалось поднять до 98-99% при существенном снижении выхода.
Еще одним узким местом в технологии получения динитрилоксидов мезитилена и триэтилбензола [20] является стадия окисления бис-гидроксиметилпроизводных в диформилмезитилен и диформилтриэтилбензол хромовым ангидридом в водном растворе серной кислоты. В этой окислительной среде возможно дальнейшее окисление альдегидных групп до карбоксильных, а также протекание процессов димеризации и полимеризации образовавшихся продуктов. Отмечается, что выход диформилпроизводных при промышленных наработках не превышал 50-55%.
В методе, предложенном в патенте фирмы Goodyear [13], при получении стабильных арилдинитрилоксидов исключена стадия окисления бис-гидроксиметильных производных хромовым ангидридом и заменена окислением замещенных бис-галоидметилбензолов с использованием Na- или К-солей нитропропана в изопропиловом спирте и переводом образующихся альдегидов без выделения в стабильные альдоксимы. Для диальдоксима мезитилена, получаемого из бис(бромметил)мезитилена, приведен выход 77,7%. Для триэтилбензола аналогичного примера не приведено, хотя в формулу изобретения включены динитрилоксиды на триэтил- и трипропилбензоле.
Целью настоящего исследования явилась разработка комплексной технологической схемы получения динитрилоксидов триметил- и триэтилбензолов высокого качества и с высоким выходом, в том числе усовершенствование отдельных стадий, описанных в работах [13].
При хлорметилировании мезитилена формальдегидом (36,5%-ным) в концентрированной соляной кислоте при температуре 102±2°С в течение трех часов при загрузке соляной кислоты в два приема выход бис(хлорметил)-мезитилена составил 85%. Нам в тех же условиях, с заменой формальдегида на параформ, удалось повысить выход до 92%.
В литературе практически отсутствуют данные о хлорметилировании триэтилбензола. Известно [6], что при хлорметилировании диэтилбензолов дополнительно в качестве катализаторов применяют уксусную и серную кислоты в мольном соотношении 2,0 и 7,0 к диэтилбензолу.
Нам удалось провести успешно хлорметилирование триэтилбензола с использованием параформа в концентрированной соляной кислоте в присутствии в качестве катализаторов уксусной и серной кислот. Получен бис(хлорметил)триэтилбензол с выходом 85-93% и качеством на уровне 89-93% при следующем мольном соотношении реагентов:
Триэтилбензол: (СН2O)4:НСl:СН3СООН:H2SO4 = 1,0:3,0-4,0:3,8-4,0:6,0:8,0
При гидролизе бис(хлорметил)триалкилбензолов разбавленными растворами едкого натра в присутствии эмульгатора получены соответствующие бис(гидоксиметил)триалкилбензолы с высоким выходом.
В работе [20] на примере окисления сернокислотным раствором хромового ангидрида бис(гидроксиметил)триэтилбензола описана оптимизация параметров процесса, применена экстракция диформилтриэтилбензола четыреххлористым углеродом и, учитывая нестабильность диальдегида, последующее выделение его в виде оксима. При этом удалось повысить качество выделяемого альдоксима до 95-98% и несколько повысить выход (66-68%).
С целью снижения потерь диальдегида триалкилбензолов мы использовали четыреххлористый углерод в качестве растворителя уже на стадии окисления. Далее из раствора в четыреххлористом углероде диальдегид с помощью гидроксиламина и едкого натра переводили в водный раствор в виде натриевой соли альдоксима с последующим подкислением и выделением аьдоксима в свободном состоянии. По двум стадиям (окисление и оксимирование) выход диальдоксима мезитилена составил 72%.
По аналогичной методике проведено получение диформилтриэтилбензола и его диальдоксима. После выделения и сушки получен диальдоксим триэтилбензола с выходом 70-72% и с содержанием основного вещества 98-100% (по данным метода ВЭЖХ).
Таким образом, в результате усовершенствования стадии окисления бис(гидроксиметил)триалкилбензолов хромовым ангидридом существенно увеличен выход диформилтриалкилбензолов и повышено качество диальдоксимов (95-100%).
Как уже отмечалось, альтернативный вариант получения диальдоксимов триалкилбензолов, позволяющий исключить стадию гидролиза бис(галоидметильных) производных и стадию окисления хромовым ангидридом, описан в патенте фирмы Goodyear [13]. Исходный 1,3-бис(бромметил)-2,4,6-триметилбензол был получен бромметилированием мезитилена параформальдегидом и 30 %-ным раствором бромистого водорода в уксусной кислоте. Примеры аналогичного синтеза с использованием других триалкилбензолов, в частности триэтилбензола, не приводятся.
Представлялось целесообразным оценить возможность получения диальдегидов и диальдоксимов триалкилбензолов, исходя из 1,3-бис(хлорметил)триалкилбензолов, учитывая, что реакционная способность в реакциях замещения атома хлора существенно ниже, чем брома.
С этой целью было увеличено время реакции бис(хлорметил)мезитилена с калиевой солью нитропропана при температуре 78-80°С до 2,5-3 часов. Последующее взаимодействие диформилмезитилена с гидроксиламином привело к мезитилендиальдоксиму с выходом 92%. При проведении реакции бис(хлорметил)триэтилбензола с калиевой солью нитропропана для обеспечения полной конверсии бис-хлорметильного производного время выдержки при температуре 78-80°С было увеличено до 4,5-5,5 часов. Кроме того, при взаимодействии образовавшегося диформилтриэтилбензола с водным раствором гидроксиламина при температуре 45-50°С время выдержки также увеличили до 5-6 часов. Выход диальдоксима триэтилбензола составил 95%. При этом содержание основного вещества в обоих случаях было достаточно высоким.
На примере бис(хлорметил)мезитилена показана возможность получения диформилмезитилена при использовании водно-спиртового раствора калиевой соли нитропропана. Аналогичным образом протекает взаимодействие бис(хлорметил)мезитилена с калиевой солью нитроциклогексана.
Таким образом, показано, что при использовании в синтезе триалкилдинитрилоксидов обоих методов бис(хлорметил)триалкилбензолы и бис(альдоксим)триалкилбензолы являются общими, а выходы и качество альдоксимов достаточно высоким.
Ранее отмечалось, что несмотря на высокое качество альдоксимов триалкилбензолов, получить соответствующие нитрилоксиды высокого качества при окислении альдоксимов щелочным раствором гипохлорита натрия не удается.
Как мы уже отмечали, нитрилоксиды можно получить из альдоксимов алкилбензолов через стадию образования гидроксилиминогалогенидов с последующим дегидрогалогенированием с помощью оснований. Нами предложен двухстадийный процесс получения динитрилоксидов триалкилбензолов с применением N-хлорсукцинимида в качестве хлорирующего агента и последующей обработкой триэтиламином.
Реакцию диальдоксимов с N-хлорсукцинимидом проводили в диметилформамиде при температуре 35-40°С. На первом этапе вводили 1/3 расчетного количества N-хлорсукцинимида или его раствора в диметилформамиде, реакционную смесь подогревали до температуры 35-40°С и после небольшого инкубационного периода (3-5 мин) начиналась реакция хлорирования, что заметно по повышению температуры. Остальное количество N-хлорсукцинимида дозировали, поддерживая температуру 35-40°С за счет выделяющегося тепла реакции. После выдержки и охлаждения смеси до 0-5°С в реакционную смесь подавали триэтиламин, поддерживая эту температуру внешним охлаждением. После выдержки смесь разбавляли водой и выделяли влажные динитрилоксиды с выходом 90-95% в пересчете на сухой продукт и содержанием основного вещества 95-99% (метод ВЭЖХ). Динитрилоксиды триалкилбензолов хранят во влажном состоянии. При необходимости динитрилоксиды сушили при температуре 40-45°С.
Образцы динитрилоксидов мезитилена и триэтилбензола прошли успешно испытания в качестве отвердителей в составе композиций на основе непредельных каучуков в ФГУП "Федеральный центр двойных технологий "Союз" г. Дзержинский Московской области.
Примеры синтезов
Пример 1. Получение бис(хлорметил)мезитилена
В реактор загружают 140 г (98%-ного) мезитилена, 100 г (98,5%-ного) параформа, 680 г (36%-ной) соляной кислоты, 12 г хлористого натрия и 3,6 г эмульгатора (стиральный порошок «Тайд»). Компоненты перемешивают в течение 15-20 минут, затем реакционную смесь медленно, в течение 2-2,5 часов подогревают до температуры 95-105°С и выдерживают при перемешивании в течение 5 часов. Степень превращения мезитилена и содержание хлорметильных производных определяют с помощью метода ГЖХ. При содержании монохлорметилмезитилена менее 1% нагрев прекращают, реакционную массу охлаждают при перемешивании до температуры 60-70°С, дальнейшее охлаждение до температуры 20-25°С ведут без перемешивания. После выдержки в течение 1 часа мелкодисперсную суспензию фильтруют, осадок на фильтре промывают водой до рН 6-7 и сушат при температуре 60-70°С. Выход бис(хлорметил)мезитилена составил 92%. Содержание основного вещества - 95%, содержание трис(хлорметил)мезитилена - 4%. Соотношение мезитилен: параформ: хлористый водород в мольном соотношении составило 1:2,9:5,9.
Аналогичные результаты получены при мольном соотношении мезитилен: параформ: хлористый водород в пределах 1:2,8-3,0:5,8-6,0.
Пример 2. Получение бис(хлорметил)триэтилбензола
В реактор загружают 91 г (99%-ную) смесь изомеров триэтилбензола, 52,5 (95,6%-ного) параформа, 201 г ледяной уксусной кислоты и 221 г (36%-ной) соляной кислоты, содержащей около 4 г хлористого натрия к 1,5 эмульгатора. Смесь перемешивают в течение 10-15 мин и дозируют 450 г (96%-ной) серной кислоты в течение 40-50 минут. При этом температура реакционной смеси поднимается до 40-45°С. Далее смесь медленно нагревают и выдерживают 1 час при 50-60°С, 1 час при 60-70°С и в течение 6-7 часов при температуре 75-78°С. При содержании монохлорметилтриэтилбензола по данным ГЖХ менее 1% реакционную массу охлаждают при интенсивном перемешивания, суспензию отстаивают при температуре 20-25°С в течение 1 час и декантируют. К осадку приливают 500 мл воды, перемешивают и фильтруют, осадок промывают на фильтре водой до рН 5-6 и сушат на воздухе. Выход бис(хлорметил)триэтилбензола в пересчете на сухой продукт составил 85-90% при содержании основного вещества 89-90%. Сырец такого качества применялся на следующей стадии без дополнительной очистки. Соотношения реагентов в мольном соотношении (С2Н5)3С6Н3: параформ: НСl:СН3СООН:H2SO4 составило 1:3,0:3,9:6,0.
Приведенные результаты были получены при проведении ряда экспериментов при следующих мольных соотношениях реагентов:
Триэтилбензол: (СН2O)4:НСl:СН3СООН:H2SO4 = 1,0:3,0-4,0:3,9:6,0:8,0
При уменьшении количества уксусной и серной кислот по отношению к триэтилбензолу до 4,5 и 6,5 молей соответственно и увеличении выдержки реакционной массы при 75-78°С до 13-14 часов выход бис(хлорметил)триэтилбензола увеличивался до 93% с повышением содержания основного вещества (91-93%).
Пример 3. Получение бис(гидроксиметил)триэтилбензолов Методика А. Получение бис(гидроксиметил)мезитилена
В реактор загружают 15 кг бис(хлорметил)мезитилена, 120 кг 5,5%-ного раствора гидроокиси натрия и 250 г эмульгатора (стиральный порошок «Тайд»). при интенсивном перемешивании реакционную смесь нагревают до 95-98°С и выдерживают в течение 2 часов, определяют остаточную концентрацию щелочи, далее анализ повторяют через каждый час до постоянного значения концентрации щелочи. Содержимое реактора охлаждают, образовавшуюся мелкодисперсную суспензию фильтруют, промывают осадок водой до нейтральной реакции. Влажный бис(гидроксиметил)мезитилен сушат при температуре 90-100°С, выход 11,2 кг (95,5%), содержание основного вещества по данным ГЖХ - 96%.
Методика Б. Получение бис(гидроксиметил)триэтилбензола
Проводили аналогично, применяя водный раствор гидроокиси натрия с концентрацией 2,2% масс. Выход составил 96%, содержание основного вещества 85%.
Пример 4. Получение диальдоксимов триалкилбензолов. Окисление гидроксиметилпроизводных хромовым ангидридом
В реактор загружают 0,12 моля бис(гидроксиметил)триалкилбензола, 400 г четыреххлористого углерода, 250 г 20%-ного раствора серной кислоты. Смесь при перемешивании нагревают до температуры 40°С и начинают прибавлять 38,0 г (0,19 мол) 50%-ного водного раствора хромового ангидрида с такой скоростью, чтобы температура в реакторе поднималась не выше 55°С. После окончания подачи хромового ангидрида смесь выдерживают при температуре 50-55°С в течение 1 часа и охлаждают до температуры 20-25°С. Слои разделяют в делительной воронке и органический слой, представляющий собой раствор диформилтриалкилбензола в четыреххлористом углероде, возвращают в реактор. К нему приливают 290 г 10%-ного раствора гидроокиси натрия и 25 г гидроксиламина солянокислого. Реакционную смесь нагревают при перемешивании до температуры 50-55°С, выдерживают в течение 1 часа, охлаждают и разделяют слои в делительной воронке. Водный слой, представляющий собой динатриевую соль диальдоксима триалкилбензола, возвращают в реактор, добавляют 1-2 г эмульгатора и подкисляют 10%-ным раствором серной кислоты при охлаждении (температура 20-30°С) до достижения значения рН среды равного 6-7. Суспензию выдерживают 1 час для завершения кристаллизации и фильтруют. Осадок промывают на фильтре водой, отжимают и сушат при температуре 90-100°С.
Выход диальдоксимов триалкилбензолов составлял 70-72% в расчете на бис(гидроксиметил)производные при содержании основного вещества 98-100% по данным ВЭЖХ.
Пример 5. Получение диформил- и диальдоксим- триалкилбензолов с использованием калиевой соли нитропропана
Диальдоксимы триалкилбензолов получают окислением бис(хлорметил)триалкилбензолов калиевой солью нитропропана в изопропиловом спирте с последующим оксимированием образующихся диформилтриалкилбензолов без выделения с участием гидроксиламина по следующей схеме:
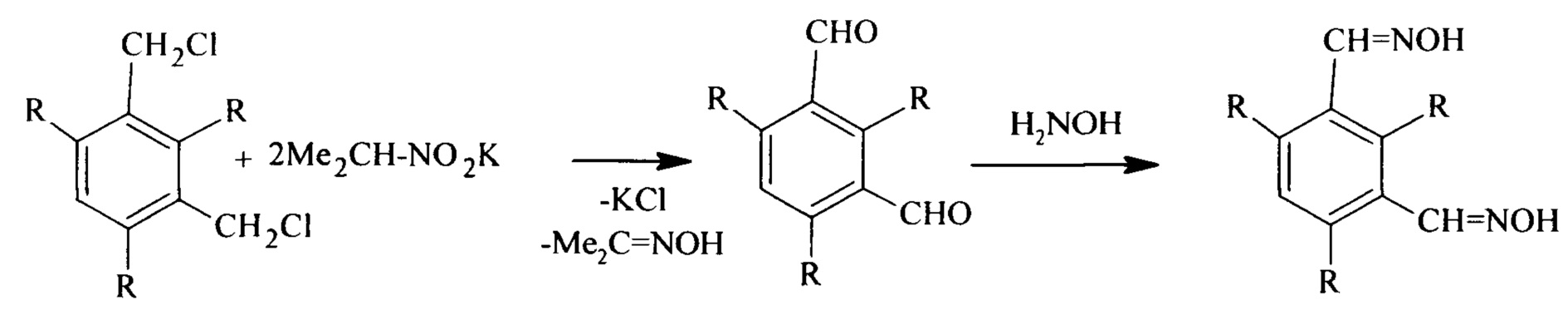
Реакцию окисления и оксимирования проводят в атмосфере инертного газа.
Методика А. Получение мезитилен- и триэтилбензол- диальдоксимов с использованием калиевой соли нитропропана
Реакцию окисления и оксимирования проводят в атмосфере инертного газа (аргона). К предварительно приготовленному раствору 140 г (2,50 мол) едкого кали в 2550 мл изопропилового спирта при перемешивании, порциями (в 2-3 приема), прибавляют 283 г (3,17 мол) нитропропана в течение 15-20 минут. При этом температура реакционной массы поднимается до 40°С. Затем проводят выдержку при температуре 40-45°С в течение 1 часа и начинают загрузку 260 г (1,20 мол) бис(хлорметил)мезитилена, порциями (в 5-6 приемов), в течение 40-50 минут. Реакция протекает с разогревом реакционной массы до 60-65°С. По окончании подачи бис(хлорметил)мезитилена температуру повышают до 78-80°С и выдерживают в течение 2,5-3 часов. Затем реакционную массу охлаждают и методом ГЖХ определяют полноту превращения бис(хлорметил)мезитилена. При необходимости реакцию продолжают.
Далее, не выделяя диформилмезитилен, при перемешивании и нагреве до 35-40°С в реакционную смесь дозируют 174,2 г (2,64 мол) 50%-ного водного раствора гидроксиламина с такой скоростью, чтобы температура не поднималась выше 50°С. После выдержки в течение 1 часа при этой температуре происходит полное превращение диформилмезитилена в диальдоксим (по данным ВЭЖХ).
После охлаждения до температуры 20-25°С реакционную массу при перемешивании выливают в 4-5-кратный объем захоложенной до 10-15°С воды. После отстаивания в течение 3-4 часов выпавший в осадок диальдоксим фильтруют, промывают водой (4×500 мл) и сушат при температуре 70-75°С.
Выход сухого мезитилендиальдоксима составил 92% при содержании основного вещества 98% (по данным ВЭЖХ).
По аналогичной методике получали диальдоксим триэтилбензола. При взаимодействии калиевой соли нитропропана с бис(хлорметил)триэтилбензолом при нагревании время реакции было увеличено до 4,5-5,5 часов. Кроме того, при взаимодействии образовавшегося диформилтриэтилбензола с водным раствором гидроксиламина при температуре 45-50°С время выдержки увеличили до 5-6 часов.
Выход диальдоксима триэтилбензола составил 95%, при содержании основного вещества в пределах 91-95%.
Методика Б. Получение мезитилендиальдоксима в водно-спиртовом растворе калиевой соли нитропропана
В токе инертного газа (аргона) растворяют при перемешивании 14,0 г едкого кали в 250 мл 80%-ного изопропилового спирта. Затем в течение 10 минут в реактор подают 30 г нитропропана. Реакционную смесь нагревают при температуре 40-45°С в течение 1 часа. К раствору калиевой соли нитропропана в течение 20 минут присыпают 25,8 г бис(хлорметил)мезитилена. Реакция протекает с выделением тепла, и температура реакционной массы поднимается до 60 °С. Для завершения реакции смесь нагревают до 75-80°С и выдерживают в течение 3-х часов. Оксимирование образовавшегося диформилмезитилена и выделение диальдоксима проводят в последовательности, описанной в методике А. Для предотвращения осаждения непрореагировавшего диформилмезитилена в присутствии воды гидроксиламин применяли также в виде раствора в 80%-ном изопропаноле.
Выход 97 %-ного диальдоксима мезитилена составил 90%.
Методика В. Получение мезитилендиальдоксима с использованием калиевой соли нитроциклогексана
В реактор помещают 14,0 г (0,25 моль) едкого кали, 22 мл воды и 110 мл изопропилового спирта и, после полного растворения едкого кали, при температуре 10-20°С прибавляют 35 г (0,27 моль) нитроциклогексана. Затем раствор калиевой соли нитроциклогексана нагревают до 70°С и прибавляют порциями в течение 20-30 минут 22,0 г (0,1 моль) бис(хлорметил)мезитилена. Реакционную смесь выдерживают при температуре 70-75°С в течение 2-х часов. После подтверждения методом ГЖХ полного превращения бис(хлорметил)мезитилена в диформилмезитилен, получение и выделение мезитилендиальдоксима ведут аналогично методике А.
Выход составил 89% в пересчете на сухой продукт.
Пример 6. Получение мезитилендинитрилоксида
Методика А
В реакторе при перемешивании растворяют 70 г (0,34 моль) мезитилендиальдоксима в 1000 мл диметилформамида. Отдельно готовят раствор 92 г (0,69 моль) N-хлорсукцинимида в 100 мл диметилформамида и загружают 1/3 части раствора в реактор. Начало реакции оценивают по повышению температуры реакционной смеси. При отсутствии теплового эффекта в реактор подают 20-25 см3 парогазовой смеси из емкости с концентрированной соляной кислотой. Через 3-5 минут наблюдается рост температуры, что свидетельствует о начале реакции. При подъеме температуры на 4-5°С начинают подачу раствора N-хлорсукцинимида с такой скоростью, чтобы температура реакционной смеси поддерживалась на уровне 35-40°С. После окончания дозировки раствора N-хлорсукцинимида проводят выдержку в течение 1 часа при этой же температуре. Окончание реакции определяют по йод-крахмальной бумаге, смоченной дистиллированной водой (образование слабого темного кольца при нанесении). Реакционную массу охлаждают до температуры 0-3°С и прибавляют 68 г (0,67 моль) триэтиламина со скоростью, позволяющей поддерживать температуру не выше 5°С. После окончания дозировки проводят выдержку в течение 30 минут с постепенным повышением температуры до комнатной. Реакционную массу выливают при перемешивании в три объема (~ 4500 мл) охлажденной (5-10°С) воды, отстаивают без перемешивания 1,5-2 часа и фильтруют. Осадок промывают водой до отсутствия ионов хлора (проба с азотнокислым серебром). Получают 160 г динитрилоксида с влажностью 60%.
После сушки при температуре 40-45°С выход составил 62 г (95%). Содержание основного вещества - 98,4% (метод ВЭЖХ).
В аналогичных условиях из диальдоксима триэтилбензола получен динитрилоксид с выходом 92-94% и содержанием основного вещества 96-97%.
Методика Б
В 20%-ный раствор мезитилендиальдоксима в диметилформамиде (6 г в 25 мл), нагретый до температуры 33-35°С, добавляют 1,6 г сухого N-хлорсукцинимида. Температура смеси снижается до 30°С, а затем в течение 1 мин поднимается до 40°С. После того, как первая порция N-хлорсукцинимида прореагировала, и температура начала снижаться, продолжают подачу 6,3 г N-хлорсукцинимида в несколько приемов, поддерживая температуру 38-40°С внешним охлаждением реактора. Для завершения реакции смесь выдерживают при этой температуре в течение 1 часа. Затем реакционную смесь охлаждают до температуры 2-3°С и обрабатывают триэтиламином (6 г). Продолжение синтеза и выделение мезитилендинитрилоксида ведут аналогично методике А.
Получено 5,6 г (выход 95,2%) продукта с содержанием основного вещества 98,5%.
Применение в синтезе сухого N-хлорсукцинимида позволяет увеличить концентрацию реагирующих веществ и съем целевого продукта с единицы реакционного объема.
Список литературы
1. Патент США 3390204 (1968) [Chem. Abstr. 1968, 69, 36900].
2. Бойко В.В. и др. «Каучук и резина» 1994, №5, 16.
3. Бойко В.В. и др. «Каучук и резина» 1998, №1, 36.
4. Бойко В.В. и др. «Химическая промышленность. Серия: Актуальные вопросы химии и химической технологии» Черкассы, 1994, выпуск 3.
5. Авторское свидетельство СССР 1824389(1993).
6. Патент РФ 2045546 (1995).
7. Бойко В.В. и др. International Polymer Science and Technology. 1993, 20, №10, 51.
8. Бойко В.В. и др. International Polymer Science and Technology. 1995, 22, №7, 21.
9. K. Ajay Kumar, M. Govindaraju, P. Jayaroopa, G. Vasanth Kumar. IJPCBS 2012, 3(1), 91-101.
10. C. Grundmann, J.M. Dean J. Org. Chem., 1965, 30, 2809-2812.
11. C. Grundmann, R.Richter J. Org. Chem., 1968, 33, 476.
12. K.C. Liu, B.R. Shelton, R.K. Howe J. Org. Chem., 1980, 45, 3916.
13. Патент США 3655826 (2002).
14. Патент РФ 2042664 (1995).
15. Якубов А.П. и др. Изв. АН СССР. Сер.хим. 1991, №5, 1201.
16. Якубов А.П. и др. Изв. АН СССР. Сер.хим. 1991, №7, 1609.
17. Авторское свидетельство СССР 1685914(1991).
18. G. Just, K. Dhal Tetrahedron 1968, 24 (15), 5251.
19. R.E. Partch. Tetrahedron Letters 1964, 3071.
20. С.Б. Апельчугин, И.В. Краукшин, А.Е. Пунин, Г.И. Цыпин, ЖПХ, 2003, 76, выпуск 8, 1312.