Результат интеллектуальной деятельности: Генетическая конструкция pA21/Fab, для получения одноцепочечного антитела, слитого с константным фрагментом иммуноглобулина человека, стереоселективно взаимодействующего с фосфорорганическими соединениями.
Вид РИД
Изобретение
Изобретение относится к биотехнологии, а именно: к технологии получения рекомбинантных антител человека (рчАт) и может быть использовано в медицине в терапии отравлений фосфорорганическими токсинами, для терапии отравлений наркотическими веществами типа кокаин.
В настоящее время антитела имеют широкое применение в медицине и биотехнологии благодаря их способности специфически узнавать и связывать антигены. Возможность искусственно создавать антитела к самым различным соединениям, не имеющим природного аналога, является одной из причин, по которой данная область науки приковывает к себе большое внимание. Однако только на связывании функции антител не ограничиваются. В конце двадцатого столетия была обнаружена способность антител к биокатализу, позволяющая им не только связывать, но и разрушать антиген. На сегодняшний день получено значительное число каталитических антител (абзимов), катализирующих разнообразные химические реакции, для которых не известно природных ферментов. В связи с этим, использование каталитических антител для нейтрализации синтетических ядов открывает широкие перспективы в борьбе с химическими отравлениями, в частности с фосфорорганическими токсинами.
Ранее в результате скрининга полусинтетической библиотеки вариабельных фрагментов генов иммуноглобулинов человека с использованием п-нитрофенил-8-метил-8-азабицикло[3.2.1]октанфенилфосфоната (фосфонат X) была отобрана панель рекомбинантных одноцепочечных антител, способных к ковалентному взаимодействию с фосфорорганическими соединениями. Наибольшей активностью из отобранных антител обладали А5 и А17, для которых было установлено, что ковалентной модификации подвергаются остатки L-Tyr33 и L-Tyr37 соответственно. Отличие в положении ключевого аминокислотного остатка в реакционном центре свидетельствует о возможной реализации разных механизмов взаимодействия абзимов с субстратом. Для антитела А17 было показано, что оно способно гидролизовать пестицид параоксон, взаимодействие с фосфорорганическими субстратами осуществляется по механизму индуцированного соответствия, а изотип константного домена легкой цепи (каппа/лямбда) оказывает влияние на структурную организацию. На основе накопленного широкого спектра структурных и функциональных данных антитело А17 было использовано в качестве модели длянаправленного улучшения его каталитических свойств: методом квантовой механики и молекулярной механики (КМ/ММ) успешно предсказаны и экспериментально охарактеризованы мутанты с улучшенной специфичностью к параоксону.
Большинство фосфорорганических соединений, обладающих токсическим действием, являются хиральными молекулами. Таким образом, создание биологических антидотов стереспецифично взаимодействующих с такими ФОТ целесообразно.
Данное изобретение описывает генетическую конструкцию, предназначенную для получения одноцепочечного антитела слитного с константным доменом антитела человека.
Известен способ получения одноцепочечных антител в клетках линии P. pastoris в составе слитного белка с константным доменом иммуноглобулина мыши (Wang DD, Su MM, Sun Y, Huang SL, Wang J, Yan WQ. Protein Expr Purif. 2012 Nov; 86(l):75-81). В данной работе использовалась одноцистронная система векторов. Авторам удалось получить выход продукта 60 мг/л при использовании 80 литрового ферментера. Недостатком этой системы является получение антитела в виде одноцепочечного фрагмента, так как существуют данные о различии в уровнях специфической активности между Fab-фрагментами и одноцепочечными антителами в пользу первых (Захаров А.В., Смирнов И.В., Серебрякова М.В. и др. // Молекуляр. биология. 2011. Т. 45, №1, С. 86-95).
Известна система получения Fab-фрагмента антитела в составе моноцистронного вектора содержащего сайт гидролиза протеазой KEX2 (Burtet RT1, Santos-Silva MA, Buss GA, Moraes LM, Maranhao AQ, Brigido MM. J Biochem. 2007 Dec; 142(6):665-9). В результате авторам удалось получить функционально активный Fab-фрагмент, однако уровень экспрессии не превышал 10 мг/л культуральной среды.
Описана система получения Fab-фрагмента антитела, состоящая из двух моноцистронных векторов, кодирующих легкие и тяжелые цепи антител, соответственно (Захаров А.В., Смирнов И.В., Серебрякова М.В. и др. // Молекуляр. биология. 2011. Т. 45, №1, С. 86-95). Система позволяла получать до 15 мг/л активного Fab-фрагмента, однако впоследствии была обнаружена невысокая стабильность получаемых препаратов белка, предположительно по причине совыделения и расщепления Fab-фрагментов протеиназами хозяйской клетки.
Для всех представленных антител не описана их стереоспецифичность действия.
Таким образом, не описаны аналоги предлагаемой системы для экспрессии одноцепочечного антитела, стереоспецифично взаимодействующего с фосфорорганическими соединениями.
Изобретение решает задачу получения рекомбинантного одноцепочечного антитела человека, стереоселективно взаимодействующего с фосфорорганическими соединениями.
Поставленная задача решается за счет создания генетической конструкции pA21/Fab, кодирующей ген рекомбинантного антитела, и состоящей из плазмиды pFUSE, которая содержит:
высокоэффективный синтетический промотор hEF/HTLV,
нуклеотидную последовательность гена вариабельных доменов легкой и тяжелой цепи антитела
нуклеотидную последовательность, кодирующую линкер (Ser-Gly3)3,
нуклеотидную последовательность гена константного фрагмента иммуноглобулина человека Fc, содержащую в своем составе СН2 и CH3 константные домены тяжелой цепи IgG1 (Fc2-3) и находящуюся в единой рамке считывания с геном вариабельных доменов антитела.
Техническим результатом использования генетической конструкции pA21/Fab является получение одноцепочечного антитела, слитого с константным фрагментом антитела человека и стереоселективно взаимодействующего с фосфорорганическими соединениями.
Изобретение иллюстрируют следующими графическими материалами:
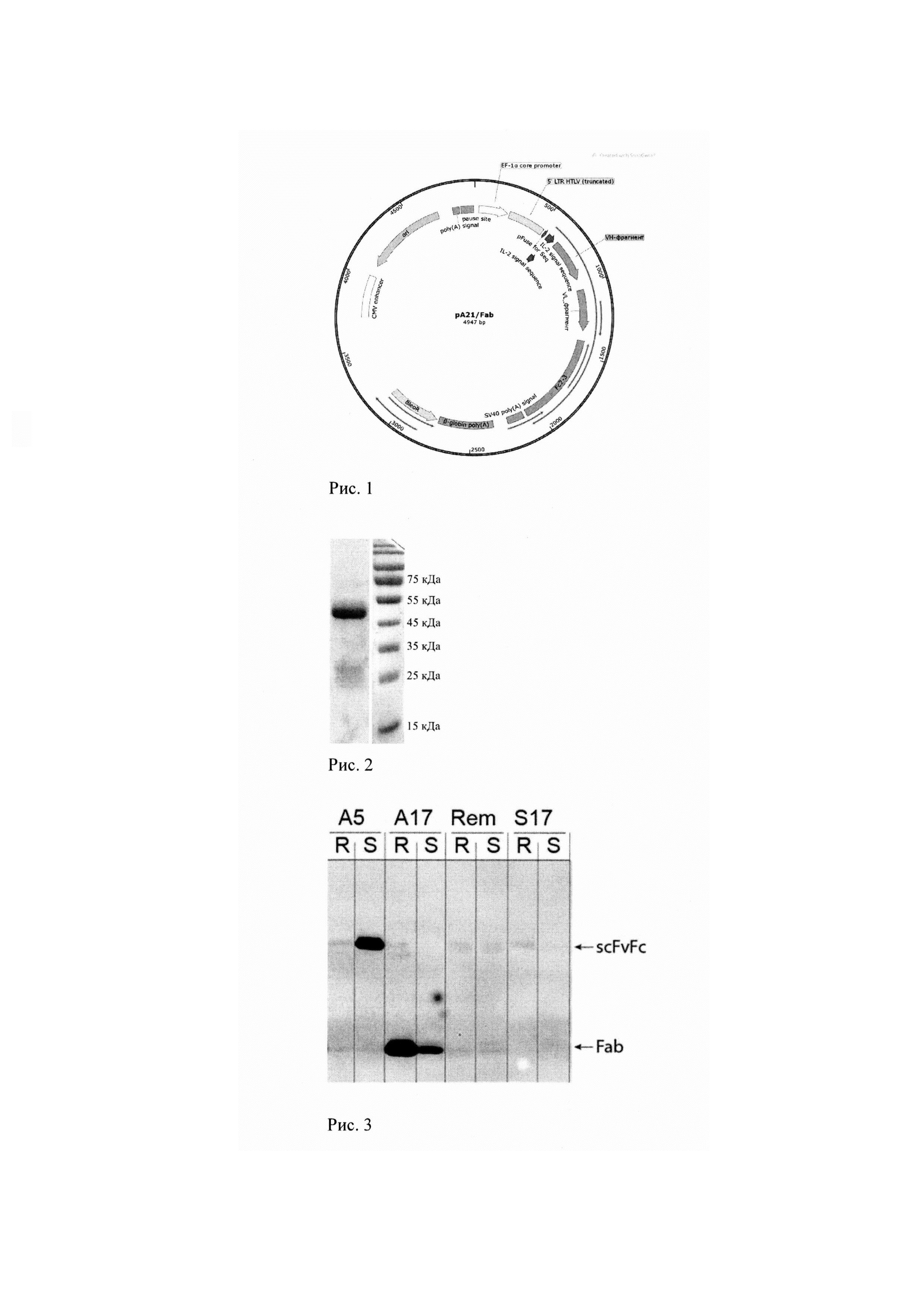
Рис. 1. Схема генетической конструкции pA21/Fab.
Рис. 2. Электрофоретический анализ экспрессии рекомбинантного антитела, полученного после трансфекции клеток линии НЕК-293.
Рис. 3. Анализ стереопецифичности взаимодействия рекомбинантного антитела.
Изобретение иллюстрируют следующими примерами.
ПРИМЕР 1
Создание генетической конструкции pA21/Fab.
Последовательность гена рекомбинантного антитела получают из генетической конструкции scFv_pHEN2 Reshetnyak et al., JACS 2007 с использованием ПЦР с перекрывающихся праймеров и набора олигонуклеотидов atctcgaggatagcaaagtcacaatcatatgcat, gtcccctatgggcacaccatccacggt, cacaccatccacggtaactttggtccgac, aagcggccgctcagagacccacacaactttctttct и последующим клонированием в вектор pFUSE с использованием эндонуклеаз рестрикции NotI и XhoI, с получением генетической конструкции pA21/Fab (Рис. 1).
ПРИМЕР 2
Трансфекция и аналитическая экспрессия генетической конструкции pA21/Fab.
Полученную генетическую конструкцию pA21/Fab линеаризуют и используют для серии трансфекций клеток линии НЕК-293. Селекцию проводят с использованием антибиотика зеоцина в концентрации 100 мкг/мл. Для отбора клонов штамма-продуцента клетки выращивают в среде Advanced DMEM, содержащей 10% фетальной бычьей сыворотки. При достижении конфлюентности более 90%, проводят замену среды на безбелковую среду ProCHO-4, ProCHO-5 или аналогичные. Через 72 часа среду центрифугируют и анализируют электрофоретически (Рис. 2).
Было установлено, что уровень экспрессии рекомбинантного антитела человека, стереоселективно взаимодействующего с фосфорорганическими соединениями, составил около 20 мкг/мл.
ПРИМЕР 3
Анализ стереопецифичности взаимодействия рекомбинантного антитела.
Среду после экспрессии инкубируют с 10 мМ раствором субстрата: (R)-изомера или (S)-изомера арил-фосфоната, конъюгированного с биотином.
Электрофоретическое разделение белков в ПААГ в денатурирующих условиях проводят по стандартной методике. Пробы, контрольный образец и образец рекомбинантного антитела, наносят в буфере: 4% ДСН, 0.25 М Трис-HCl рН6.8, 4 мМ ЭДТА-Na рН 8.0, 10% глицерина, 0.25 мг/мл бромфенолового синего. Электрофорез в концентрирующем геле проводят при силе тока 8-10 мА на 1 пластину геля, а вразделяющем геле при 15-20 мА. По окончании электрофоретического разделения белков в денатурирующем ПААГ пластину с гелем используют для переноса на нитроцеллюлозную бумагу. Перенос проводят в течение 40 минут. После чего мембрану последовательно инкубируют в растворе фосфатно-солевого буфера, содержащего 5% бычьего сывороточного альбумина и стрептавидина, конъюгированного с пероксидазой хрена. Визуализацию результатов иммуноблоттинга осуществляют с использованием прибора Bio-Rad Imager. Результаты, подтверждающие стереоселективность взаимодействия рекомбинантного антитела с арил-фосфонатом, представлены на рисунке 3.Приложение 1
Нуклеотидная последовательность рекомбинантной плазмидная ДНК pA21/Fab.