Результат интеллектуальной деятельности: Фармацевтическая композиция для лечения грибковых поражений слизистых оболочек
Вид РИД
Изобретение
Область техники, к которой относится изобретение.
Настоящее изобретение относится к биохимии, а именно к фармацевтической композиции на основе пептида SE33 (SETRPVLNRLFDKIRQVIRKFEKGIKEKSKRFF) для лечения грибковых поражений слизистых оболочек. Более конкретно данное изобретение относится к составу геля для наружного применения.
Уровень техники.
Грибковые заболевания в медицине называются микозами, и являются достаточно распространенным поводом обращения людей в дерматологическую клинику. Поражение микозами может случиться независимо от возраста. Специалистами изучено около 100 разновидностей грибков - возбудителей болезни. Результатом паразитической деятельности грибка становится непрерывный зуд, покраснение, шелушение кожи.
Трудность лечения грибковых заболеваний состоит в повышенной устойчивости грибков к воздействию лекарственных препаратов и дезинфицирующих средств. Грибки могут находиться в предметах гардероба и обихода человека более 5 лет. Источником заражения обычно выступают инфицированные микозом люди и их вещи. Само заболевание представлено различными формами, самой простой из которых считается шелушение кожи. Кроме этого основного признака, на стопах может появиться небольшое покраснение и легкий зуд.
Перспективными лекарственными кандидатами для лечения грибковых заболеваний являются пептидные препараты. В настоящее время хорошо изучены биологическая активность и механизм действия пептида LL37 (кателицидин человека) и доказан его высокий антимикробный эффект в отношении грамположительных, грамотрицательных бактерий, грибов и оболочечных вирусов (WO 2009/001087, WO 2004/067025, WO 96/08508, RU 2346950).
Исследования пептидов, гомологичных пептиду LL37, и имеющих такие же противогрибковые и иммуностимулирующие свойства, должно позволить разработать новое противогрибковое лекарственное средство, аналогичное по действию лекарственных средств на основе LL37.
Исследования показали, что аналог кателицидина с аминокислотной последовательностью: SETRPVLNRLFDKIRQVIRKFEKGIKEKSKRFF (SE33) обладает сильным антимикробным эффектом, основанным на физико-химических особенностях пептидной последовательности (RU 2434880).
Однако, для применения этих пептидов на практике для лечения бактериальных и грибковых поражений кожи и слизистых оболочек необходимо создать подходящую лекарственную форму. К настоящему времени известны составы мазей, содержащих антимикробные пептиды (RU 2467753, RU 2012103653). Однако, эти составы содержат масляную основу, что затрудняет диффузию пептида из мази в очаг инфицирования, поскольку антимикробные пептиды в неводном окружении образуют амфипатическую альфа-спираль, которая имеет высокое сродство к насыщенным и ненасыщенным углеводородам. Поэтому разработка фармацевтических композиций, содержащих антимикробные пептиды, является актуальной задачей. В случае антимикробных пептидов, представляется предпочтительным использование водорастворимых основ ( , Vitaliy V. Khutoryanskiy, European Polymer Journal 65 (2015) 252-267)
, Vitaliy V. Khutoryanskiy, European Polymer Journal 65 (2015) 252-267)
Наиболее близким аналогом заявляемому изобретению является состав гидрогеля опубликованный в WO 2009/001087.
Раскрытие изобретения.
Настоящее изобретение решает задачу расширения арсенала средств для лечения грибковых поражений слизистых оболочек. Были проведены исследования композиций, которые содержали полиэтиленгликоль-400 (ПЭГ-400), гидроксипропилметилцеллюлозу (ГПМЦ) и пептид SE33, в качестве действующего вещества. Причем концентрация полиэтиленгликоля-400 была от 1 до 10% массовых, ГПМЦ - от 1 до 8%, концентрация пептида была постоянной 1 мг/мл (0.001%). Исследовали несколько параметром: вязкость композиции, стабильность и ее биологическую активность. Вязкость композиции делает возможным ее физическое применение, поскольку слишком текучий состав не позволяет фиксировать гель на очаге поражения, а слишком вязкий (плотный) состав затрудняет выход пептида из геля в рану. Стабильность - характеристика важная для потребительских свойств композиции. Биологическая активность композиции - технический результат, основанный на ее свойствах (соотношении компонентов). В результате исследований было обнаружено оптимальное соотношение компонентов, масс. %:
|
Изобретение иллюстрируют Фиг. 1 и 2:
Фиг. 1. Киллерный эффект пептида SE33 по отношению к клеткам Candida albicans:
А - концентрация пептида 1 мг/мл,
Б - концентрация пептида 3 мг/мл,
В - концентрация пептида 10 мг/мл.
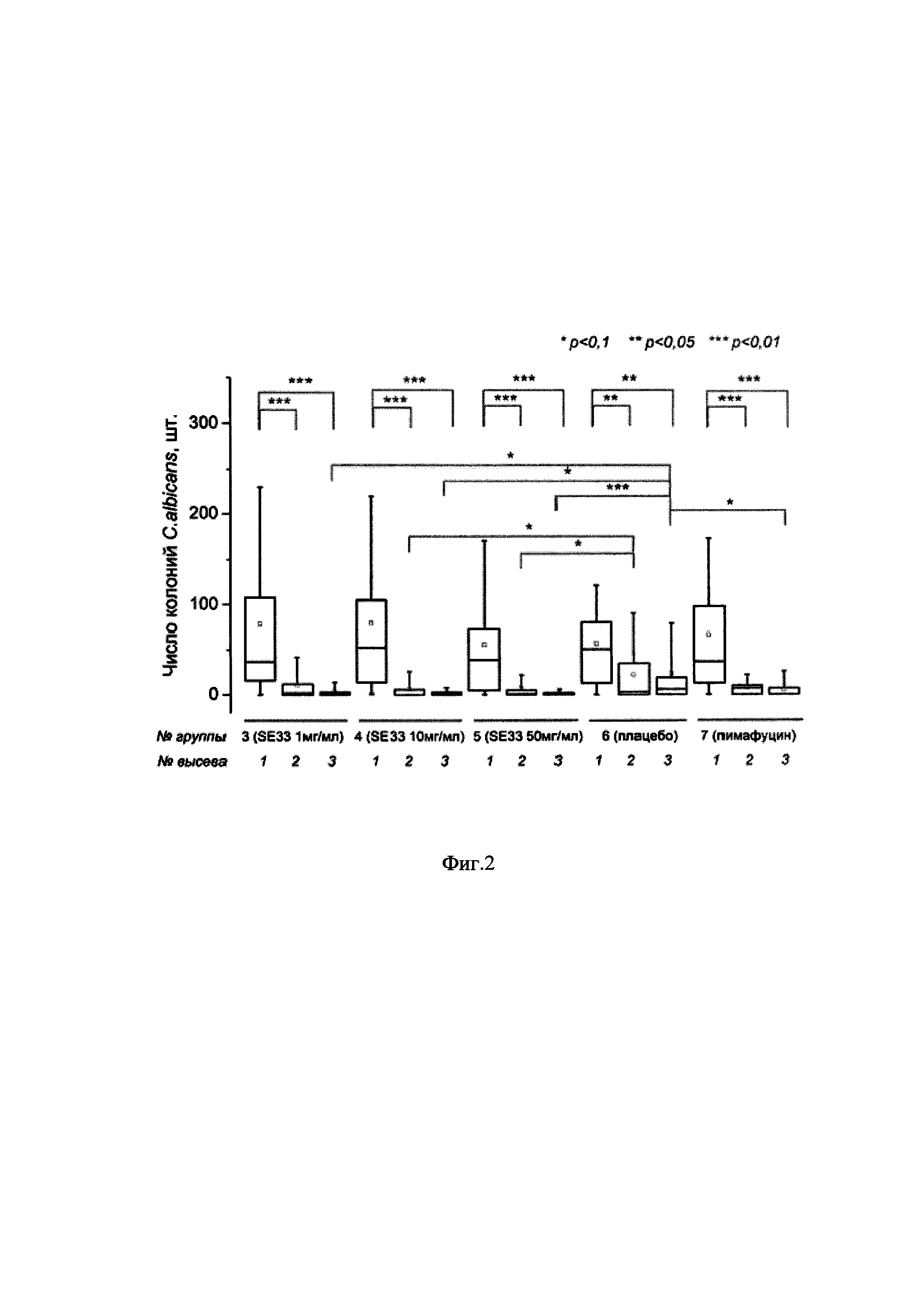
Фиг 2. Зависимость обсемененности вагины мышей дрожжами Candida albicans от дозы лечебного препарата в группах №3-7 в динамике лечения. Первый высев проводили до начала лечения, второй и третий высевы - через неделю и через две недели после начала лечения, соответственно. Wilcoxon Signed Rank Test и ANOVA on Ranks with Tukey's and Dunnet's post hoc tests, p<0,01-p<0,1.
Примеры осуществления изобретения.
Пример 1. Приготовление геля на основе гидроксипропил метилцеллюлозы (ГПМЦ)
Для приготовления геля сначала готовят 2,5% раствор ГПМЦ. Раствор готовят при перемешивании на магнитной мешалке до полного растворения при комнатной температуре за сутки до приготовления доз. Для дальнейшего использования готовый раствор ГПМЦ хранят в холодильнике 5±3°C в течение 1-7 дней. В день приготовления доз отбирают необходимую аликвоту раствора ГПМЦ. Аликвоту помещают на магнитную мешалку с подогревом или водяную баню (60-70°C). Примерно через 5 минут в подогретый раствор ГПМЦ добавляют ПЭГ-400 с доведением раствора по ПЭГ-400 до 5%. Далее через 2-5 минут в подготовленный раствор добавляют расчетное количество пептида (минимальная доза концентрация - 1,0 мг/мл; максимальная доза концентрация - 50 мг/мл). Раствор перемешивают на магнитной мешалке до полного растворения пептида примерно 60 секунд. Далее готовый раствор помещают в холодную водяную баню (температура холодной проточной воды) и примерно через 5 минут передают для использования.
Пример 2. Исследование хронической токсичности геля, содержащего пептид SE33.
Хроническая токсичность геля, содержащего пептид SE33, была изучена при его многократном накожном нанесении самцам и самкам крыс SD в течение 28 дней с последующим 14-дневным периодом отмены.
Во время исследования гибели животных или клинических признаков интоксикации животных не было. У животных всех групп в течение исследования наблюдалась положительная динамика массы тела. При этом статистически значимых различий между группами животных как самцов, так и самок с нанесением исследуемого вещества на кожу относительно соответствующих контрольных групп не было. Накожное нанесение исследуемого геля не приводило к статистически значимому изменению в потреблении корма животными. Изучение эффектов местно-раздражающего действия с использованием шкалы Дрейза выявило незначительные покраснения кожи, которые были характерны как для животных контрольной, так и для крыс экспериментальных групп в равной степени. Выявленные эффекты, вероятно, являлись следствием незначительных повреждений кожи при выстригании шерсти. Остальные изучаемые показатели (гемограмма, биохимических показатели сыворотки крови, масса внутренних органов) также статистически достоверно не различались для опытных и контрольных групп животных.
При плановой некропсии животных в ходе визуального осмотра внешнего состояния тела, внутренних поверхностей и проходов, полости черепа, грудной, брюшной и тазовой полостей с находящимися в них органами и тканями, шеи с органами и тканями, каркаса и скелетно-мышечной системы, кожи - места нанесения лекарственного средства, морфологических признаков токсического действия препарата выявлено не было. Также был проведен микроскопический анализ следующих органов: печень, почки, надпочечники, сердце, легкие, яичники/семенники, селезенка, тимус, желудок, подчелюстные и брыжеечные лимфоузлы, головной мозг и кожа из области нанесения. В перечисленных органах микроскопических повреждений и отклонений от нормы, связанных с действием тестируемого препарата, выявлено не было.
В результате проведенного исследования хронической токсичности было показано, что исследуемый гель не вызывает токсических эффектов как при использовании дозы 6 мг/кг, которая соответствует терапевтической дозе с учетом пересчета на данный вид животных, так и в дозе 75 мг/кг, которая превышает дозу эквивалентную терапевтической в 12,5 раз.
Пример 3. Определение минимальной ингибирующей концентрации (МИК).
Определение МИК проводили методом микроразведений в модифицированной синтетической питательной среде RPMI-1640, содержащей соли, аминокислоты, микроэлементы, витамины, антибиотик и глюкозу [Yarrow D., 1998]. Действие пептида SE-33 изучали в диапазоне концентраций 0,5-1024 мкг/мл. Опыты проводили в 96-тилуночных круглодонных планшетах. По горизонтали вносили препарат в конечной концентрации 1024 мкг/мл и ниже с шагом двукратного разведения (20 мкл), после чего добавляли суспензию клеток дрожжей до конечной концентрации 103 КОЕ/мл (180 мкл). Планшеты помещали в термостат при температуре 320C и инкубировали в течение 48 часов, после чего учитывали результат по изменению цвета индикатора. Такие опыты проводили дважды с интервалом в 1 неделю.
В двух независимых опытах минимальная концентрация, задерживающая рост грибов в течение 2 суток, была равна 1024 мкг/мл. На основании этих данных была выбрана наименьшая концентрация SE33 для опытов in vivo.
Пример 4. Противогрибковое действие пептида SE33 в блиц-опытах.
Суть блиц-экспериментов состояла в следующем: в пробирки типа Эппендорф вносили по 0,5 мл физраствора, содержащего 0 мг/мл 1 мг/мл, 3 мг/мл и 10 мг/мл SE33. Туда же вносили по 30 мкл экспоненциальной культуры Candida albicans №927 (конечное содержанием клеток 106 КОЕ/мл). Смесь инкубировали при 320C в термостате в течение 2 часов, после чего клетки осаждали центрифугированием, супернатант отбрасывали, а клетки окрашивали путем добавления 2 мМ раствора бромкрезолового пурпурного в течение 1 часа. После осаждения клетки микроскопировали, фотографировали, переносили данные в компьютер и подсчитывали процент окрашенных (т.е. мертвых) клеток. Проведение блиц-экспериментов показало, что воздействие SE33 на клетки Candida albicans №927 имеет дозозависимый эффект: так доля мертвых (окрашенных) клеток (за вычетом контроля) при воздействии на грибы пептида в концентрации 1 мг/мл была равна 40,4%, в концентрации 3 мг/мл - 76,9%, в концентрации 10 мг/мл - 92,0% (Фиг. 1). Таким образом из исследованных концентраций SE33 наиболее эффективной оказалась 10 мг/мл.
Пример 5. Противогрибковое действие пептида SE33 в опыте in vivo.
Для создания экспериментального вульвовагинального кандидоза мышей эстрогенизировали в процессе опыта трижды (см. схему) путем втирания 200 мг эстрожеля (примерно 0,125 мкг эстрогена) в брюшко животного. Заражение животных проводили путем однократного интравагинального введения суспензии клеток дрожжей С. albicans в физрастворе, объем инокулята 20 мкл, концентрация клеток 106 КОЕ/мл. «Лечение» животных препаратами проводили путем ежедневного интравагинального введения гелей (в случае пимафуцина - крема) в течение 5 дней, объем пробы 20 мкл. Забор материала для высевов проводили трижды путем интравагинального введения стерильной одноразовой 1 мм микробиологической петли, двукратного прокручивания ее и суспендирования содержимого петли в 200 мкл стерильного физраствора в пробирке Эппен-дорф. После перенесения пробирок из вивария в ламинар производили высевы по 10 мкл из каждой пробирки на чашки Петри со средой ГПД. Чашки инкубировали 1 сутки при 320C, после чего учитывали выросшие колонии дрожжей.
При наблюдении за поведением мышей признаков патологических побочных эффектов не зарегистрировано. Все мыши, независимо от принадлежности к той или иной группе, выжили в данном эксперименте. В группах контроля (группы 1 и 2) ни одна мышь не заболела ВВК на всем протяжении эксперимента, тогда как в опытных группах, обработанных эстрожелем (№3-7), все животные стали носителями Candida albicans.
Терапевтическое действие препаратов.
Лечебный эффект препаратов оценивали по двум показателям: динамика снижения обсемененности вагины в процессе лечения животных и доля «излеченных» (т.е. с нулевым высевом) животных, подсчитанная на 28 день эксперимента. Эти показатели отражены на Фиг. 2 и в таблице 1.
Из приведенных данных на рисунке 2 видно, что обсеменненность вагины до проведения лечения (результаты первого высева) была сравнима для всех групп животных, зараженных Candida albicans (группы 3-7). Препарат SE33 во всех исследуемых дозах (1 мг/мл, 10 мг/мл и 50 мг/мл - группы 3, 4 и 5, соответственно) статистически достоверно (p<0,1 для групп 3 и 4, p<0,01 для группы 5) снижал обсеменность вагины по сравнению с аналогичным показателем в группе плацебо (группа 6) через две недели после начала лечения (третий высев). Эффективность лечения препаратом SE33 во всех дозах была сравнима с таковой для препарата сравнения - пимафуцина в дозе 20 мг/мл (группа 7, третий высев, p<0,1). В самой высокой использованной дозе (50 мг/мл - группа 5) SE33 снижал обсемененность вагины с очень высокой степенью достоверности (p<0,01, третий высев). Стоит отметить, что повышение дозы SE33 с 1 мг/мл (группа 3) до 10 мг/мл (группа 4) и 50 мг/мл (группа 5) приводило к статистически достоверному (p<0,1) отличию в обсеменности вагины по сравнению с контрольной группой №6 уже спустя неделю после начала лечения (второй высев), чего не наблюдалось для препарата сравнения пимафуцина (20 мг/мл, группа 7). Для групп 3-5 (SE33 1 мг/мл, 10 мг/мл и 50 мг/мл, соответственно) была отмечена тенденция снижения обсеменности вагины в динамике лечения (Таблица 1)

Наиболее выраженная активность SE33 в этом исследовании наблюдалась при введении в дозе 50 мг/мл. Введение SE33 в дозах 1 и 10 мг/мл приводило к снижению медианы обсемененности вагины по сравнению с плацебо - в 1,12 раза и увеличению доли полностью излеченных животных в 1,5-1,75 раза по сравнению с плацебо. Введение SE33 в дозе 50 мг/мл приводило к снижению медианы обсемененности вагины по сравнению с плацебо в 1,15 раза и к увеличению доли полностью излеченных животных по сравнению с плацебо в 2,5 раза. Те же показатели для пимафуцина составили 1,14 раза и 2,25 раза, соответственно.