Результат интеллектуальной деятельности: Фармацевтическая композиция, проявляющая цитотоксическое действие в отношении клеток рака мочевого пузыря человека
Вид РИД
Изобретение
Изобретение относится к медицине и фармацевтической промышленности. Предложен состав и способ получения фармацевтической композиции (ФК), проявляющей цитотоксическое действие в отношении клеток рака мочевого пузыря человека.
Изобретение может быть использовано в составе адъювантной терапии немышечно-инвазивного рака мочевого пузыря (РМП).
Частота встречаемости РМП среди опухолей различных локализаций составляет от 3 до 5%. Среди онкоурологических заболеваний РМП занимает второе место после рака предстательной железы. Ежегодно в России РМП диагностируется у 11-15 тыс. людей, при этом около 7 тыс. людей погибают. Мужчины болеют в 4-6 раз чаще, чем женщины. На момент обращения у 75-80% больных диагностируют немышечно-инвазивный РМП. (Статистика злокачественных новообразований в России и странах СНГ в 2012 г. / под редакцией М.И. Давыдова и Е.М. Аксель. М.: Издательская группа РОНЦ, 2014, 226 с.)
«Золотым стандартом» лечения немышечно-инвазивного РМП остается трансуретральная резекция (ТУР). Однако высокая частота рецидивирования (до 50-70%) и возможность прогрессии заставляют искать дополнительные терапевтические подходы. Широкое распространение в связи с этим получили адъювантная химио- и иммунотерапия (например, вакциной БЦЖ и препаратами интерферона) немышечно-инвазивного РМП. Так, проведение внутрипузырной БЦЖ-терапии после ТУР мочевого пузыря позволяет в 3-4 раза уменьшить частоту рецидивов по сравнению с только оперативным лечением (David В. Thompson D.V., Siref L.E., Feloney М.Р. Hauke R.J., Agrawal D.K. Immunological Basis in the Pathogenesis and Treatment of Bladder Cancer // Expert Rev Clin Immunol. - 2015. - Vol. 11. (2): 265-279). Однако внутрипузырная БЦЖ-терапия может сопровождаться рядом побочных эффектов и осложнений (циститы, гранулемы, сепсис с очагами туберкулезного воспаления в различных органах) (Bilsen М.Р., van Meijgaarden K.Е., de Jong H.K. et al. A novel view on the pathogenesis of complications after intravesical BCG for bladder cancer. // Int J Infect Dis. - 2010. - Vol. 72. - p. 63-68). Вместе с тем, по литературным данным от 20 до 40% больных РМП не отвечают на терапию БЦЖ (Kates М., Nirschl Т., Sopko N.A. et al. Intravesical BCG Induces CD4+ T-Cell Expansion in an Immune Competent Model of Bladder Cancer. // Cancer Immunol Res. - 2017. - Vol. 5 (7): 594-603).
Таким образом, разработка менее опасных и более эффективных методов адъювантной терапии немышечно-инвазивного РМП является актуальной проблемой.
Задачей настоящего изобретения является создание ФК природного происхождения, проявляющей цитотоксическое действие в отношении клеток рака мочевого пузыря.
Поставленная задача решается тем, что в заявляемой ФК используется масляный фитоэкстракт (МФЭ) 14 видов растительного сырья с добавлением креолина бесфенольного каменноугольного.
Растительными составляющими ФК являются лекарственные растения, входящие в Государственную фармакопею:
плоды можжевельника обыкновенного (Juniperus communis L. , сем. кипарисовые - Cupressaceae),
трава зверобоя продырявленного - (Hypericum perforatum L., сем. Зверобойные -Hypericaceae);
цветки пижмы обыкновенной (Tanacetum vulgare L., сем. астровые - Asteraceae.);
плоды шиповника (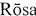 , сем. Розоцветные - Rosaceae);
, сем. Розоцветные - Rosaceae);
корневище лапчатки прямостоячей (Potentilla erecta L.Raeusch. - (syn. Potentilla tormentilla Stokes.), сем. розоцветные - Rosaceae);
корневище и корни родиолы розовой (Rhodiola rosea L., сем. толстянковые -Crassulaceae);
корни женьшеня настоящего (Panax ginseng С. А.Меу, сем. аралиевые - Araliaceae.);
корни солодки голой (Glycyrrhiza glabra L., сем. бобовые - Fabaceae);
листья мяты перечной (Mentha piperita L., сем. яснотковые - Lamiaceae);
корневище с корнями валерианы лекарственной (Valeriana officinalis L. s. I., сем. валериановые - Valerianaceae);
трава душицы обыкновенной (Origanum vulgare L., сем. яснотковые -Lamiaceae);
листья эвкалипта прутовидного (Eucalyptus viminalis Labill., сем. миртовые - Myrtaceae.);
почки сосны обыкновенной (Pinus silvestris L., сем. сосновых -Pinaceae.);
почки березы повислой (березы бородавчатой) - Betula pendula Roth. (Betula verrucosa Ehrh.) и березы пушистой - Betula pubescens Ehrh., сем. березовые - Betulaceae.), взятые в следующих соотношениях, в. ч.:
|
6 растительных составляющих ФК содержат жирные масла (плоды можжевельника, плоды шиповника, корневище родиолы розовой, корни женьшеня, корни солодки, корни валерианы), 2 компонента (корневище лапчатки, березовые почки) - жирные кислоты, 1 компонент (сосновые почки) - липиды, 9 компонентов (плоды можжевельника, трава зверобоя, цветки пижмы, корни солодки, листья мяты, корни валерианы, трава душицы, листья эвкалипта, сосновые почки) - эфирные масла.
Вместе с тем, в состав выбранных растений входят биологически активные соединения фенольной природы, в том числе флавоноиды, фенологликозиды, тритерпеновые гликозиды (гинзенозиды, салидрозид, гиперозид, нарингенин, кверцетин, рутин, лютеолин, апигенин, олеаноловая кислота, глицирризиновая кислота).
Эти вещества в той или иной степени проявляют антиоксидантные, антимутагенные, противоопухолевые, антиметастатические, антиангиогенные, противовоспалительные свойства, в том числе индуцируют апоптоз опухолевых клеток, снижают экспрессию сосудистых ростовых факторов (VEGF), ингибируют образование воспалительных медиаторов. Наряду с этим, благодаря наличию дубильных веществ, корневище лапчатки, корневище родиолы розовой, листья эвкалипта обладают антисептическими, вяжущими свойствами (Белицкий Г.А., Кирсанов К.И., Лесовая Е.А., Якубовская М.Г. Механизмы антиканцерогенного действия флавоноидов. // Успехи молекулярной онкологии 2014; (1): 56-68; Shikov A.N., Pozharitskaya O.N., Makarov V.G., Wagner H., Verpoorte R., Heinrich M. Medicinal plants of the Russian Pharmacopoeia; their history and applications. // J Ethnopharmacol. 2014; 154(3): 481-536).
Креолин бесфенольный каменноугольный (Creolinum anphenolum carbonicum - далее креолин) - лекарственный препарат ветеринарного назначения (Справочник Vidal Лекарственные средства для ветеринарного применения в России, М.: Видаль Рус. - 2016. - 480 с.). Представляет собой маслянистую жидкость, прозрачную в тонком слое, с запахом каменноугольного масла, от темно-коричневого до черно-бурого цвета; с водой образует стойкую эмульсию молочно-белого или молочно-серого цвета.
Водная эмульсия креолина обладает сильным дезинфицирующим, антисептическим, противопаразитарным, в том числе акарицидным действием. Креолин применяется для профилактики и лечения инфекционных заболеваний сельскохозяйственных животных. По степени воздействия на организм животных относится к умеренно опасным веществам (3 класс опасности по ГОСТ 12.1.007-76).
Креолин входит в состав ФК в концентрации 10 об. %.
Примеры получения заявляемой ФК.
ПРИМЕР 1.
Измельченные сухие растительные ингредиенты (в г): 500,0 плодов можжевельника, 500,0 травы зверобоя, 400,0 цветков пижмы, 400,0 плодов шиповника, 400,0 корневищ лапчатки, 200,0 корневищ родиолы розовой, 200,0 корней женьшеня, 100,0 корней солодки, 100,0 листьев мяты, 100,0 корней валерианы, 100,0 травы душицы, 100,0 листьев эвкалипта, 50,0 сосновых почек, 50,0 березовых почек заливали льняным (или кукурузным, или рапсовым) маслом в соотношении 1:5 и экстрагировали методом мацерации при температуре 37°С в течение 24 ч, затем при температуре 70-90° в течение 8 часов. Полученный экстракт сливали, отжимая растительное сырье под прессом. К масляному экстракту добавляли креолин в концентрации 10 об. %. Конечный продукт имеет вязкую консистенцию, специфический запах. Препарат расфасовывают по 20 мл во флаконы из темного стекла. Хранить в холодильнике. Перед использованием довести до температуры 35-36°С. При хранении возможно образование осадка, который удаляется при встряхивании.
ПРИМЕР 2.
Измельченные сухие растительные ингредиенты (в г): 700,0 плодов можжевельника, 700,0 травы зверобоя, 600,0 цветков пижмы, 600,0 плодов шиповника, 600,0 корневищ лапчатки, 300,0 корневищ родиолы розовой, 300,0 корней женьшеня, 200,0 корней солодки, 200,0 листьев мяты, 200,0 корней валерианы, 200,0 травы душицы, 200,0 листьев эвкалипта, 150,0 сосновых почек, 150,0 березовых почек заливали льняным (или кукурузным, или рапсовым) маслом в соотношении 1:5 и экстрагировали методом мацерации при температуре 37°С в течение 24 ч, затем при температуре 70-90° в течение 8 часов. Полученный экстракт сливали, отжимая растительное сырье под прессом. К масляному экстракту добавляли креолин в концентрации 10 об. %. Конечный продукт имеет вязкую консистенцию, специфический запах. Препарат расфасовывают по 20 мл во флаконы из темного стекла. Хранить в холодильнике. Перед использованием довести до температуры 35-36°С. При хранении возможно образование осадка, который удаляется при встряхивании.
Определение влияния отдельных растительных экстрактов и креолина на пролиферативную активность культуры клеток карциномы яичников человека CaOv
Антипролиферативную активность растительных составляющих ФК, а именно компонентов МФЭ (в виде водно-спиртовых экстрактов), а также креолина в отношении клеток карциномы яичников человека линии CaOv оценивали по изменению уровня включения 3Н-тимидина в ДНК опухолевых клеток по сравнению с контрольными пробами без тестируемого агента.
Клетки карциномы яичников человека CaOv культивировали на синтетической среде 199, содержащей 10% телячьей эмбриональной сыворотки при температуре 37°С в течение 24 часов в условиях постоянного перемешивания.
В камере Горяева подсчитывали концентрацию клеток в клеточной суспензии. Полученную суспензию в конечной концентрации 1*105 кл/мл разливали в пенициллиновые флаконы по 2 мл и помещали в термостат на 24 часа при 37°С.
Через 24 часа среду сливали и во флаконы добавляли 2 мл среды, содержащей растительные экстракты в концентрациях 100, 50, 25 мкл/мл среды или креолин в различных разведениях. В контрольные флаконы добавляли соответствующие количества 33% этилового спирта («спиртовый контроль») или среды Игла (контроль). Флаконы с клетками помещали в термостат на 24 часа при 37°С.
За 1 час до окончания экспозиции в культуру клеток добавляли 3Н-тимидин по 0,1 мл в конечной концентрации 1 мкК/мл. Инкубировали 1 час в термостате для включения метки. Через час пробы охлаждали (до 0-4°С) для остановки включения метки. Питательную среду сливали. Клетки дважды промывали холодным раствором Хенкса, а затем 2,5% раствором холодной хлорной кислоты.
После этого в каждый флакон добавляли по 3 мл 5% хлорной кислоты и помещали на водяную баню на 20 минут при 80°С для гидролиза ДНК и экстракции нуклеотидов.
Далее в сцинтилляционные флаконы наливали по 3 мл ЖС-8 и по 0,1 мл остывшего гидролизата. Доводили рН до 7 раствором аммиака и определяли уровень радиоактивности (Dpm) в жидкостном сцинтилляционном счетчике β-распадов.
Значение пролиферации опухолевых клеток определяли по уровню включения 3Н-тимидина в ДНК клеток. Долю (N) пролиферирующих клеток в процентах определяли по формуле:
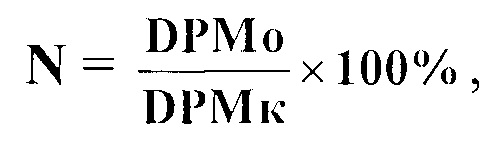 где
где
Dpmo - уровень радиоактивности в опытных образцах;
Dpmk - уровень радиоактивности в контроле.
Для характеристики антипролиферативного эффекта растительных экстрактов использовали показатель СЕ50, которым является концентрация препарата, вызывающая 50%-ное торможение включения 3Н-тимидина в ДНК опухолевых клеток. СЕ50 определяли графически с помощью таблиц пробит. В качестве положительного контроля использовали противоопухолевый препарат циклоплатам.
Для характеристики антипролиферативного эффекта креолина также использовали показатель СЕ50, за который принимали степень разведения препарата, вызывающую 50%-ное торможение включения 3Н-тимидина в ДНК опухолевых клеток.
Цитотоксическую активность ФК и МФЭ в отношении клеток рака мочевого пузыря линии RT-112 оценивали с использованием МТТ-теста (Mosmann Т. Rapid colorimetric assay for cellular growth and survival application to proliferation and cytotoxicity assays. // J Immunol Methods. 1983. -Vol. 65 (1-2): 55-63).
Проведение МТТ-теста
Клетки рака мочевого пузыря линии RT-112 культивировали в среде RPMI-1640, содержащей 10% фетальной бычьей сыворотки, 10 мМ HEPES (Sigma, США), 2 мМ L-глутамина (Sigma, США), 40 нг/мл гентамицина (ICN, США), аминокислоты, пируват натрия и раствор витаминов (ПанЭко, Россия), при 37°С в атмосфере 5% СО2. Клетки рассаживали в 180 мкл полной среды RPMI-1640 в 96-луночные плоскодонные планшеты (Costar, USA) по 5 тыс. клеток на лунку. Через сутки в лунки с клетками добавляли исследуемые экстракты в разведениях с шагом в 2 раза (по 20 мкл/лунку). Каждую исследуемую концентрацию повторяли в трех лунках. В контрольные лунки с клетками добавляли по 20 мкл среды, которую использовали для приготовления разведений тестируемых препаратов. Планшеты с клетками, обработанными ФК или МФЭ, инкубировали при 37°С в атмосфере 5% СО2 в течение 24 часов, после чего добавляли в лунки 20 мкл раствора МТТ [3-(4,5-диметилтиазолин-2)-2,5 дифенилтетразолий бромид] (маточный раствор 5 мг/мл, конечная концентрация 1 мг/мл), и инкубировали 4 ч при 37°С в 5% СО2. После образования формазана надосадочную жидкость удаляли, осадок растворяли в 150 мкл диметисульфоксида. Далее планшеты помещали на 10 минут в термостат при температуре 37°С для растворения кристаллов формазана, затем 10 минут встряхивали на шейкере для равномерного распределения в лунках раствора кристаллов формазана, после чего интенсивность окрашивания среды измеряли на фотометрическом анализаторе иммуноферментных реакций «Multiskan EX (ThermoLab systems) при X=540 нм. Величина поглощения прямо пропорциональна числу живых клеток.
Цитотоксическую активность определяли в процентах (Ц, %) по формуле:
Ц=(1-(Оо/Ок))*100%,
где Ок - оптическая плотность в контрольных лунках, Оо - оптическая плотность в опытных лунках.
Механизм клеточной гибели (апоптоз/некроз) и количество живых/погибших клеток оценивали с помощью метода двойного окрашивания аннексином V и пропидием йодидом, а также определения активной каспазы-3.
Окрашивание аннексином V, меченным FITC, является показателем ранней стадии апоптоза. На ранней стадии апоптоза мембранный фосфолипид фосфатидилсерин перемещается с внутренней поверхности плазматической мембраны на наружную. На поздних стадиях клеточной гибели (апоптотической или некротической) происходит нарушение целостности плазматической мембраны, и ДНК клетки становится доступной для окрашивания пропидием йодидом (PI). Подтверждением апоптотической гибели клеток является детекция того, как клетки последовательно проходят через раннюю и позднюю стадии апоптоза (Аннексии V+/PI-, затем Аннексии V+/PI+), детекция только двойного окрашивания (Аннексии V+/PI+) может быть признаком как апоптоза, так и некроза.
Проведение метода двойного окрашивания аннексином V и пропидием йодиом
Клетки рака мочевого пузыря человека линии RT112 рассаживали в 6-луночные планшеты в количестве 200 тысяч/лунка в 4 мл полной среды RPMI-1640 с 10% фетальной бычьей сыворотки. Через сутки в лунки с клетками добавляли исследуемый препарат в разведениях 1:8 (IC50 для 10% ФК, ранее определенное в МТТ-тесте, и 1:16 (для сравнения). В контрольных лунках клетки инкубировали без препаратов. Через 24 ч инкубации клетки снимали 500 мкл раствора Версена и отмывали. Для оценки клеточной гибели использовали FITC Annexin V Apoptosis Detection Kit I (BD, 556547). Клетки помещали в пробирки для проточной цитометрии в 100 мкл аннексин-связывающего буфера, добавляли по 5 мкл аннексина V-FITC и 5 мкл пропидия йодида (PI). Образцы инкубировали в темноте при комнатной температуре в течение 15 минут. Далее к пробам добавляли 400 мкл аннексин-связывающего буфера и проводили анализ на проточном цитомфлуориметре FACS CantoII (Becton Dickinson).
Анализ апоптотических клеток, окрашенных AnnV-FITC/PI, проводили по следующим параметрам: интактные (живые) клетки AnnV-FITC-/PI-; ранний апоптоз AnnV-FITC+/PI- и поздний апоптоз или некроз AnnV-FITC+/PI+.
Метод определения активной каспазы-3
Каспаза-3, которая активируется инициаторными каспазами-8 или -9, относится к эффекторным каспазам, провоцирующим и непосредственно участвующим в апоптотической трансформации клетки.
Для определения активации каспазы-3 использовали FITC Active Caspase-3 Apoptosis Kit (BD Pharmingen) согласно приложенному к набору протоколу.
Клетки рака мочевого пузыря человека линии RT112 рассаживали в 6-луночные планшеты в количестве 200 тысяч/лунка в 4 мл полной среды RPMI-1640 с 10% фетальной бычьей сыворотки. Через сутки в лунки с клетками добавляли исследуемые препараты в концентрациях, ранее определенных в МТТ-тесте (IC50 для 10% ФК - разведение 1:8). В контрольных лунках клетки инкубировали без препаратов. Через 24 ч инкубации клетки снимали 500 мкл раствора Версена и отмывали.
Для постановки реакции клетки дважды отмывали холодным PBS, затем ресуспенидровали в холодном Cytofix/Cytoperm буфере в концентрации 1*106 клеток/0,5 мл буфера. В течение 20 минут инкубировали клетки на льду. Затем отмывали от Cytofix/Cytoperm дважды в Perm/wash буфере (0,5 мл буфера на 1*106 клеток) при комнатной температуре. Разводили антитела к активной каспазе-3 в Perm/wash буфере (на одну пробирку 20 мкл антител в 100 мкл буфера). Клетки ресуспендировали в полученном растворе с антителами и инкубировали 30 минут при комнатной температуре в темноте. Далее отмывали каждый образец в 1 мл Perm/wash буфера, ресуспендировали в 0,5 мл Perm/wash буфере и анализировали на проточном цитометре FACS CantoII (Becton Dickinson).
При отборе растительных компонентов МФЭ учитывали их фитохимический состав и антипролиферативную активность в отношении культуры клеток карциномы яичников человека CaOv. Для окончательного варианта МФЭ были выбраны экстракты с СЕ50 от < 250 (плоды можжевельника) до 1600 мкг/мл (почки сосны и почки березы).
Антипролиферативный эффект креолина (СЕ50) в тест-системе CaOv наблюдали при разведении препарата в интервале от 4×10J до 2,5×10 раз.
Таким образом, предложенная фармкомпозиция содержит 2 компонента: масляный фитоэкстракт и креолин.
В качестве масляного экстрагента используют пищевые масла, например, льняное масло (ТУ 9141-002-55854031-03), кукурузное масло (ГОСТ 8808-2000), рапсовое масло (ГОСТ 8988-2002). Заявляемое изобретение предусматривает использование любого из перечисленных растительных масел. Соотношение сырья к экстрагенту составляет 1:5. Экстракцию проводят методом мацерации при температуре 37°С в течение 24 ч и при температуре 70-90° в течение 8 часов.
Изобретение иллюстрируется таблицами 1-5 и фигурами 1, 2.
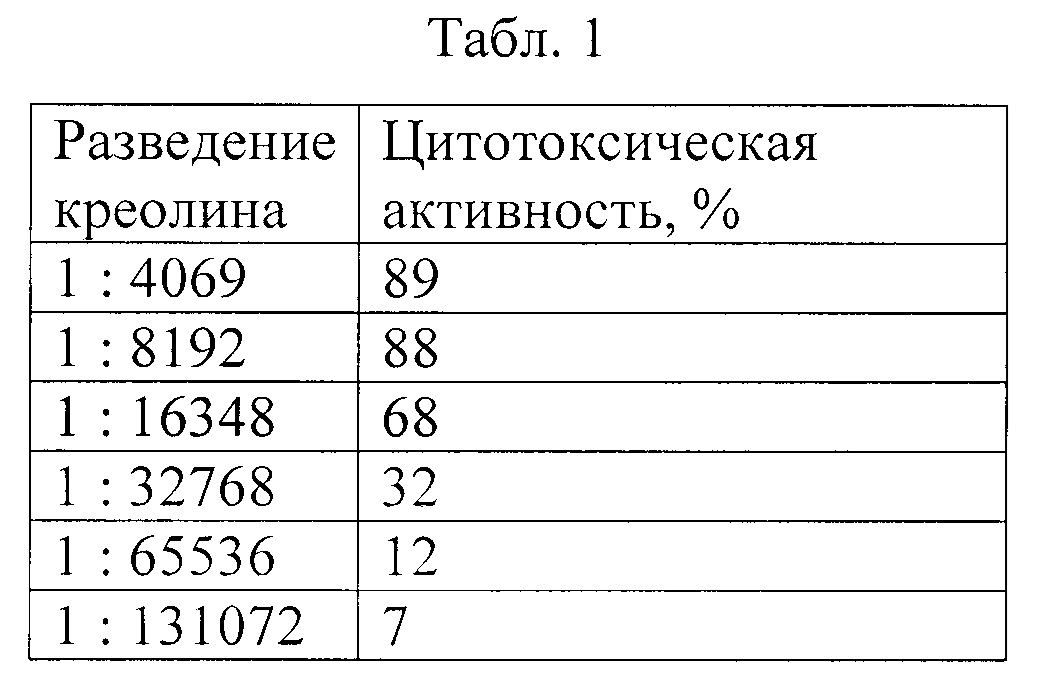
В таблице 1 представлены результаты цитотоксической активности креолина в разведениях, при которых можно было определить оптическую плотность раствора. В исходном виде и при разведении менее, чем 1:4069 креолин искажал результаты оптической плотности в лунках.
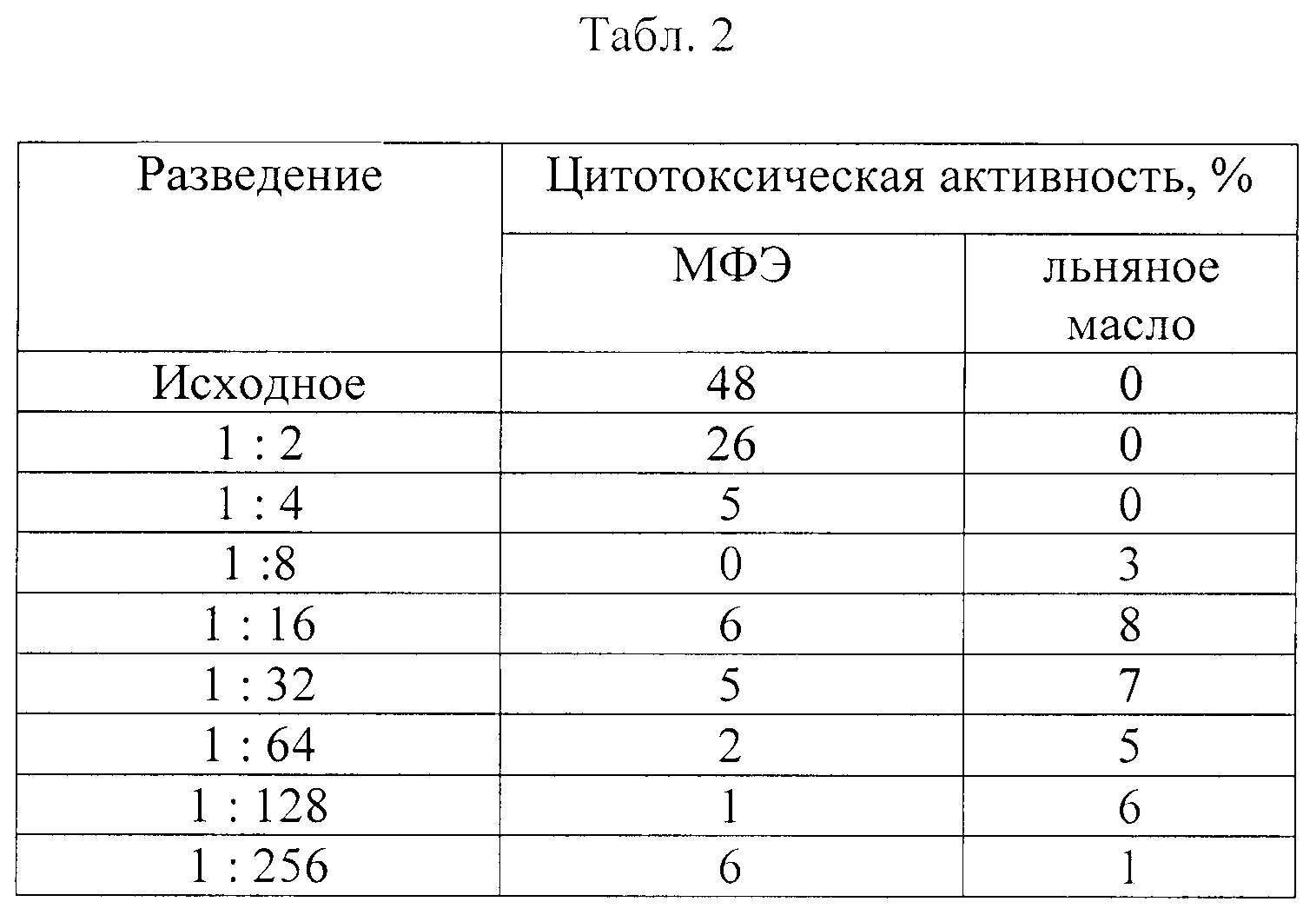
В таблице 2 представлены результаты цитотоксического действия МФЭ и льняного масла. Видно, что МФЭ в исходном виде обладает цитотоксичностью.
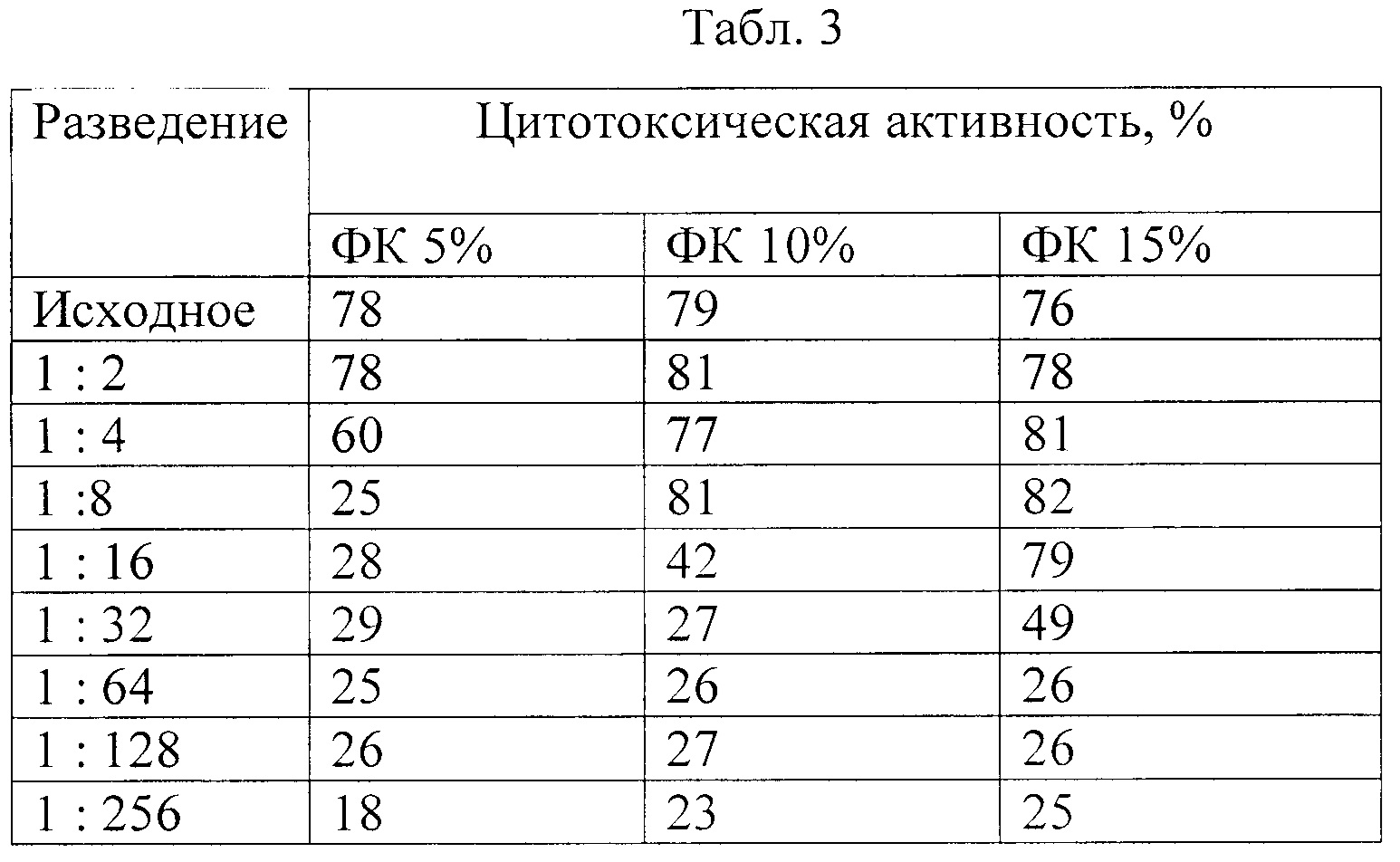
В таблице 3 представлены результаты сравнения цитотоксической активности ФК, содержащего 5%, 10% и 15% креолина, на клетки рака мочевого пузыря RT-112. Видно, что цитотоксичность ФК при 10 и 15% содержании креолина имеет похожие значения. Вместе с тем цитотокчичность ФК при 5% концентрации креолина соответственно снижена. Результаты экспериментов показали, что 10%» концентрация креолина в препарате с точки зрения цитотоксичности является оптимальной.
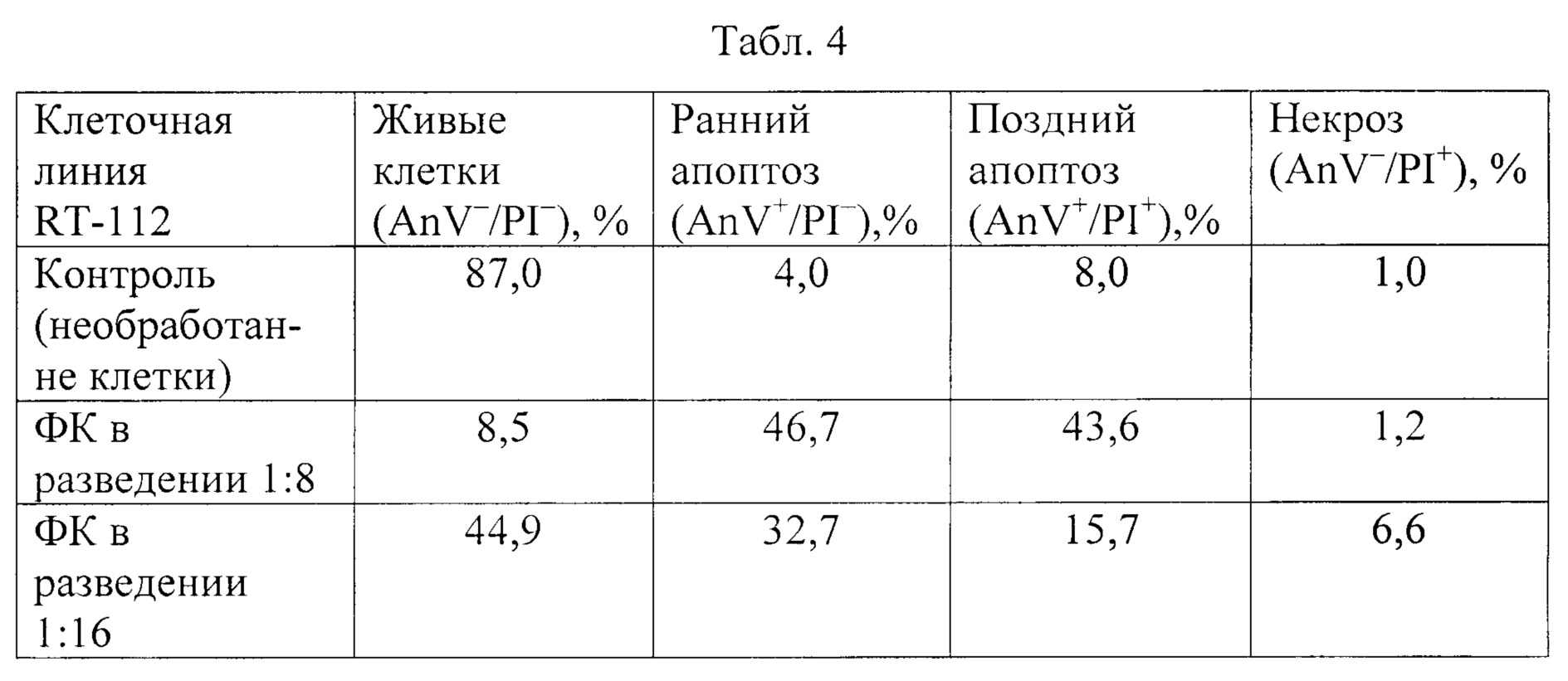
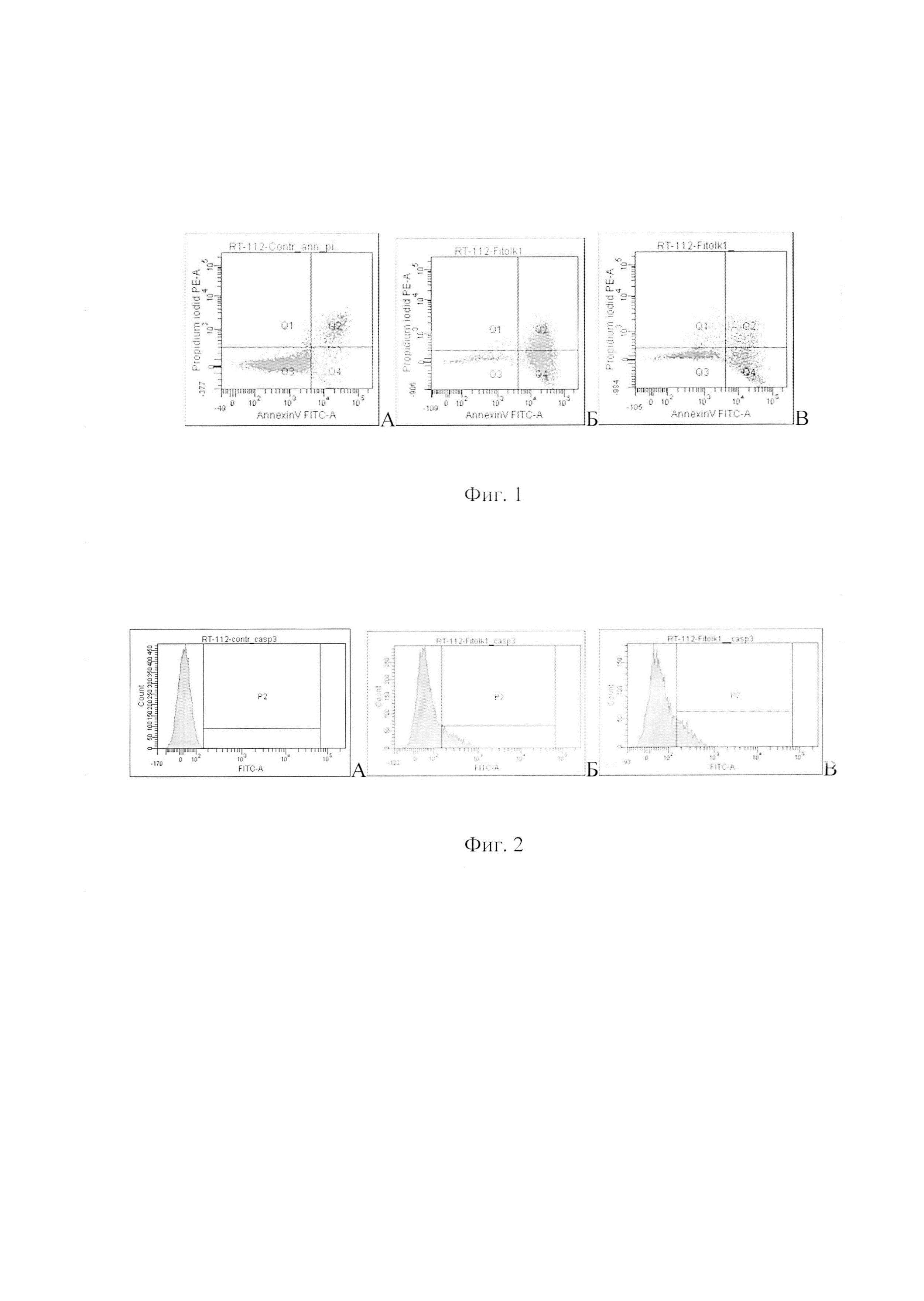
Результаты выявления механизма гибели клеток рака мочевого пузыря линии RT-112 методом двойного окрашивания аннексином V и пропидием йодидом представлены в таблице 4 и на фигуре 1.
В таблице 4 представлены результаты влияния ФК на гибель клеток рака мочевого пузыря RT-112. На фигуре 1 показаны результаты двойного окрашивание клеток рака мочевого пузыря RT-112 аннексином V, меченным FITC, и пропидием йодидом (А - контроль, интактные клетки; Б - клетки, обработанные ФК в разведении 1:8; В - клетки, обработанные ФК в разведении 1:16).
Полученные результаты подтвердили данные МТТ-теста: ФК в разведении 1:8 вызвал гибель более 90% клеток рака мочевого пузыря линии RT-112, а в разведении 1:16-50%.
В таблице 5 представлены результаты влияния ФК на активацию каспазы-3. Фигура 2 иллюстрирует активацию каспазы-3 под действием ФК (А - контроль, интактные клетки; Б - клетки, обработанные ФК в разведении 1:8; В - клетки, обработанные ФК в разведении 1:16. Исследование показало, что ФК активирует эффекторную каспазу-3.
Следовательно, ФК обладает цитотоксичностью в отношении клеток рака мочевого пузыря и вызывает их гибель, вероятно, по механизму апоптоза.
Техническим результатом изобретения является создание фармацевтической композиции природного происхождения, проявляющей цитотоксическое действие в отношении клеток рака мочевого пузыря.
Фармацевтическая композиция, проявляющая цитотоксическое действие в отношении клеток рака мочевого пузыря человека
Фармацевтическая композиция, проявляющая цитотоксическое действие в отношении клеток рака мочевого пузыря человека