Результат интеллектуальной деятельности: Способ выявления мишеней, ассоциированных с определенным диагнозом, в крови пациентов на основе ДНК-аптамеров
Вид РИД
Изобретение
Изобретение относится к области биотехнологии и медицины, а именно к способу выявления в крови больных циркулирующих мишеней, ассоциированных с определенным диагнозом, путем иммобилизации биоспецифического ДНК-аптамера (группы биоспецифических ДНК-аптамеров) на поверхности магнитных частиц, последовательных процедур промывки и инкубации анализируемого образца, промывки и инкубации универсального репортера - конъюгата Са2+-регулируемого фотопротеина обелина с олигонуклеотидом, комплементарным константной концевой последовательности ДНК-аптамера (группы биоспецифических ДНК-аптамеров). Биолюминесцентный сигнал репортера регистрируется при добавлении раствора CaCl2.
Известен микроскопический способ выявления циркулирующих опухолевых клеток (микроэмбол и апоптотических телец) в крови больных раком легкого человека с помощью пары аптамеров, меченных флуоресцентными метками [патент РФ №2571821, МПК G01N 33/18 (2006.01), опубл. 20.12.2015].
Недостатками способа являются низкая производительность и высокая стоимость флуоресцентной микроскопии.
Известен способ биолюминесцентного микроанализа с использованием специфических конъюгатов Са2+-регулируемого фотопротеина обелина и его производных с иммуноглобулинами и олигонуклеотидами [патент РФ №2497128, МПК G01N 33/532 (2006.01), опубл. 17.10.2013].
Недостатком способа является необходимость синтезировать биоспецифические конъюгаты в зависимости от природы выявляемой мишени.
В качестве прототипа взята диагностическая тест-система на основе аптамеров [патент РФ №117150, МПК С12М 1/18 (2006.01), опубл. 06.06.2012], включающая n-луночный планшет, лунки которого покрыты слоем немеченых аптамеров, специфичных к заданной биологической мишени. Выявление мишени в образце проводилось после серии процедур последовательной инкубации исследуемого образца, раствора другого аптамера, меченного флуоресцентным красителем, (репортера) и промывки. Регистрация проводилась с помощью планшетного спектрофлуориметра.
Недостатками системы является использование поверхности пластиковых планшет, обладающих ограниченной поверхностной активностью, низкая чувствительность флуоресцентной метки, а также высокая стоимость планшетного спектрофлуориметра.
Техническим результатом изобретения является разработка более чувствительного, экспрессного и технологичного биолюминесцентного способа выявления мишеней, ассоциированных с определенным диагнозом, в крови пациентов.
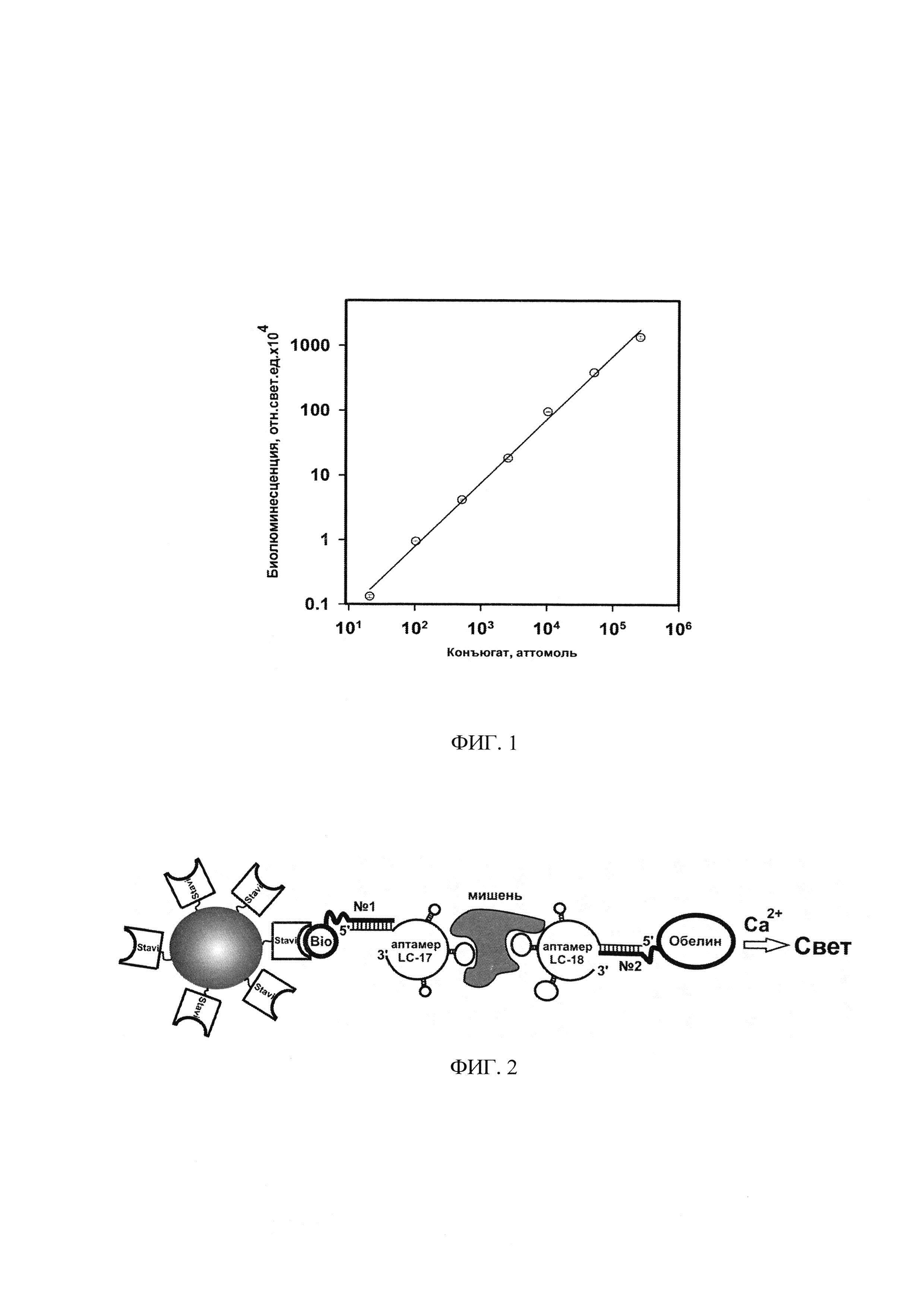
Технический результат достигается тем, что в способе выявления мишеней, ассоциированных с определенным диагнозом, в крови пациентов на основе ДНК-аптамеров, включающем обработку твердой фазы биоспецифическими реагентами, отделение непрореагировавшей жидкой фазы, инкубацию с мишенью, ассоциированной с определенным диагнозом, дальнейшую обработку твердой фазы репортером, разделение жидкой и твердой фаз и анализ твердой фазы, новым является то, что в качестве твердой фазы для анализа используют магнитные микрочастицы с ковалентно иммобилизованными молекулами стрептавидина, обладающие более высокой площадью по сравнению с поверхностью лунок пластиковых планшетов, в качестве биоспецифического реагента для первой обработки твердой фазы используют ДНК-аптамер, связывающийся с поверхностью за счет гибридизации с меченным биотином олигонуклеотидом 5'-CGTGGTTACAGTCAGAGGAG-3'-Bio, комплементарным константному концевому участку аптамера, а в качестве репортера -другой ДНК-аптамер, меченный коньюгатом того же олигонуклеотида с Са2+-регулируемым фотопротеином обелином.
Отличие заявляемого способа от прототипа заключается в том, что в заявляемом изобретении в качестве твердой фазы используют магнитные микрочастицы с ковалентно иммобилизованными молекулами стрептавидина, в качестве биоспецифического реагента для первой обработки твердой фазы используют ДНК-аптамер, связывающийся с поверхностью за счет гибридизации с меченным биотином олигонуклеотидом 5'-CGTGGTTACAGTCAGAGGAG-3'-Bio, комплементарным константному концевому участку аптамера, а в качестве репортера - другой ДНК-аптамер, меченный коньюгатом того же олигонуклеотида с Са2+-регулируемым фотопротеином обелином.
Перечисленные выше отличительные от прототипа признаки позволяют сделать вывод о соответствии заявляемых технических решений критерию «новизна».
Признаки, отличающие заявляемые технические решения от прототипа, не выявлены в других технических решениях и, следовательно, обеспечивают заявляемому решению соответствие критерию «изобретательский уровень»
Заявленный способ диагностики иллюстрируется примерами, описывающими предел обнаружения биолюминесцентной метки для выявления мишеней, ассоциированных с раком легкого, и результаты анализа образцов крови пациентов с диагнозом рак легкого, другими заболеваниями легкого, а также здоровых доноров.
В настоящее время для диагностики рака легкого применяют иммуноферментный анализ ряда белковых онкомаркеров с использованием моноклональных антител. Как правило, эти онкомаркеры могут выявляться при различных типах рака [Sung, H.J., Cho, J.Y. Biomarkers for the lung cancer diagnosis and their advances in proteomics // В MB Reports. - 2008. - V. 41. - №9. - P. 615-625], и потому остается актуальным поиск новых способов специфичной лабораторной диагностики рака легкого. В данном подходе в качестве альтернативы антителам предлагается использовать аптамеры.
Аптамеры - короткие одноцепочечные рибо- либо дезоксирибо-олигонуклеотиды, обладающие определенной пространственной структурой благодаря образованию внутримолекулярных локальных дуплексов и стэкинг-взаимодействий. С помощью технологии SELEX получают высокоспецифичные аптамеры практически к любой мишени. По сравнению с антителами аптамеры как биоспецифические аффинные молекулы имеют ряд определенных преимуществ, главными из которых являются возможность их химического синтеза и модификации, а также стабильность при хранении.
К постоперационной ткани аденокарциномы легкого была получена группа ДНК-аптамеров, характеризующихся высоким связыванием с элементами опухолевой ткани и отрицательным связыванием со здоровой тканью легкого и клетками крови [Zamay, G.S. Aptamers selected to postoperative lung adenocarcinoma detect circulating tumor cells in human blood / O.S. Kolovskaya, T.N. Zamay, Y.E. Glazyrin, A.V. Krat, O. Zubkova, E. Spivak, M. Wehbe, A. Gargaun, D. Muharemagic, M. Komarova, V. Grigorieva, A. Savchenko, A.A. Modestov, M.V. Berezovski, A.S. Zamay // Molecular Therapy. - 2015. - V. 23. - №9. - P. 1486-1496].
Данные аптамеры длинной в 80 нуклеотидных оснований (н.о) имеют константные участки с 5' и 3'- концов (20 н.о) и вариабельную часть (40 н.о), отвечающую за специфическое связывание аптамера со своими мишенями.
Для обеспечения высокой чувствительности анализа в качестве репортера в работе использовали новый, полученный сайт-направленным мутагенезом вариант рекомбинантного Са2+-регулируемого фотопротеина обелина (22,2 кДа) гидроидного полипа Obelia longissima А6С, имеющего цистеиновый остаток на доступном для синтеза NH2-конце молекулы. Это позволило увеличить выход целевого конъюгата до 83% [Krasitskaya V.V. Mutants of Ca2+-regulated photoprotein obelin for site-specific conjugation / V.V. Krasitskaya, L.P. Burakova, A.A. Komarova, E.E. Bashmakova, L.A. Frank // Photochemistry and Photobiology. - 2017. - V. 93. - №2. - P. 553-557]. Биолюминесцентный сигнал этого белка инициируется присоединением Са2+, не зависит от дополнительных субстратов, кислорода и пр. и всегда пропорционален количеству белка.
На основе данного белка был получен конъюгат с олигонуклеотидом, комплементарным 5'-константному участку аптамеров, который может быть использован для выявления всей группы аптамеров, полученных к аденокарциноме легкого. Предел обнаружения конъюгата - около 20 амоль, обеспечивает высокую чувствительность биолюминесцентного анализа с использованием данного конъюгата в качестве метки.
Ранее был описан конъюгат обелина с РНК-аптамером [Vorobjeva М. A. RNA aptamer against autoantibodies associated with multiple sclerosis and bioluminescent detection probe on its basis / M.A. Vorobjeva V.V. Krasitskaya, A.A. Fokina, V.V. Timoshenko, G.A. Nevinsky, A.G. Venyaminova, L.A. Frank // Analytical Chemistry. -2014. - V. 86. - №5. - P. 2590-2594], обладающий специфичностью к единственной мишени - патогенному аутоантителу при рассеянном склерозе. В заявленном способе предлагается использовать конъюгат обелина с олигонуклеотидом, комплементарным константному участку группы аптамеров связанными с одним диагнозом. Например, в работе [Zamay, G.S. Aptamers selected to postoperative lung adenocarcinoma detect circulating tumor cells in human blood / O.S. Kolovskaya, T.N. Zamay, Y.E. Glazyrin, A.V. Krat, O. Zubkova, E. Spivak, M. Wehbe, A. Gargaun, D. Muharemagic, M. Komarova, V. Grigorieva, A. Savchenko, A.A. Modestov, M.V. Berezovski, A.S. Zamay // Molecular Therapy. - 2015. -V. 23. - №9. - P. 1486 - 1496] описано 10 аптамеров, полученных на мишени, ассоциированной с раком легкого, и все они имеют одинаковые концевые участки. Таким образом, предложенный нами способ пригоден для выявления не только одной мишени (при использовании одной пары аптамеров), но и группы мишеней, ассоциированных с данным заболеванием (при использовании смеси аптамеров).
Получение конъюгата фотопротеина обелина с олигонуклеотидом, комплементарным константным участкам на 5' концах ДНК-аптамеров, проводили химическим синтезом с небольшими модификациями способа, разработанного ранее для РНК-аптамера [Vorobjeva М.A. RNA aptamer against autoantibodies associated with multiple sclerosis and bioluminescent detection probe on its basis / M.A. Vorobjeva V.V. Krasitskaya, A.A. Fokina, V.V. Timoshenko, G.A. Nevinsky, A.G. Venyaminova, L.A. Frank // Analytical Chemistry. - 2014. - V. 86. - №5. - P. 2590-2594].
Олигонуклеотид 5'-CGTGGTTACAGTCAGAGGAG-3'-(CH2)6-NH2, комплементарный 5'-константным участкам аптамеров, несущий свободную NH2-группу (10 нмоль), модифицировали 50-кратным молярным избытком сукцинимидного эфира 4-(N-малеимидометил-) циклогексановой кислоты (SMCC) (Thermo Scientific, США) (свежеприготовленный раствор в диметилсульфоксиде) в течение 1,5 часов при комнатной температуре в 0,1 М NaHCO3. Избыток реагентов удаляли с помощью гель-фильтрации на колонке HiTrap Desalting Columns (GE Healthcare, Великобритания), уравновешенной буфером 20 мМ Tris-HCl, рН 7.0, 5 мМ этилендиаминтетрауксусной кислоты (ЭДТА), на хроматографической системе АKТА purifier (GE Healthcare, Великобритания). SMCC-активированный олигонуклеотид инкубировали с 3-х кратным молярным избытком мутантного варианта фотопротеина обелина с заменой Ala6→Cys в течение 12-14 часов при 4°С.
Полученный конъюгат выделяли анион-обменной хроматографией на колонке Mono Q (GE Healthcare, Великобритания), уравновешенной 20 мМ Tris-HCl, рН 7.0, 5 мМ ЭДТА. Элюцию полученного конъюгата проводили линейным градиентом NaCl (0-1 М), выход целевого конъюгата - 71±12%.
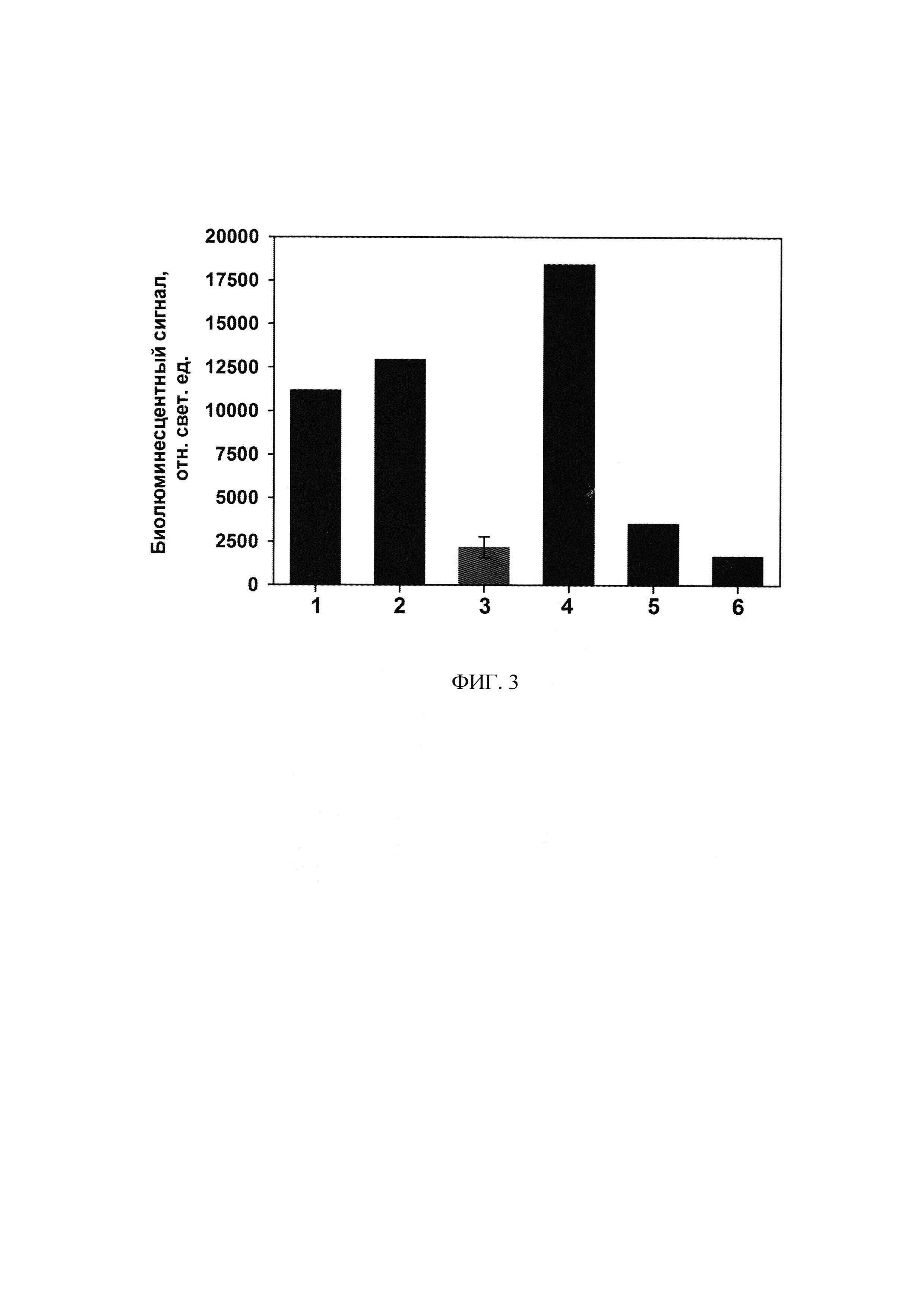
Для определения предела обнаружения конъюгата в лунки планшета вносили раствор конъюгата разной концентрации (по 100 мкл в 20 мМ Tris-HCl, рН 7.0, 5 мМ ЭДТА и 0,1% бычьего сывороточного альбумина) и измеряли биолюминесцентный сигнал сразу после быстрого добавления раствора СаС12 (100 мкл, 0,1 М в 0,1 М Tris-HCl, рН 8.8) с помощью планшетного люминометра LB 940 Multimode Reader Mithras (Berthold, Германия). Сигнал интегрировали 5 с. В контрольную лунку вносили буфер без конъюгата. Все измерения проводили в трех параллелях. Предел обнаружения определяли, как количество конъюгата, при котором отношение сигнала к контролю составляет 3. Предел обнаружения конъюгата составил 20,8 амоль (фиг. 1).
Для осуществления заявляемого способа растворы ДНК-аптамеров перед использованием прогревали при температуре 95°С в течение 5 минут и охлаждали 5 минут на льду. Образцы плазмы крови человека перед исследованием инкубировали с маскирующей дрожжевой РНК (0,1 нг/мкл), встряхивая 30 мин при комнатной температуре.
Полученную плазму инкубировали с магнитными микрочастицами с ковалентно иммобилизованными молекулами стрептавидина (Promega, США) (30 мкг/анализ), эквимолярной смесью ДНК- аптамера и биотинилированным олигонуклеотидом 5'-CGTGGTTACAGTCAGAGGAG-3'-Bio в течение 30 мин при встряхивании, при комнатной температуре (конечная концентрация аптамера и олигонуклеотида 250 нМ).
Частицы промывали трижды, суспендируя в растворе 20 мМ Трис-HCl, рН 7.0, 5 мМ ЭДТА, фиксируя частицы магнитом на стенке пробирки и удаляя надосадочную жидкость. К частицам добавляли раствор аптамера в конечной концентрации 250 нМ, инкубировали и промывали аналогичным образом. Далее к частицам добавляли конъюгат обелина с олигонуклеотидом, комплементарным 5'-константным участкам аптамеров. Инкубировали и промывали.
Суспензию частиц в 60 мкл буфера (20 мМ Tris-HCl, рН 7.0, 5 мМ ЭДТА) переносили в лунки непрозрачного 96-луночного микропланшета (Costar, США) и биолюминесцентный сигнал образовавшихся комплексов на их поверхности измеряли с помощью планшетного люминометра Mithras LB 940 Multimode Reader (Berthold, Германия) сразу после добавления 0,1 М СаСl2, в 0,1 М Tris-HCl рН 7,0 в течение 5 с.
Пример 1.
Образцы плазмы крови человека перед исследованием инкубировали с маскирующей дрожжевой РНК (0,1 нг/мкл) при встряхивании 30 мин.
Перед использованием растворы ДНК-аптамеров LC-17 и LC-18, прогревали при 95°С в течение 5 мин и охлаждали 5 мин на льду.
240 мл полученной плазмы инкубировали с магнитными микрочастицами с ковалентно иммобилизованными молекулами стрептавидина (Promega, США) (30 мкг/анализ), эквимолярной смесью аптамера LC-18 и биотинилированным олигонуклеотидом 5'-CGTGGTTACAGTCAGAGGAG-3'-Bio (конечная концентрация аптамера и олигонуклеотида 250 нМ) в течение 30 мин при встряхивании, при комнатной температуре.
Частицы промывали трижды, суспендируя в растворе 20 мМ Трис-HCl, рН 7.0, 5 мМ ЭДТА, фиксируя частицы магнитом на стенке пробирки и удаляя надосадочную жидкость. К частицам добавляли раствор ДНК-аптамера LC-17 в конечной концентрации 250 нМ, инкубировали и промывали аналогичным образом. Далее к частицам добавляли конъюгат обелина с олигонуклеотидом, который связывался с константной областью ДНК-аптамера LC-17. Инкубировали и промывали.
Суспензию частиц в 60 мкл буфера (20 мМ Tris-HCl, рН 7.0, 5 мМ ЭДТА) переносили в лунки непрозрачного 96-луночного микропланшета (Costar, США) и биолюминесцентный сигнал образовавшихся комплексов на их поверхности измеряли с помощью планшетного люминометра Mithras LB 940 Multimode Reader (Berthold, Германия) сразу после добавления 0,1 М СаСl2, в 0,1 М Tris-HCl рН 7,0 в течение 5 с.
Пример 2.
Образцы плазмы крови человека перед исследованием инкубировали с маскирующей дрожжевой РНК (0,1 нг/мкл) при встряхивании 30 мин.
Перед использованием раствор ДНК-аптамера LC-17 и LC-18 прогревали при 95°С в течение 5 мин и охлаждали 5 мин на льду.
240 мл полученной плазмы инкубировали с магнитными микрочастицами с ковалентно иммобилизованными молекулами стрептавидина (Promega, США) (30 мкг/анализ), эквимолярной смесью ДНК-аптамера LC-17 и биотинилированным олигонуклеотидом 5'-CGTGGTTACAGTCAGAGGAG-3'-Bio (конечная концентрация аптамера и олигонуклеотида 250 нМ) в течение 30 мин при встряхивании, при комнатной температуре.
Частицы промывали трижды, суспендируя в растворе 20 мМ Трис-HCl, рН 7.0, 5 мМ ЭДТА, фиксируя частицы магнитом на стенке пробирки и удаляя надосадочную жидкость. К частицам добавляли раствор ДНК-аптамера LC-18 в конечной концентрации 250 нМ, инкубировали и промывали аналогичным образом. Далее к частицам добавляли конъюгат обелина с олигонуклеотидом, который связывался с константной областью аптамера LC-18. Инкубировали и промывали.
Суспензию частиц в 60 мкл буфера (20 мМ Tris-HCl, рН 7.0, 5 мМ ЭДТА) переносили в лунки непрозрачного 96-луночного микропланшета (Costar, США) и биолюминесцентный сигнал образовавшихся комплексов на их поверхности измеряли с помощью планшетного люминометра Mithras LB 940 Multimode Reader (Berthold, Германия) сразу после добавления 0,1 М CaCl2, в 0,1 М Tris-HCl рН 7,0 в течение 5 с. Схема проведения анализа приведена на фигуре 2.
Представленные исследования выполнены в соответствии с документами, регламентирующими этические нормы проведения исследований с использованием биологического материала человеческого происхождения (решение Локального этического комитета КККОД №8/2011 от 16.03.2011).
Венозная кровь пациентов, перенесших полную резекцию опухоли, отобрана до операций и предоставлена сотрудниками КГБУЗ «Красноярский краевой клинический онкологический диспансер им. А.И. Крыжановского». Образцы плазмы крови 56 пациентов взяты перед проведением операции по удалению образований в легких. Диагнозы пациентов были верифицированы морфологически. В эксперименте использовали образцы пациентов без диагноза рак легкого (здоровые доноры), а также с другими заболеваниями легких и видами рака.
Сигналы, полученные от образцов крови здоровых доноров, достоверно отличались от сигналов остальных пациентов (р<0,05).
Результаты проведенных исследований образцов плазмы крови по примеру 1 представлены на фигуре 3, где 1, 2, 3 - среднее значение сигнала в группе с железистоклеточным (n=22), плоскоклеточным (n=23) раком легкого и в контрольной группе ± SD (n=19), соответственно, 4 - метастазы в легкое (n=3); 5 - туберкулез (n=2); 6 - хондрогамартома (n=1); отн.свет.ед. - относительные световые единицы.
Преимущества заявляемого способа заключаются в том, что в качестве твердой фазы используются магнитные частицы с ковалентно иммобилизованными молекулами стрептавидина, обладающие более высокой площадью поверхности по сравнению с поверхностью лунок пластиковых планшетов, и в использовании высокочувствительного биолюминесцентного репортера - конъюгата Са2+-регулируемого фотопротеина обелина с олигонуклеотидом, позволяющего выявлять одновременно несколько мишеней, связанных с диагностикой данного заболевания, при использовании группы ДНК-аптамеров со специфичностью к разным мишеням, но одинаковой константой концевой областью.
Способ выявления мишеней, ассоциированных с определенным диагнозом, в крови пациентов на основе ДНК-аптамеров, включающий обработку твердой фазы биоспецифическими реагентами, отделение непрореагировавшей жидкой фазы, инкубацию с мишенью, ассоциированной с определенным диагнозом, дальнейшую обработку твердой фазы репортером, разделение жидкой и твердой фаз и анализ твердой фазы, отличающийся тем, что в качестве твердой фазы используют магнитные микрочастицы с ковалентно иммобилизованными молекулами стрептавидина, в качестве биоспецифического реагента для первой обработки твердой фазы используют ДНК-аптамер, связывающийся с поверхностью за счет гибридизации с меченным биотином олигонуклеотидом 5'-CGTGGTTACAGTCAGAGGAG-3'-Bio, комплементарным константному концевому участку ДНК-аптамера, а в качестве репортера - другой ДНК-аптамер, меченный конъюгатом того же олигонуклеотида с Са-регулируемым фотопротеином обелином.