Результат интеллектуальной деятельности: Способ оценки характера аутоиммунной реакции организма человека на множественно модифицированные липопротеины низкой плотности в литическом тесте
Вид РИД
Изобретение
Изобретение относится к клинической иммунологии и может быть использовано для оценки литической активности иммунных комплексов, содержащих множественно-модифицированные липопротеины низкой плотности (ИК-ммЛНП), для прогноза течения заболеваний, связанных с повышенным уровнем ммЛНП (атеросклероз, гестоз, сахарный диабет, и.т.д.), так и для разработки препаратов, уменьшающих патогенность ммЛНП и иммунных комплексов, содержащих ммЛНП.
Атеросклероз является сложным, периодически обостряющимся хроническим воспалительным процессом повреждения сосудов, развивающимся на фоне нарушений холестеринового обмена, который приводит к структурной модификации сосудистого эндотелия и разрастанию соединительной ткани, обуславливая формирование атеросклеротической бляшки. Атеросклероз и его осложнения - ишемическая болезнь сердца, инсульт, поражение сосудов нижних конечностей продолжают оставаться наиболее частой причиной инвалидизации и смертности населения в экономически развитых странах Европы, США и особенно России [European Guidelines on Cardiovascular Disease // Eur. Heart J. - 2003. - V. 24 №17. - P. 1601-1610; NCEP. Adult Treatment Panel III Guidelines // Circulation. - 2004. - V. 110. - P. 227-239; ВНОК Российские рекомендации. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. М. - 2004. - 36 с.].
Заболевание начинается с накопления липопротеинов, в первую очередь, липопротеинов низкой плотности (ЛНП), во внеклеточном матриксе сосудов. Данные частицы ЛНП агрегируют и подвергаются модификации в результате окисления. Модифицированные окислением ЛНП (моЛНП) являются токсичными и повреждают сосуды, вызывая воспаление и фиброз [Steinberg D. The LDL modification hypothesis of atherogenesis: an update // J. Lipid Res. - 2009. - V. 50. - P. S376-S381]. Параллельно с окислением ЛНП обретают иммуногенные свойства и в организме синтезируются аутоантитела к моЛНП и образуются иммунные комплексы, содержащие моЛНП. Аутоантитела, образующиеся против неоэпитопов моЛНП, определяются в крови и титр этих антител коррелирует с тяжестью атеросклероза, и рассматривается в качестве маркера заболевания [Itabe Н., Mori М., Higashi Y., and Takano Т. Minimally modified LDL is an oxidized LDL enriched with oxidized phosphatidylcholines //J Biochem. - 2003. - V. 134. - P. 459-465; Tsimikas S. Oxidative biomarkers in the diagnosis and prognosis of cardiovascular disease //Am J Cardiol. - 2006. - V. 98. - P. 9Р-17Р].
В качестве прототипа использован способ определения литической активности множественно модифицированных липопротеинов низкой плотности (ммЛНП) [Патент РФ №2577719 от 20.03.2016 г. ]. Суть способа заключается в том, что предварительно из сыворотки крови человека выделяют ммЛНП путем обработки раствором 20% поливинилпирролидона с молекулярной массой 35000 (ПВП-35000), инкубируют, образовавшиеся агрегаты ммЛНП осаждают центрифугированием, декантируют, осадок ммЛНП растворяют в буфере без ПВП-35000, добавляют отмытые стандартизованные эритроциты барана, инкубируют в течение 48 часов при комнатной температуре, измеряют фотометрически оптическую плотность проб при длине волны 620 нм, по калибровочному графику определяют степень лизиса и при лизисе более 10% констатируют повышенную литическую активность ммЛНП.
Техническим результатом предлагаемого способа является расширение арсенала лабораторных тестов для оценки литической активности ИК-ммЛНП путем сравнения величин коэффициентов удельной литической активности ммЛНП и иммунных комплексов, содержащих ммЛНП (ИК-ммЛНП) для раннего прогноза течения и контроля эффективности патогенетической терапии атеросклероза в условиях клинико-диагностических лабораторий.
Этот результат достигается тем, что специфическую преципитацию ИК-ммЛНП, из сыворотки крови человека проводят путем инкубации супернатанта, полученного после предварительного осаждения множественно модифицированных липопротеинов низкой плотности (ммЛНП) буфером, содержащим 20% поливинилпирролидона (ПВП) с молекулярной массой 35000 (ПВП-35000), в течение 30 минут при 4°С, затем образовавшиеся агрегаты (ИК-ммЛНП) осаждают центрифугированием при 4°С в течение 10 мин при 3100g, тщательно декантируют, полученный преципитат растворяют в буфере без ПВП-35000 и определяют содержание холестерина, с использованием коммерческих ферментативных наборов. К пробам ммЛНП и ИК-ммЛНП добавляют стандартизованные эритроциты барана, инкубируют в течение 24 часов при 37°С, рассчитывают коэффициент удельной литической активности (КУЛА) ммЛНП и ИК-ммЛНП как отношение степени лизиса к холестерину в этих комплексах, сопоставляют величину КУЛА ммЛНП и ИК-ммЛНП у обследуемого человека, в случае снижения данного коэффициента ИК-ммЛНП по сравнению с КУЛА ммЛНП - оценивается как нейтрализация литической активности, при противоположном эффекте, при тенденции к увеличению данного коэффициента ИК-ммЛНП - оценивается как возрастание литической активности, равные величины КУЛА (ммЛНП) и КУЛА (ИК-ммЛНП) свидетельствуют о том, что аутоантитела, связываясь с ммЛНП в иммунных комплексах не влияют на литическую активность.
Способ осуществляют следующим образом: проводят забор крови натощак из локтевой вены человека, готовят сыворотку крови. Приготовление ммЛНП и ИК-ммЛНП, описано в работе [Патент №2632118 от 02.10.2017 г]. Кратко: к 100 мкл сыворотки крови добавляют 84 мкл буфера, содержащего 20% ПВП-35000 (конечная концентрация ПВП-35000 в пробе составляет 9,1%), тщательно перемешивают и инкубируют при комнатной температуре в течение 10 мин. Агрегированные ммЛНП осаждают центрифугированием, тщательно отбирают супернатант и инкубируют его в течение 30 мин при 4°С. Образовавшиеся агрегаты иммунных комплексов, содержащих ИК-ммЛНП, осаждают центрифугированием при 4°С при 3100g в течение 10 мин, тщательно декантируют и преципитат растворяют в буфере без ПВП-35000. К 10 мкл препаратов ммЛНП и ИК-ммЛНП, приготовленных из сыворотки крови индивидуумов, добавляют 50 мкл стандартизованные эритроциты барана (1,5×108 кл/мл), общий объем доводят до 100 мкл буфером VBS2+, инкубируют в течение 24 часов при 37°С, измеряют оптическую плотность на фотометре при длине волны 620 нм и по калибровочному графику определяют степень лизиса. Рассчитывают коэффициент удельной литической активности (КУЛА) ммЛНП и ИК-ммЛНП как отношение степени лизиса к холестерину в этих комплексах, сопоставляют величину КУЛА ммЛНП и ИК-ммЛНП у обследуемого человека, в случае снижения данного коэффициента ИК-ммЛНП по сравнению с КУЛА ммЛНП - оценивается как нейтрализация литической активности, при противоположном эффекте, при тенденции к увеличению данного коэффициента ИК-ммЛНП - оценивается как возрастание литической активности, равные величины КУЛА (ммЛНП) и КУЛА (ИК-ммЛНП) свидетельствуют о том, что аутоантитела, связываясь с ммЛНП в иммунных комплексах не влияют на литическую активность.
Для выделения иммунных комплексов, содержащих ммЛНП используют:
- Буфер-1 для преципитации множественно модифицированных липопротеинов низкой плотности, который содержит 20% ПВП-35000 в 0,01 М трис-HCl-буфере, рН 7,4, содержащем 0,15 М NaCl;
- Буфер-2 для растворения преципитата иммунных комплексов, который представляет собой 0,01М Трис-HCl-буфер, рН 7,4, содержащий 0,15 M NaCl.
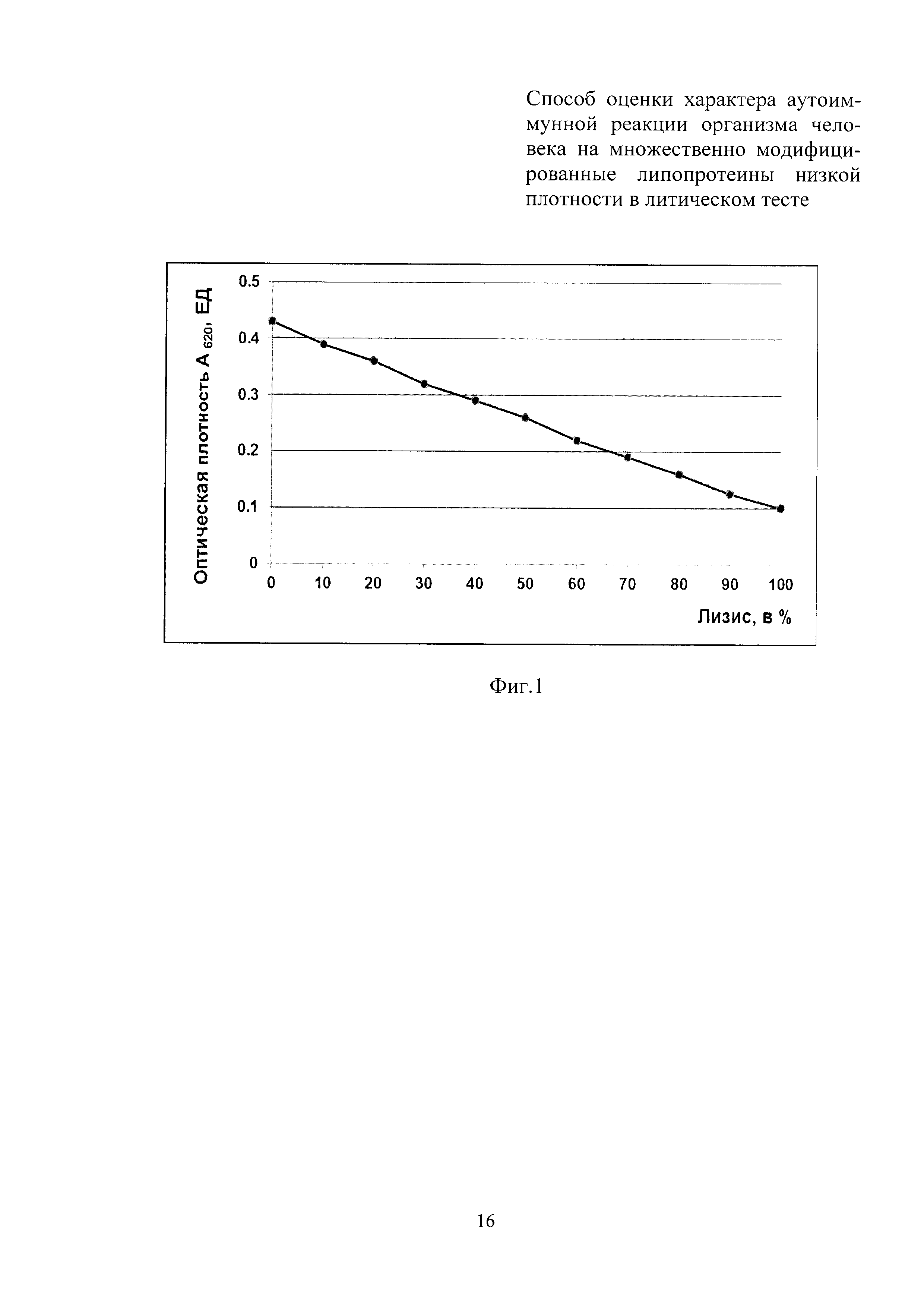
Изобретение поясняется фигурой 1 на которой представлен калибровочный график для определения степени лизиса эритроцитов барана по оптической плотности при длине волны 620 нм.
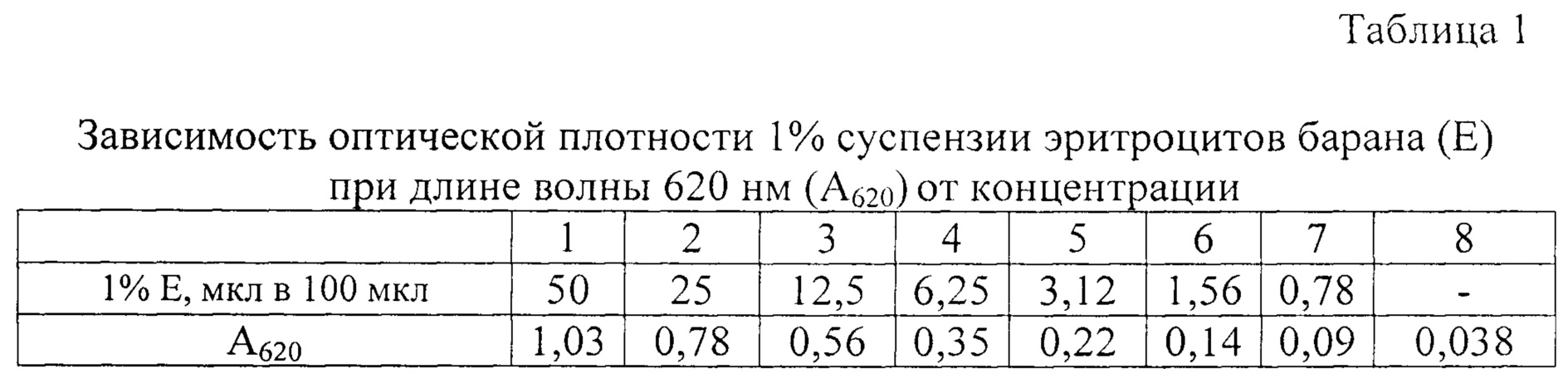
Определение оптимальной концентрации эритроцитов барана для теста определения литической активности ИК-ммЛНП. Эритроциты барана (Е) 3 раза отмывают в вероналовом солевом буфере (VBS2+) центрифугированием в течение 10 мин при 2500 об/мин. Строят график зависимости оптической плотности суспензии эритроцитов (при длине волны 620 нм) от концентрации эритроцитов. Для этого 1% суспензию эритроцитов прогрессивно разводят в плоскодонной 96-ти луночной иммунологической планшете в объеме 100 мкл 0,15М NaCl. Тщательно перемешивают и измеряют на фотометре для иммуноферментного анализа при длине волны 620 нм. Результаты представлены в таблице 1.
Как видно из данных, представленных в таблице 1, наблюдается линейная зависимость оптической плотности суспензии эритроцитов от концентрации в растворе до А620 равной 0,56 ЕД. Свыше 0,56 ЕД при А620 данная зависимость - нелинейная. Поэтому для теста определения литической активности ИК-ммЛНП нами выбрана концентрация суспензии Е, которая в объеме 100 мкл в лунке 96-луночного планшета дает оптическую плотность, равную 0,40-0,56 ЕД (1,5×108 кл/мл). Для определения степени лизиса эритроцитов нами предложен калибровочный график, в котором степень лизиса эритроцитов оценивают по снижению оптической плотности при длине волны 620 нм. За 0% лизиса принимают оптическую плотность контроля эритроцитов на спонтанный лизис (50 мкл Е + 50 мкл VBS2+), соответственно за 100% лизис принимают оптическую плотность контроля на полный лизис (50 мкл Е + 50 мкл H2O). Степень лизиса эритроцитов оценивают после 24-ти часовой инкубации при 37°С по калибровочному графику, представленному на фиг. 1.
Как видно из фиг. 1, калибровочный график позволяет определять степень лизиса эритроцитов в процентах по оптической плотности пробы без стадии центрифугирования и измерения гемоглобина в супернатанте и последующего расчета степени лизиса эритроцитов, что существенно упрощает регистрацию результатов анализа литической активности ИК-ммЛНП в рутинных исследованиях.
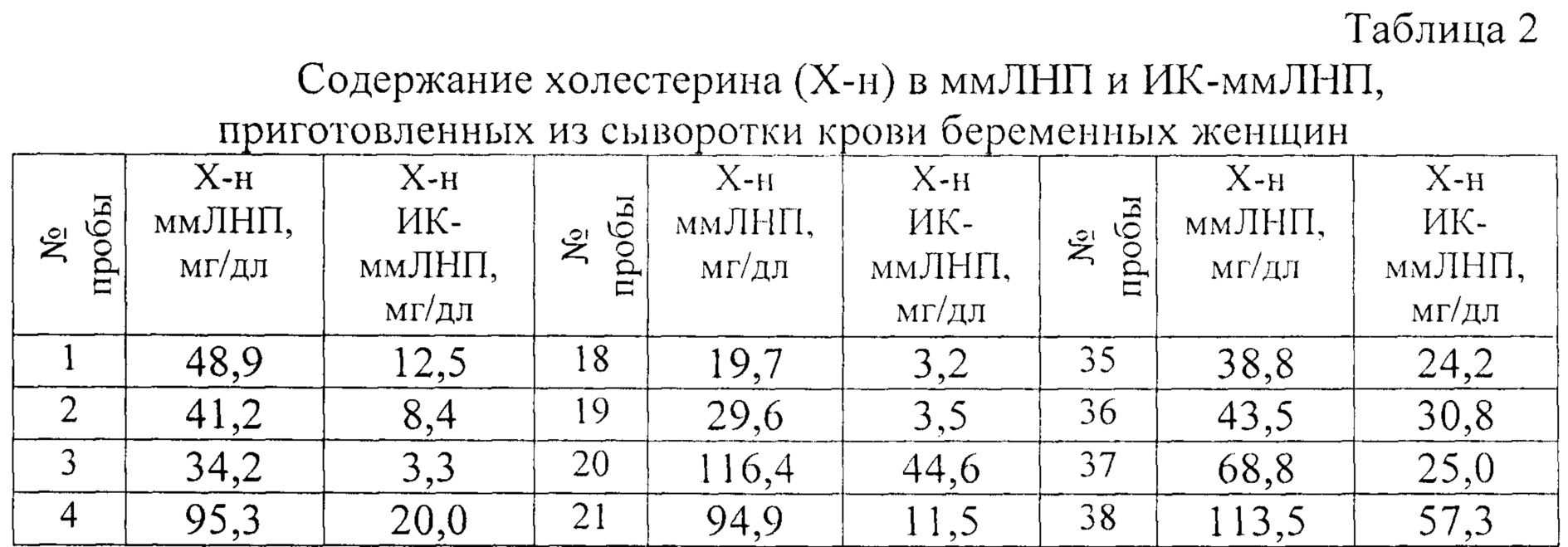
Выделение иммунных комплексов, содержащих множественно модифицированные липопротеинов низкой плотности. ИК-ммЛНП выделяли, как описано в работе [Патент №2632118 от 02.10.2017 г, бюлл. №28]. На первом этапе из индивидуальных сывороток крови выделяют ммЛНП путем добавления к 100 мкл сыворотки 84 мкл буфера, содержащего 20% ПВП (конечная концентрация ПВП-35000 составляет 9,1%), и инкубации в течение 10 мин при комнатной температуре. Агрегированные в этих условиях ммЛНП осаждают центрифугированием при 3100g в течение 10 мин при 23°С, тщательно отбирают супернатант, преципитат ммЛНП растворяют в 100 мкл Буфера-2. Далее супернатант, приготовленный как описано выше, инкубируют при 4°С в течение 30 минут. Агрегированные иммунные комплексы осаждают путем центрифугирования при 3100g в течение 10 мин при 4°С. реципитат ИК-ммЛНП тщательно декантируют и полученный осадок ресуспендируют в исходном объеме, в 100 мкл буфера-2. После растворения осадков в полученных фракциях ммЛНП и ИК-ммЛНП определяют содержание холестерина с использованием коммерческих ферментных наборов. Полученные результаты представлены в таблице 2.
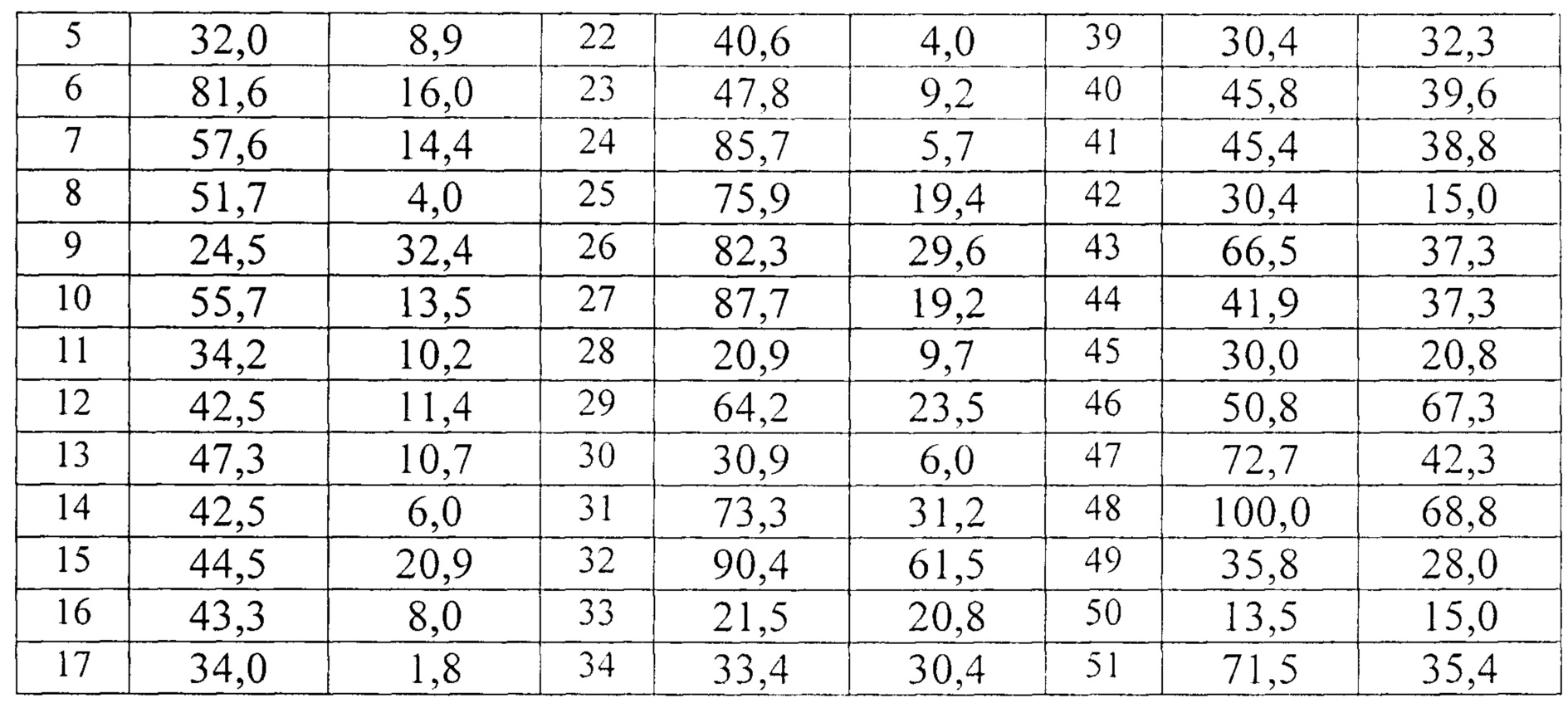
Как видно из данных, представленных в таблице 2, содержание холестерина в ммЛНП в среднем составил 53,4 мг/дл (колебания от 13,5 мг/дл до 116,4 мг/дл). Содержание холестерина в ИК-ммЛНП в среднем составил 22,6 мг/дл (колебания от 1,8 мг/дл до 68,8 мг/дл). Причем в 15 пробах ИК-ммЛНП уровень холестерина был менее 10 мг/дл.
Таким образом, во всех пробах содержание холестерина в ммЛНП было повышенным, в то время как холестерин в ИК-ммЛНП в 29% тестированных проб был менее 10 мг/дл.
Пример 1. Определение литической активности ммЛНП и ИК-ммЛНП, приготовленных из сыворотки крови беременных женщин.
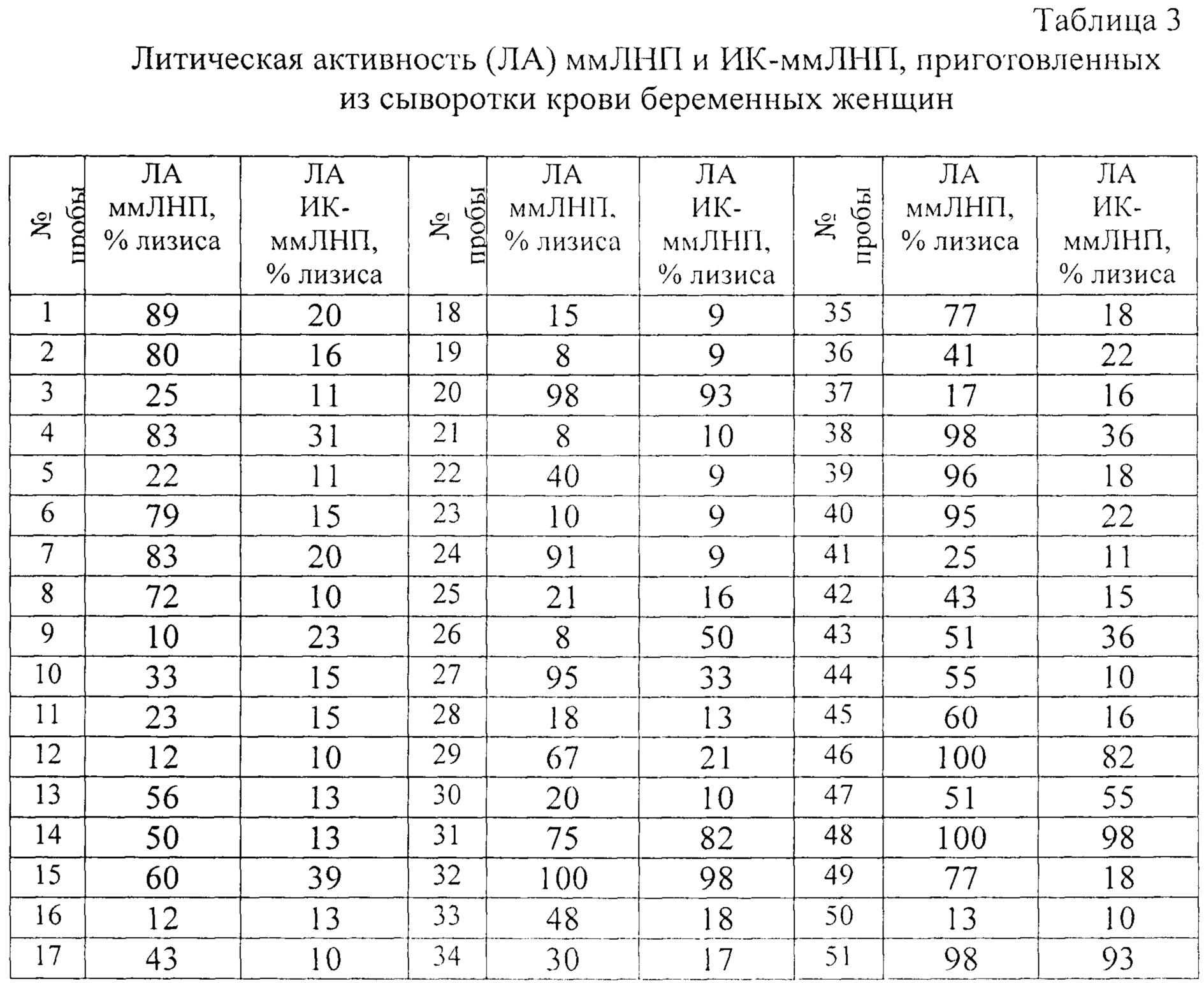
Литическую активность ИК-ммЛНП определяли аналогично определению литической активности ммЛНП как описано в патенте РФ №2577719 от 20.03.2016 г. Литический тест проводят в 96-луночных плоскодонных иммунологических планшетах. Вначале вносят в лунки по 10 мкл ммЛНП или ИК-ммЛНП, затем добавляют 40 мкл буфера VBS2+ и 50 мкл суспензии стандартизованных (1,5×108 кл/мл) эритроцитов барана. Параллельно ставят контроли: на полный лизис (50 мкл суспензии эритроцитов барана +50 мкл H2O); на спонтанный лизис (50 мкл эритроцитов барана +50 мкл буфера VBS2+). Планшету заклеивают пленкой и оставляют на 24 часа при 37°С. После инкубации планшету тщательно перемешивают и измеряют оптическую плотность проб на фотометре для иммуноферментного анализа при длине волны 620 нм и по калибровочному графику определяют степень лизиса. Полученные результаты представлены в таблице 3.
Как видно из данных, представленных в таблице 3, по литической активности исследованные пробы мм ЛНП распределяются на три группы:
1 группа с низкой литической активностью (% лизиса менее 11%), всего 5 проб;
2 группа - со средней литической активностью (% лизиса от 12% до 50%), всего 20 проб;
3 группа - с высокой литической активностью (% лизиса более 51%), всего 26 проб.
Таким же образом по величине литической активности пробы ИК-ммЛНП также распределяются на три группы:
1 группа с низкой литической активностью (менее 11%). Всего 15 проб;
2 группа - со средней литической активностью (%>лизиса от 12% до 50%). Всего 30 проб;
3 группа - с высокой литической активностью (лизис более 51%). Всего 6 проб.
Таким образом, данное условное распределение по группам было бы корректным при равном количестве холестерина в ммЛНП и ИК-ммЛНП. С другой стороны, тест определения литической активности данных физиологических макромолекулярных комплексов является функциональным и поэтому требуется стандартизация литической активности с учетом содержания холестерина в данных комплексах через расчетный коэффициент, коэфициент удельной литической активности (КУЛА).
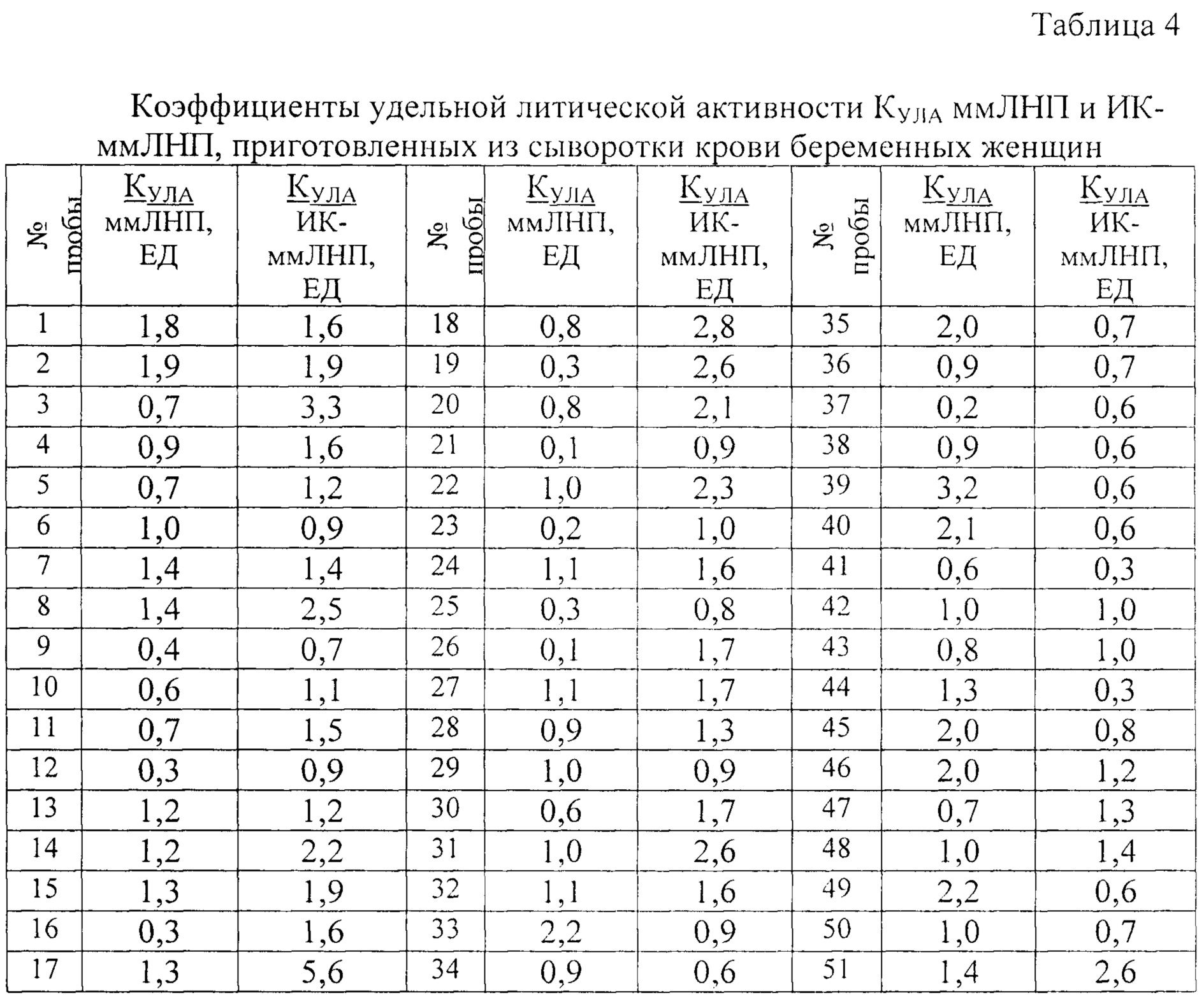
Расчет коэффициента удельной литической активности (КУЛА) ммЛНП и ИК-ммЛНП, Для комплексной оценки литической активности ммЛНП и ИК-ммЛНП предложен коэффициент удельной литической активности, который представляет собой отношение степени лизиса эритроцитов к холестерину в индивидуальных пробах ммЛНП и ИК-ммЛНП, приготовленных из сыворотки крови одного и того же человека. Полученные значения КУЛА представлены в таблице 4.
Как видно из данных, представленных в таблице 4, по величине коэффициентов удельной литической активности (КУЛА) пробы ммЛНП условно делятся на три группы:
1 группа - 24 пробы с низким КУЛА (менее 1,0 ЕД);
2 группа - 23 пробы со средним значением КУЛА (от 1,0 ЕД до 2,0 ЕД);
3 группа - 4 пробы с высоким КУЛА (более 2 ЕД).
Аналогично, пробы ИК-ммЛНП по величине КУЛА также делятся на три группы:
1 группа - 19 пробы с низким КУЛА (менее 1 ЕД);
2 группа - 22 пробы со средним значением КУЛА (от 1,0 ЕД до 2,0 ЕД);
3 группа - 10 проб с КУЛА (более 2,0 ЕД).
Анализ величины коэффициентов в парах ммЛНП и ИК-ммЛНП свидетельствует о разнонаправленных сдвигах, т.е. в одних пробах наблюдается возрастание КУЛА, в других, наоборот, снижение данного коэффициента. В третьей группе КУЛА остается постоянным.
Таким образом, для оценки литической активности иммунных комплексов, содержащих ммЛНП, в предлагаемом тесте проводится анализ в парных пробах величины КУЛА (ммЛНП и ИК-ммЛНП). Результаты парного анализа свидетельствуют:
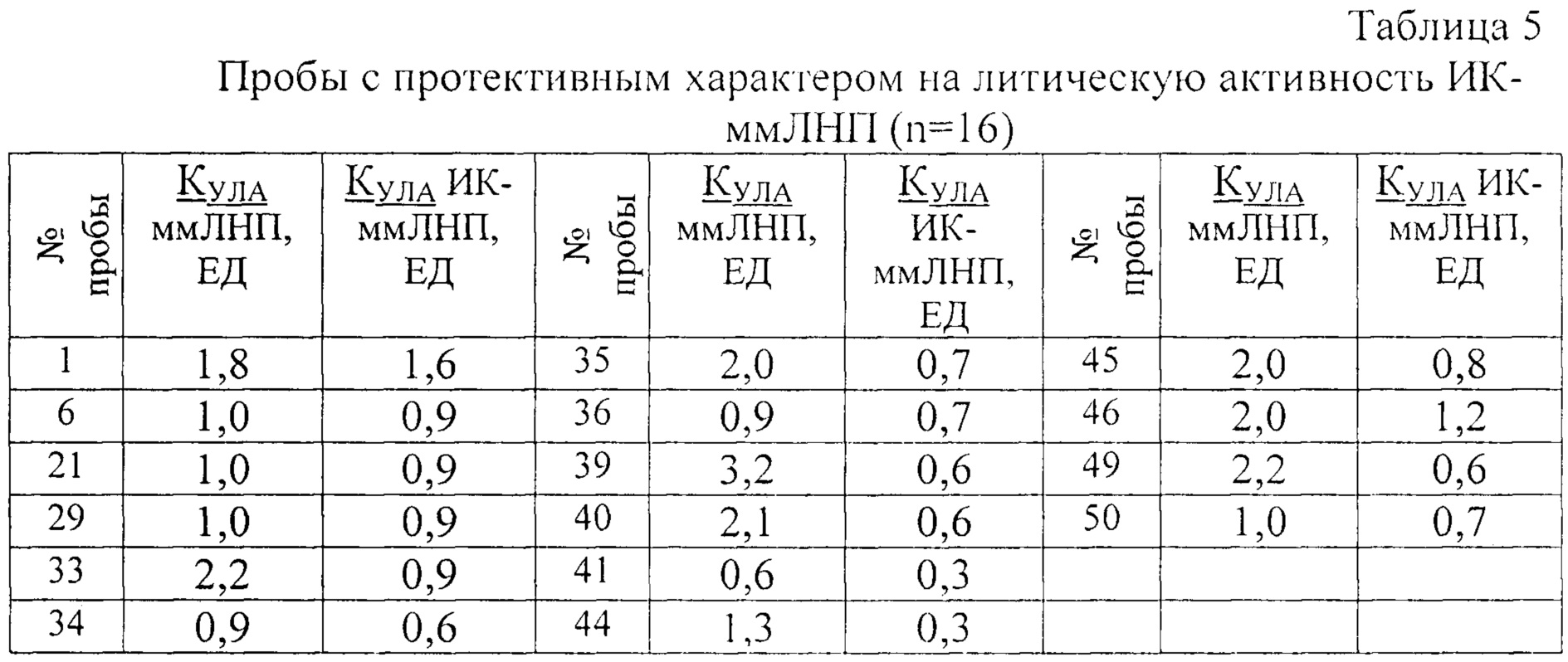
1. В случае снижения величины КУЛА ИК-ммЛНП по сравнению с КУЛА ммЛНП в парных пробах характер аутоиммунной реакции организма на ммЛНП оценивается как протективный (благоприятный). Эффект нейтрализации литической активности при взаимодействии аутоантител с ммЛНП, возможно, связан либо с нейтрализацией липопротеин-ассоциированной фосфолипаза А2, либо нейтрализацией лизофосфатидилхолина в молекуле ммЛНП в иммунных комплексах, либо связывание аутоантител с ммЛНП вызывает конформационные изменения в молекуле липопротеина, приводя к снижению патогенности в литическом тесте (см. таблицу 5);
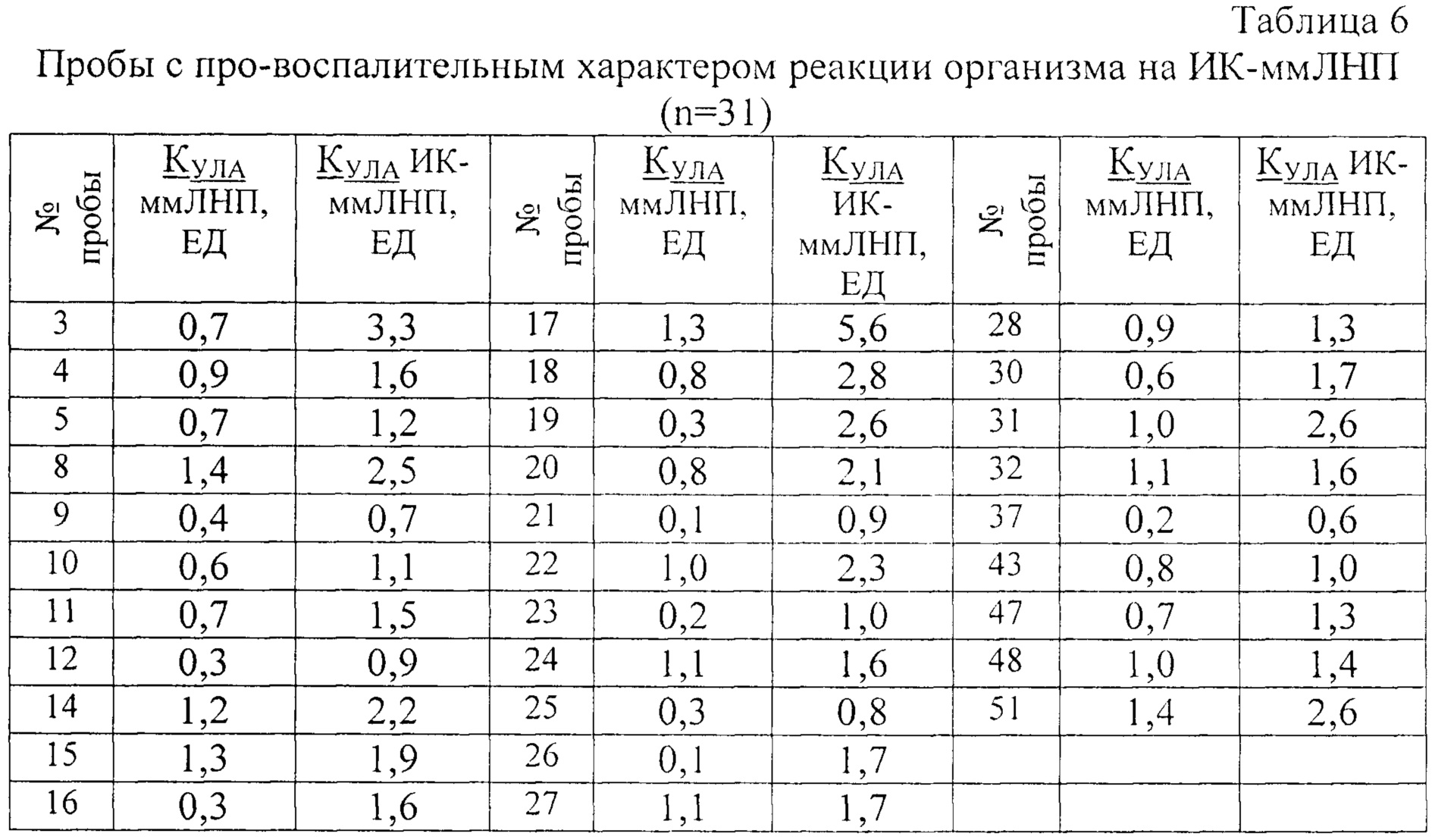
2. В случае возрастания величины КУЛА в парных пробах ммЛНП и ИК-ммЛНП характер аутоиммунной реакции организма на ммЛНП оценивается как про-воспалительный (патогенный) ответ на ммЛНП. Возможно, возрастание патогенности (литической активности) ммЛНП в составе иммунных комплексов связано с конформационными изменениями в молекуле липопротеина. Данный факт является абсолютно новым эффектом для иммунных реакций, (см. таблицу 6);
3. В случае равных значений величины КУЛА в парах ммЛНП и ИК-ммЛНП, с одной стороны, имеет значение величина данного коэффициента для оценки патогенности, с другой стороны, данный факт свидетельствует о том, что аутоантитела, связываясь с ммЛНП в иммунных комплексах не влияют на литическую активность данных комплексов. При данной ситуации патогенный эффект ммЛНП и ИК-ммЛНП зависит только от концентрации их в крови обследуемого индивидуума (таблица 7).
Таким образом, способ оценки литической активности ИК-ммЛНП в организме человека позволяет проводить диагностику течения атеросклеротического процесса, расширяет возможности для коррекции проводимой терапии под контролем коэффициента удельной литической активности ммЛНП и ИК-ммЛНП, открывает новый подход к оценке атерогенности ммЛНП и ИК-ммЛНП «от количественных» показателей к «качественным» (функциональным) показателям. То есть, при нормальном уровне ммЛНП и ИК-ммЛНП патологический процесс, обусловленный данными комплексами может протекать с разной скоростью, в зависимости от коэффициента удельной литической активности, т.е. от патогенности данных комплексов.
Предлагаемый способ прост в выполнении, не требует дорогостоящих реактивов и оборудования. Для регистрации лизиса эритроцитов не требуется стадия центрифугирования Использование простого и информативного способа оценки характера аутоиммунной реакции организма на естественный метаболит, ИК-ммЛНП, позволяет проводить скрининг и выявлять людей с острым течением патологического, в частности, атеросклеротического процесса, как на доклинических стадиях заболевания, так и при клиническом атеросклерозе.