Результат интеллектуальной деятельности: СПОСОБ ВИТРИФИКАЦИИ ОВАРИАЛЬНОЙ ТКАНИ
Вид РИД
Изобретение
Способ относится к криобиологии и медицине, в частности к онкогинекологии и репродуктивной медицине. Он может быть использован для сохранения репродуктивной функции женщин с онкологическими заболеваниями, желающих в дальнейшем иметь детей.
Современный уровень развития вспомогательных репродуктивных технологий дает возможность применять их и для пациенток с онкологическими заболеваниями. Под действием химиотерапевтических агентов клетки яичника деградируют по пути апоптоза. Этот процесс затрагивает как строму яичника, так и собственно фолликулярную систему, что приводит к уменьшению численности фолликулов, в том числе и примордиальных, а, следовательно, ведет к снижению овариального резерва, преждевременной менопаузе и, в конечном итоге, к бесплодию [David А., Van Langendonckt A., Gilliaux S., Dolmans M.M., Donnez J., Amorim C.A. Effect of cryopreservation and transplantation on the expression of kit ligand and anti-Mullerian hormone in human ovarian tissue // Hum. Reprod. 2012. Vol. 27, N 4. P. 1088-1095]. Общество клинических онкологов США (ASCO) представило рекомендации по криоконсервации яичниковой ткани как один из возможных путей сохранения фертильности у онкологических больных [American Society for Reproductive Medicine. Ovarian tissue cryopreservation: a committee opinion // Fertility and Sterility. 2014. V. 101, P. 1237-1243].
На сегодняшний день для криоконсервации овариальной ткани применяются два принципиально различающихся подхода: методом витрификации и методом медленного программируемого замораживания. Обычно при медленном замораживании используются специальные программируемые устройства, позволяющие снижать температуру постепенно с последующим хранением в жидком азоте (-196°С).
В ходе процедуры витрификации образцы ткани, так же как и при медленном замораживании помещают в раствор криопротекторов. Но при использовании этого метода охлаждение образца происходит очень быстро, со скоростью, часто превышающей 17000°С/мин. Сверх быстрое снижение температуры позволяет избежать образования кристаллов льда в клетках, которые пагубно влияют на жизнеспособность ткани.
В настоящее время после аутотрансплантации криоконсервированной яичниковой ткани родилось более 100 детей во всем мире [Andersen C.Y., Bollerup А.С., Kristensen S.G. Defining quality assurance and quality control measures in connection with ovarian tissue cryopreservation and transplantation: a call to action // Human Reproduction. 2018].
Применяя метод витрификации в мире зарегистрировано рождение 3-х детей [Kiseleva M.V., Malinova I.V., Komarova E.V., Shvedova T.I., Denisov M.S., Kaprin A.D. Vitrification and transplantation of ovarian tissue as a way to preserve and restore fertility in cancer patients / The 4th World Congress of International Society for Fertility Preservation. 2015. Nov 13-15. Shanghai, China; Zhai J, Yao G, Dong F, Bu Z, Cheng Y, Sato Y, Hu L, Zhang Y, Wang J, Dai S, Li J, Sun J, Hsueh AJ, Kawamura K, Sun Y.J. In Vitro Activation of Follicles and Fresh Tissue Auto-transplantation in Primary Ovarian Insufficiency Patients // Clin Endocrinol Metab. 2016. Vol. 101, N 11. P. 4405-4412].
Важную роль в процессе криоконсервации ткани играют криопротекторы. Для защиты клеток в процессах замораживания и размораживания в среду для замораживания добавляют специальные соединения, такие как диметилсульфоксид (ДМСО), трегалоза, глицерин и другие. Криопротекторы предохраняют клетки и их органеллы от повреждения мембран кристаллами льда и от внутриклеточной дегидратации во время перехода воды из жидкой в кристаллическую фазу. При замораживании и размораживании клеток жизнеспособность и функции в клетках зависят от типа замораживаемых клеток или ткани и от концентрации криопротекторов.
Подбор оптимальных условий и сред для криоконсервации является важной задачей для сохранения жизнеспособности клеток и тканей, эффективность составов и концентрации криозащитных агентов еще не достаточно определены, необходима оптимизация протокола витрификации. Поэтому первоочередной задачей является разработка методологических подходов, апробация методик по сохранению генетического материала, а именно половых клеток, как зрелых (ооциты преовуляторных фолликулов), так и незрелых (ооциты примордиальных и первичных фолликулов в составе эксплантатов овариальной ткани) у онкологических больных до начала лечения на стадии постановки диагноза.
Известен «Способ подготовки ткани яичника к трансплантации у пациенток со злокачественными новообразованиями органов репродуктивной системы» (RU 2336697, 20.07.2007). Способ включает этап транспортировки ткани во льду и характеризующийся тем, что осуществляют забор ткани яичника, обработку ткани средами (Medicult), отделение кортикального слоя от медуллярной части, криоконсервацию путем замораживания ткани в криовиолах со стартовой температурой +4°С и пошаговым охлаждением 2°С/мин до -9°С, инициацию кристаллизации при -9°С и выполнение пошагового охлаждения 0,3°С/мин до температуры -40°С, затем 10°С/мин до температуры -140°С, последующее погружение в криобанк с жидким азотом с температурой -196°С и хранение с последующим размораживанием ткани для трансплантации. При заборе ткани, ее обрабатывают вначале Flushing-средой с гепарином (Medicult) при комнатной температуре, затем средой Sperm Preparation Medium (Medicult), после чего отделяют кортикальный слой от медуллярной части, и ткань, находящуюся в стерильных пробирках в среде Sperm Preparation Medium (Medicult) помещают в лед для транспортировки. Кортикальный слой нарезают на фрагменты размером 5×10 мм и толщиной 1 мм на холодном столе при температуре +4°С и подвергают дегидратации в течение 95 мин путем помещения фрагментов ткани в криовиалы с раствором 1,5 моль/л пропандиола и с 0,1 моль/л сахарозы и осуществляют криоконсервацию. После размораживания ткань помещают в среду Sperm Preparation Medium (Medicult) при комнатной температуре, в которой она находится до трансплантации.
Недостаток способа заключается в том, что ткань яичника замораживается методом медленной заморозки, в результате которого возможно формирование кристаллов льда, требуется минимум 3 часа для заморозки ткани и использование дорогостоящего оборудования.
Известен «Способ восстановления фертильности у пациенток с онкологическими заболеваниями» (RU 2519637, 16.04.2014). Способ включает отбор больных и забор у них генетического материала перед проведением курса лучевой и/или химиотерапии, криоконсервацию отобранной яичниковой ткани, хранение ее для последующего размораживания и использование при аутотрансплантации, Кроме того, отбор пациенток включает проверку на наличие опухоли яичников или их метастатическое поражение.
Недостаток способа заключается в том, что недостаточно подробно описан этап криоконсервации ткани яичника (витрификация), в витрифицирующих растворах содержится высокой концентрации токсичный для ооцитов криопротектор (диметилсульфаксид).
Известен «Способ криоконсервации яичниковой ткани» (заявка на изобретение RU 2012103061/10 от 31.01.2012).
Он заключается в замораживании образца яичниковой ткани в носителе, в атмосфере ксенона (95%-99,99% степени чистоты) под давлением не менее 1,5 атм. Ткань выдерживают при температуре -20°С, а затем погружают в азот.
Недостаток способа заключается в том, что необходимо специальное оборудование для заморозки ткани и не указана техника криоконсервации ткани.
Известен «Способ витрификации яичниковой ткани» (заявка на изобретение RU 2012103059/10 от 31.01.2012). Он заключается в поэтапном насыщении препарата проникающими криопротекторами. Используют композицию состава: диметилсульфоксид 19,52%, ацетамид 14,75%, этиленгликоль 15,51%, полиэтиленгликоль с молекулярной массой 4 кДа 4%, яичный лецитин 4%, поливиниловый спирт молекулярной массой 6 кДа 1%, тетраполиглицерин 1%, кардиоплегический раствор остальное.
Недостаток способа заключается в том, что в заявке не указана техника витрификации ткани.
Известен "Ovarian tissue cryopreservation method» (CN 104222071 (А) от 2014-12-24 XIAO ZHUN). Метод криоконсервации ткани яичников заключается в: культивировании ткани яичника с раствором гиалуронидазы с объемной концентрацией 8-12% в течение 10-15 минут; криоконсервации ткани с криопротекторами при температуре 3-5°С в течение 10-15 мин; выполнение запрограммированной криоконсервации ткани яичников до -150°С, и переносе ткани яичника в жидкий азот для хранения. По сравнению с предыдущими методами медленного замораживание (90 мин) при такой методике замораживания сокращается время криоконсервации ткани и отрицательного воздействия криопротекторов.
Недостаток способа заключается в использование дорогостоящего оборудования. Известен «Cryoprotectant free of DMSO (dimethyl sulfoxide) and ovary cryopreservation» (CN 105052892-A2 от 2015-11-18. CHI Libglong, Li Dong). Способ заключается в криоконсервации ткани яичника в средах без ДМСО. Используют среды в составе которых: трегалоза 200 mmol/L, 0.3 g/ml PVP, 200 mu g/L холестерол, 200 mu g/L лецитин. Показан высокий процент морфологически нормальных фолликулов, небольшое количество апоптоза.
Недостаток способа заключается в том, что ткань яичника замораживается методом медленной заморозки, в результате которой возможно формирование кристаллов.
Известен «Method of ovary cryopreservation using antifreeze protein» (KR 20140093811 (А) от 2014-07-29, Lee Jung Ryeol; Youn Hye Won; Jee Byung Chul; Suh Chang Suk).
Метод заключается в криоконсервации ткани яичника в средах с добавлением белка в концентрации 3-7 мг/мл.
Недостаток способа заключается в том, что не указана технология процесса витрификации и нет точного состава сред для криоконсервации.
Известен «Ovarian large cortex piece vitrified cryopreservation protection liquid and cryopreservation method thereof CN 102771471 (A) - 2012-11-14 Yanrong Wang; Ling Dang; Hongyan ONGYAN Wang.
Метод заключается в криоконсервации большого кусочка коры яичниковой ткани методом витрификации. Изобретение обеспечивает защиту больших кусков коры яичников. В среды для криоконсервации добавляют гонадотропин. Метод направлен на сохранение яичников экспериментальных животных, сельскохозяйственных пород скота и диких исчезающих видов. Используя этот метод, выживаемость фолликулов может быть улучшена, время пересадки сокращается, и выживаемость трансплантированной криоконсервированной овариальной ткани в организм улучшается.
Недостаток способа заключается в том, что не указана технология процесса витрификации и нет состава сред.
Прототипом предлагаемого способа является «Ovarian tissue cryopreservation and transplantation: scientific implications» J Assist Reprod Genet, Oct 8. 2016. [Epub ahead of print, PubMed]. Способ заключается в криоконсервации кортикального слоя яичника путем витрификации в два этапа. В данном способе кортикальный слой препарировали на фрагменты размером 10 мм × 10 мм × 1 мм. На первом этапе взятые фрагменты пропитывали в растворе, содержащем 7,5% диметилсульфоксида (ДМСО), 7,5% этиленгликоля (ЭГ) и 20% сыворотки в среде ТСМ-199 (Tissue Culture Medium). Через 25 мин. выдерживания полученные фрагменты ткани помещали в раствор, содержащий 20% ЭГ, 20% ДМСО и 0,5 М сахарозы в среде ТСМ-199. В этом растворе фрагменты ткани выдерживали в течение 15 мин. Затем фрагменты ткани погружали в жидкий азот и после замораживания хранят их в криопробирках. Замороженную по такому протоколу ткань исследовали стандартными методами гистологии. В результате исследований выявлены изменения в морфологическом строении ткани и фолликулов после витрификации кортикального слоя овариальной ткани.
Недостатки прототипа заключаются в использовании высокой концентрации криопротекторов, в частности, криопротектора ДМСО, продукты распада которого обладают высокой токсичностью для ооцитов.
Технический результат предполагаемого изобретения заключается в снижении токсического эффекта и обеспечение высокой выживаемости фолликулов и клеточных компонентов стромы.
Сущность предлагаемого технического решения, включающего подготовку фрагментов кортикального слоя овариальной ткани размером 2-5 мм × 2-5 мм толщиной до 1 мм при +4°С и их поэтапное насыщение криопротекторами в среде для витрификации. Подготовленные фрагменты ткани насыщают растворами для витрификации в два этапа. На первом этапе фрагменты ткани пропитывают в течение до 20 мин в среде для витрификации, содержащей неорганические соли - 10,5 г/л, аминокислоты - 1,0 г/л, витамины - 0,10 г/л, глюкозу 1,0 - г/л, пенициллин-стрептомицин (100х) 10 мл/л и криопротекторы ДМСО - 7,5 объемных процентов (об %), ЭГ - 7,5 об. % с добавлением эмбриональной телячьей сыворотки до 20 об. % («GIBCO»). На втором этапе фрагменты ткани выдерживают до 10 мин в среде для витрификации, содержащей неорганические соли - 10,5 г/л, аминокислоты - 1,0 г/л, витамины - 0,10 г/л, глюкозу 1,0 г/л, пенициллин-стрептомицин (100х) 10 мл/л и криопротекторы - ДМСО от 17,0 об. % до 20,0 об. % и ЭГ от 10,0 об. % до 13,0 об. %, 0,5-0,6 М сахарозы. Фрагменты ткани помещают в стерильные криопробирки с жидким азотом и хранят при температуре -196С°.
Перечень фигур:
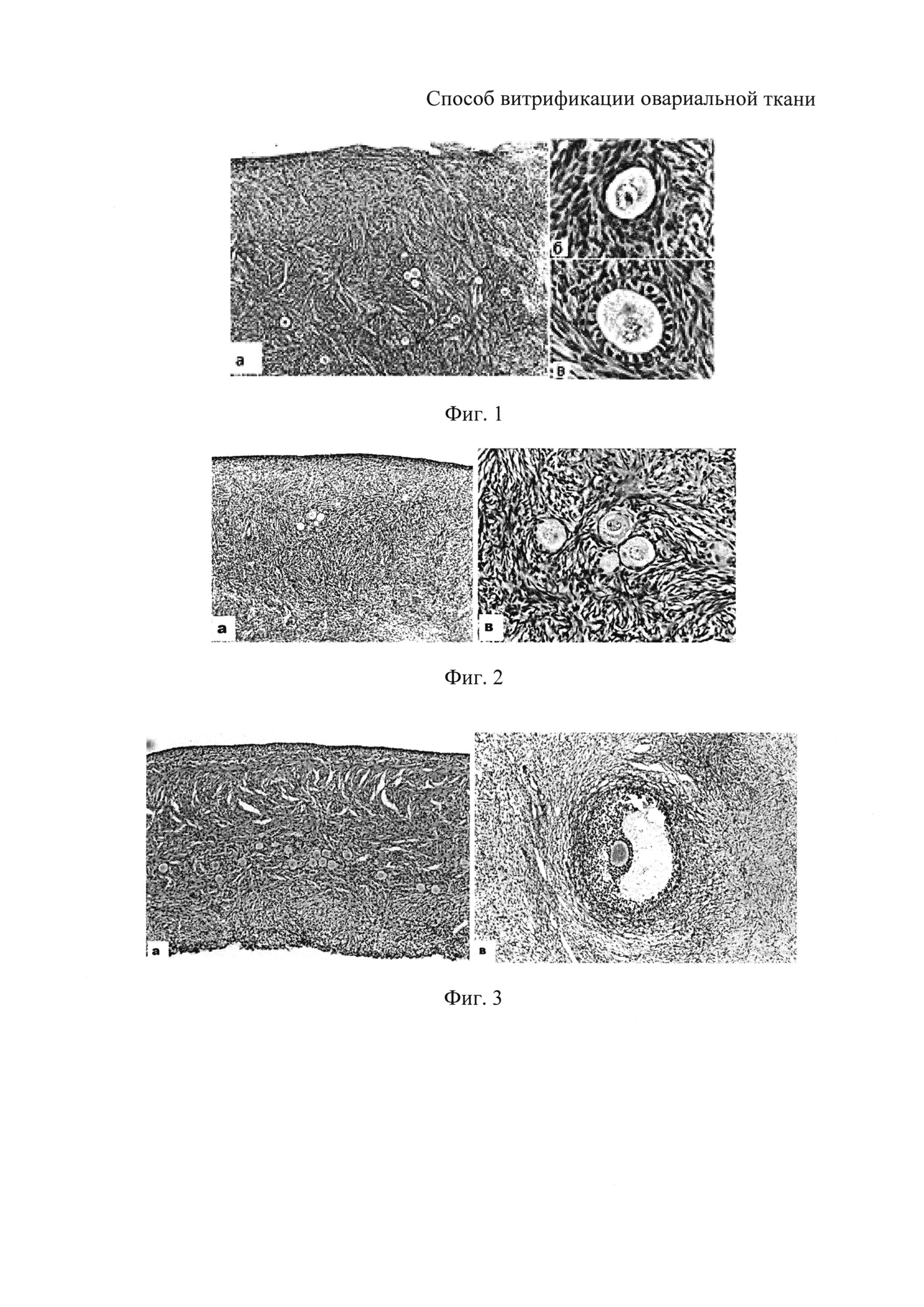
Фиг. 1. Нативная овариальная ткань: 1 (а) - кортикальный слой яичника, 2 (б) - примордиальные фолликулы, (в) - первичные фолликулы;
Фиг. 2. Фрагмент витрифицированной овариальной ткани с использованием криопротекторов ДМСО 17,0 об. % и ЭГ 13,0 об. % на втором этапе, зафиксированный после размораживания: (а) - корковое вещество с примордиальными фолликулами;
Фиг 3. Фрагмент витрифицированной овариальной ткани с использованием криопротекторов ДМСО до 20,0 об. % и ЭГ 10,0 об. % на втором этапе, зафиксированный после размораживания: 1-2 кортикальный слой ткани с фолликулами, 3 - кортикальный слой ткани;
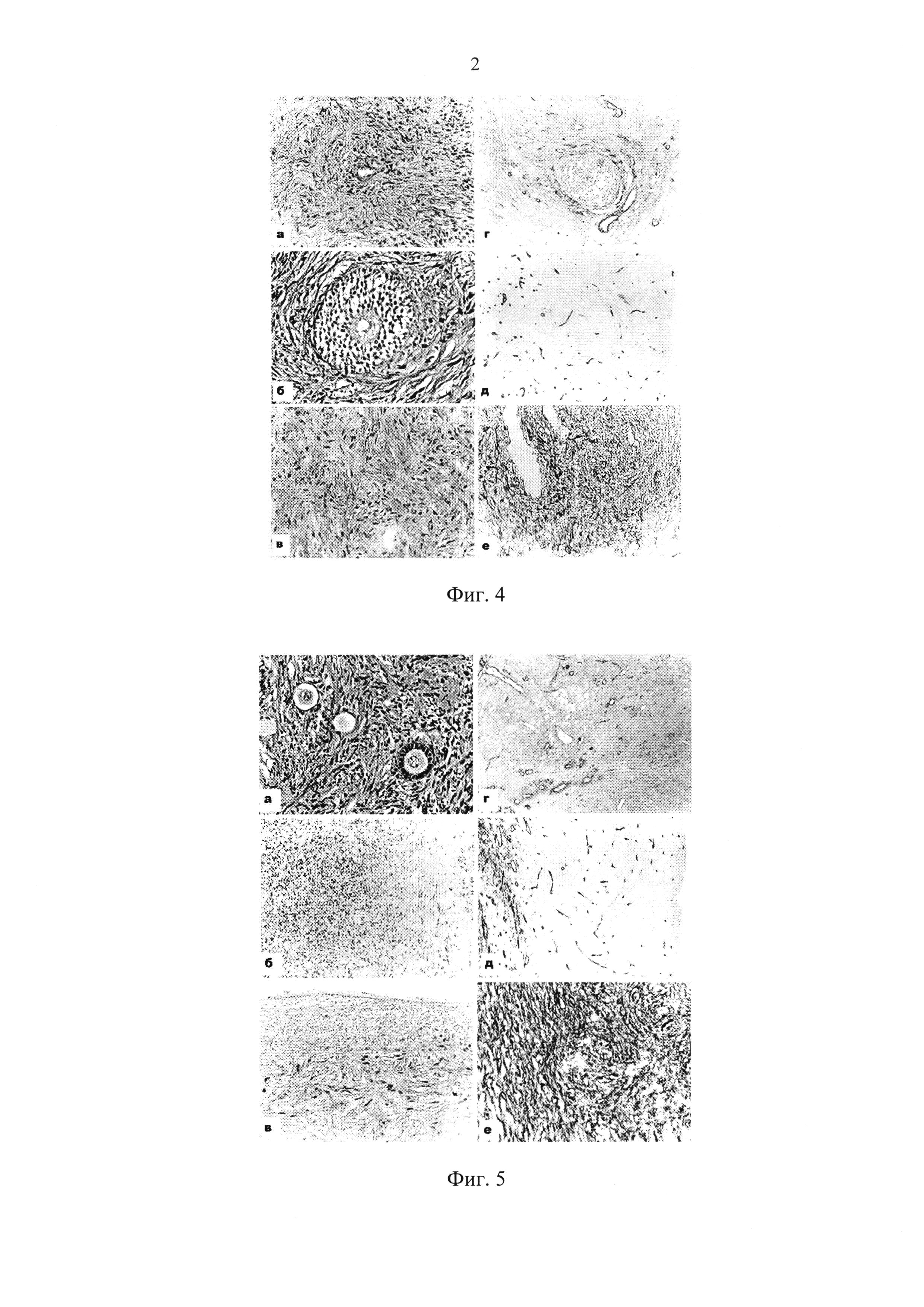
Фиг. 4. Нативная овариальная ткань: (а) и (б) - иммуноокрашивание на PCNA, (в) - на Ki-67, (г) - на CD31, (д) - на CD34, (е) - на виментин;
Фиг. 5. Функциональная морфология витрифицированной овариальной ткани с использованием криопротекторов ДМСО до 20,0 об. % и ЭГ 10,0 об. % на втором этапе после размораживания: (а) - окрашивание гематоксилином и эозином, (б) - иммуноокрашивание на PCNA, (в) - на Ki-67, (г) - на CD31, (д) - на CD34, (е) - на виментин; (а-в, д, е) - корковое вещество; (г) - мозговое вещество.
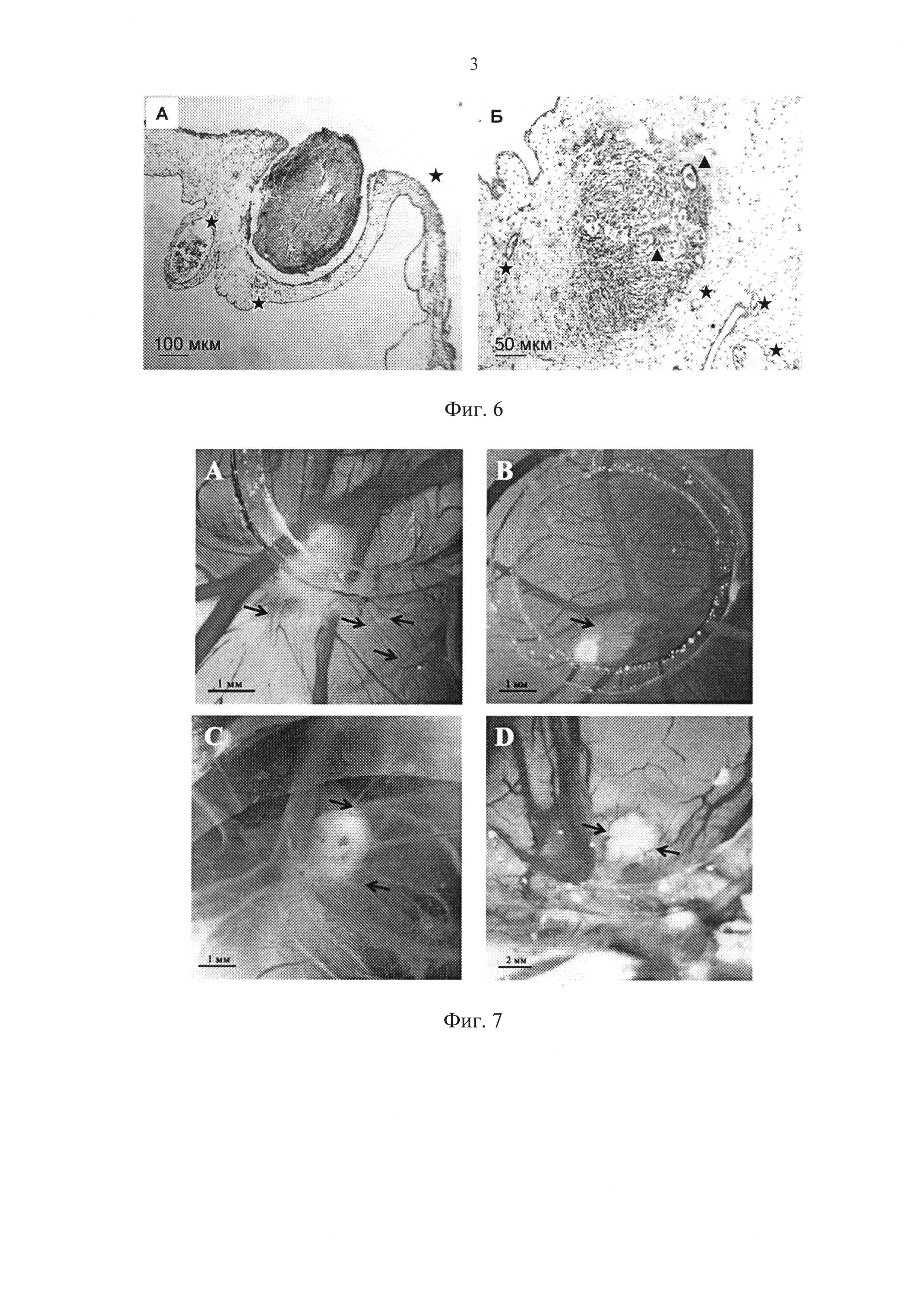
Фиг. 6. Гистологический срез овариальных эксплантатов после 4 суток культивирования на хориоаллантоисной мембране куриного эмбриона. Кровеносные сосуды отмечены звездочкой, фолликулы - треугольником.
Фиг. 7. Прорастание сосудов хориоаллантоисной мембраны куриного эмбриона к образцу витрифицированной (с использованием криопротекторов ДМСО до 20,0 об. % и ЭГ 13 об. % на втором этапе овариальной ткани человека.
Порядок реализации способа.
1. Подготовка образцов ткани яичника для витрификации: 1) скальпелем или ножницами отделяют кортикальный слой от мозгового слоя яичника, толщина кортикального слоя должна быть не более 1 мм; 2) образцы кортикального слоя ткани делят на фрагменты по 2-5 мм × 2-5 мм. 3) фрагменты ткани насыщают растворами криопротекторов в два этапа. На первом этапе фрагменты ткани пропитывают в течение до 20 мин в среде для витрификации, содержащей неорганические соли - 10,0 г/л (характерные для живых тканей, например: натрия хлорид, калия хлорид, кальция хлорид, магния сульфат, железа закисного цитрат, натрия дигидрофосфат и прочие соединения), аминокислоты - 1,0 г/л (характерные для живых тканей, например: L-аргинин-гидрохлорид, L-цистин, L-глутамин, глицин и прочие соединения), витамины - 0,10 г/л (характерные для живых тканей, например: витамины группы В, витамин С), глюкозу - 1,0 г/л, пенициллин-стрептомицин (100х) 10 мл/л и криопротекторы ДМСО - 7,5 об. %, ЭГ - 7,5 об. % с добавлением эмбриональной телячьей сыворотки до 20 об. % («GIBCO»). Среда первого этапа для витрификации остается постоянной на протяжении всех исследований. На втором этапе фрагменты ткани выдерживают до 10 мин в среде для витрификации, включающей (содержащей) неорганические соли - 10,0 г/л, аминокислоты - 1,0 г/л, витамины - 0,10 г/л, глюкозу 1,0 г/л, пенициллин-стрептомицин (100х) 10 мл/л и криопротекторы - ДМСО от 17,0 об. % до 20,0 об. % и ЭГ от 10,0 об. % до 13,0 об. %, 0,5-0,6 М сахарозы. Стерилизацию сред проводят фильтрацией через фильтры с размером пор 0,1 мкм.
Для криоконсервации овариальной ткани на одного пациента достаточно 10 мл среды для витрификации на каждом этапе. Ошибка в объеме при этом допускается в пределах от 5 до 10%.
2. Все процедуры подготовки ткани к витрификации, хранение приготовленных для витрификации растворов осуществляют при температуре до +4°С.
3. Подготовленные фрагменты ткани помещают в стерильные криопробирки с жидким азотом. Маркированные криопробирки хранятся при температуре -196С°.
Примеры реализации способа.
Для контроля эффективности процедуры криоконсервации витрифицированной овариальной ткани был выполнен гистологический и морфофункциональный анализ фрагментов овариальной ткани. Результаты исследований приведены в таблице 1 и фигурах 1-7. Были оценены образцы овариальной ткани 17 женщин в возрасте от 20 до 47 лет после витрификации. Изучали фрагменты нативной и витрифицированной овариальной ткани, включающие кортикальную зону и остатки мозгового вещества после удаления медуллярного слоя. Фрагменты ткани имели размер ≈ 2-5 мм × 2-5 мм × 1 мм.
Сравнительный гистологический анализ витрифицированной овариальной ткани с применением разных концентраций криопротекторов.
Для оптимизации протоколов витрификации овариальной ткани исследовали два варианта концентраций криопротекторов, входящих в среду для витрификации на втором этапе.
Изучение сохранности нативной (фигура 1) и витрифицированной овариальной ткани (фиг. 2-3, таблица 1) проводили методом гистологии. Общую гистологию овариальной ткани, подсчет фолликулов, верификацию стадии их развития и морфологическую сохранность изучали на срезах, окрашенных гематоксилином и эозином. Фолликулы подсчитывали по всей площади среза кортикального слоя фрагмента овариальной ткани. Его площадь определяли с помощью системы компьютерного анализа микроскопических изображений с применением прикладной лицензионной программы AnalySIS 5.0 ("Soft Imaging System GmbH", Германия).
В соответствии со стадией развития фолликулы классифицировали как примордиальные, первичные, вторичные и антральные. Примордиальные фолликулы характеризовались одним слоем уплощенных гранулезных клеток вокруг ооцита, первичные фолликулы - одним слоем кубовидных гранулезных клеток, вторичные фолликулы - двумя или несколькими слоями гранулезных клеток и антральные фолликулы - присутствием антральной полости.
Гистологическое строение коркового вещества яичников в контроле (до витрификации) соответствовало вариантам нормы (фиг. 1, а). Примордиальные фолликулы (ПМФ) (фиг. 1, б) и первичные фолликулы (ПФ) (фиг. 1, в) имели правильную округлую форму. В яйцеклетках хорошо просматривалось ядрышко и пространственная организация хроматина. Цитоплазма имела сетчатое или мелкозернистое строение. От окружающей стромы гранулезные клетки отграничены базальной мембраной. Наряду с нормальными фолликулами в кортикальном слое определялись фолликулы в стадии дегенерационной атрезии с деструкцией и гибелью ооцитов и их окружения. Согласно данным морфометрии, овариальный пул нормальных фолликулов составил 78,3% от общего числа верифицированных фолликулов в разной стадии их развития и атрезии. При этом относительное содержание примордиальных и первичных фолликулов составило 93,1 и 6,9% соответственно (см. таблицу).
Пример 1. Гистологическое строение коркового вещества витрифицированной овариальной ткани при концентрации ДМСО 17,0 об. % и ЭГ 13,0 об. % на втором этапе представлено соединительнотканными элементами и интерстициальными клетками. В строме в небольшом количестве выявлялись фолликулы различной степени зрелости (фиг. 2 а). По данным сравнительного анализа овариальный пул нормальных фолликулов составил 61,5% от общего числа верифицированных фолликулов, относительное содержание примордиальных и первичных фолликулов составило 91,0 и 9,0% соответственно (см. таблицу).
Пример 2. При изучении фрагментов овариальной ткани после витрификации концентрация ДМСО до 20,0 об. % и ЭГ 10,0 об. % на втором этапе показана хорошая гистологическая сохранность овариальной ткани (фиг. 3) после размораживания. Архитектоника кортикального слоя практически не изменилась по сравнению с контролем. По данным сравнительного анализа, содержание морфологически нормальных фолликулов снизилось до 64%. Однако относительный пул структурно не измененных примордиальных фолликулов сохранился на уровне более 91% (табл. 1). В большинстве случаев фолликулы выглядели нормальными с отсутствием признаков повреждения.
Сравнительный анализ содержания нормальных фолликулов в овариальной ткани после витрификации при разных концентрациях криопротекторов во втором растворе представлен в таблице.

В анализ включен материал после размораживания с культивированием в среде инкубации до 4 часов. ***
SОБЩ - суммарная площадь коркового вещества; NОБЩ - общее количество фолликулов на суммарной площади; NНФ - количество морфологически не измененных (нормальных) фолликулов на суммарной площади; ПМФ - примордиальные фолликулы, ПФ - первичные фолликулы
Полученные результаты свидетельствуют о том, что для сохранности клеточных и тканевых структур овариальной ткани эффективным является витрификация с использованием на втором этапе криопротекторов с концентрацией ДМСО от 17,0 до 20,0 об. % и ЭГ от 10,0 до 13,0 об. %
Пример 3. Анализ витрифицированной овариальной ткани с концентрацией криопротекторов ДМСО до 20,0 об. % ЭГ 10,0 об. % на втором этапе, используя иммуногистохимический анализ.
Изучение сохранности и жизнеспособности нативной и витрифицированной овариальной ткани проводили, используя иммуногистохимический анализ. Для изучения функциональной морфологии и жизнеспособности фолликулов, фибробластов и эндотелия сосудов овариальной ткани проводили исследования на срезах толщиной 7 мкм методом биотин-стрептавидин/экстравидин-пероксидазного комплекса с использованием моноклональных мышиных антител к ядерному антигену пролиферирующих клеток - PCNA (PC10, «Dako»), маркеру эндотелиальных клеток капилляров - CD34 (Clone QBEnd 10 «Dako»), белку промежуточных филаментов клеток мезенхимального происхождения - виментину (Clone V9 10 «Dako»), а также поликлональных кроличьих антител к специфическому маркеру эндотелия - адгезионной молекулы тромбоцит/эндотелиальной клетки-1 - РЕСАМ-1 (CD31, M-20-R, «Santa Cruz») и циклину Ki-67 (В9260 «Chemicon (Millipore).
При изучении функциональной морфологии нативной овариальной ткани методами иммуногистохимии (фиг. 5) отмечалась интенсивная иммуноположительная реакция ядер фибробластов, эндотелия сосудов и гранулезных клеток вторичных фолликулов с антителами к маркерам пролиферации - PCNA (фиг. 5, а, б) и Ki-67 (фиг. 5 в). Визуально количественная плотность Ki-67-положительных ядер была ниже, чем при использовании антител к ядерному антигену пролиферирующих клеток. Экспрессия CD31 (фиг. 5 г) и CD34 (фиг. 5 д) наблюдалась в стенке сосудов вокруг фолликулов и многочисленных капилляров, относительно равномерно заполняющих корковое вещество. При этом, как правило, антитела к CD31 позволяли более отчетливо контурировать крупные и средние сосуды мозгового вещества, в то время как иммуноокрашивание на CD34 лучше визуализировало капиллярное русло в кортикальном слое.
Поверхностный эпителий яичников на виментин не окрашивался, однако располагался на слое виментин-положительных стромальных клеток. Ооциты фолликулов всех стадий развития - от примордиальных до антральных были виментин-отрицательными. Положительная реакция на виментин наблюдалась в цитоплазме фибробластов стромы и эндотелия сосудов (фиг. 5, е).
После размораживания овариальной ткани отчетливо видна поверхностная зона кортикального слоя с репопулирующими фибробластами и эндотелиальными клетками Восстановление репопуляционной активности клеток фибробластического ряда и эндотелия сосудов начиналось с периферии культивируемых образцов и определялось, по-видимому, скоростью и глубиной диффузии, жизнеспособность стромальных и гранулезных клеток восстанавливалась (фиг. 6).
Определялась пролиферативная активность стромальных клеток и эндотелия и мало отличалась от нативного контроля (фиг. 6 б, в). Хорошая сохранность рисунка васкуляризации мозгового вещества и кортикального слоя при иммуноокрашивании гистологических срезов на CD31 и CD34 (фиг. 6 г, д) и жизнеспособность фибробластов и эндотелия сосудов по экспрессии виментина (фиг. 6, е).
Пример 4. Оценка состояния витрифицированной овариальной ткани человека с концентрацией криопротекторов ДМСО до 20,0 об. % и ЭГ 10,0 об. % на втором этапе, используя тест на хориоаллантоисной мембране куриного эмбриона.
Способность овариального трансплантата индуцировать ангиогенез при обратной подсадке пациентке - важная характеристика, описывающая состояние ткани после криоконсервации. Тест на хориоаллантоисной мембране куриного эмбриона (САМ-тест) является одним из немногих методов, способных визуально и количественно оценить данную характеристику.
Интенсивность ангиогенеза оценивали по цифровым изображениям образцов овариальной ткани и прилежащей области хориоаллантоисной мембраны, пронизанной кровеносными сосудами при помощи программного обеспечения ImageJ (NIH, США). Полученные значения сравнивали с индексом плотности сосудов хориоаллантоисной мембраны без какой-либо индукции - нейтральный контроль.
Чтобы посмотреть взаимодействие овариального эксплантата с хориоаллантоисной мембраной были изготовлены гистологические препараты некоторых образцов. При анализе этих препаратов были обнаружены два варианта взаимодействия (фиг. 6). В ряде случаев овариальный эксплантат лежал на поверхности мембраны, не нарушая ее целостности (фиг. 6 а). Но также и наблюдались варианты, когда ткань яичника внедрялась непосредственно в хориоаллантоисную мембрану, при этом иногда эксплантат содержал первичные и примордиальные фолликулы (фиг. 6, б).
Анализ способности криоконсервированной ткани индуцировать ангиогенез показал, что к овариальным эксплантатам, прошедшим процедуру витрификации, в ряде случаев прорастают кровеносные сосуды хориоаллантоисной мембраны куриного эмбриона. К некоторым образцам сосуды сходились радиальными пучками (фиг. 7). Также были обнаружены образцы, поверхность которых обрастала кровеносными сосудами (фиг. 7 а, г). Изучение индексов плотности сосудов хориоаллантоисной мембраны, прилежащей к овариальным образцам нативной и витрифицированной ткани показало, что в обоих случаях происходила индукция ангиогенеза и значения индексов плотности сосудов этих групп достоверно отличаются от нейтрального контроля.
Пример 5. Рождение ребенка после аутотрансплантации витрифицированной овариальной ткани.
У пациентки К. ранее прошедшей курс радиойодтерапии (рак щитовидной железы IV стадии) после аутотрансплантации в 2012 г. витрифицированной овариальной ткани с концентрацией криопротекторов ДМСО до 20,0 об. %, ЭГ 10,0 об. % на втором этапе восстановился менструальный цикл и нормализовался гормональный статус.
В дальнейшем была произведена пункция фолликулов, получены эмбрионы. Была получена одноплодная беременность и 25 августа 2015 года родился здоровый мальчик (см. Приложение из газеты).
Подтверждение достижения технического результата.
Комплексный гистологический и морфофункциональный анализ с применением маркеров пролиферации, ангиогенеза и структурной целостности клеток мезенхимального происхождения свидетельствует о хорошей морфологической сохранности пула примордиальных фолликулов и быстром восстановлении жизнеспособности ее клеточных компонентов после размораживания в витрифицированной овариальной ткани при использовании на втором этапе криопротекторов ДМСО от 17,0 об. % до 20,0 об. % и ЭГ от 10,0 об. % до 13,0 об. %. При количественном исследовании относительный пул примордиальных фолликулов после витрификации сохранился на уровне более 91%. Показана способность витрифицированного овариального трансплантата индуцировать ангиогенез хориоаллантоисной мембраны куриного эмбриона.
Подтверждена нормализация гормонального статуса у пациенток, которым была произведена аутотрансплантация витрифицированной овариальной ткани по предложенному протоколу. Это дает возможность восстановить гормональный статус и фертильность пациенток после трансплантации декриоконсервированного кортикального слоя овариальной ткани.
Способ витрификации овариальной ткани, включающий подготовку образцов овариальной ткани, их двухэтапное насыщение криопротекторами в среде, содержащей 7,5% раствор ДМСО и 7,5% ЭГ, 0,5 М сахарозы, фрагменты ткани хранят в стерильных криопробирках с жидким азотом, отличающийся тем, что подготовку образцов ткани яичника для витрификации проводят путем удаления кортикального слоя от мозгового слоя яичника, толщину кортикального слоя задают не более 1 мм и делят на фрагменты по 2-5 мм × 2-5 мм при +4°С, затем фрагменты ткани насыщают растворами криопротекторов в два этапа: на первом этапе фрагменты ткани пропитывают в течение до 20 мин в среде для витрификации, содержащей неорганические соли - 10,5 г/л, аминокислоты - 1,0 г/л, витамины - 0,10 г/л, глюкозу - 1,0 г/л, пенициллин-стрептомицин (100×) 10 мл/л и криопротекторы ДМСО - 7,5 об.%, ЭГ - 7,5 об.% с добавлением эмбриональной телячьей сыворотки до 20 об.%, на втором этапе фрагменты ткани выдерживают до 10 мин в среде для витрификации, содержащей неорганические соли - 10,0 г/л, аминокислоты - 1,0 г/л, витамины - 0,10 г/л, глюкозу - 1,0 г/л, пенициллин-стрептомицин (100×) 10 мл/л и криопротекторы ДМСО от 17,0 до 20,0 об.% и ЭГ от 10,0 до 13,0 об.%, 0,5-0,6 М сахарозы, подготовленные фрагменты кортикального слоя овариальной ткани помещают в стерильные маркированные криопробирки с жидким азотом для хранения при -196°С.