Результат интеллектуальной деятельности: 10-Бензил-3,4-дибензоил-2´-оксо-1´,2´,10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3´-пирролы]
Вид РИД
Изобретение
10-Бензил-3,4-дибензоил-2'-оксо-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролы]
Изобретение относится к области органической химии, а именно к новым биологически активным индивидуальным соединениям класса спиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролов], а именно к 10-бензил-3,4-дибензоил-2'-оксо-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролам] формулы
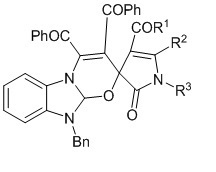
обладающим противомикробной активностью, что позволяет предположить их использование в качестве исходных продуктов для синтеза новых гетероциклических систем, в фармакологии и в медицине в качестве лекарственных средств с противомикробным эффектом.
Известны структурные аналоги заявленных соединений – бензимидазол[2,1-b][1,3]оксазин спирооксиндолы (Li-Juan Zhang, Chao-Guo Yan. Synthesis of benzimidazole[2.1-b][1,3]oxazine spirooxindoles via three-component reaction of N-benzylbenzimidazole, acetylenedicarboxylates, and N-alkylisatins // Molecular Diversity, 2014, 787–796) формулы
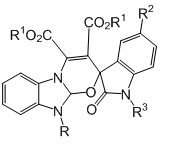
R1 = Me, Et; R2 = H, Me, Cl, F; R3 = Bn, Bu
Эталоном сравнения противомикробной эффективности был выбран диоксидин, который широко применяется в лечебной практике и является аналогом по действию [Падейская Е.Н. Антибактериальный препарат диоксидин: особенности биологического действия и значение в терапии различных форм гнойной инфекции // Инфекции и антимикробная терапия, 2001, №5, с.105-155].
Задачей изобретения является поиск в ряду производных спиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролов] веществ с выраженным противомикробным действием и расширения арсенала средств воздействия на живой организм.
Поставленная задача достигается получением 10-бензил-3,4-дибензоил-2'-оксо-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролов], которые обладают выраженной противомикробной активностью.
Заявляемые соединения синтезируют путем трехкомпонентного взаимодействия 1Н-пиррол-2,3-дионов (I) с дибензоилацетиленом и N-бензилбензимидазолом в соотношении 1:1:1 в среде растворителя с последующим выделением целевых продуктов, по следующей схеме:
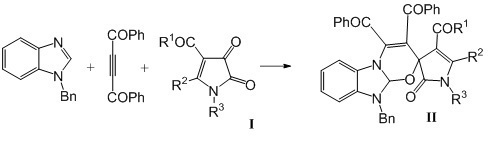
где I, II: R1= Ph; R2 = Ph, R3 = CH2Ph (а); R1 = OEt; R2 = Ph; R3= 4-C6H4Cl (б), Ph (в); R1 = Ph; R2 = СOOMe; R3 = 4-C6H4Me (г), 4-C6H4OMe (д), 4-C6H4Br (е).
Процесс ведут при комнатной температуре, а в качестве растворителя используют абсолютный хлороформ либо другие инертные апротонные растворители.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение 1',10-дибензил-3,4,4'-трибензоил-2'-оксо-5'-фенил-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пиррола] (IIа).
К раствору 1.0 ммоль 1-бензил-4-бензоил-5-фенил-1H-пиррол-2,3-диона (Iа) в 10 мл абсолютного хлороформа добавляли 1.0 дибензоилацетилена и 1.0 ммоль N-бензилбензимидазола. Реакционную массу перемешивали в течение 5 ч. при комнатной температуре. Образовавшийся осадок отфильтровывали и перекристаллизовывали из этилового спирта. Выход 89%, т.пл. 168-170°С. Соединение (IIа) C54H39N3O5.
Найдено, %: C 80.20; H 4.69; N 5.45.
Вычислено, %: C 80.08; H 4.85; N 5.19.
Соединение (IIа) – красное кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, хлороформе, дихлорметане, трудно растворимое в ацетоне, спиртах, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIа), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний лактамной карбонильной группы С2'=О при 1735 см-1 и кетонных карбонильных групп при 1671, 1614 см-1.
Спектр ЯМР 1H (400 МГц, CDCl3) δ 4.44 (д, J = 15.8 Гц, 1H), 4.69 (д, J = 14.8 Гц, 1H), 5.09 (д, J = 15.8 Гц, 1H), 4.74 (д, J = 15.8 Гц, 1H), 6.33 (д, J = 7.9 Гц, 1H), 6.49 (д, J = 7.4 Гц, 2H), 7.62 – 6.68 (м, 32H).
Пример 2. Получение этил 10-бензил-3,4-дибензоил-2'-оксо-5'-фенил-1'-(4-хлорфенил)-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пиррол]-4'-карбоксилата (IIб).
К раствору 1.0 ммоль 5-фенил-1-(4-хлорфенил)-4-этоксикарбонил-1Н-пиррол-2,3-диона (Iб) в 10 мл абсолютного хлороформа добавляли 1.0 дибензоилацетилена и 1.0 ммоль N-бензилбензимидазола. Реакционную массу перемешивали в течение 5 ч при комнатной температуре. Образовавшийся осадок отфильтровывали и перекристаллизовывали из этилового спирта. Выход 60%, т.пл. 175-177°С.
Соединение (IIб) C49H36СlN3O6.
Найдено, %: C 73.58; H 4.35; N 5.43.
Вычислено, %: C 73.72; H 4.55; N 5.26.
Соединение (IIб) – красное кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, хлороформе, дихлорметане, трудно растворимое в ацетоне, спиртах, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIб), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний лактамной карбонильной группы С2'=О и сложноэфирной карбонильной группы при 1759 см-1, а также кетонных карбонильных групп при 1680 см-1.
Спектр ЯМР 1H (400 МГц, CDCl3) δ 0.76 (т, J = 7.1 Гц, 3H), 3.81 – 3.71 (м, 2H), 4.69 (д, J = 15.7 Гц, 1H), 4.74 (д, J = 15.5 Гц, 1H), 6.30 (д, J = 7.9 Гц, 1H), 6.61 – 6.43 (м, 2H), 6.81 (т, J = 7.8 Гц, 1H), 7.01 (с, 1H), 7.68 – 7.07 (м, 24H).
Соединения (IIв-е) синтезированы способом, аналогичным описанному в примере 1.
Пример 3. Фармакологическое исследование 10-бензил-3,4-дибензоил-2'-оксо-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролов] (IIа-в) на наличие противомикробной активности.
Исследование противомикробной активности заявляемых соединений проводили на грамположительных микроорганизмах Staphylococcus aureus (штамм 906).
Противомикробное действие выявляли методом двукратных серийных разведений в соответствии с методическими указаниями по изучению противомикробной активности препаратов [Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. – М.: И-во Медицина, 2005. – 832 с.]. Готовили исходные разведения микроорганизмов в изотоническом растворе натрия хлорида из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 МЕ. Для определения противомикробного действия микробную взвесь (микробная нагрузка равна 2.5·105 микробных тел в 1 мл питательной среды) вносили в приготовленные разведения препарата в питательной среде. Факт ингибирования микробных клеток в разведениях препаратов отмечали после 20-ти часового термостатирования при 37°С. Окончательные результаты фиксировали через 7 суток после высева на скошенный агар РПА.
Противомикробную активность оценивали по минимально действующей концентрации. Максимально испытанная концентрация соединения соответствовала 1000 мкг/мл. За действующую минимальную ингибирующую концентрацию (МИК) препарата принимали разведение в последней пробирке ряда, в которой визуально отсутствовал рост культуры. Минимальной бактерицидной концентрацией (МБК) считали минимальное разведение соединения в пробирке с визуально отсутствующим ростом культуры, высев из которой на плотную питательную среду не сопровождался ростом клеток. Противомикробный эффект исследуемых соединений сравнивали с действием диоксидина [Падейская Е.Н. Антибактериальный препарат диоксидин: особенности биологического действия и значение в терапии различных форм гнойной инфекции // Инфекции и антимикробная терапия, 2001, №5, с.105-155].
Проведенные исследования показали (см. таблицу), что соединения (IIа-в) проявляют выраженное ингибирующее действие относительно штаммов золотистого стафилококка в интервале концентраций – 15.6-500 мкг/мл, что активнее диоксидина в несколько раз.
Таблица. Противомикробная активность соединений (IIа-в).
|
Примечание: Все препараты растворяли в диметилсульфоксиде; "−" – отсутствие противомикробного действия в испытанных концентрациях; *МИК – минимальная ингибирующая концентрация; **МБК – минимальная бактерицидная концентрация.
Заявляемые ранее неописанные в литературе 10-бензил-3,4-дибензоил-2'-оксо-1',2',10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3'-пирролы] могут быть синтезированы с хорошими выходами и могут найти применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств с противомикробными свойствами.
![10-Бензил-3,4-дибензоил-2´-оксо-1´,2´,10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3´-пирролы]](https://fips.edrid.ru/images/rid/15/d0/89/0b2878e74eea5f7181f4b76ca33b6f68.jpg)
![10-Бензил-3,4-дибензоил-2´-оксо-1´,2´,10,10a-тетрагидроспиро[бензо[4,5]имидазо[2,1-b][1,3]оксазин-2,3´-пирролы]](https://fips.edrid.ru/images/rid/15/d0/89/d1fe19828e797dd88498050cbc3d17fd.jpg)

