Результат интеллектуальной деятельности: СПОСОБ ОЦЕНКИ СТЕПЕНИ РИСКА НЕБЛАГОПРИЯТНОГО ИСХОДА ЗАБОЛЕВАНИЯ У БОЛЬНЫХ РАКОМ ЖЕЛУДКА
Вид РИД
Изобретение
Изобретение относится к области медицины, конкретно к онкологии, касается способов определения степени риска неблагоприятного исхода заболевания у больных раком желудка.
К числу наиболее распространенных онкологических заболеваний органов желудочно-кишечного тракта как в России, так и за рубежом относится рак желудка (РЖ). В структуре общей заболеваемости онкологической патологией он составляет 7,0%. Следует отметить, что РЖ более распространен среди мужского населения (8,6%), нежели среди женского (5,5%) [1]. Известно, что главным прогностическим фактором при РЖ служит резектабельность [6]. После радикального хирургического лечения 5-летняя выживаемость в зависимости от окончательной стадии заболевания составляет: IA - 95%, IB - 85%, II - 54%, IIIA - 37%, IIIB - 11%, IV - менее 7% [7]. На сегодня разработаны алгоритмы лечения РЖ на разных стадиях заболевания, включающие радикальное хирургическое лечение, неоадьювантную химиотерапию, адьювантную химио- и лучевую терапию. В этой связи для коррекции тактики планируемой терапии актуальной является оценка прогноза исхода заболевания на основании показателей внутриклеточного протеолиза и, как следствие, формирование групп повышенного риска.
В литературе представлено немного объективных и надежных критериев прогноза исхода заболевания у пациентов с диагнозом рак желудка.
Одним из существующих способов оценки прогноза исхода заболевания при раке желудка является способ прогнозирования гематогенного метастазирования при кишечном типе рака желудка, который заключается в проведении иммуногистохимической оценки процента экспрессии протеина альдо-кето редуктазы I В 10 семейства (AKR1B10) в клетках рака желудка кишечного типа, формирующих железистоподобные структуры, располагающиеся в слизистом, подслизистом, мышечном и серозном слоях стенки желудка, рассчитывают коэффициент регрессии β с помощью метода множественной регрессии из пакета программ Statistica 6,0 for Windows, при этом в качестве переменного параметра используют процент экспрессии AKR1B10 в слизистом, подслизистом, мышечном и серозном слоях стенки желудка, а в качестве независимого параметра используют показатель, отражающий наличие опухолевых структур в разных слоях стенки желудка: «1» - в слизистом слое, «2» - подслизистом, «3» - мышечном, «4» - серозном, причем если опухоль прорастает до мышечного слоя, то оценивают экспрессию только в трех слоях, и при значении коэффициента регрессии β, равном или более «0,25», случай относят к группе высокого риска развития гематогенных метастазов, при значении коэффициента регрессии β менее «-0,25» случай относят к группе низкого риска развития гематогенных метастазов [5].
Известен способ прогнозирования метастазирования опухолевого процесса у больных раком желудка, заключающийся в том, что в периферической венозной крови обследуемых лиц определяют абсолютное содержание моноцитов и концентрацию фактора некроза опухоли альфа (TNF-α). При содержании моноцитов менее 0,35⋅109 кл/л и TNF-α более 55 пг/мл прогнозируют высокую вероятность метастазирования [4].
Наиболее близким к заявляемому способу является способ прогнозирования исхода заболевания, использующий математическое моделирование. Способ, предложенный Е.М. Непомнящей с соавт., включает определение молекулярных показателей: маркера пролиферативной активности Ki-67 и маркеров апоптоза р53 и bcl-2 методом иммуногистохимии [3]. Проводят иммуногистохимическое исследование и устанавливают, что при абсолютных значениях при перстневидно-клеточном раке: р53 - 10%, bcl-2 - 10%, Ki-67 - 12%; при недифференцированном раке: р53 - 13%, bcl-2 - 11%, Ki-67 - 9%; при аденокарциноме: р53 - 10%, bcl-2 - 9%, Ki-67 - 12% прогнозируют возникновение метастазов в лимфоузлах. При р53 - 6%, bcl-2 - 5%, Ki-67 - 10% прогнозируют отсутствие метастатического поражения лимфоузлов. С помощью этих прогностических факторов можно предсказать исход заболевания, выживаемость и вероятность возникновения метастазов у больных при отсутствии лечения, планирования лечебных мероприятий [6].
Недостатками этого способа являются:
- отсутствие чувствительности и специфичности, что не позволяет оценить практическую значимость и эффективность применения способа;
- сложность, длительность и высокая стоимость проведения анализа, связанная с иммуногистохимическим исследованием.
Новая техническая задача - повышение точности информативности, сокращение времени способа.
Для решения поставленной задачи в способе определения степени риска неблагоприятного исхода заболевания у больных раком желудка, включающем исследование ткани опухоли, причем в опухоли желудка определяют общую кальпаиновую активность, химотрипсинподобную тотальную активность протеасом, активность 26S и 20S пулов протеасом, содержание субъединиц сумма α Σα, содержание субъединицы LMP7, содержание субъединицы LMP2, содержание субъединицы РА28β, содержание субъединицы Rpt6, также учитывают возраст пациентов, затем рассчитывают значения дискриминантных функций Y1, Y2 по уравнениям:
Y=-0,015*X1+0,006*X2+0,085*X3+0,011*X4+0,083*X5+0,006*X6+0,100*X7+0,087*X8+0,066*X9+0,681*X10-45,698;
Y2=-0,017*X1-0,006*X2+0,146*X3+0,004*X4+0,122*X5+0,012*X6+0,123*X7+0,098*X8+0,102*X9+0,831*X10-74,476,
где X1 - общая кальпаиновая активность, ⋅103 Ед./мг белка;
Х2 - химотрипсинподобная тотальная активность протеасом, ⋅103 Ед./мг белка;
Х3 - активность 26S пула протеасом, ⋅103 Ед./мг белка;
Х4 - активность 20S пула протеасом, ⋅103 Ед./мг белка;
Х5 - содержание субъединиц сумма α;
Х6 - содержание субъединицы LMP7;
Х7 - содержание субъединицы LMP2;
Х8 - содержание субъединицы РА28β;
Х9 - содержание субъединицы Rpt6;
Х10 - возраст пациентов;
при Y1>Y2, пациента относят к группе с низким, а при Y1<Y2 - к группе с высоким риском неблагоприятного исхода рака желудка, в случае когда признаки объекта, предъявляемого для распознавания, удовлетворяют условию Y1=Y2, распознавание невозможно без привлечения дополнительной информации.
Чувствительность метода составляет 67%, специфичность - 96%. Результаты классификации представлены в таблице 1.
Способ осуществляют следующим образом.
Для оценки прогноза исхода заболевания у больных РЖ проводят определение активности следующих молекулярных параметров: кальпаинов, химотрипсинподобной тотальной активности протеасом, активности 26S и 20S пулов протеасом, содержание Σα, LMP7, LMP2, РА28Рβ Rpt6 субъединиц протеасом в опухоли желудка. Для этого образец опухоли желудка, взятый при хирургическом вмешательстве, гомогенизируют до порошкообразного состояния в жидком азоте. 26S и 20S протеасомы выделяют методом высаливания с помощью сульфата аммония до 40% и до 70% насыщения соответственно [2]. Химотрипсинподобную активность протеасом и активность кальпаинов оценивают по гидролизу флуорогенного олигопептида Suc-LLVY-AMC (Sigma, США) [13]. Образовавшийся продукт регистрируют на флуориметре «Hitachi-850» (Япония) при длине волны возбуждения 380 нм и эмиссии 440 нм. Для оценки активности примесных протеаз применяют специфический ингибитор протеасом - MG132, и специфический ингибитор кальпаинов - ALLN. За единицу активности протеасом и кальпаинов принимают количество фермента, при котором гидролизуется 1 нмоль Suc-LLVY-AMC в течение 1 мин. Удельную активность протеасом и кальпаинов выражают в единицах активности на 1 мг белка. Содержание белка определяют по методу Лоури.
Электрофоретическое разделение белков для последующего Вестерн-блоттинга проводят по Laemmli в 13% полиакриламидном геле. Пробы наносят в буфере, содержащем 0,0625М трис-HCl (рН 6,8), 2% SDS, 5% 2-меркаптоэтанол, 10% глицерин, 0,01% бромфеноловый синий. После электрофореза осуществляют перенос полипептидов на PVDF-мембрану (Immobylon, Millipore, США). Иммунодетекцию проводят согласно протоколу для «SNAP i.d.» (Millipore, США) с первичными антителами к субъединицам α1α2α3α5α6α7, LMP7, Rpt6, LMP2 и РА28β протеасом и к β-актину, а также вторичными антителами goat anti-mouse IgG-horseradish peroxidase (HRP) и goat ani-rabbit IgG-HRP (Santa Cruz Biotechnology, США) в разведениях, рекомендованных производителем. Затем мембрану подвергают обработке системой хемилюминесцентной детекции ECL (GE Healthcare, Великобритания). Плотность полос оценивают с помощью компьютерной программы «ImageJ». Стандартизацию проводят относительно β-актина. Результаты выражают в процентах от содержания субъединиц протеасом в неизмененной ткани.
Такой подход к оценке прогноза исхода заболевания у больных РЖ обусловлен рядом предпосылок.
На развитие и прогрессирование РЖ, помимо клинико-морфологических параметров заболевания, влияют и индивидуальные биологические особенности злокачественных опухолей. Новые молекулярные маркеры, отражающие прогрессирования РЖ, позволят расширить возможности персонализированной терапии и помогут прогнозировать ее отдаленные результаты, что в конечном итоге повысит качество и эффективность лечения РЖ. Известно, что протеолитические процессы, протекающие в опухоли, отличаются от процессов, идущих в нормально функционирующей ткани. Исключением для данного процесса не являются протеасомная и кальпаиновая протеолитические системы.
Изучалось состояние активации убиквитин-протеасомной системы в скелетных мышцах при РЖ. Показано, что расщепление определенных флуорогенных оснований увеличивалось в мышцах больных РЖ по сравнению с контрольной группой, что свидетельствует об увеличении активности протеасом не только в ткани РЖ, но и в скелетных мышцах, как следствие развивающейся кахексии [12]. Показано, что протеасомная система является важным механизмом при развитии РЖ, индуцированного HP. Бактерии, инфицирующие слизистую оболочку желудка, способны влиять на активность протеасом в ее клетках, повреждая процесс деубиквитинирования белков, не подлежащих деградации. К числу таких белков относится опухолевый супрессор RUNX3, который инактивируется при РЖ, индуцированном HP [11].
Известно, что экспрессия специфического для ткани желудка кальпаина-9 снижена в опухоли, но неизвестно, можно ли это отнести к опухолевым изменениям или это является специфичным для ткани ЖКТ [8]. Следует отметить, что для гастро-эзофагеальных аденокарцином возможно определение экспрессии кальпаинов-1 и -2 для оценки прогноза данной патологии. Кроме того, аналогичные результаты характерны для злокачественных новообразований яичников: высокая экспрессия кальпаина-2 ассоциирована с резистентностью к препаратам платины и низкой безметастатистической и общей выживаемостью [9, 10].
Информативность отобранных критериев подтверждена также наличием значимых различий в активности протеасом и кальпаинов, а также экспрессии субъединиц протеасом в опухоли желудка и неизмененной ткани, выявленных при исследовании 70 пациентов (средний возраст 57,9±10,2 лет) с морфологически верифицированным диагнозом РЖ Т1-4N0-3M0, которым было проведено хирургическое лечение.
Оценка прогноза исхода заболевания у больных РЖ проводилась на основании показателей состояния протеолитических систем (химотрипсинподобная активность тотального пула протеасом, пулов 26S и 20S, субъединичный состав протеасом, активность кальпаинов), клинико-морфологических данных (возраст пациентов, стадия Т, наличие метастазов в регионарные лимфоузлы, степень дифференцировки опухоли). Общее количество пациентов, включенных в анализ, составило 45 человек.
Классификация проводилась для групп 1 - неблагоприятный исход, 0 - благоприятный исход.
Дискриминантный анализ включал следующие этапы: первичный отбор признаков для построения модели, набор обучающей выборки (группы пациентов, у которых регистрируются отобранные признаки), отбор информативных признаков и формирование на их основе группы дифференциальных функций, проверка качества полученной модели. Наиболее значимые прогностические показатели представлены в таблице 1. Общая кальпаиновая активность (XI), Химотрипсинподобная тотальная активность протеасом (Х2), Активность 26S пула протеасом (Х3) Активность 20S пула протеасом (Х4) Содержание субъединиц сумма α (Х5) Содержание субъединиц сумма α (Х5) Содержание субъединицы LMP7 (Х6) Содержание субъединицы LMP2 (Х7) Содержание субъединицы РА28β (Х8) Содержание субъединицы Rpt6 (Х9) Возраст пациентов (Х10).
Оценку качества полученных функций проводили на 20 пациентах, не включенных в основную выборку. Чувствительность и специфичность полученной дискриминантной модели составили, соответственно, 67% и 96%.
Клинические примеры
Пример 1: Больная Н., 64 года, поступила в торако-абдоминальное отделение Томского НИИ онкологии 07.11.2012 с жалобами на боли в эпигастральной области, отсутствие аппетита. Пациентке была проведена видиогастроскопия с биопсией из слизистой оболочки для верификации диагноза. Гистологическое заключение: аденокарцинома желудка низкой степени гистологической дифференцировки. Для определения прогноза исхода у данной пациентки была использована разработанная математическая модель прогноза исхода. При исследовании получены следующие значения показателей Х1-Х10:
X1=35⋅103 Ед./мг белка;
Х2=152⋅103 Ед./мг белка;
Х3=175⋅103 Ед./мг белка;
Х4=144,8⋅103 Ед./мг белка;
Х5=43,62%;
Х6=118,63%;
Х7=87,57%;
Х8=153,96%;
Х9=156,22%;
X 10=64 года.
На первом этапе проводился расчет дискриминантных функций Y1 и Y2 с учетом показателей у данной больной.
Y1=-0,015*35,0+0,006*152,0+0,085*175,0+0,011*144,8+0,083*43,62+0,006*118,63+0,100*87,57+0,087*153,96+0,066*156,22+0,681 *64-45,698=51,53
Y2=-0,017*35-0,006*152,0+0,146*175,0+0,004*144,8+0,122*43,62+0,012*118,63+0,123*87,57+0,098*153,96+0,102*156,22+0,831 *64-74,476=51,89
При расчете дискриминантных функций выяснилось, что Y1<Y2. Таким образом, пациентка классифицируется в группу «высокий прогноз неблагоприятного исхода», с уровнем значимости р<0,05, что означает высокий прогноз неблагоприятного исхода у данной пациентки.
Дальнейшее наблюдение за пациенткой показало, что 18.01.2013 она умерла.
Пример 2: Больная Т., 50 лет, поступила в торако-абдоминальное отделение Томского НИИ онкологии 25.09.2013 с жалобами на боли в эпигастральной области, отсутствие аппетита, нарушения пищеварения. Пациентке была проведена видеогастроскопия с биопсией из слизистой оболочки для верификации диагноза. Гистологическое заключение: аденокарцинома желудка высокой степени гистологической дифференцировки. Для определения прогноза исхода у данной пациентки была использована разработанная математическая модель прогноза исхода. При исследовании получены следующие значения показателей Х1-Х10:
X1=25,31⋅103 Ед./мг белка;
Х2=157,84⋅103 Ед./мг белка;
Х3=92,86⋅103 Ед./мг белка;
Х4=35,19⋅103 Ед./мг белка;
Х5=38,15%;
Х6=158,52%;
Х7=116,85%;
Х8=174,14%;
Х9=215,48%;
X 10=50 лет.
На первом этапе проводился расчет дискриминантных функций Y1 и Y2 с учетом показателей у данной больной.
Y1=-0,015*25,31+0,006*157,84+0,085*92,86+0,011*35,19+0,083*38,15+0,006*158,52+0,100*116,85+0,087*174,14+0,066*215,48+0,681*50-45,698=42,35
Y2=-0,017*25,31-0,006*157,84+0,146*92,86+0,004*35,19+0,122*38,15+0,012*158,52+0,123*116,85+0,098*174,14+0,102*215,48+0,831*50-74,476=39,37
При расчете дискриминантных функций выяснилось, что Y1>Y2. Таким образом, пациентка классифицируется в группу «низкий прогноз неблагоприятного исхода», с уровнем значимости р<0,05, что означает низкий прогноз неблагоприятного исхода у данной пациентки.
В настоящее время пациентка жива, данных за рецидив и метастазирование не получено.
Таким образом, разработанный способ позволяет объективизировать критерии прогноза исхода у больных РЖ, а также с высокой долей чувствительности и специфичности прогнозировать у них развитие исхода, что в свою очередь позволяет планировать адекватный объем лечения в рамках послеоперационной терапии РЖ.
Источники информации
1. Злокачественные новообразования в России в 2013 году (заболеваемость и смертность) [текст] // Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой / М.: МНИОИ им. П.А. Герцена филиал ФГБУ «ФМИЦ им. П.А. Герцена» Минздрава России. 2015. - 250 с.
2. Множественность форм протеасомы и некоторые подходы к их разделению / Е.Б. Абрамова, Т.М. Астахова, П.А. Ерохов и др. // Известия РАН. Серия биологическая. - 2004. -№2. - С. 150-156.
3. Пат. 2445632, Российская Федерация, МПК G01N 33/53, G01N 33/68. Способ прогнозирования метастазов у больных раком желудка / Е.М. Непомнящая [и др.]; заявитель и патентообладатель Федеральное государственное учреждение «Ростовский научно-исследовательский онкологический институт Федерального агентства по высокотехнологичной медицинской помощи». 2010132604/15; заявл. 03.08.2010; опубл. 20.03.2012.
4. Пат. 2455924, Российская Федерация, МПК А61В 5/00, G01N 33/48. Способ прогнозирования метастазирования опухолевого процесса у больных раком желудка / А.В. Полетаева [и др.]; заявитель и патентообладатель Учреждение Российской академии наук Институт физиологии природных адаптаций Уральского отделения Российской Академии Наук. - 2011112226/14; заявл. 30.03.2011; опубл. 20.07.2012.
5. Пат. 2470308, Российская Федерация, МПК G01N 33/53. Способ прогнозирования гематогенного метастазирования при кишечном типе рака желудка / М.В. Завьялова [и др.]; заявитель и патентообладатель Федеральное государственное бюджетное учреждение «Научно-исследовательский институт онкологии» Сибирского отделения Российской академии медицинских наук, Учреждение Российской академии наук Институт молекулярной биологии им. В.А. Энгельгарда РАН. - 2011134537/15; заявл. 17.08.2011; опубл. 20.12.2012.
6. Пути улучшения результатов лечения больных раком желудка IV стадии [текст] / В.И. Чиссов, Л.А. Вашакмадзе, А.В. Бутенко и др. // Сибирский онкологический журнал. - 2005. - №2 (14). - С. 3-7.
7. Скоропад, В.Ю. Метахромные злокачественные опухоли у больных, радикально оперированных по поводу рака желудка [текст] / В.Ю. Скоропад, Б.А. Бердов, И.Г. Козлов // Сибирский онкологический журнал. - 2010. - №6(42). - С. 5-11.
8. Спирина, Л.В. Роль внутриклеточного специфического протеолиза в онкогенезе [текст] / Л.В. Спирина, И.В. Кондакова // Вопросы онкологии. - 2008. - Т. 54, №6. - С. 690-694.
9. Calpain-2 expression is associated with response to platinum based chemotherapy, progression-free and overall survival in ovarian cancer / S.J. Storr, S. Safuan, C.M. Woolston, et al. // J Cell Mol Med. - 2012. - Vol. 16, №.10. - P. 2422-2428.
10. Expression of the calpain system is associated with poor clinical outcome in gastro-oesophageal adenocarcinomas / S.J. Storr, X. Pu, J. Davis, et al. // J Gastroenterol. - 2013. - [Epub ahead of print].
11. Helicobacter pylori CagA targets gastric tumor suppressor RUNX3 for proteasome-mediated degradation / Y.H. Tsang, A. Lamb, J. Romero-Gallo et al. // Oncogene. - 2010. - Vol. 14. - P. 5643-5650.
12. Increased Muscle Proteasome Activity Correlates With Disease Severity in Gastric Cancer Patients / M. Bossola, M. Muscaritoli, P. Costelli et al. // Annals of surgery. - 2003. - Vol.237, №3. - P. 384-389.
13. 26 S proteasome-mediated production of an authentic major histocompatibility class I-restricted epitope from an intact protein substrate / Ben-Shahar S., Komlosh A., Nadav E. et al. // The J of Biol. Chem. - 1999. - Vol. 274. - №. 31. - P. 21963-21972.
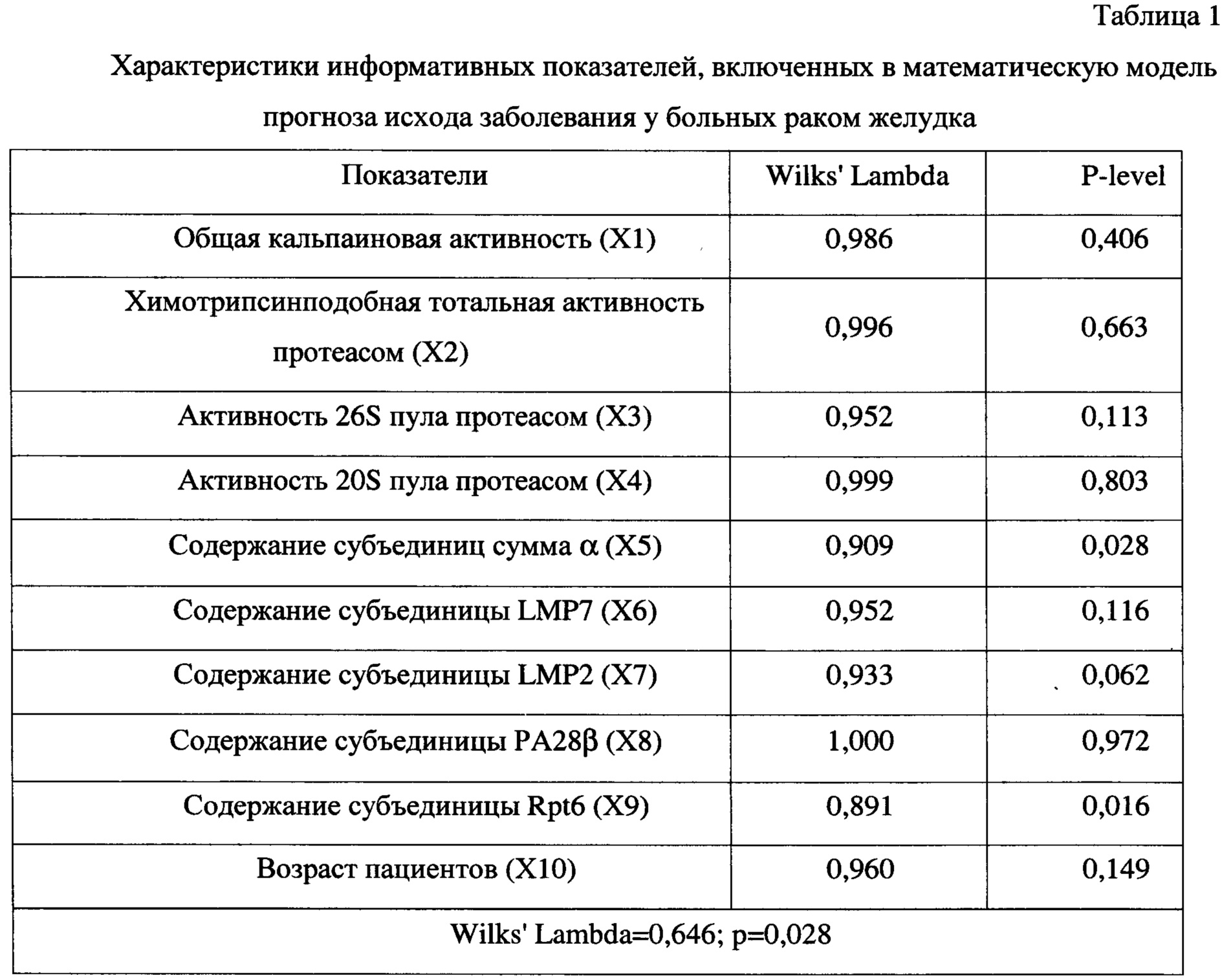
Примечание: Wilks Lambda - величина, отвечающая за выполнение условий о правомерности включения показателя в модель и значимости различий значений дискриминантной функции в группах, что является необходимым условием при создании модели; P-level - уровень значимости.

