Результат интеллектуальной деятельности: Способ получения активного начала вакцины против ротавирусной инфекции белка FliCVP6VP8
Вид РИД
Изобретение
Изобретение относится к молекулярной биологии, а именно к технологии получения вакцинных препаратов для профилактики и лечения ротавирусной инфекции, и предназначено для использования в медицине и ветеринарии.
По данным Всемирной организации здравоохранения (ВОЗ), ротавирусы являются одной из ведущих причин возникновения тяжелой диареи, приводящей к дегидратации организма у детей младшего возраста. Большинство детей инфицируется до достижения 5-летнего возраста. В результате возникновения состояния тяжелой диареи ежегодно гибнет порядка 525000 младенцев и маленьких детей, особенно в развивающихся странах (WHO, 2017 http://www.who.int/mediacentre/factsheets/fs330/en/).
Ротавирусная инфекция изменяет функционирование эпителия тонкого кишечника, результатом чего является диарея. Считается, что диарея возникает из-за малабсорбции (нарушения всасывания), что вторично приводит к деструкции энтероцитов (Kapikian A.Z., Y. Hoshino, R.M. Chanock. Rotaviruses // Fieldsvirology. - 2001. - 4 ed. - P. 1787-1833). В результате нарушения всасывания происходит перемещение непереваренных моно- и ди-сахаридов, жиров и белков в ободочную кишку. Непереваренный комок пищи является осмотически активным, ободочная кишка не способна поглотить достаточное количество воды, что приводит к диарее (Graham D.Y., M.K. Esters. Viralinfectionsoftheintestine // Gastroenterology. - 1988. - P. 566-578). Широкий спектр клинических проявлений колеблется от преходящей легкой диареи до тяжелой диареи и рвоты, вызывающих дегидратацию, нарушение электролитного баланса, шок и при отсутствии лечения смерть. Иммунитет к ротавирусной инфекции в большинстве случаев возникает в раннем детстве после перенесенного заболевания. Иммунитет нестойкий, поэтому у взрослых с низким уровнем антител заболевание может повториться. Невосприимчивость у переболевших обусловлена не только гуморальными, но и секреторными антителами.
Ротавирусы относятся к семейству Reoviridae, род Rotavirus. Ротавирион представляет собой безоболочечный, сложно организованный трехслойный капсид, который окружает геном, представленный 11 сегментами двуцепочечной РНК (Schnagl R.D., I.H. Holmes. Characteristicsofthegenomeofhumaninfantileenteritisvirus (Rotavirus) // Journalofvirology - 1976. - V. 19. - N. 1. - P. 267-270). Род ротавирус подразделяется на серологические группы A-F. Все эти группы инфицируют животных, но лишь группы А-С - человека.
Существующие в настоящее время вакцины для профилактики ротавирусной инфекции, как правило, основаны на живых аттенуированных штаммах ротавируса человеческого и/или животного происхождения, которые размножаются в кишечнике человека (RU 2246956, 1999; DK 1660123, 2016; ЕР 2453917, 2017; WO 2017106115, 2017 и другие).
Использование вакцин на основе рекомбинантных белков позволяет избежать рисков, связанных с введением вируса в организм, пусть и аттенуированного.
Как правило, для этих целей используют гибридные белки, содержащие субъединичный белок ротавируса или его иммуногенную часть, а также другой белок, адъювант используется в совокупности с гибридным белком Ротавирусный субъединичный белок выбирают из VP1, VP2, VP3, VP4, VP6, VP7, NSP1, NSP2, NSP3, NSP4 или NSP5 (US 658952, KR 20120066559, CN Китай). Назначение вакцины - индуцировать формирование нейтрализующих указанные вирусы антител и уменьшать степень заражения ими животных.
Однако проведенные исследования показали, что целесообразнее использовать не полноразмерные белки в составе гибридной конструкции, а их фрагменты - иммуногенные эпитопы, связанные гибкими мостиками, для уменьшения размера белка и облегчения его получения. Нейтрализующие IgA антитела, связываясь с белком клеточной оболочки вируса (VP8), останавливают проникновение вируса в энтероциты и индуцируют его выведение из клеток, а при связывании белка внутреннего капсида VP6 IgA-антителами непосредственно в энтероците останавливается внутриклеточное размножение вируса. Ввиду этого целесообразно использовать в качестве иммуногена, помимо фрагмента белка VP4, также белок именно внутреннего капсида (VP6), поскольку именно он остается на поверхности вирусной частицы после попадания в энтероцит (RU 2129017, 1999; CN 105085639; CN 106167518).
Среди используемых эпитопов, наиболее перспективными являются эпитопы флагеллина сальмонеллы. На данный момент флагеллин является одним из наиболее перспективных и хорошо изученных адъювантов нового поколения. Результаты исследований показывают, что рекомбинантные белки, вводимые с флагеллином, имеют повышенные иммуногенные и антигенные характеристики. Ответы на них регистрируются в более короткие сроки и вызывают более сильный клеточный и гуморальный иммунный ответ. В этих условиях перспективно использование фрагментов флагеллина в составе белков, воздействующих на РТИ. Так, предложен препарат (US 6130082), содержащий первый эпитоп h1-d структурного гена флагеллина и хотя бы один эпитоп гетерологичного организма, включенного в последовательность флагеллина таким образом, что флагеллин способен связываться с антителом к флагеллину, причем этот эпитоп помещен вместо ДНК, находящейся между естественными EcoRV сайтами гена h1-d. В вакцинную композицию входит также белок VP7 в качестве адъюванта.
Однако данный препарат показал недостаточно высокую эффективность.
Наиболее близким по технической сущности к заявляемому изобретению является разработанная ранее автором настоящего изобретения вакцина против ротавирусной инфекции групп А, В и С, содержащая в качестве активного начала гибридный белок, состоящий из состоящего из иммуногенных эпитопов белков VP6 и VP8 и адъюванта - фрагментов флагеллина, соединенных гибкими мостиками (RU 2539913, 2014). Гибридный белок получают в клетках прокариот и эукариот с использованием технологии рекомбинантной ДНК с его последующей очисткой. В результате использования эпитопов FliC1, FliC2 флагеллина в конструкции белка достигается усиление иммунного ответа. Ответы на них регистрируются в более короткие сроки и вызывают более сильный клеточный и гуморальный иммунный ответ [Balaram Р, Kien Р.K. Toll-like receptors and cytokines in immune responses to persistent mycobacterial and Salmonella infections. Int J Med Microbiol. 2009 Mar; 299(3): 177-85. doi: 10.1016 / j.ijmm. 2008.08.004. Epub 2008 Oct 8. Review.]. Гибридный белок FHCVP6VP8 получают по технологии, включающей в себя разрушение клеток штамма Е. coli - продуцента химерного белка с помощью лизирующего раствора, содержащего 20 мМ трис-HCl pH 7,5, 5 мМ ЭДТА и 1 мМ феноксиметилсульфонилфторид при pH 8.6, и ультразвука, с последующим отделением телец включения, содержащих целевой белок, центрифугированием и их промывкой 5 различных буферных растворов. Для солюбилизации белка использовали раствор (9М мочевина, 2 мМ ЭДТА, 50 мМ ТрисНCl, pH 8.6) или раствор (8М GuHCl, 2 мМ ЭДТА, 50 мМ ТрисHCl, pH 8.6), содержащий гуанидингидрохлорид. Солюбилизированные тельца включения центрифугировали при 30000 g в течение 20 мин при температуре 10°C. Рефолдинг солюбилизированного белка проводили методом 10-кратного разведения солюбилизированных телец включения в буфере для рефолдинга при температуре +4°C. Затем к раствору гибридного белка добавляли MgCl2 до концентрации 6 мМ и проводили очистку гибридного белка с использованием метода иммобилизованной металлоаффинной хроматографии (ИМАХ) с использованием сорбента Ni-НТУ сефарозы. Сорбент осаждали центрифугированием и в минимальном объеме наносили на гравитационную хроматографическую колонку, содержащую 2 мл сорбента. Элюцию проводили ступенчатым градиентом имидазола (20, 40, 100, 150, 200 и 300 мМ).
Недостатком технологии получения белка FliCVP6VP8 является высокое содержание в конечном продукте эндотоксинов, достигающее 500 нг и 200 нг других примесных белков на 1 мг целевого белка, что ограничивает его практическое использование.
Задачей, решаемой в рамках настоящего изобретения, является создание технологии, позволяющей получить белок FliCVP6VP8, очищенный от негативных примесей.
Технический результат достигается тем, что способ получения активного начала вакцины против ротавирусной инфекции белка FliCVP6VP8, включающий в себя культивирование генно-инженерного штамма Esherihia coli pET28a+flicvp6vp8 BL21 (DE3), дезинтеграцию клеток-продуцентов воздействием лизирующего раствора и ультразвука, с последующим центрифугированием, отделением телец включения, их промывку и солюбилизацию с использованием солюбилизирующего раствора, рефолдинг солюбилизированного белка, и многостадийную хроматографическую очистку, в котором лизис проводят при pH 8.0-8.5, перед хроматографией раствора проводят его диализ, а хроматограграфию проводят сначала на анионите HiTrap Q Sepharose FF 16/10, а затем на на гель-фильтрационной колонке с сорбентом Superdex S-100.
Целевой белок FlCVP6VP8 в результате синтеза накапливается в клетках штамма-продуцента в виде телец включения, то есть в частично денатурированном состоянии. Для ренатурации белка производили его солюбилизацию в 8М мочевине и последующий рефолдинг методом постепенного разбавления. Высокое содержание мономерной формы целевого рекомбинантного белка достигается проведением процесса рефолдинга при низкой температуре (+4°C), а также постепенным добавлением раствора солюбилизированного белка небольшими порциями в буфер для рефолдинга, что обеспечивает независимый эффективный фолдинг отдельных порций белка. Выбранный pH рефолдирующего буфера, а также последующая очистка с использованием анионообменной хроматографии объясняется изоэлектрической точкой химерного рекомбинантного белка, равной 4,63. Добавление в буфер для рефолдинга 1М аргинина, являющегося эффективным фолдирующим агентом, обеспечивало высокий выход правильно свернутого целевого белка. Для облегчения проведения последующей стадии хроматографической очистки с использованием анионообменной хроматографии проводили диализ полученного раствора ренатурированного белка.
При этом оптимально лизис клеток проводить при pH 8,0-8,5 с использованием в качестве лизирующего раствора буферного раствора, содержащего 100 мМ трис-HCl, 100 мМ NaCl, 10 мМ ЭДТА, 5% глюкозы, 1% Тритон X-114, из расчета 3 мл буфера на 1 г клеток. При этом солюбилизацию телец включения оптимально проводить в солюбилизирующем 50 мМ натрий-фосфатном буферном растворе, содержащем 150 мМ NaCl, 8М мочевины при pH 7,0. Промывку осуществляют в отмывочном растворе - 50 мМ трис-HCl, 20 мМ ЭДТА, 2% дезоксихолат натрия при pH 8,5-9,0.
Диализ раствора рефолдированного белка FliCVP6VP8 проводят, как правило, в течение 6 часов при +4°C против буферного раствора, содержащего 50 мМ натрий-фосфатный буфер, 5 мМ ЭДТА, 5% сахарозы при pH 6,5.
Анионообменную хроматографию на HiTrap Q Sepharose FF 16/10, проводят, как правило, на сорбенте предварительно уравновешенным буферным раствором, содержащим 50 мМ натрий-фосфата, 5 мМ ЭДТА, 5% сахарозы при pH 6,5, элюцию осуществляли лйнейным градиентом 50 мМ натрий-фосфатного буферного раствора, содержащего 1М NaCl, 5 мМ ЭДТА, 5% сахарозы при pH 6,5-7,0, а очистку на гель-фильтрационной колонке с сорбентом Superdex S-100, проводят на колонке, предварительно уравновешенным 10-50 мМ натрий-фосфатный буферным раствором, содержащим 2% сахарозы, 0,1% полисорбата 20, pH 7,0.
Финальная стадия очистки химерного белка FliCVP6VP8 представляет собой гель-фильтрацию. Добавление в элюирующий буфер 2% сахарозы, а также 0,1% полисорбата 20 существенно (более чем на 20% по сравнению с использованием фосфатно-солевого буфера) повышает выход целевого рекомбинантного белка FliCVP6VP8, а также обеспечивает его высокую чистоту после применения данного типа хроматографии.
Заявляемая технология позволяет эффективно связывать липополисахариды, эндотоксины, а также концентрации солей, превышающие физиологгические значения, что также позволило эффективно снизить количество примесных ДНК и белков штамма-продуцента.
Сущность и промышленная применимость заявляемого белка иллюстрируются следующими примерами.
Пример 1.Очистка химерного рекомбинантного белка FliCVP6VP8
1.1. Разрушение клеток штамма-продуцента химерного белка FliCVP6VP8
Сконцентрированную влажную клеточную биомассу штамма-продуцента Е. coli pET28a+flicvp6vp8 BL21 (DE3) рекомбинантного белка FliCVP6VP8 ресуспендировали в лизирующем буфере (100 мМ трис-HCl, 100 мМ NaCl, 10 мМ ЭДТА, 5% глюкоза, 1% Тритон Х-114, pH 8,0-8,5) из расчета 3 мл буфера на 1 г клеток. Ресуспендированную биомассу подвергали разрушению с помощью ультразвука.
Обработку ультразвуком проводили с помощью ультразвукового дезинтегратора UP400S или Model W225R (Heat System, Ultrasonics Inc.) на льду при следующих условиях:
- время импульса - 20 сек;
- время паузы между импульсами - 40 сек;
- амплитуда 40%;
- время озвучивания - 20 мин при температуре 10°C.
Тельца включения осаждали центрифугированием в течение 30 минут при 20000g, +8°C. Полученные тельца включения хранили при температуре -70°C.
1.2. Отмывка телец включения, содержащих химерный рекомбинантный белок FliCVP6VP8
Тельца включения отмывают от примесей белка, ДНК, а также липополисахаридов штамма-продуцента следующим образом:
1. Тельца включения ресуспендировали в отмывочном растворе 1 (50 мМ трис-HCl, 20 мМ ЭДТА, 2% дезоксихолат натрия, pH 8,7). Инкубировали в течение 30 минут при комнатной температуре при постоянном перемешивании. Центрифугировали в течение 30 минут при 20000g, +8°C. После центрифугирования супернатант удаляли.
2. Тельца включения ресуспендировали в отмывочном растворе 2 (50 мМ трис-HCl, 20 мМ ЭДТА, 1% дезоксихолат натрия, pH 8,8). Инкубировали в течение 30 минут при комнатной температуре при постоянном перемешивании. Центрифугировали в течение 30 минут при 20000g, +8°C. После центрифугирования супернатант удаляли
3. Тельца включения ресуспендировали в отмывочном растворе 3 (50 мМ трис-HCl, 20 мМ ЭДТА, pH 9,0). Инкубировали в течение 30 минут при комнатной температуре при постоянном перемешивании. Центрифугировали в течение 30 минут при 20000g, +4°C. После центрифугирования супернатант удаляли. Процедуру повторяли дважды.
4. Тельца включения ресуспендировали в стерильной дистиллированной воде. Инкубировали в течение 30 минут при комнатной температуре при постоянном перемешивании. Центрифугировали в течение 30 минут при 20000g, +8°C. После центрифугирования супернатант удаляли.
Отмытые тельца включения хранили при -70°C.
1.3. Солюбилизация телец включения
Брали 5 г телец включения. Солюбилизацию телец включения проводили при постоянном перешивании при комнатной температуре в течение 1 часа в 15 мл - 50 мМ натрий-фосфатного буферного раствора, содержащего 150 мМ NaCl, 8М мочевины при pH 7,0.
Солюбилизированный белок FliCVP6VP8 фильтровали через капсульный фильтр с размером пор 0,45 мкм. В результате получали 15 мл солюбилизированного рекомбинантного белка FliCVP6VP8.
1.4. Рефординг рекомбинантного белка FliCVP6VP8
Рефолдинг солюбилизированного белка FliCVP6VP8 проводили методом разведения в 50 мМ натрий-фосфатного буферного раствора, содержащего 1М L-аргинин, 5 мМ ЭДТА при pH 7,0. Процедуру проводили при +4°C. Солюбилизированный белок для рефолдинга небольшими порциями (по 3-5 мл) добавляли в буферный раствор с интервалами в 1 час. После добавления последней порции солюбилизированного белка инкубировали в течение 1 часа при +4°C.
Затем проводили диализ раствора рефолдированного белка FliCVP6VP8 в течение 6 часов при +4°C против буфера, содержащего 50 мМ натрий-фосфатный буфер, 5 мМ ЭДТА, 5% сахарозы при pH 6,5.
Результаты анализировали с помощью электрофореза в ПААГ денатурирующих нередуцирующих условиях, концентрацию белка измеряли методом Лоури.
В результате рефолдинга получали 650 мл раствора белка, концентрация целевого белка FliCVP6VP8 0,2 мг/мл, содержание мономерного рекомбинантного FliCVP6VP8 87%.
1.5. Хроматографическая очистка рекомбинантного белка FliCVP6VP8 с помощью анионообменной хроматографии
Рефолдированный белок FliCVP6VP8 подвергали первой стадии очистки с использованием анионообменной хроматографии. Раствор рефолдированного белка наносили на колонку HiTrap Q Sepharose FF 16/10 (GE, США), предварительно уравновешенную для нанесения 50 мМ натрий-фосфатным буферным раствором, содержащим 5 мМ ЭДТА, 5% сахарозы при pH 6,5. Элюцию осуществляли линейным градиентом NaCl с помощью 50 мМ натрий-фосфатного буферного раствора, содержащего 1М NaCl, 5 мМ ЭДТА, 5% сахарозы при pH 6,8.
Белок элюируется одним пиком. Полученный на данной стадии белок анализировали с помощью электрофореза в ПААГ в денатурирующих условиях по Леммли, концентрацию белка измеряли методом Лоури. Чистота полученного белка на данной стадии составляла 96%. Выход рекомбинантного белка FliCVP6VP8 60 мг с концентрацией 3 мг/мл. Далее рекомбинантный белок, полученный после проведения данной стадии, подвергали гель-фильтрации.
1.6. Хроматографическая очистка рекомбинантного белка FliCVP6VP8 с помощью гель-фильтрации
Полученный после стадии анионообменной хроматографии рекомбинантный белок FliCVP6VP8 подвергали очистке на гель-фильтрационной колонке XK26/60 с сорбентом Superdex S-100, предварительно уравновешенным 10-50 мМ натрий-фосфатным буферным раствором, содержащим 2% сахарозы, 0,1% полисорбата 20 при pH 7,0. Хроматографический процесс проводили при скорости 1,0 мл/мин. Белок элюируется одним пиком. Добавление 2% сахарозы, а также 0,1% полисорбата 20 в элюирующий буферный раствор на 24% по сравнению с использованием фосфатно-солевого буферного раствора повышает выход целевого рекомбинантного белка FliCVP6VP8, а также обеспечивает его высокую чистоту после применения данного типа хроматографии. Полученный на данной стадии белок анализировали с помощью электрофореза в ПААГ в дентурирующих условиях по Леммли, концентрацию белка измеряли методом Лоури. Чистота полученного рекомбинантного белка FliCVP6VP8 составляет 99,2%. Содержание эндотоксинов 4,8 едЭ, ДНК штамма-продуцента 480 нг, остаточный белок 160 нг на 1 мг рекомбинантного белка FliCVP6VP8. Выход белка составляет 48 мг с концентрацией не менее 1 мг/мл.
Пример 2. Изучение протективной активности провиротавирусной вакцины на основе химерного белка FliCVP6VP8
2.1. Препараты для иммунизации
Препарат - «Вакцина против ротавирусной инфекции, рекомбинантная», раствор для внутримышечного введения, 0,04 мг/мл».
Вакцина представляет собой раствор, состоящий из химерного рекомбинантного белка FliCVP6VP8, полученного методом рекомбинантных ДНК технологий на культуре клеток Е. coli, трансформированных путем включения в их геном гена, кодирующего антиген, состоящий из иммуногенных эпитопов поверхностных белков ротавируса - VP6, VP8, а также фрагмента флагеллина Salmonella typhimurium. Одна ампула препарата содержит: активный компонент - рекомбинантный белок FliCVP6VP8 0,02 мг; вспомогательные компоненты маннитол (ЕР, Panreac, 142067) - 25,0 мг; натрия сукцинат (EP/USP, Sigma, 150-90-3) - 0,36 мг; полисорбат 20 (ЕР, Sigma, 9005-64-5) - 0,05 мг; вода для инъекций до 0,5 мл.
Препарат - «Вакцина против ротавирусной инфекции, рекомбинантная», раствор для интраназального введения, 0,2 мг/мл».
Вакцина представляет собой раствор, состоящий из химерного рекомбинантного белка FliCVP6VP8, полученного методом рекомбинантных ДНК технологий на культуре клеток Е.coli, трансформированных путем включения в их геном гена, кодирующего антиген, состоящий из иммуногенных эпитопов поверхностных белков ротавируса - VP6, VP8, а также фрагмента флагеллина Salmonella typhimurium. Одна ампула препарата содержит: активный компонент - рекомбинантный белок FliCVP6VP8 0,02 мг; вспомогательные компоненты маннитол (EP, Panreac, 142067) - 5,0 мг; натрия сукцинат (EP/USP, Sigma, 150-90-3) - 0,072 мг; полисорбат 20 (ЕР, Sigma, 9005-64-5) - 0,01 мг; вода для инъекций до 0,1 мл.
В качестве препарата сравнения использовали моновалентную живую ротавирусную вакцину для орального применения Rotarix® (GlaxoSmithKline) (серия 81/234, срок годности до XII-2017).
Rotarix® представляет собой жидкую живую моновалентную вакцину аттенуированного штамма человеческого ротавируса RIX4414 (G1 и не-G1 серотипы: G2, G3, G4, G9), культивируемого на клетках Веро. Предназначен для профилактики ротавирусной инфекции. Суспензия для приема внутрь, 1.5 мл/1 доза в полиэтиленовой тубе.
Состав:
1 доза (1,5 мл) содержит: живой ослабленный ротавирус человека (штамм RIX4414), не менее 106 ТЦД50.
Вспомогательные вещества: сахароза, динатрияадипат, среда DMEM, вода стерильная.
Способ применения и дозы:
Дозирование: курс вакцинации состоит из 2 доз. Первую дозу можно применять у детей в возрасте с 6 нед. Интервал между применением 1-й и 2-й дозы должен быть не менее 4 нед. Курс вакцинации следует завершить до достижения ребенком возраста 24 нед.
В качестве контрольного вещества использовали физиологический раствор (0,9% раствор хлорида натрия).
2.1. Лабораторные животные
В экспериментах использовали самок мышей линии BALB/c 9-12-недельного возраста, которых содержали в стандартном виварии. Мыши поступили из питомника РАМН «Рапполово» Ленинградской области.
Животных содержали в соответствии с правилами, принятыми в Европейской конвенции по защите позвоночных животных (Страсбург, 1986 г.). Мыши находились по 10 особей в пластиковых клетках фирмы VELAZ на подстилке из мелкой древесной стружки.
Кормление животных - дважды в день.
Для проверки антигенной активности белка FliCVP6VP8 мышей иммунизировали внутримышечно два раза с двухнедельными интервалами.
2.2. Иммунизация
Иммунизацию животных противоротавирусной вакциной на основе белка FliCVP6VP8 осуществляли внутримышечно и интраназально. Внутримышечную иммунизацию проводили шприцевым методом, при этом оцениваемые препараты вводили в бедро в объеме 500 мкл. После инъекции место введения обрабатывали раствором диоксида хлора (Clidox-S; Pharmacol, Naugatuck, Conn). При интраназальной иммунизации препарат вводили животному по 50 мкл в каждую ноздрю.
Препарат сравнения вводили животным перорально.
В обоих случаях схема иммунизации предусматривала либо однократное, либо двукратное введение иммунобиологических лекарственных препаратов. В последнем случае повторное введение каждого препарата осуществляли спустя 14 суток после первичной иммунизации.
Животных разделили на 8 групп, по 10 животных в каждой:

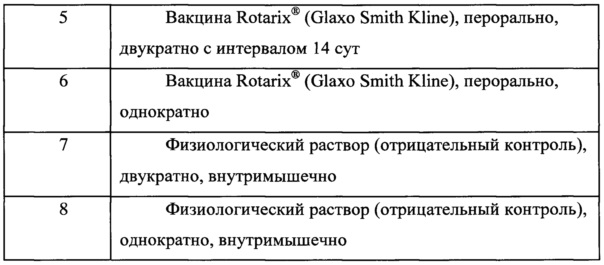
2.3. Заражение животных и получение материала на исследование
В исследовании был использован штамм EDC ротавируса мышей, депонированный в Государственной коллекции вирусов Института вирусологии им. Д.И. Ивановского под номером ГКВ М 2113. Спустя 21 сутки после последней иммунизации (однократной или двукратной) животных заражали штаммом EDC ротавируса мышей. В предварительных исследованиях было установлено, что 1 DD50 составила 1×104 БОЕ. Для заражения была взята в 100 раз превышающая 1 DD50 доза вируса (1×106 БОЕ), которую животным вводили перорально в объеме 0,2 мл.
В первые 8 сут поствакцинального периода ежедневно после заражения у животных всех подопытных групп (по 3 животных из группы, которые были помещены в отдельные клетки) производили забор фекалий для последующего определения в них содержания вирусного антигена. Каждый образец фекалий был помещен в 500 мкл буферного раствора Earle (Gibco, GrandIslsnd, N.Y.).
Спустя 8 сут после заражения производили тотальный забор крови от животных каждой группы, индивидуально от каждого животного методом декапитации. Из полученной крови готовили сыворотки, которые были в дальнейшем в качестве субстрата использованы для определения в них уровня общих (IgA, IgM и IgG) и IgG- или IgA-специфических антиротавирусных антител.
Кроме этого методом ИФА в супернатантах субстратов кишечника подопытных животных также определяли уровни ротавирус-специфических и общее количество IgM, IgG, IgA согласно стандартной методике.
Фекальная суспензия (10% [вес/объем]) проверялась на наличие ротавирусного антигена. В индивидуальную лунку 96-луночного планшета (Costar, Cambridge, Mass.) вносят 100 мкл коровьей антиротавирусной гипериммунной сыворотки в разведении 1:2000 на растворе, содержащем 1,5 мМ карбоната натрия и 3,5 мМ бикарбоната натрия. Планшеты покрывают и инкубируют во влажной атмосфере при температуре +40C. По истечении инкубационного времени планшеты промывают с помощью мультиреагентного планшетного вошера (Dynatech, Chantilly, Va) четыре раза и затем еще два раза буферным раствором, содержащим 1,73 М NaCl, 0,03 М KH2PO4, 0,13 М Na2HPO4 и 0,25% твин 20 (Sigma, St. Luis, Mo.), и два раза дистиллированной водой. Затем в каждую лунку вносят 100 мкл 0,5% раствора желатина (Sigma) и 100 мкл 0,05% раствора твина 20, планшеты оставляют при комнатной температуре на 1 ч. По истечении времени инкубации лунки четырехкратно промывают вышеописанным буферным раствором и еще два раза дистиллированной водой. В дальнейшем, в опытные лунки вносят 50 мкл исследуемого образца фекалий, а в контрольные - 50 мкл раствора, содержащего 0,5% желатин и 0,05% твин 20. Планшеты оставляют при комнатной температуре на 1 час, после чего лунки промывают буферным раствором и дистиллированной водой. Затем в каждую лунку разведенную на растворе 0,5% желатина и 0,05% твина 20 до разведения 1:2000 кроличью антиротавирусную гипериммунную сыворотку в количестве 100 мкл на лунку и планшеты инкубируют в течение 1 ч при комнатной температуре. По истечении инкубации планшеты промывают буферным раствором и дистиллированной водой и в каждую лунку вносят по 100 мкл конъюгата на основе щелочной фосфатазы и антикроличьих IgG козы (Cappel, Durham, N.C.). После инкубации в течение 1 ч при комнатной температуре планшеты промывают буфером и дистиллированной водой и затем в каждую лунку вносят по 100 мкл раствора 1 М диэтаноламина и р-нитрофенил фосфата (Kirkegaardand Perry Laboratories, Gaithersburg, Md.). После инкубации при комнатной температуре в течение 90 минут планшеты просматривали при длине волны λ=405 нм на ИФА ридере (Dynatech). Проба считалась положительной, если оптическая плотность (ОП) в экспериментальной (опытной) лунке >0,1 ОП единицы и в 2 раза превышала оптическую плотность в соответствующих контрольных лунках.
2.4. Оценка выживаемости животных
Специальная серия исследований, выполненная на 60 мышах, была спланирована с целью оценки влияния иммунизации на выживаемость инфицированных животных. В этом случае животных иммунизировали согласно выбранным схемам. По окончании иммунизации за ними наблюдали в течение трех недель, после чего заражали мышиным ротавирусом перорально в дозе, в 1000 раз превышающей 1 DD50 (1×107 БОЕ). За инфицированными животными наблюдали в течение 14 суток, ежедневно отмечая количество живых и павших особей.
Оцениваемыми показателями служили процент выживших животных в группе и уровень защиты, представляющий собой разность между показателями выживаемости в группах вакцинированных животных и контрольных группах.
Иммунизация вакциной против ротавирусной инфекции на основе белка FliCVP6VP8 как внутримышечно, так и интраназально обеспечивает надежный уровень защиты животных от заражения мышиным ротавирусом (Фиг. 1). При этом коммерческий препарат в 100% случаев препятствовал гибели животных как при однократном, так и двукратном применении. Вакцина против ротавирусной инфекции на основе химерного рекомбинантного белка FliCVP6VP8 также оказалась весьма эффективной - в случае двукратного внутримышечного, а также интраназального способов введения вакцина обеспечивала защиту 90% инфицированных мышей, а в случае однократного применения обоими исследованными способами - только 50% животных.
2.5. Оценка способности вакцинных препаратов индуцировать защиту против заражения мышиным ротавирусом EDI
Оценка способности вакцинных препаратов индуцировать защиту против заражения мышиным ротавирусом EDI, которое проводили спустя 21 сутки после окончания схемы вакцинации препаратом показала его эффективность в данном аспекте (Фиг. 1). Как следует из представленных данных, у контрольных животных (отрицательный контроль) в фекалиях достаточно интенсивно выявлялся ротавирусный антиген, причем заметных отличий в зависимости от кратности введения им физиологического раствора не выявлено. На этом фоне, применение коммерческого препарата вне зависимости от схемы иммунизации оказалось достаточно эффективным и практически полностью предупреждало размножение ротавируса в организме животных. В обоих случаях количество выявляемого ротавируса в фекалиях <10 нг/мл, то есть практически в 50-60 раз меньшее, чем в контроле. Оцениваемый препарат в этом плане не уступал коммерческому, особенно в случае его двукратного применения интервалом 14 суток - как внутримышечно, так и интраназально. При этом в обоих случаях количество определяемого ротавирусного антигена в фекалиях <10 нг/мл. Под влиянием однократного внутримышечного введения вацины на основе белка FliCVP6VP8 наблюдалось выделение ротавирусного антигена на уровне 195 нг/мл, однократного интраназального введения - 44 нг/мл, что характеризует однократное ввдение исследуемого препарата как менее эффективное по сравнению с двукратным.
2.6. Оценка уровня ротавирусспецифических антител IgA и IgG в сыворотках крови и содержимом кишечника
Полная защита от мышиного ротавируса после его перорального введения иммунизированным как внутримышечно, так и интраназально вакциной против ротавирусной инфекции на основе рекомбинантного белка FliCVP6VP8 животным ассоциировалась с продукцией вирусспецифических IgA в содержимом кишечника животных и в сыворотке крови, а также вирусспецифических IgG в этих же биосубстратах (Фиг. 3 и Фиг. 4). При введении вакцины против ротавирусной инфекции на основе рекомбинантного белка FliCVP6VP8 в сыворотке крови наблюдается уровень ротавирусспецифических антител, как IgA, так и IgG, сопоставимый с уровнем, наблюдаемым при введении коммерческого препарата - живой вакцины против ротавирусной инфекции Rotarix. При введении вакцины против ротавирусной инфекции на основе рекомбинантного белка FliCVP6VP8 в содержимом кишечника наблюдается более высокий уровень ротавирус специфических антител IgA, по сравнению с уровнем, наблюдаемым при введении коммерческого препарата - живой вакцины против ротавирусной инфекции Rotarix, при этом уровень IgG сопоставим при иммунизации кандидатной вакциной по сравнению с коммерческим препаратом. Следует отметить, что доля ротавирус-специфических IgA существенно выше при двукратной иммунизации кандидатной вакциной против ротавирусной инфекции, тогда как доля ротавирус-специфических IgG при обеих схемах иммунизации не имеет существенных различий.
В результате использования изобретения удается получить высокий выход целевого химерного рекомбинантного белка FliCVP6VP8, освобожденного от негативных примесей. Содержание эндотоксинов в конечном белке сократилось с 500 до 5 нг на 1 мг целевого белка, а прочих примесных белков с 200 до 100 нг на 1 мг целевого белка.
Полученный белок показал высокую эффективность для профилактики и лечения ротавирусной инфекции.

