Результат интеллектуальной деятельности: КАТИОННЫЕ ЭМУЛЬСИИ МАСЛО-В-ВОДЕ
Вид РИД
Изобретение
РОДСТВЕННЫЕ ЗАЯВКИ
[001] Настоящая заявка претендует на приоритет предварительной заявки США 61/50109, поданной 6 июля 2011 г., предварительной заявки США 61/545936, поданной 11 октября 2011 г. и предварительной заявки США 61/585641, поданной 11 января 2012 г., содержание которых включено в настоящее описание во всей своей полноте в виде ссылки.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
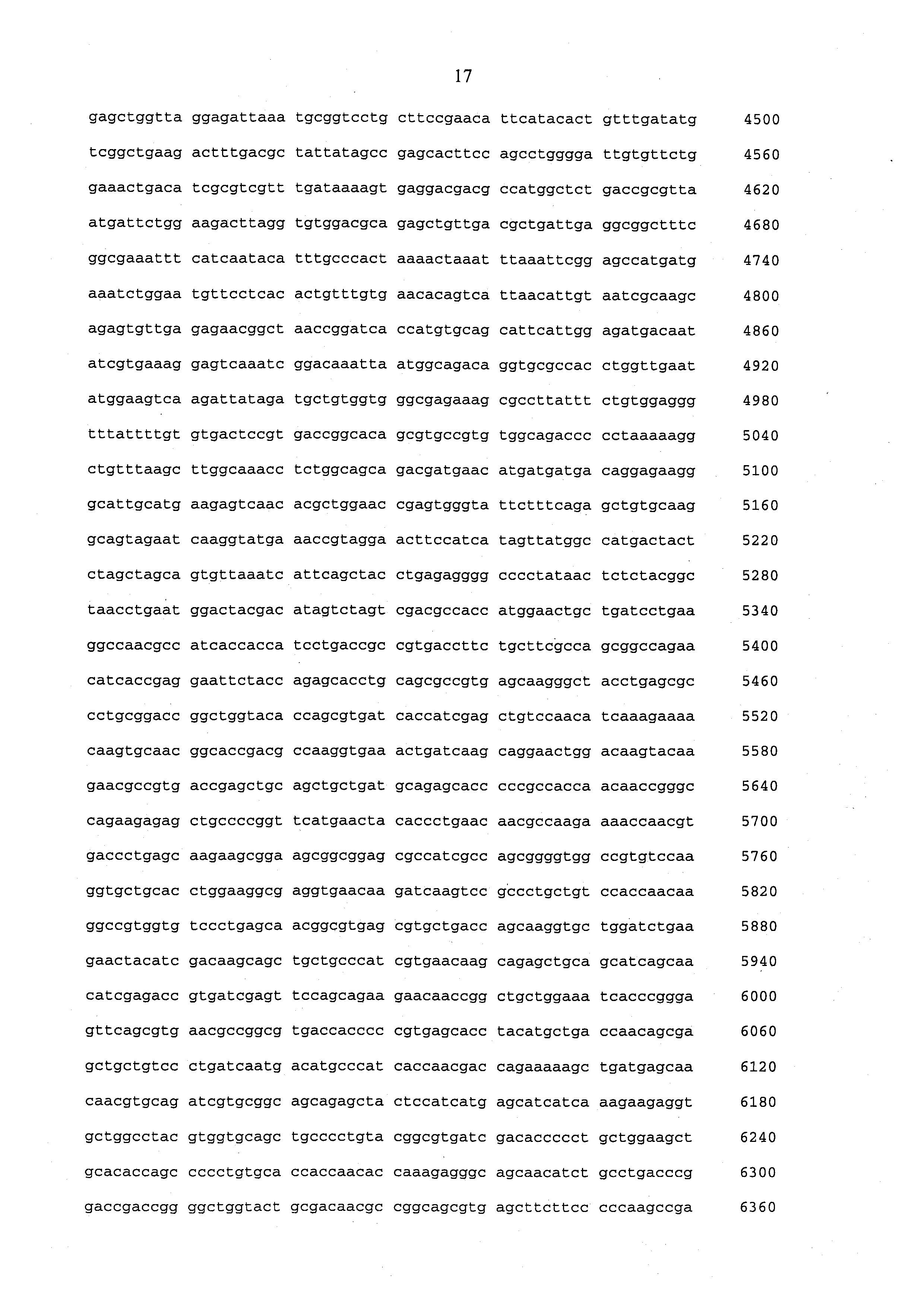
[002] Настоящая заявка содержит список последовательностей, который подан в формате ASCII через систему on-line подачи заявок EFS-Web и таким образом включен в настоящее описание во всей своей полноте в виде ссылки. Указанная ASCII копия, созданная 5 июля 2012 г., представлена в файле PAT54691.txt, размер которого составляет 424203 байт.
УРОВЕНЬ ТЕХНИКИ
[003] Терапевтические средства на основе нуклеиновых кислот являются потенциальными средствами для лечения заболеваний, от наследственных заболеваний до приобретенных состояний, таких как рак, инфекционные заболевания (СПИД), сердечные заболевания, артрит и нейродегенеративные расстройства (например, болезни Паркинсона и Альцгеймера). Можно доставлять не только функциональные гены для восстановления генетического дефицита или стимулирования экспрессии продуктов экзогенных генов, но также можно доставлять нуклеиновую кислоту для подавления экспрессии эндогенных генов с целью обеспечения терапевтического эффекта. Подавление экспрессии генов может происходить опосредованно, например, при участии антисмысловых олигонуклеотидов, двухнитевых РНК (например, миРНК, микроРНК) или рибосом.
[004] Ключевым этапом такой терапии является доставка молекул нуклеиновых кислот в клетки in vivo. Однако in vivo доставка молекул нуклеиновых кислот, в частности, молекул РНК, связана с некоторыми техническими сложностями. Во-первых, из-за воздействия клеточных и сывороточных нуклеаз время полувыведения РНК, вводимой in vivo, составляет всего около 70 секунд (см., например, Kurreck, Eur. J. Bioch. 270:1628-44 (2003)). Были предприняты попытки увеличить стабильность инъецированной РНК за счет химических модификаций; однако в некоторых случаях химические модификации приводят к увеличению цитотоксических эффектов или потере или ослаблению функции. В одном из конкретных примеров клетки были восприимчивы к дозам дуплекса интерферирующих РНК, в котором каждый второй фосфат заменяли фосфоротиоатом (Harborth, et al., Antisense Nucleic Acid Drug Rev. 13(2):83-105 (2003)). Соответственно, существует необходимость в разработке систем доставки, которые могут доставлять in vivo количество молекул нуклеиновых кислот (в частности, молекул РНК), достаточное для стимулирования терапевтического ответа, которые при этом не являются токсичными для хозяина.
[005] Вакцины на основе нуклеиновых кислот являются многообещающим подходом к вакцинации. Например, внутримышечная (IM) иммунизация плазмидной ДНК, кодирующей антиген, может индуцировать клеточный и гуморальный иммунные ответы и защитить от инфицирования. ДНК-вакцины имеют преимущества по сравнению с традиционными вакцинами на основе белковых антигенов или ослабленных патогенов. Например, в отличие от белковых вакцин, вакцины на основе ДНК могут быть более эффективными для продуцирования правильно свернутых антигенов в их нативной конформации и для генерации клеточного иммунного ответа. К тому же ДНК-вакцины свободны от некоторых проблем, связанных с безопасностью, которые возникают в случае применения убитых или ослабленных патогенов. Например, препараты на основе убитых вирусов могут содержать остаточное количество живых вирусов, а ослабленные вирусы могут мутировать и восстановить свой патогенный фенотип.
[006] Одно из ограничений для вакцин на основе нуклеиновых кислот заключается в том, что для получения эффективных иммунных ответов у приматов, не относящихся к человеку, и у людей обычно требуются большие дозы нуклеиновой кислоты. Следовательно, для усиления эффективности вакцин на основе нуклеиновых кислот требуются системы доставки и адъюванты. Для введения молекул нуклеиновой кислоты в клетку были разработаны различные способы, такие как кальций-фосфатная трансфекция, полипреновая трансфекция, слияние протопластов, электропорация, микроинъекция и липофекция.
[007] Для доставки генов в клетку катионные липиды составляли в виде липосом. Кроме того, для доставки в клетки молекул ДНК были разработаны эмульсии на основе катионных липидов. См., например, Kim, et al., International Journal of Pharmaceutics, 295, 35-45 (2005).
[008] Ott et al. (Journal of Controlled Release, volume 79, pages 1-5, 2002) описывает подход, в котором используется катионная субмикронная эмульсия в качестве системы/адъюванта для ДНК. Подход применения субмикронной эмульсии основан на использовании MF59, эффективном адъюванте сквален-в-воде, который является компонентом, одобренного для продажи продукта Fluad®. Для облегчения межклеточной доставки плазмидной ДНК используется 1,2-диолеоил-3-триметиламмоний-пропан (DOTAP).
[009] Yi et al. (Pharmaceutical Research, 17, 314-320 (2000)) описывает катионные эмульсии масло-в-воде, в которых в качестве катионного липида используются соевое масло и DOTAP. Некоторые эмульсии также содержат холестерин, DOPE и полимерные липиды. Было показано, что эмульсии усиливают эффективность in vitro трансфекции ДНК в присутствии сыворотки в количестве вплоть 90%. Средний размер частиц эмульсии находился в пределах от 181 нм до 344 нм, и размер частиц увеличивался после разбавления эмульсий буфером PBS.
[010] Kim et al. (Pharmaceutical Research, vol. 18, pages 54-60, 2001) и Chung et al. (Journal of Controlled Release, volume 71, pages 339-350, 2001) описывают различные эмульсии масло-в-воде, которые использовались для усиления эффективности in vitro и in vivo трансфекции молекул ДНК. Среди протестированных катионных липидов DOTAP чаще всего образовывал стабильную эмульсию, эффективную для доставки ДНК. Среди протестированных масел сквален, легкое минеральное масло, и масло бобов жожоба образовывали стабильные эмульсии с небольшими частицами. Было показано, что эффективность in vitro трансфекции коррелировала со стабильностью эмульсий (например, эмульсия, образованная скваленом в концентрации 100 мг/мл и DOTAP в концентрации 24 мг/мл, демонстрировала высокую эффективность в in vitro трансфекции). Эту эмульсию готовили сначала смешиванием катионного липида с водой для образования липосомной суспензии (при обработке ультразвуком). Затем липосомы добавляли в масло (такое как сквален), и смесь обрабатывали ультразвуком до образования эмульсии масло-в-воде.
[011] Молекулы РНК, кодирующие антиген или его производные, также могут быть использованы в качестве вакцин. РНК-вакцины обладают некоторыми преимуществами по сравнению с ДНК-вакцинами. Однако по сравнению с ДНК-вакцинами, РНК-вакцинам было уделено относительно незначительное внимание. РНК легко подвергаются расщеплению нуклеазами при их введении в качестве терапевтического средства или вакцины. Кроме того, РНК не транспортируются активно в клетки. См., например, Vajdy, M., et al., Mucosal adjuvants and delivery systems for protein, DNA- and RNA-based vaccines, Immunol Cell Biol, 2004, 82(6): p. 617-27.
[012] Следовательно, имеется потребность в предоставлении систем для доставки молекул нуклеиновых кислот или других отрицательно заряженных молекул. Такие системы доставки являются полезными для вакцин на основе нуклеиновых кислот, в частности, РНК-вакцин.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[013] Изобретение относится к катионным эмульсиям масло-в-воде, которые содержат высокие концентрации катионных липидов и имеют определенное соотношение масло:липид. Масло и катионный липид являются отдельными компонентами эмульсий, при этом масло предпочтительно не является ионным. Катионный липид может взаимодействовать с отрицательно заряженной молекулой, связывая таким образом молекулу с частицами эмульсии. Описанные здесь катионные эмульсии можно использовать для доставки отрицательно заряженных молекул, таких как молекулы нуклеиновых кислот (например, РНК молекула, кодирующая антиген), в клетки и для получения вакцин на основе нуклеиновых кислот.
[014] В одном из аспектов изобретение предоставляет эмульсию масло-в-воде, содержащую частицы, которые диспергированы в непрерывной водной фазе, где эмульсия отличается тем, что: (a) средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и катионный липид, при этом (i) соотношение масло:катионный липид (моль:моль) составляет по меньшей мере примерно 8:1 (моль:моль), (ii) концентрация катионного липида в указанной эмульсии оставляет по меньшей мере примерно 2,5 мМ, и (iii) при условии, что катионный липид не является DC-холестерином. Предпочтительно, эмульсия масло-в-воде является стабильной. В некоторых вариантах осуществления соотношение масло:липид (моль:моль) находится в пределах от примерно 10:1 (моль:моль) до примерно 43:1 (моль:моль). Эмульсия масло-в-воде может содержать от примерно 0,2% до примерно 8% (масс./об.) масла. В некоторых вариантах осуществления масло представляет собой сквален или сквалан.
[015] В другом аспекте настоящее изобретение предоставляет эмульсию масло-в-воде, содержащую частицы, которые диспергированы в непрерывной водной фазе, при этом эмульсия отличается тем, что: (a) средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и катионный липид, при этом (i) соотношение масло:липид (моль:моль) составляет по меньшей мере примерно 4:1 (моль:моль), (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ, (iii) содержание масла составляет от примерно 0,2% до примерно 8% (масс./об.); и (iv) при условии, что катионный липид не является DC-холестерином. Предпочтительно, эмульсия масло-в-воде является стабильной. В некоторых вариантах осуществления соотношение масло:липид (моль:моль) находится в пределах от примерно 4:1 (моль:моль) до примерно 43:1 (моль:моль). В некоторых вариантах осуществления масло представляет собой сквален или сквалан. В некоторых вариантах осуществления содержание масла составляет от 0,6% до 4% (масс./об.). В некоторых вариантах осуществления содержание масла составляет от примерно 1% до примерно 3,2% (масс./об.).
[016] Эмульсия масло-в-воде согласно этому аспекту может дополнительно содержать поверхностно-активное вещество (ПАВ), такое как неионогенное ПАВ. Предпочтительно, ПАВ не представляет собой полиэтиленгликоль (ПЭГ)-липид. ПАВ может находиться в пределах от примерно 0,01% до примерно 2,5% (масс./об.). В некоторых вариантах осуществления ПАВ представляет собой SPAN85 (сорбитана триолеат), Tween® 80 (полисорбат 80) или их комбинацию. В некоторых вариантах осуществления эмульсия масло-в-воде содержит равные количества SPAN85 (сорбитана триолеат) и Tween® 80 (полисорбат 80), например, по 0,5% (масс./об.) каждого.
[017] Предпочтительно, головная группа катионного липида содержит четвертичный амин. Например, в некоторых вариантах осуществления катионный липид выбирают из группы, состоящей из: 1,2-диолеоилокси-3-(триметиламмонио)пропан (DOTAP), 1,2-диолеоил-sn-глицеро-3-этилфосфохолин (DOEPC), N,N-диолеоил-N,N-диметиламмония хлорид (DODAC), и N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорид (DOTMA).
[018] В некоторых вариантах осуществления эмульсия отличается тем, что: (a) средний диаметр частиц эмульсии находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и DOTAP, при этом (i) соотношение масло:DOTAP (моль:моль) составляет по меньшей мере примерно 8:1 (моль:моль), и (ii) концентрация DOTAP в указанной эмульсии составляет по меньшей мере примерно 2,58 мМ (1,8 мг/мл) или находится в пределах от примерно 2,58 мМ (1,8 мг/мл) до примерно 7,16 мМ (5 мг/мл). Масло может представлять собой сквален или сквалан.
[019] В некоторых вариантах осуществления эмульсия отличается тем, что: (a) средний диаметр частиц эмульсии находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и DOTAP, при этом (i) соотношение масло:DOTAP (моль:моль) составляет по меньшей мере примерно 4:1 (моль:моль), (ii) концентрация DOTAP в указанной эмульсии составляет по меньшей примерно 2,58 мМ (1,8 мг/мл), и (iii) содержание масла составляет от примерно 0,2% до примерно 8% (масс./об.). В некоторых вариантах осуществления масло представляет собой сквален или сквалан. В некоторых вариантах осуществления концентрация DOTAP находится в пределах от примерно 2,58 мМ (1,8 мг/мл) до примерно 7,16 мМ (5 мг/мл). В некоторых вариантах осуществления содержание масла составляет от 0,6% до 4% (масс./об.). В некоторых вариантах осуществления содержание масла составляет от примерно 1% до примерно 3,2% (масс./об.).
[020] Изобретение также предоставляет способ получения эмульсии масло-в-воде, содержащей частицы, которые диспергированы в непрерывной водяной фазе, где эмульсия отличается тем, что: (a) средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и катионный липид, при этом (i) соотношение масло:катионный липид (моль:моль) составляет по меньшей мере примерно 8:1 (моль:моль), (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ, и (iii) при условии, что катионный липид не является DC-холестерином, при этом способ содержит (a) непосредственное растворение катионного липида в масле для образования масляной фазы; (b) предоставление водной фазы эмульсии; и (c) диспергирование масляной фазы в водной фазе путем гомогенизации. Чтобы облегчить процесс растворения катионного липида в масле, масло может быть нагрето до температуры от примерно 30°C до примерно 65°C. Также могут быть использованы более высокие температуры, при условии, что это не приведет к значительному разложению масла или катионного липида.
[021] Изобретение предоставляет способ получения эмульсии масло-в-воде, содержащей частицы, которые диспергированы в непрерывной водяной фазе, где эмульсия отличается тем, что: (a) средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и катионный липид, при этом (i) соотношение масло:катионный липид (моль:моль) составляет по меньшей мере примерно 4:1 (моль:моль), (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ, (iii) содержание масла составляет от примерно 0,2% до примерно 8% (масс./об.); (iv) при условии, что катионный липид не является DC-холестерином, при этом способ содержит (a) непосредственное растворение катионного липида в масле для образования масляной фазы; (b) предоставление водной фазы эмульсии; и (c) диспергирование масляной фазы в водной фазе путем гомогенизации. Чтобы облегчить процесс растворения катионного липида в масле, масло может быть нагрето до температуры от примерно 30°C до примерно 65°C. Также могут быть использованы более высокие температуры, при условии, что это не приведет к разложению масла или катионного липида.
[022] В другом аспекте изобретение предоставляет композицию, содержащую молекулу нуклеиновой кислоты (предпочтительно, молекулу РНК), находящейся в комплексе с частицей катионной эмульсии масло-в-воде, где частица содержит масло, которое находится в жидкой фазе при 25°C, и катионный липид; и (i) соотношение масло:липид (моль:моль) составляет по меньшей мере примерно 8:1 (моль:моль); (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 1,25 мМ; и (iii) при условии, что катионный липид не является DC-холестерином. Предпочтительно, средний диаметр частиц эмульсии находится в пределах от примерно 80 нм до 180 нм или от примерно 80 нм до 150 нм, или от примерно 80 нм до примерно 130 нм, и соотношение N/P композиции составляет по меньшей мере примерно 4:1, или находится в пределах от примерно 4:1 до примерно 20:1 или от примерно 4:1 до примерно 15:1. В некоторых вариантах осуществления соотношение масло:липид (моль:моль) находится в пределах от примерно 10:1 (моль:моль) до примерно 43:1 (моль:моль). Эмульсия масло-в-воде может содержать от примерно 0,1% до примерно 5% (масс./об.) масла. В некоторых вариантах осуществления масло представляет собой сквален или сквалан.
[023] В другом аспекте изобретение предоставляет композицию, содержащую молекулу нуклеиновой кислоты (предпочтительно, молекулу РНК), находящуюся в комплексе с частицей катионной эмульсии масло-в-воде, где частица содержит масло, которое находится в жидкой фазе при 25°C, и катионный липид; и (i) соотношение масло:липид (моль:моль) составляет по меньшей мере примерно 4:1 (моль:моль); (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 1,25 мМ; (iii) содержание масла составляет от примерно 0,1% до примерно 4% (масс./об.); и (iv) при условии, что катионный липид не является DC-холестерином. Предпочтительно, средний диаметр частиц эмульсии находится в пределах от примерно 80 нм до 180 нм или от примерно 80 нм до 150 нм, или от примерно 80 нм до примерно 130 нм, и соотношение N/P композиции составляет по меньшей мере примерно 4:1, или находится в пределах от примерно 4:1 до примерно 20:1 или от примерно 4:1 до примерно 15:1. В некоторых вариантах осуществления соотношение масло:липид (моль:моль) находится в пределах от примерно 4:1 (моль:моль) до примерно 43:1 (моль:моль). В некоторых вариантах осуществления масло представляет собой сквален или сквалан. В некоторых вариантах осуществления содержание масла составляет от 0,6% до 4% (масс./об.). В некоторых вариантах осуществления содержание масла составляет от примерно 1% до примерно 3,2% (масс./об.).
[024] Эмульсия масло-в-воде согласно этому аспекту может дополнительно содержать ПАВ, такое как неионогенное ПАВ. Предпочтительно, ПАВ не представляет собой полиэтиленгликоль (ПЭГ)-липид. ПАВ может находиться в пределах от примерно 0,005% до примерно 1,25% (масс./об.). В некоторых вариантах осуществления ПАВ представляет собой SPAN85 (сорбитана триолеат), Tween® 80 (полисорбат 80) или их комбинацию. В некоторых вариантах осуществления эмульсия масло-в-воде содержит равные количества SPAN85 (сорбитана триолеат) и Tween® 80 (полисорбат 80), например, 0,25% или 0,5% (масс./об.) каждого.
[025] Предпочтительно, головная группа катионного липида содержит четвертичный амин. Например, в некоторых вариантах осуществления катионный липид выбирают из группы, состоящей из: 1,2-диолеоилокси-3-(триметиламмонио)пропан (DOTAP), 1,2-диолеоил-sn-глицеро-3-этилфосфохолин (DOEPC), N,N-диолеоил-N,N-диметиламмония хлорид (DODAC) и N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорид (DOTMA).
[026] В других вариантах осуществления изобретение предоставляет композицию, содержащую молекулу нуклеиновой кислоты (предпочтительно, молекулу РНК), находящуюся в комплексе с частицей катионной эмульсии масло-в-воде, где частица содержит масло, которое находится в жидкой фазе при 25°C, и (i) соотношение масло:DOTAP (моль:моль) составляет по меньшей мере примерно 8:1 (моль:моль), (ii) концентрация DOTAP в указанной композиции составляет по меньшей мере примерно 1,29 мМ, или находится в пределах от примерно 1,29 мМ (0,9 мг/мл) до примерно 3,58 мМ (2,5 мг/мл). Масло может представлять собой сквален или сквалан. Соотношение N/P необязательно составляет по меньшей мере 4:1.
[027] В предпочтительных вариантах осуществления композиция содержит буфер (например, цитратный буфер, сукцинатный буфер, ацетатный буфер) и имеет pH в пределах от примерно 6,0 до примерно 8,0, предпочтительно от примерно 6,2 до примерно 6,8. Композиция может дополнительно содержать неорганическую соль, при этом концентрация неорганической соли предпочтительно не превышает 30 мМ. Композиция необязательно может дополнительно содержать неионный регулирующий тоничность агент и предпочтительно является изотоничной.
[028] Изобретение также предоставляет способ получения композиции, содержащей молекулу нуклеиновой кислоты (предпочтительно, молекулу РНК), находящуюся в комплексе с частицей катионной эмульсии масло-в-воде, включающий: (i) предоставление эмульсии масло-в-воде согласно тому, как описано здесь; (ii) предоставление водного раствора, содержащего молекулу РНК; и (iii) объединение эмульсии масло-в-воде, полученной на этапе (i), и водного раствора, полученного на этапе (ii), получая таким образом композицию. В некоторых вариантах осуществления катионную эмульсию масло-в-воде и раствор РНК объединяют в соотношении 1:1 (об./об.). Водный раствор, содержащий молекулу РНК, предпочтительно содержит буфер (например, цитратный буфер, сукцинатный буфер, ацетатный буфер) и может содержать неорганическую соль (например, NaCl), которая предпочтительно присутствует в количестве 20 мМ или меньше. В одном из вариантов осуществления водный раствор, содержащий молекулу РНК, содержит 2 мМ цитратного буфера и 20 мМ NaCl. Водный раствор, содержащий молекулу РНК, необязательно дополнительно содержит неионный регулирующий тоничность агент и является изотоничным. В одном из вариантов осуществления водный раствор дополнительно содержит примерно 560 мМ сахарозы. Водный раствор, содержащий молекулу РНК, необязательно дополнительно содержит полимер или неионогенное ПАВ, такое как Pluronic® F127, в количестве от примерно 0,05% до примерно 20% (масс./об.).
[029] В другом аспекте настоящее изобретение предоставляет эмульсию масло-в-воде, содержащую частицы, которые диспергированы в непрерывной водной фазе, при этом эмульсия содержит масло и катионный липид, средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм, содержание масла составляет от 0,6% до 4% (масс./об.). и концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 1,25 мМ. Предпочтительно, эмульсия масло-в-воде является стабильной. В некоторых вариантах осуществления концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ. В некоторых вариантах осуществления масло представляет собой сквален или сквалан.
[030] Эмульсия масло-в-воде согласно этому аспекту может дополнительно содержать ПАВ, такое как неионогенное ПАВ. Предпочтительно, ПАВ не представляет собой полиэтиленгликоль (ПЭГ)-липид. ПАВ может находиться в пределах от примерно 0,01% до примерно 2,5% (масс./об.). В некоторых вариантах осуществления ПАВ представляет собой SPAN85 (сорбитана триолеат), Tween® 80 (полисорбат 80) или их комбинацию. В некоторых вариантах осуществления эмульсия масло-в-воде содержит равные количества SPAN85 (сорбитана триолеат) и Tween® 80 (полисорбат 80), например, 0,25% или 0,5% (масс./об.) каждого.
[031] Предпочтительно головная группа катионного липида содержит четвертичный амин. Например, в некоторых вариантах осуществления катионный липид выбирают из группы, состоящей из: 1,2-диолеоилокси-3-(триметиламмонио)пропан (DOTAP), 1,2-диолеоил-sn-глицеро-3-этилфосфохолин (DOEPC), N,N-диолеоил-N,N-диметиламмония хлорид (DODAC) и N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорид (DOTMA).
[032] Изобретение предоставляет композицию, содержащую молекулу нуклеиновой кислоты (предпочтительно, молекулу РНК), находящуюся в комплексе с частицей эмульсии масло-в-воде, в которой частицы диспергированы в непрерывной водной фазе, где эмульсия содержит масло и катионный липид, средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм, масло находится в пределах от 0,6% до 4% (масс./об.), и концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 1,25 мМ. Предпочтительно, эмульсия масло-в-воде является стабильной. В некоторых вариантах осуществления концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ. В некоторых вариантах осуществления масло представляет собой сквален или сквалан. Соотношение N/P композиции предпочтительно составляет по меньшей мере примерно 4:1.
[033] В предпочтительных вариантах осуществления композиция содержит буфер (например, цитратный буфер, сукцинатный буфер, ацетатный буфер) и имеет pH в пределах от примерно 6,0 до примерно 8,0, предпочтительно от примерно 6,2 до примерно 6,8. Композиция может дополнительно содержать неорганическую соль, при этом концентрация неорганической соли предпочтительно не превышает 30 мМ. Композиция необязательно может дополнительно содержать неионный регулирующий тоничность агент и предпочтительно является изотоничной.
[034] Изобретение также относится к способу генерации иммунного ответа у субъекта, включающему введение нуждающемуся в этом субъекту описанной здесь композиции. Количество катионного липида, введенного субъекту (в качестве компонента композиции), при единичном применении предпочтительно не превышает 30 мг. В конкретных вариантах осуществления катионный липид представляет собой DOTAP, и общее количество DOTAP, введенное субъекту при единичном применении, не превышает примерно 24 мг или не превышает 4 мг.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
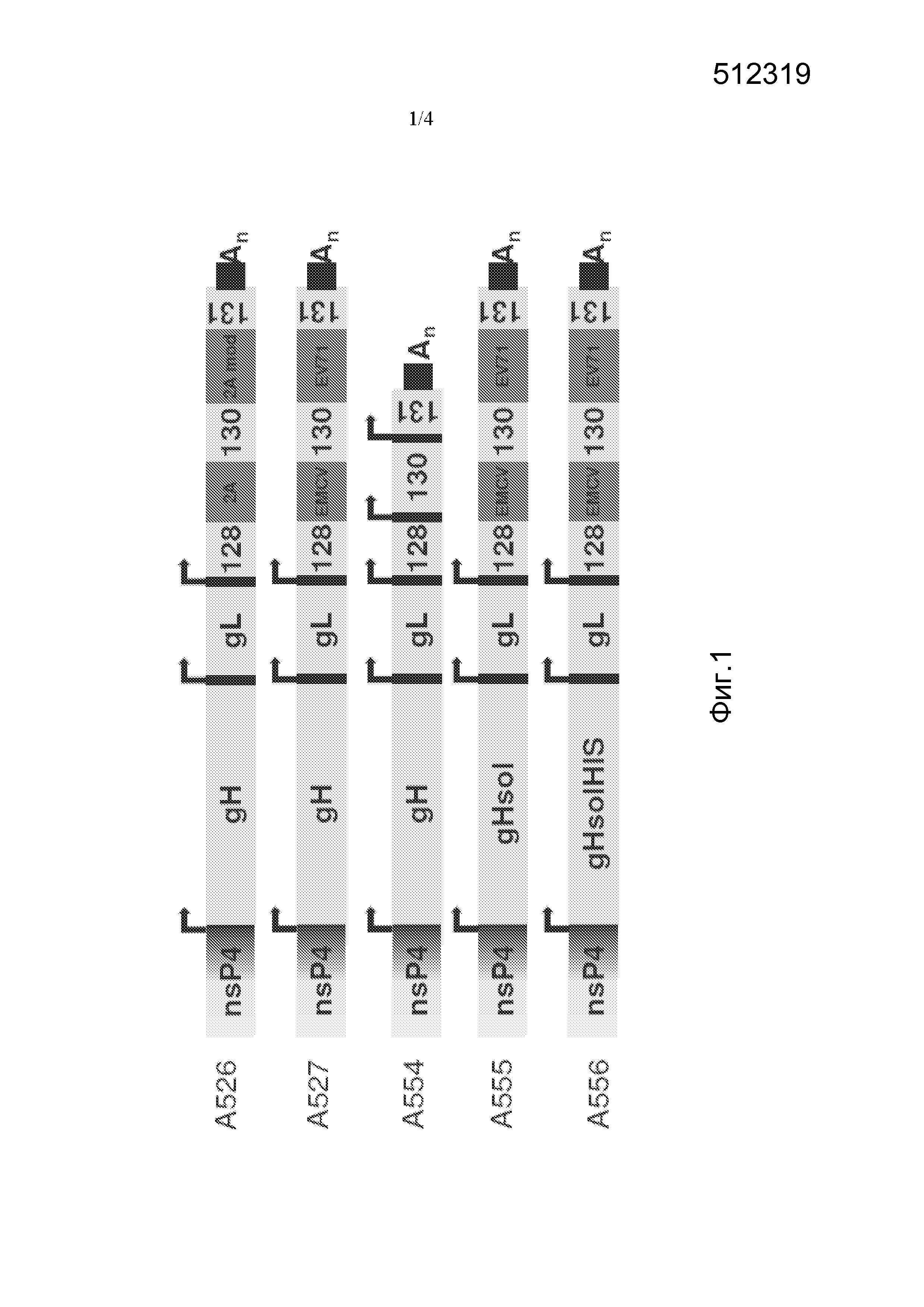
[035] Фиг. 1 представляет собой схематичную диаграмму пентацистронных РНК репликонов, A526, A527, A554, A555 и A556, которые кодируют пять белков CMV. Субгеномные промоторы обозначены стрелками, также отмечены другие регуляторные элементы.
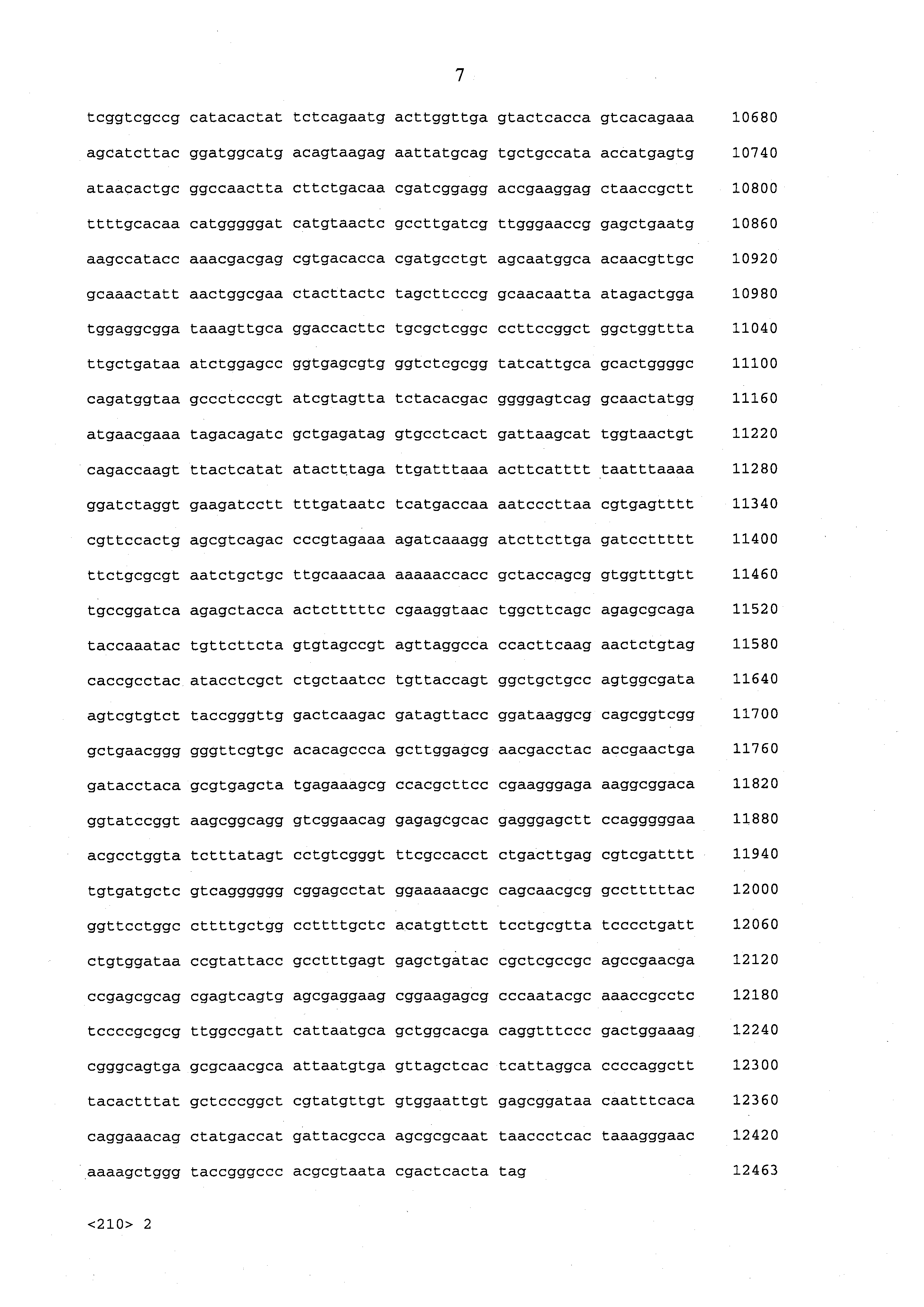
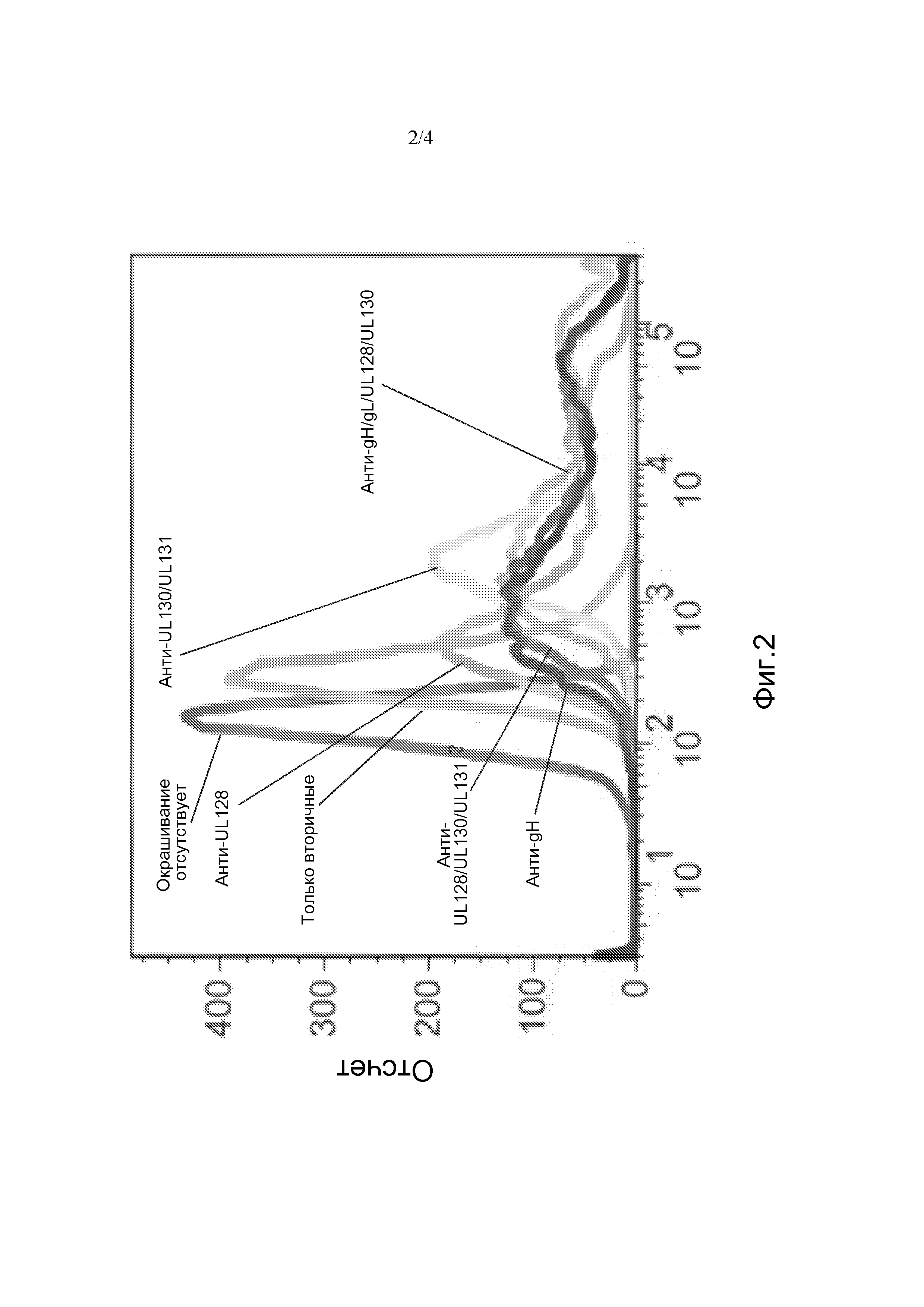
[036] Фиг. 2 представляет собой гистограмму флуоресценции, демонстрирующую, что клетки BHKV, трансфицированные РНК репликоном A527, экспрессируют пентамерный комплекс gH/gL/UL128/UL130/UL131. Окрашивание клеток осуществляли, используя антитело, которое связывается с конформационным эпитопом, присутствующим в пентамерном комплексе.
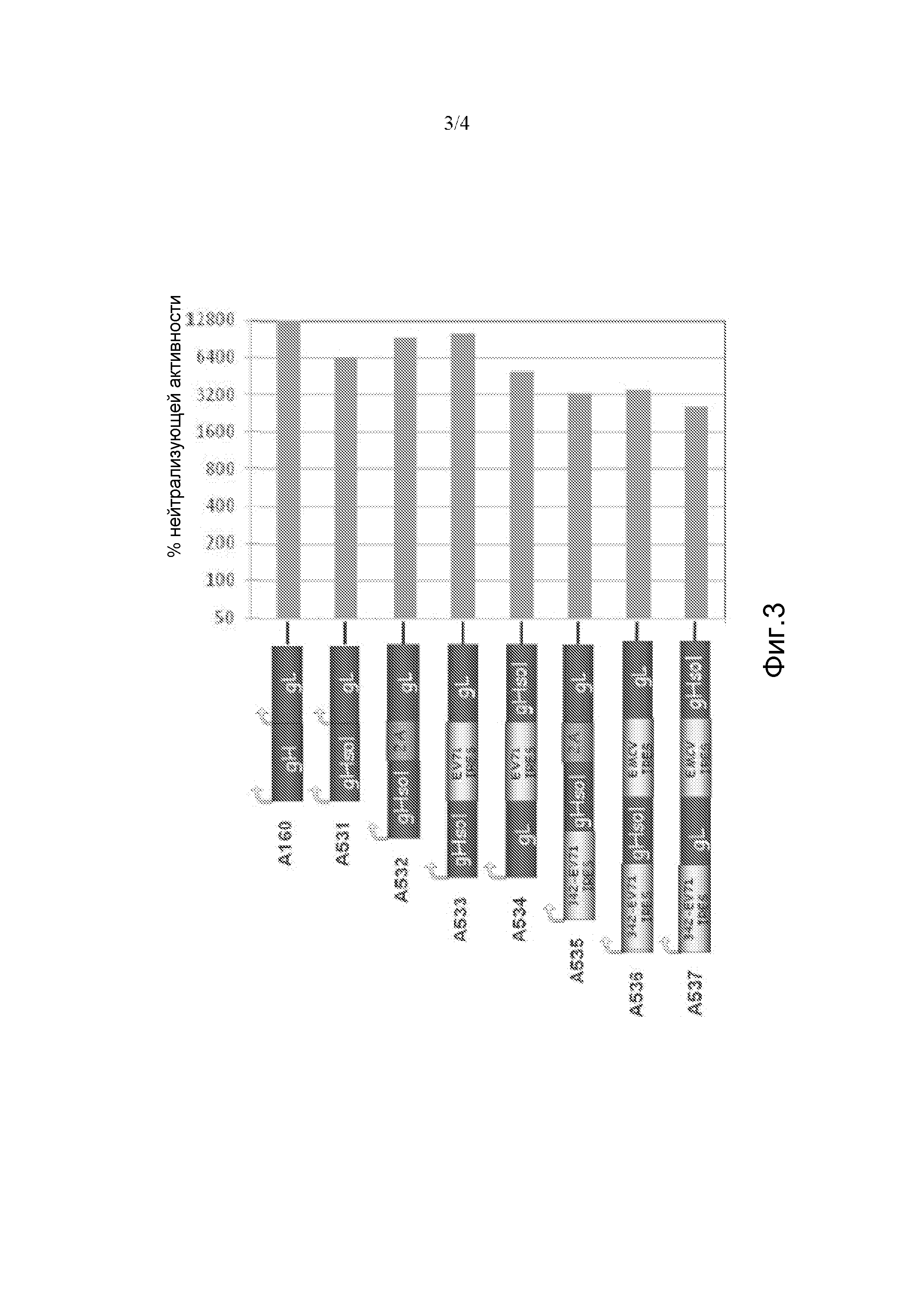
[037] Фиг. 3 представляет собой схематичную диаграмму или график. На схематичной диаграмме показаны бицистронные РНК репликоны, A160 и A531-A537, которые кодируют gH и gL CMV. На графике показана нейтрализующая активность иммунной сыворотки, полученной от мышей, иммунизированных VRP, которые содержали репликоны.
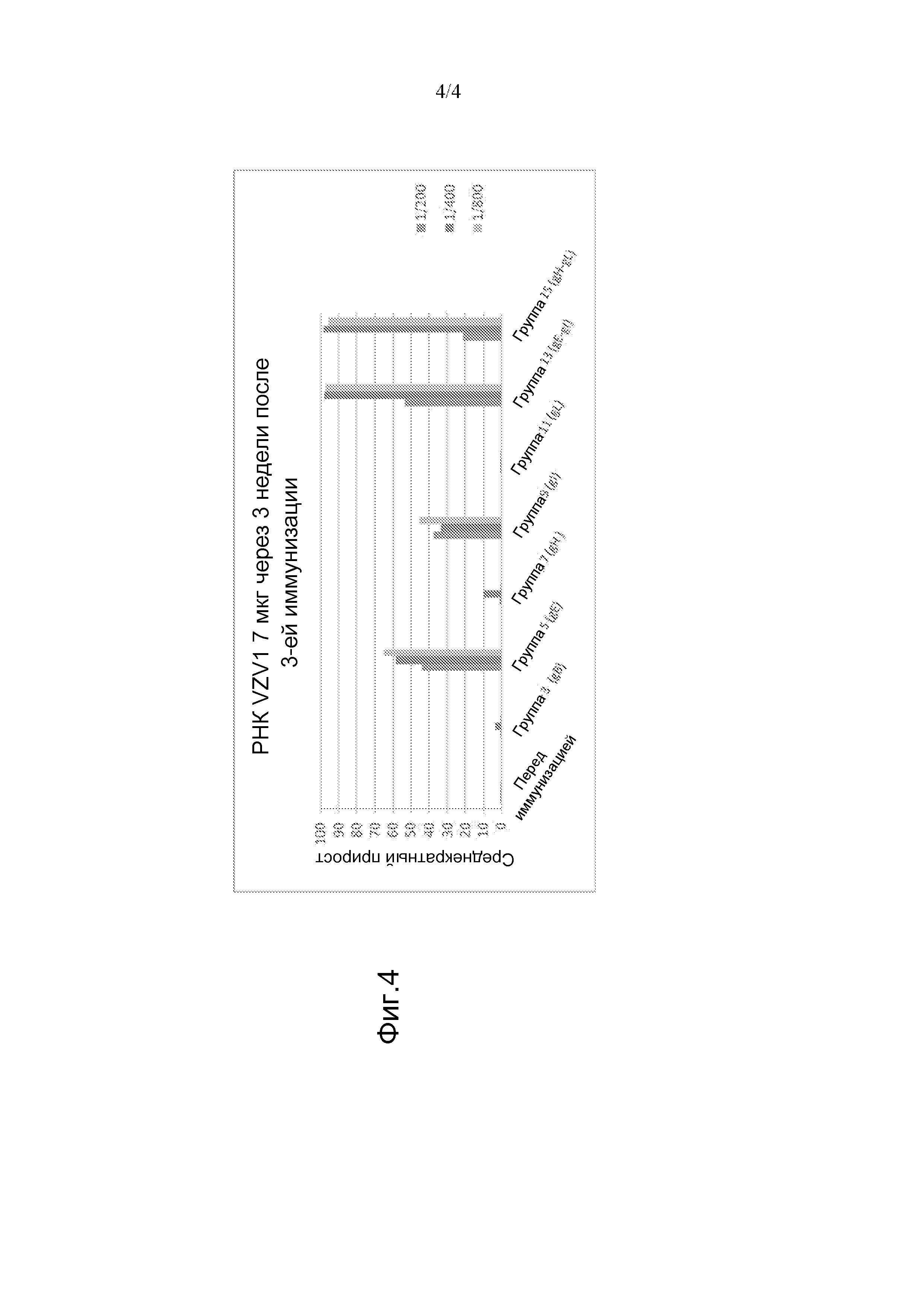
[038] Фиг. 4 представляет собой график, демонстрирующий антительный ответ на белок VZV в иммунной сыворотке, полученный от мышей, иммунизированных моноцистронными РНК репликонами, которые кодировали белки VZV, или бицистронными РНК репликонами, которые кодировали gE и gI или gH и gL VZV. Мышей иммунизировали 7 мкг РНК, находящейся в составе с CMF32.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
1. Общее описание
[039] В целом, изобретение относится к катионным эмульсиям масло-в-воде, которые содержат высокие концентрации катионных липидов и имеют определенное соотношение масло:катионный липид. Масло и катионный липид являются отдельными компонентами эмульсий, при этом масло предпочтительно не является ионным. Катионный липид может взаимодействовать с отрицательно заряженной молекулой, такой как нуклеиновая кислота, связывая таким образом отрицательно заряженную молекулу с частицами эмульсии. Описанные здесь катионные эмульсии можно использовать для доставки in vivo отрицательно заряженных молекул, таких как молекулы нуклеиновых кислот (например, РНК молекула, кодирующая белок или пептид, небольшая интерферирующая РНК, самореплицирующаяся РНК и т.п.), и для получения вакцин на основе нуклеиновых кислот.
[040] В частности, настоящее изобретение основано на открытии того, что могут быть успешно созданы стабильные катионные эмульсии масло-в-воде, которые содержат высокие концентрации катионных липидов и имеют определенное соотношение масло:катионный липид. Эмульсии, которые содержат высокие концентрации катионных липидов, позволяют получать препаративные формы молекул с более высоким отрицательным зарядом (такие как молекулы РНК) с частицами эмульсии, увеличивая таким образом эффективность доставки. В частности, для многих терапевтических средств, таких как вакцины, предпочтительными для введения являются небольшие объемы (например, 0,5 мл на дозу). Эмульсии, которые содержат высокие концентрации катионных липидов и имеют определенное соотношение масло:катионный липид, как описано здесь, позволяют доставлять более высокие дозы РНК в заданных объемах.
[041] В предпочтительных вариантах осуществления молекула РНК находится в комплексе с частицей эмульсии масло-в-воде. Образующая комплекс РНК молекула стабилизирована и защищена от разрушающего воздействия РНКаз, и поглощается клетками более эффективно по сравнению со свободной ("голой") РНК.
[042] Кроме того, когда РНК доставляется для стимуляции экспрессии кодируемого белка, например, как в случае РНК вакцины, эмульсии, которые содержат высокие концентрации катионных липидов, могут увеличивать количество молекул РНК, которые находятся в комплексе с частицами эмульсии. Поскольку в клетки-хозяева доставляется большее количество молекул РНК, продуцируется более высокое количество кодируемого белкового антигена, что в свою очередь усиливает эффективность и иммуногенность РНК-вакцины. Наконец, иммуногенность кодируемого белка может быть усилена за счет адъювантных эффектов эмульсии. Следовательно, помимо более эффективной доставки отрицательно заряженных молекул (например, молекулы РНК, которая кодирует антиген), катионные эмульсии также могут усиливать иммунный ответ за счет адъювантной активности. Например, согласно приведенному здесь описанию и раскрытым примерам, препаративные формы, в которых молекулы РНК (кодирующие белок F респираторно-синцитиального вируса (RSV)) находились в комплексе с эмульсиями, содержащими высокие концентрации DOTAP, генерировали более сильные иммунные ответы в мышиной модели RSV и модели RSV хлопкового хомяка по сравнению с молекулами РНК, находящимися в комплексе с эмульсиями, содержащими низкие концентрации DOTAP.
[043] Соответственно, в одном из аспектов изобретение предоставляет эмульсию масло-в-воде, содержащую частицы, которые диспергированы в непрерывной водной фазе, при этом эмульсия отличается тем, что: (a) средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и катионный липид, при этом (i) соотношение масло:катионный липид (моль:моль) составляет по меньшей мере примерно 8:1 (моль:моль), (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ, и (iii) при условии, что катионный липид не является DC-холестерином.
[044] В другом аспекте настоящее изобретение предоставляет эмульсию масло-в-воде, содержащую частицы, которые диспергированы в непрерывной водной фазе, причем эмульсия отличается тем, что: (a) средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм; (b) эмульсия содержит масло и катионный липид, при этом (i) соотношение масло:катионный липид (моль:моль) составляет по меньшей мере примерно 4:1 (моль:моль), (ii) концентрация катионного липида в указанной эмульсии составляет по меньшей мере примерно 2,5 мМ, (iii) содержание масла составляет от примерно 0,2% до примерно 8% (масс./об.); и (iv) при условии, что катионный липид не является DC-холестерином.
[045] Катионная эмульсия может дополнительно содержать ПАВ (например, Tween® 80, SPAN85 или их комбинацию).
[046] В других аспектах изобретение также предоставляет несколько конкретных препаративных форм катионных эмульсий масло-в-воде, которые содержат высокие концентрации катионных липидов и могут быть использованы для доставки отрицательно заряженных молекул.
[047] В другом аспекте изобретение предоставляет способ получения эмульсии масло-в-воде, включающий: (1) непосредственное растворение катионного липида в масле для образования масляной фазы; (2) предоставление водной фазы эмульсии; и (3) диспергирование масляной фазы в водной фазе (например, путем гомогенизации). При необходимости, для облегчения процесса растворения липида в масле, масло может быть нагрето до температуры в пределах от примерно 30°C до примерно 65°C. Предпочтительно, соотношение масло:катионный липид (моль:моль) в масляной фазе составляет по меньшей мере примерно 8:1 (моль:моль), и, альтернативно или дополнительно, средний диаметр указанных частиц находится в пределах от примерно 80 нм до 180 нм, и/или концентрация катионного липида в масляной фазе составляет по меньшей мере примерно 5 мМ.
[048] В другом аспекте изобретение предоставляет способ получения композиции, которая содержит отрицательно заряженную молекулу (такую как молекула РНК), находящуюся в комплексе с частицей катионной эмульсии масло-в-воде, включающий: (i) предоставление эмульсии масло-в-воде, как описано здесь; (ii) предоставление водного раствора, содержащего молекулу РНК; и (iii) объединение водного раствора, полученного на этапе (ii), и эмульсии масло-в-воде, полученной на этапе (i), получая таким образом композицию. При необходимости, водный раствор, содержащий молекулу РНК, может содержать соль (например, NaCl), буфер (например, цитратный буфер), неионный регулирующий тоничность агент (например, сахарозу, трегалозу, сорбит или декстрозу), полимер (например, Плюроник F127) или их комбинацию.
[049] Катионные эмульсии по изобретению могут быть использованы для доставки отрицательно заряженной молекулы, такой как нуклеиновая кислота (например, РНК). Композиции могут быть введены нуждающемуся в этом субъекту для генерации или индуцирования иммунного ответа. Композиции также могут вводиться совместно с другой иммуногенной молекулой, иммуногенной композицией или вакциной для усиления эффективности индуцированного ответа.
2. Определения
[050] Используемый здесь термин "примерно" означает до ±5% от указанного значения.
[051] "Антиген" относится к молекуле, содержащей один или более эпитопов (либо линейных, конформационных, либо обоих типов).
[052] "Буфер" относится к водному раствору, который устойчив к изменениям pH раствора.
[053] Используемый здесь термин "нуклеотидный аналог" или "модифицированный нуклеотид" относится к нуклеотиду, который содержит одну или более химических модификаций (например, замещений) в или на азотистом основании нуклеозида (например, цитозине (C), тимине (T) или урациле (U), аденине (A) или гуанине (G)).
[054] Используемый здесь термин "частица" эмульсии относится к капле масла, суспендированной в водной (непрерывной) фазе эмульсии масло-в-воде. Частица дополнительно содержит катионный липид и необязательно дополнительные компоненты, такие как ПАВ.
[055] Термин "полимер" относится к молекуле, состоящей из отдельных соединенных вместе химических фрагментов, которые могут быть одинаковыми или разными. Используемый здесь термин "полимер" относится к отдельным химическим фрагментам, которые соединены последовательно, образуя линейную молекулу, а также отдельным химическим фрагментам, соединенным вместе в виде разветвленной (например, "с многочисленными ответвлениями" или "звездчатой") структуры. Иллюстративные полимеры включают, например, полоксамеры. Полоксамеры представляют собой неионные трехблочные полимеры, имеющие центральную гидрофобную цепь полиоксипропилена (поли(пропиленоксида)), фланкированную двумя гидрофильными цепями полиоксиэтилена (поли(этиленоксида)).
[056] Используемый здесь термин "сахарид" охватывает моносахариды, олигосахариды или полисахариды в виде прямой цепи или в кольцевых формах, или их комбинации, образующие сахаридную цепь. Олигосахариды представляют собой сахариды, содержащие два или более моносахаридных остатков. Примеры сахаридов включают глюкозу, мальтозу, мальтотриозу, мальтотетраозу, сукрозу и трегалозу.
[057] Эмульсия является "стабильной", если частицы эмульсии остаются разделенными без какой-либо существенной агломерации или коагуляции в течение по меньшей мере месяца, предпочтительно по меньшей мере двух месяцев, при 4°C. Средний диаметр частиц (среднеарифметический диаметр) стабильной эмульсии не изменяется более чем на 10% при хранении эмульсии при 4°C в течение одного месяца, или предпочтительно двух месяцев.
[058] Термин "поверхностно-активное вещество (ПАВ)" представляет собой термин, известный в уровне техники, относящийся к любой молекуле, имеющей как гидрофильные группы (например, полярные группы), для которых с энергетической точки зрения предпочтительна сольватация водой, так и гидрофобные группы, которые не сольватируются водой. Термин "неионогенное ПАВ" является термином, известным в данной области техники, и обычно относится к молекулам ПАВ, гидрофильные группы которого (например, полярные группы) не являются электрически заряженными.
[059] "Дзета-потенциал" эмульсии определяется электрофоретической подвижностью частиц эмульсии. Скорость частицы в единичном электрическом поле называется ее электрофоретической подвижностью. Дзета-потенциал относится к электрофоретической подвижности согласно уравнению Генри:

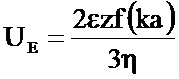
где UE - электрофоретическая подвижность, z - дзета-потенциал, ε - диэлектрическая константа, η - вязкость, и f(ka) - функция Генри. Дзета-потенциал обычно измеряют устройством измерения электрофоретической подвижности, таким как анализатор размера частиц и дзета-потенциала Zetasizer Nano Z (Malvern Instruments Ltd, United Kingdom).
3. Катионные эмульсии масло-в-воде
Раскрытые здесь катионные эмульсии масло-в-воде описаны традиционным для данного уровня техники способом, путем указания концентраций компонентов, используемых для их приготовления. Как известно в данной области техники, в процессе приготовления эмульсий, включающем стерилизацию и последующие стадии обработки, происходит естественная потеря некоторого количества масла (например, сквалена), катионного липида (например, DOTAP) или других компонентов, и реальная концентрация этих компонентов в конечном продукте (например, упакованной, стерилизованной эмульсии, готовой для применения) может быть немного ниже по сравнению с исходным количеством, иногда примерно на 10%, примерно на 20%, примерно на 25% или примерно на 35%.
[061] Настоящее изобретение относится к катионным эмульсиям масло-в-воде, которые содержат высокие концентрации катионных липидов и имеют определенное соотношение масло:катионный липид. Эмульсии по существу являются подходящими для доставки в клетку отрицательно заряженных молекул, таких как молекула РНК. Катионный липид может вступить во взаимодействие с отрицательно заряженной молекулой, например, под действием электростатических сил и гидрофобных/гидрофильных взаимодействий, таким образом сцепляя молекулу с частицами эмульсии. Описанные здесь катионные эмульсии можно использовать для доставки в клетку in vivo отрицательно заряженной молекулы, такой как молекула РНК, кодирующая антиген, или малая интерферирующая РНК. Например, описанные в настоящем документе катионные эмульсии обеспечивают преимущества для доставки молекул РНК, которые кодируют один или более антигенов, включая самореплицирующиеся РНК, в качестве вакцин.
[062] Дискретная фаза (или диспергированная фаза) эмульсии содержит масло и катионный липид, причем катионный липид облегчает процесс диспергирования масла в водной (непрерывной) фазе. В эмульсии могут присутствовать один или более компонентов, таких как описанные ниже ПАВ (например, неионогенные ПАВ).
[063] Частицы эмульсии масло-в-воде имеют средний диаметр (т.е., среднеарифметический диаметр) 1 микрометр или меньше. По существу, желательно, чтобы средний диаметр частиц катионных эмульсий составлял примерно 180 нм или меньше, примерно 170 нм или меньше, примерно 160 нм или меньше, примерно 150 нм или меньше, примерно 140 нм или меньше, примерно 130 нм или меньше, примерно 120 нм или меньше, примерно 110 нм или меньше, примерно 100 нм или меньше; например, от примерно 80 нм до 180 нм, от примерно 80 нм до 170 нм, от примерно 80 нм до 160 нм, от примерно 80 нм до 150 нм, от примерно 80 нм до 140 нм, от примерно 80 нм до 130 нм, от примерно 80 нм до 120 нм, от примерно 80 нм до 110 нм, от примерно 80 нм до 100 нм. Особенно предпочтительный средний диаметр частиц составляет примерно 100 нм или от примерно 100 нм до примерно 130 нм.
[064] Размер (средний диаметр) частиц эмульсии может варьировать в зависимости от изменения отношения ПАВ к маслу (увеличение этого соотношения приводит к уменьшению размера частиц), рабочего давления при гомогенизации (увеличение рабочего давления при гомогенизации обычно приводит к уменьшению размера частиц), температуры (увеличение температуры приводит к уменьшению размера частиц), изменения типа масла, включения определенных типов буферов в водную фазу и других параметров процесса, что более подробно описано ниже. В некоторых случаях размер частиц эмульсий может влиять на иммуногенность комплекса РНК-эмульсия, что показано в приведенных ниже примерах.
[065] Описанные здесь эмульсии масло-в-воде являются стабильными.
[066] Частицы описанных здесь эмульсий могут формировать комплекс с отрицательно заряженной молекулой. Перед образованием комплекса с отрицательно заряженной молекулой суммарный заряд частиц (обычно измеряемый как дзета-потенциал) должен быть положительным (катионным). Суммарный заряд частиц может изменяться в зависимости от типа катионного липида и количества катионного липида в эмульсии, количества масла в эмульсии (например, более высокое процентное содержание масла обычно приводит к уменьшению заряда на поверхности частиц), а также может зависеть от влияния любого дополнительного компонента (например, ПАВ), присутствующего в эмульсии. Предпочтительно, дзета-потенциал частиц перед образованием комплекса не превышает примерно 50 мВ, примерно 45 мВ, примерно 40 мВ, примерно 35 мВ, примерно 30 мВ, примерно 25 мВ, примерно 20 мВ; находится в диапазоне от примерно 5 мВ до примерно 50 мВ, от примерно 10 мВ до примерно 50 мВ, от примерно 10 мВ до примерно 45 мВ, от примерно 10 мВ до примерно 40 мВ, от примерно 10 мВ до примерно 35 мВ, от примерно 10 мВ до примерно 30 мВ, от примерно 10 мВ до примерно 25 мВ или от примерно 10 мВ до примерно 20 мВ. На дзета-потенциал может оказывать влияние (i) pH эмульсии, (ii) проводимость эмульсии (например, содержание соли) и (iii) концентрация различных компонентов эмульсии (полимер, неионогенные ПАВ и т.д.). Дзета-потенциал катионных эмульсий масло-в-воде измеряют анализатором размера частиц и дзета-потенциала Malvern Nanoseries (Westborough, MA). Образцы разбавляют в соотношении 1:100 в воде (вязкость: 0,8872 cp, RI: 1,330, диэлектрическая постоянная: 78,5) и добавляют в капиллярную ячейку, изготовленную из полистирольного латекса (Malvern, Westborough, MA). Дзета-потенциал измеряют при 25°C с временем установления равновесия 2 минуты и анализируют, используя модель Смолуховского (Smoluchowski) (значение F(Ka)=1,5). Данные приведены в мВ.
[067] Иллюстративная катионная эмульсия по настоящему изобретению обозначена здесь как "CMF32". Масло в CMF32 представляет собой сквален (4,3% масс./об.), а катионный липид представляет собой DOTAP (3,2 мг/мл). CMF32 также содержит ПАВ SPAN85 (сорбитана триолеат в количестве 0,5% об./об.) и Tween® 80 (полисорбат 80; полиоксиэтиленсорбитана моноолеат; 0,5% об./об.). Таким образом, частицы эмульсии CMF32 содержат сквален, SPAN85, Tween® 80 и DOTAP. Было показано, что молекулы РНК эффективно образуют комплексы с частицами CMF32 при соотношениях N/P, равных 4:1, 6:1, 8:1, 10:1, 12:1 и 14:1. Другие иллюстративные катионные эмульсии включают, например, эмульсии, обозначенные здесь как "CMF34" (4,3% масс./об. сквалена, 0,5% Tween® 80, 0,5% SPAN85 и 4,4 мг/мл DOTAP), "CMF35" (4,3% масс./об. сквалена, 0,5% Tween® 80, 0,5% SPAN85, 5,0 мг/мл DOTAP) и другие описанные здесь эмульсии.
[068] Некоторые иллюстративные катионные эмульсии масло-в-воде по изобретению содержат DOTAP и сквален в концентрациях от 2,1 мг/мл до 2,84 мг/мл (предпочтительно, от 2,23 мг/мл до 2,71 мг/мл) и от 30,92 мг/мл до 41,92 мг/мл (предпочтительно, от 32,82 мг/мл до примерно 40,02 мг/мл), соответственно, и дополнительно содержат равные количества SPAN85 и Tween® 80 (например, примерно по 0,5% каждого). Другие иллюстративные катионные эмульсии масло-в-воде по изобретению содержат DOTAP и сквален в концентрациях от 2,78 мг/мл до 3,76 мг/мл (предпочтительно, от 2,94 мг/мл до 3,6 мг/мл) и от 18,6 мг/мл до 25,16 мг/мл (предпочтительно, от 19,69 мг/мл до примерно 24,07 мг/мл), соответственно, и дополнительно содержат равные количества SPAN85 и Tween® 80 (например, примерно по 0,5% каждого). Предпочтительно, частицы этих эмульсий имеют средний диаметр от 80 нм до 180 нм.
[069] Отдельные компоненты эмульсий масло-в-воде по настоящему изобретению известны в данной области, хотя такие композиции не объединены описанным здесь образом. Соответственно, отдельные компоненты, хотя и описаны ниже как в общем виде, так и более детально в предпочтительных вариантах осуществления, хорошо известны в данной области техники, и используемые здесь термины, такие как масло, ПАВ и т.д., в достаточной степени известны специалистам в данной области без дополнительного их описания. Кроме того, несмотря на указание предпочтительных диапазонов количества отдельных компонентов эмульсии, может возникнуть необходимость в подборе фактических соотношений компонентов в конкретной эмульсии с тем, чтобы гарантированно были образованы частицы эмульсии желаемого размера, обладающие желаемыми физическими свойствами. Например, если используется конкретное количество масла (например, 5% об./об. масло), то количество ПАВ должно быть на уровне, который является достаточным для диспергирования частиц масла в водной фазе с образованием стабильной эмульсии. Фактическое количество ПАВ, требуемое для диспергирования масла в водной фазе, зависит от типа ПАВ и типа используемого для эмульсии масла; а количество масла также может изменяться в зависимости от требуемого размера частиц (так как это изменяет площадь поверхности между двумя фазами). Специалист в данной области легко определит фактические количества и относительные соотношения компонентов желаемой эмульсии.
А. Масло
[070] Частицы катионных эмульсий масло-в-воде содержат масло.
[071] Масло предпочтительно находится в жидкой фазе при температуре 1°C или выше и является нерастворимым в воде.
[072] Предпочтительно, масло представляет собой метаболизируемое нетоксичное масло; более предпочтительно, масло содержит от примерно 6 до примерно 30 атомов углерода, включая, без ограничения, алканы, алкены, алкины и соответствующие их кислоты и спирты, их простые и сложные эфиры и смеси. Масло может быть любым растительным маслом, рыбьим маслом, животным маслом или маслом, полученным синтетическим способом, которое может быть метаболизировано в организме субъекта, которому введена эмульсия, и которое не является токсичным для субъекта. Субъект может быть животным, как правило, млекопитающим, предпочтительно человеком.
[073] В некоторых вариантах осуществления масло находится в жидкой фазе при 25°C. Масло находится в жидкой фазе при 25°C, когда оно проявляет свойства жидкости (поскольку отличается от твердого вещества и газа; и имеет определенный объем, но не имеет определенной формы) при хранении при 25°C. Однако эмульсия может храниться и применяться при любой подходящей температуре. Предпочтительно, масло находится в жидкой фазе при 4°C.
[074] Масло может представлять собой алкан, алкен или алкин любой длины, или его кислотное или спиртовое производное либо в виде свободной кислоты, соли, либо в виде сложного эфира, такого как моно- или ди- или триэфира, такого как триглицериды и сложные эфиры 1,2-пропандиола или аналогичных полигидроксиспиртов. Спирты могут быть ацилированы моно- или полифункциональной кислотой, например, уксусной кислотой, пропановой кислотой, лимонной кислотой и т.п. Также могут быть использованы эфиры, являющиеся производными спиртов с длинной цепью, которые представляют собой масла и соответствуют другим приведенным здесь критериям.
[075] Отдельный алкановый, алкеновый или алкиновый фрагмент и его кислотные или спиртовые производные обычно содержат от примерно 6 до примерно 30 атомов углерода. Этот фрагмент может иметь линейную или разветвленную цепь. Он может быть полностью насыщенным или может иметь одну или более двойных или тройных связей. Если используются сложные моно- или полиэфиры или простые эфиры масел, ограничение на количество атомов углерода от примерно 6 до примерно 30 относится к отдельной жирной кислоте или фрагментам жирных спиртов, а не к общему количеству атомов углерода.
[076] Можно использовать любые подходящие масла, полученные от животного, рыбьего или растительного источника. Источники растительных масел включают орехи, семена и зерна, а подходящие масла включают арахисовое масло, соевое масло, кокосовое масло, оливковое масло и т.п. Другие подходящие масла, полученные из семян, включают сафлоровое масло, хлопковое масло, подсолнечное масло, кунжутное масло и т.д. Что касается масел, полученных из зерна, можно использовать кукурузное масло и масло, полученное из зерен других злаковых, таких как пшеница, овес, рожь, рис, тефф, тритикале и т.п. Технология производства растительных масел хорошо разработана и хорошо известна. Состав этих и других аналогичных масел можно найти, например, в Мерк Индексе (Merck Index) и других источниках, относящихся к пищевым продуктам, питанию и технологиям производства пищевых продуктов.
[077] Путем гидролиза, разделения и этерификации подходящих материалов, используя в качестве исходных материалов масло, полученное из орехов или семян, могут быть получены сложные эфиры глицерина и 1,2-пропандиола с жирными кислотами, содержащими от примерно 6 до примерно 10 атомов углерода, которые в естественных условиях отсутствуют в получаемых из семян маслах. Эти продукты доступны на рынке под торговой маркой NEOBEES от компании PVO International, Inc., Chemical Specialties Division, 416 Division Street, Boongon, N.J. и т.д.
[078] Животные масла и жиры в диапазоне физиологических температур часто находятся в твердой фазе, поскольку они существуют в виде триглицеридов и имеют более высокую степень насыщения по сравнению с маслами, полученными из рыб или растений. Однако жирные кислоты могут быть получены из животных жиров путем частичного или полного омыления триглицеридов с получением свободных жирных кислот. Жиры и масла, полученные из молока млекопитающих, являются метаболизируемыми и, следовательно, могут быть использованы при реализации настоящего изобретения. В данной области техники хорошо известны процедуры разделения, очистки, сапонификации и другие средства, необходимые для получения чистых масел из животных источников.
[079] Большинство рыб содержит метаболизируемые масла, которые являются легко извлекаемыми. Например, масло печени трески, масло печени акулы и китовое масло, такое как спермацетовое масло, являются несколькими примерами рыбьих масел, которые могут быть использованы в настоящем изобретении. Несколько видов масел с разветвленной структурой, которые обычно называются терпеноидами, могут быть получены путем биохимического синтеза из изопреновых 5-углеродных звеньев. Особенно предпочтительным в настоящем изобретении является сквален (2,6,10,15,19,23-гексаметил-2,6,10,14,18,22-тетракозагексаен), разветвленный ненасыщенный терпеноид. Основным источником сквалена является масло печени акулы, хотя подходящими источниками также являются растительные масла (преимущественно овощные масла), включая масла, полученные из семян амаранта, рисовых отрубей, ростков пшеницы, и оливковое масло, а также масла из других подходящих источников. Сквален также может быть получен из дрожжей и других подходящих микробов. В некоторых вариантах осуществления сквален предпочтительно получают из масел неживотного происхождения, например, из маслин, оливкового масла или дрожжей. Предпочтительным также является сквалан, насыщенный аналог сквалена. Различные виды рыбьего масла, включая сквален и сквалан, являются коммерчески доступными или могут быть получены способами, известными в данной области техники.
[080] В некоторых вариантах осуществления масло выбирают из группы, состоящей из касторового масла, кокосового масла, кукурузного масла, хлопкового масла, масла энотеры, рыбьего масла, масла жожоба, лярд-масла, льняного масла, оливкового масла, арахисового масла, сафлорового масла, кунжутного масла, соевого масла, сквалена, сквалана, подсолнечного масла и масла зародышей пшеницы. В иллюстративных вариантах осуществления масло содержит сквален или сквалан.
[081] Масляный компонент эмульсии может находиться в количестве от примерно 0,2% до примерно 10% (об./об.). Например, катионная эмульсия масло-в-воде может содержать от примерно 0,2% до примерно 10% (об./об.) масла, от примерно 0,2% до примерно 9% (об./об.) масла, от примерно 0,2% до примерно 8% (об./об.) масла, от примерно 0,2% до примерно 7% (об./об.) масла, от примерно 0,2% до примерно 6% (об./об.) масла, от примерно 0,2% до примерно 5% (об./об.) масла, от примерно 0,3% до примерно 10% (об./об.) масла, от примерно 0,4% до примерно 10% (об./об.) масла, от примерно 0,5% до примерно 10% (об./об.) масла, от примерно 1% до примерно 10% (об./об.) масла, от примерно 2% до примерно 10% (об./об.) масла, от примерно 3% до примерно 10% (об./об.) масла, от примерно 4% до примерно 10% (об./об.) масла, от примерно 5% до примерно 10% (об./об.) масла, от примерно 0,2% до примерно 10% (масс./об.) масла, от примерно 0,2% до примерно 9% (масс./об.) масла, от примерно 0,2% до примерно 8% (масс./об.) масла, от примерно 0,2% до примерно 7% (масс./об.) масла, от примерно 0,2% до примерно 6% (масс./об.) масла, от примерно 0,2% до примерно 5% (масс./об.) масла, от примерно 0,2% до примерно 4,3% (масс./об.) масла, от примерно 0,6% до примерно 4% (масс./об.) масла, от примерно 0,7% до примерно 4% (масс./об.) масла, от примерно 0,8% до примерно 4% (масс./об.) масла, от примерно 0,9% до примерно 4% (масс./об.) масла, от примерно 1,0 % до примерно 4% (масс./об.) масла, от примерно 0,6% до примерно 3,5% (масс./об.) масла, от примерно 0,6% до примерно 3% (масс./об.) масла, примерно 0,5% (об./об.) масла, примерно 0,6% (об./об.) масла, примерно 0,7% (об./об.) масла, примерно 0,8% (об./об.) масла, примерно 0,9% (об./об.) масла, примерно 1% (об./об.) масла, примерно 1,5% (об./об.) масла, примерно 2% (об./об.) масла, примерно 2,5% (об./об.) масла, примерно 3% (об./об.) масла, примерно 3,5% (об./об.) масла, примерно 4% (об./об.) масла, примерно 5% (об./об.) масла, примерно 10% (об./об.) масла, примерно 0,5% (масс./об.) масла, примерно 1% (масс./об.) масла, примерно 1,5% (масс./об.) масла, примерно 2% (масс./об.) масла, примерно 2,5% (масс./об.) масла, примерно 3% (масс./об.) масла, примерно 3,5% (масс./об.) масла, примерно 4% (масс./об.) масла, примерно 4,3% (масс./об.) масла, примерно 5% (масс./об.) масла, примерно 5,5% (масс./об.) масла, примерно 6% (масс./об.) масла, примерно 6,5% (масс./об.) масла, примерно 7% (масс./об.) масла, примерно 7,5% (масс./об.) масла или примерно 8% (масс./об.) масла.
[082] Катионная эмульсия масло-в-воде также может содержать от примерно 0,2% до примерно 8% (об./об.) масла, например, от 0,6% (масс./об.) до 4% (масс./об.), от примерно 1% (масс./об.) до примерно 3,2% (масс./об.), примерно 1% (масс./об.), примерно 1,1% (масс./об.), примерно 1,2% (масс./об.), примерно 1,3% (масс./об.), примерно 1,4% (масс./об.), примерно 1,5% (масс./об.), примерно 1,6% (масс./об.), примерно 1,7% (масс./об.), примерно 1,8% (масс./об.), примерно 1,9% (масс./об.), примерно 2,0% (масс./об.), примерно 2,1% (масс./об.), примерно 2,15% (масс./об.), примерно 2,2% (масс./об.), примерно 2,3% (масс./об.), примерно 2,4% (масс./об.), примерно 2,5% (масс./об.), примерно 2,6% (масс./об.), примерно 2,7% (масс./об.), примерно 2,8% (масс./об.), примерно 2,9% (масс./об.), 3,0% (масс./об.), примерно 3,1% (масс./об.), примерно 3,2% (масс./об.), примерно 3,3% (масс./об.), примерно 3,4% (масс./об.), примерно 3,5% (масс./об.), примерно 3,6% (масс./об.), примерно 3,7% (масс./об.), примерно 3,8% (масс./об.), примерно 3,9% (масс./об.) или примерно 4,0% (масс./об.) масла.
[083] В иллюстративном варианте осуществления изобретения катионная эмульсия масло-в-воде содержит примерно 5% (об./об.) масла. В другом иллюстративном варианте осуществления изобретения катионная эмульсия масло-в-воде содержит примерно 4,3% (масс./об.) сквалена. В другом иллюстративном варианте осуществления изобретения катионная эмульсия масло-в-воде содержит от 0,6% (масс./об.) до 4% (масс./об.) сквалена, например, от примерно 1% (масс./об.) до примерно 3,2% (масс./об.) сквалена, например, 1,08% (масс./об.), 2,15% (масс./об.) или 3,23% (масс./об.) сквалена, как показано в примерах.
[084] Как указывалось выше, процентное содержание описанного выше масла определяется, исходя из начального количества масла, которое используется для получения эмульсий. В данной области техники хорошо известно, что фактическая концентрация масла в конечном продукте (например, упакованной, стерилизованной эмульсии, готовой для введения) может быть немного ниже, иногда на примерно 10%, до примерно 20%, до примерно 25% или до примерно 35%.
В. Катионные липиды
[085] Описанные здесь частицы эмульсии содержат катионный липид, который может взаимодействовать с отрицательно заряженной молекулой, таким образом связывая эту молекулу с частицами эмульсии.
[086] Можно использовать любой подходящий катионный липид. Катионный липид обычно содержит атом азота, который в физиологических условиях заряжен положительно. Головная группа катионного липида может содержать четвертичный амин или, предпочтительно, четвертичный амин. Некоторые подходящие катионные липиды содержат две цепи насыщенных или ненасыщенных жирных кислот (например, боковые цепи, имеющие от примерно 10 до примерно 30 атомов углерода).
[087] Катионный липид может иметь положительный заряд при примерно pH 12, примерно pH 11, примерно pH 10, примерно pH 9, примерно pH 8, примерно pH 7 или примерно pH 6.
[088] Подходящие катионные липиды включают безалкония хлорид (ВАК), бензетония хлорид, цетримид (который содержит тетрадецилтриметиламмония бромид и может содержать небольшое количество додецилтриметиламмония бромида и гексадецилтриметиламмония бромида), цетилпиридиния хлорид (CPC), цетилтриметиламмония хлорид (CTAC), соли первичных аминов, вторичных аминов, третичных аминов, включая без ограничений N,N',N'-полиоксиэтилен(10)-N-таллоу-1,3-диаминопропан, другие соли четвертичных аминов, включая, без ограничения, додецилтриаммония бромид, гексадецилтриметиламмония бромид, смешанный алкил-триметил-аммония бромид, бензилдиметилдодециламмония хлорид, бензилдиметилгексадециламмония хлорид, бензилтриметиламмония метоксид, цетилдиметилэтиламмония бромид, диметилдиоктадециламмония бромид (DDAB), метилбензетония хлорид, декаметония хлорид, метил(смешанный триалкил)аммония хлорид, метилтриоктиламмония хлорид, N,N-диметил-N-[2-(2-метил-4-(1,1,3,3-тетраметилбутил)фенокси]этокси)этил]бензол-метанаминиум хлорид (DEBDA), соли диалкилдиметиламмония, [1-(2,3-диолеилокси)-]-N,N,N,триметиламмония хлорид, 1,2-диацил-3-(триметиламмонио)пропан(ацильная группа=димиристоил, дипальмитоил, дистеароил, диолеоил), 1,2-диацил-3-(диметиламмонио)пропан(ацильная группа=димиристоил, дипальмитоил, дистеароил, диолеоил), 1,2-диолеоил-3-(4'-триметил-аммонио)бутаноил-sn-глицерин, холиновый эфир 1,2-диолеоил 3-сукцинил-sn-глицерина, холестерил(4'-триметиламмонио)бутаноат), соли N-алкилпиридиния (например, цетилпиридиния бромид и цетилпиридиния хлорид), соли N-алкилпиперидиния, дикатионные болаформные электролиты (C12Me6; C12Bu6), диалкилглицетилфосфорилхолин, лизолецитин, L-α диолеоилфосфатидилэтаноламин, холиновый эфир холестерин гемисукцината, липополиамины, включая, без ограничения, диоктадециламидоглицилспермин (DOGS), дипальмитоил фосфатидилэтанол-амидоспермин (DPPES), липополи-L (или D)-лизин (LPLL, LPDL), поли (L (или D)-лизин, конъюгированный с N-глутарилфосфатидилэтаноламином, эфир дидодецил глутамата с пендантной аминогруппой (C12GluPhCnN+), эфир дитетрадецил глутамата с пендантной аминогруппой (C14GluCnN+), катионные производные холестерина, включая, без ограничения, соль холестерил-3β-оксисукцинамидоэтилентриметиламмония, холестерил-3β-оксисукцинамидоэтилендиметиламин, соль холестерил-3β-карбоксиамидоэтилентриметиламмония, холестерил-3β-карбоксиамидоэтилендиметиламина и 3γ-[N-(N',N-диметиламиноэтанкарбомоил]холестерин)(DC-холестерин), 1,2-диолеоилокси-3-(триметиламмонио)пропан (DOTAP), диметилдиоктадециламмония (DDA), 1,2-димиристоил-3-триметиламмонияпропан (DMTAP), дипальмитоил(C16:0)триметиламмония пропан (DPTAP), дистеароилтриметиламмония пропан (DSTAP), N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорид (DOTMA), N,N-диолеоил-N,N-диметиламмония хлорид (DODAC), 1,2-диолеоил-sn-глицеро-3-этилфосфохолин (DOEPC), 1,2-диолеоил-3-диметиламмония-пропан (DODAP), 1,2-дилинолеилокси-3-диметиламинопропан (DLinDMA) и их комбинацию.
[089] В предпочтительных вариантах осуществления катионный липид выбирают из группы, состоящей из 1,2-диолеоилокси-3-(триметиламмонио)пропан (DOTAP), 1,2-диолеоил-sn-глицеро-3-этилфосфохолин (DOEPC), N,N-диолеоил-N,N-диметиламмония хлорид (DODAC) и N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония хлорид (DOTMA). В некоторых вариантах осуществления катионный липид не является DC-холестерин.
[090] Предпочтительно, катионные липиды, выбираемые для эмульсии, являются растворимыми в выбранном для эмульсии масле. Это позволяет получать высокие концентрации катионных липидов в эмульсии, путем растворения липида в масле перед диспергированием в подвижной фазе. Определение того, является ли конкретный липид растворимым в масле, и выбор подходящего масла и, соответственно, липидной комбинации находится в пределах объема знаний данного уровня техники. Например, растворимость можно предсказать по структуре липида и масла (например, растворимость липида может быть определена по структуре его концевой группы). Например, растворимыми в сквалене или сквалане являются липиды, имеющие одну или две цепи ненасыщенной жирной кислоты (например, олеоильные концевые группы или линолильные концевые группы), такие как DOTAP, DOEPC, DODAC, DOTMA. Альтернативно, растворимость может быть определена по количеству липида, который растворяется в заданном количестве масла, образуя насыщенный раствор. Такие способы известны в данной области техники. В примерах также приводится растворимость иллюстративных насыщенных или ненасыщенных жирных кислот в сквалене. Предпочтительно, концентрация насыщения липида в масле составляет по меньшей мере примерно 1 мг/мл, по меньшей мере примерно 5 мг/мл, по меньшей мере примерно 10 мг/мл, по меньшей мере примерно 25 мг/мл, по меньшей мере примерно 50 мг/мл или по меньшей мере примерно 100 мг/мл.
[091] Предпочтительно, концентрация катионного липида в эмульсии до образования комплекса с отрицательно заряженной молекулой составляет по меньшей мере примерно 1,25 мМ, по меньшей мере примерно 1,5 мМ, по меньшей мере примерно 1,75 мМ, по меньшей мере примерно 2,0 мМ, по меньшей мере примерно 2,25 мМ, по меньшей мере примерно 2,5 мМ, по меньшей мере примерно 2,75 мМ, по меньшей мере примерно 3,0 мМ, по меньшей мере примерно 3,25 мМ, по меньшей мере примерно 3,5 мМ, по меньшей мере примерно 3,75 мМ, по меньшей мере примерно 4,0 мМ, по меньшей мере примерно 4,25 мМ, по меньшей мере примерно 4,5 мМ, по меньшей мере примерно 4,75 мМ, по меньшей мере примерно 5,0 мМ, по меньшей мере примерно 5,25 мМ, по меньшей мере примерно 5,5 мМ, по меньшей мере примерно 5,75 мМ, по меньшей мере примерно 6 мМ, по меньшей мере примерно 6,25 мМ, по меньшей мере примерно 6,5 мМ, по меньшей мере примерно 6,75 мМ, по меньшей мере примерно 7 мМ, по меньшей мере примерно 7,25 мМ, по меньшей мере примерно 7,5 мМ, по меньшей мере примерно 7,75 мМ, по меньшей мере примерно 8 мМ, по меньшей мере примерно 8,25 мМ, по меньшей мере примерно 8,5 мМ, по меньшей мере примерно 8,75 мМ, по меньшей мере примерно 9 мМ, по меньшей мере примерно 9,25 мМ, по меньшей мере примерно 9,5 мМ, по меньшей мере примерно 9,75 мМ, по меньшей мере примерно 10 мМ.
[092] В некоторых вариантах осуществления катионный липид представляет собой DOTAP. Катионная эмульсия масло-в-воде может содержать от примерно 0,8 мг/мл до примерно 10 мг/мл DOTAP. Например, катионная эмульсия масло-в-воде может содержать DOTAP от примерно 1,7 мг/мл до примерно 10 мг/мл, от примерно 1,8 мг/мл до примерно 10 мг/мл, от примерно 2,0 мг/мл до примерно 10 мг/мл, от примерно 2,2 мг/мл до примерно 10 мг/мл, от примерно 2,4 мг/мл до примерно 10 мг/мл, от примерно 2,6 мг/мл до примерно 10 мг/мл, от примерно 2,8 мг/мл до примерно 10 мг/мл, от примерно 3,0 мг/мл до примерно 10 мг/мл, от примерно 3,2 мг/мл до примерно 10 мг/мл, от примерно 3,4 мг/мл до примерно 10 мг/мл, от примерно 3,6 мг/мл до примерно 10 мг/мл, от примерно 4,0 мг/мл до примерно 10 мг/мл, от примерно 4,4 мг/мл до примерно 10 мг/мл, от примерно 4,8 мг/мл до примерно 10 мг/мл, от примерно 5 мг/мл до примерно 10 мг/мл, от примерно 1,7 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 6 мг/мл, от примерно 1,8 мг/мл до примерно 7 мг/мл, от примерно 1,8 мг/мл до примерно 8 мг/мл, от примерно 1,8 мг/мл до примерно 9 мг/мл, примерно 1,7 мг/мл, примерно 1,8 мг/мл, примерно 2,0 мг/мл, примерно 2,2 мг/мл, примерно 2,4 мг/мл, примерно 2,6 мг/мл, примерно 2,8 мг/мл, примерно 3,0 мг/мл, примерно 3,2 мг/мл, примерно 3,4 мг/мл, примерно 3,6 мг/мл, примерно 3,8 мг/мл, примерно 4,0 мг/мл, примерно 4,2 мг/мл, примерно 4,4 мг/мл, примерно 4,6 мг/мл, примерно 4,8 мг/мл, примерно 5,0 мг/мл, примерно 5,2 мг/мл, примерно 5,5 мг/мл, примерно 6,0 мг/мл, по меньшей мере примерно 0,8 мг/мл, по меньшей мере примерно 0,85 мг/мл, по меньшей мере примерно 0,9 мг/мл, по меньшей мере примерно 1,0 мг/мл, по меньшей мере примерно 1,1 мг/мл, по меньшей мере примерно 1,2 мг/мл, по меньшей мере примерно 1,3 мг/мл, по меньшей мере примерно 1,4 мг/мл, по меньшей мере примерно 1,5 мг/мл, по меньшей мере примерно 1,6 мг/мл, по меньшей мере примерно 1,7 мг/мл и т.д.
[093] В иллюстративном варианте осуществления катионная эмульсия масло-в-воде содержит от примерно 1,8 мг/мл до примерно 5,0 мг/мл DOTAP.
[094] В некоторых вариантах осуществления катионный липид представляет собой DOEPC. Катионная эмульсия масло-в-воде может содержать от примерно 0,8 мг/мл до примерно 10 мг/мл DOEPC. Например, катионная эмульсия масло-в-воде может содержать DOEPC от примерно 1,7 мг/мл до примерно 10 мг/мл, от примерно 1,8 мг/мл до примерно 10 мг/мл, от примерно 2,0 мг/мл до примерно 10 мг/мл, от примерно 2,2 мг/мл до примерно 10 мг/мл, от примерно 2,4 мг/мл до примерно 10 мг/мл, от примерно 2,6 мг/мл до примерно 10 мг/мл, от примерно 2,8 мг/мл до примерно 10 мг/мл, от примерно 3,0 мг/мл до примерно 10 мг/мл, от примерно 3,2 мг/мл до примерно 10 мг/мл, от примерно 3,4 мг/мл до примерно 10 мг/мл, от примерно 3,6 мг/мл до примерно 10 мг/мл, от примерно 4,0 мг/мл до примерно 10 мг/мл, от примерно 4,4 мг/мл до примерно 10 мг/мл, от примерно 4,8 мг/мл до примерно 10 мг/мл, от примерно 5 мг/мл до примерно 10 мг/мл, от примерно 1,7 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 6 мг/мл, от примерно 1,8 мг/мл до примерно 7 мг/мл, от примерно 1,8 мг/мл до примерно 8 мг/мл, от примерно 1,8 мг/мл до примерно 9 мг/мл, примерно 1,7 мг/мл, примерно 1,8 мг/мл, примерно 2,0 мг/мл, примерно 2,2 мг/мл, примерно 2,4 мг/мл, примерно 2,6 мг/мл, примерно 2,8 мг/мл, примерно 3,0 мг/мл, примерно 3,2 мг/мл, примерно 3,4 мг/мл, примерно 3,6 мг/мл, примерно 3,8 мг/мл, примерно 4,0 мг/мл, примерно 4,2 мг/мл, примерно 4,4 мг/мл, примерно 4,6 мг/мл, примерно 4,8 мг/мл, примерно 5,0 мг/мл, примерно 5,2 мг/мл, примерно 5,5 мг/мл, примерно 6,0 мг/мл, по меньшей мере примерно 0,8 мг/мл, по меньшей мере примерно 0,85 мг/мл, по меньшей мере примерно 0,9 мг/мл, по меньшей мере примерно 1,0 мг/мл, по меньшей мере примерно 1,1 мг/мл, по меньшей мере примерно 1,2 мг/мл, по меньшей мере примерно 1,3 мг/мл, по меньшей мере примерно 1,4 мг/мл, по меньшей мере примерно 1,5 мг/мл, по меньшей мере примерно 1,6 мг/мл, по меньшей мере примерно 1,7 мг/мл и т.д.
[095] В некоторых вариантах осуществления катионный липид представляет собой DODAC. Катионная эмульсия масло-в-воде может содержать от примерно 0,8 мг/мл до примерно 10 мг/мл DODAC. Например, катионная эмульсия масло-в-воде может содержать DODAC от примерно 1,7 мг/мл до примерно 10 мг/мл, от примерно 1,8 мг/мл до примерно 10 мг/мл, от примерно 2,0 мг/мл до примерно 10 мг/мл, от примерно 2,2 мг/мл до примерно 10 мг/мл, от примерно 2,4 мг/мл до примерно 10 мг/мл, от примерно 2,6 мг/мл до примерно 10 мг/мл, от примерно 2,8 мг/мл до примерно 10 мг/мл, от примерно 3,0 мг/мл до примерно 10 мг/мл, от примерно 3,2 мг/мл до примерно 10 мг/мл, от примерно 3,4 мг/мл до примерно 10 мг/мл, от примерно 3,6 мг/мл до примерно 10 мг/мл, от примерно 4,0 мг/мл до примерно 10 мг/мл, от примерно 4,4 мг/мл до примерно 10 мг/мл, от примерно 4,8 мг/мл до примерно 10 мг/мл, от примерно 5 мг/мл до примерно 10 мг/мл, от примерно 1,7 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 6 мг/мл, от примерно 1,8 мг/мл до примерно 7 мг/мл, от примерно 1,8 мг/мл до примерно 8 мг/мл, от примерно 1,8 мг/мл до примерно 9 мг/мл, примерно 1,7 мг/мл, примерно 1,8 мг/мл, примерно 2,0 мг/мл, примерно 2,2 мг/мл, примерно 2,4 мг/мл, примерно 2,6 мг/мл, примерно 2,8 мг/мл, примерно 3,0 мг/мл, примерно 3,2 мг/мл, примерно 3,4 мг/мл, примерно 3,6 мг/мл, примерно 3,8 мг/мл, примерно 4,0 мг/мл, примерно 4,2 мг/мл, примерно 4,4 мг/мл, примерно 4,6 мг/мл, примерно 4,8 мг/мл, примерно 5,0 мг/мл, примерно 5,2 мг/мл, примерно 5,5 мг/мл, примерно 6,0 мг/мл, по меньшей мере примерно 0,8 мг/мл, по меньшей мере примерно 0,85 мг/мл, по меньшей мере примерно 0,9 мг/мл, по меньшей мере примерно 1,0 мг/мл, по меньшей мере примерно 1,1 мг/мл, по меньшей мере примерно 1,2 мг/мл, по меньшей мере примерно 1,3 мг/мл, по меньшей мере примерно 1,4 мг/мл, по меньшей мере примерно 1,5 мг/мл, по меньшей мере примерно 1,6 мг/мл, по меньшей мере примерно 1,7 мг/мл и т.д.
[096] В некоторых вариантах осуществления катионный липид представляет собой DOTMA. Катионная эмульсия масло-в-воде может содержать от примерно 0,8 мг/мл до примерно 10 мг/мл DOTMA. Например, катионная эмульсия масло-в-воде может содержать DOTMA от примерно 1,7 мг/мл до примерно 10 мг/мл, от примерно 1,8 мг/мл до примерно 10 мг/мл, от примерно 2,0 мг/мл до примерно 10 мг/мл, от примерно 2,2 мг/мл до примерно 10 мг/мл, от примерно 2,4 мг/мл до примерно 10 мг/мл, от примерно 2,6 мг/мл до примерно 10 мг/мл, от примерно 2,8 мг/мл до примерно 10 мг/мл, от примерно 3,0 мг/мл до примерно 10 мг/мл, от примерно 3,2 мг/мл до примерно 10 мг/мл, от примерно 3,4 мг/мл до примерно 10 мг/мл, от примерно 3,6 мг/мл до примерно 10 мг/мл, от примерно 4,0 мг/мл до примерно 10 мг/мл, от примерно 4,4 мг/мл до примерно 10 мг/мл, от примерно 4,8 мг/мл до примерно 10 мг/мл, от примерно 5 мг/мл до примерно 10 мг/мл, от примерно 1,7 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 5 мг/мл, от примерно 1,8 мг/мл до примерно 6 мг/мл, от примерно 1,8 мг/мл до примерно 7 мг/мл, от примерно 1,8 мг/мл до примерно 8 мг/мл, от примерно 1,8 мг/мл до примерно 9 мг/мл, примерно 1,7 мг/мл, примерно 1,8 мг/мл, примерно 2,0 мг/мл, примерно 2,2 мг/мл, примерно 2,4 мг/мл, примерно 2,6 мг/мл, примерно 2,8 мг/мл, примерно 3,0 мг/мл, примерно 3,2 мг/мл, примерно 3,4 мг/мл, примерно 3,6 мг/мл, примерно 3,8 мг/мл, примерно 4,0 мг/мл, примерно 4,2 мг/мл, примерно 4,4 мг/мл, примерно 4,6 мг/мл, примерно 4,8 мг/мл, примерно 5,0 мг/мл, примерно 5,2 мг/мл, примерно 5,5 мг/мл, примерно 6,0 мг/мл, по меньшей мере примерно 0,8 мг/мл, по меньшей мере примерно 0,85 мг/мл, по меньшей мере примерно 0,9 мг/мл, по меньшей мере примерно 1,0 мг/мл, по меньшей мере примерно 1,1 мг/мл, по меньшей мере примерно 1,2 мг/мл, по меньшей мере примерно 1,3 мг/мл, по меньшей мере примерно 1,4 мг/мл, по меньшей мере примерно 1,5 мг/мл, по меньшей мере примерно 1,6 мг/мл, по меньшей мере примерно 1,7 мг/мл и т.д.
[097] Как уже ранее указывалось, описанная выше концентрация липида определяется, исходя из начального количества липида, которое используется для получения эмульсий. В данной области техники является очевидным, что фактическая концентрация масла в конечном продукте (например, упакованной, стерилизованной эмульсии, готовой для введения) может быть немного ниже, иногда на примерно 10%, до примерно 20%, до примерно 25% или до примерно 35%.
С. Соотношение масла к липиду
[098] Катионные эмульсии масло-в-воде по настоящему изобретению имеют определенное соотношение масло:липид. Например, соотношение масло:липид (моль:моль) в эмульсии может составлять по меньшей мере примерно 8:1 (моль:моль), по меньшей мере примерно 8,5:1 (моль:моль), по меньшей мере примерно 9:1 (моль:моль), по меньшей мере примерно 9,5:1 (моль:моль), по меньшей мере примерно 10:1 (моль:моль), по меньшей мере примерно 10,5:1 (моль:моль), по меньшей мере примерно 11:1 (моль:моль), по меньшей мере примерно 11,5:1 (моль:моль), по меньшей мере примерно 12:1 (моль:моль), по меньшей мере примерно 12,5:1 (моль:моль), по меньшей мере примерно 13:1 (моль:моль), по меньшей мере примерно 13,5:1 (моль:моль), по меньшей мере примерно 14:1 (моль:моль), по меньшей мере примерно 14,5:1 (моль:моль), по меньшей мере примерно 15:1 (моль:моль), по меньшей мере примерно 15,5:1 (моль:моль), по меньшей мере примерно 16:1 (моль:моль), по меньшей мере примерно 16,5:1 (моль:моль), по меньшей мере примерно 17:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 9:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 10:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 49:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 48:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 47:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 46:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 45:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 44:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 42:1 (моль:моль), от примерно 8:1 (моль:моль) до примерно 41:1 (моль:моль), от примерно 9:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 10:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 11:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 12:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 13:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 14:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 15:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 16:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 17:1 (моль:моль) до примерно 43:1 (моль:моль) и т.д.
[099] При необходимости, соотношение масло:липид (моль:моль) в эмульсии может составлять по меньшей мере примерно 4:1 (моль:моль), по меньшей мере примерно 4,2:1 (моль:моль), по меньшей мере примерно 4,5:1 (моль:моль), по меньшей мере примерно 5:1 (моль:моль), по меньшей мере примерно 5,5:1 (моль:моль), по меньшей мере примерно 6:1 (моль:моль), по меньшей мере примерно 6,5:1 (моль:моль), 7:1 (моль:моль), по меньшей мере примерно 7,5:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 5:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 6:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 7:1 (моль:моль) до примерно 50:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 49:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 48:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 47:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 46:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 45:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 44:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 42:1 (моль:моль), от примерно 4:1 (моль:моль) до примерно 41:1 (моль:моль), от примерно 5:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 6:1 (моль:моль) до примерно 43:1 (моль:моль), от примерно 7:1 (моль:моль) до примерно 43:1 (моль:моль) и т.п.
[0100] В некоторых случаях может возникнуть необходимость в нахождении баланса между желанием увеличить концентрацию катионного липида (увеличивая таким образом количество молекул нуклеиновой кислоты, загружаемой в частицу эмульсии) и токсичностью или переносимостью липида при введении in vivo. Например, имеются сообщения о том, что высокие дозы DOTAP могут иметь токсические эффекты. См., например, Lappalainen et al., Pharm. Res., vol. 11(8):1127-31 (1994). Клиницист может определить оптимальный диапазон количества липида в конкретной эмульсии, исходя из своего опыта и знаний.
[0101] Если масло содержит смесь молекул, молярную концентрацию масла можно рассчитать, исходя из средней молекулярной массы масла. Например, средняя молекулярная масса соевого масла (292,2) может быть вычислена, исходя из среднего распределения жирных кислот (12 масс.% пальмитиновой кислоты; 52 масс.% линоленовой кислоты; и т.д.), молекулярной массы каждого компонента.
С. Дополнительные компоненты
[0102] Описанные здесь катионные эмульсии масло-в-воде также могут содержать дополнительные компоненты. Например, эмульсии могут содержать компоненты, способствующие образованию частиц, улучшающие образование комплекса отрицательно заряженных молекул с катионными частицами или увеличивающие стабильность отрицательно заряженной молекулы (например, предотвращающие расщепление молекулы РНК). При необходимости, катионная эмульсия масло-в-воде может содержать антиоксидант, такой как цитрат, аскорбат или их соли.
Поверхностно-активные вещества (ПАВ)
[0103] В некоторых вариантах осуществления описанная здесь катионная эмульсия масло-в-воде дополнительно содержит ПАВ.
[0104] В фармацевтике используется достаточно большое количество ПАВ. Они включают встречающиеся в природе материалы, такие как смолы деревьев, растительные белки, полимеры на основе сахаров, такие как альгинаты, и т.п. Некоторые оксиполимеры или полимеры, углеродная цепь которых содержит гидроксид в качестве заместителя или другие гидрофильные заместители, представляют собой ПАВ, например, повидон, поливиниловый спирт и моно- и полифункциональные соединения на основе глицерина. В настоящем изобретении также можно использовать ионные или неионные детергенты и соединения, являющиеся производными жирных кислот с длинной цепью.
[0105] Конкретные примеры подходящих ПАВ включают следующие вещества:
[0106] 1. Водорастворимые мыла, такие как натриевые, калиевые, аммониевые и алканол-аммониевые соли высших жирных кислот (C10-C22), в частности, натриевые и калиевые мыла на основе таллового и кокосового масел.
[0107] 2. Анионные синтетические ПАВ, не являющиеся мылами, которые могут быть представлены водорастворимыми солями органических продуктов, получающихся в результате реакции с серной кислотой, содержащих в своей молекулярной структуре алкильный радикал, состоящий из примерно 8-22 атомов углерода, и радикал, выбранный из группы, состоящей из радикалов сульфоновой кислоты и сложных эфиров серной кислоты. Примерами этих веществ являются натриевые или калиевые алкилсульфаты, полученные из таллового или кокосового масла; натриевые или калиевые алкилбензольные сульфонаты; натриевые сульфонаты простых эфиров алкилглицерина; натриевые сульфонаты и сульфаты моноглицеридов жирных кислот кокосового масла; натриевые или калиевые соли сложных эфиров серной кислоты с продуктами реакции одного моля высшего жирного спирта и примерно 1-6 молей этиленоксида; натриевые или калиевые сульфонаты простых эфиров алкилфенола и этиленоксида, содержащие 1-10 звеньев этиленоксида на молекулу и в которых алкильные группы содержат от 8 до 12 атомов углерода; продукты реакции жирных кислот, этерифицированных изетионовой кислотой и нейтрализованных гидроксидом натрия; натриевые или калиевые соли амида жирных кислот метилтаурида; и натриевые и калиевые соли SO3-сульфонированных С10-С24 α-олефинов.
[0108] 3. Неионогенные синтетические ПАВ, полученные конденсацией алкиленоксидных групп с органическим гидрофобным соединением. Типичные гидрофобные группы включают продукты конденсации пропиленоксида с пропиленгликолем, алкильными фенолами, продукт конденсации пропиленоксида и этилендиамина, алифатические спирты, содержащие 8-22 атомов углерода, и амиды жирных кислот.
[0109] 4. Неионогенные ПАВ, такие как оксиды аминов, оксиды фосфинов и сульфоксиды, имеющие донорно-акцепторные характеристики. Конкретные примеры оксидов третичных аминов с длинной цепью включают оксид диметилдодециламина и бис-(2-гидроксиэтил)додециламин. Конкретные примеры оксидов фосфинов раскрыты в патенте США 3304263, выданном 14 февраля 1967 г., и включают оксид диметилдодецилфосфина и оксид диметил-(2-гидроксидодецил)фосфина.
[0110] 5. Сульфоксиды с длинной цепью, в том числе и те, которые соответствуют формуле R1-SO-R2, где R1 и R2 представляют собой замещенные или незамещенные алкильные радикалы, где R1 содержат от примерно 10 до примерно 28 томов углерода, а R2 содержит от 1 до 3 атомов углерода. Конкретные примеры этих сульфоксидов включают додецилметилсульфоксид и 3-гидрокситридецилметилсульфоксид.
[0111] 6. Амфолитные синтетические ПАВ, такие как натрия 3-додециламинопропионат и натрия 3-додециламинопропан сульфонат.
[0112] 7. Цвиттерионные синтетические ПАВ, такие как 3-(N,N-диметил-N-гексадециламмонио)пропан-1-сульфонат и 3-(N,N-диметил-N-гексадециламмонио)-2-гидроксипропан-1-сульфонат.
[0113] Помимо этого, в композиции по настоящему изобретению могут быть использованы все приведенные ниже типы ПАВ: (a) мыла (т.е. соли щелочных металлов) жирных кислот, смоляные кислоты и талловое масло; (b) алкиларенсульфонаты; (c) алкилсульфаты, в том числе ПАВ, содержащие гидрофобные группы как с разветвленной цепью, так и прямой цепью, а также группы первичных и вторичных сульфатов; (d) сульфаты и сульфонаты, содержащие промежуточную связь между гидрофобными и гидрофильными группами, такие как жирные ацилированные метилтауриды и сульфатированные жирные моноглицериды; (e) эфиры длинноцепочечных кислот и полиэтиленгликоля, в частности, сложные эфиры таллового масла; (f) эфиры полиэтиленгликоля с алкилфенолами; (g) эфиры полиэтиленгликоля с длинноцепочечными спиртами и меркаптанами; и (h) жирные ацилдиэтаноламиды. Поскольку ПАВ могут быть классифицированы более чем одним способом, несколько классов ПАВ, приведенных в этом параграфе, пересекаются с ранее описанными классами ПАВ.
[0114] Существует несколько видов ПАВ, специально предназначенных и широко используемых в области биологии. Такие ПАВ можно разделить на четыре основных типа: анионные, катионные, цвиттерионные (амфотерные) и неионогенные. Типичные анионные ПАВ включают, например, перфтороктаноат (PFOA или PFO), перфтороктансульфонат (ПФОС), алкилсульфаты, такие как додецилсульфат натрия (SDS) или лаурилсульфат аммония, лауретсульфат натрия (также известный как эфир лаурилсульфата натрия, SLES), алкилбензолсульфонат и соли жирных кислот. Примеры катионных ПАВ включают, например, соли алкилтриметиламмония, такие как цетилтриметиламмония бромид (СТАВ, или гексадецилтриметиламмония бромид), цетилпиридиния хлорид (CPC), полиэтоксилированный амин таловой кислоты (POEA), хлорид бензалкония (ВАС), бензетония хлорид (BZT). Примеры цвиттерионных (амфотерных) ПАВ включают, например, додецилбетаин, кокамидопропилбетаин и кокоамфоглицинат. Типичные неионогенные ПАВ включают, например, алкил-поли(этиленоксид), алкилфенол-поли(этиленоксид), сополимеры поли(этиленоксида) и поли(пропиленоксида) (известные на рынке как полоксамеры или полоксамины), арил полиглюкозиды (например, октилглюкозид или децилмальтозид), жирные спирты (например, цетиловый спирт или олеиловый спирт), кокамид МЕА, кокамид DEA, Pluronic© F-68 (блок-сополимер полиоксиэтилена и полиоксипропилена) и полисорбаты, такие как Tween® 20 (полисорбат 20), Tween® 80 (полисорбат 80; полиоксиэтиленсорбитан моноолеат), додецил диметиламина оксид и витамин Е токоферола пропиленгликоль сукцинат (витамин Е TPGS).
[0115] Наиболее предпочтительной группой ПАВ являются неионогенные ПАВ на основе сорбитана. Эти ПАВ получают дегидратацией сорбита для получения 1,4-сорбитана, который затем подвергают взаимодействию с одним или несколькими эквивалентами жирной кислоты. Затем можно осуществить дополнительную реакцию этого фрагмента замещенной жирной кислоты с этиленоксидом для получения второй группы ПАВ.
[0116] ПАВ на основе сорбитана, замещенного жирной кислотой, получают взаимодействием 1,4-сорбитана с жирной кислотой, такой как лауриновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота или аналогичная длинноцепочечная жирная кислота, с получением моноэфира 1,4-сорбитана, сесквиэфира 1,4-сорбитана или триэфира 1,4-сорбитана. Общепринятые названия этих ПАВ включают, например, монолаурат сорбитана, монопальмитат сорбитана, моностеарат сорбитана, моноолеат сорбитана, сесквиолеат сорбитана и триолеат сорбитана. Эти ПАВ представлены на рынке под торговой маркой Span® или Arlacel®, как правило, с обозначением буквы или числа, по которому отличают различные моно-, ди- и триэфиры замещенных сорбитанов.
[0117] ПАВ SPAN® и Arlacel® являются гидрофильными и, как правило, растворимыми или диспергируемыми в масле. Они также растворимы в большинстве органических растворителей. Эти вещества обычно являются нерастворимыми, но диспергируемыми в воде. Как правило, гидрофильно-липофильный баланс (ГЛБ) этих ПАВ находится в диапазоне от 1,8 до 8,6. Такие ПАВ могут быть легко получены способами, известными в данной области, или являются коммерчески доступными.
[0118] Родственная группа ПАВ включает моноэфиры полиоксиэтилен-сорбитана и триэфиры полиоксиэтилен-сорбитана. Эти вещества получают присоединением этиленоксида к моноэфиру или триэфиру 1,4-сорбитана. Добавление полиоксиэтилена превращает липофильное ПАВ на основе моно- или триэфира сорбитана в гидрофильное ПАВ, обычно растворимое или диспергируемое в воде и в разной степени растворимое в органических жидкостях.
[0119] Эти вещества, доступные на рынке под торговой маркой Tween®, пригодны для получения эмульсий и дисперсий масло-в-воде или для растворения масел и приготовления безводных растворимых в воде или смываемых мазей. Для увеличения стабильности эмульсии ПАВ Tween® могут быть объединены с родственными ПАВ на основе моноэфира или триэфира сорбитана. Значение ГЛБ ПАВ Tween®, как правило, находится в диапазоне от 9,6 до 16,7. ПАВ Tween® являются коммерчески доступными.
[0120] Третья группа неионогенных ПАВ, которые могут быть использованы по отдельности или в сочетании с ПАВ SPAN©, ARLACEL® и Tween®, являются жирными кислотами на основе полиоксиэтилена, полученными в результате реакции этиленоксида с длинноцепочечной жирной кислотой. Наиболее известное ПАВ этого типа, доступное под названием MYRJ®, является твердым полиоксиэтилен-производным стеариновой кислоты. ПАВ MYRJ® являются гидрофильными и растворимыми или диспергируемыми в воде, аналогично таким ПАВ, как Tween®. Для получения эмульсий ПАВ MYRJ® могут быть смешаны с ПАВ Tween® или со смесью ПАВ Tween®/SPAN® или Arlacel®. ПАВ MYRJ® могут быть получены способами, известными в данной области, или являются коммерчески доступными.
[0121] Четвертая группа неионогенных ПАВ на основе полиоксиэтилена представляет собой сложные эфиры полиоксиэтилена жирных кислот, полученные из лауриловых, ацетиловых, стеариловых и олеиловых спиртов. Эти вещества получают, как описано выше, добавлением этиленоксида к жирному спирту. Эти ПАВ известны на рынке под торговой маркой BRIJ®. ПАВ BRIJ® могут быть гидрофильными или липофильными в зависимости от размера полиоксиэтиленового фрагмента в ПАВ. Хотя в данной области известны способы их получения, их также можно приобрести на рынке у производителей.
[0122] Другие неионогенные ПАВ, которые могут быть потенциально использованы, представляют собой, например, полиоксиэтилен, сложные эфиры полиолов и жирных кислот, полиоксиэтиленовый эфир, эфиры полиоксипропилена и жирных кислот, полиоксиэтилированные производные пчелиного воска, производное полиоксиэтиленланолина, полиоксиэтиленовые глицериды жирных кислот, сложные эфиры глицерина и жирных кислот или другого полиоксиэтиленового спирта или производные эфиров длинноцепочечных жирных кислот, содержащих от 12 до 22 атомов углерода.
[0123] В качестве эмульсий и препаративных форм по изобретению используются многофазные системы, предпочтительным является выбор неионогенного образующего эмульсию ПАВ, значение ГЛБ которого находится в интервале от примерно 7 до 16. Это значение может быть получено путем использования одного неионогенного ПАВ, такого как ПАВ Tween®, или может быть получено путем использования смеси ПАВ, таких как ПАВ на основе моно-, ди- или триэфира сорбитана; сложного эфира полиоксиэтиленсорбитана и жирной кислоты; сложного эфира сорбитана в комбинации с ПАВ на основе производного полиоксиэтиленланолина; ПАВ на основе сложного эфира сорбитана в комбинации с ПАВ на основе эфира полиоксиэтиленовой жирной кислоты, имеющего высокое значение ГЛБ; или ПАВ на основе полиэтиленового эфира или эфира полиоксиэтиленсорбитана и жирной кислоты.
[0124] В некоторых вариантах осуществления эмульсия содержит одно неионогенное ПАВ, в частности, ПАВ Tween®, в качестве неионогенного ПАВ, стабилизирующего эмульсию. В иллюстративном варианте осуществления эмульсия содержит Tween® 80, иначе известный как полисорбат 80, или полиоксиэтилен 20 сорбитана моноолеат. В других вариантах осуществления эмульсия содержит два или более неионогенных ПАВ, в частности, ПАВ Tween® и ПАВ SPAN®. В иллюстративном варианте осуществления эмульсия содержит Tween® 80 и SPAN® 85.
[0125] Эмульсии масло-в-воде могут содержать от примерно 0,01% до примерно 2,5% ПАВ (масс./об.), от примерно 0,01% до примерно 2% ПАВ, от 0,01% до примерно 1,5% ПАВ, от 0,01% до примерно 1% ПАВ, от 0,01% до примерно 0,5% ПАВ, от 0,05% до примерно 0,5% ПАВ, от 0,08% до примерно 0,5% ПАВ, примерно 0,08% ПАВ, примерно 0,1% ПАВ, примерно 0,2% ПАВ, примерно 0,3% ПАВ, примерно 0,4% ПАВ, примерно 0,5% ПАВ, примерно 0,6% ПАВ, примерно 0,7% ПАВ, примерно 0,8% ПАВ, примерно 0,9% ПАВ или примерно 1% ПАВ.
[0126] Альтернативно или дополнительно, эмульсии масло-в-воде могут содержать от 0,05% до примерно 1%, от 0,05% до примерно 0,9%, от 0,05% до примерно 0,8%, от 0,05% до примерно 0,7%, от 0,05% до примерно 0,6%, от 0,05% до примерно 0,5%, примерно 0,08%, примерно 0,1%, примерно 0,2%, примерно 0,3%, примерно 0,4%, примерно 0,5%, 0,6%, 0,7%, 0,8%, 0,9% или примерно 1% (масс./об.) Tween® 80 (полисорбат 80; полиоксиэтилен сорбитана моноолеат).
[0127] В иллюстративном варианте осуществления эмульсия масло-в-воде содержит 0,08% (масс./об.) Tween® 80 (полисорбат 80; полиоксиэтилен сорбитана моноолеат).
[0128] Альтернативно или дополнительно, эмульсии масло-в-воде могут содержать от 0,05% до примерно 1%, от 0,05% до примерно 0,9%, от 0,05% до примерно 0,8%, от 0,05% до примерно 0,7%, от 0,05% до примерно 0,6%, от 0,05% до примерно 0,5%, примерно 0,08%, примерно 0,1%, примерно 0,2%, примерно 0,3%, примерно 0,4%, примерно 0,5%, примерно 0,6%, примерно 0,7%, примерно 0,8%, примерно 0,9% или примерно 1% (масс./об.) SPAN 85 (сорбитан триолеат).
[0129] Эмульсии масло-в-воде могут содержать комбинацию описанных здесь ПАВ. Например, может быть использована комбинация Tween 80 (полисорбат 80; полиоксиэтилен сорбитана моноолеат) и SPAN 85 (сорбитана триолеат). Эмульсии могут содержать разные (например, см. приведенные выше примеры) или равные количества Tween 80 и SPAN 85. Например, эмульсии масло-в-воде могут содержать (масс./об.) примерно 0,05% Tween 80 и примерно 0,05% SPAN 85, примерно 0,1% Tween 80 и примерно 0,1% SPAN 85, примерно 0,2% Tween 80 и примерно 0,2% SPAN 85, примерно 0,3% Tween 80 и примерно 0,3% SPAN 85, примерно 0,4% Tween 80 и примерно 0,4% SPAN 85, примерно 0,5% Tween 80 и примерно 0,5% SPAN 85, примерно 0,6% Tween 80 и примерно 0,6% SPAN 85, примерно 0,7% Tween 80 и примерно 0,7% SPAN 85, примерно 0,8% Tween 80 и примерно 0,8% SPAN 85, примерно 0,9% Tween 80 и примерно 0,9% SPAN 85 или примерно 1% Tween 80 и примерно 1,0% SPAN 85.
[0130] В некоторых вариантах осуществления ПАВ представляет собой полиэтиленгликоль (ПЭГ)-липид. В других вариантах осуществления эмульсия не содержит ПЭГ-липида. В качестве ПАВ также могут быть использованы ПЭГ-липиды, такие как ПЭГ, присоединенный к диалкилоксипропилам (ПЭГ-ДАО), ПЭГ, присоединенный к диацилглицерину (ПЭГ-ДАГ), ПЭГ, присоединенный к фосфатидилэтаноламину (ФЭ) (ПЭГ-ФЭ), или некоторым другим фосфолипидам (ПЭГ-фосфолипиды), ПЭГ, конъюгированный с церамидами (ПЭГ-Церамид), или их комбинации (см., например, патент США № 5885613; публикации заявок на патент США №2003/0077829, 2005/0175682 и 2006/0025366). Другие подходящие ПЭГ-липиды включают, например, ПЭГ-диалкилоксипропиловые (ДАО) липиды или ПЭГ-диацилглицериновые (ДАГ) липиды. Иллюстративные ПЭГ-ДАГ липиды включают, например, ПЭГ-дилауроилглицериновые (C12) липиды, ПЭГ-димиристоилглицериновые (C14) липиды, ПЭГ-дипальмитоилглицериновые (C16) липиды или ПЭГ- дистеароилглицериновые (C18) липиды. Иллюстративные липиды ПЭГ-ДАО включают, например, ПЭГ-дилауроилоксипропиловые (C12) липиды, ПЭГ-димиристилоксипропиловые (C14) липиды, ПЭГ-дипальмитилоксипропиловые (C16) липиды или ПЭГ-дистеарилоксипропиловые (C18) липиды.
[0131] ПЭГ классифицируют по их молекулярной массе, например, ПЭГ 2000 имеет среднюю молекулярную массу, равную примерно 2000 дальтон, а ПЭГ 5000 имеет среднюю молекулярную массу, равную примерно 5000 дальтон. ПЭГ можно приобрести у фирмы Sigma Chemical Co, а также у других компаний, и они включают, например, следующие соединения: монометоксиполиэтиленгликоль (MePEG-OH), монометоксиполиэтиленгликоль-сукцинат (MePEG-S), монометоксиполиэтиленгликоль-сукцинимидил сукцинат (MePEG-S-NHS), монометоксиполиэтиленгликоль-амин (MePEG-NH2), монометоксиполиэтиленгликоль-трезилат (MePEG-TRES) и монометоксиполиэтиленгликоль-имидазолил-карбонил (MePEG-IM). Кроме того, монометоксиполиэтиленгликоль уксусной кислоты (MePEG-CH2COOH) является предпочтительным для получения конъюгатов ПЭГ-липид, включая, например, конъюгаты ПЭГ-ДАО.
D. Водная фаза (непрерывная фаза)
[0132] Водная фаза (непрерывная фаза) эмульсий масло-в-воде представляет собой воду или водный раствор, который может содержать соль (например, NaCl), буфер (например, цитратный буфер), неионный регулирующий тоничность агент (например, сахарид), полимер, ПАВ или любую их комбинацию. Водная фаза эмульсий до комплексообразования (эмульсии масло-в-воде перед добавлением отрицательно заряженных молекул) может отличаться от водной фазы эмульсий после комплексообразования (эмульсии масло-в-воде, в которых отрицательно заряженные молекулы образуют комплекс с частицами эмульсии). В общем случае, эмульсии до комплексообразования получают в водном растворителе, который способствует образованию частиц с требуемыми свойствами (например, средним диаметром и т.п.). Эмульсии до комплексообразования разбавляют водным раствором, который содержит отрицательно заряженные молекулы и другие необходимые компоненты, для получения конечной катионной эмульсии масло-в-воде, которая содержит конечную водную фазу, имеющую требуемую осмолярность и тоничность. Водная фаза может содержать антиоксидант, такой как цитрат, аскорбат или его соли.
[0133] При получении препаративной формы на основе эмульсий для in vivo введения предпочтительно, чтобы приготовленный конечный раствор эмульсии имел тоничность и осмолярность по существу такую же, как у нормальных физиологических жидкостей, для предотвращения нежелательных последствий, возникающих после введения, таких как набухание или быстрая абсорбция композиции. Также предпочтительно забуферить водную фазу для поддержания рН на уровне, совместимом с нормальными физиологическими условиями. Кроме того, в некоторых случаях желательно поддерживать рН на определенном уровне для обеспечения стабильности некоторых компонентов эмульсии. Например, может быть желательным получение изотонической и изоосмотической эмульсии. Для регулирования тоничности эмульсия может содержать физиологическую соль, такую как натриевая соль. Хлорид натрия (NaCl), например, может быть использован в количестве примерно 0,9% (масс./об.) (физиологический солевой раствор). Другие соли, которые могут присутствовать, включают хлорид калия, дигидрофосфат калия, динатрия фосфат, хлорид магния, хлорид кальция и т.д. Для регулирования тоничности также могут быть использованы неионные регулирующие тоничность агенты. Количество неионных регулирующих тоничность агентов обычно известно специалистам в данной области. Эти агенты, как правило, представляют собой углеводы согласно различным классификациям (см., например, Voet и Voet (1990), Biochemistry (John Wiley & Sons, New York). В качестве неионных регулирующих тоничность агентов в настоящем изобретении могут быть использованы моносахариды, классифицированные как альдозы, такие как глюкоза, манноза, арабиноза, рибоза, а также классифицированные как кетозы, такие как фруктоза, сорбоза и ксилоза. Также могут быть использованы дисахариды, такие как сахароза, мальтоза, трегалоза и лактоза. Кроме того, к неионным регулирующим тоничность агентам, используемым в настоящем изобретении, также относятся альдитолы (ациклические полигидроксиспирты, также называемые сахарными спиртами), такие как глицерин, маннит, ксилит и сорбит. Неионные регулирующие тоничность агенты могут присутствовать в концентрации от примерно 0,1% до примерно 10% или от примерно 1% до примерно 10%, в зависимости от используемого агента.
[0134] Водная фаза может быть забуференной. В настоящем изобретении может быть использован любой физиологически приемлемый буфер, такой как вода, цитратный буфер, фосфатный буфер, ацетатный буфер, трис буфер, бикарбонатный буфер, карбонатный буфер, сукцинатный буфер или т.д. Значение рН водного компонента предпочтительно находится в пределах между 6,0-8,0, более предпочтительно от примерно 6,2 до примерно 6,8. В иллюстративном варианте осуществления буфер представляет собой 10 мМ цитратный буфер с рН 6,5. В другом иллюстративном варианте водную фазу или буфер получают, используя воду, не содержащую РНКазы или обработанную DEPC. В некоторых случаях высокое содержание соли в буфере может мешать комплексообразованию отрицательно заряженных молекул с частицами эмульсии, следовательно, этого следует избегать. В других случаях в буфере может содержаться некоторое количество соли.
[0135] В иллюстративном варианте осуществления буфер представляет собой 10 мМ цитратный буфер с рН 6,5. При необходимости, водную фазу или буфер получают, используя воду, не содержащую РНКазы или обработанную DEPC.
[0136] Водная фаза может также содержать дополнительные компоненты, такие как молекулы, которые изменяют осмолярность водной фазы, или молекулы, которые стабилизируют отрицательно заряженные молекулы после комплексообразования. Предпочтительно, осмолярность водной фазы регулируют, используя неионный регулирующий тоничность агент, такой как сахар (например, трегалозу, сахарозу, декстрозу, фруктозу, восстановленную палатинозу и т.д.), сахарный спирт (например, маннит, сорбит, ксилит, эритрит, лактит, мальтит, глицерин и т.д.). При необходимости может быть использован неионный полимер (например, поли(алкилгликоль), такой как полиэтиленгликоль, полипропиленгликоль или полибутиленгликоль) или неионогенное ПАВ.
[0137] В некоторых вариантах осуществления водная фаза катионной эмульсии масло-в-воде может содержать полимер или ПАВ или их комбинацию. В иллюстративном варианте осуществления эмульсия масло-в-воде содержит полоксамер. Полоксамеры представляют собой неионные трехблочные полимеры, имеющие центральную гидрофобную цепь полиоксипропилена (поли(пропиленоксид)), фланкированную двумя гидрофильными цепями полиоксиэтилена (поли(этиленоксид)). Полоксамеры также известны под торговым названием Pluronic® (плюрониевые) полимеры. Полоксамеры могут обеспечивать улучшенную стабильность и увеличенную устойчивость молекулы РНК к РНКазе после образования РНК-комплексов.
[0138] Альтернативно или дополнительно, катионная эмульсия масло-в-воде может содержать от примерно 0,1% до примерно 20% (масс./об.) полимера или от примерно 0,05% до примерно 10% (масс./об.) полимера. Например, катионная эмульсия масло-в-воде может содержать полимер (например, полоксамер, такой как Pluronic® F127 ((блок-сополимер этиленоксид/пропиленоксид: Н(ОСН2СН2)х(ОСН3СН(СН3))y(ОСН2СН2)zOH)) в количестве от примерно 0,1% до примерно 20% (масс./об.), от примерно 0,1% до примерно 10% (масс./об.), от примерно 0,05% до примерно 10% (масс./об.) или от примерно 0,05% до примерно 5% (масс./об.).
[0139] В иллюстративном варианте осуществления эмульсия масло-в-воде содержит около 4% (масс./об.) или примерно 8% (масс./об.) Pluronic® F127.
[0140] Количество водного компонента, используемого в этих композициях, представляет собой количество, необходимое для доведения количества композиции до единицы. Другими словами, количество водного компонента, смешиваемого с другими перечисленными выше компонентами, должно быть достаточным для получения 100% нужного объема композиций.
4. Отрицательно заряженные молекулы
[0141] При добавлении отрицательно заряженных молекул, они могут образовывать комплекс с частицами катионных эмульсий масло-в-воде. Отрицательно заряженные молекулы образуют комплекс с частицами эмульсии, например, благодаря взаимодействию между отрицательно заряженной молекулой и катионным липидом на поверхности частиц, а также гидрофобным/гидрофильным взаимодействиям между отрицательно заряженной молекулой и поверхностью частиц. Не углубляясь в какую-либо конкретную теорию, предполагается, что отрицательно заряженные молекулы взаимодействуют с катионным липидом посредством нековалентного взаимодействия между заряженными ионами (электростатические силы), и прочность комплекса, а также количество отрицательно заряженного соединения, которое может образовывать комплекс с частицей, связана с количеством катионного липида в частице. Кроме того, гидрофобные/гидрофильные взаимодействия между отрицательно заряженной молекулой и поверхностью частиц также могут играть роль.
[0142] Примеры отрицательно заряженных молекул включают отрицательно заряженные пептиды, полипептиды или белки, молекулы нуклеиновых кислот (например, одно- или двухцепочечной РНК или ДНК), малые молекулы (например, малая молекула иммунных потенциаторов (SMIP), фосфонат, фторфосфонат и т.д.) и т.п. В предпочтительных аспектах отрицательно заряженная молекула представляет собой молекулу РНК, такой как РНК, кодирующей пептид, полипептид или белок, включая самореплицирующиеся молекулы РНК или малые интерферирующие РНК.
[0143] Комплекс может быть образован способами, известными в данной области, примеры которых приведены в описании. Например, комплекс нуклеиновая кислота-частица может быть образован путем смешивания катионной эмульсии с молекулами нуклеиновой кислоты, например, путем встряхивания. Количество отрицательно заряженных молекул и катионного липида в эмульсиях может быть изменено или оптимизировано для обеспечения требуемой прочности связывания и связывающей способности. Например, как описано здесь и продемонстрировано в примерах, иллюстративные комплексы РНК-частица были получены путем изменения соотношений РНК:катионный липид (представленного в виде "соотношение N/P"). Термин “соотношение N/P” относится к количеству (моль) протонируемых атомов азота в катионном липиде, деленному на количество (моль) фосфатов в РНК.
[0144] Предпочтительное соотношение N/P составляет от примерно 1:1 до примерно 20:1, от примерно 2:1 до примерно 18:1, от примерно 3:1 до 16:1, от примерно 4:1 до примерно 14:1, от примерно 6:1 до примерно 12:1, примерно 3:1, примерно 4:1, примерно 5:1, примерно 6:1, примерно 7:1, примерно 8:1, примерно 9:1, примерно 10:1, примерно 11:1, примерно 12:1, примерно 13:1, примерно 14:1, примерно 15:1 или примерно 16:1. Кроме того, предпочтительные соотношения N/P составляют, по меньшей мере, примерно 3:1, по меньшей мере, примерно 4:1, по меньшей мере, примерно 5:1, по меньшей мере, примерно 6:1, по меньшей мере, примерно 7:1, по меньшей мере, примерно 8:1, по меньшей мере примерно 9:1, по меньшей мере, примерно 10:1, по меньшей мере примерно 11:1, по меньшей мере примерно 12:1, по меньшей мере примерно 13:1, по меньшей мере примерно 14:1, по меньшей мере, примерно 15:1 или по меньшей мере примерно 16:1. Более предпочтительное соотношение N/P составляет примерно 4:1 или более.
[0145] Каждая эмульсия может иметь свое собственное оптимальное или предпочтительное соотношение N/P для получения желаемого эффекта (например, требуемого уровня экспрессии РНК в комплексе), которое может быть определено экспериментально (например, при помощи описанных здесь анализов или других методов, известных в данной области, таких как измерение уровня экспрессии белка, кодируемого РНК, или измерение процента молекул РНК, высвобождаемых из комплекса в присутствии гепарина). Как правило, соотношение N/P должно быть на уровне, при котором по меньшей мере примерно 5%, примерно 10%, примерно 15%, примерно 20%, примерно 25%, примерно 30%, примерно 35%, примерно 40%, примерно 45%, примерно 50%, примерно 55%, примерно 60%, примерно 65%, примерно 70%, примерно 75%, примерно 80%, примерно 85%, примерно 90% или примерно 95% молекул РНК высвобождается из комплексов РНК-частица, когда комплексы РНК-частица поглощаются клетками. В некоторых вариантах осуществления соотношение N/P представляет собой значение, которое обеспечивает высвобождение по меньшей мере 0,5% или по меньшей мере 1% молекул РНК из комплексов РНК-частица при поглощении комплексов РНК-частица клетками.
[0146] Уровень экспрессии антигена, кодируемого молекулой РНК, не обязательно коррелирует с иммуногенностью антигена. В таких случаях оптимальное или предпочтительное для обеспечения иммуногенности соотношение N/Р может быть определено, например, измерением конкретных титров антител.
[0147] Описанные здесь катионные эмульсии масло-в-воде являются особенно подходящими для составления вакцин на основе нуклеиновой кислоты (например, ДНК-вакцин, РНК-вакцин). Образование комплекса нуклеиновая кислота-частица эмульсии облегчает поглощение нуклеиновой кислоты клеткой-хозяином и защищает молекулу нуклеиновой кислоты от разрушения нуклеазой. После этого трансфицированные клетки могут экспрессировать кодируемый молекулой нуклеиновой кислоты антиген, который может вызывать иммунный ответ на этот антиген. Подобно живым или ослабленным вирусам, вакцины на основе нуклеиновых кислот могут эффективно активизировать системы как MHC-I, так и MHC-II класса, позволяющие индуцировать CD8+ и CD4+ Т-клеточный ответ, тогда как антиген, присутствующий в растворимой форме, например, в виде рекомбинантного белка, как правило, приводит только к образованию антител.
[0148] В некоторых вариантах описанная здесь отрицательно заряженная молекула представляет собой молекулу РНК. В некоторых вариантах осуществления молекула РНК кодирует антиген (пептид, полипептид или белок), и катионная эмульсия масло-в-воде является подходящей для использования в качестве вакцины на основе РНК. Композиция может содержать более одного вида молекул РНК, кодирующих антиген, например, два, три, пять или десять различных видов молекул РНК, которые находятся в комплексе с частицами эмульсии. Другими словами, композиция может содержать один или несколько различных видов молекул РНК, каждый из которых кодирует другой антиген. Альтернативно или дополнительно, одна молекула РНК также может кодировать более одного антигена, например, бицистронная или трицистронная молекула РНК, которая кодирует разные или идентичные антигены. Соответственно, катионная эмульсия масло-в-воде является подходящей для использования в качестве вакцины на основе РНК, т.е. моновалентной или поливалентной вакцины. При необходимости, молекула РНК может быть полицистронной.
[0149] Последовательность молекулы РНК может быть оптимизирована или не оптимизирована по кодонам для обеспечения экспрессии в желаемом хозяине, таком как человеческая клетка.
[0150] Последовательность молекулы РНК при необходимости может быть модифицирована, например, для увеличения эффективности экспрессии или репликации РНК или для обеспечения дополнительной стабильности или устойчивости к расщеплению. Например, последовательность РНК может быть модифицирована в отношении использования кодонов, например, для увеличения эффективности трансляции и периода полувыведения молекулы РНК. С целью увеличения времени полувыведения к 3'-концу РНК может быть присоединен поли-А "хвост" (поли-А последовательность) (например, около 30 или более остатков аденозина) (SEQ ID NO:28). 5'-конец молекулы РНК может быть кэпирован модифицированным рибонуклеотидом, имеющим структуру m7G (5')ррр(5')N (структура "кэп 0") или его производным, которое может быть включено в процессе синтеза РНК или может быть создано при участии ферментов после транскрипции РНК (например, при помощи фермента кэпирующего вирус осповакцины (VCE), состоящего из мРНК трифосфатазы, гуанилил-трансферазы и гуанин-7-метилтрансферазы, который катализирует образование структур N7-монометилированного кэпа 0). Структура "кэп 0" играет важную роль в поддержании стабильности и эффективности трансляции молекулы РНК. 5'-кэп молекулы РНК может быть дополнительно модифицирован 2'-О-метилтрансферазой, что приводит к образованию структуры "кэп 1" (m7Gppp[m2'-O]N), которая может дополнительно увеличивать эффективность трансляции.
[0151] При необходимости, молекула РНК может содержать один или несколько модифицированных нуклеотидов дополнительно к любой структуре 5'-кэпа. Существует более 96 природных модификаций нуклеозидов, которые были обнаружены у РНК млекопитающих. См., например, Limbach et al., Nucleic Acids Research, 22(12):2183-2196 (1994). Способы получения нуклеотидов и модифицированных нуклеотидов и нуклеозидов хорошо известны в данной области, например, раскрыты в патентах США 4373071, 4458066, 4500707, 4668777, 4973679, 5047524, 5132418, 5153319, 5262530 и 5700642, которые включены в виде ссылки во всей своей полноте в данное описание, и многие модифицированные нуклеозиды и модифицированные нуклеотиды являются коммерчески доступными.
[0152] Модифицированные основания нуклеиновых кислот, которые могут быть включены в модифицированных нуклеозиды и нуклеотиды и присутствовать в молекуле РНК, включают следующие: m5C (5-метилцитидин), m5U (5-метилуридин), m6A (N6-метиладенозин), s2U (2-тиоуридин), Um (2'-O-метилуридин), m1A (1-метиладенозин); m2A (2-метиладенозин); Am (2-1-O-метиладенозин); ms2m6A (2-метилтио-N6-метиладенозин); i6A (N6-изопентениладенозин); ms2i6A (2-метилтио-N6-изопентениладенозин); io6A (N6-(цис-гидроксиизопентенил)аденозин); ms2io6A (2-метилтио-N6-(цис-гидроксиизопентенил)аденозин); g6A (N6-глицинилкарбамоиладенозин); t6A (N6-треонилкарбамоиладенозин); ms2t6A (2-метилтио-N6-треонилкарбамоиладенозин); m6t6A (N6-метил-N6-треонилкарбамоиладенозин); hn6A (N6-гидроксинорвалилкарбамоиладенозин); ms2hn6A (2-метилтио-N6-гидроксинорвалилкарбамоиладенозин); Ar(р) (2'-O-рибозиладенозин(фосфат)); I (инозин); m1I (1-метилинозин); m'Im (1,2'-O-диметилинозин); m3C (3-метилцитидин); Cm (2T-O-метилцитидин); s2C (2-тиоцитидин); ac4C (N4-ацетилцитидин); f5C (5-фоннилцитидин); m5Cm (5,2-О-диметилцитидин); ac4Cm (N4-ацетил-2TO-метилцитидин); k2C (лизидин); m1G (1-метилгуанозин); m2G (N2-метилгуанозин); m7G (7-метилгуанозин); Gm (2'-O-метилгуанозин); m22G (N2,N2-диметилгуанозин); m2Gm (N2,2'-O-диметилгуанозин); m22Gm (N2,N2,2'-O-триметилгуанозин); Gr(р) (2'-O-рибозилгуанозин(фосфат)); yW (вибутозин); o2yW (пероксивибутозин); OHyW (гидроксивибутозин); OHyW* (немодифицированный гидроксивибутозин); imG (виозин); mimG (метилгуанозин), Q (квеуозин); oQ (эпоксиквеуозин); galQ (галактозил-квеуозин); manQ (маннозил-квеуозин); preQo (7-циано-7-деазагуанозин); preQi (7-аминометил-7-деазагуанозин); G* (архаэозин); D (дигидроуридин); m5Um (5,2'-O-диметилуридин); s4U (4-тиоуридин); m5s2U (5-метил-2-тиоуридин); s2Um (2-тио-2'-O-метилуридин); acp3U (3-(3-амино-3-карбоксипропил)уридин); ho5U (5-гидроксиуридин); mo5U (5-метоксиуридин); cmo5U (уридин 5-оксиуксусной кислоты); mcmo5U (уридин метил-5-оксиуксусной кислоты); chm5U (5-(карбоксигидроксиметил)уридин)); mchm5U (5-(карбоксигидроксиметил)уридин метиловый эфир); mcm5U (5-метоксикарбонилметилуридин); mcm5Um (S-метоксикарбонилметил-2-O-метилуридин); mcm5s2U (5-метоксикарбонилметил-2-тиоуридин); nm5s2U (5-аминометил-2-тиоуридин); mnm5U (5-метиламинометилуридин); mnm5s2U (5-метиламинометил-2-тиоуридин); mnm5se2U (5-метиламинометил-2-селеноуридин); ncm5U (5-карбамоилметилуридин); ncm5Um (5-карбамоилметил-2'-O-метилуридин); cmnm5U (5-карбоксиметиламинометилуридин); cnmm5Um (5-карбоксиметиламинометил-2-L-O-метилуридин); cmnm5s2U (5-карбоксиметиламинометил-2-тиоуридин); m62A (N6,N6-диметиладенозин); Tm (2'-O-метилинозин); m4C (N4-метилцитидин); m4Cm (N4,2-O-диметилцитидин); hm5C (5-гидроксиметилцитидин); m3U (3-метилуридин); cm5U (5-карбоксиметилуридин); m6Am (N6,Т-O-диметиладенозин); rn62Am (N6,N6,O-2-триметиладенозин); m2'7G (N2,7-диметилгуанозин); m2'2'7G (N2,N2,7-триметилгуанозин); m3Um (3,2Т-O-диметилуридин); m5D (5-метилдигидроуридин); f5Cm (5-формил-2'-O-метилцитидин); m1Gm (1,2'-O-диметилгуанозин); m'Am (1,2-O-диметиладенозин)иринометилуридин); tm5s2U (S-тауринометил-2-тиоуридин)); imG-14 (4-деметилгуанозин); imG2 (изогуанозин); ac6A (N6-ацетиладенозин), гипоксантин, инозин, 8-оксо-аденин, 7-замещенные производные, дигидроурацил, псевдоурацил, 2-тиоурацил, 4-тиоурацил, 5-аминоурацил, 5-(C1-C6)-алкилурацил, 5-метилурацил, 5-(С2-С6)-алкенилурацил, 5-(С2-С6)-алкинилурацил, 5-(гидроксиметил)урацил, 5-хлорурацил, 5-фторурацил, 5-бромурацил, 5-гидроксицитозин, 5-(C1-C6)-алкилцитозин, 5-метилцитозин, 5-(С2-С6)-алкенилцитозин, 5-(С2-С6)-алкинилцитозин, 5-хлорцитозин, 5-фторцитозин, 5-бромцитозин, N2-диметилгуанин, 7-деазагуанин, 8-азагуанин, 7-деаза-7-замещенный гуанин, 7-деаза-7-(С2-С6)алкинилгуанин, 7-деаза-8-замещенный гуанин, 8-гидроксигуанин, 6-тиогуанин, 8-оксогуанин, 2-аминопурин, 2-амино-6-хлорпурин, 2,4-диаминопурин, 2,6-диаминопурин, 8-азапурин, замещенный 7-деазапурин, 7-деаза-7-замещенный пурин, 7-деаза-8-замещенный пурин, водород (без азотистого основания), m5C, m5U, m6A, s2U, W или 2'-O-метил-U. Многие из этих модифицированных нуклеотидных оснований и их соответствующие рибонуклеозиды можно приобрести у поставщиков. См., например, WO 2011/005799, включенный в настоящее описание в виде ссылки.
[0153] При желании, молекула РНК может содержать фосфорамидатные, фосфоротиоатные и/или метилфосфонатные связи.
[0154] В некоторых вариантах осуществления молекула РНК не содержит модифицированные нуклеотиды, например, не содержит модифицированные нуклеотидные основания, и все нуклеотиды в молекуле РНК являются обычными стандартными рибонуклеотидами A, U, G и C, за исключением необязательного 5'-кэпа, который может содержать, например, 7-метилгуанозин. В других вариантах осуществления РНК может включать 5'-кэп, содержащий 7'-метилгуанозин, а первые 1, 2 или 3, 5'-рибонуклеотиды могут быть метилированными в 2'-положении рибозы.
А. Самореплицирующиеся РНК
[0155] В некоторых аспектах катионная эмульсия масло-в-воде содержит самореплицирующуюся молекулу РНК. В некоторых вариантах осуществления самореплицирующуюся молекулу РНК получают из альфавируса или используют его в качестве основы.
[0156] Самореплицирующиеся молекулы РНК хорошо известны в данной области и могут быть получены с использованием элементов репликации, полученных, например, из альфавирусов, и заменой структурных вирусных белков нуклеотидной последовательностью, кодирующей представляющий интерес белок. Клетки, трансфицированные самореплицирующейся РНК, недолго продуцируют антиген до наступления апоптоза. Возможно такая гибель является результатом активности соответствующих двухцепочечных (дц, ds) РНК, являющихся промежуточным продуктом, которые, как было показано, вызывают мощную активацию дендритных клеток. Таким образом, усиленная иммуногенность самореплицирующейся РНК может приводить к продуцированию провоспалительной дцРНК, которая имитирует инфекцию клеток-хозяев РНК-вирусом.
[0157] Преимущественно, молекулы самореплицирующейся РНК используют механизмы клеточной системы для экспоненциального увеличения кодированных генных продуктов, таких как белки или антигены, которые могут накапливаться в клетках или могут секретироваться клетками. Сверхэкспрессия молекулами самореплицирующейся РНК белков или антигенов обеспечивает преимущество в иммуностимулирующих адъювантных эффектах, включая стимулирование толл-подобных рецепторов (TLR) 3, 7 и 8, и не-TLR систем (например, RIG-1, MD-5) за счет продуктов РНК репликации и амплификации, и трансляции, которая индуцирует апоптоз трансфицированных клеток.
[0158] Самореплицирующаяся РНК обычно содержит по меньшей мере один или несколько генов, выбранных из группы, состоящей из вирусных репликаз, вирусных протеаз, вирусные геликаз и других неструктурных белков вируса, а также содержит 5'- и 3'-конец цис-активных последовательностей репликации и, если необходимо, гетерологичные последовательности, кодирующие требуемые аминокислотные последовательности (например, представляющие интерес антигены). В самореплицирующуюся РНК может быть включен субгеномный промотор, который направляет экспрессию гетерологичной последовательности. При необходимости, гетерологичная последовательность (например, представляющего интерес антигена) может быть слита в рамке считывания с другими кодирующими участками в самореплицирующейся РНК и/или может регулироваться участком внутренней посадки рибосомы (IRES).
[0159] В некоторых вариантах осуществления молекула самореплицирующейся РНК не инкапсулирована в вирусоподобную частицу. Молекула самореплицирующейся РНК по изобретению может быть сконструирована таким образом, чтобы молекула самореплицирующейся РНК не могла индуцировать продукцию инфекционных вирусных частиц. Это может быть достигнуто, например, путем исключения из самореплицирующейся РНК одного или нескольких вирусных генов, кодирующих структурные белки, которые необходимы для продуцирования вирусных частиц. Например, если молекула самореплицирующейся РНК основана на альфавирусе, например, таком как вирус Sinebis (SIN), вирус лесов Семлики и вирус венесуэльского лошадиного энцефалита (VEE), один или более генов, кодирующих вирусные структурные белки, такие как гликопротеины капсида и/или оболочки, могут быть удалены.
[0160] При необходимости, молекулы самореплицирующейся РНК по данному изобретению также могут быть разработаны таким образом, чтобы они индуцировали продуцирование инфекционных вирусных частиц, которые являются ослабленными или вирулентными, или продуцировали вирусные частицы, которые способны на единственный цикл последующей инфекции.
[0161] Доставленная в клетку позвоночных молекула самореплицирующейся РНК может обеспечивать продуцирование множества дочерних РНК путем транскрипции самой себя (или своей антисмысловой копии). Самореплицирующаяся РНК может быть подвергнута прямой трансляции сразу после доставки в клетку, и эта трансляция обеспечивает РНК-зависимую РНК-полимеразу, которая затем продуцирует транскрипты с доставленной РНК. Таким образом, доставленная РНК обеспечивает продуцирование множества дочерних РНК. Эти транскрипты являются антисмысловыми по отношению к доставленной РНК и могут сами транслироваться для обеспечения in situ экспрессии генного продукта или могут транслироваться для обеспечения дополнительных транскриптов с той же самой смысловой последовательности, что и доставленная РНК, которая транслируется для обеспечения in situ экспрессии генного продукта.
[0162] Одной из подходящих систем для достижения саморепликации является использование РНК репликона на основе альфавируса. Альфавирусы содержат набор генетически, структурно и серологически родственных арбовирусов семейства Togaviridae. В пределах рода альфавирусов были классифицированы двадцать шесть известных вирусов и подтипов вирусов, включая вирус Синдбис, вирус леса Семлики, вирус Росс-Ривер и вирус венесуэльского конского энцефалита. Таким образом, самореплицирующаяся РНК по изобретению может включать РНК репликазу, полученную из вируса леса Семилики (SFV), вируса Синдбис (SIN), вируса венесуэльского лошадиного энцефалита (VEE), вируса Росс-Ривера (RRV) или других вирусов, принадлежащих к семейству альфавирусов.
[0163] В настоящем изобретении могут быть использованы векторы экспрессии "репликоны" на основе альфавирусов. Векторы репликоны могут быть использованы в нескольких форматах, в том числе ДНК, РНК и частиц рекомбинантных репликонов. Такие векторы репликоны были получены из альфавирусов, которые включают, например, вирус Синдбис (Xiong et al. (1989) Science 243:1188-1191; Dubensky et al, (1996) J. Virol. 70:508-519; Hariharan et al. (1998) J. Virol. 72:950-958; Polo et al. (1999) PNAS 96:4598-4603), вирус леса Семлики (Liljestrom (1991) Bio/Technology 9:1356-1361; Berglund et al. (1998) Nat. Biotech. 16:562-565), и вирус венесуэльского лошадиного энцефалита (Pushko et al. (1997) Virology 239:389-401). Репликоны, полученные из альфавирусов, как правило, имеют достаточно одинаковые общие характеристики (например, структуру, репликацию), отдельные альфавирусы могут демонстрировать некоторое определенное свойство (например, связывание рецепторов, чувствительность к интерферону и профиль заболевания), которое является уникальным. Таким образом, также могут быть использованы химерные репликоны на основе альфавирусов, полученные из дивергентных семейств вирусов.
[0164] Репликоны на основе альфавирусов являются (+)-нитевыми репликонами, которые могут транслироваться после доставки в клетку для обеспечения репликазы (или репликазы-транскриптазы). Репликаза транслируется как полипротеин, который саморасщепляется, обеспечивая комплекс репликации, который создает геномные (-)-нитевые копии доставленной РНК, состоящей из (+)-нитей. Эти (-)-нитевые транскрипты могут транслироваться сами, обеспечивая дополнительные копии (+)-нитевой материнской РНК, а также обеспечивая субгеномный транскрипт, который кодирует нужный генный продукт. Трансляция субгеномного транскрипта, таким образом, обеспечивает in situ экспрессию целевого генного продукта посредством инфицированной клетки. Подходящие репликоны на основе альфавирусов могут использовать репликазу вируса Синдбис, вируса леса Семлики, вируса восточного конского энцефалита, вируса венесуэльского конского энцефалита и др.
[0165] Предпочтительная молекула самореплицирующейся РНК, таким образом, кодирует (i) РНК-зависимую РНК-полимеразу, которая может осуществлять транскрипцию РНК молекулы самореплицирующейся РНК, и (ii) полипептидный антиген. Полимераза может представлять собой репликазу альфавируса, например, содержащую белок nsP4 альфавируса.
[0166] В то время как природные геномы альфавирусов кодируют структурные белки вириона в дополнение к неструктурной репликазе, предпочтительно, чтобы молекула самореплицирующейся РНК на основе альфавируса по изобретению не кодировала структурные белки альфавируса. Таким образом, самореплицирующаяся РНК может обеспечивать продуцирование в клетке копий геномной РНК, но не вирионы альфавирусов, содержащие РНК. Неспособность продуцировать эти вирионы означает, что, в отличие от альфавируса дикого типа, молекула самореплицирующейся РНК не может самоподдерживаться в инфекционной форме. В структурные белки альфавируса, которые необходимы для продолжения существования вирусов дикого типа, отсутствуют в самореплицирующихся РНК по изобретению, вместо них содержится ген(ы), кодирующий требуемый генный продукт, с тем, чтобы субгеномный транскрипт кодировал требуемый генный продукт, а не структурные белки вириона альфавируса.
[0167] Таким образом, используемая в изобретении молекула самореплицирующейся РНК может иметь две открытые рамки считывания. Первая (5') открытая рамка считывания кодирует репликазу, вторая (3') открытая рамка считывания кодирует полипептидный антиген. В некоторых вариантах РНК может иметь дополнительные (расположенные ниже по ходу транскрипции) открытые рамки считывания, например, которые кодируют другие требуемые генные продукты. Молекула самореплицирующейся РНК может иметь 5'-последовательность, совместимую с кодируемой репликазой.
[0168] В других аспектах молекулу самореплицирующейся РНК получают из или конструируют на основе вируса, отличного от альфавируса, предпочтительно, вируса с положительной цепью РНК, более предпочтительно, пикорнавируса, флавивируса, рубивируса, пестивируса, гепацивируса, калицивируса или коронавируса. Подходящие последовательности альфавируса дикого типа хорошо известны и доступны из депозитариев последовательностей, таких как Американская коллекция типовых культур (American Type Culture Collection, Rockville, MD). Репрезентативные примеры подходящих альфавирусов включают Аура (Aura) вирус (АТСС VR-368), вирус Бебару (Bebaru) (АТСС VR-600, АТСС VR-1240), Кабассу (Cabassou) (ATCC VR-922), вирус Чикунгунья (Chikungunya) (АТСС VR-64, АТСС VR-1241), вирус восточного лошадиного энцефаломиелита (АТСС VR-65, АТСС VR-1242), Форт Моргана (Fort Morgan) (АТСС VR-924), вирус Гета (Getah) (АТСС VR-369, АТСС VR-1243), Кызылагачский (Kyzylagach) (АТСС VR-927), Майаро (Mayaro) (АТСС VR-66), вирус Майаро (АТСС VR-1277), Миддлбург (Middleburg) (АТСС VR-370), вирус Мукамбо (Mucambo) (АТСС VR-580, АТСС VR-1244), Ндуму (Ndumu) (АТСС VR-371), вирус Пиксуна (Pixuna) (АТСС VR-372, АТСС VR-1245), вирус реки Росс (Ross River) (АТСС VR-373, АТСС VR-1246), вирус леса Семилики (Semliki Forest) (АТСС VR-67, АТСС VR-1247), вирус Синдбис (Sindbis) (АТСС VR-68, АТСС VR-1248), вирус Тонате (Tonate) (АТСС VR-925), Тринити (Triniti) (АТСС VR-469), Уна (Una) (АТСС VR-374), вирус венесуэльского конского энцефаломиелита (АТСС VR-69, АТСС VR-923, АТСС VR-1250, АТСС VR-1249, АТСС VR-532), вирус западного энцефаломиелита лошадей (АТСС VR-70, АТСС VR-1251, АТСС VR-622, АТСС VR-1252), Ватароа (Whataroa) (АТСС VR-926) и Y-62-33 (АТСС VR-375).
[0169] Молекулы самореплицирующейся РНК по изобретению больше, чем другие типы РНК (например, мРНК). Как правило, молекулы самореплицирующийся РНК по изобретению содержат по меньшей мере около 4 т.п.н. Например, самореплицирующаяся РНК может содержать по меньшей мере примерно 5 т.п.н., по меньшей мере примерно 6 т.п.н., по меньшей мере примерно 7 т.п.н., по меньшей мере примерно 8 т.п.н., по меньшей мере примерно 9 т.п.н., по меньшей мере примерно 10 т.п.н., по меньшей мере примерно 11 т.п.н., по меньшей мере примерно 12 т.п.н. или более 12 т.п.н. В некоторых примерах, самореплицирующаяся РНК составляет от примерно 4 т.п.н. до примерно 12 т.п.н., от примерно 5 т.п.н. до примерно 12 т.п.н., от примерно 6 т.п.н. до примерно 12 т.п.н., от примерно 7 т.п.н. до примерно 12 т.п.н., от примерно 8 т.п.н. до примерно 12 т.п.н., от примерно 9 т.п.н. до примерно 12 т.п.н., от примерно 10 т.п.н. до примерно 12 т.п.н., от примерно 11 т.п.н. до примерно 12 т.п.н., от примерно 5 т.п.н. до примерно 11 т.п.н., от примерно 5 т.п.н. до примерно 10 т.п.н., от примерно 5 т.п.н. до примерно 9 т.п.н., от примерно 5 т.п.н. до примерно 8 т.п.н., от примерно 5 т.п.н. до примерно 7 т.п.н., от примерно 5 т.п.н. до примерно 6 т.п.н., от примерно 6 т.п.н. до примерно 12 т.п.н., от примерно 6 т.п.н. до примерно 11 т.п.н., от примерно 6 т.п.н. до примерно 10 т.п.н., от примерно 6 т.п.н. до примерно 9 т.п.н., от примерно 6 т.п.н. до примерно 8 т.п.н., от примерно 6 т.п.н. до примерно 7 т.п.н., от примерно 7 т.п.н. до примерно 11 т.п.н., от примерно 7 т.п.н. до примерно 10 т.п.н., от примерно 7 т.п.н. до примерно 9 т.п.н., от примерно 7 т.п.н. до примерно 8 т.п.н., от примерно 8 т.п.н. до примерно 11 т.п.н., от примерно 8 т.п.н. до примерно 10 т.п.н., от примерно 8 т.п.н. до примерно 9 т.п.н., от примерно 9 т.п.н. до примерно 11 т.п.н., от примерно 9 т.п.н. до примерно 10 т.п.н. или от примерно 10 т.п.н. до примерно 11 т.п.н.
[0170] Молекулы самореплицирующейся РНК по изобретению могут содержать один или несколько модифицированных нуклеотидов (например, псевдоуридин, N6-метиладенозин, 5-метилцитидин, 5-метилуридин).
[0171] Молекула самореплицирующейся РНК может кодировать один полипептидный антиген или, необязательно, два или более полипептидных антигена, соединенных друг с другом таким образом, что каждая из последовательностей сохраняет свою идентичность (например, соединены последовательно) во время экспрессии в виде аминокислотной последовательности. Полипептиды, сгенерированные самореплицирующейся РНК, затем могут быть получены в виде слитого полипептида, или могут быть сконструированы таким образом, чтобы был получен отдельный полипептид или пептидные последовательности.
[0172] Самореплицирующаяся РНК по изобретению может кодировать один или несколько полипептидных антигенов, которые содержат широкий спектр эпитопов. Предпочтительно эпитопы способны вызывать либо хелперный Т-клеточный ответ, либо цитотоксический Т-клеточный ответ, либо оба типа ответов.
[0173] Описанные здесь молекулы самореплицирующейся РНК могут быть сконструированы для экспрессии множества нуклеотидных последовательностей из двух или более открытых рамок считывания, тем самым обеспечивая коэкспрессию белков, например двух или более антигенов вместе с цитокинами или другими иммуномодуляторами, которые могут усиливать выработку иммунного ответа. Такая молекула самореплицирующейся РНК может быть особенно полезной, например, для одновременного продуцирования различных генных продуктов (например, белков), например, в виде бивалентной или поливалентной вакцины.
[0174] Молекулы самореплицирующейся РНК по изобретению могут быть получены любым подходящим способом. В данной области известно несколько способов, подходящих для получения молекул РНК, которые содержат модифицированные нуклеотиды. Например, молекула самореплицирующейся РНК, которая содержит модифицированные нуклеотиды, может быть получена транскрипцией (например, in vitro транскрипцией) ДНК, которая кодирует самореплицирующуюся молекулу РНК с использованием подходящей ДНК-зависимой РНК-полимеразы, такой как РНК-полимеразы фага Т7, РНК-полимеразы фага SP6, РНК-полимеразы фага T3 и т.п., или мутантов этих полимераз, которые позволяют обеспечить эффективное введение модифицированных нуклеотидов в молекулы РНК. В реакции транскрипции могут быть задействованы нуклеотиды и модифицированные нуклеотиды и другие компоненты, которые поддерживают активность выбранной полимеразы, например, подходящий буфер и подходящие соли. Возможно введение нуклеотидных аналогов в самореплицирующуюся РНК, например, для изменения стабильности таких молекул РНК, увеличения устойчивости к действию РНКаз, подтверждения репликации после введения в соответствующие клетки-хозяева ("инфицирующая способность" РНК) и/или усиления или уменьшения врожденного и адаптивного иммунных ответов.
[0175] Для получения молекулы самореплицирующейся РНК по изобретению могут быть использованы подходящие синтетические способы по отдельности или в комбинации с одним или несколькими другими способами (например, способ получения рекомбинантной ДНК или РНК). Подходящие способы синтеза de novo хорошо известны в данной области и могут быть адаптированы для конкретных приложений. Типичные способы включают, например, химический синтез с использованием подходящих защитных групп, таких как СЕМ (Masuda et al., (2007) Nucleic Acids Symposium Series 51:3-4), 3-цианоэтил фосфорамидитный способ (Beaucage S.L. et al. (1981) Tetrahedron Lett 22:1859); нуклеозид H-фосфонатный способ (Garegg Р. et al. (1986) Tetrahedron Lett 27:4051-4; Froehler В.С. et al. (1986) Nucl Acid Res 14:5399-407; Garegg P. et al. (1986) Tetrahedron Lett 27:4055-8; Gaffney В.L. et al. (1988) Tetrahedron Lett 29:2619-22). Эти химические способы могут выполняться или могут быть адаптированы для выполнения на коммерчески доступных автоматизированных синтезаторах нуклеиновых кислот. Дополнительные подходящие способы синтеза описаны у Uhlmann et al. (1990) Chem Rev 90:544-84, и Goodchild J. (1990) Bioconjugate Chem 1:165. Синтез нуклеиновых кислот также можно выполнять подходящими рекомбинантными способами, которые хорошо известны и являются обычными в данной области, включая клонирование, процессинг и/или экспрессию полинуклеотидов и генных продуктов, кодируемых такими полинуклеотидами. ДНК-перестановка методом случайной фрагментации и ПЦР-сборка генных фрагментов и синтетических полинуклеотидов являются примерами известных методов, которые могут быть использованы для создания и конструирования полинуклеотидных последовательностей. Для модификации нуклеиновых кислот и кодируемых белков может быть использован сайт-направленный мутагенез, например, для добавления новых сайтов рестрикции, изменения характера гликозилирования, изменения кодонного предпочтения, получения сплайсированных вариантов, введения мутаций и т.п. Подходящие способы транскрипции, трансляции и экспрессии последовательностей нуклеиновых кислот являются известными и широко применяются в данной области техники. (Для общего сведения см. Current Protocols in Molecular Biology, Vol. 2, Ed. Ausubel, et al., Greene Publish. Assoc. & Wiley Interscience, Ch. 13, 1988; Glover, DNA Cloning, Vol. II, IRL Press, Wash., D.C., Ch. 3, 1986; Bitter, et al., in Methods in Enzymology 153:516-544 (1987); The Molecular Biology of the Yeast Saccharomyces, Eds. Strathern et al., Cold Spring Harbor Press, Vols. I and II, 1982; и Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, 1989.)
[0176] Присутствие и/или количество одного или более модифицированных нуклеотидов в молекуле самореплицирующейся РНК может быть определено любым подходящим способом. Например, самореплицирующаяся РНК может быть расщеплена до монофосфатов (например, нуклеазой P1) и дефосфорилирована (например, подходящей фосфатазой, например, CIAP), и полученные нуклеозиды могут быть проанализированы методом обращенно-фазовой ВЭЖХ (например, с использованием колонки YMC Pack ODS-AQ (5 микрон, 4,6×250 мм) и элюцией в градиенте от 30% В (0-5 мин) до 100% В (5-13 мин) и при 100% В (13-40 мин), скорости потока (0,7 мл/мин), УФ-детектированием (длина волны: 260 нм), температуре колонки 30°C), буфера А (20 мМ уксусная кислота-ацетат аммония, рН 3,5), буфера В (20 мМ уксусная кислота-ацетат аммония, рН 3,5/метанол [90/10])).
[0177] Необязательно, молекулы самореплицирующейся РНК по изобретению могут включать один или несколько модифицированных нуклеотидов с тем, чтобы молекула самореплицирующейся РНК имела более низкую иммуномодулирующую активность при введении в клетку-хозяина (например, человеческую клетку) по сравнению с соответствующей молекулой самореплицирующейся РНК, которая не содержит модифицированных нуклеотидов.
[0178] Необязательно, молекулы самореплицирующейся РНК могут быть подвергнуты скринингу или проанализированы для подтверждения терапевтических и профилактических свойств при помощи различных in vitro или in vivo методов тестирования, которые известны специалистам в данной области. Например, вакцины, содержащие молекулу самореплицирующейся РНК, могут быть протестированы в отношении их воздействия на индукцию пролиферации или эффекторную функцию конкретного представляющего интерес типа лимфоцитов, например, В-клеток, Т-клеток, Т-клеточных линий, а также клонов Т-клеток. Например, могут быть выделены клетки селезенки иммунизированных мышей, и исследована способность цитотоксических Т-лимфоцитов лизировать аутологичные клетки-мишени, которые содержат молекулу самореплицирующейся РНК, кодирующую полипептидный антиген. Кроме того, может быть проанализирована дифференцировка хелперных T-клеток путем измерения пролиферации или продуцирования TH1 (IL-2 и IFN-γ) и/или ТН2 (IL-4 и IL-5) цитокинов методом ELISA или непосредственно в CD4+ Т-клетках путем окрашивания цитоплазматических цитокинов и способом проточной цитометрии.
[0179] Молекулы самореплицирующейся РНК, которые кодируют полипептидный антиген, также могут быть протестированы в отношении их способности индуцировать гуморальный иммунный ответ, который проявляется, например, через индукцию продуцирования В-клетками антител, специфичных в отношении представляющего интерес антигена. Эти анализы можно осуществлять с использованием, например, периферических В-лимфоцитов, полученных от иммунизированных индивидуумов. Такие способы анализа известны специалистам в данной области. Для характеристики молекулы самореплицирующейся РНК по изобретению можно использовать другие методы анализы, которые могут включать детектирование экспрессии кодируемого антигена целевыми клетками. Например, для детектирования экспрессии антигена на поверхности клеток или внутриклеточную экспрессию можно использовать FACS. Другое преимущество выбора FACS заключается в возможности отсортировать разные уровни экспрессии; иногда желательной может быть экспрессия на более низком уровне. Другой подходящий способ идентификации клеток, которые экспрессируют конкретный антиген, включает пэннинг с использованием моноклональных антител на планшете или захват при помощи магнитных гранул, покрытых моноклональными антителами.
В. Антигены
[0180] В некоторых вариантах осуществления описанная здесь отрицательно заряженная молекула представляет собой молекулу нуклеиновой кислоты (например, молекулу РНК), которая кодирует антиген. Подходящие антигены включают, без ограничения, бактериальный антиген, вирусный антиген, грибковый антиген, антиген простейших, растительный антиген, раковый антиген или их комбинацию.
[0181] Подходящие антигены включают белки и пептиды патогена, такого как вирусы, бактерии, грибы, простейшие, растение или опухоль. Вирусные антигены и иммуногены, которые могут кодироваться молекулой самореплицирующейся РНК, включают, без ограничения, белки и пептиды ортомиксовирусов, таких как вирусы гриппа А, В и С; вирусов семейства Paramyxoviridae, таких как пневмовирусы (RSV), парамиксовирусы (PIV), метапневмовирусы и морбилливирусы (например, корь); пневмовирусов, таких как респираторно-синцитиальный вирус (RSV), респираторно-синцитиальный вирус крупного рогатого скота, вирус пневмонии мышей и вирус ринотрахеита индеек; парамиксовирусов, таких как типы 1-4 вируса парагриппа (PIV), вирус паротита, вирусы Сендай, обезьяний вирус 5, вирус бычьего парагриппа, вирус Нипах (Nipahvirus), вирусы рода Henipavirus и вирус болезни Ньюкасла; вирусов семейства Poxviridae, в том числе ортопоксвирусов, таких как Variola vera (включая, без ограничения, Variola major и Variola minor); метапневмовирусов, таких как человеческий метапневмовирус (HMPV) и птичий метапневмовирус (AMPV); морбилливирусов, таких как вирус кори; пикорнавирусов, таких как энтеровирусы, риновирусы, гепарнавирусы, парэховирусы, кардиовирусы и афтовирусы; энтеровирусов, таких как типы 1, 2 или 3 полиовируса, типы 1-22 и 24 вируса Коксаки А, типы 1-6 вируса Коксаки В, типы 1-9, 11-27 и 29-34 эховируса (ECHO) и эховирусы 68-71, буньявирусы, включая ортобуньявирусы, такие как вирус энцефалита Калифорнии; флебовирусов, таких как вирус лихорадки Рифт-Валли; найровирусов, таких как вирус конго-крымской геморрагической лихорадки; гепарнавирусов, таких как вирус гепатита А (HAV); тогавирусов (краснуха), таких как рубивирусы, альфавирусы или артеривирусы; флавивирусов, таких как вирус клещевого энцефалита (TBE), денге (типы 1, 2, 3 или 4), вирус желтой лихорадки, вирус японского энцефалита, вирус Кьясанурского леса, вирус энцефалита Западного Нила, вирус энцефалита Сент-Луис, вирус русского весенне-летнего энцефалита, вирус энцефалита Повассан; пестивирусов, таких как вирус бычьей диареи (BVDV), вирус классической чумы свиней (CSFV) или вирус болезни Бордера (BDV); гепаднавирусов, таких как вирус гепатита В, вирус гепатита С; рабдовирусов, таких как лиссавирусы (вирус бешенства) и везикуловирусы (VSV); вирусов семейства Caliciviridae, таких как вирус Норволк и Норволк-подобные вирусы, такие как вирус Гавайи и вирус снежных гор (Snow Mountain Virus); коронавирусов, таких как атипичная пневмония, респираторный коронавирус человека, инфекционный бронхит птиц (IBV), вирус гепатита мышей (MHV) и вирус трансмиссивного гастроэнтерита свиней (TGEV); ретровирусов, таких как онковирусы, лентивирусы или спумавирусы; реовирусов, таких как ортореовирусы, ротавирусы, орбивирусы или колтивирусы; парвовирусов, таких как парвовирус В19; вируса гепатита Дельта (HDV); вируса гепатита Е (HEV); вируса гепатита G (HGV); вирусов герпеса человека, таких как вирусы простого герпеса (HSV), вирус Варицелла-Зостер (VZV), вирус Эпштейна-Барр (EBV), цитомегаловирус (CMV), вирус герпеса человека 6 (HHV6), вирус герпеса человека 7 (HHV7) и вирус простого герпеса 8 (HHV8); паповавирусов, таких как папилломавирусы и полиомавирусы, аденовирусы и аренавирусы.
[0182] В некоторых вариантах антиген вызывает иммунный ответ против вируса, который инфицирует рыб, такого как вирус инфекционной анемии лососевых (ISAV), вирус болезни поджелудочной железы лососевых (SPDV), вирус инфекционного некроза поджелудочной железы (IPNV), вирус канального сома (CCV), вирус лимфоцистиса рыб (FLDV), вирус инфекционного некроза гемопоэтической ткани (IHNV), герпевирус КОИ, пикорнаподобный вирус лососевых (также известный как пикорнаподобный вирус атлантического лосося), вирус озерного лосося (LSV), ротавирус атлантического лосося (ASR), вирус земляничной болезни форели (TSD), вируса опухоли кижуча (CSTV) или вирус вирусной геморрагической септицемии (VHSV).
[0183] В некоторых вариантах осуществления антиген вызывает иммунный ответ против паразита рода Plasmodium, такого как P.falciparum, P.vivax, P.malariae или P.ovale. Таким образом, изобретение может быть использовано для иммунизации против малярии. В некоторых вариантах осуществления антиген вызывает иммунный ответ против паразита семейства Caligidae, в частности паразитов рода Lepeophtheirus и рода Caligus, например, морских вшей, таких как Lepeophtheirus salmonis или Caligus rogercresseyi.
[0184] Бактериальные антигены и иммуногены, которые могут кодироваться молекулой самореплицирующейся РНК, включают, без ограничения, белки и пептиды Neisseria meningitides, Streptococcus pneumoniae, Streptococcus pyogenes, Moraxella catarrhalis, Bordetella pertussis, Burkholderia sp. (например, Burkholderia mallei, Burkholderia pseudomallei и Burkholderia cepacia), Staphylococcus aureus, Staphylococcus epidermis, Haemophilus influenzae, Clostridium tetani (столбняк), Clostridium perfringens, Clostridium botulinums (ботулизм), Cornynebacterium diphtheriae (дифтерия), Pseudomonas aeruginosa, Legionella pneumophila, Coxiella burnetii, Brucella sp. (например, B. abortus, B. canis, B. melitensis, B. neotomae, B. ovis, B. suis и B. pinnipediae), Francisella sp. (например, F. novicida, F. philomiragia и F. tularensis), Streptococcus agalactiae, Neiserria gonorrhoeae, Chlamydia trachomatis, Treponema pallidum (сифилис), Haemophilus ducreyi, Enterococcus faecalis, Enterococcus faecium, Helicobacter pylori, Staphylococcus saprophyticus, Yersinia enterocolitica, E. coli (такие как энтеротоксигенные E. coli (ETEC), энтероаггрегативные E. coli (EAggEC), диффузно-адгерентные E. coli (DAEC), энтеропатогенные E. coli (EPEC), экстраинтестинальные E. coli (ExPEC; такие как уропатогенные E. coli (UPEC) и менингит/сепсис-ассоциированные E. coli (MNEC)), и/или энтерогеморрагические E. coli (EHEC), Bacillus anthracis (сибирская язва), Yersinia Pestis (чума), Mycobacterium tuberculosis, Rickettsia, Listeria monocytogenes, Chlamydia pneumoniae, Vibrio cholerae, Salmonella typhi (брюшной тиф), Borrelia burgdorfer, Porphyromonas gingivalis, Klebsiella, Mycoplasma pneumoniae и т.д.
[0185] Грибковые антигены и иммуногены, которые могут кодироваться молекулой самореплицирующейся РНК, включают, без ограничения, белки и пептиды Dermatophytres, включая Epidermophyton floccusum, Microsporum audouini, Microsporum canis, Microsporum distortum, Microsporum equinum, Microsporum gypsum, Microsporum nanum, Trichophyton concentricum, Trichophyton equinum, Trichophyton gallinae, Trichophyton gypseum, Trichophyton megnini, Trichophyton mentagrophytes, Trichophyton quinckeanum, Trichophyton rubrum, Trichophyton schoenleini, Trichophyton tonsurans, Trichophyton verrucosum, T. verrucosum var. album, var. discoides, var. ochraceum, Trichophyton violaceum, и/или Trichophyton faviforme; или Aspergillus fumigatus, Aspergillus flavus, Aspergillus niger, Aspergillus nidulans, Aspergillus terreus, Aspergillus sydowi, Aspergillus flavatus, Aspergillus glaucus, Blastoschizomyces capitatus, Candida albicans, Candida enolase, Candida tropicalis, Candida glabrata, Candida krusei, Candida parapsilosis, Candida stellatoidea, Candida kusei, Candida parakwsei, Candida lusitaniae, Candida pseudotropicalis, Candida guilliermondi, Cladosporium carrionii, Coccidioides immitis, Blastomyces dermatidis, Cryptococcus neoformans, Geotrichum clavatum, Histoplasma capsulatum, Klebsiella pneumoniae, Microsporidia, Encephalitozoon spp., Septata intestinalis и Enterocytozoon bieneusi; менее распространенными являются Brachiola spp, Microsporidium spp., Nosema spp., Pleistophora spp., Trachipleistophora spp., Vittaforma spp Paracoccidioides brasiliensis, Pneumocystis carinii, Pythiumn insidiosum, Pityrosporum ovale, Sacharomyces cerevisae, Saccharomyces boulardii, Saccharomyces pombe, Scedosporium apiosperum, Sporothrix schenckii, Trichosporon beigelii, Toxoplasma gondii, Penicillium marneffei, Malassezia spp., Fonsecaea spp., Wangiella spp., Sporothrix spp., Basidiobolus spp., Conidiobolus spp., Rhizopus spp., Mucor spp., Absidia spp., Mortierella spp., Cunninghamella spp., Saksenaea spp., Alternaria spp., Curvularia spp., Helminthosporium spp., Fusarium spp., Aspergillus spp., Penicillium spp., Monolinia spp., Rhizoctonia spp., Paecilomyces spp., Pithomyces spp. и Cladosporium spp.
[0186] Антигены и иммуногены простейших, которые могут кодироваться молекулой самореплицирующейся РНК, включают, без ограничения, белки и пептиды Entamoeba histolytica, Giardia lambli, Cryptosporidium parvum, Cyclospora cayatanensis и Toxoplasma.
[0187] Антигены и иммуногены растений, которые могут кодироваться молекулой самореплицирующейся РНК, включают, без ограничения, белки и пептиды Ricinus communis.
[0188] Подходящие антигены включают белки и пептиды вируса, такого как, например, вирус иммунодефицита человека (ВИЧ), вирус гепатита А (HAV), вирус гепатита В (HBV), вирус гепатита С (HCV), вирус простого герпеса (HSV), цитомегаловирус (CMV), вирус гриппа (flu), респираторно-синцитиальный вирус (RSV), парвовирус, норовирус, вирус папилломы человека (HPV), риновирус, вирус желтой лихорадки, вирус бешенства, вирус лихорадки денге, вирус кори, вирус эпидемического паротита, вирус краснухи, вирус ветряной оспы, энтеровирус (например, энтеровирус 71), вирус Эбола и вирус бычьей диареи. Предпочтительно, антигенное вещество выбирают из группы, состоящей из гликопротеина gD HSV, гликопротеина gp120 ВИЧ, гликопротеина gp40 ВИЧ, gag/p55 ВИЧ и полипептидов областей pol и tat. В других предпочтительных вариантах осуществления изобретения антиген представляет собой белок или пептид, полученный из бактерии, такой как, например, Helicobacter pylori, Haemophilus influenza, Vibrio cholerae (холера), C. diphtheriae (дифтерия), C. tetani (столбняк), Neisseria meningitidis, B. pertussis, Mycobacterium tuberculosis и т.п.
[0189] Антигены ВИЧ, которые могут кодироваться молекулами самореплицирующейся РНК по изобретению, описаны в заявке США 490858, поданной 9 марта 1990 г., и опубликованной Европейской заявке 181150 (14 мая 1986 г.), а также заявках США 60/168471; 09/475515; 09/475504 и 09/610313, которые включены в настоящее описание во всей полноте в виде ссылки.
[0190] Антигены цитомегаловирусов, которые могут кодироваться молекулой самореплицирующейся РНК по изобретению, описаны в патенте США 4689225, заявке на патент США 367363, поданной 16 июня 1989 г., и публикации заявки РСТ WO 89/07143, раскрытие которых включено в настоящее описание во всей полноте в виде ссылки.
[0191] Антигены гепатита С, которые можно кодировать молекулами самореплицирующейся РНК по изобретению, описаны в PCT/US88/04125, опубликованной европейский заявке 318216 (31 мая 1989 г.), опубликованной японской заявке 1-500565, поданной 18 ноября 1988 г., канадской заявке 583561 и EPO 388232, раскрытие которых включено в настоящее описание во всей полноте в виде ссылки. Другой набор антигенов HCV описан в европейской заявке на патент 90/302866.0, поданной 16 марта 1990 г., заявке США 456637, поданной 21 декабря 1989 г., и PCT/US90/01348, раскрытие которых включено в настоящее описание во всей полноте в виде ссылки.
[0192] В некоторых вариантах осуществления антиген получают из аллергена, такого как аллергены пыльцы (аллергены пыльцы деревьев, травянистых растений, сорняков и трав); аллергены насекомых или паукообразных (аллергены ингалянтов, слюны и яда, например, клещевые аллергены, аллергены тараканов и мошки, аллергены яда перепончатокрылых насекомых); аллергены шерсти и перхоти животных (например, собак, кошек, лошадей, крыс, мышей и т.д.), а также пищевые аллергены (например, глиадин). Важными аллергенами пыльцы деревьев, трав и растений являются те, которые происходят из таксономических отрядов Fagales, Oleales и Pinales, включая, без ограничения, березу (Betula), ольху (Alnus), орешник (Corylus), граб (Carpinus) и оливу (Olea), кедр (Cryptomeria и Juniperus), платан (Platanus), отряда Poales, включая травы родов Lolium, Phleum, Роа, Cynodon, Dactylis, Holcus, Phalaris, Secale и Sorghum, отрядов Asterales и Urticales, включая растения родов Ambrosia, Artemisia и Parietaria. Другими важными вдыхаемыми аллергенами являются такие, источниками которых являются клещи домашней пыли родов Dermatophagoides и Euroglyphus, амбарные клещи, например, Lepidoglyphys, Glycyphagus и Tyrophagus, тараканы, мошки и блохи, например, Blatella, Periplaneta, Chironomus и Ctenocepphalides, и такие, источниками которых являются млекопитающие, такие как кошки, собаки и лошади, аллергены яда, включая такие, источниками которых являются жалящие или кусающие насекомые, такие как те, которые относятся к таксономической группе отряда Hymenoptera, включая пчел (Apidae), ос (Vespidea) и муравьев (Formicoidae).
[0193] В некоторых вариантах осуществления молекулой самореплицирующейся РНК можно кодировать иммуноген или антиген опухоли или иммуноген или антиген рака. В некоторых вариантах осуществления иммуногены и антигены опухоли представляют собой антигены опухоли, содержащие пептид, такие как полипептидный антиген опухоли или гликопротеиновые антигены опухоли.
[0194] Иммуногены и антигены опухоли, пригодные для использования по изобретению, включают в себя широкий спектр молекул, таких как (а) содержащие полипептид антигены опухоли, включая полипептиды (которые могут составлять в длину, например, от 8-20 аминокислот, хотя их длина может выходить за границы указанного диапазона), липополипептиды и гликопротеины.
[0195] В некоторых вариантах осуществления иммуногены опухоли представляют собой, например, (а) молекулы полной длины, ассоциированные с раковыми клетками, (б) гомологи и их модифицированные формы, включая молекулы с удаленными, добавленными и/или замещенными участками, и (в) фрагменты молекул. Иммуногены опухоли включают, например, антигены, рестриктированные по классу I, узнаваемые CD8+ лимфоцитами, или антигены, рестриктированные по классу II, узнаваеме CD4+ лимфоцитами.
[0196] В некоторых вариантах осуществления иммуногены опухоли включают, без ограничения, (а) антигены рака яичка, такие как NY-ESO-1, SSX2, SCP1, а также семейство полипептидов RAGE, BAGE, GAGE и MAGE, например, GAGE-1, GAGE-2, MAGE-1, MAGE-2, MAGE-3, MAGE-4, MAGE-5, MAGE-6 и MAGE-12 (которые можно использовать, например, для лечения меланомы, рака легких, головы и шеи, НМРЛ, опухоли молочной железы, желудочно-кишечного тракта и мочевого пузыря), (b) мутированные антигены, например, р53 (ассоциированный с различными солидными опухолями, например, раком толстой кишки, легких, рака головы и шеи), p21/Ras (ассоциированный, например, с меланомой, раком поджелудочной железы и колоректальным раком), CDK4 (ассоциированный, например, с меланомой), MUM1 (ассоциированный, например, с меланомой), каспазу-8 (ассоциированную, например, с раком головы и шеи), CIA 0205 (ассоциированный, например, с раком мочевого пузыря), HLA-A2-R1701, бета катенин (ассоциированный, например, с меланомой), TCR (ассоциированный, например, с T-клеточной неходжкинской лимфомой), BCR-abl (ассоциированный, например, с хроническим миелолейкозом), триозефосфат изомеразу, KIA 0205, CDC-27 и LDLR-FUT, (с) сверхэкспрессируемые антигены, например, Galectin 4 (ассоциированный, например, с колоректальным раком), Galectin 9 (ассоциированный, например, с болезнью Ходжкина), протеиназу 3 (ассоциированную, например, с хроническим миелолейкозом), WT 1 (ассоциированный, например, с различными лейкозами), карбоангидразу (ассоциированную, например, с раком почек), альдолазу (ассоциированную, например, с раком легких), PRAME (ассоциированный, например, с меланомой), HER-2/neu (ассоциированный, например, с раком молочной железы, толстой кишки, легких и яичников), альфа-фетопротеин (ассоциированный, например, с гепатомой), KSA (ассоциированный, например, с раком прямой кишки), гастрин (ассоциированный, например, с раком поджелудочной железы и раком желудка), каталитический белок теломеразу, MUC-1 (ассоциированный, например, с раком молочной железы и раком яичников), G-250 (ассоциированный, например, с почечно-клеточной карциномой), p53 (ассоциированный, например, с раком молочной железы, раком толстой кишки) и карциноэмбриональный антиген (ассоциированный, например, с раком молочной железы, раком легкого и желудочно-кишечного тракта, такой как колоректальный рак), (d) общие антигены, например, антигены дифференцировки меланомы-меланоцитов, такие как MART-1/Melan A, gp100, MC1R, рецепторы меланоцит-стимулирующего гормона, тирозиназа, родственный тирозиназе белок-1/TRP1 и родственный тирозиназе белок 2/TRP2 (ассоциированный, например, с меланомой), (е) простата-специфические антигены, такие как PAP, PSA, PSMA, PSH-P1, PSM-P1, PSM-P2, ассоциированные, например, с раком простаты, (f) идиотипы иммуноглобулинов (ассоциированные с миеломой и В-клеточные лимфомы, например).
[0197] В некоторых вариантах осуществления иммуногены опухоли включают, без ограничения, p15, Hom/Mel-40, H-Ras, E2A-PRL, H4-RET, IGH-IGK, MYL-RAR, антигены вируса Эпштейна-Барр, EBNA, антигены вируса папилломы человека (ВПЧ), включая E6 и E7, антигены вируса гепатита В и С, антигены Т-лимфотропного вируса человека, TSP-180, p185erbB2, p180erbB-3, c-met, mn-23H1, TAG-72-4, CA 19-9, CA 72-4, CAM 17.1, NuMa, K-ras, p16, TAGE, PSCA, CT7, 43-9F, 5T4, 791 Tgp72, beta-HCG, BCA225, BTAA, CA 125, CA 15-3 (CA 27.29\BCAA), CA 195, CA 242, CA-50, CAM43, CD68\KP1, CO-029, FGF-5, Ga733 (EpCAM), HTgp-175, M344, MA-50, MG7-Ag, MOV18, NB/70K, NY-CO-1, RCAS1, SDCCAG16, TA-90 (Mac-2-связывающий белок/циклофилин C-ассоциированный белок), TAAL6, TAG72, TLP, TPS и т.п.
С. Препаративные формы отрицательно заряженных молекул
[0198] Отрицательно заряженная молекула (такая как РНК) обычно предоставлена в виде водного раствора или в форме, которая может легко растворяться в водном растворе (например, лиофилизированной). Водный раствор может представлять собой воду или водный раствор, который содержит соль (например, NaCl), буфер (например, цитратный буфер), неионный регулирующий тоничность агент (например, сахарид), полимер, ПАВ или любую их комбинацию. Если препаративная форма предназначена для in vivo введения, то предпочтительно, чтобы водный раствор представлял собой физиологически приемлемый буфер, который поддерживает значение рН, совместимое с нормальными физиологическими условиями. Кроме того, в некоторых случаях желательно поддерживать рН на определенном уровне для обеспечения стабильности некоторых компонентов препаративной формы.
[0199] Например, может быть желательным получение водного раствора, который является изотоническим и/или изоосмотическим. Гипертонические и гипотонические растворы иногда могут вызвать осложнения и нежелательные эффекты при введении, такие как отек после введения или быструю абсорбцию композиции из-за разницы концентраций ионов между композицией и физиологическими жидкостями. Для регулирования тоничности эмульсия может содержать физиологическую соль, такую как соль натрия. Хлорид натрия (NaCl), например, может быть использован в количестве примерно 0,9% (масс./об.) (физиологический солевой раствор). Другие соли, которые могут присутствовать, включают хлорид калия, дигидрофосфат калия, динатрий фосфат, хлорид магния, хлорид кальция и т.д. В иллюстративном варианте водный раствор содержит 10 мМ NaCl и другие соли или неионные регулирующие тоничность агенты. Согласно описанию, неионные регулирующие тоничность агенты также можно использовать для регулирования тоничности.
[0200] Водный раствор может быть забуференным. В настоящем изобретении может быть использован любой физиологически приемлемый буфер, такой как цитратный буфер, фосфатный буфер, ацетатный буфер, сукцинатный буфер, трис буфер, бикарбонатный буфер, карбонатный буфер или т.д. Значение рН водного раствора предпочтительно находится между 6,0-8,0, более предпочтительно от примерно 6,2 до примерно 6,8. В некоторых случаях буфер может содержать некоторое количество соли. В некоторых случаях высокое содержание соли в буфере может мешать комплексообразованию отрицательно заряженных молекул с частицами эмульсии, следовательно, этого следует избегать.
[0201] Водная фаза также может содержать дополнительные компоненты, такие как молекулы, которые изменяют осмолярность водного раствора, или молекулы, которые стабилизируют отрицательно заряженные молекулы после комплексообразования. Например, осмотическое давление можно регулировать при помощи неионного регулирующего тоничность агента, который обычно представляет собой углевод, но также может быть полимером. (См., например, Voet and Voet (1990) Biochemistry John Wiley & Sons, New York.) Примеры подходящих неионных регулирующих тоничность агентов включают сахара (например, моносахариды, дисахариды или полисахариды, такие как трегалоза, сахароза, декстроза, фруктоза), сахарные спирты (например, маннит, сорбит, ксилит, эритрит, лактит, мальтит, глицерин, восстановленная палатиноза) и их комбинации. При необходимости, может быть использован неионный полимер (например, поли(алкилгликоль), такой как полиэтиленгликоль, полипропиленгликоль или полибутиленгликоль) или неионогенный ПАВ. Эти типы агентов, в частности, сахара и сахарные спирты, являются также криопротекторами, которые могут защитить РНК, а также другие отрицательно заряженные молекулы во время лиофилизации. В иллюстративных вариантах осуществления буфер содержит от примерно 560 нМ до 600 мМ трегалозы, сахарозы, сорбита или декстрозы. В других иллюстративных вариантах осуществления буфер содержит от примерно 500 нМ до 600 мМ трегалозы, сахарозы, сорбита или декстрозы.
[0202] В некоторых случаях может оказаться предпочтительным в качестве гипертонического раствора приготовить водный раствор, содержащий отрицательно заряженные молекулы, а также приготовить катионные эмульсии с использованием чистой воды или гипотонического буфера. При объединении эмульсии и отрицательно заряженных молекул смесь становится изотонической. Например, водный раствор, содержащий РНК, может быть 2х гипертоническим раствором, а катионные эмульсии могут быть приготовлены с использованием 10 мМ цитратного буфера. При смешивании раствора РНК и эмульсии в соотношении 1:1 (об./об.) композиция становится изотонической. Исходя из желательных относительных количеств эмульсии в водном растворе, который содержит отрицательно заряженные молекулы (например, 1:1 (об./об.) смесь, 2:1 (об./об.) смесь, 1:2 (об./об.) смесь и т.д.), можно легко определить тоничность водного раствора, необходимого для получения изотонический смеси.
[0203] Кроме того, для in vivo введения могут быть желательны композиции, которые имеют физиологическую осмоляльность. Физиологическая осмоляльность составляет от примерно 255 мОсм/кг воды до примерно 315 мОсм/кг воды. Иногда предпочтительным может быть приготовление водного раствора, содержащего отрицательно заряженные молекулы, в виде гиперосмолярного раствора, а также приготовление катионной эмульсии с использованием чистой воды или гипоомолярного буфера. При объединении эмульсии и отрицательно заряженных молекул получают физиологическую осмоляльность. Исходя из желательных относительных количеств эмульсии в водном растворе, который содержит отрицательно заряженные молекулы (например, 1:1 (об./об.) смесь, 2:1 (об./об.) смесь, 1:2 (об./об.) смесь и т.д.), можно легко определить осмотическое давление водного раствора, необходимое для получения изоосмолярной смеси.
[0204] В некоторых вариантах осуществления водный раствор, содержащий отрицательно заряженные молекулы, может дополнительно содержать полимер или ПАВ или их комбинации. В иллюстративном варианте осуществления эмульсия масло-в-воде содержит полоксамер. В частности, авторы изобретения обнаружили, что добавление Pluronic® F127 к водному раствору РНК до комплексообразования с частицами катионной эмульсии приводило к увеличению стабильности и увеличению устойчивости молекул РНК к действию РНКаз. Также было обнаружено, что добавление Pluronic F127 к водному раствору РНК уменьшает размер частиц комплекса РНК/CNE. Полоксамерные полимеры также могут способствовать соответствующему распаду комплекса/высвобождению молекул РНК, предотвращают агрегацию частиц эмульсии и имеют иммуномодулирующий эффект. Другие полимеры, которые могут быть использованы, включают, например, Pluronic® F68 или ПЭГ 300.
[0205] Альтернативно или дополнительно, водный раствор, содержащий отрицательно заряженные молекулы, может содержать от примерно 0,05% до примерно 20% (масс./об.) полимера. Например, катионные эмульсии масло-в-воде могут содержать полимер (например, полоксамер, такой как Pluronic® F127, Pluronic® F68 или ПЭГ 300) в количестве от примерно 0,05% до примерно 10% (масс./об.), таком как 0,05%, 0,5%, 1% или 5%.
[0206] Буферная система может содержать любую комбинацию двух или более описанных выше молекул (соль, буфер, сахарид, полимер и т.п.). В предпочтительном варианте осуществления буфер содержит 560 мМ сахарозу, 20 мМ NaCl и 2 мМ цитрат, который может быть смешан с описанной здесь катионной эмульсией масло-в-воде, для получения окончательной водной фазы, которая содержит 280 мМ сахарозу, 10 мМ NaCl и 1 мМ цитрат.
5. Способы получения
[0207] В другом аспекте изобретение предоставляет способ получения эмульсии масло-в-воде, содержащий: (1) объединение масла и катионного липида для образования масляной фазы эмульсии, (2) предоставление водного раствора для образования водной фазы эмульсии, и (3) диспергирование масляной фазы в водной фазе, например, путем гомогенизации. Гомогенизацию можно осуществлять любым подходящим способом, например, с использованием коммерческого гомогенизатора (например, IKA T25 гомогенизатора, предоставляемого компанией VWR International (West Chester, PA)).
[0208] В некоторых вариантах осуществления эмульсии масло-в-воде получают путем (1) непосредственного растворения катионного липида в масле для образования масляной фазы; (2) предоставления водной фазы эмульсии; и (3) диспергирования масляной фазы в водной фазе путем гомогенизации. В способе не используется органический растворитель (такой как хлороформ (CHCl3), дихлорметан (DCM), этанол, ацетон, тетрагидрофуран (THF), 2,2,2-трифторэтанол, ацетонитрил, этилацетат, гексан, диметилформамид (DMF), диметилсульфоксид (ДМСО) и т.д.) для растворения катионного липида перед добавлением липида в масло.
[0209] С тем, чтобы облегчить растворение липида, может быть желательным нагреть масло до температуры от примерно 37°C до примерно 65°C. Для достижения желаемой конечной концентрации может быть отмерено требуемое количество катионного липида (например, DOTAP) и добавлено непосредственно в масло.
[0210] Если эмульсия содержит один или более ПАВ, ПАВ могут быть добавлены в масляную фазу или в водную фазу в соответствии с обычной практикой, принятой в данной области техники. Например, SPAN85 может быть растворен в масляной фазе (например, сквалене), а Tween 80 может быть растворен в водной фазе (например, в цитратном буфере).
[0211] В другом аспекте изобретение предоставляет способ получения композиции, которая содержит отрицательно заряженные молекулы (такие как РНК), находящиеся в комплексе с частицами эмульсии масло-в-воде, включающий: (i) предоставление описанной здесь эмульсии масло-в-воде; (ii) предоставление водного раствора, содержащего отрицательно заряженные молекулы (например, РНК); и (iii) объединение эмульсии масло в воде, полученной на этапе (i), и водного раствора, полученного на этапе (ii), с тем, чтобы образовался комплекс отрицательно заряженных молекул с частицами эмульсии.
[0212] Например, катионные эмульсии масло-в-воде могут быть объединены с водным раствором РНК в любых желаемых относительных количествах, например, примерно 1:1 (об./об.), примерно 1,5:1 (об./об.), примерно 2:1 (об./об.), примерно 2,5:1 (об./об.), 3:1 (об./об.), примерно 3,5:1 (об./об.), примерно 4:1 (об./об.), примерно 5:1 (об./об.), примерно 10:1 (об./об.), примерно 1:1,5 (об./об.), примерно 1:2 (об./об.), примерно 1:2,5 (об./об.), примерно 1:3 (об./об.), примерно 1:3,5 (об./об.), примерно 1:4 (об./об.), примерно 1:1,5 (об./об.) или примерно 1:1,10 (об./об.) и т.д.
[0213] Могут быть включены дополнительные необязательные этапы для обеспечения образования частиц, для улучшения комплексообразования между отрицательно заряженными молекулами и катионными частицами, повышения устойчивости отрицательно заряженных молекул (например, для предотвращения расщепления молекул РНК), для облегчения соответствующего распада комплекса/высвобождения отрицательно заряженных молекул (таких как молекула РНК) либо для предотвращения агрегации частиц эмульсии. Например, полимер (например, Pluronic® F127) или ПАВ может быть добавлен в водный раствор, который содержит отрицательно заряженные молекулы (например, РНК).
[0214] Размер частиц эмульсии может изменяться путем изменения отношения ПАВ к маслу (увеличение соотношения уменьшает размер частиц), рабочего давления (увеличение рабочего давления уменьшает размер частиц), температуры (повышение температуры уменьшает размер частиц), а также других параметров процесса. Фактический размер частиц также будет изменяться в зависимости от используемого конкретного ПАВ, масла и катионного липида и выбранных конкретных рабочих условий. Размер частиц эмульсии можно проверить при помощи устройств для сортировки частиц по размеру, таких как коммерческий анализатор субмикронных частиц (модель N4MD), производимый фирмой Coulter Corporation, при этом параметры можно менять, пользуясь изложенными выше руководящими принципами, таким образом, чтобы средний диаметр частиц был меньше, чем примерно 200 нм, меньше, чем примерно 150 нм или меньше, чем примерно 100 нм. Предпочтительно, средний диаметр частиц составляет примерно 180 нм или менее, примерно 150 нм или менее, примерно 140 нм или менее, или примерно 130 нм или менее, примерно 120 нм или менее, или примерно 100 нм или менее, от примерно 50 нм до 200 нм, от примерно 80 нм до 200 нм, от примерно 50 нм до 180 нм, от примерно 60 нм до 180 нм, от примерно 70 до 180 нм или от примерно 80 нм до 180 нм, от примерно 80 нм до примерно 170 нм, от примерно 80 нм до примерно 160 нм, от примерно 80 нм до примерно 150 нм, от примерно 80 нм до примерно 140 нм, от примерно 80 нм до примерно 130 нм, от примерно 80 нм до примерно 120 нм, от примерно 80 нм до примерно 110 нм или от примерно 80 нм до примерно 100 нм. Эмульсии, в которых средний размер частиц составляет примерно 200 нм или менее, обеспечивают стерильную фильтрацию.
[0215] Дополнительные способы получения катионной эмульсии масло-в-воде (эмульсии до образования комплекса) или комплекса отрицательно заряженная молекула-эмульсия включают, например, стерилизацию, выбор размера частиц (например, удаление крупных частиц), наполнение, упаковку и маркировку и т.д. Например, если эмульсия до образования комплекса или комплекс отрицательно заряженная молекула-эмульсия составлен для in vivo введения, он может быть стерилизован. Например, препаративная форма может быть стерилизована путем фильтрации через стерилизующий фильтр (например, через 0,22-микронный фильтр). Другие способы стерилизации включают тепловой процесс или процесс стерилизации излучением, или с использованием импульсного света для получения стерильной композиции.
[0216] Описанная здесь катионная эмульсия масло-в-воде может быть использована для производства вакцин. Стерильные и/или используемые для клинических целей катионные эмульсии масло-в-воде могут быть получены с использованием методов, аналогичных описанным для MF59. См., например, Ott et al., Methods in Molecular Medicine, 2000, Volume 42, 211-228, в Vaccine Adjuvants (O'Hagan ed.), Humana Press. Например, аналогично процессу изготовления MF59, масляная фаза и водная фаза эмульсии могут быть объединены и обработаны роторно-статорным гомогенизатором или поточным гомогенизатором с получением неочищенной эмульсии. Неочищенную эмульсию затем можно подать в микрофлюидизатор, где она может быть подвергнута дальнейшей обработке для получения стабильной субмикронной эмульсии. Неочищенную эмульсию можно пропускать несколько раз через камеру взаимодействия микрофлюидизатора до тех пор, пока не будет получен желаемый размер частиц. Нерасфасованную эмульсиию можно отфильтровать (например, через 0,22-мкм фильтр в атмосфере азота) для удаления крупных частиц, получая объем эмульсии, которым можно заполнить соответствующие контейнеры (например, стеклянные бутылки). Для вакцинных антигенов, которые продемонстрировали длительную стабильность в присутствии эмульсии масло-в-воде при хранении, антиген и эмульсия могут быть объединены и подвергнуты стерильной фильтрации (например, через 0,22-мкм мембранный фильтр). Объединенную в одном флаконе вакцину можно залить в контейнеры, содержащие единичную дозу. Для вакцинных антигенов, для которых не была показана длительная стабильность, эмульсия может поставляться в отдельном флаконе. В таких случаях объем эмульсии может быть отфильтрован-стерилизован (например, через 0,22-мкм фильтрационную мембрану), разлит и упакован в конечных флаконах, содержащих единичную дозу.
[0217] Контроль качества можно необязательно выполнять на небольшой выборке объема эмульсии или смешанной вакцины, а объем или смешанную вакцину можно упаковать в виде доз, только если образец прошел тест на контроль качества.
6. Наборы, фармацевтические композиции и введение
[0218] В другом аспекте настоящее изобретение относится к фармацевтической композиции, содержащей отрицательно заряженные молекулы (например, РНК) в комплексе с частицами катионной эмульсии масло-в-воде, как описано здесь, и может дополнительно содержать один или несколько фармацевтически приемлемых носителей, разбавителей или эксципиентов. В предпочтительных вариантах осуществления фармацевтическая композиция представляет собой иммуногенную композицию, которая может быть использована в качестве вакцины.
[0219] Альтернативно, описанные здесь композиции могут быть использованы для доставки отрицательно заряженных молекул в клетки. Например, молекулы нуклеиновых кислот (например, ДНК или РНК) могут быть доставлены в клетки для различных целей, например, для индукции производства желаемого генного продукта (например, белка), для регулировки экспрессии гена, для генной терапии и т.п. Описанные здесь композиции также могут быть использованы для доставки молекул нуклеиновой кислоты (например, ДНК или РНК) в клетки для терапевтических целей, таких как для лечения заболеваний, таких как рак или пролиферативные нарушения, заболевания обмена веществ, сердечно-сосудистых заболеваний, инфекций, аллергии, для индуцирования иммунного ответа и т.п. Например, молекулы нуклеиновой кислоты могут быть доставлены в клетки для ингибирования экспрессии целевого гена. Такие молекулы нуклеиновых кислот включают, например, антисмысловые олигонуклеотиды, двухцепочечные РНК, такие как малые интерферирующие РНК, и т.п. Двухцепочечные молекулы РНК, такие как малые интерферирующие РНК, могут вызывать РНК-интерференцию, которая приводит в частности к выключению соответствующего целевого гена (нокдауну гена). Антисмысловые олигонуклеотиды представляют собой одиночные нити ДНК или РНК, которые комплементарны выбранной последовательности. Как правило, антисмысловая РНК может предотвратить трансляцию белка с нитей определенных матричных РНК за счет связывания с ними. Для нацеливания на определенную, комплементарную (кодирующую или некодирующую) РНК можно использовать антисмысловую ДНК. Таким образом, описанные здесь катионные эмульсии могут быть использованы для доставки антисмысловых олигонуклеотидов или двухцепочечных РНК для лечения, например, рака путем ингибирования продуцирования онкологической мишени.
[0220] Настоящее изобретение также относится к наборам, в которых отрицательно заряженные молекулы (такие как РНК) и катионная эмульсия масло-в-воде находятся в отдельных контейнерах. Например, набор может содержать первый контейнер, содержащий композицию, содержащую отрицательно заряженные молекулы (например, РНК), и второй контейнер, содержащий катионную эмульсию масло-в-воде. Два компонента могут быть смешаны перед введением, например, в течение примерно 72 часов, примерно 48 часов, примерно 24 часов, примерно 12 часов, примерно 10 часов, примерно 9 часов, примерно 8 часов, примерно 7 часов, примерно 6 часов, примерно 5 часов, примерно 4 часов, примерно 3 часов, примерно 2 часов, примерно 1 часа, примерно 45 минут, примерно 30 минут, примерно 15 минут, примерно 10 минут, примерно 5 минут до введения. Два компонента могут быть также смешаны за примерно 1 минуту или непосредственно перед введением.
[0221] Отрицательно заряженные молекулы (например, РНК) могут находиться в жидкой форме или могут быть в твердой форме (например, лиофилизированной). Если они находятся в твердой форме, набор может содержать третий контейнер, содержащий подходящий водный раствор для регидратации отрицательно заряженных молекул. Подходящие водные растворы включают фармацевтически приемлемые буферы, такие как фосфатно-солевой буфер, раствор Рингера, раствор декстрозы или любой из описанных выше водных растворов. В некоторых вариантах осуществления в качестве водного раствора для регидратации можно использовать стерильную воду, в частности, в тех случаях, когда дополнительные компоненты, такие как регулирующие тоничность агенты и/или регулирующие осмомоляльность агенты, лиофилизируют вместе с отрицательно заряженными молекулами (например, РНК). Альтернативно, лиофилизованные отрицательно заряженные молекулы (например, РНК) могут быть смешаны непосредственно с катионной эмульсией.
[0222] Если композиция (например, вакцина) содержит отрицательно заряженные молекулы (например, РНК) и дополнительный компонент, такой как белок иммуногена, оба компонента могут быть заморожены и лиофилизированы (либо отдельно, либо в виде смеси), а перед введением восстановлены и смешаны с катионной эмульсией.
[0223] Набор может дополнительно содержать другие материалы, полезные для конечного пользователя, в том числе другие фармацевтически приемлемые используемые в препаративных формах растворы, такие как буферы, разбавители, фильтры, иглы и шприцы или другое устройство доставки. Например, набор может включать шприц с двойной камерой, который содержит воду или эмульсию в одной камере, а отрицательно заряженные молекулы (например, РНК), находящиеся в твердой (например, лиофилизированной) форме, в другой камере.
[0224] Набор может дополнительно включать другой контейнер, содержащий адъювант (такой как адъювант, содержащий алюминий, или MF59). Обычно адъюванты, содержащие алюминий, не являются предпочтительными, так как они могут мешать процессу комплексообразования отрицательно заряженной молекулы с катионной эмульсией.
[0225] Подходящие контейнеры для композиций включают, например, бутыли, флаконы, шприцы и пробирки. Контейнеры могут быть изготовлены из различных материалов, включая стекло или пластик. Контейнер может иметь стерильное входное отверстие (например, контейнер может представлять собой пакет для внутривенного раствора или флакон, имеющий пробку, прокалываемую иглой для подкожной инъекции). Также может использоваться шприц с двойной камерой, в котором отрицательно заряженные молекулы (например, РНК) лиофилизуют и либо восстанавливают, используя воду в шприце, либо восстанавливают, используя непосредственно описанную здесь катионную эмульсию.
[0226] Набор также может содержать вкладыш, содержащий письменные инструкции способов индуцирования иммунитета или способов лечения инфекций. Вкладыш может представлять собой неутвержденный проект инструкций по применению или может представлять собой инструкции по применению, утвержденные управлением по контролю за продуктами и лекарствами (FDA) или другим регулирующим органом.
[0227] Настоящее изобретение также предоставляет устройство доставки, предварительно заполненное описанной выше композицией.
[0228] Фармацевтические композиции по настоящему изобретению могут вводиться отдельно или в комбинации с одним или несколькими дополнительными терапевтическими агентами. Способы введения включают, без ограничения, пероральное введение, ректальное введение, парентеральное введение, подкожное введение, внутривенное введение, интравитреальное введения, внутримышечное введение, ингаляцию, интраназальное введение, местное введение, введение в глаз или введение в ухо.
[0229] Терапевтически эффективное количество описанных здесь композиций может варьировать в зависимости от, среди прочего, указанного заболевания, тяжести заболевания, возраста и относительного здоровья субъекта, активности вводимого соединения, способа введения и желаемого типа лечения.
[0230] В других вариантах осуществления описанные здесь фармацевтические композиции могут водиться в комбинации с одним или несколькими дополнительными терапевтическими агентами. Дополнительные терапевтические агенты могут включать, без ограничения, антибиотики или антибактериальные агенты, противорвотные средства, противогрибковые агенты, противовоспалительные агенты, противовирусные агенты, иммуномодулирующие агенты, цитокины, антидепрессанты, гормоны, алкилирующие агенты, антиметаболиты, противоопухолевые антибиотики, антимитотические агенты, ингибиторы топоизомеразы, цитостатики, антиинвазивные агенты, антиангиогенные средства, ингибиторы функции факторов роста, ингибиторы вирусной репликации, ингибиторы вирусных ферментов, противораковые средства, α-интерферон, β-интерферон, рибавирин, гормоны и другие модуляторы Toll-подобных рецепторов, иммуноглобулины (Igs) и антитела, модулирующие функцию Ig (например, анти-IgE (омализумаб)).
[0231] В некоторых вариантах осуществления представленные здесь фармацевтические композиции используются для лечения инфекционных заболеваний, включая, без ограничения, болезнь, вызываемую раскрытыми здесь патогенами, в том числе вирусные заболевания, такие как генитальные бородавки, обыкновенные бородавки, подошвенные бородавки, бешенство, респираторно-синцитиальный вирус (RSV), гепатит В, гепатит С, вирус денге, вирус желтой лихорадки, вирус простого герпеса (на примере только HSV-I, HSV-II, CMV или VZV), вирус контагиозного моллюска, вирус коровьей оспы, вирус оспы, лентивирус, вирус иммунодефицита человека (ВИЧ), вирус папилломы человека (ВПЧ), вирус гепатита (вирус гепатита С, вирус гепатита В, вирус гепатита А), цитомегаловирус (CMV), вирус ветряной оспы (VZV), риновирус, энтеровирус (например, EV71), аденовирус, коронавирус (например, SARS), вирус гриппа, вирус парагриппа, вирус эпидемического паротита, вирус кори, вирус краснухи, паповавирус, гепаднавирус, флавивирус, ретровирус, ареновирус (на примере только LCM, вирус Хунин, вирус Мачупо, вирус Гуанарито и лихорадки Ласса) и филовирус (на примере только вируса Эбола или вируса Марбурга).
[0232] В некоторых вариантах осуществления представленные здесь фармацевтические композиции используются для лечения бактериальных, грибковых и протозойных инфекций, включая, без ограничения, малярию, туберкулез и Mycobacterium avium, проказу; пневмоцитоза, вызываемого Pneumocystis carnii, криптоспоридиоза, гистоплазмоза, токсоплазмоза, трипаносомной инфекции, лейшманиоза, инфекций, вызванных бактериями родов Escherichia, Enterobacter, Salmonella, Staphylococcus, Klebsiella, Proteus, Pseudomonas, Streptococcus и Chlamydia, и грибковых инфекций, таких как кандидоз, аспергиллез, гистоплазмоз и криптококкового менингита.
[0233] В некоторых вариантах осуществления представленные здесь фармацевтические композиции используются для лечения респираторных заболеваний и/или расстройств, дерматологических расстройств, глазных болезней и/или нарушений, заболеваний и/или расстройств мочеполовой системы, включая отторжение аллотрансплантата, аутоиммунные и аллергические заболевания, рак или повреждения или старение кожи, такие как рубцы и морщины.
[0234] В другом аспекте изобретение предоставляет способ генерации или стимуляции иммунного ответа у субъекта, нуждающегося в этом, например, млекопитающего, включающий введение эффективного количества описанной здесь композиции. Иммунный ответ предпочтительно является защитным и предпочтительно включает в себя антительный и/или клеточно-опосредованный иммунитет. Способ может использоваться для индуцирования первичного иммунного ответа и/или усиления иммунной реакции.
[0235] В некоторых вариантах осуществления описанные здесь композиции могут использоваться в качестве лекарственного средства, например, для повышения или усиления иммунного ответа у нуждающегося в этом субъекта, такого как млекопитающее.
[0236] В некоторых вариантах осуществления описанные здесь композиции могут использоваться для производства лекарственного средства, предназначенного для генерации или потенцирования иммунного ответа у нуждающегося в этом субъекта, например, млекопитающего.
[0237] Млекопитающее является предпочтительно человеком, но может быть, например, коровой, свиньей, курицей, кошкой или собакой, так как охватываемые настоящим изобретением патогены могут вызывать проблемы у широкого спектра видов. Если вакцина предназначена для профилактического применения, человек является предпочтительно ребенком (например, дошкольного возраста или младенец), подростком или взрослым; если вакцина предназначена для терапевтического применения, человек является предпочтительно подростком или взрослым. Вакцина, предназначенная для детей, может также вводиться взрослым, например, для оценки безопасности, дозировки, иммуногенности и т.д.
[0238] Один из способов проверки эффективности терапевтического лечения включает мониторинг патогенной инфекции после введения раскрытых здесь композиций или вакцин. Один из способов проверки эффективности профилактического лечения включает мониторинг иммунных ответов на антиген, системный (например, мониторинг уровня продуцирования IgG1 и IgG2a) и/или слизистой (например, мониторинг уровня продуцирования IgA). Как правило, реакции на сывороточные антиген-специфические антитела определяют после иммунизации, но до контрольного заражения, тогда как антиген-специфические реакции слизистой определяют после первой иммунизации и после контрольного заражения.
[0239] Другой способ оценки иммуногенности раскрытых здесь композиций или вакцин, в которых молекула нуклеиновой кислоты (например, РНК) кодирует белковый антиген, заключается в экспрессии белкового антигена с использованием рекомбинантных способов для скрининга сывороточных или слизистых выделений пациентов иммуноблот-анализом и/или при помощи микрочипов. Положительная реакция между белком и образцом пациента указывает на то, что пациент имеет иммунный ответ на исследуемый белок. Этот способ также может быть использован для идентификации иммунодоминантных антигенов и/или эпитопов в белковых антигенах.
[0240] Эффективность композиций также можно определять in vivo, заражая соответствующие животные модели возбудителем представляющей интерес инфекции.
[0241] Дозировка может осуществляться в режиме единичных доз или множественных доз. Множественные дозы могут использоваться в режиме первичной иммунизации и/или в режиме вторичной иммунизации. В режиме множественных доз разные дозы могут вводиться одним и тем же или разными путями, например, первичное воздействие путем парентерального введения, а вторичная бустерная прививка через слизистую; первичное воздействие на слизистую и бустерное парентеральное введение, и т.д. Множественные дозы обычно вводят по меньшей мере через 1 неделю (например, примерно 2 недели, примерно 3 недели, примерно 4 недели, примерно 6 недель, примерно 8 недель, примерно 10 недель, примерно 12 недель, примерно 16 недель и т.д.).
[0242] В конкретных вариантах осуществления общее количество катионного липида, такого как DOTAP, которое вводят субъекту за одно введение, не превышает примерно 30 мг или не превышает 24 мг.
[0243] В некоторых вариантах осуществления общее количество катионного липида, такого как DOTAP, который вводят субъекту за одно введение, составляет не более 4 мг.
[0244] Раскрытые здесь композиции, которые включают в себя один или несколько антигенов или используются в сочетании с одним или несколькими антигенами, могут быть использованы для лечения детей и взрослых. Таким образом, человеческий субъект может быть младше 1 года, 1-5 лет, 5-15 лет, 15-55 лет или по меньшей мере 55 лет. Предпочтительными субъектами для получения композиций являются пожилые люди (например, >50 лет, >60 лет и, предпочтительно, >65 лет), молодые (например, <5 лет), госпитализированные пациенты, медицинские работники, вооруженные службы и военный персонал, беременные женщины, больные хроническими заболеваниями или иммунодефицитом. Однако композиции пригодны не только исключительно для этих групп, а могут иметь более широкое применение, во всей популяции.
[0245] Раскрытые здесь композиции, которые включают в себя один или несколько антигенов или используются в сочетании с одним или несколькими антигенами, могут вводиться пациентам по существу одновременно (например, во время одной медицинской консультации или посещения врача или центр вакцинации) с другими вакцинами, например, по существу в то же самое время в качестве вакцины против кори, вакцины против паротита, вакцины против краснухи, MMR вакцины, вакцины против ветряной оспы, MMRV вакцины, вакцины против дифтерии, вакцины против столбняка, вакцины против коклюша, DTP вакцины, конъюгированной вакцины против H. influenzae типа b, инактивированной вакцины против полиовируса, вакцины против вируса гепатита В, конъюгированной менингококковой вакцины (например, четырехвалентной вакцины А С W135 и Y), вакцины против респираторно-синцитиального вируса и т.д.
[0246] В некоторых вариантах осуществления представленные здесь композиции включают или необязательно включают один или несколько иммунорегуляторных средств, таких как адъюванты. Примеры адъювантов включают, без ограничения, TH1 адъювант и/или TH2 адъювант, которые дополнительно обсуждаются ниже. В некоторых вариантах осуществления вспомогательные вещества, используемые в представленных здесь иммуногенных композициях, включают, без ограничения:
1. композиции, содержащие минералы;
2. масляные эмульсии;
3. препараты сапонина;
4. виросомы и вирусоподобные частицы;
5. вещества бактериального или микробного происхождения;
6. биоадгезивы и мукоадгезивы;
7. липосомы;
8. препаративные формы на основе полиоксиэтиленового простого эфира и полиоксиэтиленового сложного эфира;
9. полифосфазен (РСРР);
10. мурамилпептиды;
11. имидазохинолоновые соединения;
12. тиосемикарбазоновые соединения;
13. триптантриновые соединения;
14. человеческие иммуномодуляторы;
15. липопептиды;
16. бензонафтиридины;
17. микрочастицы;
18. иммуностимулирующий полинуклеотид (например, РНК или ДНК; например, CpG-содержащие олигонуклеотиды).
ПРИМЕРЫ
[0247] Описанное в общем виде настоящее изобретение станет более понятным при ознакомлении с приведенными ниже примерами, которые включены исключительно с целью иллюстрации определенных аспектов и вариантов осуществления настоящего изобретения и не предназначены для его ограничения.
Пример 1: Разработка катионных эмульсий масло-в-воде
[0248] В этом примере для доставки самореплицирующейся РНК были разработаны катионные наноэмульсии (называемые здесь "CNE"), которые содержат высокие концентрации катионного липида (DOTAP).
[0249] Композиции CNE суммированы в приведенной ниже таблице 1 и были модифицированы на основе CNE01. В сравнительных исследованиях в качестве эталонных образцов были использованы CNE01, CMF40, CNE16, CNE02 и CNE17.
|
|
[0250] CNE были получены аналогично заряженному MF59, как описано ранее (Ott et al., Journal of Controlled Release, volume 79, pages 1-5, 2002), исключая одну основную модификацию. DOTAP растворяли непосредственно в сквалене без использования органического растворителя. Было обнаружено, что включение растворителя в эмульсии, которые содержали больше чем 1,6 мг/мл DOTAP, приводило к получению пенистого исходного материала, из которого нельзя образовать микрофлюиды для получения эмульсии. Нагревание сквалена до 37°C позволило растворить DOTAP непосредственно в сквалене, а затем позволило успешно диспергировать масляную фазу в водной фазе (например, путем гомогенизации) с получением эмульсии. DOTAP растворяется в сквалене, и могут быть получены более высокие концентрации DOTAP в сквалене, чем те, которые приведены в таблице 1. Однако имеются сообщения о том, что высокие дозы DOTAP могут быть токсичными. См., например, Lappalainen et al., Pharm. Res., vol. 11(8):1127-31 (1994).
[0251] Сквален нагревали до 37°C, и DOTAP растворяли непосредственно в сквалене в присутствии Span 85. Затем полученную масляную фазу объединяли с водной фазой (Tween 80 в цитратном буфере) и сразу гомогенизировали в течение 2 мин в гомогенизаторе IKA T25 при 24K об/мин для получения гомогенного маточного раствора (первичной эмульсии). Первичные эмульсии пропускали пять раз через микрофлюидизатор M-110S или микрофлюидизатор М-110P мл (Microfluidics, Newton, MA), используя охлаждающий змеевик на ледяной бане, при давлении гомогенизации около 15K-20K psi (фунт/дюйм2). Из емкости отбирали по 20 мл образца партии и помещали на хранение при 4°C.
[0252] Следует отметить, что приведенные в таблице 1 концентрации компонентов CNE представляют собой концентрации, рассчитанные с учетом начального количества компонентов, использованных для приготовления эмульсии. Известно, что в процессе получения эмульсий или во время стерилизации фильтрованием, происходит естественная потеря некоторого количества сквалена, DOTAP или других компонентов, и реальная концентрация этих компонентов в конечном продукте (например, упакованной, стерилизованной эмульсии, готовой для применения) может быть немного ниже, обычно до примерно 20%, иногда до примерно 25% или до примерно 35%. Тем не менее, в данной области техники общепринято описывать концентрацию конкретного компонента, исходя из его исходного количества, которое используется для приготовления эмульсии, а не фактической концентрации в конечном продукте.
[0253] В приведенной ниже таблице 2 показана разница между "теоретическими" концентрациями сквалена и DOTAP (рассчитанными, исходя из исходных количеств сквалена и DOTAP, которые были использованы для приготовления эмульсии) и фактическими концентрациями сквалена и DOTAP, измеренными в конечном продукте.
|
|
Пример 2: Получение комплексов РНК-частица
1. Синтез РНК
[0254] Плазмидную ДНК, кодирующую репликон на основе альфавируса (самореплицирующуюся РНК), использовали в качестве матрицы для in vitro синтеза РНК. Каждый репликон содержал генетические элементы, необходимые для репликации РНК, но в нем отсутствовали последовательности, кодирующие генные продукты, необходимые для сборки частиц. Структурные гены генома альфавируса были заменены на последовательности, кодирующие гетерологичный белок (экспрессия которого инициируется субгеномным промотором альфавируса). После доставки репликонов в эукариотические клетки положительная нить РНК транслировалась для продуцирования четырех неструктурных белков, которые вместе реплицировали геномную РНК и транскрибировали избыточное количество субгеномных мРНК, кодирующих гетерологичный белок. Поскольку экспрессия структурных белков альфавирусов отсутствовала, репликоны были не способны образовывать инфекционные частицы. Промотор бактериофага Т7 был расположен выше кДНК альфавируса для облегчения синтеза РНК-репликона in vitro, а рибозим вируса гепатита дельта (HDV), расположенный сразу за "хвостом" поли(А), генерировал правильный 3'-конец в результате саморепликации.
[0255] После линеаризации плазмидной ДНК ниже от рибозима HDV при помощи соответствующей рестрикционной эндонуклеазы, была синтезирована in vitro опытная партия транскриптов с использованием ДНК-зависимой РНК-полимеразы, полученной из бактериофага T7 или SP6. Транскрипцию проводили в течение 2 часов при 37°C в присутствии конечной концентрации каждого из нуклеозидтрифосфатов (АТФ, ЦТФ, ГТФ и УТФ), составляющей 7,5 мМ (РНК-полимеразы Т7) или 5 мМ (РНК-полимеразы SP6), следуя инструкциям изготовителя (Ambion, Austin, TX). После транскрипции ДНК-матрицу разрушали ДНКазой TURBO (Ambion, Austin, TX). РНК-репликон осаждали LiCl и восстанавливали в воде, свободной от нуклеаз. Некэппированную РНК кэпировали после транскрипции, используя фермент коровьей оспы (VCE) с системой кэпирования ScriptCap m7G (Epicentre Biotechnologies, Madison, WI), следуя инструкциям в руководстве пользователя. Посттранскрипционно кэпированную РНК осаждали LiCl и восстанавливали в воде, свободной от нуклеаз. Альтернативно, репликоны могут быть кэпированы в ходе дополнительной реакции транскрипции с 6 мМ (для РНК-полимеразы Т7) или 4 мМ (для РНК-полимеразы SP6) при помощи m7G(5')ppp(5')G, аналога необратимой кэп-структуры (New England Biolabs, Beverly, MA), и уменьшением концентрации гуанозинтрифосфата до 1,5 мМ (для РНК-полимеразы T7) или 1 мМ (для РНК-полимеразы SP6). Затем транскрипты могут быть очищены путем расщепления под действием ДНКазы TURBO (Ambion, Austin, TX) с последующим осаждением LiCl и промывкой 75%-ным этанолом.
[0256] Концентрацию образцов РНК определяли путем измерения оптической плотности при 260 нм. Целостность in vitro транскриптов подтверждали наличием конструкций полной длины, выявляемых методом денатурирующего электрофореза в агарозном геле.
2. РНК комплексообразование
[0257] Термин ссоотношение N/P относится к количеству азота в катионном липиде относительно количества фосфатов на РНК. Азот представляет собой элемент, несущий заряд, в тестируемых катионных липидах. Фосфат можно найти на каркасе РНК. Соотношение зарядов N/P, равное 10/1, указывает, что на каждые 10 положительно заряженных атомов азота в катионном липиде имеется один отрицательно заряженный фосфат на РНК.
[0258] Количество атомов азота в растворе рассчитывают, исходя из концентрации катионного липида, DOTAP, например, имеет один атом азота, который может быть протонирован в расчете на одну молекулу. Концентрацию РНК использовали для вычисления количества фосфата в растворе из расчета 3 нмоль фосфата на мкг РНК. Соотношение N/P может быть модифицировано изменением соотношения РНК:липид. В некотором диапазоне соотношений азот/фосфат (N/P) РНК образует комплекс с CNE. Соотношение N/P вычисляли путем определения количества молей протонируемого азота в эмульсии на миллилитр. Для вычисления количества фосфатов использовали постоянное значение, равное 3 нмоль фосфата на мкг РНК. После определения значений, к РНК добавляли эмульсию в количестве, необходимом для получения подходящего соотношения. Используя эти значения, РНК разводили до соответствующей концентрации и добавляли непосредственно в равный объем эмульсии при слабом помешивании. Раствор выдерживали при комнатной температуре в течение примерно 2 часов. После процесса комплексообразования полученный раствор разбавляли до соответствующей концентрации и использовали в течение 1 часа.
3. Анализ размера частиц
[0259] Размер частиц эмульсии измеряли, используя анализатор размера частиц Nano ZS (Malvern Instruments, Worcestershire, UK), следуя инструкциям изготовителя. Размеры частиц представлены в виде Z-средней (ZAve) с индексом полидисперсности (pdi). Все образцы разбавляли перед измерением водой. Кроме того, размер частиц эмульсии измеряли классификатором частиц Horiba LA-930 (Horiba Scientific, USA). Перед измерением образцы разводили водой. Дзета-потенциал измеряли анализатором размера частиц Nano ZS, используя разбавленные образцы, следуя инструкциям изготовителя.
4. Частицы вирусных репликонов (VRP)
[0260] Для сравнения РНК-вакцин с традиционными подходами с использованием векторной РНК для достижения in vivo экспрессии репортерных генов или антигенов, использовали частицы вирусных репликонов (VRP), продуцированных в клетках ВНК способом, описанным у Perri et al., J. Virol, 77:10394-10403 (2003). В этой системе репликоны антигенов (или гена-репортера) состояли из химерных репликонов альфавируса (VCR), полученных из генома вируса венесуэльского лошадиного энцефалита (VEEV), сконструированного таким образом, чтобы он содержал 3'-концевые последовательности (3'-UTR) вируса Синдбис и сигнальную последовательность, обеспечивающую упаковку вируса Синдбис (PS) (см. Фиг. 2, Perri S., et al., J Virol 77:10394-10403 (2003)). Эти репликоны были упакованы в VRP путем их совместной электропорации в клетки почки детеныша хомячка (ВНК) вместе с дефектными хелперными РНК, кодирующими капсид вируса Синдбис и гены гликопротеина (см. Фиг. 2, Perri et al.). Затем VRP собирали и титровали стандартными методами и инокулировали животным в культуральной жидкости или других изотонических буферах.
Пример 3: Влияние концентрации DOTAP на иммуногенность
[0261] Этот пример показывает, что катионные эмульсии масло-в-воде, полученные с высокой концентрацией DOTAP, увеличивали иммуногенность РНК репликона, кодирующего RSV-F антиген в мышиной модели.
1. Материалы и методы
Анализ связывания гепарина
[0262] Был образован описанный выше комплекс РНК. Комплекс РНК/CNE инкубировали с разными концентрациями сульфата гепарина (Alfa Aesar, Ward Hill MA) в течение 30 минут при комнатной температуре. Затем полученные растворы помещали в ультрацентрифугу с воздушным приводом (Beckman Coulter, Brea, CA) на 15 минут. Центрифужные пробирки прокалывали туберкулиновым шприцем и удаляли жидкость под осадком. Затем раствор анализировали в отношении концентрации РНК, используя анализ Ribogreen (Invitrogen, Carlsbad CA), следуя инструкциям производителя. Образцы анализировали на флуоресцентном планшетном ридере Biotek Synergy 4 (Winooski, VT). Величину свободных РНК рассчитывали, используя стандартную кривую.
2. Влияние концентрации DOTAP на взаимодействие РНК-частица
[0263] В таблице 3 показано влияние концентрации DOTAP на взаимодействие РНК-частица (определенное анализом связывания гепарина, которым измеряли плотность взаимодействия РНК-частица) и иммуногенность.
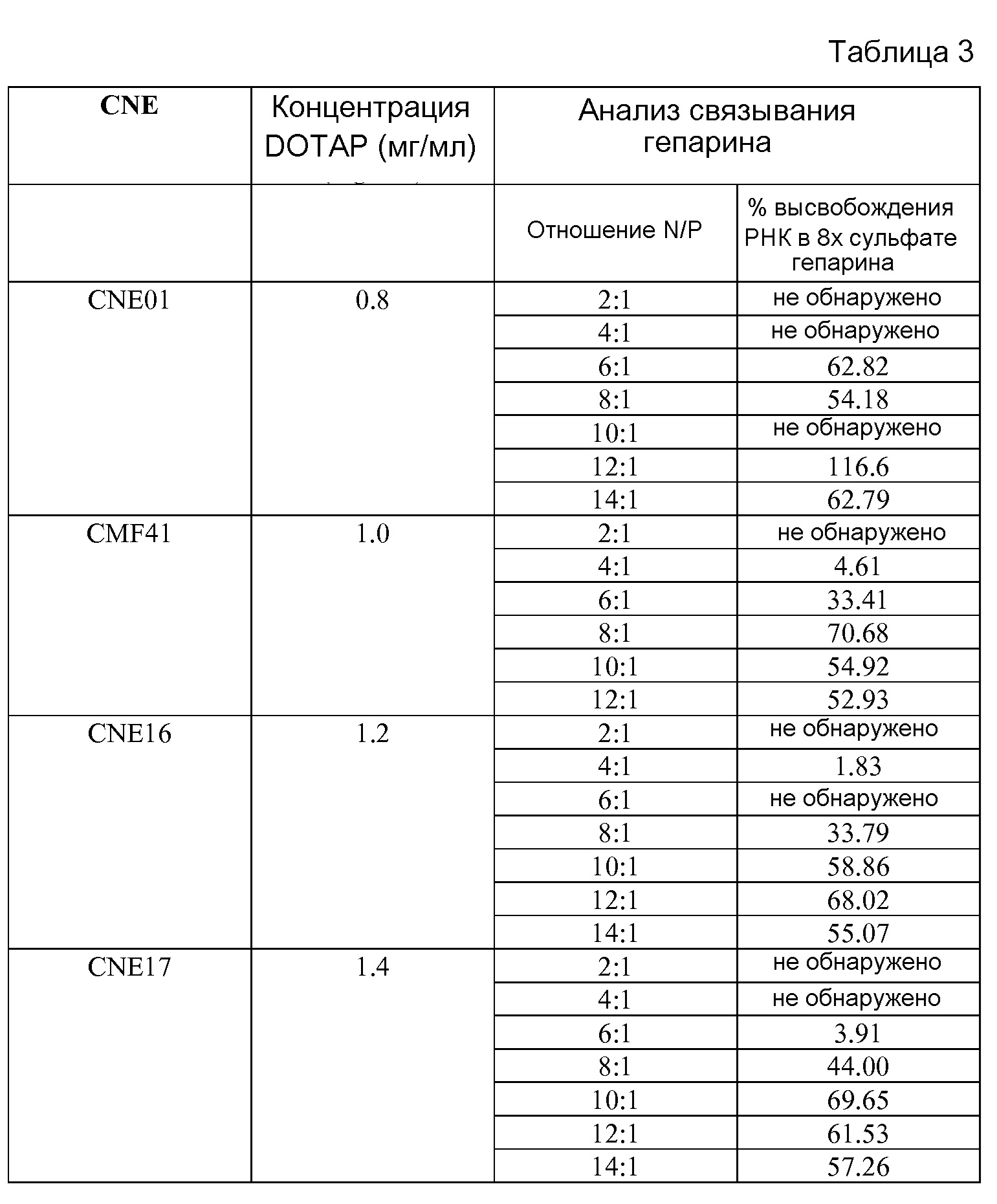
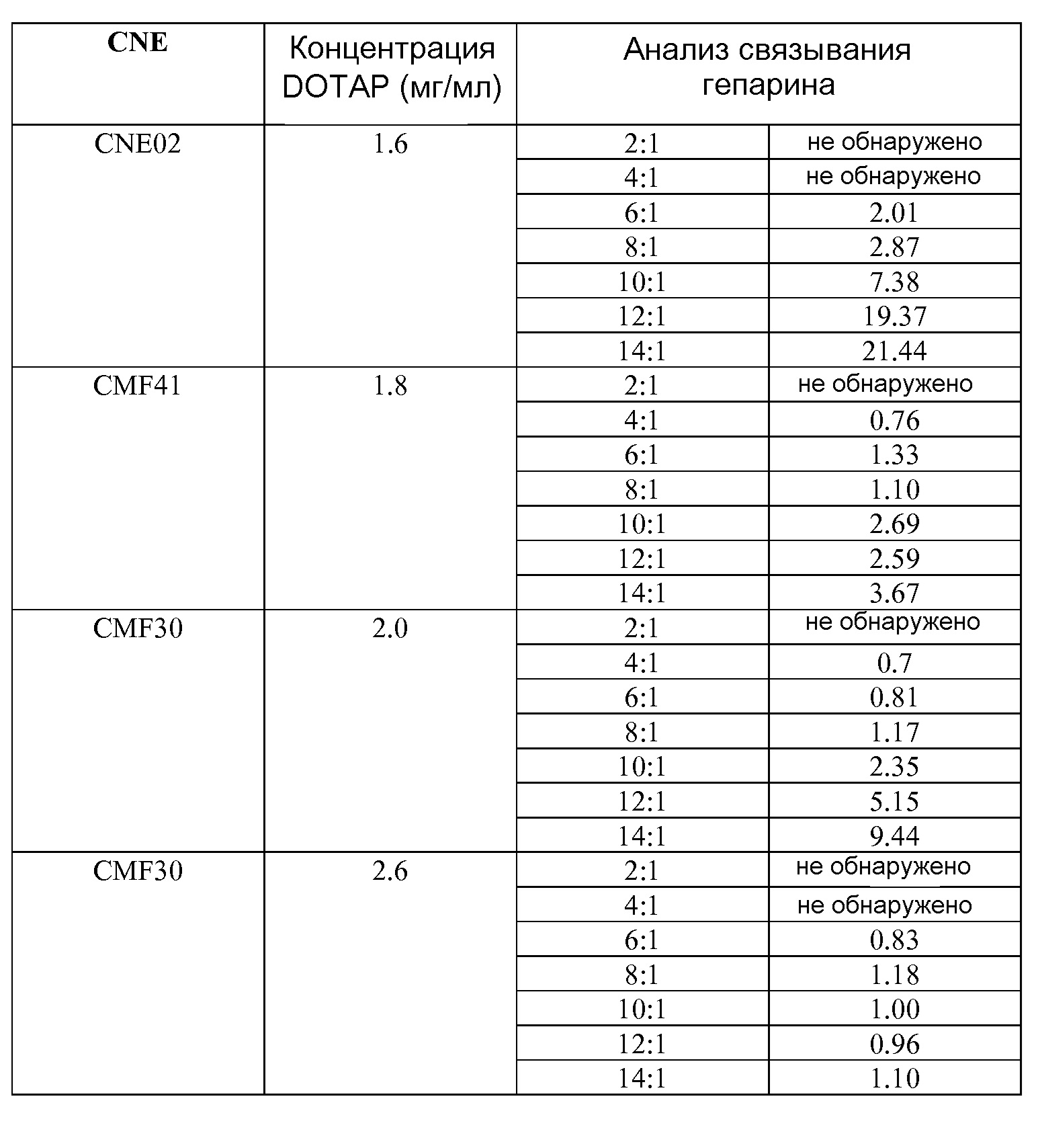
[0264] Из Таблицы 3 видно, что молекулы РНК сильно связаны с частицами эмульсии, которая была получена при высокой концентрации DOTAP (1,8 мг/мл или выше).
3. Влияние концентрации DOTAP на содержание РНК
[0265] В таблице 4 показано влияние концентрации DOTAP на содержание РНК. Повышение концентрации DOTAP приводило к увеличению количества молекул РНК, вовлеченных в комплексообразование РНК-частица.
|
4. Влияние концентрации DOTAP на иммуногенность
[0266] В таблице 5 показано влияние концентрации DOTAP на иммуногенность RSV-F антигена в in vivo мышиной модели.
[0267] Для этого исследования был использован репликон vA317, который экспрессирует слитый поверхностный гликопротеин RSV (RSV-F). 8-10-недельным мышам BALB/с весом около 20 г (по 10 животных в группе) делали двусторонние внутримышечные прививки. На день 0 и 21 всем животным в четырехглавую мышцу двух задних ног вводили эквивалентные объемы (по 50 мкл на ногу) голой самореплицирующейся РНК, экспрессирующей RSV-F (vA317, 1 мкг), 1 мкг A317, находящейся в составе липосомы, которая содержала 40% DlinDMA, 10% DSPC, 48% Chol, 2% PEG DMG 2000 (RV01(15)), или самореплицирующейся РНК, находящейся в составе указанных CNE (1 мкг vA317). Для каждого введения использовали свежеприготовленные препаративные препараты. Сыворотку собирали для анализа антител на 14 день (2wp1) и 35 день (2wp2).
|
|
[0268] Как показано в Таблице 5, увеличение концентрации DOTAP приводило к увеличению количества РНК, содержащейся в частицах эмульсии, что в свою очередь усиливало иммунный ответ. Для CMF31 наблюдалось увеличение титра антител в 3 раза (при 2wp2) по сравнению с CNE17. В этой модели плато иммуногенности наблюдалось при концентрации DOTAP, равной 2,6 мг/мл (CMF31).
[0269] Когда количество РНК и DOTAP, введенное каждой мыши оставалось постоянным (что означает, что в эмульсиях с более высокими концентрациями DOTAP были использованы меньшие объемы эмульсии для получения комплекса РНК/частицы эмульсии; затем перед иммунизацией препаративные формы РНК/частицы эмульсии разводили таким образом, чтобы мышам вводились равные объемы препаративных форм РНК/частицы эмульсии), титры F-специфических суммарных IgG сравнивали с разными препаративными формами CNE (таблица 6). Для всех препаративных форм CNE был использован репликон vA317. РНК получали, используя набор Ambion. Данные GMT отражают среднегеометрическое значение титра отдельных мышей в каждой группе (8 мышей/группу). Результат показывает, что для эмульсий с более высокими концентрациями DOTAP потребовалось меньшее количество препаративной формы.
|
Титры сыворотки для предварительной иммунизации содержали недетектируемые титры.
[0270] Когда количество сквалена и соотношение N/P (DOTAP:РНК), вводимое каждой мыши, поддерживали на постоянном уровне, титры F-специфических IgG увеличивались, поскольку в препаративных формах увеличивалось количество РНК и DOTAP (таблица 7). Для всех препаративных форм CNE использовали репликон vA317. РНК получали, используя набор Ambion. Данные GMT отражают среднегеометрическое значение титра для отдельных мышей в каждой группе (8 мышей/группу). Результаты показывают, что увеличение концентрации DOTAP приводило к увеличению количества РНК, содержащейся в частицах эмульсии, что в свою очередь приводило к усилению иммунного ответа.
|
|
[0271] Были проведены дальнейшие исследования CMF32 и CMF34 при разных соотношениях N/P. В таблице 8 показаны титры F-специфических суммарных IgG для препаративных составов. Теоретические соотношения N/P отражают соотношения N/P, вычисленные, исходя из начальных объемов DOTAP и РНК, которые использовались для получения композиций. Фактические значения N/P были несколько ниже, чем теоретические соотношения N/P, в связи с потерями небольших количеств DOTAP во время приготовления эмульсии. Для всех CNE и CMF использовали vA317. Данные GMT отражают среднее логарифмическое значение титра отдельных мышей в каждой группе (8 мышей/группу). Осмоляльность всех препаративных форм доводили до 300 мОсм/кг, используя сахарозу. Для всех препаративных форм CMF32 и CMF34 не наблюдалось никаких явных признаков непереносимости (например, масса тела, ранние цитокины в сыворотке).
[0272] Фактические соотношения N/P определяли по количественному содержанию DOTAP в партиях CNE или CMF методом ВЭЖХ, используя заряженный аэрозольный детектор (Corona Ultra, Chelmsford, MA). Образцы CNE и CMF разбавляли изопропанолом и вводили в 4,6×150 мм 3,5 мкм колонку XTera C18 (Waters, Milford, MA). Площадь под кривой измеряли для пика DOTAP на хроматограмме, и концентрацию интерполировали, исходя из стандартной кривой DOTAP. Используя фактическую концентрацию DOTAP, вычисляли фактическое соотношение N/P.
|
|
Пример 4: Влияние концентрации DOTAP на иммуногенность
[0273] В этом примере показано, что катионные эмульсии масло-в-воде, полученные с высокой концентрацией DOTAP, увеличивали иммуногенность РНК репликона, кодирующего RSV-F антиген в модели хлопковой крысы.
1. Материалы и методы
[0274] РНК репликон. Последовательность РНК репликона, vA142 RSV-F-delFP-полный рибозим.
[0275] Вакцинация хлопковых крыс. Самок хлопковых крыс (Sigmodon hispidis) получали из лабоаторий Harlan. Все исследования были одобрены и проводились в соответствии с требованиями комитета Novartis по уходу и использованию животных. Группы животных были иммунизированы внутримышечно (i.m., 100 мкл) указанными вакцинами в день 0. Образцы сыворотки отбирали через 3 недели после каждой иммунизации. Иммунизированных или невакцинированных контрольных животных инфицировали интраназально (i.n.) 1×105 PFU RSV через 4 недели после последней иммунизации.
[0276] Вакцина тримерной субъединицы RSV-F. RSV-F тример представляет собой рекомбинантный белок, содержащий эктодомен RSV-F с делецией участка слитого белка, которая препятствует связыванию с другими тримерами. Полученная конструкция образует гомогенный тример, обнаруживаемый при помощи гель-проникающей хроматографии, и имеет ожидаемое фенотипическое соответствие образуемой после слияния F-конформации, наблюдаемой посредством электронной микроскопии. Белок экспрессировали в клетках насекомых или клетках СНО и очищали путем слияния His-метки с С-концом этой конструкции с последующей гель-проникающей хроматографией, используя обычные методы. Полученный образец белка имел чистоту больше чем 95%. Для in vivo оценки F-субъединичной вакцины 100 мкг/мл тримерного белка адсорбировали на 2 мг/мл квасцов в 10 мМ гистидиновом буфере, рН 6,3, и доводили изотоничность хлоридом натрия до 150 мМ. F-субъединичный белок адсорбировали на квасцах в течение ночи при осторожном перемешивании при 2-8°C.
[0277] RSV-F-специфический ELISA. Отдельные образцы сыворотки анализировали на наличие RSV-F-специфического IgG твердофазным иммуноферментным анализом (ELISA). Планшеты ELISA (MaxiSorp 96-луночный, Nunc) покрывали 1 мкг/мл очищенным RSV-F (delp23-furdel-укороченный нерасщепленный) в PBS в течение ночи при 4°C. После промывки (PBS с 0,1% Tween®-20), планшеты блокировали блокирующим буфером Superblock в PBS (Thermo Scientific) в течение по меньшей мере 1,5 часов при 37°C. Затем планшеты промывали, добавляли серийные разведения в аналитическом разбавителе (PBS с 0,1% Tween®-20 и 5% козьей сыворотки) сывороток, полученных из экспериментальных или контрольных хлопковых крыс, и планшеты инкубировали в течение 2 часов при 37°C. После промывки планшеты инкубировали с конъюгированными с пероксидазной хрена (HRP) куриными антителами к IgG хлопковой крысы (иммунопероксидазный конъюгат chicken anti-cotton rat IgG-HRP, Immunology Consultants Laboratory, Inc, разбавленный 1:5000 в аналитическом разбавителе) в течение 1 часа при 37°C. Наконец, планшеты промывали, и в каждую лунку добавляли по 100 мкл раствора субстрата пероксидазы ТМВ (Kirkegaard & Perry Laboratories, Inc). Реакции останавливали добавлением 100 мкл 1М H3PO4, и, используя планшет-ридер, считывали оптическую плотность при 450 нм. Для каждого образца сыворотки строили график зависимости оптической плотности (OD) от логарифма разведения сыворотки, взятого с обратным знаком, методом нелинейной регрессии (GraphPad Prism). Титры определяли как разведение сыворотки, взятое с обратным знаком, при значении OD, равном примерно 0,5 (нормализованном для стандарта, объединенная сыворотка, полученная из RSV-инфицированных хлопковых крыс с определенным титром - 1:2500, которая вводилась в каждый планшет).
[0278] Микроанализ на нейтрализацию. Образцы сыворотки проверяли на наличие нейтрализующих антител при помощи теста на нейтрализацию бляшкообразования (PRNT). Двукратные серийные разведения HI-сыворотки (в PBS с 5% HI-FBS) добавляли к равному объему длинных RSV, предварительно оттитрованных до примерно 115 PFU/25 мкл. Смеси сыворотка/вирус инкубировали в течение 2 часов при 37°C и 5% CO2, обеспечивая возможность для осуществления нейтрализации вируса, а затем 25 мкл этой смеси (содержащей примерно 115 PFU) инокулировали в парные лунки, содержащие Нер-2 клетки в 96-луночных планшетах. Через 2 ч после выдерживания при 37°C и 5% CO2 клетки покрывали 0,75% метилцеллюлозы/5% EMEM с HI-FBS и инкубировали в течение 42 часов. Количество инфекционных вирусных частиц определяли путем выявления образования синцитий методом иммунного окрашивания с последующим автоматизированным подсчетом. Титры нейтрализации определяли как взятое с обратным знаком разведение сывороток, приводящее к по меньшей мере 60% уменьшению количества сцинтий на лунку относительно контроля (без сыворотки).
2. Влияние концентрации DOTAP на иммуногенность
[0279] В таблице 9 показано влияние концентрации DOTAP на иммуногенность антигена RSV-F в in vivo модели хлопковой крысы. В первых двух вакцинациях использовали препаративные формы РНК/CNE, как показано в таблице 9. Для третьей вакцинации использовали 3 мкг F-субъединичного белка RSV (в квасцах) для всех животных, за исключением интактной группы.
|
|
Ambion MegaScript РНК и синтезированную в лошадях РНК получали, используя разные способы.
[0280] Из приведенных в таблице 9 данных видно, что все препаративные формы CNE-РНК индуцировали дозозависимый иммунный ответ у хозяев (суммарные титры IgG, а также титры нейтрализующих антител). Введение препаративных форм CMF31-РНК и РНК-CMF34 продуцировало аналогичные F-специфические суммарные IgG титры, и каждый был больше, чем у CNE17 для каждой из указанных доз РНК. Кроме того, все препаративные формы CNE-РНК индуцировали появление хороших титров нейтрализующих антител при 10 мкг РНК. Титры нейтрализующих антител для групп CMF31-РНК, CMF34-РНК и CNE17-РНК были сходными, за исключением удивительно высокого титра для группы, получившей 1 мкг РНК/CMF31.
[0281] Пример 5: Оценка влияния буферных композиций на иммуногенность
[0282] В этом примере различные эмульсии на основе CMF34 были приготовлены с использованием различных буферных компонентов.
[0283] В таблице 10 суммированы результаты изучения иммуногенности у мышей при использовании РНК в препаративных формах CMF34, приготовленных с использованием различных буферных систем.
|
|
Пример 6: Стабильность эмульсий
[0284] Стабильность CMF34 оценивали путем измерения среднего диаметра частиц эмульсии и полидисперсности после процесса приготовления эмульсии (Т=0), через 1 месяц хранения при 4°C (Т=1 месяц) и через 2 месяца хранения при 4°C (Т=2 месяца). Стабильность оценивали также через 3, 6 и 12 месяцев хранения при 4°C. Результаты, представленные в таблице 11, показывают, что эмульсия была стабильной по меньшей мере в течение 12 месяцев.
|
Пример 7: Иммуногенность репликонов, кодирующих белок А вируса герпеса.
А. Белки CMV
[0285] Получали бицистронные и пентацистронные репликоны альфавируса, которые экспрессировали гликопротеиновые комплексы из человеческого цитомегаловируса (HCMV) и которые схематически показаны на Фиг. 1 и Фиг. 3. Репликоны альфавируса были сконструированы на основе вируса венесуэльского конского энцефалита (VEE). Репликоны были упакованы в частицы вирусных репликонов (VRP), инкапсулированы в липидные наночастицы (LNP) или приготовлены в виде составленных препаратов с CMF34. Экспрессию кодируемых белков HCMV и белковых комплексов из каждого репликона подтверждали иммуноблот-анализом, методами со-иммунопреципитации и проточной цитометрии. Проточную цитометрию использовали для проверки экспрессии пентамерного комплекса gH/gL/UL128/UL130/UL131 из пентамерных репликонов, кодирующих белковые компоненты комплекса, с использованием человеческих моноклональных антител, специфичных к конформационным эпитопам, имеющимся в напентамерном комплексе (Macagno et al. (2010), J. Virol. 84(2):1005-13). На Фиг. 2 показано, что эти антитела связываются с клетками BHKV, трансфицированными РНК репликоном, экспрессирующим пентамерный комплекс gH/gL/UL128/UL130/UL131 (A527) HCMV. Аналогичные результаты были получены при инфицировании клеток VRP, полученных из такого же конструкта репликона. Это доказывает, что репликоны, предназначенные для экспрессии пентамерного комплекса, действительно экспрессируют нужный антиген, а не потенциальный побочный продукт gH/gL.
[0286] VRP, инкапсулированные в LNP РНК и РНК в препаративных формах с CMF34 использовали для иммунизации мышей линии BALB/с путем внутримышечных инъекций в заднюю четырехглавую мышцу. Мышей иммунизировали три раза с промежутком в три недели, и перед каждой иммунизацией, а также через три недели после третьей и последней иммунизациями отбирали образцы сыворотки. Сыворотки исследовали анализом микронейтрализации, а также оценивали эффективность ответа нейтрализующих антител, вызванных вакцинацией. Титры выражены в виде 50% нейтрализующего титра.
[0287] Оценивали иммуногенность нескольких разных конфигураций бицистронной экспрессионной кассеты для растворимого комплекса gH/gL HCMV в VRP. На Фиг. 3 показано, что VRP, экспрессирующие прикрепленный к мембране комплекс gH/gL полной длины, вызывал выработку активных нейтрализующих антител при немного более высоких титрах по сравнению с растворимым комплексом (gHsol/gL), экспрессированным из аналогичной бицистронной экспрессионной кассеты. Изменение порядка генов, кодирующих gHsol и gL, или замена одного из субгеномных промоторов на участок IRES или FMDV 2А по существу не улучшает иммуногенность.
[0288] Чтобы убедиться в том, что бицистронные и пентацистронные репликоны, экспрессирующие комплексы gH/gL и пентамерные комплексы, могут вызвать продуцирование нейтрализующих антител в разных препаративных формах, хлопковых крыс иммунизировали бицистронными или пентацистронными репликонами, смешанными с CMF34. В таблице 12 показано, что репликоны в CMF34 вызвали сопоставимые титры нейтрализующих антител по сравнению с таким же репликоном, инкапсулированным в LNP.
|
|
B. Белки VZV
[0289] Нуклеиновые кислоты, кодирующие белки VZV, были клонированы в вектор VEE репликона для продуцирования моноцистронных репликонов, которые кодируют gB, gH, gL, gE и gI, и для продуцирования бицистронных репликонов, которые кодируют gH/gL или gE/gI. В бицистронных репликонах экспрессия каждой открытой рамки считывания VZV была обусловлена отдельным субгеномным промотором.
[0290] Для приготовления РНК репликона плазмиду, кодирующую репликон, линеаризовали расщеплением PmeI, и линеаризованную плазмиду экстрагировали смесью фенол/хлороформ/изоамиловый спирт, осаждали в смеси ацетат натрия/этанол и ресуспендировали в 20 мкл воды, свободной от РНКазы.
[0291] РНК получали in vitro транскрипцией 1 мкг линеаризованной ДНК, используя набор MEGAscript Т7 (AMBION # AM1333). 20 мкл реакционного продукта получали согласно инструкциям изготовителя без кэп аналога и инкубировали в течение 2 часов при 32°C. Добавляли ДНКазу (1 мкл) и смесь инкубировали в течение 30 мин при 32°C. Добавляли воду (30 мкл), свободную от РНКаз, и раствор ацетата аммония (30 мкл). Раствор перемешивали и охлаждали в течение по меньшей мере 30 мин при -20°C. Затем раствор центрифугировали при максимальной скорости в течение 25 мин при 4°C. Супернатант отбрасывали, а осадок промывали 70% этанолом и снова центрифугировали при максимальной скорости в течение 10 мин при 4°C. Осадок сушили на воздухе и ресуспендировали в 50 мкл свободной от РНКазы воды. Концентрацию РНК измеряли, качество проверяли, используя денатурирующий гель.
[0292] РНК кэпировали, используя систему для кэпирования m7G ScriptCap (Epicentre # SCCE0625). Объем реакционной смеси увеличивали путем объединения РНК и свободной от РНКазы воды. Затем РНК денатурировали в течение 5-10 мин при 65°C. Денатурированную РНК быстро переносили на лед, а затем добавляли реагенты в следующем порядке: буфер для кэпирования ScriptCap, 10 мМ GTP, 2 мМ свежеприготовленного SAM, ингибитор РНКазы ScriptGuard и фермент для кэпирования ScriptCap. Смесь инкубировали в течение 60 мин при 37°C. Реакцию останавливали добавлением свободной от РНКазы воды и 7,5 М LiCl, смесь перемешивали и хранили в течение по меньшей мере 30 мин при -20°C. Затем смесь центрифугировали при максимальной скорости в течение 25 мин при 4°C, осадок промывали 70% этанолом, снова центрифугировали при максимальной скорости в течение 10 мин при 4°C, и осадок сушили на воздухе. Осадок ресуспендировали в свободной от РНКазы воде. Измеряли концентрацию РНК, а качество проверяли, используя денатурирующий гель.
Трансфекция РНК
[0293] Клетки (BHK-V клетки) высевали на 6-луночные планшеты и доводили до 90-95% слияния во время трансфекции. Для каждой трансфекции 3 мкг РНК разводили в 50 мл среды OPTIMEM в первой пробирке. Во вторую пробирку, содержащую 50 мл среды OPTIMEM, добавляли липофектамин 2000. Первую и вторую пробирки объединяли и выдерживали в течение 20 мин при комнатной температуре. Культуральную среду в 6-луночных планшетах заменяли свежей средой, и в клетки вводили комплекс РНК-липофектамин и смешивали осторожным встряхиванием планшеты. Планшеты инкубировали в течение 24 часов при 37°C в СО2-инкубаторе.
[0294] Для иммунофлуоресценции трансфицированные клетки собирали и высевали в 96-луночный планшет, и выполняли внутриклеточное окрашивание, используя коммерчески доступные мышиные mAb (диапазон разведения 1:100-1:400). Клеточную массу фиксировали и пермеабилизировали растворами Citofix-Citoperm. Использовали второй реагент Alexa488, меченный козьими антителами против мышиных F(ab')2 (конечное разведение 1:400).
[0295] Экспрессию белков gE и gI VZV детектировали в клетках, трансфицированных моноцистронными конструкциями (gE или gI), и экспрессию как gE или gI детектировали в клетках, трансфицированных бицистронным конструктом gE/gI вестерн-блот анализом, используя коммерчески доступные мышиные антитела, 13B1 для gE и 8C4 для gI. Экспрессию белка gB VZV детектировали в клетках, трансфицированных моноцистронным конструктом, кодирующим gB, иммунофлуоресценцией, используя коммерчески доступные антитела 10G6. Экспрессию белкового комплекса gH/gL VZV детектировали иммунофлуоресценцией в клетках, трансфицированных моноцистронной конструкцией gH и моноцистронной конструкцией gL или бицистронной конструкцией gH/gL. Комплекс gH/gL детектировали, используя коммерчески доступное антитело SG3.
Изучение иммуногенности на мышах
[0296] Группы из 8 самок мышей BALB/с в возрасте 6-8 недель и весом около 20 г иммунизировали внутримышечно 7,0 или 1,0 мкг РНК репликона, находящегося в составе с CMF32 или LNP (RV01) на день 0, 21 и 42. Образцы крови отбирали из иммунизированных животных через 3 недели после второй иммунизации и через 3 недели после третьей иммунизации. Эти группы представлены в таблице 13.
|
[0297] Образцы сыворотки проверяли на наличие антител к gB внутриклеточным окрашиванием клеток MRC-5, трансфицированных репликоном на основе VZV. Клетки MRC-5 поддерживали в модифицированной по Дульбекко среде Игла с добавлением 10% эмбриональной телячьей сыворотки. Инокулят штамма Oka VZV (полученный из АТСС) использовали для инфицирования клеточной культуры MRC-5, и инфицированные целевые клетки использовали для последующего пассажа вируса. Соотношение между инфицированными и неинфицированными клетками составило 1:10. Через 30 часов после инфицирования клетки диспергировали в трипсине для посева в 96-луночный планшет для выполнения внутриклеточного окрашивания пулами мышиных сывороток (диапазон разбавления от 1:200 до 1:800), полученных после иммунизации. Коммерческие mAb использовали в качестве контроля для количественного определения уровня инфекции. Клеточную массу фиксировали и пермеабилизировали растворами Citofix-Citoperm. Использовали дополнительный реагент Alexa488, меченный козьими антителами против мышиных F(ab')2 (конечное разведение 1:400).
[0298] Коммерческие антитела к gB (10G6), gH (SG3) и gE (13B1 (SBA) и 8612 (Millipore)) использовали в качестве положительного контроля, и выполняли внутриклеточную окраску клеток MRC-5, инфицированных каждым из них. Иммунные сыворотки, полученные через 3 недели после третьей иммунизации 1 или 7 мкг РНК, находящейся в составе с CMF32, разводили в соотношениях 1/200, 1/400 и 1/800 и использовали для внутриклеточно окрашенных инфицированных клеток MRC-5. Результаты показаны на фиг.4 (исследование 1, группы 1, 5, 7, 9, 11, 13 и 15, препаративная форма CMF32).
Анализ нейтрализации
[0299] Каждую иммунизированную мышиную сыворотку серийно разводили каждый раз в два раза, начиная с разведения 1:20, в стандартной культуральной среде и добавляли к равным объемам суспензии VZV в присутствии комплемента морской свинки. После инкубации в течение 1 часа при 37°C добавляли линию человеческих эпителиальных клеток A549. Инфицированные клетки можно измерять через одну неделю культивирования путем подсчета под микроскопом образованных в культуре бляшек. По числу бляшек вычисляли % подавления для каждого разведения сыворотки. Для каждого образца строили зависимость подавления, выраженного в %, от логарифма коэффициента разбавления. Затем проводили прямую, аппроксимирующую соотношение между коэффициентом разбавления и % ингибирования. После этого определяли значение титра при 50% нейтрализации как коэффициент разбавления, где прямая пересекала значение, равное 50%-му подавлению.
[0300] В таблице 14 показано, что сыворотки, полученные от мышей, иммунизированных моноцистронной конструкцией gE, бицистронной конструкцией gE/gI и бицистронной конструкцией gH/gL, содержали устойчивые титры нейтрализующих антител.
|
Пример 8: Растворимость жирных кислот в сквалене
[0301] В этом примере изучали представленную в таблице 15 растворимость различных жирных кислот в сквалене. Жирные кислоты в указанных количествах (40, 20, 10 или 5 мг/мл) смешивали со скваленом при 60°C. В таблице 15 (√) означает, что жирные кислоты растворяются в сквалене при определенной концентрации; "x" означает, что жирные кислоты не растворяются в сквалене при определенной концентрации, и "-" означает, что растворимость жирных кислот при определенной концентрации не исследовали (поскольку жирные кислоты являются растворимыми при более высокой концентрации). Затем жирные кислоты растворяли в сквалене, и растворы выдерживали при 4°C в течение ночи. Столбец, обозначенный "4°C в течение ночи" показывает растворимость растворов, в которых каждая жирная кислота находилась при самой высокой для нее концентрации. Например, олеиновая кислота была растворимой в сквалене при 40 мг/мл и оставалась растворимой в сквалене после ее выдерживания при 4°C в течение ночи.
|
|
|
Последовательности
[0302] Нуклеотидная последовательность ДНК, кодирующая РНК vA317, которая кодирует антиген RSV-F (SEQ ID NO:1).
[0303] Нуклеотидная последовательность ДНК, кодирующая РНК vA142 (SEQ ID NO:2).
[0304] Нуклеотидная последовательность ДНК, кодирующая РНК vA375 (SEQ ID NO:3).
[0305] Вектор A526: SGP-gH-SGP-gL-SGP-UL128-2A-UL130-2Amod-UL131 (SEQ ID NO:4).
[0306] Вектор A527: SGP-gH-SGP-gL-SGP-UL128-EMCV-UL130-EV71-UL131(SEQIDNO:5).
[0307] Вектор A531: SGP-gHsol-SGP-gL (SEQ ID NO:6).
[0308] Вектор A532: SGP-gHsol-2A-gL (SEQ ID NO:7).
[0309] Вектор A533: SGP-gHsol-EV71-gL (SEQ ID NO:8).
[0310] Вектор A534: SGP-gL-EV71-gH (SEQ ID NO:9).
[0311] Вектор A535: SGP-342-EV71-gHsol-2A-gL (SEQ ID NO:10).
[0312] Вектор A536: SGP-342-EV71-gHsol-EMCV-gL (SEQ ID NO:11).
[0313] Вектор A537: SGP-342-EV71-gL-EMCV-gHsol (SEQ ID NO:12).
[0314] Вектор A554: SGP-gH-SGP-gL-SGP-UL128-SGP-UL130-SGP-UL131 (SEQ ID NO:13).
[0315] Вектор A555: SGP-gHsol-SGP-gL-SGP-UL128-SGP-UL130-SGP-UL131(SEQ ID NO:14).
[0316] Вектор A556: SGP-gHsol6His-SGP-gL-SGP-UL128-SGP-UL130-SGP-UL131(SEQ ID NO:15).
[0317] VZV gB (SEQ ID NO:16).
[0318] VZV gH (SEQ ID NO:17).
[0319] VZV gL (SEQ ID NO:18).
[0320] VZV gI (SEQ ID NO:19).
[0321] VZV gE (SEQ ID NO:20).
[0322] VZV VEERep.SGPgB (SEQ ID NO:21).
[0323] VZV VEERep.SGPgH (SEQ ID NO:22).
[0324] VZV VEERep.SGPgL (SEQ ID NO:23).
[0325] VZV VEERep.SGPgH-SGPgL (SEQ ID NO:24).
[0326] VZV VEERep.SGPgE (SEQ ID NO:25).
[0327] VZV VEERep.SGPgI (SEQ ID NO:26).
[0328] VZV VEErep.SGPgE-SGPgI (SEQ ID NO:27).
[0329] Описание станет более понятным в свете данных, приведенных в документах, ссылки на которые приведены в описании. Приведенные в описании варианты осуществления следует рассматривать как иллюстрацию вариантов осуществления изобретения, которую не следует истолковывать как ограничение объема изобретения. Для специалиста в данной области ясно, что в объем изобретения входят многие другие варианты осуществления. Все публикации и патенты, ссылки на которые приведены в описании, включены в описание во всей их полноте в виде ссылки. Там, где материал, включенный в виде ссылки, противоречит или не соответствует описанию, описание следует рассматривать как отменяющее любой такой материал. Цитирование в данном описании любых ссылок не является признанием того, что такие ссылки являются предшествующим уровнем техники для настоящего изобретения.
[0330] Специалистам в данной области известно, или они могут определить с использованием не более чем общепринятых экспериментов, множество эквивалентов конкретных вариантов осуществления по изобретению, описанных в настоящем описании. Такие эквиваленты охватываются следующими вариантами осуществления.