Результат интеллектуальной деятельности: КОМБИНАЦИИ, СОДЕРЖАЩИЕ МОДУЛЯТОРЫ mGluR, ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА
Вид РИД
Изобретение
Настоящее изобретение относится к фармацевтической комбинации, включающей соединения, являющиеся модуляторами метаботропных глутаматных рецепторов (модуляторы mGluR), включая антагонисты метаботропных глутаматных рецепторов (антагонисты mGluR) и по крайней мере одну L-допу, модулятор допамина, например, агонист допамина, ингибитор допа-декарбоксилазы или ингибитор катехол-O-метилтрансферазы.
Прежде всего, настоящее изобретение относится к новым комбинациям, включающим антагонисты метаботропных глутаматных рецепторов типа-5 (антагонисты mGluR5).
В заявках WO 2005/079802, WO 2003/047581, WO 2004/000316, WO 2005/044265, WO 2005/044266, WO 2005/044267, WO 2006/114262 и WO 2007/071358 описаны антагонисты mGluR5 и их применение в качестве фармацевтических препаратов.
Неожиданно было установлено, что комбинация, включающая модуляторы метаботропных глутаматных рецепторов, например, описанные ниже, и по крайней мере одно соединение, выбранное из группы, включающей L-допу, агонист допамина, ингибитор допа-декарбоксилазы или ингибитор катехол-O-метилтрансферазы, характеризуется благоприятным действием и ее можно использовать для лечения нарушений или состояний/нарушений, которые поддаются лечению за счет модуляции метаботропного глутаматного рецептора.
Таким образом, настоящее изобретение относится к комбинациям, таким как комбинированные препарат или фармацевтическая композиция, соответственно, включающим модулятор метаботропного глутаматного рецептора или его фармацевтически приемлемую соль и по крайней мере одно из следующих соединений
1) L-допа или
2) ингибитор допа-декарбоксилазы или
3) ингибитор катехол-O-метилтрансферазы
4) агонист допамина
или в каждом случае их фармацевтически приемлемую соль. Ингибитором допа-декарбоксилазы является, например, карбидопа или бензеразид.
Ингибиотором катехол-O-метилтрансферазы является, например, толкапон или энтакапон.
Агонисты допамина включают, например, бромкриптин, перголид, прамипексол, ропинирол, каберголин, апоморфин или лизурид.
Предпочтительно комбинация по настоящему изобретению представляет собой фармацевтическую композицию или комбинированный фармацевтический препарат.
В указанной фармацевтической композиции компоненты, т.е. модулятор метаботропного глютаматного рецептора или его фармацевтически приемлемую соль и по крайней мере одно из следующих соединений:
1) L-допа или
2) ингибитор допа-декарбоксилазы или
3) ингибитор катехол-O-метилтрансферазы
4) агонист допамина,
можно вводить одновременно, последовательно или раздельно в виде одной комбинированной стандартной лекарственной формы или в виде двух отдельных стандартных лекарственных форм. Стандартная лекарственная форма может также обозначать фиксированную комбинацию.
Термин «комбинации», использованный в данном контексте, обозначает одно или более соединений, которые вводят одновременно, последовательно или раздельно в виде одной стандартной лекарственной формы или двух отдельных стандартных лекарственных форм.
Лекарственные формы можно вводить одновременно, частично одновременно, раздельно или последовательно. Лекарственные формы, содержащие комбинации, не обязательно содержатся в составе одной лекарственной формы и могут представлять собой одну из следующих форм:
Энтеральную: для перорального (капсулы, таблетки, раствор), ректального введения (суппозиторий),
Парентальную: для внутривенных инъекций, подкожных инъекций, внутримышечных инъекций, внутрибрюшинных инъекций, интрамаммарных инъекций,
Респираторную: для ингаляции, интраназального, внутритрахеального введения,
Местную: для введения на слизистую оболочку, на кожу.
Кроме того, профиль высвобождения лекарственного средства может отличаться, например, один или более компонентов комбинации могут представлять собой форму с пролонгированным высвобождением.
Недавно было установлено, что соединения, характеризующиеся моделирующей активностью в отношении mGluR, прежде всего, антагонистической активностью, можно использовать для лечения болезни Паркинсона и нарушений, связанных с болезнью Паркинсона.
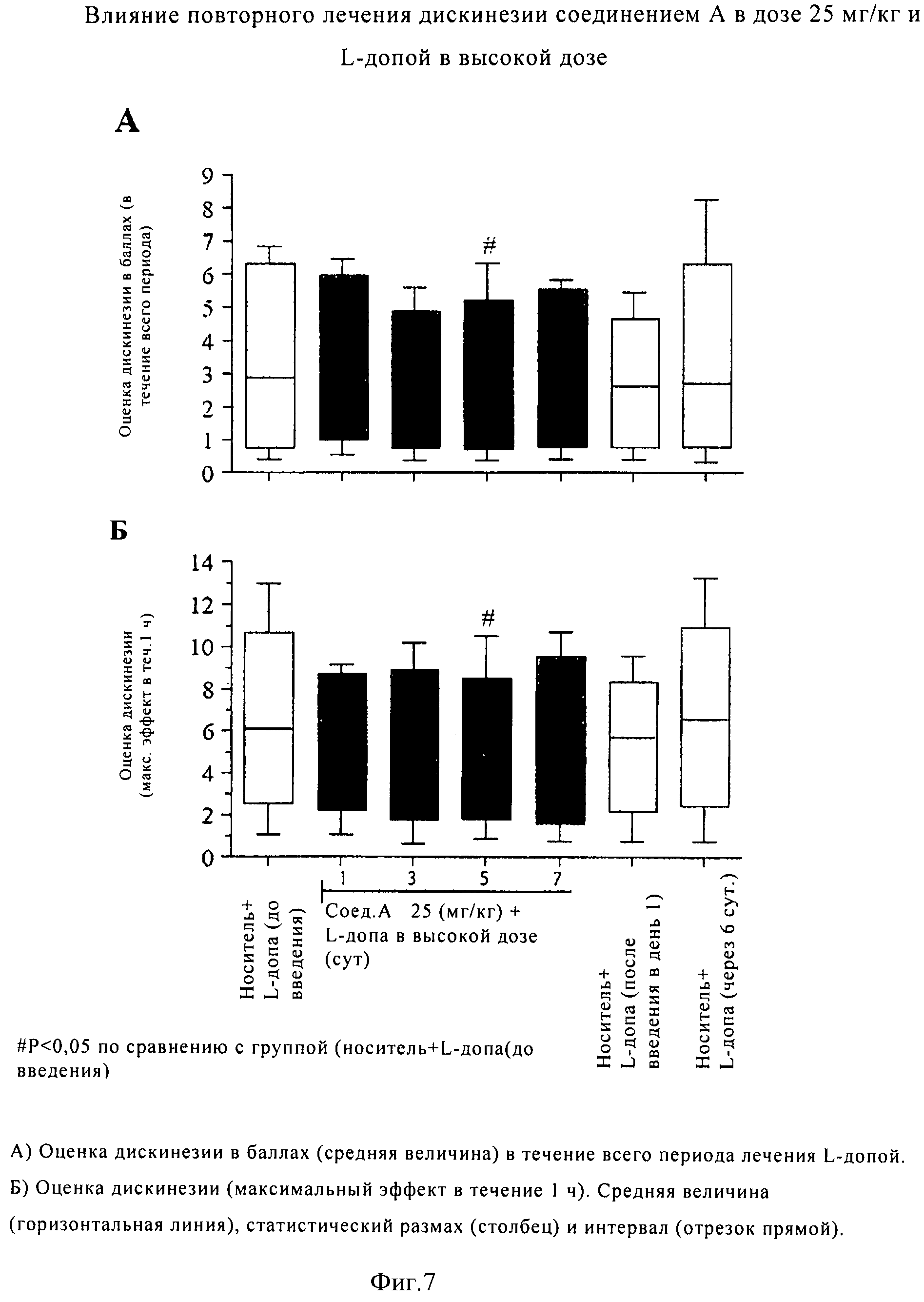
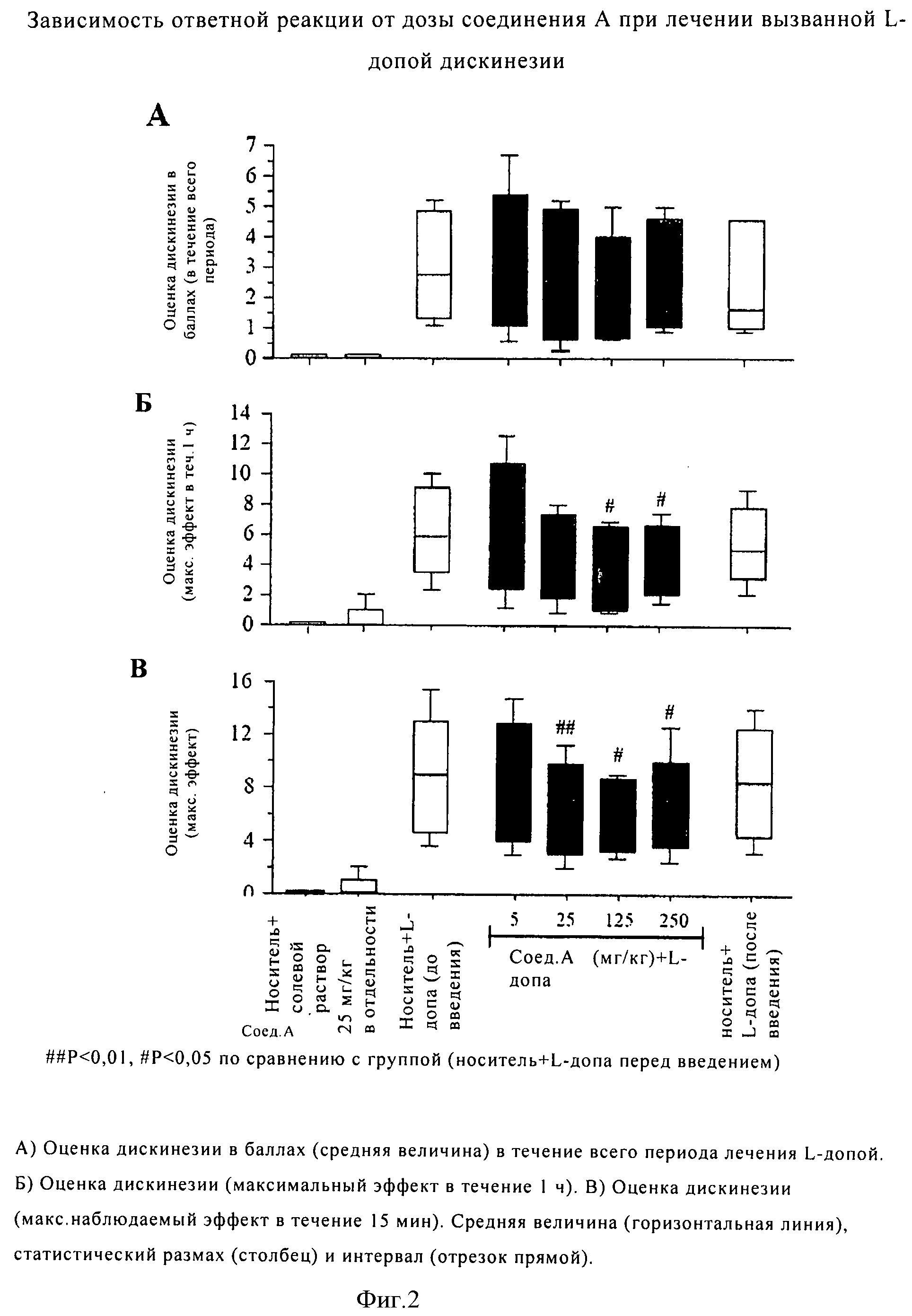
Прежде всего было установлено, что модуляторы mGluR можно использовать для лечения дискинезии, нарушения, связанного с болезнью Паркинсона и с лечением указанного заболевания. Прежде всего, было установлено, что модуляторы mGluR5, например, антагонисты mGluRS, можно использовать для лечения болезни Паркинсона и связанных с ней нарушений, например, дискинезии Паркинсона, например, леводопа-(L-допа)индуцированной дискинезии при болезни Паркинсона.
Неожиданно было установлено, что комбинация, содержащая модуляторы метаботропных глютаматных рецепторов, например, описанные ниже, и по крайней мере одно соединение, выбранное из группы, включающей L-допу, агонист допамина, ингибитор допа-декарбоксилазы или ингибитор катехол-O-метилтрансферазы, оказывает благоприятное действие и ее можно использовать для лечения нарушений или состояний/нарушений, которые поддаются лечению с использованием модулятора метаботропного глютаматного рецептора, например, таких как болезнь Паркинсона и/или связанные с ней нарушения.
Соответственно, первый объект настоящего изобретения относится к применению модулятора mGluR в комбинации со вторым активным агентом для лечения (терапевтического или профилактического), профилактики и/или замедления прогрессирования болезни Паркинсона и/или связанных с ней нарушений.
В одном объекте настоящего изобретения предлагается применение модулятора mGluR, например, антагониста, в комбинации со вторым агентом для лечения, профилактики и/или замедления прогрессирования дискинезии Паркинсона, например, леводопа(L-допа)-индуцированной дискинезии при болезни Паркинсона.
В другом объекте настоящего изобретения используют специфическую комбинацию. Указанная комбинация включает:
агент по настоящему изобретению, прежде всего, модулятор mGluR5, и L-допу,
по крайней мере один активный агент, выбранный из группы, включающей карбидопу, бензеразид толкапона или энтакапона, бромкриптин, перголид, прамипексол, ропинирол, каберголин, апоморфин или лизурид.
В еще одном объекте настоящего изобретения используют специфическую комбинацию. Указанная комбинация включает:
агент по настоящему изобретению, прежде всего, модулятор mGluR5, и
по крайней мере один активный агент, выбранный из группы, включающей L-допу, карбидопу, бензеразид толкапона или энтакапона, бромкриптин, перголид, прамипексол, ропинирол, каберголин, апоморфин или лизурид.
Еще один объект настоящего изобретения относится к способу лечения, профилактики или замедления прогрессирования болезни Паркинсона и/или нарушений, связанных с болезнью Паркинсона, у субъекта, нуждающегося в таком лечении, и указанный способ заключается во введении указанному субъекту терапевтически эффективного количества mGluR, например, модулятора mGluR5, в комбинации со вторым агентом, например, по крайней мере одним соединением, выбранным из группы, включающей L-допу, агонист допамина, ингибитор допа-декарбоксилазы или ингибитор катехол-O-метилтрансферазы.
В одном объекте способ используют для лечения, профилактики и/или замедления прогрессирования дискинезии при болезни Паркинсона, например, леводопа-(L-допа)-индуцированной дискинезии при болезни Паркинсона.
Другой объект настоящего изобретения относится к фармацевтической композиции, включающей mGluR, например, модулятор mGluR5, для лечения, профилактики или замедления прогрессирования болезни Паркинсона и/или нарушений, связанных с болезнью Паркинсона, в комбинации со вторым агентом, например, по крайней мере одним соединением, выбранным из группы, включающей L-допу, ингибитор допа-декарбоксилазы или ингибитор катехол-О-метилтрансферазы. В одном варианте композицию используют для лечения, профилактики или замедления прогрессирования дискинезии при болезни Паркинсона, например, леводопа-(L-допа)-индуцированной дискинезии при болезни Паркинсона. В другом объекте фармацевтическую композицию используют для лечения, профилактики или замедления прогрессирования болезни Паркинсона.
В другом объекте настоящего изобретения предлагается применение модулятора mGluR, например, mGluR5, в комбинации со вторым агентом, например, по крайней мере с одним соединением, выбранным из группы, включающей L-допу, ингибитор допа-декарбоксилазы или ингибитор катехол-О-метилтрансферазы, для получения лекарственного средства, предназначенного для лечения, профилактики или замедления прогрессирования болезни Паркинсона и/или нарушений, связанных с болезнью Паркинсона. В одном объекте лекарственное средство предназначено для лечения, профилактики или замедления прогрессирования дискинезии при болезни Паркинсона, например, леводопа-(L-допа)-индуцированной дискинезии при болезни Паркинсона (PD-LID).
Модулятор mGluR может обозначать модулятор mGluR5. В некоторых вариантах модулятор mGluR обозначает антагонист mGluR, например, антагонист mGluR5.
Особый интерес представляет леводопа-(L-допа)-индуцированная дискинезия при болезни Паркинсона.
Агенты по настоящему изобретению, прежде всего, модуляторы рецепторов mGluR5, можно использовать для лечения, профилактики или замедления прогрессирования дискинезии Паркинсона, например, леводопа-(L-допа)-индуцированной дискинезии при болезни Паркинсона. Дискинезия Паркинсона часто, хотя и не во всех случаях, развивается в результате побочного эффекта при лечении болезни Паркинсона леводопой (L-допой), предшественником допамина. Симптомы дискинезии Паркинсона включают двигательную недостаточность, например, наличие медленных и непроизвольных неконтролируемых движений, тремора, скованности и проблем при ходьбе. У пациентов, которым вводили L-допу, часто наблюдается ослабление симптомов болезни Паркинсона, однако у них наблюдается усиливающиеся проблемы сохранения положения стоя или даже положения сидя. После длительного использования L-допы у большинства пациентов развивается дискинезия.
Дискинезия может развиваться в любой момент во время курса лечения с использованием L-допы. В одном варианте модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности, можно использовать для лечения дискинезии, развивающейся в момент максимальной концентрации L-допы в плазме у пациента. В другом варианте модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности, можно использовать для лечения дискинезии, развивающейся при увеличении или уменьшении концентрации L-допы в плазме пациента (двухфазная дискинезия).
Дискинезия также может развиваться у пациентов, страдающих болезнью Паркинсона, которым не вводили L-допу. В одном варианте соединения по настоящему изобретению предназначены для лечения не-L-допа1 индуцированной дискинезии при болезни Паркинсона.
Лечение агентом по настоящему изобретению в комбинации со вторым агентом, например, по крайней мере с одним соединением, выбранным из группы, включающей L-допу, ингибитор допа-декарбоксилазы или ингибитор катехол-O-метилтрансферазы, может включать снижение интенсивности симптомов, связанных с дискинезией при болезни Паркинсона, включая, например, но не ограничиваясь только ими, снижение интенсивности непроизвольных движений, снижение числа непроизвольных движений, повышение способности выполнять обычные действия, улучшение способности хождения, увеличение временных интервалов между эпизодами дискинезии.
В случае профилактического лечения, агенты по настоящему изобретению, прежде всего агенты, перечисленные в списке P, можно использовать для замедления или профилактики развития дискинезии при болезни Паркинсона.
В настоящем описании, если не указано иное, использованы следующие определения.
Термин «алкил» обобозначает алкильную группу с прямой или разветвленной цепью, предпочтительно C1-C12алкил с прямой или разветвленной цепью, прежде всего C1-C6алкил с прямой или разветвленной цепью, например, метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, прежде всего, предпочтительно метил, этил, н-пропил и изопропил.
Термин «алкандиил» обозначает алкандиильную группу с прямой или разветвленной цепью, присоединенную к молекуле через различные атомы углерода, предпочтительно C1-C12алкандиил с прямой или разветвленной цепью, более предпочтительно C1-C6алкандиил с прямой или разветвленной цепью, например, метандиил (-СН2-), 1,2-этандиил (-СН2-СН2-), 1,1-этандиил ((-СН(CH3)-), 1,1-, 1,2-, 1,3-пропандиил и 1,1-, 1,2-, 1,3-, 1,4-бутандиил, еще более предпочтительно метандиил, 1,1-этандиил, 1,2-этандиил, 1,3-пропандиил или 1,4-бутандиил.
Каждый алкил в составе группы «алкокси», «алкоксиалкил», «алкоксикарбонил», «алкоксикарбонилалкил» и «галогеналкил» имеет значение, определенное для «алкила».
Термин «алкенил» обозначает алкенильную группу с прямой или разветвленной цепью, предпочтительно C2-C6алкенил, например, винил, аллил, 1-пропенил, изопропенил, 2-бутенил, 2-пентенил, 2-гексенил и т.п., предпочтительно C2-C4алкенил.
Термин «алкендиил» обозначает алкендиильную группу с прямой или разветвленной цепью, присоединенную к молекуле через два различных атома углерода, предпочтительно C2-C6алкендиил с прямой или разветвленной цепью, например, -СН=СН-, -СН=С(СН3)-, -СН=СН-СН2-, -C(СН3)=СН-СН2-, -СН=С(СН3)-СН2-, -СН=СН-С(СН3)H-, -СН=СН-СН=СН-, -C(СН3)=СН-СН=СН-, -СН=С(СН3)-СН=СН-, прежде всего предпочтительно -CH=CXH-CH2-, -СН-СН-СН=СН-.
Термин «алкинил» обозначает алкинильную группу с прямой или разветвленной цепью, предпочтительно C2-C6алкинил, например, этенил, пропаргил, 1-пропинил, изопропенил, 1- (2- или 3)-бутинил, 1- (2- или 3-)пентинил, 1- (2- или 3-)гексенил и т.п., предпочтительно C2-C4алкинил, еще более предпочтительно этинил.
Термин «арил» обозначает ароматическую углеводородную группу, предпочтительно ароматическую углеводородную группу C6-C10, например, фенил, нафтил, прежде всего, фенил.
Термин «аралкил» обозначает «арил», присоединенный к «алкильной» группе (как определено выше) и обозначает, например, бензил, α-метилбензил, 2-фенилэтил, α,α-диметилбензил, прежде всего, бензил.
Термин «гетероцикл» обозначает насыщенную, частично насыщенную или ароматическую кольцевую систему, содержащую по крайней мере один гетероатом. Предпочтительно, гетероциклы содержат от 3 до 11 атомов в цикле, из которых 1-3 атома являются гетероатомами. Гетероциклы представляют собой моноциклическую систему, бициклическую или трициклическую системы, предпочтительно оноиклическую систему или бензоконденсированную кольцевую систему. Бициклическая или трициклическая кольцевая системы образуются при конденсировании двух или более колец, через мостиковый атом, например, атом кислорода, серы, азота или через мостиковую группу, например, алкандиил или алкендиил. Гетероцикл может содержать один или более заместителей, выбранных из группы, включающей оксогруппу (=0), галоген, нитрогруппу, цианогруппу, алкил, алкандиил, алкендиил, алкоксигруппу, алкоксиалкил, алкоксикарбонил, алкоксикарбонилалкил, галогеналкил, арил, арилоксигруппу и арилалкил. Примеры гетероциклических остатков включают пиррол, пирролин, пирролидин, пиразол, пиразолин, пиразолидин, имидазол, имидазолин, имидазолидин, триазол, триазолин, триазолидин, тетразол, фуран, дигидрофуран, тетрагидрофуран, фуразан (оксадиазол), диоксолан, тиофен, дигидротиофен, тетрагидротиофен, оксазол, оксазолин, оксазолидин, изоксазол, изоксазолин, изоксазолидин, тиазол, тиазолин, тиазолидин, изотиазол, изотиазолин, изотиазолидин, тиадиазол, тиадиазолин, тиадиазолидин, пиридин, пиперидин, пиридазин, пиразин, пиперазин, триазин, пиран, тетрагидропиран, тиопиран, тетрагидротиопиран, оксазин, тиазин, диоксин, морфолин, пурин, птерин и соответствующие бензо-аннелированные гетероциклы гетероциклы, например, индол, изоиндол, кумарин, кумаронцинолин, изохинолин, циннолин и т.п.
Термин «гетероатом» обозначает атом, в отличие от атома углерода и водорода, предпочтительно атом азота (N), кислорода (О) или серы (S).
Термин «галоген» обозначает фтор, хлор, бром или иод, предпочтительно фтор, хлор или бром, еще более предпочтительно хлор.
В настоящей заявке описаны различные соединения, характеризующиеся модулирующей активностью в отношении mGluR, прежде всего mGluR5. Если описание относится к соединениям, агентам или активным ингредиентам по настоящему изобретению, то, если не указано иное, они в основном обозначают соединение, характеризующееся модулирующей активностью в отношении mGluR. В вариантах осуществления настоящего изобретения модуляторы mGluR являются антагонистами mGluR5. Если описание относится к антагонистам mGluR, то они в основном обозначают соединения, которые взаимодействуют с mGluR и ингибируют действие природного лиганда mGluR, например, в результате не стимулируется ответный путь экспрессирующих mGluR клеток.
В одном варианте модулятор mGluR обозначает антагонист mGluR5.
Модуляторы mGluR, описанные в данном контексте, могут находиться в свободном состоянии или в виде кислотно-аддитивной соли. В настоящей заявке, если не указано иное, термин «модуляторы mGluR, как описано в данном контексте» включает соединения в любой форме, например, в форме свободного основания или в форме кислотно-аддитивной соли. В указанное определение также включены соли, которые не пригодны для применения в фармацевтике, но которые можно использовать, например, для выделения или очистки модуляторов mGluR в свободной форме, как описано в данном контексте, такие как пикраты или перхлораты. Для терапевтического применения используют только фармацевтически приемлемые соли или соединения в свободной форме (если их можно перерабатывать в фармацевтические композиции), которые являются предпочтительными.
Следует понимать, что любое обсуждение способов или ссылки на активные ингредиенты также включают фармацевтически приемлемые соли. Если указанные активные ингредиенты содержат, например, по крайней мере один основный центр, то они могут образовывать кислотно-аддитивные соли. Соответствующие кислотно-аддитивные соли при необходимости также можно получать при наличии дополнительного основного центра. Активные ингредиенты, содержащие кислотную группу (например, COOH), также могут образовывать соли с основаниями. Активный ингредиент или его фармацевтически приемлемую соль можно также использовать в форме гидрата или они могут включать другие растворители, используемые для кристаллизации. Примеры модуляторов mGluR5, например, антагонистов, и их получение известны специалистам, и описаны, например, в заявках WO 03/047581 и WO 2006/114262, включенных в настоящее описание в качестве ссылок.
В связи с наличием асимметрического атома(ов) углерода, которые могут присутствовать в модуляторах mGluR, описанных в данном контексте, и их солях, соединения могут существовать в оптически активной форме или в форме смеси оптических изомеров, например, в форме рацемических смесей или смесей диастереомеров. Все оптические изомеры и их смеси, включая рацемические смеси, включены в объем настоящего изобретения.
В одном варианте модулятор mGluR представляет собой соединение формулы (I)
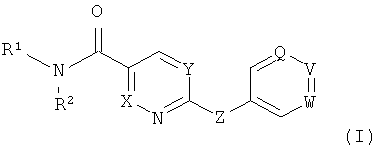
где
R1 обозначает необязательно замещенный алкил или необязательно замещенный бензил, а
R2 обозначает водород (H), необязательно замещенный алкил или необязательно замещенный бензил, или,
R1 и R2 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенный гетероцикл, содержащий менее 14 атомов в цикле,
R3 обозначает галоген, алкил, алкоксигруппу, алкиламиногруппу или диалкиламиногруппу,
R4 обозначает гидроксигруппу (OH), галоген, алкил или алкоксигруппу,
Q обозначает СН, CR4 или N,
V обозначает СН, CR4 или N,
W обозначает СН, CR4 или N,
X обозначает СН или N,
Y обозначает СН, CR3 или N, и
Z обозначает СН2, NH или O,
при условии, что Q, V и W одновременно не обозначают N, в форме свободного основания или кислотно-аддитивной соли.
В другом варианте модулятор mGluR обозначает соединение формулы (II), причем соединение формулы (II) обозначает соединение формулы (I), где по крайней мере один из заместителей Q, V и W обозначает N, в форме свободного основания или кислотно-аддитивной соли.
В еще одном варианте осуществления настоящего изобретения модулятор mGluR обозначает соединение формулы (III), причем соединение формулы (III) обозначает соединение формулы (II), где заместитель Y обозначает CR3; в форме свободного основания или кислотно-аддитивной соли.
Предпочтительные заместители, предпочтительные числовые значения или предпочтительные значения радикалов, содержащихся в формулах (I), (II) и (III), и соответствующих промежуточных соединениях, определены ниже.
X предпочтительно обозначает СН.
Y предпочтительно обозначает СН или CR3, где R3 предпочтительно обозначает галоген, прежде всего, предпочтительно хлор. Z предпочтительно обозначает NH.
R3 предпочтительно обозначает фтор, хлор, C1-C4алкил, например, метил.
R3 предпочтительно обозначает хлор.
R1 и R2 предпочтительно вместе с атомом азота, к которому они присоединены, образуют незамещенный или замещенный гетероцикл, содержащий 3-11 атомов в цикле и 1-4 гетероатома, которые выбраны из группы, включающей N, O или S, а заместители выбраны из группы, включающей оксогруппу (=O), гидроксигруппу, галоген, аминогруппу, нитрогруппу, цианогруппу, C1-C4алкил, C1-C4алкоксигруппу, C1-C4алкоксиалкил, C1-C4алкоксикарбонил, C1-C4алкоксикарбонилалкил, C1-C4галогеналкил, C6-C10арил, галоген(C6-C10)арил, C6-C10арилоксигруппу и C6-C10арил(C1-C4)алкил.
R1 и R2 вместе с атомом азота, к которому они присоединены, образуют незамещенный, содержащий один или два заместителя гетероцикл, содержащий 5-9 атомов в цикле и 1-3 гетероатома, выбранных из группы, включающей N и O, а заместители выбраны из группы, включающей галоген и C1-C4алкил.
R1 и R2 предпочтительно вместе с атомом азота, к которому они присоединены, образуют незамещенный или содержащий один заместитель гетероцикл, выбранный из группы, включающей 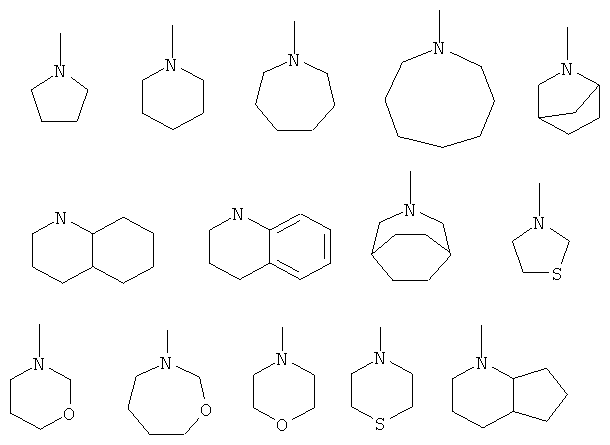
и заместители выбраны из группы, включающей фтор, хлор, метил, этил, пропил, бутил, трифторметил, фторпропил и дифторпропил.
R1 R2 предпочтительно независимо друг от друга обозначают C1-C4алкил или бензил, необязательно замещенный C1-C4алкоксигруппой или галогеном.
Приведенные выше общие или предпочтительные значения радикалов относятся как к конечным продуктам формул (I), (II) и (III), так и, соответственно, к исходным или промежуточным соединениям, используемым в каждом случае для синтеза. Указанные радикалы можно при необходимости комбинировать друг с другом, включая комбинации приведенных предпочтительных значений. Кроме того, отдельные определения могут не использоваться.
Предпочтительными согласно настоящему изобретению являются соединения формул (I), (II) и (III), содержащие комбинацию значений, указанных выше в качестве предпочтительных.
Прежде всего, предпочтительными согласно настоящему изобретению являются соединения формул (I), (II) и (III), содержащие комбинацию значений, указанных выше в качестве более предпочтительных.
Наиболее предпочтительными согласно настоящему изобретению являются соединения формулы (I), содержащие комбинацию значений, указанных выше в качестве наиболее предпочтительных.
Предпочтительными являются соединения формул (I), (II) и (III), где R обозначает незамещенный или замещенный гетероцикл.
Прежде всего, предпочтительными являются соединения формул (IIa-IIee), приведенные ниже:
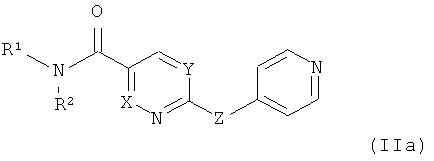
где заместители определены в данном описании,
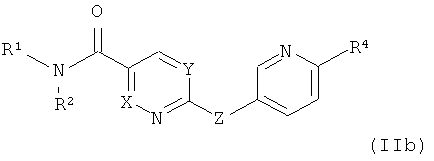
где заместители определены в данном описании,
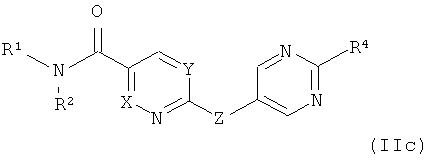
где заместители определены в данном контексте,
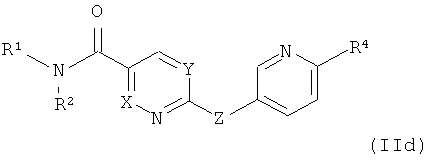
где R4 обозначает C1-C4алкил, предпочтительно метил, а другие заместители определены в данном контексте,
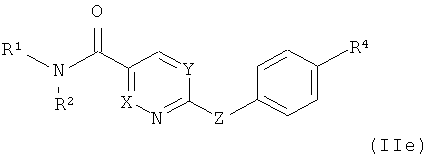
где R4 обозначает галоген, предпочтительно хлор, а другие заместители
определены в данном контексте.
Кроме того, предпочтительными соединениями по настоящему изобретению являются соединения формул (IIIa-IIIe), приведенные ниже:
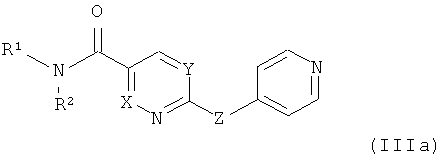
где все заместители определены в данном описании,
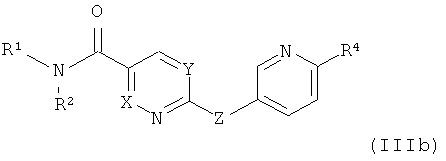
где заместители определены в данном описании,
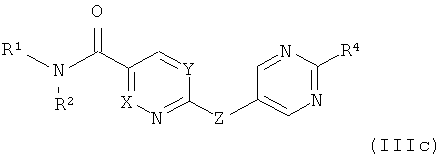
где заместители определены в данном описании,
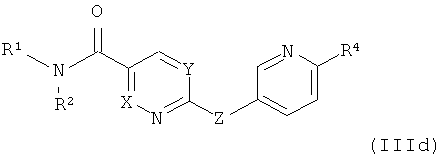
где R4 обозначает C1-C4алкил, предпочтительно метил, а другие заместители определены в данном описании,
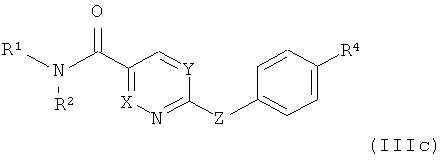
где R4 обозначает галоген, предпочтительно хлор, а другие заместители
определены в данном контексте.
Прежде всего, соединения формул (I), (II) и (III) включают соединения, описанные в примерах, приведенных в настоящем описании.
В другом варианте модулятор mGluR обозначает соединение формулы (IV):
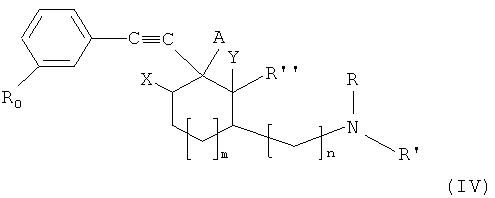
где
m равно 0 или 1,
n равно 0 или 1, и
A обозначает гидроксигруппу,
X обозначает водород,
Y обозначает водород, или
A образует простую связь с X или Y,
Ro обозначает водород, C1-C4алкил, C1-C4алкоксигруппу, трифторметил, галоген, цианогруппу, нитрогруппу, -COOR1, где R1 обозначает C1-C4алкил или -COR2, где R2 обозначает водород или C1-C4алкил, и
R обозначает -COR3, -COOR3, -CONR4R5 или -SO2R6, где R3 обозначает C1-C4алкил, C3-C7циклоалкил или необязательно замещенный фенил, 2-пиридил или 2-тиенил, R4 и R5 независимо обозначают водород или C1-C4алкил, a R6 обозначает C1-C4алкил, C3-C7Диклоалкил или необязательно замещенный фенил,
R' обозначает водород или C1-C4алкил, и
R'' обозначает водород или C1-C4алкил или
R' и R'' вместе образуют группу -СН2-(СН2)m-,
где m равно 0, 1 или 2, в каждом случае один из индексов n и m отличается от 0,
при условии, что R0 не обозначает водород, трифторметил и метоксигруппу, если n равен 0, A обозначает гидроксигруппу, X и Y оба обозначают водород, R обозначает COOEt, a R' и R'' вместе образуют группу -(СН2)2-,
в форме свободного основания или кислотно-аддитивной соли.
Примеры соединений формулы (IV) включают:
метиловый эфир (-)-(3aR,4S,7aR)-4-гидрокси-4-мета-толилэтинилоктагидроиндол-1-карбоновой кислоты,
этиловый эфир (-)-(3aR,4S,7aR)-4-гидрокси-4-мета-толилэтинилоктагидроиндол-1-карбоновой кислоты,
(-)-(3aR,4S,7aR)-фуран-2-ил(4-гидрокси-4-мета-толилэтинилоктагидроиндол-1-ил)метанон,
этиловый эфир (±)-(3aRS,4SR,7aRS)-4-(3-хлорфенилэтинил)-4-гидроксиоктагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4SR,7aRS)-4-(3-фторфенилэтинил)-4-гидроксиоктагидроиндол-1-карбоновой кислоты,
(S)-тетрагидрофуран-3-иловый эфир (3aRS,4SR,7aRS)-4-гидрокси-4-фенилэтинилоктагидроиндол-1-карбоновой кислоты,
(R)-тетрагидрофуран-3-иловый эфир (3aRS,4SR,7aRS)-4-гидрокси-4-фенилэтинилоктагидроиндол-1-карбоновой кислоты,
(S)-тетрагидрофуран-3-иловый эфир (3aRS,4SR,7aRS)-4-гидрокси-4-(3-хлорфенилэтинил)октагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4SR,7aRS)-4-гидрокси-4-мета-толилэтинилоктагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4SR,7aRS)-4-(4-фторфенилэтинил)-4-гидроксиоктагидроиндол-1-карбоновой кислоты,
(±)-(3aRS,4SR,7aRS)-4-(3-хлорфенилэтинилд)-4-гидрокси-1-метансульфонилоктагидроиндол,
этиловый эфир (±)-(3aRS,7aRS)-4-фенилэтинил-2,3,3a,6,7,7a-гексагидроиндол-1-карбоновой кислоты и
этиловый эфир (±)(RS)-4-фенилэтинил-2,3,5,6,7,7a-гексагидроиндол-1-карбоновой кислоты,
(±)-(3RS,7aRS)-2,2,2-трифтор-1-(4-фенилэтинил-2,3,За,6,7,7a-гексагидроиндол-1-ил)этанон,
этиловый эфир (±)-(RS)-4-мета-толилэтинил-2,3,5,6,7,7а-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3RS,7aRS)-4-мета-толилэтинил-2,3,3a,6,7,7a-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3RS,7aRS)-4-(4-хлорфенилэтинил)-2,3,3a,6,7,7a-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3RS,7aRS)-4-(2-фторфенилэтинил)-2,3,3a,6,7,7a-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3RS,7aRS)-4-(3-фторфенилэтинил)-2,3,3a,6,7,7a-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(RS)-4-(3-фторфенилэтинил)-2,3,5,6,7,7а-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3RS,7aRS)-4-(3-метоксифенилэтинил)-2,3,3a,6,7,7a-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(RS)-4-(3-метоксифенилэтинил)-2,3,5,6,7,7а-гексагидроиндол-1-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-фенилэтинилоктагидроизоиндол-2-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-мета-толилэтинилоктагидроизоиндол-2-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-пара-толилэтинилоктагидроизоиндол-2-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4RS,7aSR)-4-(3-цианофенилэтинил)-4-гидроксиоктагидроизоиндол-2-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-(3-метоксифенилэтинил)октагидроизоиндол-2-карбоновой кислоты,
этиловый эфир (±)-(3aRS,4RS,7aSR)-4-(3-фторфенилэтинил)-4-гидроксиоктагидроизоиндол-2-карбоновой кислоты,
трет-бутиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-фенилэтинилоктагидроизоиндол-2-карбоновой кислоты,
трет-бутиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-мета-толилэтинилоктагидроизоиндол-2-карбоновой кислоты,
метиловый эфир (±)-(3aRS,4RS,7aSR)-4-гидрокси-4-мета-толилэтинилоктагидроизоиндол-2-карбоновой кислоты,
(±)-(3aRS,4RS,7aSR)-фуран-2-ил(4-гидрокси-4-мета-толилэтинилоктагидроизоиндол-2-ил)метанон,
(±)-(3aRS,4RS,7aSR)-циклопропил(4-гидрокси-4-мета-толилэтинилоктагидроизоиндол-2-ил)метанон,
(±)-(3aRS,4RS,7aSR)-(4-гидрокси-4-мета-толилэтинилоктагидроизоиндол-2-ил)пиридин-3-илметанон,
метиловый эфир (±)-((1SR,3SR)-3-гидрокси-3-мета-толилэтинилциклогексил)метилкарбаминовой кислоты и
метиловый эфир (±)-((1RS,3SR)-3-гидрокси-3-мета-толилэтинилциклогексил)метилкарбаминовой кислоты,
этиловый эфир (±)-(1RS,3SR)-((3-гидрокси-3-мета-толилэтинилциклогексил)(4-метоксибензил)карбаминовой кислоты,
этиловый эфир (±)-(1RS,3RS)-((3-гидрокси-3-мета-толилэтинилциклогексил)(4-метоксибензил)карбаминовой кислоты,
метиловый эфир (±)-[(1RS,3SR)-3-гидрокси-3-(3-метоксифенилэтинил)-5,5-диметилциклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-(1RS,3SR)-(3-гидрокси-5,5-диметил-3-мета-толилэтинилциклогексил)метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3SR)-3-(3-фторфенилэтинил)-3-гидрокси-5,5-диметилциклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3RS)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3SR)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3RS)-3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3SR)-3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3RS)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]метилкарбаминовой кислоты,
метиловый эфир (±)-[(1RS,3SR)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]метилкарбаминовой кислоты,
(±)-(1RS,3RS)-N-(3-гидрокси-3-мета-толилэтиниг циклогексил)ацетамид,
(±)-(1RS,3SR)-N-(3-гидрокси-3-мета-толилэтинилциклогексил)ацетамид,
этиловый эфир (±)-(1RS,3RS)-(3-гидрокси-3-мета-толилэтинилциклогексил)карбаминовой кислоты,
этиловый эфир (±)-(1RS,3SR)-(3-гидрокси-3-мета-толилэтинилциклогексил)карбаминовой кислоты,
этиловый эфир (±)-(1RS,3RS)-[3-(3-фторфенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
этиловый эфир (±)-(1RS,3SR)-[3-(3-фторфенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
этиловый эфир (±)-(1RS,3RS)-[3-(3-метоксифенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
(±)-(1RS,3RS)-N-[3-(3-фторфенилэтинил)-3-гидроксициклогексил]ацетамид,
(±)-(1RS,3SR)-N-[3-(3-фторфенилэтинил)-3-гидроксициклогексил]ацетамид,
этиловый эфир (±)-(1RS,3SR)-[3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]карбаминовой кислоты,
(±)-(1RS,3RS)-N-[3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]ацетамид,
(±)-(1RS,3SR)-N-[3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]ацетамид,
трет-бутиловый эфир (±)-(1RS,3RS)-[3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]карбаминовой кислоты,
трет-бутиловый эфир (±)-(1RS,3SR)-[3-гидрокси-3-(3-метоксифенилэтинил)циклогексил]карбаминовой кислоты,
трет-бутиловый эфир (±)-(1RS,3RS)-(3-гидрокси-3-мета-толилэтинилциклогексил)карбаминовой кислоты,
трет-бутиловый эфир (±)-(1RS,3SR)-(3-гидрокси-3-мета-толилэтинилциклогексил)карбаминовой кислоты,
трет-бутиловый эфир (±)-(1RS,3RS)-(3-(3-фторфенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
трет-бутиловый эфир (±)-(1RS,3SR)-(3-(3-фторфенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
метиловый эфир (±)-(1RS,3RS)-[3-(3-фторфенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
метиловый эфир (±)-(1RS,3SR)-[3-(3-фторфенилэтинил)-3-гидроксициклогексил]карбаминовой кислоты,
этиловый эфир (±)-(3-фенилэтинилциклогекс-2-енил)карбаминовой кислоты и
этиловый эфир (±)-3-фенилэтинилциклогекс-3-енил)карбаминовой кислоты, этиловый эфир (±)-метил(3-фенилэтинилциклогекс-3-енил)карбаминовой кислоты,
этиловый эфир (±)-(4aRS,5RS,8aSR)-5-гидрокси-5-фенилэтинилоктагидрохинолин-1-карбоновой кислоты,
(±)-[(4aRS,5SR,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-ил]фуран-2-илметанон,
(±)-[(4aRS,5RS,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-ил]фуран-2-илметанон,
трет-бутиловый эфир (±)-(4aRS,5RS,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-карбоновой кислоты,
(±)-[(4aRS,5SR,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-ил]морфолин-4-илметанон,
(±)-[(4aRS,5SR,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-ил](4-метилпиперазин-1-ил)метанон,
этиловый эфир (±)-(4aRS,5RS,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-карбоновой кислоты и
этиловый эфир (±)-(4aRS,5SR,8aSR)-5-(3-хлорфенилэтинил)-5-гидроксиоктагидрохинолин-1-карбоновой кислоты,
этиловый эфир (±)-(4aRS,5SR,8aSR)-5-гидрокси-5-мета-толилэтинилоктагидрохинолин-1-карбоновой кислоты,
этиловый эфир (±)-(4aRS,5RS,8aSR)-5-гидрокси-5-мета-толилэтинилоктагидрохинолин-1-карбоновой кислоты.
Соединение формулы (IV), кроме того, обозначает октагидроиндол.
В одном примере настоящего изобретения предлагается комбинация перечисленных выше соединений формулы (IV) по крайней мере с одним активным агентом, выбранным из группы, включающей L-допу, карбидопу, бензеразид толкапона или энтакапона.
В другом объекте настоящего изобретения модулятор MeTaGluR обозначает соединение формулы (V):
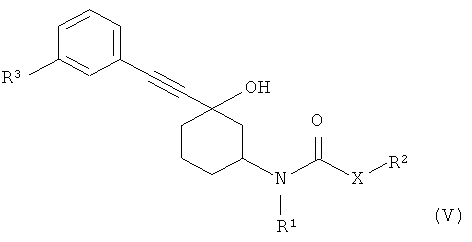
где
R1 обоначает водород или алкил,
R2 обозначает незамещенный или замещенный гетероцикл или
R2 обозначает незамещенный или замещенный арил,
R3 обозначает алкил или галоген,
X обозначает простую связь или алкандиильную группу, необязательно прерванную одним или более атомов кислорода или карбонильных групп или карбонилоксигрупп,
в форме свободного основания или кислотно-аддитивной соли.
Примеры соединений формулы V включают:
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-2карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3H-имидазол-4-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексид]амид 3H-имидазол-4-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 4Н-[1,2,4]триазол-3-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 4Н-[1,2,4]триазол-3-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2-метилфуран-3-карбоновой кислоты,
N-[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3,4-дифторбензамид,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензо[1,3]диоксол-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилпиразин-2-карбоновой кислоты,
[(±)-(1R,1R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид хиноксалин-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензофуран-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензоксазол-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2,5-диметилфуран-3-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (R,S)-тетрагидрофуран-3-карбоновой кислоты,
((1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-3-карбоновой кислоты,
((1S,3S)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-3-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-3-карбоновой кислоты,
((1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-2-карбоновой кислоты,
((1S,3S)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-2карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-2-карбоновой кислоты,
((1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид изоксазол-5-карбоновой кислоты,
((1S,3S)-3-гидрокси-3-мета-толилэтинилциклогексил)амид изоксазол-5-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид изоксазол-5-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид 5-метилпиразин-2-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид 4Н-[1,2,4]триазол-3-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид ЗН-имидазол-4-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид тетрагидропиран-4-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид 1-метил-1Н-имидазол-4-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид (R,S)-тетрагидрофуран-2-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид (R,S)-тетрагидрофуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1S,3S)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид 3H-имидазол-4-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3,4-дифторбензамид,
N-[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3,4-дифторбензамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридин-2-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
N-[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензо[1,3]диоксол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилпиразин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2-метилфуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (R)-тетрагидрофуран-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (S)-тетрагидрофуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид изоксазол-5-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилпиразин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2-метилфуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид изоксазол-5-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорфуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорфуран-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (S)-тетрагидрофуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (R)-тетрагидрофуран-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид
N-[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3,5-дифторпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3,5-дифторпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-метилпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-метилпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-хлорпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-хлорпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1-метил-1H-пиррол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1-метил-1H-пиррол-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1Н-пиррол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1Н-пиррол-2-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-диметиламинобензамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 1Н-пиррол-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метилбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метилбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3-фторбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-этилбутирамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-(2,5-диметоксифенил)-4-оксобутирамид,
2-(2-бензилоксиэтокси)-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]ацетамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-фенилацетамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3-(1Н-индол-4-ил)пропионамид,
2-бензо[1,3]диоксол-5-ил-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]ацетамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-феноксипропионамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(2-фторфенил)ацетамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-гидрокси-1Н-индол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 1-метил-1Н-пиррол-2-карбоновой кислоты,
метиловый эфир N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]терефталамовой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(2-трифторметоксифенил)ацетамид,
5-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-гидроксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-гидроксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-гидроксибензамид,
4-амино-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]бензамид,
4-амино-5-хлор-N-[(18,38)-3-(3-хлорфенилэтинил)-3-гидрокси
3-амино-4-хлор-N-[(18,38)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]бензамид,
3-амино-N-[-[(18,38)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метилбензамид,
2-амино-N-[(18,38)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-гидрокси-3-метоксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-фторбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метансульфонилбензамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3-аминопиразин-2-карбоновой кислоты,
6-амино-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 4-(4-аминобензоиламино)бензойной кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2,6-диоксо-1,2,3,6-тетрагидропиримидин-4-карбоновой кислоты,
N-[(18,38)-3-(3-[хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
3-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]бензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2,3-диметоксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-оксо-4-фенилбутирамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
5-бром-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид изохинолин-1-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиразин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3-бензоилпиридин-2-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-метилникотинамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид хиноксалин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридазин-4-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-метилсульфанилникотинамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-трифторметилникотинамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-6-метилникотинамид,
6-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-6-метилизоникотинамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(4,5-диметокси-3-оксо-1,3-дигидроизобензофуран-1-ил)ацетамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 1,4,5,6-тетрагидроциклопентапиразол-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3-(1Н-индол-2-ил)пропионамид,
изопропиловый эфир 6-[(18,38)-3-(3-хлорфенилэтинил)-3-гидроксициклогексилкарбамоил]пиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид хинолин-6-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилизоксазол-4-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензофуран-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(2-метоксифенокси)ацетамид.
В одном варианте настоящего изобретения предлагается комбинация перечисленных выше соединений формулы (V) по крайней мере с одним активным агентом, выбранным из группы, включающей L-допу, карбидопу, бензеразид толкапона или энтакапона.
В другом варианте настоящего изобретения модулятор mGluR обозначает соединение формулы (VI)
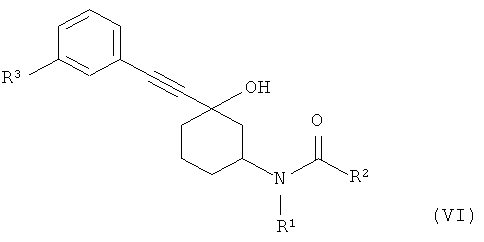
где
R1 обозначает водород или алкил,
R2 обозначает незамещенный или замещенный гетероцикл или
R2 обозначает незамещенный или замещенный арил,
R3 обозначает алкил или галоген,
в форме свободного основания или кислотно-аддитивной соли.
В еще одном варианте модулятор mGluR обозначает соединение формулы (VII):
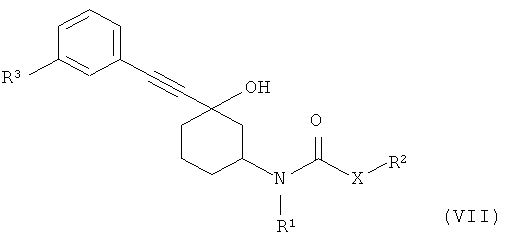
где
R1 обозначает водород или алкил,
R2 обозначает незамещенный или замещенный гетероцикл или
R2 обозначает незамещенный или замещенный арил,
R3 обозначает алкил или галоген,
X обозначает простую связь или алкандиильную группу, необязательно прерванную одним или более атомов кислорода или карбонильных групп или карбонилоксигрупп
в форме свободного основания или кислотно-аддитивной соли.
В другом варианте настоящего изобретения предлагается соединение формулы (VIII)
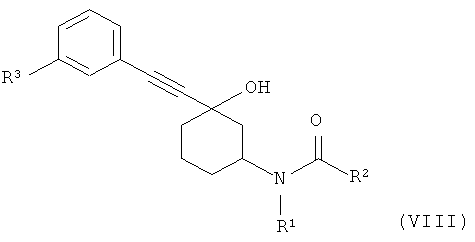
где
R1 обозначает водород или алкил,
R2 обозначает незамещенный или замещенный гетероцикл или
R2 обозначает незамещенный или замещенный арил,
R3 обозначает алкил или галоген,
в форме свободного основания или кислотно-аддитивной соли. Предпочтительные заместители, числовые значения или радикалы в формулах (VII) и (VIII) определены ниже.
R1 предпочтительно обозначает водород или C1-C4алкил.
R1 более предпочтительно обозначает водород,
R3 предпочтительно обозначает фтор, хлор или C1-C4алкил.
R3 более предпочтительно обозначает хлор или метил,
R2 предпочтительно обозначает незамещенный или замещенный гетероцикл, содержащий 3-11 атомов в цикле и 1-4 гетероатома, выбранных из группы, включающей N, O, S, а заместитель выбран из группы, включающей оксогруппу (=O), гидроксигруппу, галоген, аминогруппу, нитрогруппу, цианогруппу, C1-C4алкил, C1-C4алкоксигруппу, C1-C4алкоксиалкил, C1-C4алкоксикарбонил, C1-C4алкоксикарбонилалкил, C1-C4галогеналкил, C6-C10арил, галоген(C6-C10)арил, C6-C10арилоксигруппу, C6-C10арил(C1-C4)алкил.
R2 более предпочтительно обозначает фенил или замещенный фенил, причем заместитель выбран из группы, включающей гидроксигруппу, аминогруппу, галоген, нитрогруппу, цианогруппу, C1-C4алкил, C1-C4алкоксигруппу, C1-C4алкоксиалкил, C1-C4алкоксикарбонил, C1-C4алкоксикарбонилалкил, C1-C4галогеналкил, C6-C10арил, галоген(C6-C10 C6-C10)арил, C6-C10арилоксигруппу, C6-C10арил(C1-C4)алкил.
R2 более предпочтительно обозначает незамещенный, одно- или двухзамещенный гетероцикл, содержащий 5-9 атомов в цикле и 1-3 гетероатома, выбранных из группы, включающей N и O, а заместитель выбран из группы, включающей галоген и C1-C4алкил.
R2 более предпочтительно обозначает незамещенный, одно- или двухзамещенный фенил, причем заместители выбраны из группы, включающей фтор, хлор, гидроксигруппу, метил, метоксигруппу, метоксикарбонил, трифторметоксигруппу, аминогруппу, диметиламиногруппу, метилтиогруппу, метилсульфонил.
R2 наиболее предпочтительно обозначает незамещенный, одно- или двухзамещенный гетероцикл, выбранный из группы, включающей
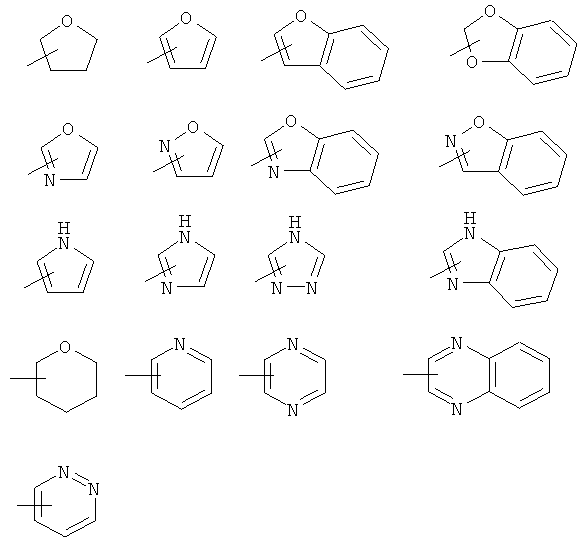
где заместитель выбран из группы, включающей фтор, хлор, метил, метилтиогруппу и аминогруппу.
R2 прежде всего предпочтительно обозначает заместитель, выбранный из группы, включающей
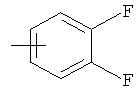 .
.
X предпочтительно обозначает C1-C6алкандиил, C1-C6алкандиил, содержащий кислородную группу в концевом фрагменте или C1-C6алкандиил, содержащий карбонильную группу в концевом фрагменте, C1-C6алкандиил, содержащий карбонилоксигруппу в концевом фрагменте.
X прежде всего предпочтительно обозначает метандиил (-СН2-), 1,2-этандиил (-CH2-СН2-), 1,1-этандиил ((-СН(CH3)-), метандиилоксигруппу (-O-СН2-), 1,2-этандиилоксигруппу (-O-СН2-СH2-), 1,1-этандиилоксигруппу ((-O-СН(CH3)-), метандиилкарбонил (-CO-СН2-), 1,2-этандиилкарбонил (-СО-СН2-CH2-), 1,1-этандиилкарбонил ((-CO-CH(CH3)-), метандиилкарбонилоксигруппу (-C(O)O-CH2-), 1,2-этандиилкарбонилоксигруппу (-C(O)O-СН2-CH2-), 1,1-этандиилкарбонилоксигруппу ((-C(O)O-CH(CH3)-). Функциональные группы X предпочтительно присоединены к группе R2.
Приведенные выше общие или предпочтительные определения радикалов можно комбинировать друг с другом, включая комбинации приведенных предпочтительных значений. Кроме того, отдельные определения могут не применяться.
Согласно настоящему изобретению предпочтительными являются соединения формулы (VII), содержащие комбинацию значений, описанных выше в качестве предпочтительных.
Более предпочтительными согласно настоящему изобретению являются соединения формулы (VII), содержащие комбинацию значений, указанных выше в качестве более предпочтительных.
Наиболее предпочтительными согласно настоящему изобретению являются соединения формулы (VII), содержащие комбинацию значений, указанных выше в качестве наиболее предпочтительных.
Предпочтительными являются соединения формулы (VII), где R2 обозначает незамещенный или замещенный гетероцикл.
В еще одном варианте предлагается соединение формулы (IX)
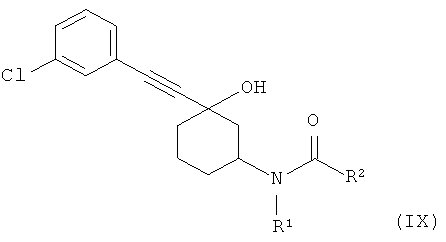
где R1 и R2 определены выше.
В другом варианте настоящего изобретения предлагается соединение формулы (IX), описанное выше, где R2 определен выше, a R1 обозначает водород.
Примеры соединений формул (VII), (VIII) и (IX) включают: [(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3H-имидазол-4-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3H-идазол-4-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 4Н-[1,2,4]триазол-3-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 4Н-[1,2,4]триазол-3-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2-метилфуран-3-карбоновой кислоты,
N-[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3,4-дифторбензамид,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензо[1,3]диоксол-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилпиразин-2-карбоновой кислоты,
[(±)-(1R,3R.)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид хиноксалин-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензофуран-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензоксазол-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2,5-диметилфуран-3-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (R,S)-тетрагидрофуран-3-карбоновой кислоты,
((1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-3-карбоновой кислоты,
((1S,3S)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-3-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-3-карбоновой кислоты,
((1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-2-карбоновой кислоты,
((1S,3S)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-2-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид фуран-2-карбоновой кислоты,
((1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид изоксазол-5-карбоновой кислоты,
((1S,3S)-3-гидрокси-3-мета-толилэтинилциклогексил)амид изоксазол-5-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид изоксазол-5-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид 5-метилпиразин-2-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид 4Н-[1,2,4]триазол-3-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид ЗН-имидазол-4-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид тетрагидропиран-4-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид 1 -метил-1Н-имидазол-4-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид (R,S)-тетрагидрофуран-2-карбоновой кислоты,
((±)-(1R,3R)-3-гидрокси-3-мета-толилэтинилциклогексил)амид (R,S)-тетрагидрофуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1S,3S)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид фуран-2-карбоновой кислоты,
[(±)-(1R,3R)-3-(3-фторфенилэтинил)-3-гидроксициклогексил]амид ЗН-имидазол-4-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3,4-дифторбензамид,
N-[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3,4-дифторбензамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксии,иклогексил]амид пиридин-2-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
N-[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензо[1,3]диоксол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилпиразин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2-метилфуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (R)-тетрагидрофуран-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (S)-тетрагидрофуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид изоксазол-5-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилпиразин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2-метилфуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид изоксазол-5-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорфуран-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорфуран-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (S)-тетрагидрофуран-3-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид (R)-тетрагидрофуран-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
N-[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3,5-дифторпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3,5-дифторпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-метилпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-метилпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлорпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-хлорпиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 6-хлорпиридин-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1-метил-1Н-пиррол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1-метил-1 Н-пиррол-2-карбоновой кислоты,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1Н-пиррол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-хлор-1Н-пиррол-2-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-диметиламинобензамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 1Н-пиррол-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метилбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метилбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3-фторбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-этилбутирамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-(2,5-диметоксифенил)-4-оксобутирамид,
2-(2-бензилоксиэтокси)-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]ацетамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-фенилацетамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3-(1Н-индол-4-ил)пропионамид,
2-бензо[1,3]диоксол-5-ил-N-[(18,38)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]ацетамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-феноксипропионамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(2-фторфенил)ацетамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид-5-гидрокси-1Н-индол-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-амид 1-метил-1Н-пиррол-2-карбоновой кислоты,
метиловый эфир N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]терефталамовой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(2-трифторметоксифенил)ацетамид,
5-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-гидроксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-гидроксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-гидроксибензамид,
4-амино-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]бензамид,
4-амино-5-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-метоксибензамид,
3-амино-4-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]бензамид,
3-амино-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метилбензамид,
2-амино-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-гидрокси-3-метоксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-фторбензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-метансульфонилбензамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридин-2-карбоноврй кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3-аминопиразин-2-карбоновой кислоты,
6-амино-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
[(1R,3R)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 4-(4-аминобензоиламино)бензойной кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 2,6-диоксо-1,2,3,6-тетрагидропиримидин-4-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
3-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]бензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2,3-диметоксибензамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-оксо-4-фенилбутирамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
5-бром-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]никотинамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид изохинолин 1-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиразин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 3-бензоилпиридин-2-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-метилникотинамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид хиноксалин 2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид пиридазин-4-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-метилсульфанилникотинамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-4-трифторметилникотинамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]изоникотинамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-6-метилникотинамид,
6-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-никотинамид,
2-хлор-N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-6-метилизоникотинамид,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(4,5-диметокси-3-оксо-1,3-дигидроизобензофуран-1-ил)ацетамид,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 1,4,5,6-тетрагидроциклопентапиразол-3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-3-(1Н-индол-2-ил)пропионамид,
изопропиловый эфир 6-[(18,38)-3-(3-хлорфенилэтинил)-3-гидроксициклогексилкарбамоил]пиридин-2-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид хинолин-6-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид 5-метилизоксазол-4-карбоновой кислоты,
[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]амид бензофуран 3-карбоновой кислоты,
N-[(1S,3S)-3-(3-хлорфенилэтинил)-3-гидроксициклогексил]-2-(2-метоксифенокси)ацетамид.
В одном варианте настоящего изобретения предлагается комбинация перечисленных выше соединений формул (VII), (VIII) и (IX) по крайней мере с одним активным агентом, выбранным из группы, включающей L-допу, карбидопу, бензеразид толкапона или энтакапона.
В другом варианте предлагается комбинация октагидроиндола с энтакапоном.
В еще одном варианте предлагается комбинация октагидроиндола с L-допой, карбидопой и энтакапоном, а также комбинация октагидроиндола с продуктом Stalevo®.
В других примерах модулятор mGluR обозначает модулятор mGluR5 октагидроиндол, например, метиловый эфир 4-гидрокси-4-мета-толилэтинилоктагидроиндол-1-карбоновой кислоты.
Настоящее изобретение включает комбинацию метилового эфира 4-гидрокси-4-мета-толилэтинилоктагидроиндол-1-карбоновой кислоты и один или более следующих агентов L-допа, карбидопа, бенреразид толкапона или энтакапона, бромкриптин, перголид, прамипексол, ропинирол, каберголин, апоморфин или лизурид.
Кроме того, примеры модуляторов mGluR, прежде всего модулятора mGluR5, включают соединения формулы (I), описанные в заявке WO 2004/014881, и соединения формулы (I), описанные в заявке WO 2007/021575, содержание которых включено в настоящее описание в полном объеме.
Модуляторы mGluR, описанные в данном контексте, могут характеризоваться значительным и селективным модулирующим действием, прежде всего антагонистическим действием в отношении mGluR человека, прежде всего, mGluR5. Указанное свойство можно оценивать in vitro, например, с использованием рекомбинантных метаботропных глутаматных рецепторов человека, прежде всего связанных с PLC подтипов, например, mGluR5, по различным методикам, таким как, например, по ингибированию индуцированного агонистом повышения внутриклеточной концентрации Ca2+, как описано в статьях L.P.Daggett и др., Neuropharm., т.34, сс.871-886 (1995), P.J.Flor и др., J. Neurochem. т.67, сс.58-63 (1996) или по степени ингибирования индуцированного агонистом повышения оборота инозитфосфата, как описано в статьях T.Knoepfel и др., Eur. J. Pharmacol., т.288, сс.389-392 (1994), L.P.Daggett и др., Neuropharm., т.67, сс.58-63 (1996) и приведенных в указанных статьях ссылках. Выделение и экспрессия подтипов mGluR человека описано в заявке US No. 5521297. Отдельные агенты по настоящему изобретению характеризуются ингибированием индуцированного агонистом (например, глутаматом или квисквалатом) повышения внутриклеточной концентрации Ca2+ или индуцированного агонистом (например, глутаматом или квисквалатом) оборота инозитфосфата, которое определяют по данным анализа в рекомбинантных клетках, экспрессиирующих hmGluR5a, т.е. значение IC50 составляет от приблизительно 1 нМ до приблизительно 50 мкМ.
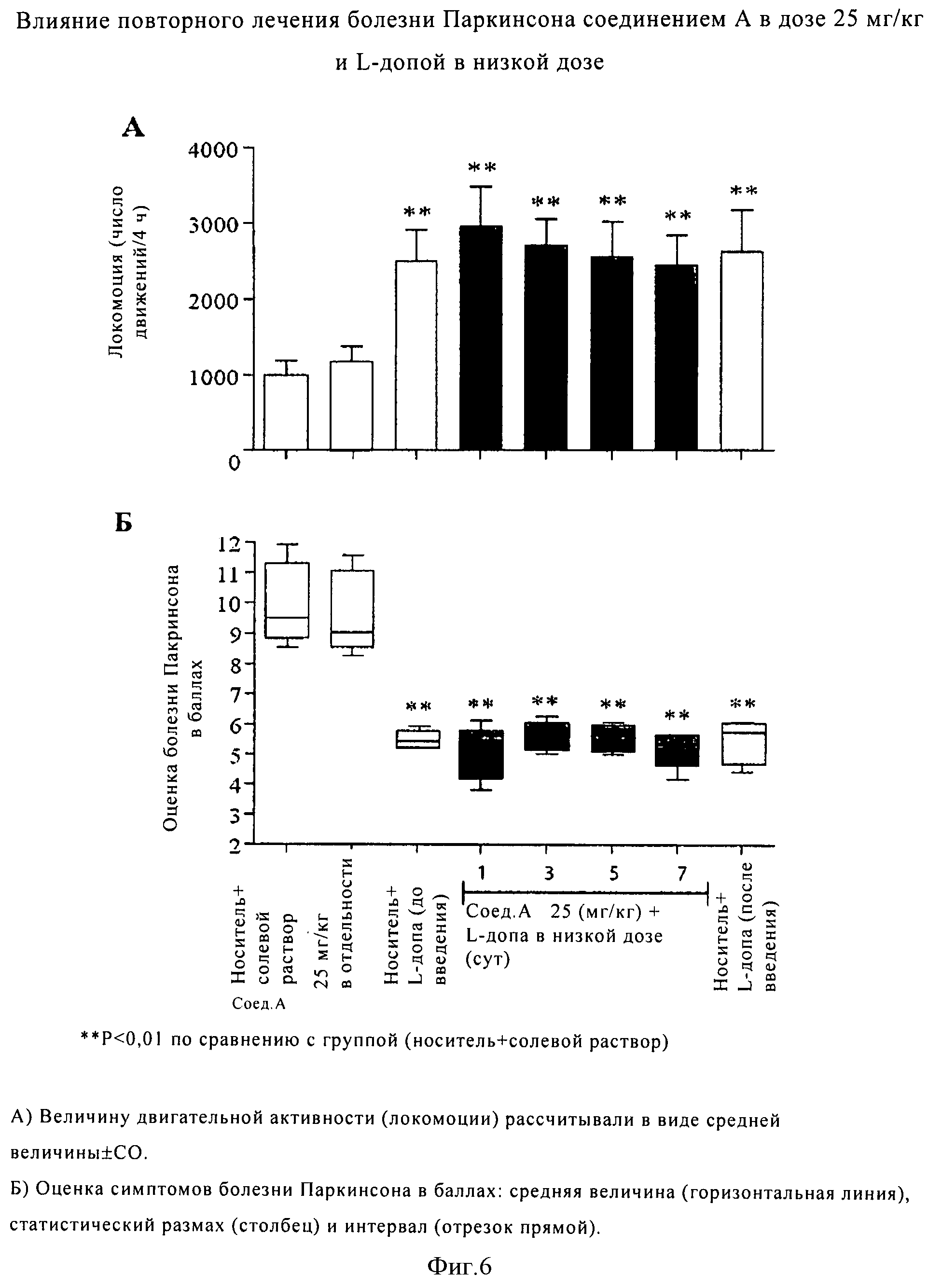
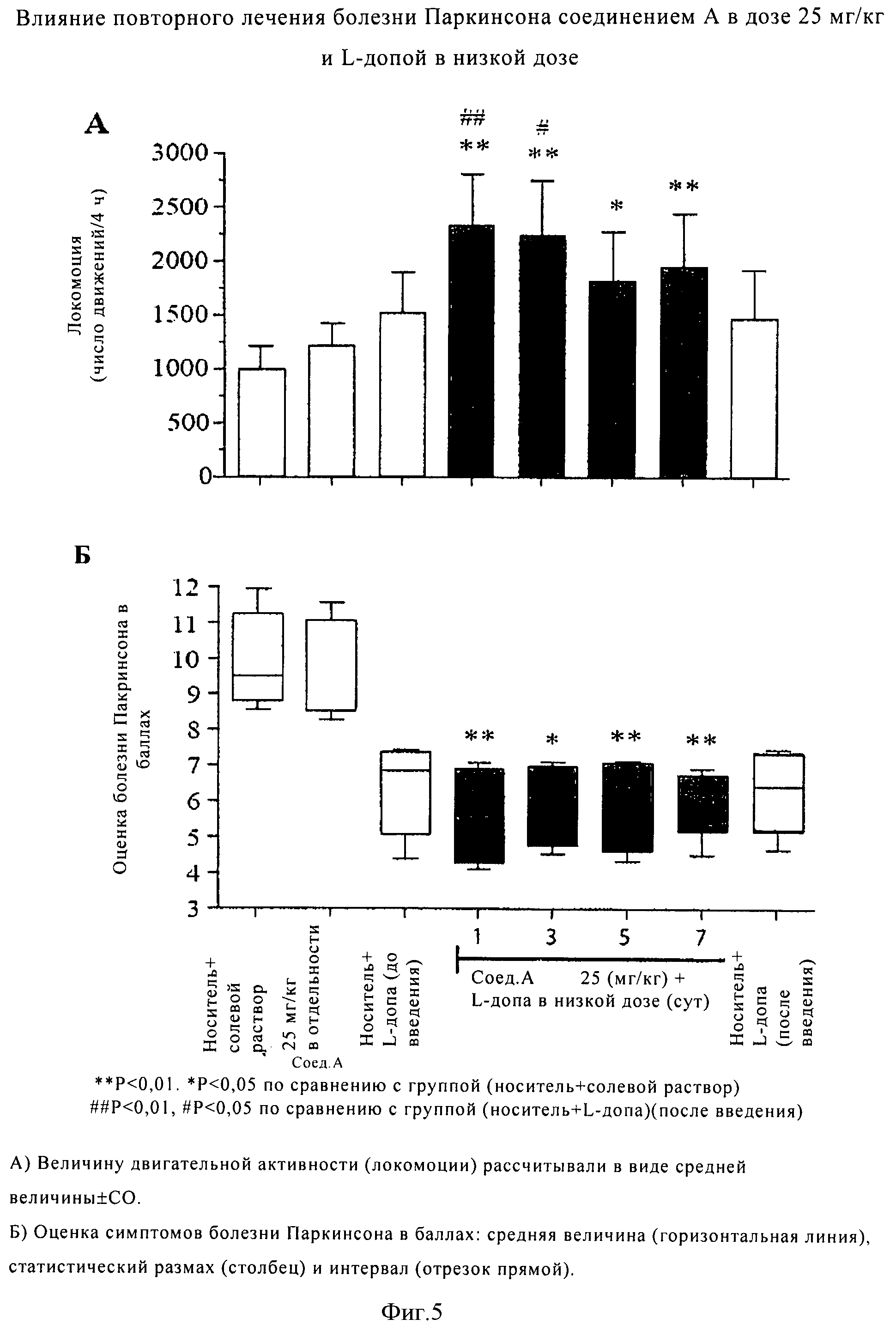
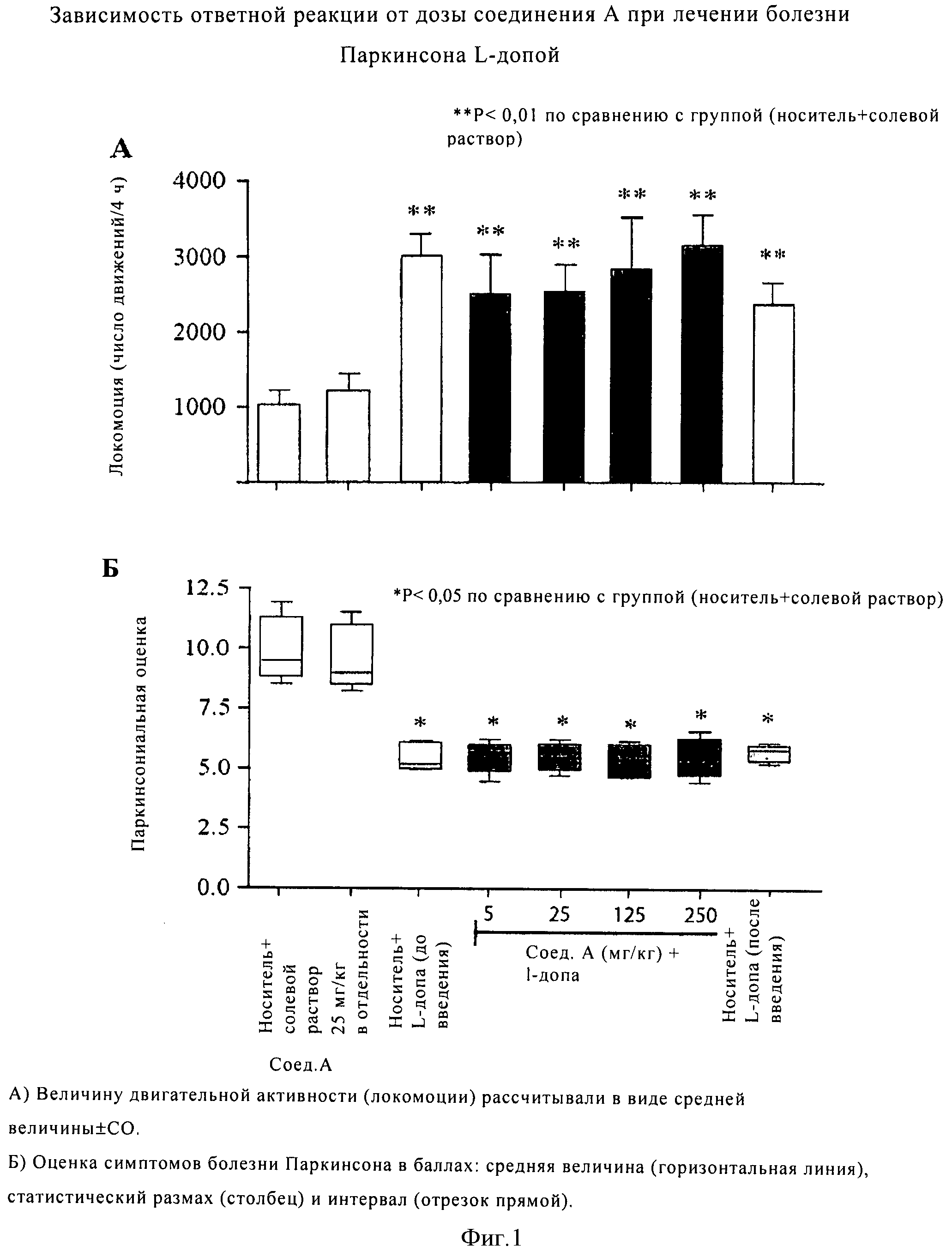
Модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности, можно использовать для лечения, профилактики или замедления прогрессирования болезни Паркинсона и нарушений, связанных с болезнью Паркинсона. Болезнь Паркинсона является дегенеративным заболеванием центральной нервной системы, при котором в большинстве случаев наблюдается нарушение двигательных и речевых способностей пациента. Характеристики болезни Паркинсона различаются и включают один или несколько следующих симптомов: тремор, ригидность, брадикинезия, акинезия, нарушения при ходьбе и неустойчивость положения тела в состоянии покоя, нестабильность положения тела в состоянии покоя, нарушение речи и глотательной функции и нарушения когнитивных способностей, например, потеря памяти, слабоумие и замедленное время реакции. Модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности можно использовать для лечения, профилактики или замедления прогрессирования одного или более симптомов болезни Паркинсона.
В одном варианте модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности, можно использовать для лечения, профилактики или замедления прогрессирования нарушений, связанных с болезнью Паркинсона. Примеры указанных заболеваний включают дискинезию Паркинсона, например, леводопа-индуцированную дискинезию при болезни Паркинсона. Дискинезия Паркинсона часто, но необязательно развивается в результате побочного действия при лечении болезни Паркинсона с использованием леводопы (L-допы), предшественника допамина. Симптомы дискинезии Паркинсона включают нарушение двигательной функции, например, наблюдаются медленные и неконтролируемые непроизвольные движения, дрожь, ригидность и проблемы при ходьбе. При лечении пациентов с использованием L-допы часто наблюдается ослабление симптомов болезни Паркинсона, но при этом такие пациенты испытывают усиливающиеся трудности в положении стоя или даже сидя. После длительного использования L-допы у большинства пациентов развивается дискинезия.
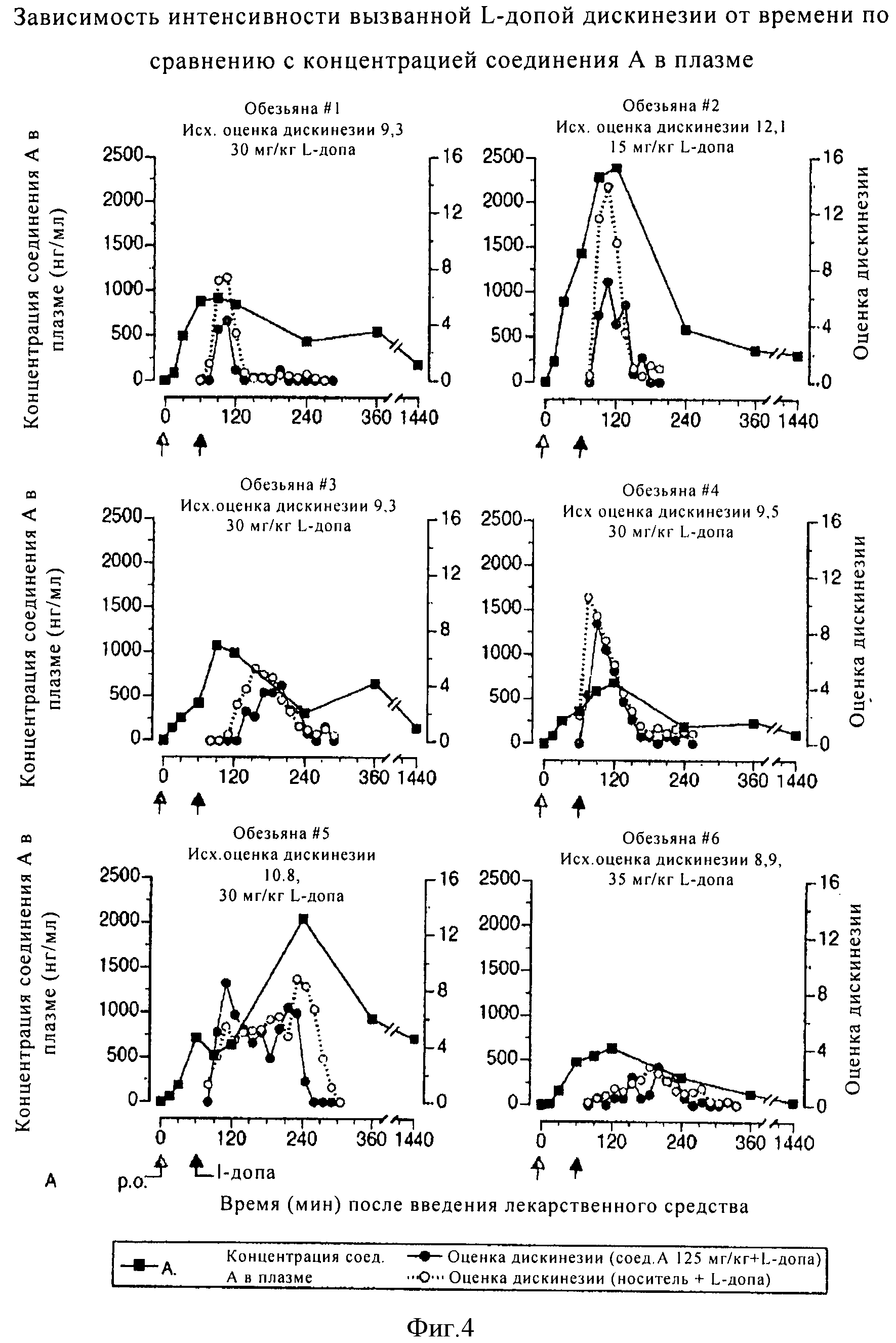
Дискинезия может развиваться в любой момент во время курса лечения L-допой. В одном варианте модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности, и можно использовать для лечения дискинезии, развивающейся в период максимальной концентрации L-допы в плазме пациента. В другом варианте модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности, можно использовать для лечения дискинезии, развивающейся при увеличении или снижении концентрации L-допы в плазме пациента (двухфазная дискинезия).
Дискинезия также может развиваться у пациентов, страдающих от болезни Паркинсона, не принимающих L-допу. В одном варианте соединения по настоящему изобретению можно использовать для лечения дискинезии Паркинсона, не связанной с L-допой.
Лечение может включать снижение интенсивности симптомов, связанных с дискинезией Паркинсона, включая, например, но не ограничиваясь только ими, снижение интервала неконтролируемых движений, снижение числа неконтролируемых движений, улучшение способности выполнять повседневные задачи, улучшение способности хождения, увеличение периодов времени между эпизодами дискинезии.
В случае профилактического лечения, модуляторы mGluR, описанные в данном контексте, в комбинации, как описано в данном контексте, или в отдельности можно использовать для замедления или профилактики развития дискинезии Паркинсона.
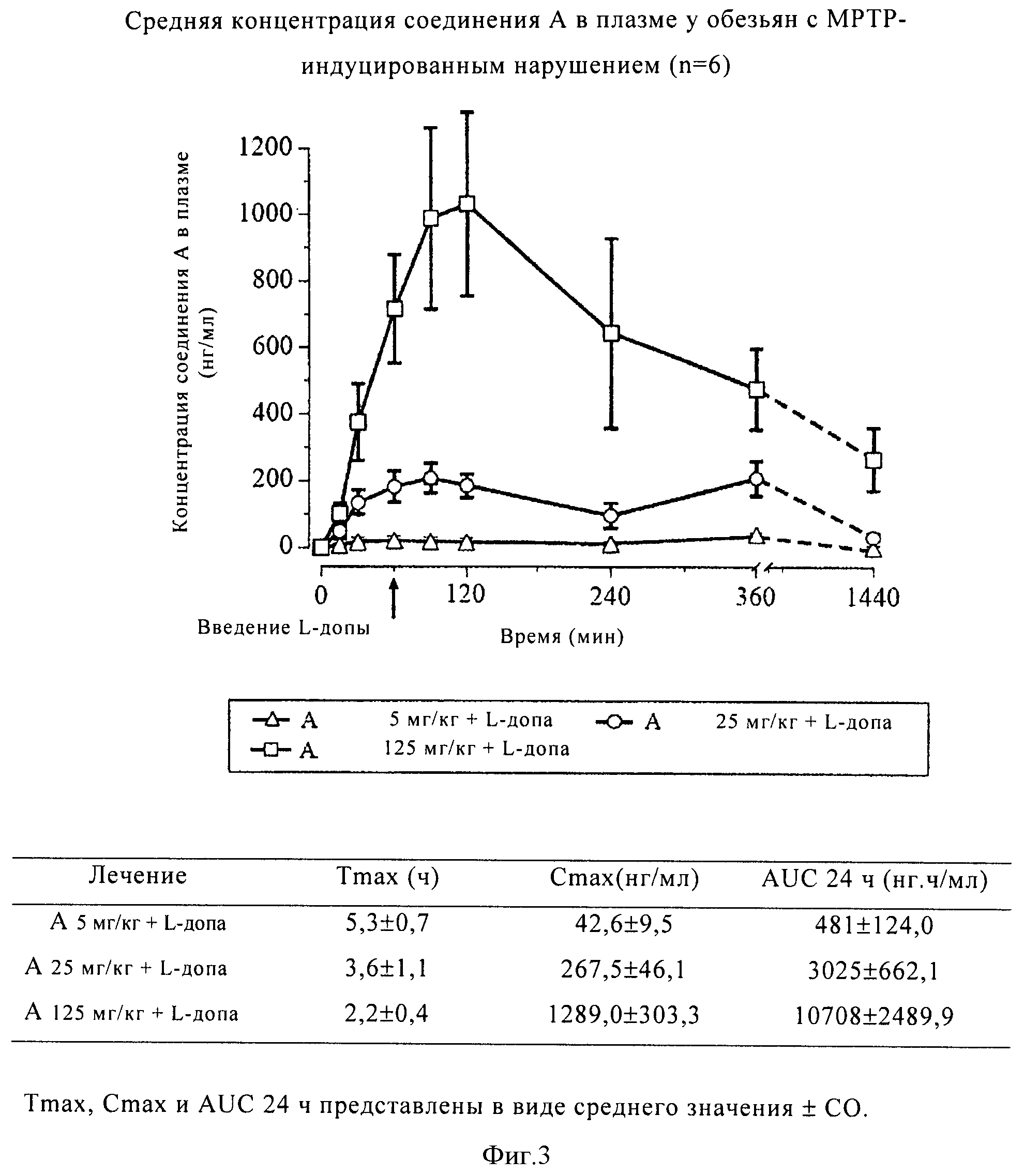
Пригодные дозы для лечения указанных выше показаний (состояний или нарушений) различаются в зависимости, например, от используемого соединения, пациента, способа введения, а также природы и тяжести состояния, подлежащего лечению. Однако, в общем случае, удовлетворительные результаты на животных можно получить при введении суточной дозы от приблизительно 0,01 до приблизительно 100 мг/кг массы тела, предпочтительно от приблизительно 0,1 до приблизительно 10 мг/кг массы тела, например, 1 мг/кг. Для крупных млекопитающих, например, человека, рекомендуемая суточная доза составляет от приблизительно 0,1 до приблизительно 1000 мг, предпочтительно от приблизительно 1 до приблизительно 400 мг, наиболее предпочтительно от приблизительно 10 до приблизительно 100 мг антагониста или другого модулятора mGluR, например, mGluR5, который вводят стандартным способом, например, в виде разделенных доз до четырех раз в сутки.
Для применения согласно настоящему изобретению модулятор mGluR (например, модулятор mGluR5, прежде всего, антагонист mGluR5) можно вводить в виде одного активного агента или в комбинации с другими активными агентами, любым пригодным способом, например, перорально, например, в виде таблеток или капсул, или парентерально, например, в виде растворов или суспензий для инъекций.
Кроме того, в настоящем изобретении предлагается фармацевтическая композиция, содержащая модулятор mGluR (например, модулятор mGluR5, прежде всего, антагонист mGluR5) в смеси по крайней мере с одним фармацевтическим носителем или разбавителем для применения при лечении болезни Паркинсона. В одном варианте композиция предназначена для лечения дискинезии Паркинсона, например, L-допа-индуцированной дискинезии при болезни Паркинсона. Указанные композиции можно получать стандартным способом. Стандартная лекарственная форма может содержать, например, от приблизительно 2,5 до приблизительно 25 мг одного или более модуляторов mGluR, например, антагониста или другого модулятора mGluR5.
Фармацевтические композиции по настоящему изобретению представляют собой композиции для энтерального, например, назального, ректального или перорального, или для парентерального, например, внутримышечного или внутривенного, введения теплокровным животным (человеку и животным), причем указанные композиции включают эффективную дозу фармакологического активного ингредиента в отдельности или в смеси со значительным количеством фармацевтически приемлемого носителя. Доза активного ингредиента зависит от вида теплокровного животного, массы тела, возраста и индивидуального состояния, индивидуальных фармакокинетических данных, заболевания, подлежащего лечению и способа введения.
Фармацевтические композиции включают от приблизительно 1% до приблизительно 95%, предпочтительно от приблизительно 20% до приблизительно 90% активного ингредиента. Фармацевтические композиции по настоящему изобретению представляют собой, например, стандартную лекарственную форму, например, ампулы, флаконы, суппозитории, драже, таблетки или капсулы.
Фармацевтические композиции по настоящему изобретению получают известными способами, например, при стандартном растворении, лиофилизации, перемешивании, грануляции или ином процессе переработки. Указанные способы описаны в заявках WO 2005/079802, WO 2003/047581, WO 2004/000316, WO 2005/044265, WO 2005/044266, WO 2005/044267, WO 2006/1 14262 и WO 2007/071358.
Фармацевтические композиции и лекарственные средства можно характеризовать «объемным соотношением» смеси двух или более компонентов, что соответствует объему одного компонента, деленному на объем всех компонентов композиции. Указанное соотношение можно пересчитать в процентное содержание в расчете на общий объем композиции. Указанное соотношение указано в об.%. Аналогичным образом «массовое соотношение» рассчитывают при делении массы компонента на массу всех компонентов композиции. Указанное соотношение можно пересчитать в массовые % (мас.%) в расчете на общую массу композиции. Указанное соотношение указано в мас.%.
В еще одном объекте настоящего изобретения предлагается набор для профилактики, замедления прогрессирования или лечения заболевания или состояния согласно настоящему изобретению, включающий
(а) количество модулятора mGluR или его фармацевтически приемлемой соли в стандартной лекарственной форме,
(б) количество по крайней мере одного активного ингредиента, выбранного из группы, включающей L-допу или ингибитор допа-декарбоксилазы, или ингибитор катехол-O-метилтрансферазы или агонист допамина или в каждом случае, при необходимости фармацевтически приемлемую соль указанных соединений и
(в) контейнер, содержащий указанные первую, вторую лекарственные формы и т.п.
В другом варианте настоящего изобретения предлагается набор компонентов, например, компоненты, которые необходимо комбинировать согласно настоящему изобретению, и которые можно вводить независимо или с использованием различных фиксированных комбинаций, содержащих различные количества компонентов, т.е. одновременно или в различные периоды времени.
Таким образом, компоненты набора можно вводить одновременно или поочередно, т.е. в различные периоды времени через одинаковые или различные интервалы времени для каждого компонента набора. Предпочтительно интервалы времени выбирают таким образом, чтобы обеспечить более эффективное лечение заболевания или состояния при комбинированном использовании компонентов по сравнению с применением каждого компонента в отдельности.
Таким образом настоящее изобретение также относится к набору компонентов, включающему:
(а) количество модулятора mGluR или его фармацевтически приемлемой соли в составе первой стандартной лекарственной формы,
(б) количество по крайней мере одного активного ингредиента, выбранного из группы, включающей L-допу или ингибитор допа-декарбоксилазы, ингибитор катехол-O-метилтрансферазы или агонист допамина, или в каждом случае при необходимости их фармацевтически приемлемую соль,
в форме двух, трех или более отдельных лекарственных форм компонентов (а) и (б), и указанный набор предназначен прежде всего для профилактики, замедления прогрессирования заболевания или состояния по настоящему изобретению.
Настоящее изобретение, кроме того, относится к коммерческой упаковке, включающей комбинацию по настоящему изобретению, а также инструкции по одновременному, раздельному или последовательному введению.
В предпочтительном варианте коммерческий продукт представляет собой упаковку, включающую активные ингредиенты в виде комбинации по настоящему изобретению (в форме двух, трех или более отдельных лекарственных форм (а) или (б)), а также инструкции для одновременного, раздельного или последовательного введения, или любую их комбинацию, и указанный набор предназначен для замедления прогрессирования или лечения заболеваний, упомянутых в данном контексте.
Все предпочтительные варианты, упомянутые в настоящем изобретении, относятся к комбинации, композиции, применению, способу лечения, набору компонентов и коммерческой упаковке согласно настоящему изобретению.
Указанные фармацевтические составы предназначены для энтерального, например, перорального, а также ректального или парентерального введения теплокровным животным, причем указанные составы содержат фармакологически активное соединение в отдельности или в смеси со стандартными фармацевтическими вспомогательными соединениями. Например, фармацевтическая композиция содержит от приблизительно 0,1% до 90%, предпочтительно от приблизительно 1% до приблизительно 80% активного соединения. Фармацевтические композиции для энтерального или парентерального, а также для внутриглазного введения, например, можно получать в виде стандартных лекарственных форм, например, таблеток, капсул или суппозиториев, а также ампул. Указанные композиции получают известными способами, например, с использованием стандартных способов смешивания, грануляции, нанесения покрытия, солюбилизации или лиофилизации. Таким образом, фармацевтические композиции для перорального введения можно получать при смешивании активного соединения(ий) с твердыми эксципиентами, при необходимости в процессе грануляции полученной смеси и при необходимости при переработке смеси или гранулята в таблетки или ядра таблеток с покрытием после добавления пригодных вспомогательных соединений.
Доза активного соединения зависит от различных факторов, таких как способ введения, вид теплокровного животного, возраст и/или индивидуальное состояние.
Предпочтительные дозы активных ингредиентов фармацевтической комбинации по настоящему изобретению представляют собой терапевтически эффективные дозы, прежде всего, в виде коммерческих форм.
Обычно в случае перорального введения приблизительная суточная доза составляет от приблизительно 1 мг до приблизительно 360 мг, например, для одного пациента с массой тела приблизительно 75 кг.
Доза активного соединения может зависеть от различных факторов, таких как способ введения, вид теплокровного животного, возраст и/или индивидуальное состояние.
Фармацевтическую композицию по настоящему изобретению, описанную в данном контексте, можно использовать для одновременного или последовательного введения в любом порядке, для раздельного введения или в виде фиксированной комбинации.
Действие модуляторов mGluR, например антагонистов mGluR на пациентов, страдающих от болезни Паркинсона или связанных с ней нарушений, например, дискинезии Паркинсона, например, индуцированной введением леводопы (L-допа) дискинезии Паркинсона, можно оценивать следующим образом.
Во-первых, методом визуализации тканей было установлено, что соединения по настоящему изобретению проникают в мозг и связываются с рецепторами mGluR, прежде всего, с рецепторами mGlu5. Во-вторых, было установлено, что у пациентов, которым вводили соединение, например, модуляторы mGluR, описанные в данном контексте, наблюдались улучшение когнитивной способности и другие аналогичные улучшения.
Клинические испытания соединений, описанных в данном контексте, можно проводить, например, по одной из следующих схем. Квалифицированный терапевт может оценивать ряд параметров поведения пациентов и их способностей. Специалисту, конечно, представляется очевидным, что указанные испытания рассматриваются в качестве рекомендуемых, и некоторые параметры испытаний можно модифицировать и изменять, например, в зависимости от обстоятельств и окружающих условий.
Эффективность модуляторов mGluR, описанных в данном контексте, в комбинации или в отдельности, для лечения описанных выше заболеваний можно подтвердить в серии стандартных испытаний, включая описанные ниже.
Схема клинических испытаний: усовершенствованные испытания
Испытание A. Популяция пациентов с нормальным контролем
Популяции пациентов с нормальным контролем вводили лекарственное средство один раз в сутки в течение недели или более. В ходе испытаний оценивали увеличение параметра нарушенной функции у пациента. Пациентов обследовали перед началом испытаний, и после окончания периода лечения, результаты сравнивали и анализировали.
Испытание Б. Популяция пациентов с нарушениями
Популяции пациентов с нарушениями, связанными с болезнью Паркинсона, и связанными с ней нарушениями, например, дискинезией Паркинсона, например, индуцированной введением леводопы (L-допы) дискинезией Паркинсона, вводили лекарственное средство один раз в сутки в течение недели или более и пациентов обследовали. В ходе испытаний оценивали увеличение параметра нарушенной функции у пациента. Пациентов обследовали перед началом испытания и после окончания лечения, результаты сравнивали анализировали.
Условия планирования испытаний
- При планировании испытаний специалисту в данной области медицины представляется очевидным, что следует исключить слишком сильные или слишком слабые эффекты. Другими словами, в ходе испытаний при оценке параметров когнитивные способности следует оценивать в измеримом диапазоне.
- Одним из способов оценки повышения функции являются состояния, которые искусственно нарушают функцию, например, когнитивные способности. Указанные состояния включают, например, нарушение сна и провоцирующее введение лекарственного средства.
- В ходе всех испытаний необходимо использовать контроль плацебо.
- При анализе полученных данных необходимо проводить оценку вероятности влияния практических навыков и запоминания при повторных испытаниях. При планировании испытаний следует учитывать вероятность влияния таких навыков, которые могут привести к ложно-положительным результатам, например, нельзя использовать одинаковые схемы тестирования (например, не рекомендуется использовать одинаковый список слов для запоминания), однако испытания необходимо планировать по одному и тому же механизму. Другие контрмеры могут включать единое тестирование только после завершения испытаний.
Пример 1
Оценка действия соединения A, селективного антагониста mGluR5, в комбинации с леводопой на дискинезию у человека
Метод
Проводили клинические испытания двойным слепым методом с контролем плацебо в параллельных группах пациентов, страдающих от болезни Паркинсона, с леводопа-индуцированной дискинезией при болезни Паркинсона от средней до тяжелой степени, в ходе стабильного лечения допаминергетическими средствами (L-допа, 800-1000 мг/сут, некоторым пациентам также вводили каберголин, ропинорол или прамипексол). Плацебо или соединение A вводили два раза в сутки (дозу титровали от 50 до максимум 300 мг/сут) в качестве дополнительного лечения. В испытаниях участвовали 31 рандомизированных пациента, (средний возраст 61,1 год, женщины 48,4%), 15 пациентам вводили соединение A (25-150 мг дважды в сутки) и 16 пациентам вводили плацебо. Все пациенты прошли полный курс лечения в течение 16 сут.
Оценка
Первичные параметры эффективности в отношении дискинезии оценивали по шкале оценки способности к самообслуживанию Lang-Fahn Activities of Daily Living Dyskinesia Scale (LFADLDS) и в отношении болезни Паркинсона по унифицированной шкале оценки симптомов болезни Паркинсона, часть III. Для оценки вторичных параметров использовали шкалу патологических непроизвольных движений (AIMS) и шкалу UPDRS, часть IV, пп.32-33.
Результаты
Изменение параметров LFADLDS в течение 16 сут по сравнению с базовой линией свидетельствует об эффективности соединения A по сравнению с плацебо (различие составляет 3,02, p=0,02), а также отклонение от базовой линии параметров AIMS (5,31, p<0,001) и суммарное число баллов UPDRS (1,16, p=0,01). Незначительные отличия в лечении наблюдалось при оценке по шкале UPDRS часть III. Таким образом, соединение A в комбинации с леводопой оказывает клинически значимое и значительное антидискинетическое действие без изменения противопаркинсонического действия L-допы.
Пример 2
Оценка действия соединения A, селективного антагониста mGluR5, в комбинации с леводопой на дискинезию и болезнь Паркинсона у обезьян, индуцированную МРТР.
Метод
Исследовали двигательную функцию обезьян Масаса fascicularis с двухсторонним нигростриатным повреждением, индуцированным 1-метил-4-фенил-1,2,3,6-тетрагидропиридином (МРТР). Обезьянам с индуцированным МРТР повреждением в течение длительного времени вводили леводопу, что приводило к развитию дискинезии. Соединение A (5, 25, 125 или 250 мг/кг) вводили за 1 час до введения леводопы, соединение A также вводили в дозе 25 мг/кг один раз в сутки в течение 1 недели в комбинации с леводопой.
Оценка
Первичные параметры эффективности в отношении дискинезии оценивали по шкале оценки способности к самообслуживанию Lang-Fahn Activities of Daily Living Dyskinesia Scale (LFADLDS) и в отношении болезни Паркинсона по унифицированной шкале оценки симптомов болезни Паркинсона, часть III.
Результаты
Введение леводопы улучшает локализацию и снижает параметры оценки болезни Паркинсона у обезьян с индуцированным МРТР повреждением, однако при этом развивается дискинезия. Соединение A (5, 25, 125 или 250 мг/кг) вводили за 1 час до введения леводопы, при этом сохранялась противопаркинсоническая активность леводопы, по данным оценки локализации и оценки баллов противопаркинсонического эффекта, и в тоже время снижались симптомы дискинезии при введении соединения A в дозе 25, 125 и 250 мг/кг. Фармакокинетика однократного введения соединения A указанным обезьянам свидетельствует о доззависимом увеличении концентрации соединения A в плазме после введения в дозе 5, 25 и 125 мг/кг. Введение соединения A за 1 ч до введения леводопы является целесообразным, так как максимальное проявление дискинезии наблюдается примерно в то же время, что и максимальное или повышенное содержание соединения A в плазме.
Кроме того, соединение A вводили 1 раз в сутки в дозе 25 мг/кг в течение 1 недели в комбинации с леводопой. Соединение A в дозе 25 мг/кг в комбинации с низкой дозой леводопы улучшает локализацию у обезьян по сравнению с ответной реакцией на введение только леводопы в отдельности. При введении соединения А в дозе 25 мг/кг в комбинации с высокой дозой леводопы для индукции дискинезии наблюдается максимальный противопаркинсонический эффект и снижение симптомов дискинезии. Во всех экспериментах соединение А в отдельности или в комбинации с леводопой не вызывало отрицательных побочных эффектов.
Полученные результаты свидетельствуют о благоприятном действии комбинации соединения А и леводопы при лечении обезьян с индуцированной МРТР болезнью Паркинсона. Полученные результаты подтверждают эффективность использования антагониста mGluR5 для восстановления нейротрансмиссии мозговых рецепторов mGluR5 при болезни Паркинсона и для снижения симптомов дискинезии.
Изобретение проиллюстрировано на фиг.1-7.