Результат интеллектуальной деятельности: СПОСОБ ДООПЕРАЦИОННОЙ ОЦЕНКИ РИСКА РАЗВИТИЯ ПРОГРЕССИИ ПОСЛЕ РАДИОЧАСТОТНОЙ ТЕРМОАБЛАЦИИ МЕТАСТАЗОВ КОЛОРЕКТАЛЬНОГО РАКА В ПЕЧЕНИ ПРИ ЦИТОРЕДУКТИВНЫХ ОПЕРАЦИЯХ
Вид РИД
Изобретение
Изобретение относится к медицине, в частности к хирургической гепатологии, может быть использовано при лечении метастатического поражения печени. Способ дооперационной оценки риска развития прогрессии заболевания после радиочастотной термоаблации метастазов колоректального рака в печени при циторедуктивных операциях, включающий определение до операции уровня раково-эмбрионального антигена (X1), наличия мутаций в гене KRAS (Х2), индекса метастатического поражения печени (Х3), отличающийся вычислением вероятности прогрессии заболевания по формуле: 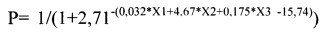 , при значении Р меньше или равного 0,37 - риск прогрессии заболевания низкий, при значении больше 0,37 риск высокий.
, при значении Р меньше или равного 0,37 - риск прогрессии заболевания низкий, при значении больше 0,37 риск высокий.
Изобретение относится к области медицины, а именно к хирургической гепатологии, может быть использовано для определения тактики лечения метастатического поражения печени.
Одним из важных этапов лечения больных колоректальным раком IV стадии является удаление метастазов в печени, так как печень является одним из первых органов на пути гематогенного распространения метастазов колоректального рака (Ганцев Ш.Х., 2008). Как следствие, частота ее поражения достигает 70%. В 25% случаев печень является единственным органом, пораженным метастазами (Ramia J.M. et al., 2011, Вишневский В.А. с соавт., 2010, Каприн А.Д. с соавт., 2014). Несмотря на многочисленные исследования до настоящего времени нет четких показаний к тому или иному объему операции на печени у больных с единичными и множественными билобарными метастазами в зависимости от объема поражения. Это связано с высоким риском дальнейшей прогрессии заболевания после проведенного хирургического лечения.
Известен способ прогнозирования риска развития прогрессии заболевания после хирургического лечения больных с метастазами в печень по данным компьютерной или магнитно-резонансной томографии. Принцип данной методики заключается в оценке количества, размеров и локализации метастатических образований в печени, на основании чего делается прогноз заболевания (Г.Г. Кармазановский и др. Метастатический рак печени: материалы Пленума правления Междунар. Обществ. орг. «Ассоциация хирургов-гепатологов». - 2010. - С. 57-58).
Недостатком данного способа является то, что оценивается только объем опухолевой ткани и локализация метастазов, но не учитывается возможный иммунологический ответ организма больного, соответственно нельзя прогнозировать риск развития прогрессии после выполнения радиочастотной термоаблации (РЧА).
Предшественником предлагаемого способа по технической сущности являются критерии оценки ответа солидных опухолей (Response Evaluation Criteria In Solid Tumors - RECIST), принятые в 2000 г. ВОЗ и пересмотренные в 2008 г. Этот способ основан на изменении линейных размеров метастатического образования, определяемых лучевыми методами исследования, в процессе химиотерапии.
Недостатком данного метода является оценка изменения линейных размеров метастатических очагов в печени в ответ на проведение химиотерапии. Данный метод не дает полной оценки объема метастатического поражения печени на «долечебном» этапе, в данном методе не учитывается число выявленных метастатических очагов, отсутствует учет данных иммунологических маркеров крови, так же не учитывается наличие генных мутаций.
Задачей, на решение которой направлено изобретение, является разработка способа дооперационной оценки риска развития прогрессии после радиочастотной термоаблации множественных билобарных метастазов колоректального рака в печень во время циторедуктивной операции по удалению первичной опухоли, за счет анализа дооперационных данных компьютерной томографии и уровня онкомаркеров крови, определения индекса метастатического поражения печени и наличия или отсутствия мутаций в гене KRAS, до начала какого-либо метода лечения.
Данная задача решается за счет того, что до операции определяется уровень раково-эмбрионального антигена в венозной крови, индекс метастатического поражения печени (ИМПП) и наличие мутаций в гене KRAS и вычисляется вероятность прогрессии заболевания по формуле:
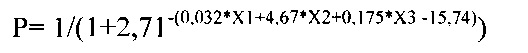
где Р - вероятность того, что произойдет прогрессия заболевания после выполнения радиочастотной термоабляции множественных билобарных метастазов колоректального рака в печень во время выполнения циторедуктивной операции по удалению первичной опухоли в долях единиц; X1 - значение раково-эмбрионального антигена; Х2 - наличие или отсутствие мутаций в гене KRAS; Х3 - индекс метастатического поражения печени; и при получении значения Р меньше или равного 0,37 риск развития прогрессии процесса является низким, а при получении значения Р больше 0,37 риск развития прогрессии процесса является высоким.
Техническим результатом настоящего предложения является оценка риска развития прогрессии после радиочастотной термоабляции множественных билобарных метастазов колоректального рака в печень на «дооперационном» этапе для выбора тактики лечения множественных метастазов колоректального рака в печени.
Предлагаемый способ осуществляют следующим образом. Пациенту перед выполнением циторедуктивной операции по удалению первичной опухоли с одновременной РЧА множественных билобарных метастазов в печень определяют уровень раково-эмбрионального антигена в венозной крови. Определяют наличие или отсутствие мутаций в гене KRAS из биоптата, полученного при эндоскопическом исследовании кишечника. Выполняют компьютерную томографию печени и рассчитывают ИМПП. Полученные данные подставляются в формулу:
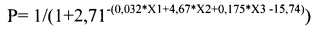
где Р - вероятность того, что произойдет прогрессия заболевания после выполнения радиочастотной термоабляции множественных билобарных метастазов колоректального рака в печень во время выполнения циторедуктивной операции по удалению первичной опухоли в долях единиц; X1 - значение раково-эмбрионального антигена; Х2 - наличие или отсутствие мутаций в гене KRAS; Х3 - индекс метастатического поражения печени; и при получении значения Р меньше или равного 0,37 риск развития прогрессии процесса является низким, а при получении значения Р больше 0,37 риск развития прогрессии процесса является высоким.
Так как технически невозможно смоделировать дихотомическую зависимую переменную, учитывая бесконечное множество значений предикторов (X), задачу регрессии формулируют следующим образом: вместо дихотомической переменной предсказывают непрерывную переменную со значениями на отрезке от 0 до 1 при любых значениях предикторов с помощью логит-преобразования:
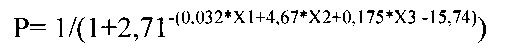
где Р - вероятность того, что произойдет прогрессия заболевания после выполнения радиочастотной термоабляции множественных билобарных метастазов колоректального рака в печень во время выполнения циторедуктивной операции по удалению первичной опухоли в долях единиц; значение 2,71 - основание натуральных логарифмов;
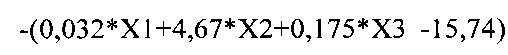 - формула множественной линейной регрессии, где X1 - значение раково-эмбрионального антигена; Х2 - наличие или отсутствие мутаций в гене KRAS; Х3 - индекс метастатического поражения печени.
- формула множественной линейной регрессии, где X1 - значение раково-эмбрионального антигена; Х2 - наличие или отсутствие мутаций в гене KRAS; Х3 - индекс метастатического поражения печени.
В модель были включены 77 пациентов, которым выполнялось РЧА.
Создание математической модели было направлено на определение факторов риска возникновения рецидива в области РЧА и появления новых метастазов по КТ брюшной полости с контрастным усилением после проведенной термоаблации. Кодировка случая проводилась следующим образом:
а) в течение первого года наблюдения после операции рецидива либо появления новых метастазов не было - 0 (N=40);
б) в течение первого года наблюдения после операции был выявлен рецидив либо появление новых метастазов - 1 (N=37).
В модель в качестве предикторов были включены:
1. Возраст;
2. Пол;
3. Т (2,3,4);
4. N (0,1,2);
5. ИМПП;
6. Диффернцировка (высоко-, умеренно-, низкодифференицированные опухоли);
7. Значение СА-242 до операции в Ед/мл;
8. Значение СЕА до операции в нг/мл;
9. Значение СА19-9 до операции в Ед/мл;
10. Наличие мутаций в гене KRAS.
Кодировка предикторов проводилась следующим образом:

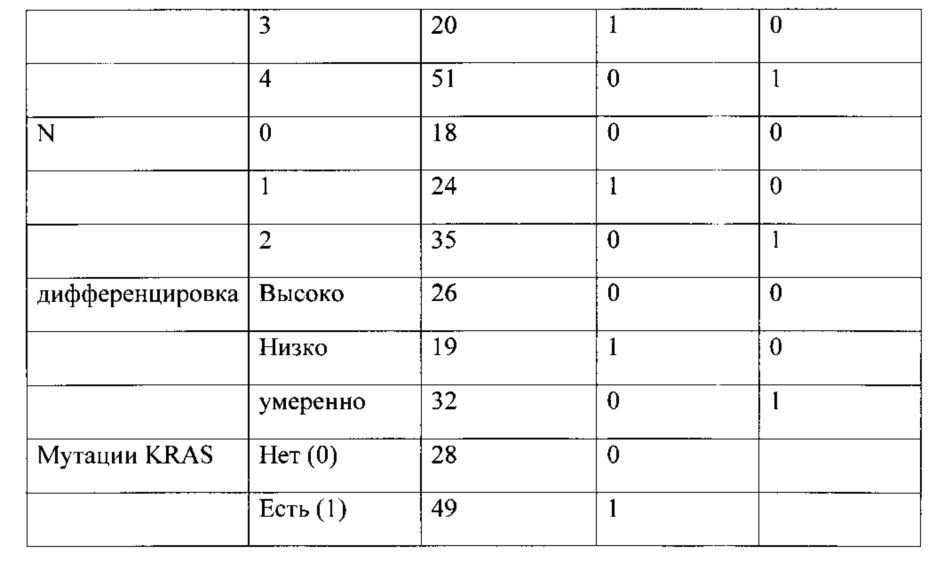
В настоящем исследовании математическую модель строили в модуле логистической регрессии по алгоритму Вальда, с пошаговым включением в программе SPSS. При использовании этого метода предикторы по уровню значимости автоматически пошагово включаются в модель. Относительный вклад отдельных предикторов выражался величиной следующих критериев:
1. Статистика Вальда;
2. Х2;
3. Величина стандартизированного коэффициента регрессии.
В результате была получена модель, включающая в себя 3 наиболее значимых предиктора (X1-Х3):
X1 - CEA
Х2 - Мутации KRAS
Х3 - ИМПП
Параметры математической модели для предсказания развития рецидива на первом году наблюдения после РЧА.
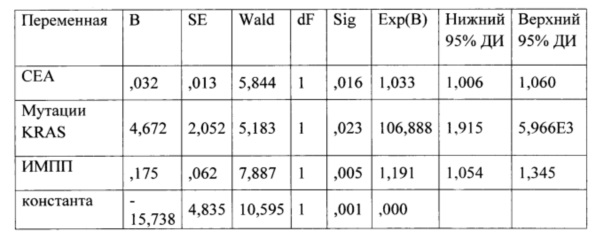
В1-3 - коэффициенты регрессии;
В0 - константа с отрицательным знаком;
p - уровень значимости отличий;
ехрВ - экспонент коэффициентов регрессии.
Все 3 предиктора статистически значимо отличаются от 0 (проверка значимости проводится при помощи статистики Вальда). Число степеней свободы равно 1, если проверяется гипотеза о равенстве нулевого коэффициента обычной или индексной переменной, и для категорильной переменной, равно числу значений без единицы (числу соответствующих индексных переменных). В таблице коэффициенты всех переменных были на уровне 5%, что свидетельствует об их значимости. Учитывая результаты статистики Вальда и стандартизированных коэффициентов регрессии, наибольшее влияние на формирование метастазов на первом году после РЧА играет ИМПП до операции, увеличение этого показателя на единицу на 19,1% увеличивает вероятность рецидива, на втором месте - СЕА - увеличение его на единицу приводит к повышению риска на 3,3%, на 3 месте - мутации гена KRAS.
Таким образом, математическая модель, рассчитываемая по формуле: 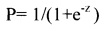 , где
, где 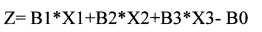
(т.к. В0 - контанта с отрицательным знаком)
выглядит следующим образом:
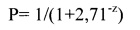 , где
, где 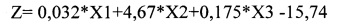
Качество приближения математической модели (соответствие математической модели реальным данным) оценивается при помощи объединенных тестов.
Объединенные тесты для коэффициентов математической модели
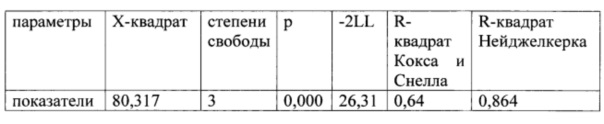
Мерой функции подобия служит отрицательное значение удвоенного логарифма этой функции - 2LL. Введение или удаление предикторов ведет к изменению этой функции, разность этих функций обозначается как X-квадрат и в нашем случае является значимой. Показатели R-квадрат Кокса и Снелла, R-квадрат Нейджелкерка являются мерами определенности. Это псевдокоэффициенты детерминации, полученные на основе отношения функции правдоподобия моделей лишь с константой и со всеми коэффициентами. Они указывают на ту часть дисперсии, которую можно определить с помощью логистической регрессии. Мера определенности по Коксу и Снеллу имеет тот недостаток, что значение, равное 1, является теоретически недостижимым. Этот недостаток устранен благодаря модификации данной меры по методу Нейджелкерка. После 4 шага получена наиболее адекватная модель: критерий X - квадрат составляет 80,317 (р=0,000), коэффициент детерминации Нейджелкерка - 86,4%, именно этот процент изменчивости переменной можно объяснить с помощью использованных предикторов.
Далее приведена классификационная таблица, рассчитанная на основании вышеуказанной модели. Проведено сравнение результатов у 77 больных, полученных при выполнении КТ брюшной полости с целью выявления рецидива и прогрессии метастатического процесса (наблюдаемые результаты) и предсказанных результатов, полученных при помощи математической модели. Кодирование зависимой переменной проводилось следующим образом:
а) в течение первого года наблюдения после операции рецидива либо появления новых метастазов не было - 0;
б) в течение первого года наблюдения после операции был выявлен рецидив либо появление новых метастазов - 1.
Точкой разделения (порог отсечения) при оценке результатов, полученных с применением модели, для наступления и не наступления события являлось значение 0,5. Если значение получалось меньшее 0,5, то можно предположить, что событие (в нашем случае возникновение прогрессии заболевания на 1 году) не наступит, в противном случае предполагается наступление события.
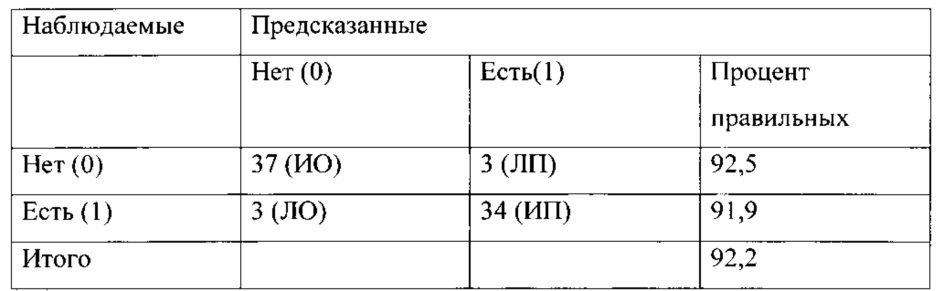
Точка разделения 0,5
Из общего числа больных 77 на основании рассчетов развитие прогрессии можно было прогнозировать у 37 больных - из них диагноз подтвержден на КТ у 34 пациентов (истинноположительный результат - ИП), оставшиеся 3 составили ложноположительный (ЛП) результат. Прогрессия в течение 1 года по результатам модели не выявлена в 40 наблюдениях, из них у 3 пациентов с диагностированными метастазами по КТ (ложнооотрицательный результат - ЛО), у остальных 37 больных новых метастазов и рецидивов не было (истинноотрицательный результат - ИО). Учитывая полученные данные, была просчитана чувствительность (Se), специфичность (Sp) и точность данной математической модели при точке отсечения 0,5.
Чувствительность (Se)=(ИП/(ИП+ЛО))*100=34/(34+3)=91,9%
Специфичность (Sp)=(ИО/(ИО+ЛП))*100=37/(37+3)=92,5%
Точность = ((ИП+ИО)/(ИП+ЛП+ЛО+ИО))*100=34+37/34+3+3+37=92,21%
При точке отсечения 0,5 для модели в целом были правильно распознаны 92,21% от всех обследованных и 91,9% тех, у кого в течение года действительно возникли метастазы.
Для достижения максимальной суммарной чувствительности и специфичности модели необходимо определить оптимальный порог отсечения. Для определения оптимального выбора значения порога отсечения была построена ROC-кривая и проведен ее анализ.
Компьютерной программой SPSS была создана таблица предсказанных результатов, полученных при помощи математической модели, в которую вошли значения Р для 93 больных. Диапазон значений был от 0 до 1.
Затем при помощи компьютерной программы SPSS рассчитывались значения чувствительности (se) и специфичности (sp) для каждого предсказанного значения (Р), которое программой принималось за порог отсечения.
Таблица координат для ROC-кривой

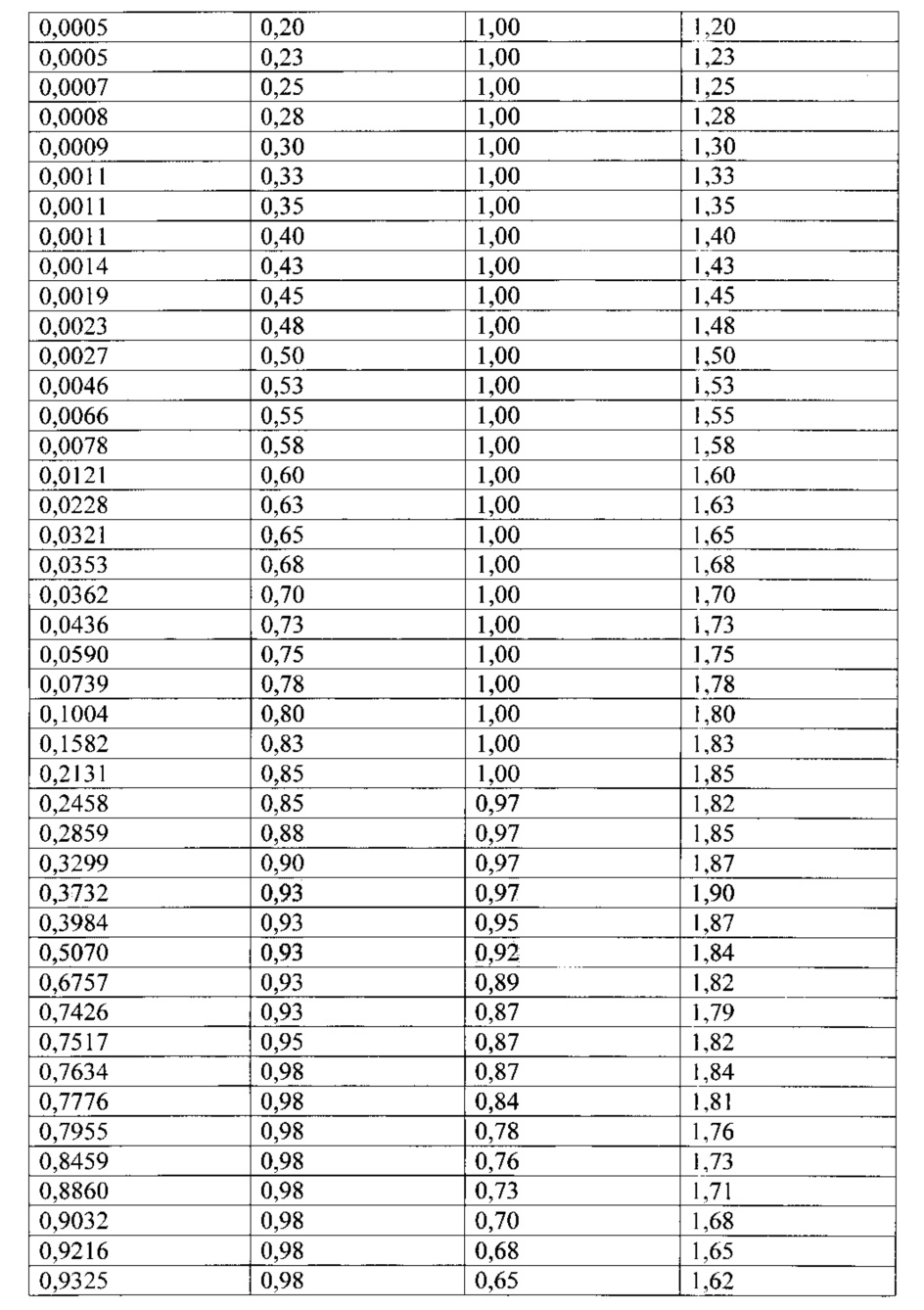
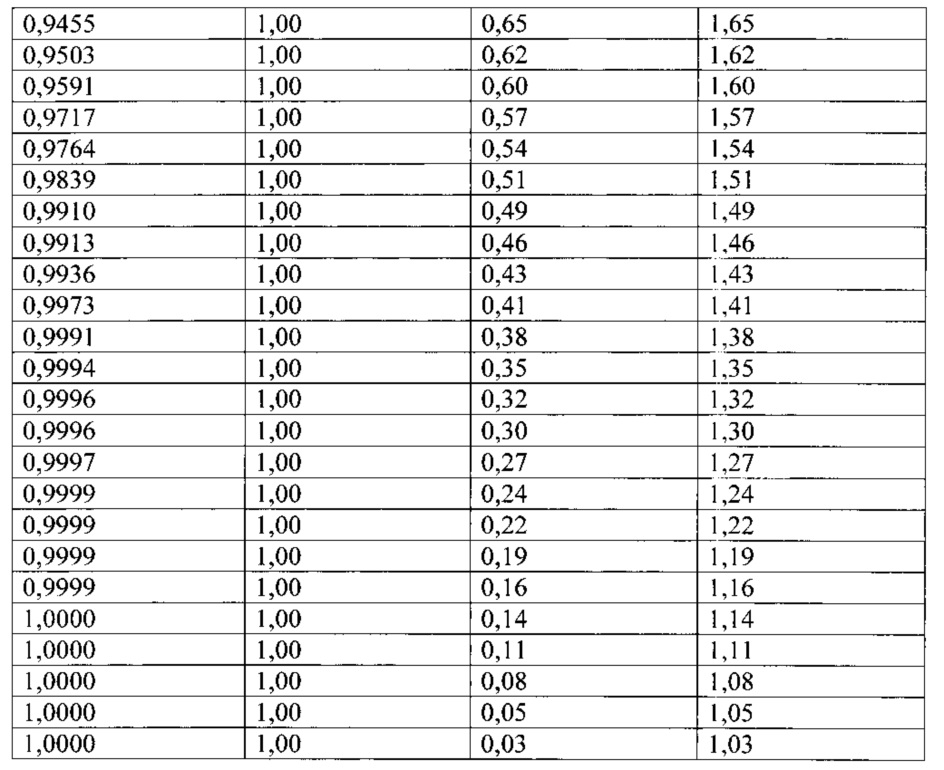
Желтым шрифтом выделены строки с точкой отсечения, равной 0,50, которая использовалась программой по умолчанию, и соответствующие ей чувствительность и специфичность, и точка отсечения 0,37, которой соответствовала максимальная чувствительность и специфичность для данной группы исследуемых больных. Далее приведена классификационная таблица, рассчитанная на основании данных исследования 77 больных с применением КТ брюшной полости с контрастным усилением и предсказанных результатов с применением математической модели с точкой отсечения 0,37.
Классификационная таблица для обучающей выборки с порогом отсечения 0,37


Учитывая полученные данные, была просчитана чувствительность (Se), специфичность (Sp) и точность данной математической модели при точке отсечения 0,37.
Чувствительность (Se)=(ИП/(ИП+ЛО))*100=36/(36+1)*100=97,3%.
Специфичность (Sp)=(ИО/(ИО+ЛП))*100=37/40*100=92,5%.
Точность = ((ИП+ИО)/(ИП+ЛП+ЛО+ИО))*100=37+36/36+1+3+37=94,8%.
Таким образом, изменение точки разделения позволило нам повысить чувствительность модели до 97,3% при сохранении уровня специфичности. Высокая чувствительность метода позволяет выявить максимальное количество пациентов, у которых возможно развитие рецидива, так при точке разделения 0,5 2 пациента ускользнули от нашего внимания и были отнесены к группе низкого риска, тогда как у них были выявлены рецидивы на 1 году, изменение точки разделения исправило эту ошибку.
Для окончательного определения качества математической модели по данным таблицы координат для ROC-кривой была построена ROC-кривая (по оси ординат откладываются значения Se, а по оси абсцисс значение = 100%-Sp). Площадь под кривой (AUC) составляет 0,982±0,011, что соответствует отличному качеству модели.
Разработанный нами способ позволяет объединить и упорядочить вышеперечисленные факторы прогрессии заболевания после выполнения радиочастотной термоабляции синхронных метастазов колоректального рака в печень, упрощает и систематизирует подходы к анализу полученных данных, что позволяет составить правильный план лечения.
Предлагаемый способ поясняется следующими примерами.
Пациент Н., 55 лет. Диагноз: «Рак сигмовидной кишки cT2NxM1 (hepar). 2 а кл.гр.»
Инструментальные обследования: фиброколоноскопия - на 25 см от ануса определяется экзофитная бугристая опухоль, занимающая 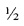 окружности кишки, деформирующая просвет кишки; гистологическое исследование - аденокарцинома; КТ печени: Структура печени неоднородная: в третьем сегменте определяется два гиперэхогенных образования диаметром 18 и 23 мм, в четвертом и шестом сегментах два образования схожей структуры диаметром 25 и 22 мм соответственно. Заключение: множественные метастазы в печень.
окружности кишки, деформирующая просвет кишки; гистологическое исследование - аденокарцинома; КТ печени: Структура печени неоднородная: в третьем сегменте определяется два гиперэхогенных образования диаметром 18 и 23 мм, в четвертом и шестом сегментах два образования схожей структуры диаметром 25 и 22 мм соответственно. Заключение: множественные метастазы в печень.
Рассчитан Индекс метастатического поражения печени (ИМПП): (1,8+2,3+2,5+2,2)*4=35,2. Данные анализа крови на раково-эмбриональный антиген = 9,1 нг/мл. Мутаций в гене KRAS не выявлено.
Полученные данные подставляем в формулу:
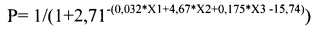
где Р - вероятность того, что произойдет прогрессия заболевания после выполнения радиочастотной термоабляции множественных билобарных метастазов колоректального рака в печень во время выполнения циторедуктивной операции по удалению первичной опухоли в долях единиц; X1 - значение раково-эмбрионального антигена; Х2 - наличие или отсутствие мутаций в гене KRAS; Х3 - индекс метастатического поражения печени.
Получен результат менее 0,37, что соответствует низкому риску развития прогрессии заболевания.
Выполнена операция: резекция сигмовидной кишки, радиочастотная термоаблация четырех метастазов в печень. Выписан на 12 сутки после операции в удовлетворительном состоянии. Прошел 4 курса химиотерапии по схеме FOLFOX. При прохождении контрольного обследования через 6 месяцев данных за прогрессию заболевания нет, что подтверждает достоверность произведенных расчетов.
Пациентка Е., 63 лет. Диагноз: «Рак прямой кишки cT3NxM1 (hepar). 2 а кл.гр.»
Инструментальные обследования: фиброколоноскопия - на 12 см от ануса определяется экзофитная крупнобугристая опухоль, занимающая 2/3 окружности кишки, деформирующая и суживающая просвет кишки; гистологическое исследование - аденокарцинома; КТ печени: Структура неоднородная: во втором, третьем, четвертом, пятом, восьмом сегментах определяются гиперэхогенные образования диаметром от 22 до 30 мм в диаметре. Заключение: множественные метастазы в печень.
Рассчитан Индекс метастатического поражения печени (ИМПП): (2,5+2,2+3,0+2,6+2,3+2,4)*6=90. Данные анализа крови на раково-эмбриональный антиген=36,7 нг/мл. Выявлены мутации в гене KRAS.
Полученные данные подставляем в формулу:
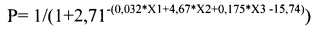
где Р - вероятность того, что произойдет прогрессия заболевания после выполнения радиочастотной термоабляции множественных билобарных метастазов колоректального рака в печень во время выполнения циторедуктивной операции по удалению первичной опухоли в долях единиц; X1 - значение раково-эмбрионального антигена; Х2 - наличие или отсутствие мутаций в гене KRAS; Х3 - индекс метастатического поражения печени.
Получен результат более 0,37, что соответствует высокому риску развития прогрессии заболевания.
Выполнена операция: резекция прямой кишки, радиочастотная термоаблация шести метастазов в печень.
Выписана на 13 сутки после операции в удовлетворительном состоянии. Прошла 4 курса химиотерапии по схеме FOLFOX. На 6 месяц после операции при контрольном обследовании у пациентки диагностирована прогрессия заболевания в виде появления новых метастазов в печень, забрюшинные лимфоузлы, что подтверждает достоверность произведенных расчетов.
Способ предназначен для дооперационной оценки риска развития прогрессии заболевания в течение первого года и может быть использован в онкологических подразделениях для определения тактики лечения пациентов с диагнозом колоректальный рак IV стадии с синхронными множественными билобарными метастазами в печень.
Способ дооперационной оценки риска развития прогрессии заболевания после радиочастотной термоаблации метастазов колоректального рака в печени при циторедуктивных операциях, включающий определение до операции уровня раково-эмбрионального антигена (X1), наличия мутаций в гене KRAS (Х2), индекса метастатического поражения печени (Х3), отличающийся вычислением вероятности прогрессии заболевания по формуле: P=1/(1+2,71), при значении P меньше или равного 0,37 - риск прогрессии заболевания низкий, при значении больше 0,37 риск высокий.
