Результат интеллектуальной деятельности: Гетерогенный катализатор жидкофазного окисления органических соединений
Вид РИД
Изобретение
Изобретение относится к химической промышленности, а именно к области производства гетерогенных катализаторов процессов жидкофазного окисления органических соединений (в том числе, производных фенолов) и может быть применено на предприятиях различных отраслей промышленности для проведения реакций окисления, а также для каталитической очистки сточных вод от токсичных органических контаминантов.
Известен катализатор окисления соединений фенольного ряда в технологических растворах и сточных водах (RU, №2239494, B01J 23/34, B01J 33/00, С07С 37/58, C02F 1/72, 17.06.2003), содержащий соединение марганца (II), при этом в качестве соединения марганца катализатор содержит комплексное соединение, полученное взаимодействием соединения хлорида марганца (II) и хелатообразующего соединения, выбранного из N-фенилантраниловой кислоты или ацетил ацетона, при соотношении металл:лиганд 1:1.
Недостатком данного катализатора является его недостаточно высокая активность и селективность в окислении соединений фенольного ряда.
Известен также гетерогенный катализатор окисления неорганических и/или органических соединений на полимерном носителе (RU, №2255805, B01J 23/70, B01J 23/94, B01D 53/86, 10.07.2005), содержащий активный компонент на полимерном носителе - полиэтилене или полипропилене, или полистироле, или другом полимере, который в качестве активного компонента содержит оксиды и/или гидроксиды, и/или шпинели металлов переменной валентности, и дополнительно модифицирующую добавку, в качестве которой используют органические основания и/или гетерополикислоты, и/или углеродсодержащий материал при следующем содержании компонентов катализатора, массовая доля в %: активный компонент 15-50; модифицирующая добавка 0,5-20; носитель - остальное.
Недостатком этого катализатора является его недостаточно высокая операционная стабильность из-за непрочного связывания активного компонента с поверхностью носителя, а также высокое содержание активного компонента, что обуславливает высокую стоимость катализатора.
Наиболее близким к предлагаемому катализатору является гетерогенный катализатор окисления органических соединений (RU, №2288033; B01J 31/02, B01J 31/08, C12N 9/08, C02F 1/72; 27.11.2006), включающий полимерный носитель, модифицирующую добавку, активный компонент и сшивающий агент, при этом в качестве сшивающего агента используют глутаровый альдегид или карбодиимид, в качестве полимерного носителя катализатор содержит ионообменную смолу, в качестве модифицирующей добавки - альгинат натрия или хитозан, а в качестве активного компонента - экстракт корня хрена или редьки, при следующем соотношении компонентов, % масс.: активный компонент - 1-2%; модифицирующая добавка - 0,1-1%; сшивающий агент - 3-6%; носитель - 90-95%.
Недостатками катализатора являются недостаточно прочная сшивка активного компонента с поверхностью твердого носителя, следствием чего является его низкая активность и стабильность в окислении органических соединений, а также большой мертвый объем частиц катализатора из-за пришивки активного компонента только на поверхности ионообменной смолы.
Задачей, решаемой при создании изобретения, является разработка высокоактивного, стабильного и селективного гетерогенного катализатора многократного использования в реакции жидкофазного окисления органических соединений перекисью водорода.
Техническим результатом изобретения является повышение активности, селективности и операционной стабильности гетерогенного катализатора в реакции жидкофазного окисления органических соединений перекисью водорода.
Поставленная задача и заявленный технический результат достигаются тем, что гетерогенный катализатор жидкофазного окисления органических соединений содержит носитель, глутаровый диальдегид в качестве сшивающего агента и экстракт корня хрена (Armoracia Rusticana) в качестве активного компонента. Согласно изобретению в качестве носителя используют диоксид титана, модифицированный 0,095÷0,105 н. раствором соляной кислоты, 0,195÷0,205%-ным раствором хитозана в 0,0045÷0,0055 М растворе соляной кислоты и 4,95÷5,05%-ным раствором аминопропилтри-этоксисилана в 95,5÷96,5%-ном этаноле, при следующем соотношении компонентов, % масс.:
-ТiO2 - 45÷55;
- Хитозан - 7,5÷12,5;
- Аминопропилтриэтоксисилан - 17,5÷22,5;
- Сшивающий агент (глутаровый диальдегид) - 7,5÷12,5;
- Активный компонент (экстракт корня хрена) - 7,5÷12,5.
Предлагаемый катализатор обладает:
- высокой активностью в реакции окисления органических субстратов в присутствии перекиси водорода;
- стабильностью при многократном использовании;
- удобством отделения от реакционной среды простым фильтрованием.
Включение в катализатор каждого из этих компонентов является обязательным и ни один из них нельзя исключить из данной системы, а также изменить их количественное соотношение, так как это приведет к существенному снижению активности и стабильности катализатора в реакции окисления органических соединений.
Диоксид титана необходим для создания твердой основы для катализатора, что способствует легкому отделению катализатора от реакционной среды простым фильтрованием.
Обработка поверхности диоксида титана раствором соляной кислоты необходима для удаления воды из его пор, а также для появления на поверхности диоксида титана групп ОН-, способных к взаимодействию с другими функциональными группами.
Хитозан необходим для стабилизации частиц диоксида титана и предотвращения их слипания, а также для появления на поверхности носителя групп NН3+ с высокой реакционной способностью.
Аминопропилтриэтоксисилан (АПТЭС) необходим для образования прочной связи между компонентами катализатора (за счет образования связи между гидроксигруппами на поверхности диоксида титана и кремнием, входящим в состав аминопропилтриэтоксисилана) и для появления на поверхности носителя групп NН3+ с высокой реакционной способностью.
Сшивающий агент (глутаровый диальдегид) необходим для образования азометиновой связи (оснований Шиффа) между аминогруппами на поверхности носителя и аминогруппами фермента, входящего в состав экстракта корня хрена.
Активный компонент (экстракт корня хрена) катализирует реакцию окисления органических соединений (в том числе, производных фенола). Получение экстракта методом водной экстракции и центрифугирования позволяет, во-первых, извлечь наибольшее количество фермента, во-вторых, отделить фермент, находящийся в жидкой фазе, от остатков измельченного корня хрена.
Относительное массовое содержание компонентов катализатора выбрано экспериментально. Уменьшение содержания хитозана, аминопропилтриэтоксисилана и глутарового диальдегида меньше представленных значений существенно снижает активность катализатора, так как значительно снижается количество фермента, прочно связанного с поверхностью носителя, и он легко смывается с нее в процессе промывки дистиллированной водой от неспецифически связанных реагентов. Увеличение содержания хитозана больше указанного значения приводит к увеличению адсорбционных свойств катализатора за счет высокой сорбционной емкости хитозана, что существенно снижает активность катализатора из-за удаления субстрата из реакционной среды. Увеличение содержания аминопропилтриэтоксисилана и глутарового альдегида выше указанных значений нецелесообразно, так как, по результатам экспериментов, не приводит к существенному увеличению скорости катализируемой реакции окисления органических субстратов. Содержание активного компонента ниже представленного значения значительно снижает активность катализатора в реакции окисления органических субстратов, а увеличение его содержания нецелесообразно, так как, по результатам экспериментов, не приводит к существенному увеличению активности катализатора в реакции окисления органических субстратов.
Гетерогенный катализатор готовили следующим образом.
Для выделения пероксидазы из сердцевины корня хрена (Armoracia rusticana) свежую сердцевину корня хрена измельчали, после чего 4 г дезинтегрированного корня хрена выдерживали в 30 мл фосфатного буферного раствора (рН=7,0) в течение 1 часа при непрерывном перемешивании. Затем полученную смесь центрифугировали при скорости 5000 об/мин в течение 20 минут, после чего центрифугат фильтровали на микропористом фильтре и сушили при температуре 25°С. Полученный экстракт обладал пероксидазной активностью. До проведения иммобилизации экстракт хранили в холодильнике при температуре 3°С без потери активности.
Навеску диоксида титана (0,5 г) вносили в коническую колбу, содержащую от 25 мл 0,1 н. раствора соляной кислоты, после чего колбу закрывали пробкой и выдерживали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию фильтровали на фильтре Шотта и промывали 200 мл дистиллированной водой. Промежуточная промывка катализатора дистиллированной водой необходима для полного удаления неспецифически связанных компонентов из пор диоксида титана с целью повышения эффективности связывания компонентов катализатора между собой. Образовавшийся осадок переносили в коническую колбу, содержащую 50 мл 0,2%-ного раствора хитозана в 0,005 М НСl, после чего колбу закрывали пробкой и выдерживали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию фильтровали на фильтре Шотта и промывали 200 мл дистиллированной водой. Образовавшийся осадок переносили в коническую колбу, содержащую 4 мл 5%-ного раствора аминопропилтриэтоксисилана в 96%-ном этаноле, после чего колбу закрывали пробкой и выдерживали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию фильтровали на фильтре Шотта и промывали 200 мл дистиллированной водой. Образовавшийся осадок переносили в коническую колбу, содержащую 50 мл 2%-ного раствора глутарового диальдегида, после чего колбу закрывали пробкой и выдерживали в течение 24 часов при постоянном перемешивании. Затем полученную суспензию фильтровали на фильтре Шотта и промывали 200 мл дистиллированной водой. Образовавшийся осадок переносили в коническую колбу, содержащую 30 мл ферментативного экстракта, после чего колбу закрывали пробкой и выдерживали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию фильтровали на фильтре Шотта, промывали 200 мл дистиллированной водой и высушивали на воздухе при температуре 24°С до постоянной массы.
В результате сформировали катализатор со следующим соотношением компонентов, % масс.:
-ТiO2 - 50;
- Хитозан - 10;
- Аминопропилтриэтоксисилан - 20;
- Глутаровый диальдегид - 10;
- Активный компонент (экстракт корня хрена) - 10.
В проведенных экспериментах была исследована активность синтезированного катализатора в реакции окисления 4-хлорфенола при варьировании соотношения компонентов катализатора и условий проведения. Реакцию окисления 4-хлорфенола проводили в присутствии перекиси водорода и 4-аминоантипирина. Наблюдение за ходом реакции вели по изменению оптической плотности реакционной смеси при длине волны 506 нм за счет образования окрашенного продукта реакции - хинонимина. Для исследования активности катализатора в термостатируемую стеклянную ячейку с возвратно-поступательным качанием (300 мин-1) вносили 0,5 г катализатора, 25 мл фосфатного буферного раствора (рН=7,0), 2 мл раствора 4-аминоантипирина (2,3 ммоль/л), 2 мл раствора 4-хлорфенола (2,1 ммоль/л) и 2 мл раствора перекиси водорода (2,3 ммоль/л), через определенные промежутки времени отбирали пробы и измеряли оптическую плотность раствора при 506 нм (раствор сравнения - дистиллированная вода).
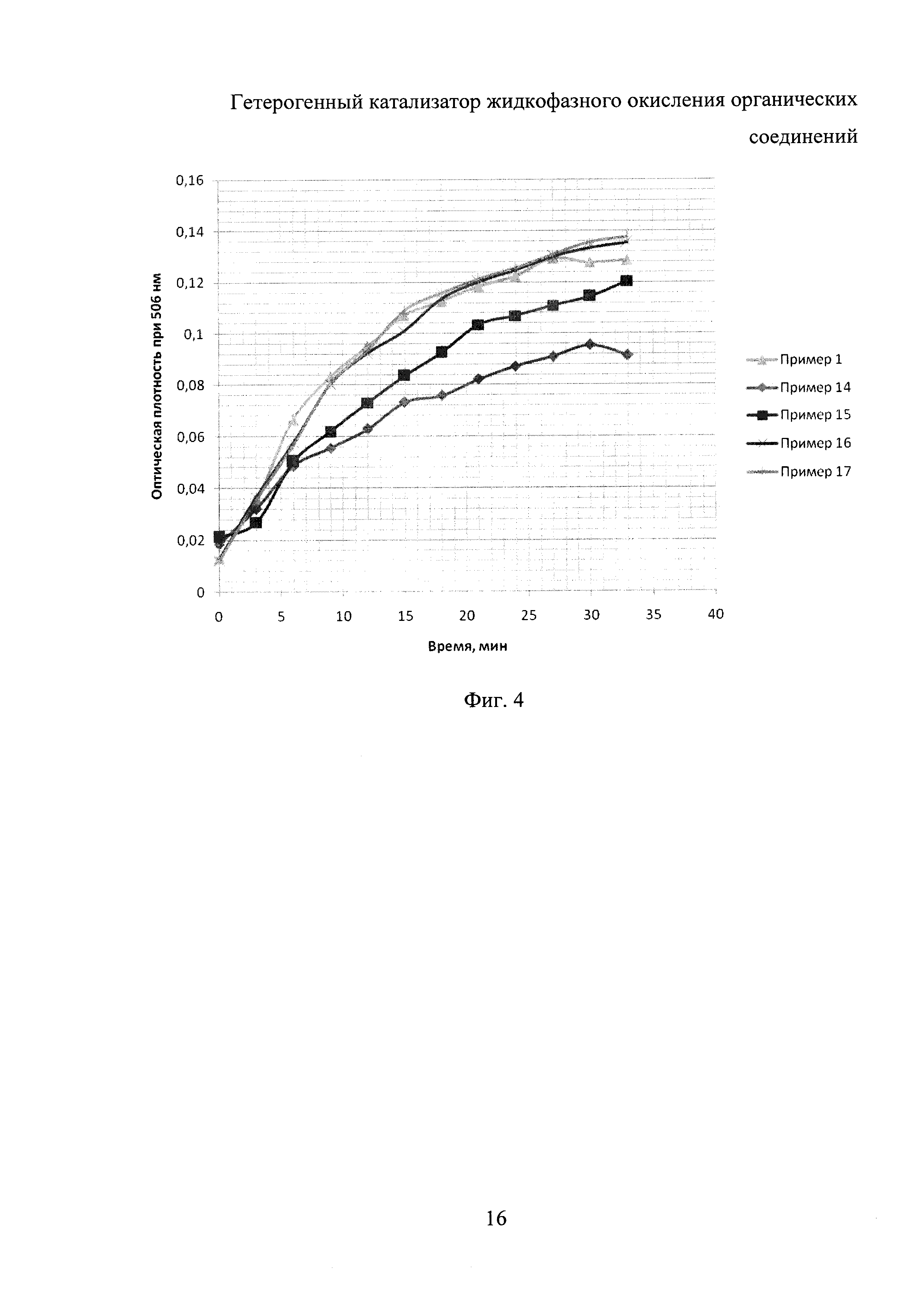
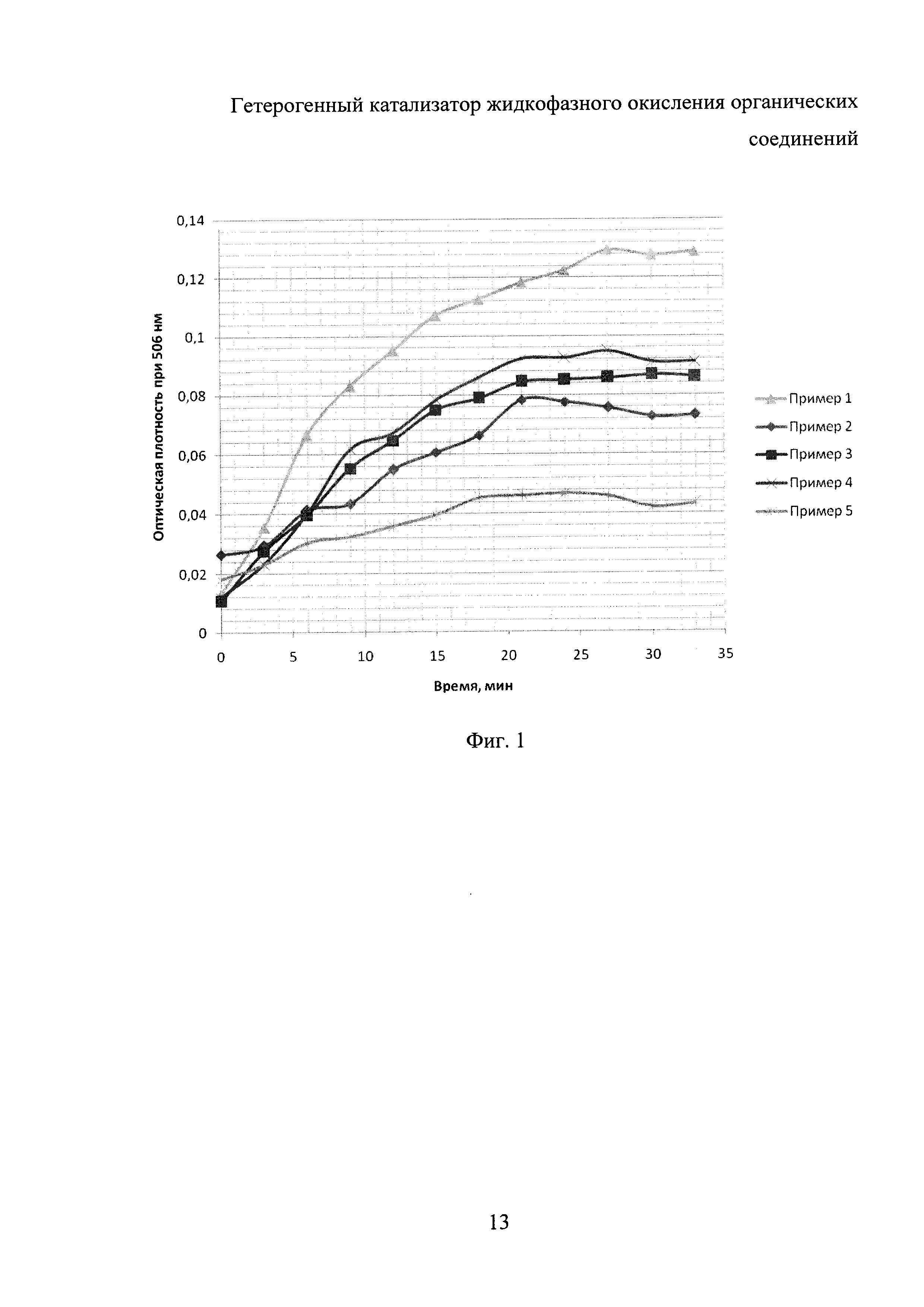
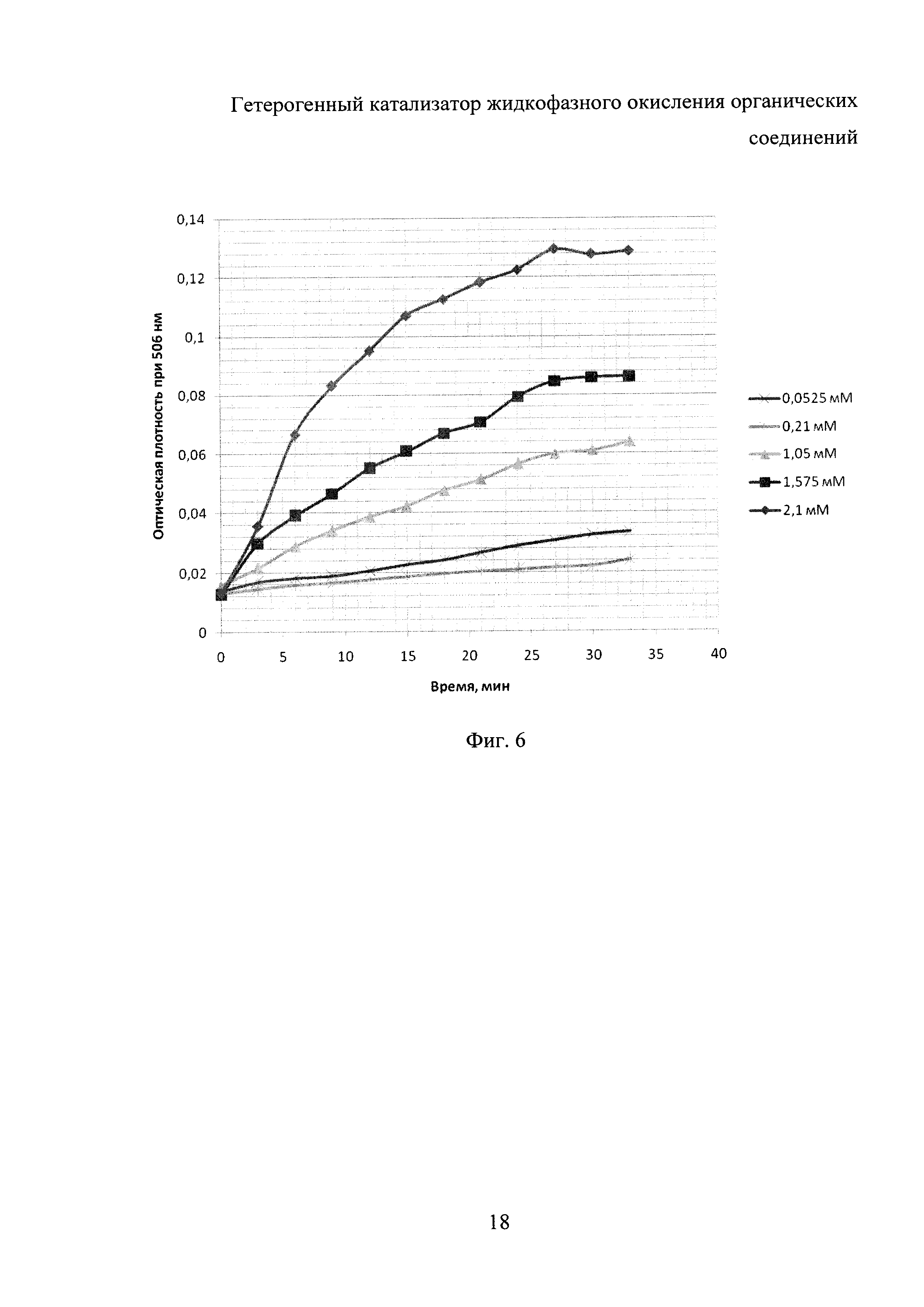
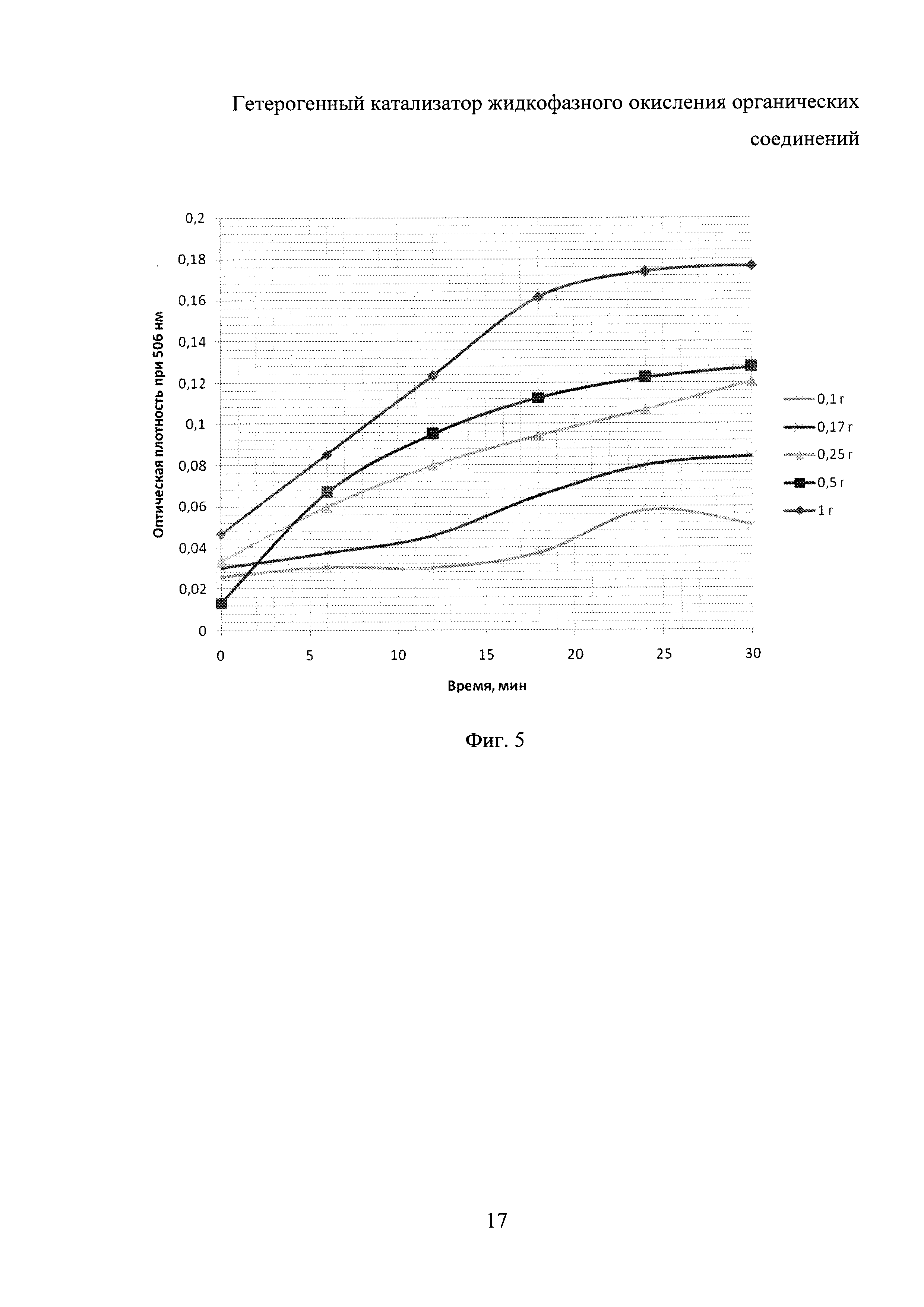
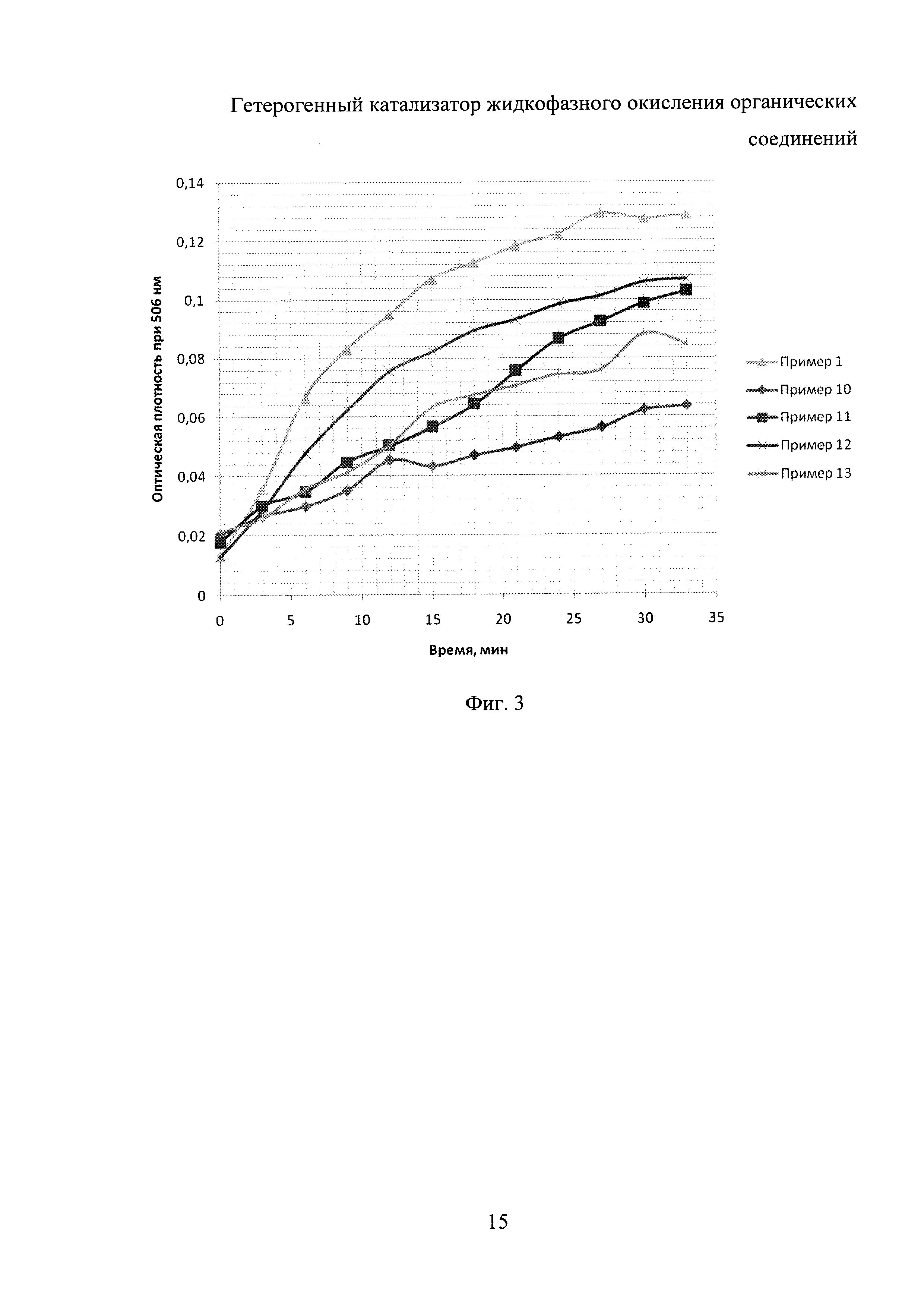
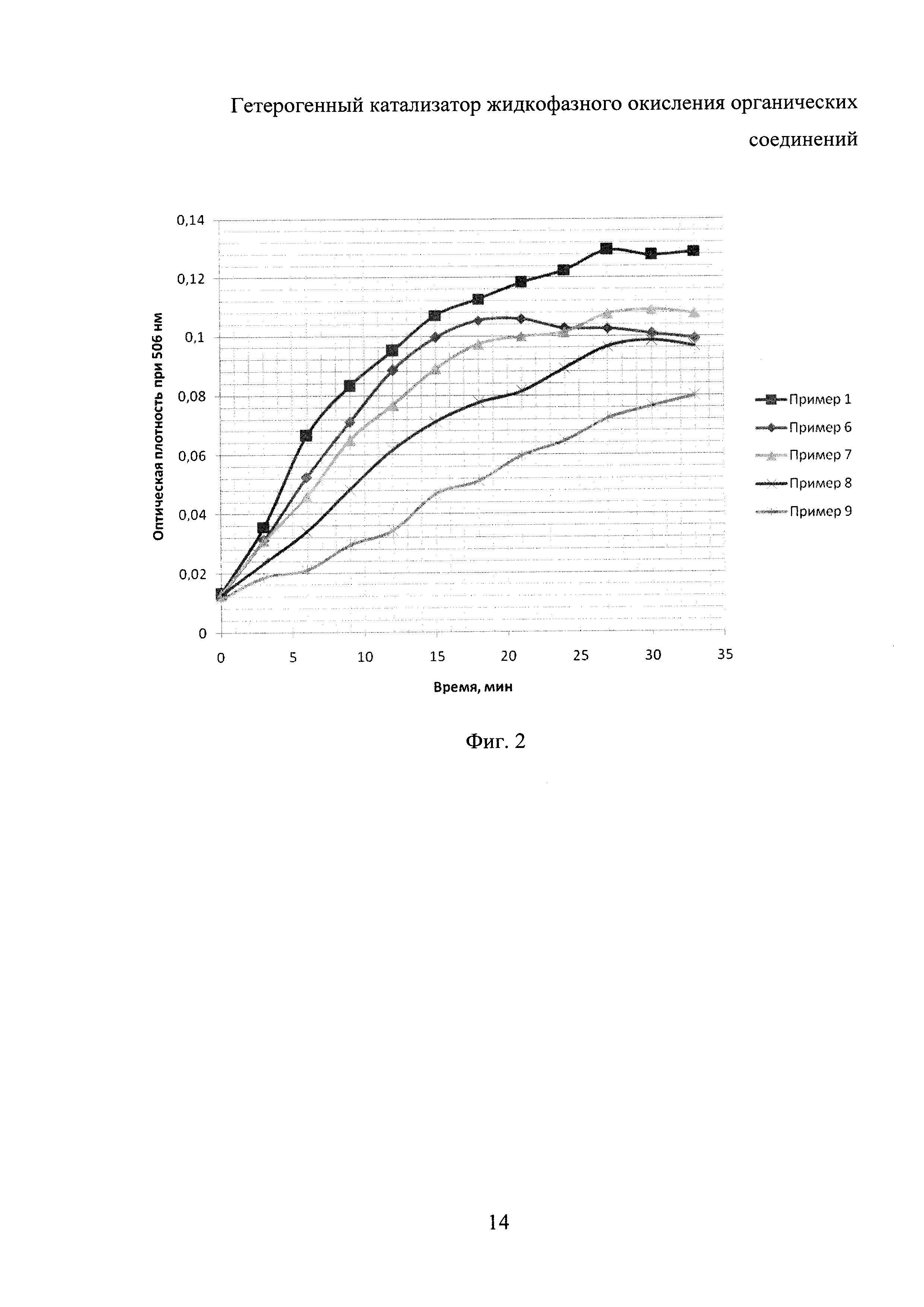
Для пояснения результатов экспериментов используют графики на фиг. 1-6: на фиг. 1 представлены результаты исследований (в виде зависимости оптической плотности реакционной смеси при длине волны 506 нм) по примерам 1-5, на фиг. 2 - по примерам 6-9, на фиг. 3 - по примерам 10-13, на фиг. 4 - по примерам 14-17, на фиг. 5 - по примеру 18, на фиг. 6 - по примеру 19.
Пример 1
Навеску диоксида титана (0,5 г) внесли в коническую колбу, содержащую от 25 мл 0,1 н. раствора соляной кислоты, после чего колбу закрыли пробкой и выдержали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию отфильтровали на фильтре Шотта и промыли 200 мл дистиллированной воды. Образовавшийся осадок перенесли в коническую колбу, содержащую 50 мл 0,2%-ного раствора хитозана в 0,005 М НСl, после чего колбу закрыли пробкой и выдержали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию отфильтровали на фильтре Шотта и промыли 200 мл дистиллированной воды. Образовавшийся осадок перенесли в коническую колбу, содержащую 4 мл 5%-ного раствора аминопропилтриэтоксисилана в 96%-ном этаноле, после чего колбу закрыли пробкой и выдержали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию отфильтровали на фильтре Шотта и промыли 200 мл дистиллированной воды. Образовавшийся осадок перенесли в коническую колбу, содержащую 50 мл 2%-ного раствора глутарового диальдегида, после чего колбу закрыли пробкой и выдержали в течение 24 часов при постоянном перемешивании. Затем полученную суспензию отфильтровали на фильтре Шотта и промыли 200 мл дистиллированной воды. Образовавшийся осадок перенесли в коническую колбу, содержащую 30 мл ферментативного экстракта, после чего колбу закрыли пробкой и выдержали в течение 1 часа при постоянном перемешивании. Затем полученную суспензию отфильтровали на фильтре Шотта, промыли 200 мл дистиллированной воды и высушили на воздухе при температуре 25°С до постоянной массы.
Пример 2
Аналогичен примеру 1, однако использовался 0,05%-ный раствор хитозана в 0,005 М НСl.
Пример 3
Аналогичен примеру 1, однако использовался 0,1%-ный раствор хитозана в 0,005 М НСl.
Пример 4
Аналогичен примеру 1, однако использовался 0,35%-ный раствор хитозана в 0,005 М НСl.
Пример 5
Аналогичен примеру 1, однако использовался 0,5%-ный раствор хитозана в 0,005 М НСl.
Наибольшую скорость реакции (скорость увеличения оптической плотности реакционной смеси) наблюдали в примере 1, что соответствовало использованию 0,2%-ного раствора хитозана (фиг. 1).
Пример 6
Аналогичен примеру 1, однако добавляли 2 мл 5%-ного раствора АПТЭС в этаноле.
Пример 7
Аналогичен примеру 1, однако добавляли 6 мл 5%-ного раствора АПТЭС в этаноле.
Пример 8
Аналогичен примеру 1, однако добавляли 8 мл 5%-ного раствора АПТЭС в этаноле.
Пример 9
Аналогичен примеру 1, однако добавляли 10 мл 5%-ного раствора АПТЭС в этаноле.
Наибольшую скорость реакции (скорость увеличения оптической плотности реакционной смеси) при использовании различных объемов раствора АПТЭС также наблюдали в примере 1, что соответствовало добавлению 4 мл 5%-ного раствора АПТЭС в этаноле.
Пример 10
Аналогичен примеру 1, однако добавляли 10 мл 5%-ного раствора АПТЭС в этаноле.
Пример 11
Аналогичен примеру 1, однако добавляли 25 мл 5%-ного раствора АПТЭС в этаноле.
Пример 12
Аналогичен примеру 1, однако добавляли 75 мл 5%-ного раствора АПТЭС в этаноле.
Пример 13
Аналогичен примеру 1, однако добавляли 100 мл 5%-ного раствора АПТЭС в этаноле.
Наибольшую скорость реакции (скорость увеличения оптической плотности реакционной смеси) при использовании различных объемов раствора глутарового альдегида также наблюдали в примере 1, что соответствовало добавлению 50 мл 2%-ного раствора глутарового диальдегида.
Пример 14
Аналогичен примеру 1, однако добавляли 5 мл ферментативного экстракта.
Пример 15
Аналогичен примеру 1, однако добавляли 15 мл ферментативного экстракта.
Пример 16
Аналогичен примеру 1, однако добавляли 45 мл ферментативного экстракта.
Пример 17
Аналогичен примеру 1, однако добавляли 60 мл ферментативного экстракта.
Как видно из фиг. 4, активность катализатора прямо пропорциональна содержанию экстракта, однако при увеличении содержания экстракта более 30 мл не наблюдали дальнейшего увеличения активности катализатора, что может быть связано с отсутствием на поверхности носителя свободных групп для закрепления увеличенного количества фермента. В связи с этим нецелесообразно использовать большее количество экстракта, так как это существенно повысит себестоимость катализатора.
Таким образом, по результатам экспериментов было определено оптимальное соотношение компонентов биокатализатора:
- 0,5 г диоксида титана;
- 25 мл 0,1 н. раствора соляной кислоты;
- 50 мл 0,2%-ного раствора хитозана;
- 4 мл 5%-ного раствора аминопропилтриэтоксисилана;
- 50 мл 2%-ного раствора глутарового диальдегида;
- 15 мл ферментативного экстракта.
С данным оптимальным катализатором были проведены эксперименты в примерах 18-19.
Пример 18
Катализатор приготавливался аналогично примеру 1, после чего были проведены эксперименты по варьированию концентрации катализатора в реакционной смеси (0,1; 0,17; 0,25; 0,5; 1 г катализатора на 30 мл реакционной смеси согласно описанию). Результаты экспериментов приведены на фиг. 5.
Пример 19
Катализатор приготавливался аналогично примеру 1, после чего были проведены эксперименты по варьированию концентрации 4-хлорфенола (0,21; 0,0525; 1,05; 1,525; 2,1 ммоль/л; аминоантипирин и перекись водорода взяты в 10%-ном избытке относительно концентрации 4-хлорфенола). Результаты экспериментов приведены на фиг. 6.
Аналогичные результаты экспериментов были получены при окислении других субстратов: фенола, пирокатахина, о-дианизидина, 2,4-дихлорфенола. В связи с этим можно сделать вывод об эффективности данного катализатора в реакции окисления органических соединений перекисью водорода.
Таким образом, совмещение двух способов модификации поверхности диоксида титана (хитозаном и аминопропилтриэтоксисиланом) существенно повышает эффективность сшивки, а также активность и операционную стабильность иммобилизованного фермента.
Полученные результаты свидетельствуют о том, что применение катализатора на основе пероксидазы хрена, иммобилизованной на модифицированных диоксид титана, является перспективной возможностью для создания эффективных катализаторов окисления органических субстратов, в том числе в коммунальных и промышленных сточных водах.