Результат интеллектуальной деятельности: ПОЛУГИДРАТ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТА МЕЛАМИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ
Вид РИД
Изобретение
Изобретение относится к химии полиэдрических боргидридньгх соединений и меламина (МА), а именно к полугидрату додекагидро-клозо-додекабората меламина состава (C3H6N6H)2В12Н12⋅0,5Н2О и способу его получения. Полученное соединение может найти применение в качестве энергоемких компонентов различных составов, например пиротехнических.
Элементный состав додекагидро-клозо-додекаборатного аниона 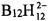 , открывает определенные перспективы для получения соединений, пригодных в качестве энергоемких компонентов энергонасыщенных материалов различного назначения.
, открывает определенные перспективы для получения соединений, пригодных в качестве энергоемких компонентов энергонасыщенных материалов различного назначения.
Так известно использование соли 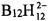 -аниона с катионами следующих металлов: K, Са, La, Zr, Mo, Fe, Co, Ag, Cd, Al, Pb, Bi в качестве горючего в составе физических смесей с рядом окислителей: CsNO3, NaNO3, Pb3O4, KClO3, LClO4, KMnO4, Na2Cr2O7⋅2H2O, BaO2, Na2S2O3) (Pat. US №3126305, опубл. 24.03.1964 г.).
-аниона с катионами следующих металлов: K, Са, La, Zr, Mo, Fe, Co, Ag, Cd, Al, Pb, Bi в качестве горючего в составе физических смесей с рядом окислителей: CsNO3, NaNO3, Pb3O4, KClO3, LClO4, KMnO4, Na2Cr2O7⋅2H2O, BaO2, Na2S2O3) (Pat. US №3126305, опубл. 24.03.1964 г.).
Вышеуказанные соли 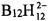 - аниона получают нейтрализацией додекагидро-клозо-додекаборатной кислоты Н2В12Н12 оксидами, гидрооксидами или карбонатами соответствующих элементов. Выделение целевых соединений проводят выпариванием их растворов досуха (за исключением солей серебра и свинца, которые выпадают в осадок и отделяются фильтрованием).
- аниона получают нейтрализацией додекагидро-клозо-додекаборатной кислоты Н2В12Н12 оксидами, гидрооксидами или карбонатами соответствующих элементов. Выделение целевых соединений проводят выпариванием их растворов досуха (за исключением солей серебра и свинца, которые выпадают в осадок и отделяются фильтрованием).
Недостатком вышеприведенных солей 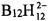 -аниона является их высокая растворимость в воде (за исключением солей серебра и свинца), сложность и энергозатратность их выделения из растворов в чистом виде. Труднорастворимые соли серебра и свинца относительно легко выделить из растворов в виде безводных солей, но соль серебра отличается дороговизной, а соль свинца экологически опасна.
-аниона является их высокая растворимость в воде (за исключением солей серебра и свинца), сложность и энергозатратность их выделения из растворов в чистом виде. Труднорастворимые соли серебра и свинца относительно легко выделить из растворов в виде безводных солей, но соль серебра отличается дороговизной, а соль свинца экологически опасна.
Известны двойные соли M2B12H12×MNO3, где М - Rb, Cs, которые запатентованы в качестве энергоемких воспламеняющих веществ (Pat. US №3184286, опубл. 18.05.1965).
Двойные соли M2B12H12×MNO3 получают взаимодействием в водном растворе веществ, содержащих в своем составе 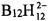 -,
-, 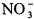 -анионы и Rb+-, Cs+-катионы.
-анионы и Rb+-, Cs+-катионы.
Образовавшийся труднорастворимый осадок двойных солей M2B12H12×MNO3 отфильтровывают и, с целью очистки от примесей, проводят перекристаллизацию (Канаева О. А., Кузнецов Н.Т. Сосновская О.О., Гоева Л.В. // Журн. неорг.хим. 1980. №9. С. 2380-2383).
Недостатком M2B12H12×MNO3 в качестве энергоемких компонентов является дороговизна входящих в их состав рубидия и цезия.
Известна соль додекагидро-клозо-додекаборатной кислоты Н2В12Н12 и хитозана C6O4H9NH2 - додекагидро-ктгозо-додекаборат хитозания (C6O4H9NH3)2В12Н12 (Пат. РФ №2158221, опубл. 27.10.2000 г., бюл. №30). Образование этого соединения происходит благодаря наличию в структуре хитозана донорных атомов азота. При этом два донорных электрона азота NH2-группы взаимодействуют со свободной 1S орбиталью Н+-катиона кислоты Н2В12Н12 с образованием по донорно-акцепторному механизму катиона хитозания 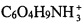 , который в сочетании с
, который в сочетании с 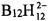 -анионом дает труднорастворимую соль.
-анионом дает труднорастворимую соль.
Додекагидро-клозо-додекаборат хитозания (C6O4H9NH3)2B12H12 получают взаимодействием хитозана C6O4H9NH2 с кислотой H2B12H12 или по обменной реакции между растворимыми солями хитозана и растворимыми солями додекагидро-клозо-додекаборатной кислоты Н2В12Н12. Образовавшийся нерастворимый (C6O4H9NH3)2B12H12 отделяют фильтрованием или центрифугированием, отмывают от остатков маточного раствора и сушат при 105°С до постоянной массы. В результате получают твердый компактный продукт (в виде пленок, пластин, объемных материалов), который может быть измельчен в порошок.
Недостатком соли (C6O4H9NH3)2В12Н12 является отсутствие на сегодняшний день промышленного производства хитозана как исходного продукта, что сказывается на его стоимости.
Наиболее близким к заявляемому соединению является додекагидро-клозо-додекаборат полиэтиленимина состава C2H4NH⋅0,4 Н2В12Н12, который может применяться в качестве энергоемких компонентов пиротехнических составов (Патент РФ №2556930, опубл. 20.07.2015 г., бюл. №20). Известно, что полиэтиленимин (ПЭИ), как и хитозан, благодаря наличию в его составе донорных атомов азота, проявляет ярко выраженные свойства основания. Со многими кислотами он образует соли: перхлораты, нитраты и др. Полиэтиленимин и его модификаты широко используются во многих отраслях промышленности в качестве ионитов, комплексообразователей, флокулянтов (например, для очистки сбросовых вод целлюлозно-бумажного производства). Это достаточно дешевый химический продукт, выпускаемый в промышленном масштабе (Гембицкий П.А. Пути практического использования полиэтиленимина и его модификатов. М., 1986).
Додекагидро-клозо-додекаборат полиэтиленимина получают взаимодействием водных растворов полиэтиленимина (C2H4NH)n с додекагидро-клозо-додекаборатной кислотой Н2В12Н12, взятых в мольном соотношении 1 к (0,5-0,6), с последующим выделением целевого продукта. Образовавшийся продукт, выделяющийся в виде вязкой липкой густой массы, отделяют от раствора и сушат до твердого состояния.
Недостатком додекагидро-клозо-додекабората полиэтиленимина является сложность его выделения из раствора, а также низкая термическая устойчивость (не выше 160°С).
Задачей изобретения является получение нового химического энергоемкого соединения на основе 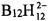 -аниона с высокой термической устойчивостью.
-аниона с высокой термической устойчивостью.
Поставленная задача решается соединением, образующимся при взаимодействии додекагидро-клозо-додекаборатной кислоты с меламином (МА). Полученное новое соединение состава (C3H6N6H)2В12Н12⋅0,5Н2О (полугидрат додекагидро-клозо-додекабората меламина) является малорастворимым.
Меламин C3H6N6 (2,4,6-триамин-1,3,5-триазин) является одним из известных и широко используемых в различных отраслях промышленности продуктом. Меламин, как хитозан или полиэтиленимин, содержит в своей структуре донорные атомы азота и поэтому может давать соли с кислотами, например с хлористоводородной (Химическая энциклопедия в 5 т.Т. 3. Гл. ред. И.Л. Кнунянц. М.: Большая Российская энциклопедия, 1992. С. 21; Janczak J1,  GJ. Melaminiurn chloride hemihydrate // Acta Crystallogr C. 2001. V. 57. N 9. P. 1120.). Известны также соли меламина (МА) с циануровой (Патент Японии 5455587, 1979; Европейский патент 1438353, 2004; Патент РФ 2292341, 2007), борной (Патент США 5854155, 1998; Патент РФ 2292341, 2007), пирофосфорной (Патент США 6268494, 2001; Патент РФ 2292341, 2007), серной (Janczak J1,
GJ. Melaminiurn chloride hemihydrate // Acta Crystallogr C. 2001. V. 57. N 9. P. 1120.). Известны также соли меламина (МА) с циануровой (Патент Японии 5455587, 1979; Европейский патент 1438353, 2004; Патент РФ 2292341, 2007), борной (Патент США 5854155, 1998; Патент РФ 2292341, 2007), пирофосфорной (Патент США 6268494, 2001; Патент РФ 2292341, 2007), серной (Janczak J1,  GJ. Bis(melaminium) sulfate dihydrate. // Acta Crystallogr C. 2001. V. 57. N 12. P. 1431; Bao-Yong Zhu, De-Liang Cui, and Hai-Peng Jing Melaminiurn sulfate // Acta Crystallogr Sect. E. 2008. V. 64. N 2. P. o351), уксусной (Perpetuo GJ1, Janczak J. Melaminiurn acetate acetic acid solvate monohydrate. // Acta Crystallogr C. 2002 V. 58. N 2. P. oll2-4), трифтор- и трихлоруксусной (Perpetuo GJ1, Janczak J. Two crystals of doubly protonated melaminiurn salts: melaminiurn bis(trifluoroacetate) trihydrate and melaminiurn bis(trichloroacetate) dihydrate // Acta Crystallogr C. 2006. V. 62. №7. P. o372), иодистоводородной (Min Min Zhao and Ping Ping Shi Melaminiurn iodide monohydrate //Acta Crystallogr Sect. E. 2010. V. 66. N 6. Р. о1415), хлорной (Min Min Zhao and Ping Ping Shi. Melaminium perchlorate monohydrate // Acta Crystallogr Sect E. 2010. V. 66. N 6. P. o1463) и другими кислотами.
GJ. Bis(melaminium) sulfate dihydrate. // Acta Crystallogr C. 2001. V. 57. N 12. P. 1431; Bao-Yong Zhu, De-Liang Cui, and Hai-Peng Jing Melaminiurn sulfate // Acta Crystallogr Sect. E. 2008. V. 64. N 2. P. o351), уксусной (Perpetuo GJ1, Janczak J. Melaminiurn acetate acetic acid solvate monohydrate. // Acta Crystallogr C. 2002 V. 58. N 2. P. oll2-4), трифтор- и трихлоруксусной (Perpetuo GJ1, Janczak J. Two crystals of doubly protonated melaminiurn salts: melaminiurn bis(trifluoroacetate) trihydrate and melaminiurn bis(trichloroacetate) dihydrate // Acta Crystallogr C. 2006. V. 62. №7. P. o372), иодистоводородной (Min Min Zhao and Ping Ping Shi Melaminiurn iodide monohydrate //Acta Crystallogr Sect. E. 2010. V. 66. N 6. Р. о1415), хлорной (Min Min Zhao and Ping Ping Shi. Melaminium perchlorate monohydrate // Acta Crystallogr Sect E. 2010. V. 66. N 6. P. o1463) и другими кислотами.
Вышеуказанные соли получают взаимодействием МА с соответствующими кислотами в водных средах или взаимодействием меламина в отсутствии растворителя, например, с циануровой кислотой (Пат. США, US 5493023, опубл. 20.02.1996), борной, фосфорной и циануровой кислотами (Пат. РФ №2292341, опубл. 27.01. 2007).
Недостатком вышеуказанных солей является их низкая эффективность в качестве энергоемких соединений, о чем свидетельствуют перспективные области их практического использования.
Выполненный анализ научно-технических и патентных источников информации показал, что заявляемое соединение полугидрат додекагидро-клозо-додекабората меламина (C3H6N6H)2B12H12⋅0,5H2O в уровне техники на настоящий момент не выявлено, соответственно, его синтез и свойства не описаны. В результате проведенных исследований полученного вещества (химический анализ, рентгенофазовый анализ, ИК-спектроскопия, термогравиметрия) установлен состав и изучены свойства нового вещества. Показано, что соединение обладает низкой растворимостью в воде, близкой к растворимости исходного МА (0,5 г в 100 г воды при 20°С). Термогравиметрические исследования показали, что соединение начинает обезвоживаться в интервале 180-190°С. Окисление при нагревании на воздухе начинается при температуре порядка 250°С.
Полугидрат додекагидро-клозо-додекабората меламина (C3H6N6H)2B12H12⋅0,5H2O получают взаимодействием меламина с додекагидро-клозо-додекаборатной кислотой в водной среде согласно стехиометрии следующего уравнения реакции:
2C3H6N6+H2B12H12+0,5Н2О=(C3H6N6H)2B12H12⋅0,5H2O
Полученный осадок малорастворимого полугидрата додекагидро-клозо-додекабората меламина (C3H6N6H)2B12H12⋅0,5H2O отделяют от раствора и сушат при температуре не выше 180°С.
В этом случае целевой продукт полугидрат додекагидро-клозо-додекабората меламина (C3H6N6H)2B12H12⋅0,5H2O теоретически будет иметь максимальную чистоту и максимальную энергоемкость. Соответственно энергетические конденсированные системы (ЭКС), например, пороха, пиротехнические составы и др., приготовленные на основе (C3H6N6H)2B12H12⋅0,5H2O (полученного по стехиометрии), теоретически также будут иметь максимальную энергоемкость.
Однако поскольку (C3H6N6H)2B12H12⋅0,5H2O мало растворим в воде, как сам меламин, предпочтительно использовать небольшой избыток кислоты (по сравнению со стехиометрией реакции), который легко отделить от малорастворимого целевого соединений.
Это достигается при оптимальном мольном соотношении C3H6N6 к Н2 В12Н12, равном (1,8-1,9) к 1. В этом случае для повышения выхода целевого соединения и полноты использования достаточно дорогой кислоты Н2В12Н12 полученный осадок малорастворимого полугидрата додекагидро-клозо-додекабората меламина (C3H6N6H)2B12H12⋅0,5H2O после отделения фильтрованием от маточного раствора, промывают свежей порцией воды и сушат, а фильтрат, содержащий избыток кислоты и промывные воды, объединяют и используют в обороте. Меньшее соотношение (больший избыток кислоты) не сказывается на выходе и чистоте целевого соединения.
Экспериментально установлено, что при соотношении C3H6N6 к H2B12H12 больше 1,9 (например, 1,95-2,0) возникает опасность загрязнения целевого продукта исходным меламином вследствие, например, неточности дозировки компонентов. Кроме того, в этом случае требуется непозволительно длительное время для вовлечения последних молекул кислоты в реакцию с меламином. Поэтому целесообразно не работать с такими соотношениями. При соотношении C3H6N6 к Н2В12Н12 больше стехиометрического целевой (C3H6N6H)2B12H12⋅0,5H2O тем более будет загрязнен исходным меламином, что приведет к снижению его выхода и энергоемкости, т.е. снижению энергетических характеристик. Использование такого низкокачественного (C3H6N6H)2B12H12⋅0,5H2O как энергоемкого компонента в составе ЭКС также возможно, но при этом будут ухудшены энергетические характеристики ЭКС.
Кроме того, гетерофазные реакции быстрее и полнее проходят при повышенной температуре. Известно, что растворимость меламина существенно возрастает при нагревании (с 0,5% при 20°С, до 4% при 90°С). Оптимальная температура синтеза целевого продукта составляет 70-80°С. При меньшей температуре снижается скорость растворения МА и его последующего протонирования кислотой Н2В12Н12, что требует увеличения времени синтеза. При большей температуре возможен гидролиз Н2В12Н12, что приводит к потере этой дорогостоящей кислоты. Улучшает условия синтеза также перемешивание, в результате которого растворяющиеся в воде молекулы меламина быстрее покидают приграничную зону вблизи твердой поверхности и вступают в реакцию с молекулами кислоты. При проведении процесса без активного перемешивания трудно растворимое целевое соединение может отлагаться на поверхности твердого меламина и мешать подходу новых молекул кислоты к нижележащим слоям меламина, т.е. существенно затрудняются диффузионные процессы на межфазной границе твердое - раствор.
Техническим результатом заявляемого изобретения является получение нового химического энергоемкого соединения на основе 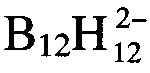 -аниона с высокой термической устойчивостью из доступного исходного сырья. Дополнительным результатом заявляемого изобретения является расширение арсенала средств аналогичного назначения.
-аниона с высокой термической устойчивостью из доступного исходного сырья. Дополнительным результатом заявляемого изобретения является расширение арсенала средств аналогичного назначения.
При реализации способа-прототипа додекагидро-клозо-додекаборат полиэтиленимина прочно прилипает ко дну, что требует предварительного перенесения его на фторопластовую пластину. Заявляемое соединение образуется в виде легко фильтруемого осадка, что упрощает его выделение в виде тонкодисперсного порошка.
По сравнению со способами получения некоторых солей МА, заявляемый способ не требует сложного специального оборудования (механического реактора шнекового типа, цилиндрического двухлопастного смесителя) и применения повышенной температуры, вплоть до 250°С (Патент США, US 5493023, опубл. 20.02.1996, пат. РФ №2292341, опубл. 27.01.2007).
По данным рентгенофазового анализа соединение содержит собственный набор отражений, не принадлежащих исходным компонентам, что подтверждает образование соединения, а не физической (механической смеси).
О вхождении боргидридного аниона в состав целевого соединения говорит наличие полосы поглощения в области 2490 см-1, характеризующей валентные колебания В-Н-связи боргидридного аниона 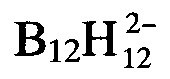 на фоне основных полос поглощения МА.
на фоне основных полос поглощения МА.
Химический анализ целевого соединения на 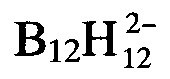 -анион осуществляли по стандартной методике (Кузнецов Н.Т., Куликова Л.Н., Канаева О.А. // Журн. аналит. химии. 1976. Т. 31. N 7. С. 1382-1383). Для этого навеску вещества разлагали в щелочной среде, осаждали из полученного раствора нерастворимый Ag2B12H12 и рассчитывали содержание полиэдрического аниона в соединении.
-анион осуществляли по стандартной методике (Кузнецов Н.Т., Куликова Л.Н., Канаева О.А. // Журн. аналит. химии. 1976. Т. 31. N 7. С. 1382-1383). Для этого навеску вещества разлагали в щелочной среде, осаждали из полученного раствора нерастворимый Ag2B12H12 и рассчитывали содержание полиэдрического аниона в соединении.
Изобретение иллюстрируется следующими примерами.
Пример 1. 5,6133 г 99,0%-ного меламина, содержащего 5,5572 г (44,05 мг-моль) C3H6N6, вносят в стакан со 100 мл воды и добавляют к полученной дисперсии меламина 10 мл раствора, содержащего 3,5203 г (24,47 мг-моль) Н2В12Н12, что соответствует их мольному соотношению 1,8 к 1. Смесь интенсивно перемешивают с помощью магнитной мешалки при температуре 70°С в течение 6 ч. Образовавшийся раствор, сконцентрированный до ~50 мл в ходе перемешивания при 70°С, охлаждают до комнатной температуры и отфильтровывают осадок от маточного раствора на предварительно взвешенном стеклянном пористом фильтре под разрежением, создаваемым водоструйным насосом. Для удаления небольшого избытка кислоты в фильтр с осадком заливают 20 мл дистиллированной воды и фильтруют также под разрежением, создаваемым водоструйным насосом. Затем фильтр с отжатым осадком сушат при 105°С до постоянного веса.
В результате получают 8,5763 г белого продукта, что соответствует 96,1%-ному выходу (C3H6N6H)2B12H12⋅0,5H2O. Пониженный выход связан с потерями целевого соединения с маточным и промывным растворами. Для повышения выхода (C3H6N6H)2B12H12⋅0,5H2O и полноты использования H2B12H12 маточный и промывной растворы объединяют и используют в обороте для последующих синтезов целевого соединения.
Вычислено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%:  - 35,01.
- 35,01.
Найдено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%: 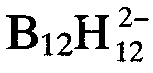 - 34,84.
- 34,84.
Чистота целевого соединения 99.5%.
Пример 2. 6,6630 г 99,0%-ного меламина, содержащего 6,5964 г (52,29 мг-моль) C3H6N6, вносят в стакан со 100 мл воды и добавляют к полученной дисперсии меламина 10 мл раствора, содержащего 3,9591 г (27,52 мг-моль) H2B12H12, что соответствует их мольному соотношению 1,9 к 1. Смесь интенсивно перемешивают с помощью магнитной мешалки при температуре 80°С в течение 5 ч. Образовавшийся раствор, сконцентрированный до ~50 мл в ходе перемешивания при 80°С, охлаждают до комнатной температуры и отфильтровывают осадок от маточного раствора на предварительно взвешенном стеклянном пористом фильтре под разрежением, создаваемым водоструйным насосом. Для удаления небольшого избытка кислоты в фильтр с осадком заливают 20 мл дистиллированной воды и фильтруют также под разрежением, создаваемым водоструйным насосом. Затем фильтр с отжатым осадком сушат при 105°С до постоянного веса. В результате получают 10,1432 г белого продукта, что соответствует 95,8%-ному выходу полугидрата додекагидро-клозо-додекабората меламина (C3H6N6H)2B12H12⋅0,5H2O. Пониженный выход связан с потерями целевого соединения с маточным и промывным растворами. Для повышения выхода (C3H6N6H)2B12H12⋅0,5H2O и полноты использования H2B12H12 маточный и промывной растворы объединяют и используют для последующих синтезов целевого соединения.
Вычислено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%: 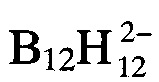 - 35,01.
- 35,01.
Найдено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%:  - 34,84.
- 34,84.
Чистота целевого соединения 99.5%.
Пример 3. 5,0116 г 99,0%-ного меламина, содержащего 4,9615 г (39,33 мг-моль) C3H6N6, вносят в стакан со 100 мл воды и добавляют к полученной дисперсии 10 мл раствора кислоты, содержащего 3,2325 г (22,47 мг-моль) H2B12H12, что соответствует их мольному соотношению 1,75 к 1. Смесь интенсивно перемешивают с помощью магнитной мешалки при температуре 60°С в течение 5 ч. Образовавшийся раствор, сконцентрированный до ~50 мл в ходе перемешивания при 60°С, охлаждают до комнатной температуры и отфильтровывают осадок от маточного раствора на предварительно взвешенном стеклянном пористом фильтре под разрежением, создаваемым водоструйным насосом. Для удаления небольшого избытка кислоты в фильтр с осадком заливают 20 мл дистиллированной воды и фильтруют также под разрежением, создаваемым водоструйным насосом. Затем фильтр с отжатым осадком сушат при 105°С до постоянного веса. В результате получают 7,6490 г белого продукта, что соответствует 96,0%-ному выходу (C3H6N6H)2B12H12⋅0,5H2O. Пониженный выход связан с потерями целевого соединения с маточным и промывным растворами. Для повышения выхода (C3H6N6H)2B12H12⋅0,5H2O и полноты использования H2B12H12 маточный и промывной растворы объединяют и используют для последующих синтезов целевого соединения.
Вычислено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%: 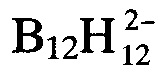 - 35,01.
- 35,01.
Найдено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%: 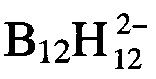 - 34,86.
- 34,86.
Чистота целевого соединения 99.6%.
Пример 4. 4,9920 г 99,0%-ного меламина, содержащего 4,9420 г (39,20 мг-моль) C3H6N6, вносят в стакан со 100 мл воды и добавляют к полученной дисперсии 10 мл раствора, содержащего 2,8916 г (20,10 мг-моль) H2B12H12, что соответствует их мольному соотношению 1,95 к 1 и проводят перемешивание смеси при 80°С в течение 8 ч. Образовавшийся раствор, сконцентрированный до ~50 мл в ходе перемешивания при 80°С, охлаждают до комнатной температуры и отфильтровывают осадок от маточного раствора на предварительно взвешенном стеклянном пористом фильтре под разрежением, создаваемым водоструйным насосом. Для удаления небольшого избытка кислоты в фильтр с осадком заливают 20 мл дистиллированной воды и фильтруют также под разрежением, создаваемым водоструйным насосом. Затем фильтр с отжатым осадком сушат при 105°С до постоянного веса. В результате получают 7,2618 г белого продукта, что соответствует 91,5%-ному выходу (C3H6N6H)2B12H12⋅0,5H2O.
Пониженный выход связан с неполным переходом меламина в целевое соединение, а также потерями целевого соединения с маточным и промывным растворами. Для повышения выхода (C3H6N6H)2B12H12⋅0,5H2O и полноты использования Н2В12Н12 маточный и промывной растворы объединяют и используют для последующих синтезов целевого соединения.
Вычислено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%:  - 35,01.
- 35,01.
Найдено для (C3H6N6H)2B12H12⋅0,5H2O, вес.%: 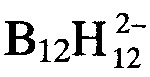 -34,16.
-34,16.
Чистота целевого соединения составляет 97.6%.
Как следует из примера 3 при уменьшении мольного соотношения МА к H2B12H12 выход продукта практически не увеличивается по сравнению с примером 1 и 2, в которых компоненты взяты в оптимальном соотношении. Однако использование большего избытка кислоты ведет к перерасходу дорогостоящей кислоты. При мольном соотношении МА к H2B12H12 больше оптимального (1,95 к 1, пример 4), заметно снижается выход (с ~96% в примерах 1-3 до 91,5%) и чистота целевого соединения (97,6% по сравнению с 99,5% в примерах 1 и 2 и 99,6% в примере 3), несмотря на оптимальную температуру и увеличенное время синтеза.

