Результат интеллектуальной деятельности: Способ определения формальдегида в моче методом газохроматографического анализа
Вид РИД
Изобретение
Изобретение относится к области медицины, в частности к медицинским, токсикологическим исследованиям, и может быть использовано при диагностике экологически обусловленной патологии, вызванной формальдегидом, в лабораториях биохимии, специализированных учреждениях и клинико-диагностических лабораториях медицинских учреждений.
Известный способ определения формальдегида, а также и других альдегидов основан на дериватизации 2,4-динитрофенилгидразином (ДНФГ) в кислой среде, экстракцией гексаном с последующим упариванием экстракта до сухого остатка и реэкстракции ацетонитрилом [МУК 4.1.2110 - 06. Определение вредных веществ в биологических средах. Сборник методических указаний. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2008. С. 96 - 109]. Анализ ацетонитрильного экстракта осуществляется методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на колонке С18 с ультрафиолетовым (УФ) детектированием. Предел обнаружения составляет 1 мкг/дм3 при объеме пробы 50 см3. К недостаткам данной пробоподготовки можно отнести большой объем пробы, трудоемкость и длительность процедур дериватизации, экстракции, концентрирования экстракта, низкие степени извлечения 2,4-динитрофенилгидразон формальдегида. В литературе нет данных по определению формальдегида в моче методом газовой (газожидкостной) хроматографией с этой же пробоподготовкой.
Среди других дериватизирующих реагентов особое внимание заслуживает фторсодержащее соединение о-замещенного гидроксиламина, а именно о-(2,3,4,5,6-пентафторбензил) гидроксиламин гидрохлорид (ПФБГА). Это соединение используется в качестве дериватизирующего реагента для карбонильных соединений в самых разнообразных биомедицинских и экологических исследованиях [Cancilla D.A, Que Нее S. o-(2,3,4,5,6-pentafluorophenyl)methyl hydroxylamine hydrochloride: a versatile reagent for the determination of carbonyl-containing compounds. // J. Chromatography. -1992. -V. 627. - P. 1-16]. ПФБГА, как гидроксиламин, реагирует с карбонильными функциональными группами с образованием соответствующих оксимов. Образование оксима легко протекает в водных и органических растворах в широком интервале рН. Оксимы легко экстрагируются в органические растворители, и не прореагировавший ПФБГА удаляется через кислотные промывки. Оксимы могут быть разделены с помощью газовой хроматографии (ГХ) с различными детекторами в виде симметричных пиков. Электронно-захватное детектирование (ЭЗД) является особенно чувствительным для определения этих пентафторированных производных.
Существует стандартизованный ЕРА метод определения карбонильных соединений в питьевой воде газожидкостной хроматографией с использованием реагента ПФБГА [Method 556. Determination of carbonyl compounds in drinking water by pentafluorobenzylhydroxylamine derivatization and capillary gas chromatography with electron capture detection. Cincinnati: EPA, 1998. 37 р.]. Суть метода заключается в дериватизации определяемых соединений ПФБГА, экстракции гексаном, промывки экстракта с последующим газохроматографическим анализом на неполярной капиллярной колонке с электронно-захватным детектированием. Недостатком указанного способа является трудоемкость пробоподготовки за счет проведения процедур жидкостной экстракции с последующей промывкой экстракта.
Технической задачей предлагаемого способа является упрощение процедуры пробоподготовки, за счет использования реагента ПФБГА и газохроматографического анализа равновесного пара.
Указанная техническая задача достигается путем обработки пробы 0,1 см3 0,1% водного раствора пентафторбензилгидроксиламина (ПФБГА), нагревания ее в виале вместимостью 20 см3 при 60°С 30 мин и проведении газохроматографического анализа паровой фазы на капиллярной колонке с пламенно-ионизационным детектором.
По сравнению с прототипом в предлагаемом способе пробоподготовка включает обработку пробы реагентом ПФБГА с последующим нагреванием для получения паровой фазы, использование пламенно-ионизационного детектора вместо электронно-захватного детектора.
Из патентной и научно-технической литературы нам не известны способы количественного определения формальдегида в моче, содержащие совокупность предложенных нами признаков, что позволяет сделать вывод о новизне заявляемого технического решения.
Кроме того, из существующего уровня техники нам неизвестно использование существенных признаков, характеризующих предлагаемый способ, для достижения описываемого технического результата.
Краткое описание чертежей.
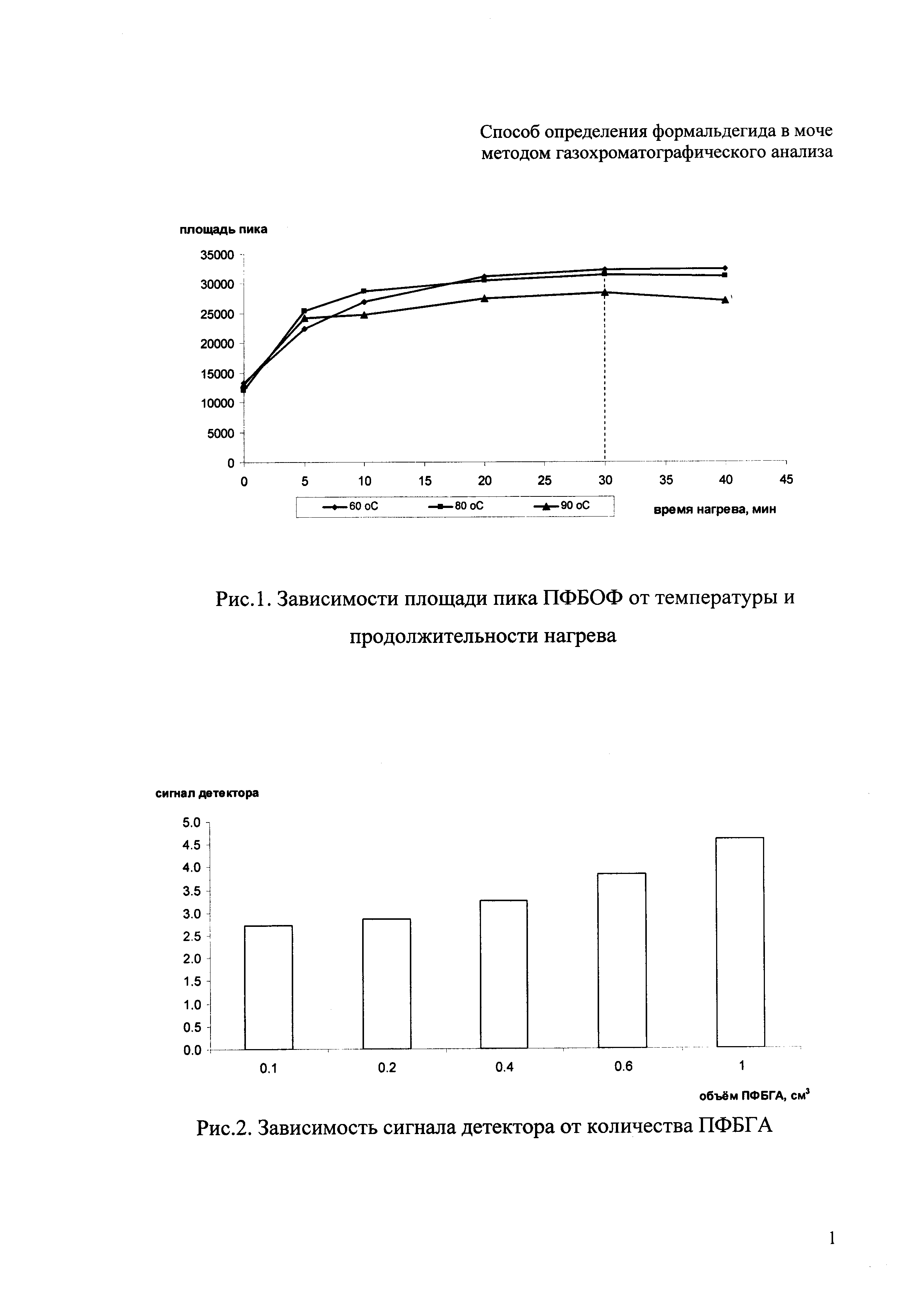
На рисунке 1 приведен график зависимости площади пика ПФБОФ от температуры и продолжительности нагрева. На рисунке 2 приведена диаграмма зависимости сигнала детектора от количества ПФБГА.
На рисунке 3 приведена хроматограмма образца мочи человека. Способ осуществляют следующим образом:
пробу мочи объемом 1 см3 помещают во флакон, вносят 0,1 см3 0,1% водного раствора пентафторбензилгидроксиламина, запечатывают флакон алюминиевой крышкой с тефлоновой мембраной и помещают в парофазный пробоотборник. Отбор перовой фазы и газохроматографический анализ осуществляют в следующих условиях (табл. 1). 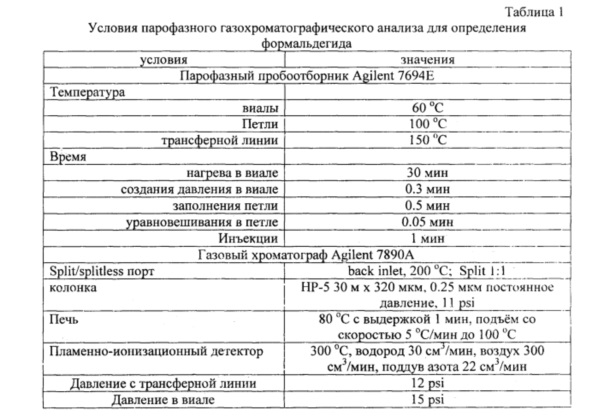
Количественное определение по предлагаемому способу проводят методом абсолютной калибровки по стандартным растворам формальдегида в моче, предварительно обработанным аналогично анализируемым пробам. В связи с тем фактом, что формальдегид присутствует в моче любого человека, градуировочный график не идет от начала координат нуля, поэтому обязательно площадь пика определяемого вещества в моче, используемой для приготовления градуировочного образца, вычитают из площади пика каждого градуировочного образца. Таким путем градуировочный график приводят к началу координат.
Экспериментальным путем получены зависимости площади пика формальдегида от температуры и времени нагрева. Парофазный газохроматографический анализ (ПФА-ГХ) стандартной смеси (1 см3) производного формальдегида (пентафторбензилоксима формальдегида ПФБОФ) в моче с концентрацией 90 мкг/дм3 осуществляли в закрытых флаконах емкостью 20 см3 при однократном отборе паровоздушной фазы (1 см3) с последующим ее газохроматографическим анализом. Зависимость площади пика (сигнал ЭЗД) от продолжительности при разных температурах отражена на рис. 1.
Как показывают кривые, рост площади пика идет с увеличением продолжительности нагрева, зато с ростом температуры от 60 до 90°С площадь пика падает. Таким образом, максимум сигнала наблюдается при следующих оптимальных условиях парофазного извлечения: температура 60°С и продолжительность нагрева 30 мин.
При выборе условий хроматографирования были опробованы капиллярные колонки разной полярности (НР-5-(5% фенил)-метилполисилокеан, HP-INNOWAX-полиэтиленгликоль); различные температурные режимы (изотермический и с программированием температуры), два детектора (пламенно-ионизационный и электронно-захватный). В результате опробования установлено, что оптимальное разделение осуществляется в режиме программирования температуры, а наилучшая чувствительность на ЭЗД. Несмотря на такую высокую чувствительность детектора, хроматографирование о-пентафторбензилоксима формальдегида (ПФБОФ) с ЭЗД дает повышенное содержание его в дериватизирующем реагенте - 0.1% водном растворе ПФБГА. (табл. 2).
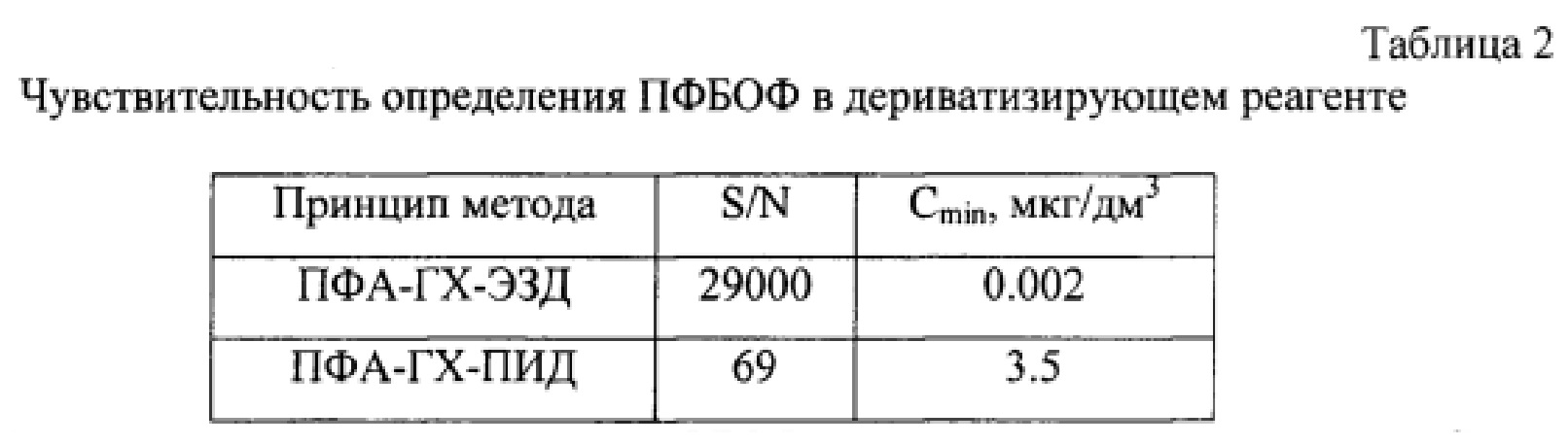
S/N - отношение сигнала к шуму ПФБОФ в дериватизирующем реагенте, Cmin - предел обнаружения.
Как видно из табл. 2, при хроматографировании с пламенно-ионизационным детектором значительно снижается содержание ПФБОФ в дериватизирующем реагенте ПФБГА. Присутствие ПФБОФ в дериватизирующем реагенте объясняется абсорбцией формальдегида из воздушной среды водным раствором ПФБГА, и в результате реакции образуется ПФБОФ, который и дает дополнительный сигнал в исследуемых пробах (градуировочный образец, реальная проба мочи). Это также подтверждается зависимостью сигнала детектора от объема 0.1% водного раствора ПФБГА (рис. 2).
Как видно из зависимости, содержание ПФБОФ растет с увеличением количества дериватизирующего реагента. Поэтому раствор ПФБГА лучше использовать в объеме 0.1 см3 и каждый результат анализа пробы мочи необходимо корректировать содержанием формальдегида в холостом образце (дистиллированная вода + 0.1 см3 0.1% водного раствора ПФБГА), т.е. вычитать его.
Оценены метрологические характеристики способа количественного определения формальдегида в моче: повторяемость, воспроизводимость, правильность (границы неисключенной систематической погрешности) и точность (границы относительной погрешности), представленные в табл. 3.

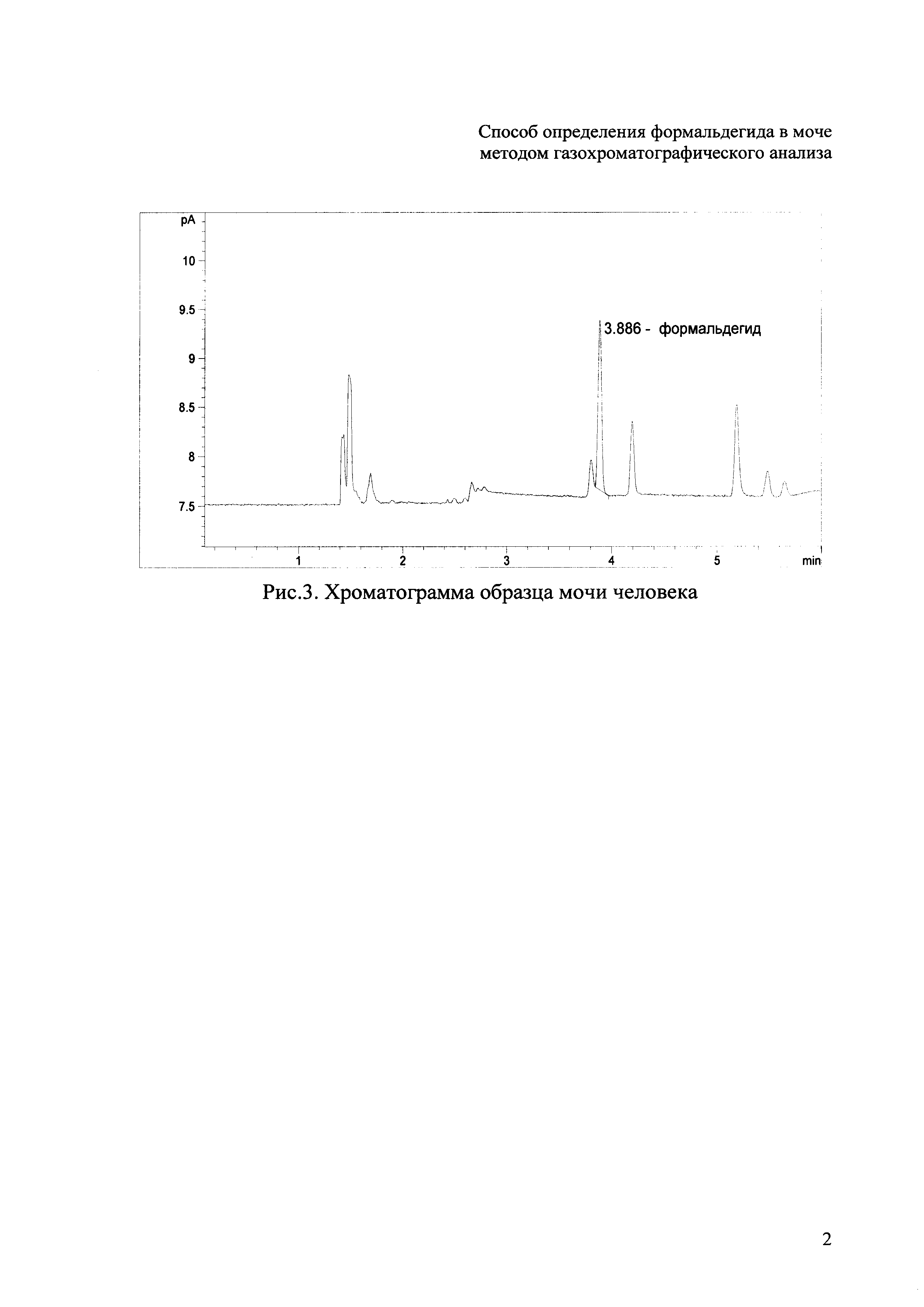
Пример. Брали 1 см3 пробы мочи, помещали во флакон вместимостью 20 см3, вносили 0,1 см3 0,1% водного раствора ПФБГА, запечатывали флакон алюминиевой крышкой с тефлоновой мембраной и помещали в парофазный пробоотборник. Анализ осуществляли в соответствие с табл. 1. На полученной хроматограмме проводили идентификацию определяемого компонента по абсолютному времени удерживания (Рис. 3). Количественный расчет делали по градуировочному графику. Содержание (концентрация) формальдегида в моче корректировали вычетом результата анализа 1 см3 дистиллированной воды с 0.1 см3 0.1% водного раствора ПФБГА. Таким образом, концентрация формальдегида составила 38 мкг/дм3. В других образцах мочи содержание формальдегида лежит в интервале 30-83 мкг/дм3, что намного выше предела обнаружения.
Таким образом, предлагаемым способом с удовлетворительным пределом обнаружения 3.5 мкг/дм3 можно определять формальдегид в моче при использовании малого объема анализируемой проб 1 см3. Применение данного способа позволяет уменьшить продолжительность анализа за счет упрощенной пробоподготовки по сравнению с аналогами. Более дорогой метод высокоэффективной жидкостной хроматографии заменен газохроматографическим анализом равновесного пара.