Результат интеллектуальной деятельности: КОНТРАСТИРУЮЩИЙ АГЕНТ ДЛЯ ВВЕДЕНИЯ ФТОР-19 МЕТКИ В БЕЛКИ, СОДЕРЖАЩИЕ ОСТАТКИ ЛИЗИНА
Вид РИД
Изобретение
Изобретение относится к фармакологии и медицинской диагностике, конкретнее к контрастирующим агентам для введения фтор-19 метки в белки для последующей визуализации процессов фармакокинетики и фармакодинамики белковых препаратов в режиме фтор-19 ЯМР и магнитно-резонансной томографии (МРТ).
Ядерный магнитный резонанс (ЯМР) представляет собой сегодня широко применяемый метод медицинской диагностики, используемый для создания изображения in vivo, с помощью которого можно получить изображение сосудов и тканей тела (включая злокачественные опухоли), замеряя магнитные свойства ядер атомов в жидкости организма.
Исключительно перспективным ядром для ЯМР спектроскопии in vivo и томографических измерений является фтор-19 [Jesus Ruiz-Cabello, Brad P. Barnett, and Jeff W.M. Bulte / Fluorine (19F) MRS and MRI in biomedicine // NMR Biomed., 2011, 24(2), 114-129]. Он имеет почти такой же большой магнитный момент (40 МГц/Тл), как и протон (42,6 МГц/Тл), и его природное содержание составляет 100%. Ядер 19F в живых организмах практически нет, однако возможности реализовать томографию на ядрах фтор-19 (19F-МРТ) появляются благодаря особым свойствам фторорганических соединений, в которых с углеродом вместо атомов водорода связаны атомы фтора. Вещества, имеющие перфторированный радикал, применяются в МРТ для распознавания различных физиологических и патофизиологических структур и, таким образом, для улучшения диагностической информации, например, местоположения заболевания, для выбора и оценки результата направленной терапии и для профилактики заболеваний и расстройств.
В качестве агентов для МРТ по сигналу 19F широко используются эмульсии перфторуглерода [Díaz-López R, Tsapis N, Fattal E. Liquid perfluorocarbons as contrast agents for ultrasonography and (19)F-MRI // Pharm Res. 2010. V. 1. P. 1-16]. Однако эти препараты обладают серьезными недостатками: они гетерогенны, нестабильны, имеют расщепленные сигналы в спектрах 19F-MPT и, что наиболее важно, они могут задерживаться в различных тканях и органах на продолжительное (иногда месяцы) время.
Перечисленные недостатки агентов на основе перфторуглерода могут быть преодолены при условии использования в качестве контрастирующих агентов ковалентных или нековалентных комплексов фторсодержащих соединений, желательно с единичным сигналом 19F от множественных атомов фтора, с белками.
Так, например, в патентной заявке WO 2003045441, опубл. 05.06.2003 для in vivo для визуализации ферментативной активности используют конъюгаты субстратов различных ферментов, аномальная активность которых связана с конкретными заболеваниями, с соединениями, содержащими перфторалкильную или перфторарильную группу.
В заявке WO 2014135590, опубл. 12.09.2014, предложен универсальный реагент для визуализации биомолекул, в том числе для нужд тераностики, представляющий собой металлоцен, с обогащенными атомами фтора лигандами и линкерной группой для присоединения металлоцена к биополимерам. Визуализация может осуществляться как за счет атомов 19F, так и 18F или любого другого подходящего радионуклида, который может формировать металлоцен.
В заявке WO 2014041150, опубл. 12.09.2014, также предложен универсальный реагент для визуализации, состоящий из наночастиц сополимера молочной и гликолевой кислот, включающих полифторированные краунэфиры и комплексы гадолиния.
Однако для таких реагентов характерно «вымывание» ионов металлов из металлокомплексов, что, с одной стороны, повышает токсичность таких реагентов, а с другой стороны, приводит к расщеплению сигналов от атомов фтора и, в конечном итоге, к снижению чувствительности. Кроме того, реагенты, описанные в приведенных выше примерах, перед присоединением к белкам нуждаются в дополнительной активации.
Ближайшим к заявляемому контрастирующему агенту - прототипом, является контрастирующий агент на основе трифторацетилированного производного тиолактона гомоцистеина для введения в белки фтор-19 метки (19F). Реагент не требует предварительной активации и имеет единичный сигнал от трех атомов фтора -CF3 группы [A.S. Chubarov et. al. Bioorgan. Med. Chem. Lett. (2011) V. 21. P. 4050-4053]. Однако присоединение фтор-метки через трифторацетамидную связь делает такой реагент не достаточно устойчивым.
Задачей изобретения является получение нового контрастирующего агента, содержащего для увеличения интенсивности сигнала более одной CF3 группы, не содержащего нестабильной трифторацетамидной связи и не требующего для мечения белков предварительной активации.
Технический результат: повышение качества и стабильности контрастирующего агента.
Поставленная задача достигается предлагаемым контрастирующим агентом на основе фторпроизводного тиолактона гомоцистеина для введения фтор-19 метки в белки, содержащие в своем составе остатки лизина.
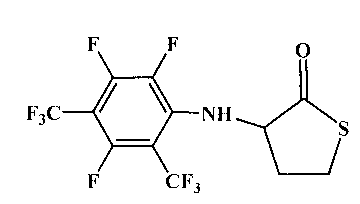
Заявляемый контрастирующий агент представляет собой N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)-тиолактон гомоцистеина со следующей структурной формулой (I):

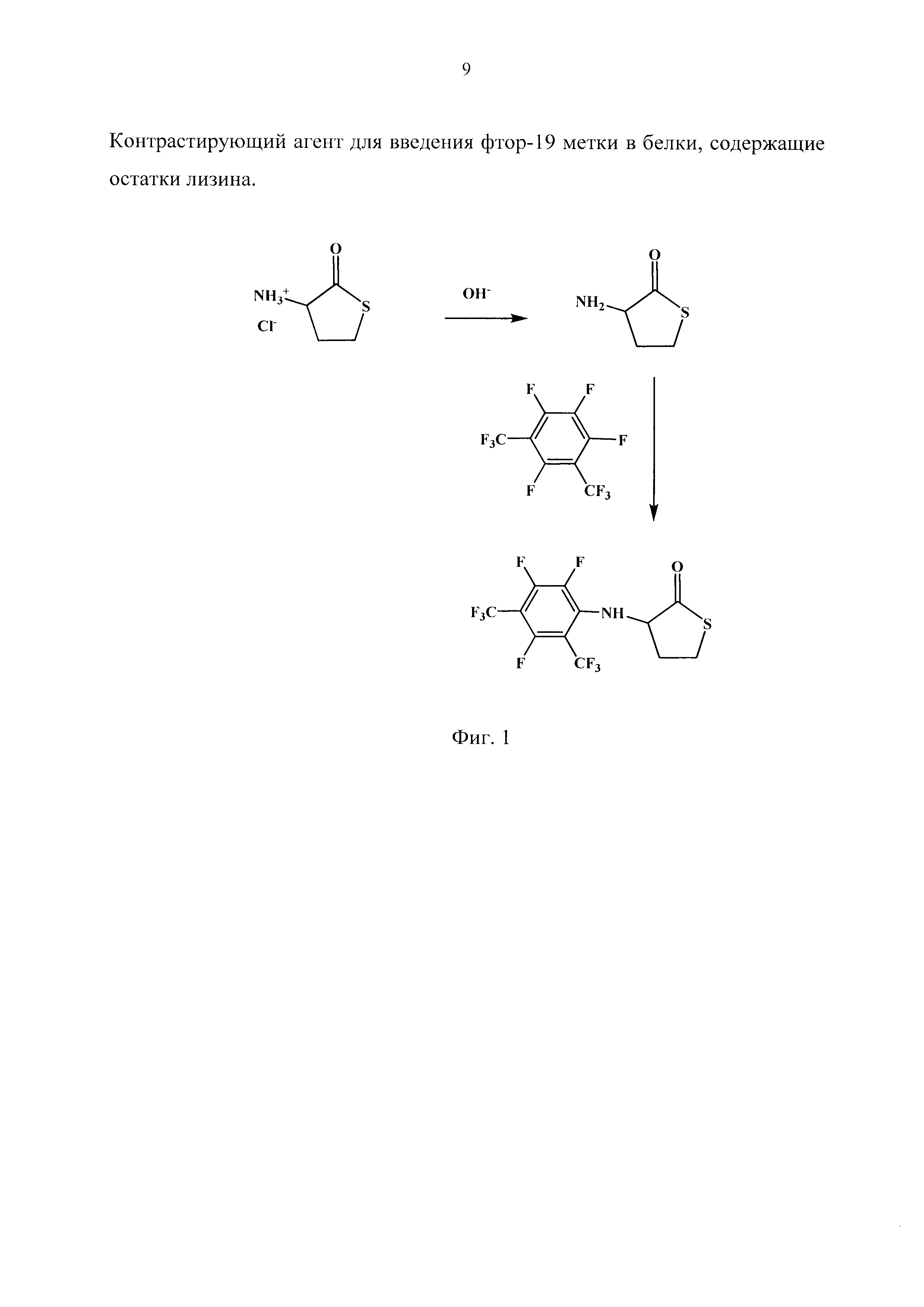
Способ получения заявляемого контрастирующего агента заключается в следующем (на фиг. 1 представлена общая схема его синтеза).
Исходную смесь оптических изомеров гидрохлорида тиолактона гомоцистеина (DL-гидрохлорид тиолактона гомоцистеина) переводят в основание 0,25 М раствором карбонатного буфера (pH 10,5) с последующей экстракцией свободного основания тиолактона гомоцистеина этилацетатом и последующим удалением органического растворителя на ротационном испарителе. Полученное свободное основание тиолактона сразу растворяют в диметилсульфоксиде (ДМСО) и добавляют эквивалентное количество м-перфторксилола и перемешивают на магнитной мешалке в течение 16 ч при 25°C. Целевой продукт осаждают из реакционной смеси водой, осадок отделяют центрифугированием. После двухкратной промывки осадка водой осадок высушивают в вакууме. Выход целевого продукта составляет 93,4-95,1%.
Полученный реагент отличается большей стабильностью, позволяет вводить в человеческий сывороточный альбумин до 6 трифторметильных групп на одну молекулу белка, не нуждаются в дополнительной активации перед присоединением к белкам.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Получение N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)-тиолактон гомоцистеина.
К 20,4 мг DL-гидрохлориду тиолактона гомоцистеина добавляют 0,5 мл 0,25 М карбонатного буфера (pH 10,5), перемешивают в течение 40 секунд при комнатной температуре. Полученное свободное основание тиолактона гомоцистеина экстрагируют 10 мл этилацетата с последующим удалением органического растворителя на ротационном испарителе. Продукт сразу используется для следующей стадии синтеза ввиду его нестабильности.
К 15 мг свободного основания тиолактона гомоцистеина (tHcy) (0,128 ммоль) добавляют 0,6 мл ДМСО и 8,1 мкл м-перфторксилола. Перемешивают в течение 16 ч при 25°C. К реакционной смеси добавляют 0,6 мл дистиллированной воды и центрифугируют до полного осаждения осадка, декантируют. К осадку приливают 0,4 мл воды, интенсивно перемешивают в течение 5 мин, центрифугируют, декантируют. Процедуру повторяют еще один раз. Выход целевого продукта составляет 95,1% в виде светло-желтого твердого вещества. 19F ЯМР (CD3CN, δ, м.д., J, Гц): 108,78 (д, 3F, CF3(1)), 108,17 (т, 3F, CF3(2)), 45,18 (м, 1F, F-3a), 31,60 (м, 1F, F-5a), 7,91 (м, 1F, F-6а), JCF3(1),3a=30,9, JCF3(1),5a=3,6, JCF3(2),3a=JCF3(2),5a=22,3, J3a,5a=2,6, J3a,6a=10,0, J5a,6a=18,0, JNH,6a=2,0. 1H ЯМР (DMSO-d6, δ, м.д., J, Гц): 6,52 (ш. д, 1H, NH), 4,71 (м, 1H, H-3), 3,43 (м, 1H, H-5′), 3,31 (м, 1H, H-5), 2,76 (м, 1H, H-4′), 2,26 (м, 1H, H-4), J3,4=12,8, J3,4′=7,0, J3,5=0,5, J3,NH=8,4, J4,4′=12,2, J4,5=7,0, J4,5′=12,2, J4′,5=1,3, J4′,5′=5,3, J5,5′=11,5, J4,NH=2,0, J4′,NH=1,0. 13C ЯМР (CD3CN, δ, м.д., J, Гц): 207,2 (CO), 155,0 (C-3a), 141,6 (C-5a), 140,7 (C-6a), 138,3 (C-1a), 125,8 (CF3), 124,4 (CF3), 123,1 (C-4a), 121,6 (C-2a), 66,2 (C-3), 33,4 (C-5,5′), 28,0 (C-4,4′). ESI MS (m/z) рассч. C12H5NOSF9 [M-H]: 381.995, найдено 381.896. УФ-спектр (CH3CN), λmax/нм (ε, M-1 см-1): 296 ((6,0±0,1)×103), 255 ((1,3±0,1)×104), 325 ((1,9±0,1)×103).
Пример 2.
Получение N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)-тиолактон гомоцистеина.
К 204 мг DL-гидрохлориду тиолактона гомоцистеина добавляют 5 мл 0,25 М карбонатного буфера (pH 10,5), перемешивают в течение 2 мин. при комнатной температуре. Полученное свободное основание тиолактона гомоцистеина экстрагируют 3×40 мл этилацетата с последующим удалением органического растворителя на ротационном испарителе. Продукт сразу используется для следующей стадии синтеза ввиду его нестабильности.
К 150 мг свободного основания tHcy (1,28 ммоль) добавляют 6 мл ДМСО и 81 мкл м-перфторксилола. Перемешивают в течение 16 ч при 25°C. К реакционной смеси добавляют 6 мл дистиллированной воды и центрифугируют до полного осаждения осадка, декантируют. К осадку приливают 5 мл воды, интенсивно перемешивают в течение 5 мин, центрифугируют, декантируют. Процедуру повторяют еще один раз. Выход: 93,4% в виде светло-желтого твердого вещества.
Пример 3.
Взаимодействие N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)-тиолактон гомоцистеина с человеческим сывороточным альбумином.
Человеческий сывороточный альбумин 66,5 мг растворяют в 1 мл фосфатного буферного раствора (PBS), добавляют 109 мкл 29,4 мМ раствора N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил) тиолактона гомоцистеина в ДМСО и инкубируют при 37°C в течение 18 ч. После инкубации реакционную смесь очищают от низкомолекулярных веществ с помощью концентраторов «Centricon» (Amicon Centriprep YM30, Millipore, Bedford) при 9000 g. Для этого раствор белка концентрируют до минимально возможного объема (~0,2 мл), добавляют буфер PBS (0,4 мл×4), а затем воду (0,4 мл×6), после добавления каждой порции буфера или воды раствор концентрируют. Затем порции раствора человеческого сывороточного альбумина раскапывают по пробиркам порциями по 0,2 мл, упаривают досуха на вакуумной центрифуге Speed Vac при 30°C и хранят при -20°C. УФ-спектр (буфер PBS pH 7,4), λmax/нм: 259, 278, 300. 19F ЯМР (pH 7,4, буфер PBS): δ 109,3 (м, 3F, CF3(1)), 108,5 (м, 3F, CF3(2)), 47,0 (м, 1F, F-3a), 33,8 (м, 1F, F-5a), 4,0 (м, 1F, F-6а). Выход модифицированного белка составляет ~95%. С использованием 5,5′-дитиобис(2-нитробензойной кислоты) было показано, что на одну молекулу белка в среднем приходится 3,0±0,1 остатка N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)гомоцистеина. Молярная масса конъюгата, по данным MALDI-TOF масс-спектрометрии, составила 67,6 кг/моль (что соответствует присоединению 3 остатков N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)гомоцистеина).
С помощью метода гель-электрофореза (SDS-PAGE) было показано отсутствие образования высокомолекулярных агломератов и соответствие полос белка нативному человеческому сывороточному альбумину.
Использование предлагаемого контрастирующего агента позволит увеличить чувствительность метода ЯМР спектроскопии за счет увеличения на одну молекулу белка числа CF3 групп, дающих единичный сигнал и повышения стабильности метки за счет исключения из реагента лабильной трифторацетамидной группы.
Контрастирующий агент для введения фтор-19 метки в белки, содержащие остатки лизина, представляющий собой N-(2,3,5-трифтор-4,6-бис(трифторметил)фенил)-тиолактон гомоцистеин со следующей структурной формулой (I):