Результат интеллектуальной деятельности: ИНТРАВАГИНАЛЬНОЕ ВВЕДЕНИЕ МИЗОПРОСТОЛА
Вид РИД
Изобретение
Область изобретения
Данное изобретение в целом относится к интравагинальному введению мизопростола беременным субъектам женского пола.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
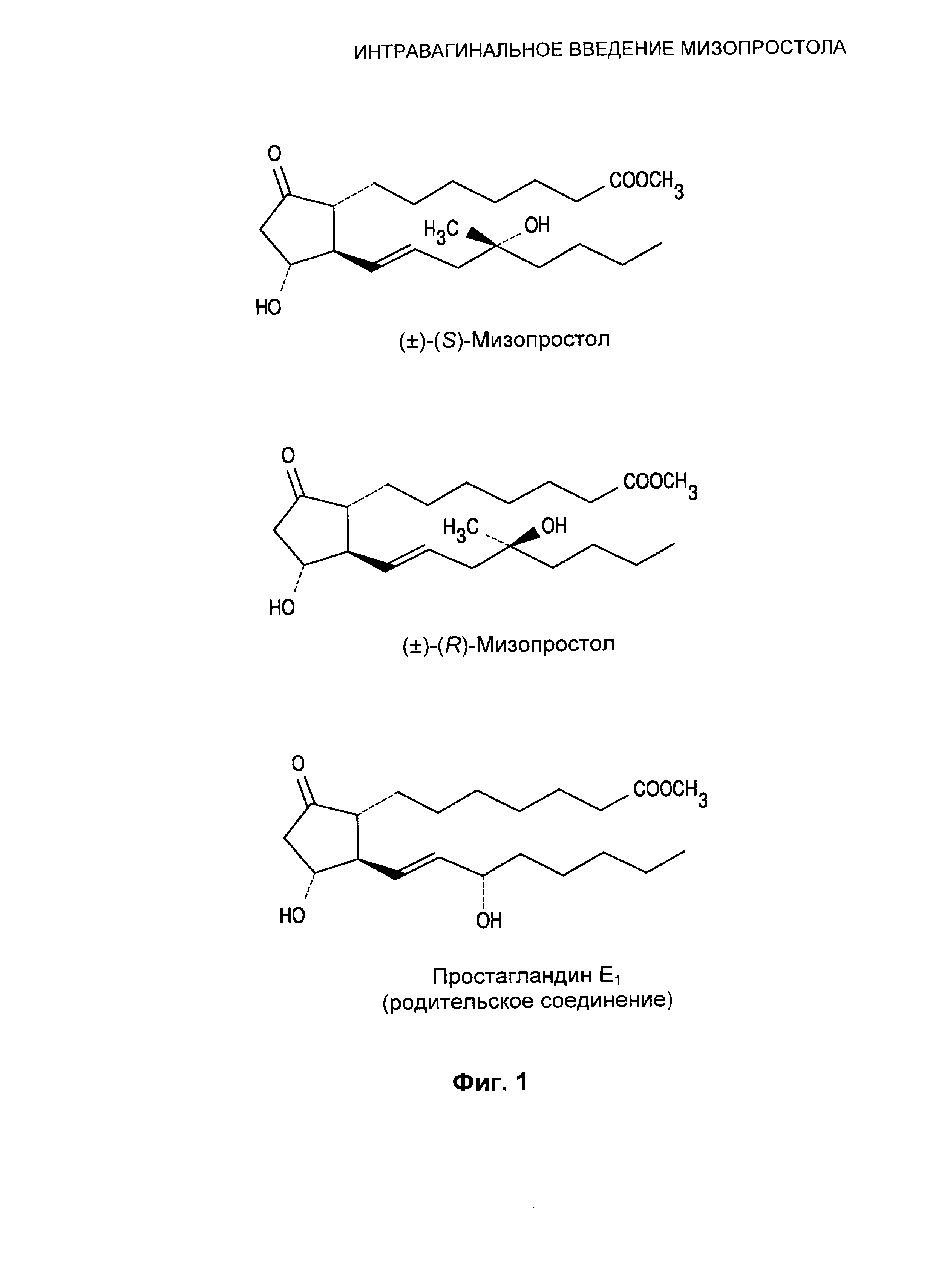
Фиг.1 иллюстрирует структуру мизопростола и родительского соединения.
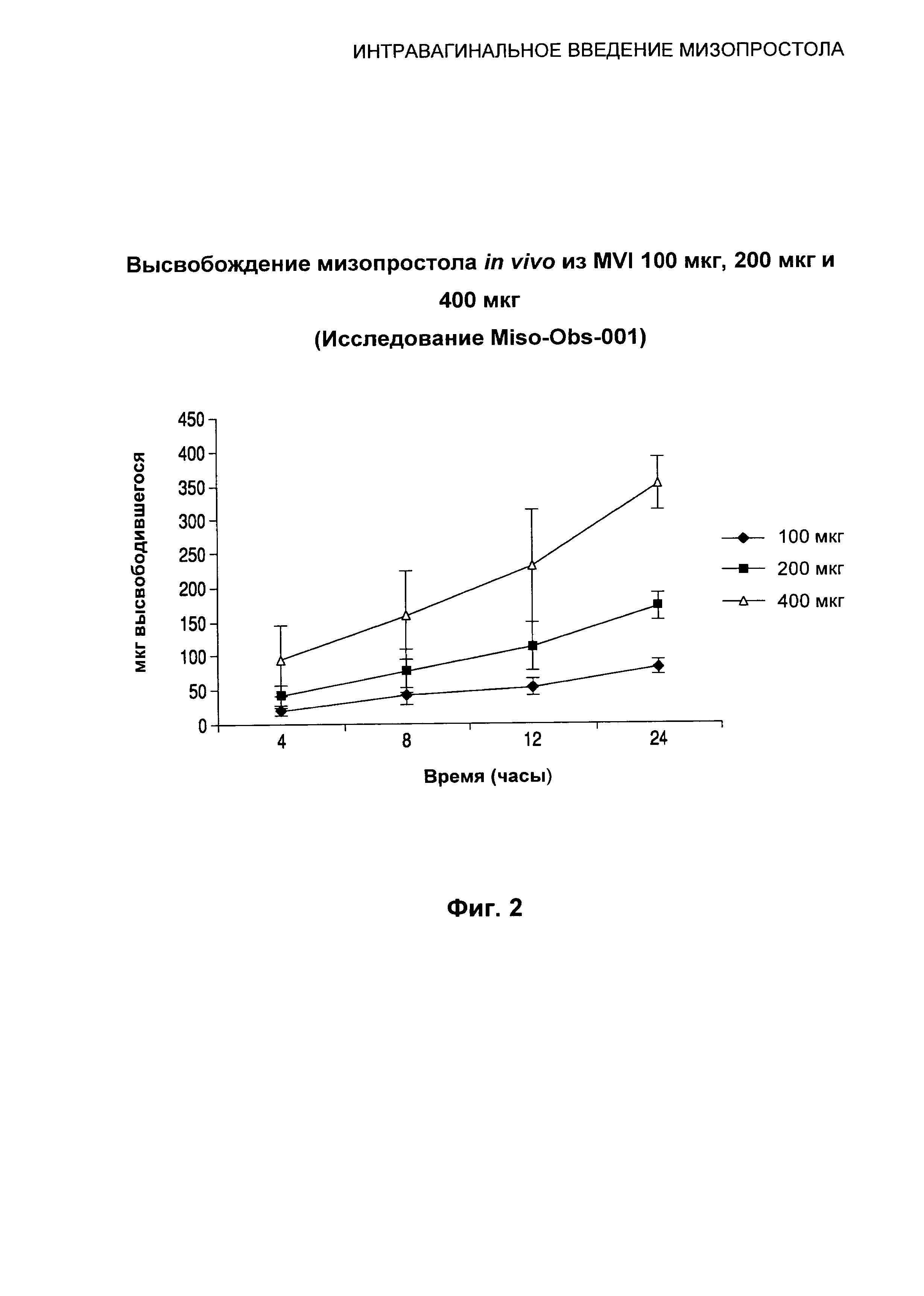
Фиг.2 иллюстрирует высвобождение мизопростола in vivo из вагинального вкладыша с содержанием мизопростола 100 мкг, 200 мкг и 400 мкг у небеременных субъектов женского пола.
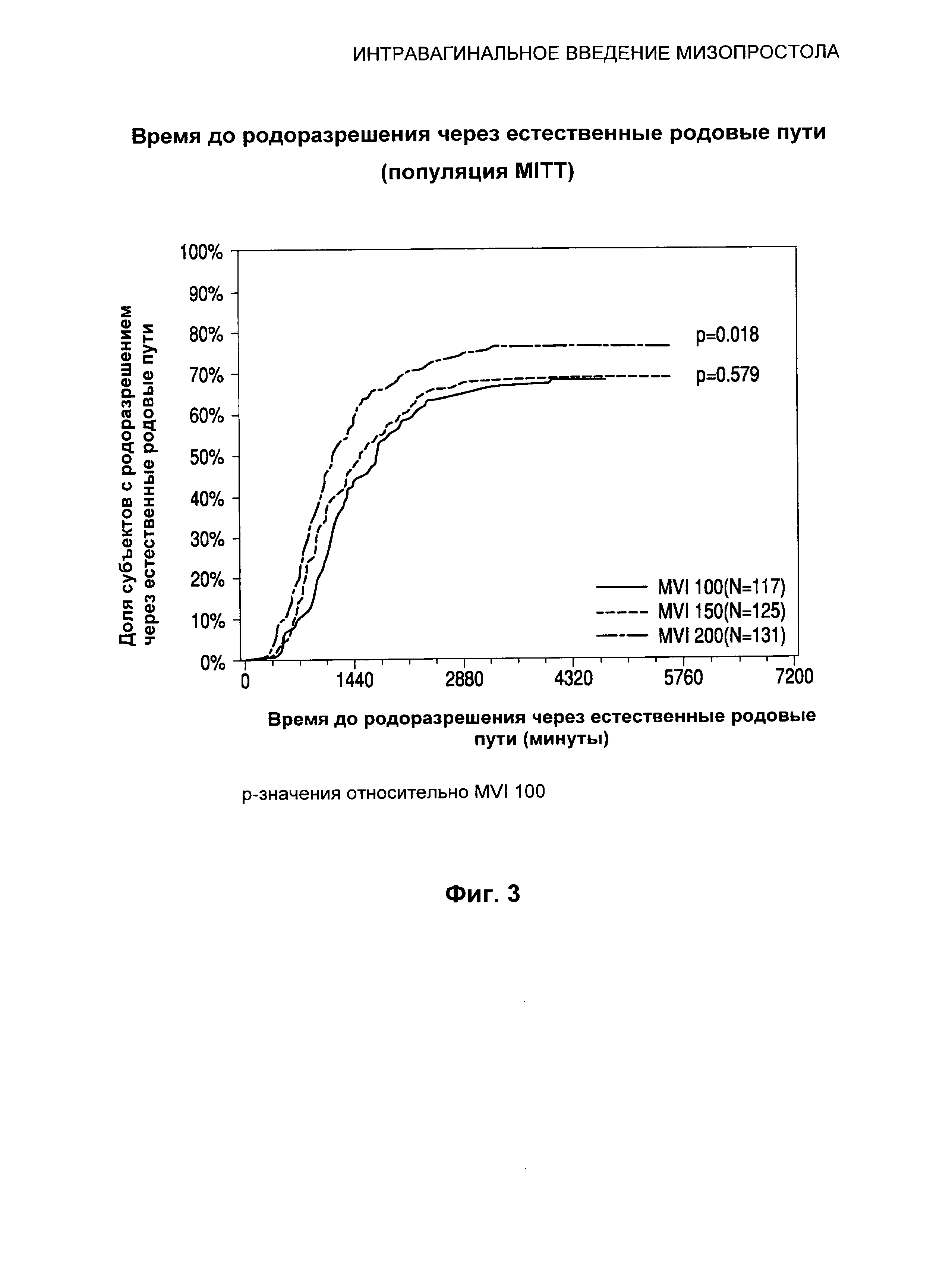
Фиг.3 иллюстрирует время от введения до родоразрешения через естественные родовые пути.
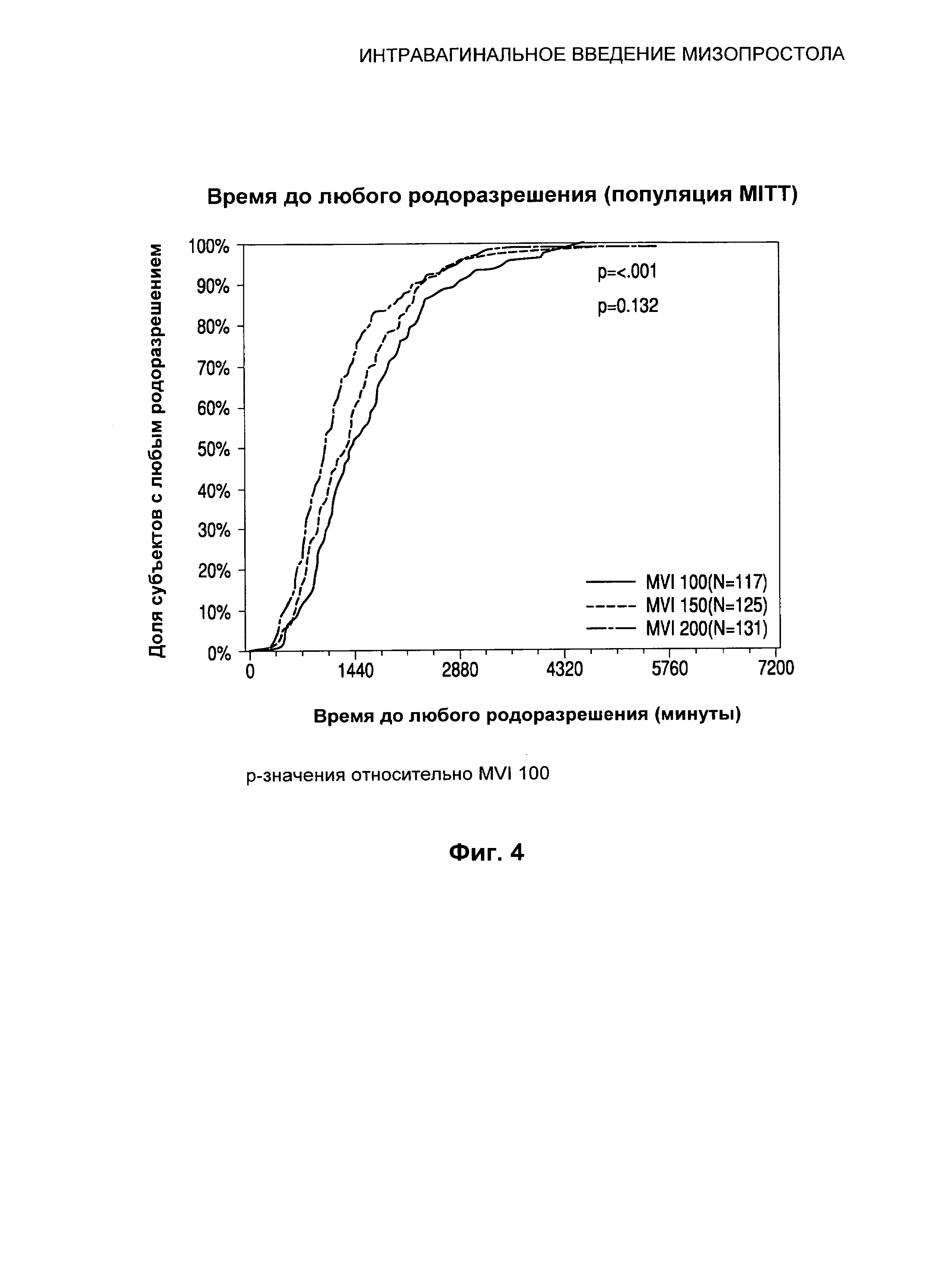
Фиг.4 иллюстрирует время от введения до любого родоразрешения.
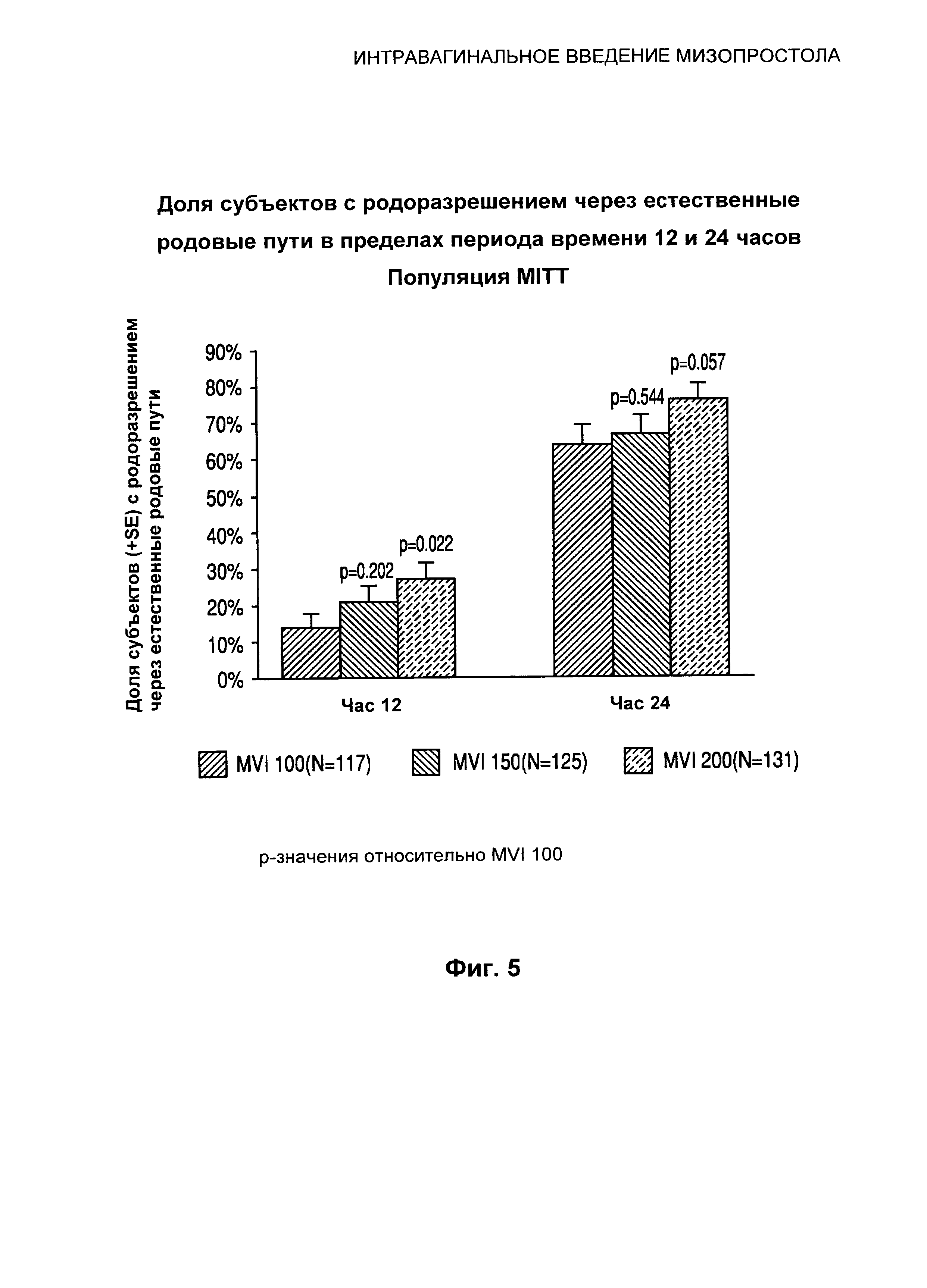
Фиг.5 иллюстрирует долю субъектов с родоразрешением через естественные родовые пути в пределах периода времени 12 и 24 часов.
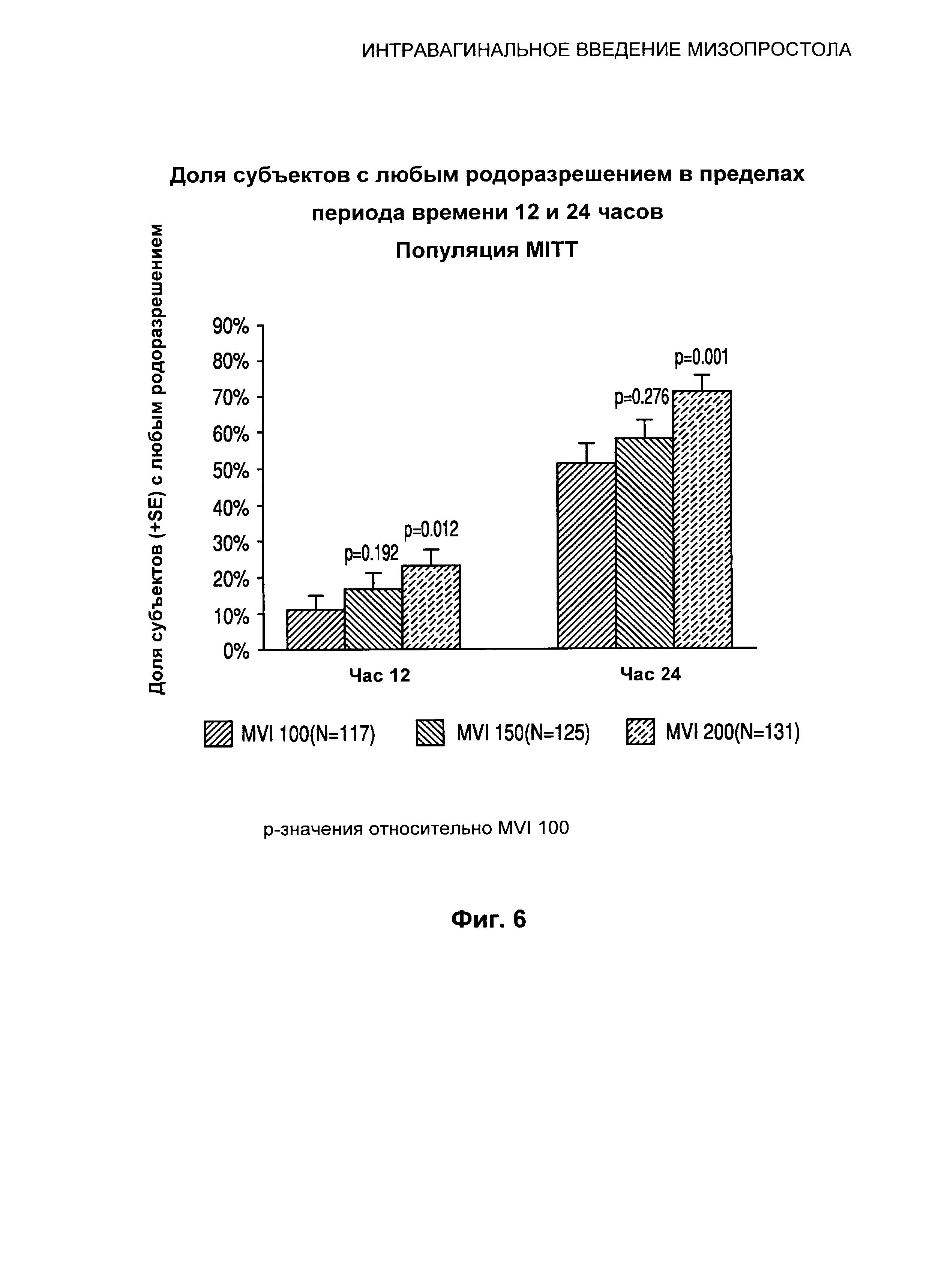
Фиг.6 иллюстрирует долю субъектов с любым родоразрешением (через естественные родовые пути или посредством кесарева сечения) в пределах периода времени 12 и 24 часов.
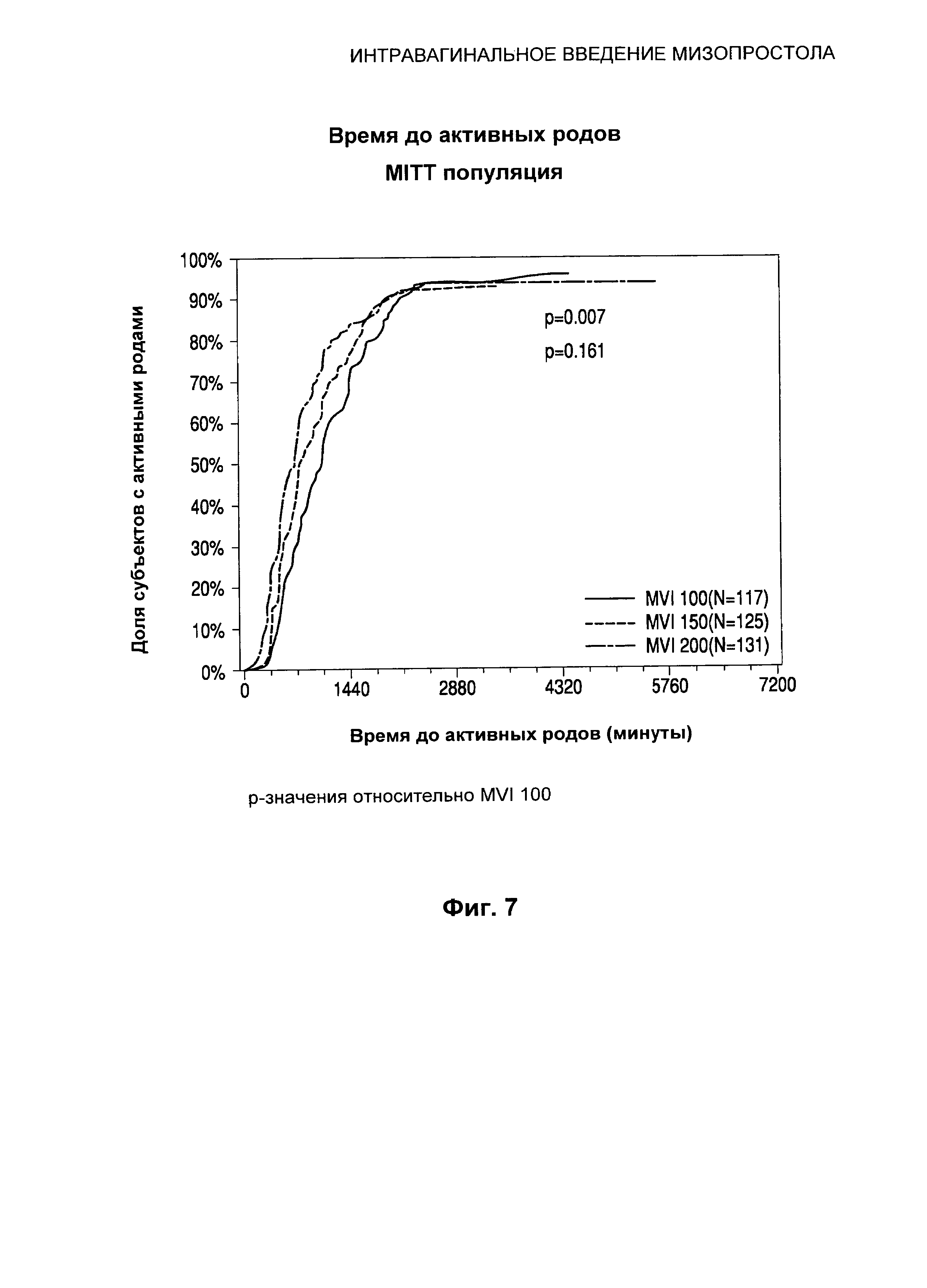
Фиг.7 иллюстрирует время до активных родов (популяция MITT (модифицированная популяция пациентов, сформированная в соответствии с назначенным вмешательством), нерожавшие и рожавшие).
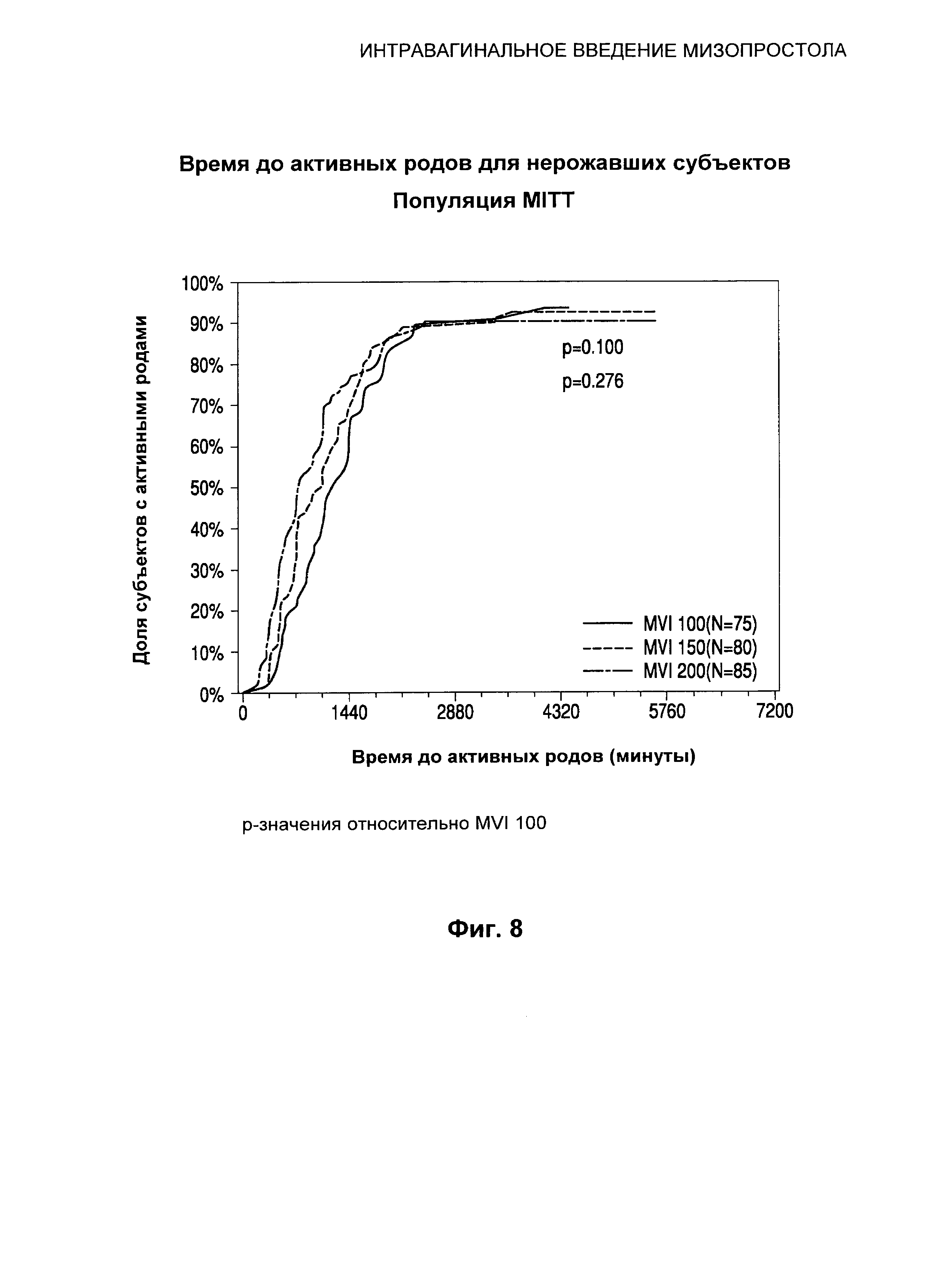
Фиг.8 иллюстрирует время до активных родов для нерожавших субъектов.
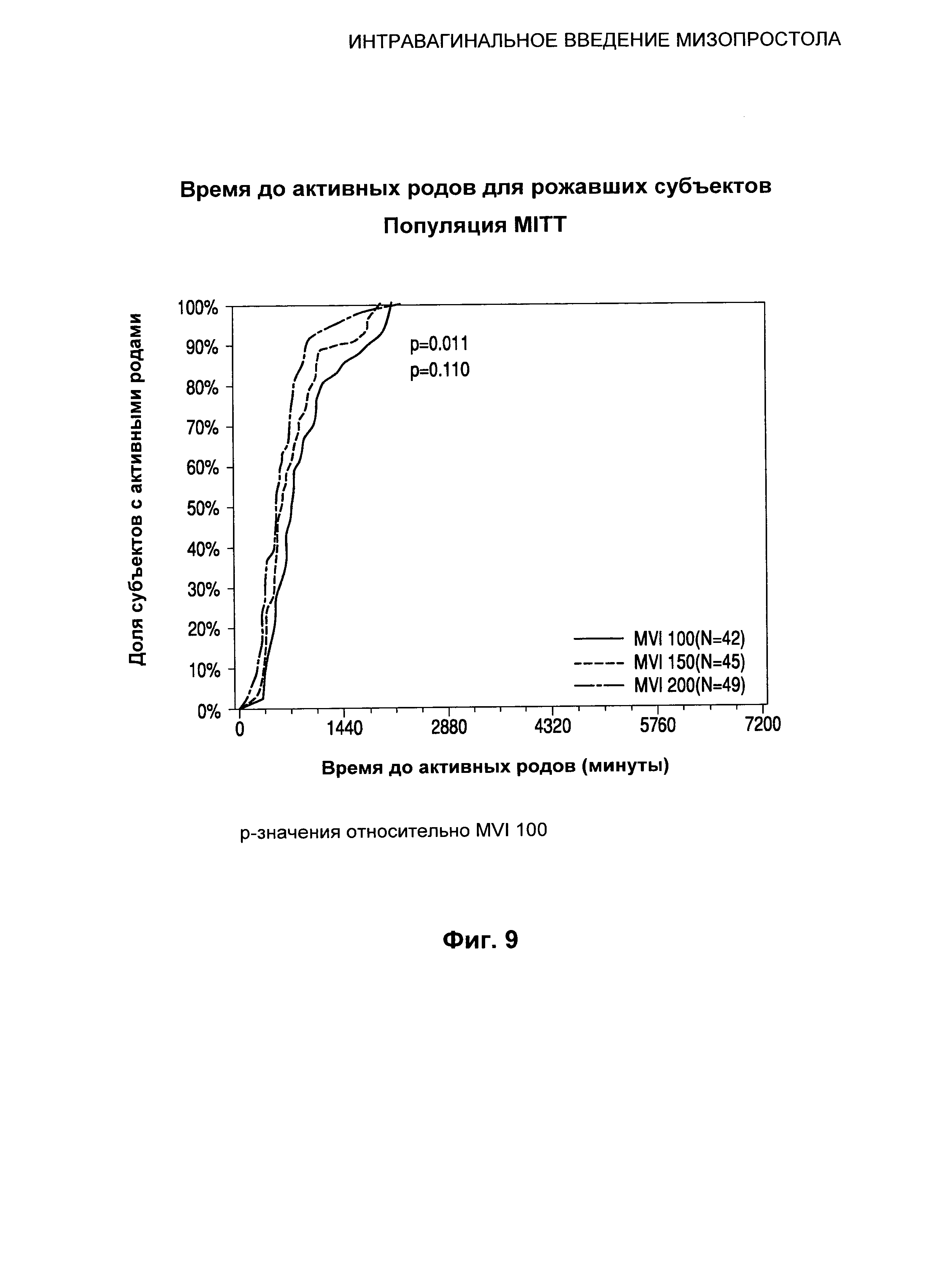
Фиг.9 иллюстрирует время до активных родов для рожавших субъектов.
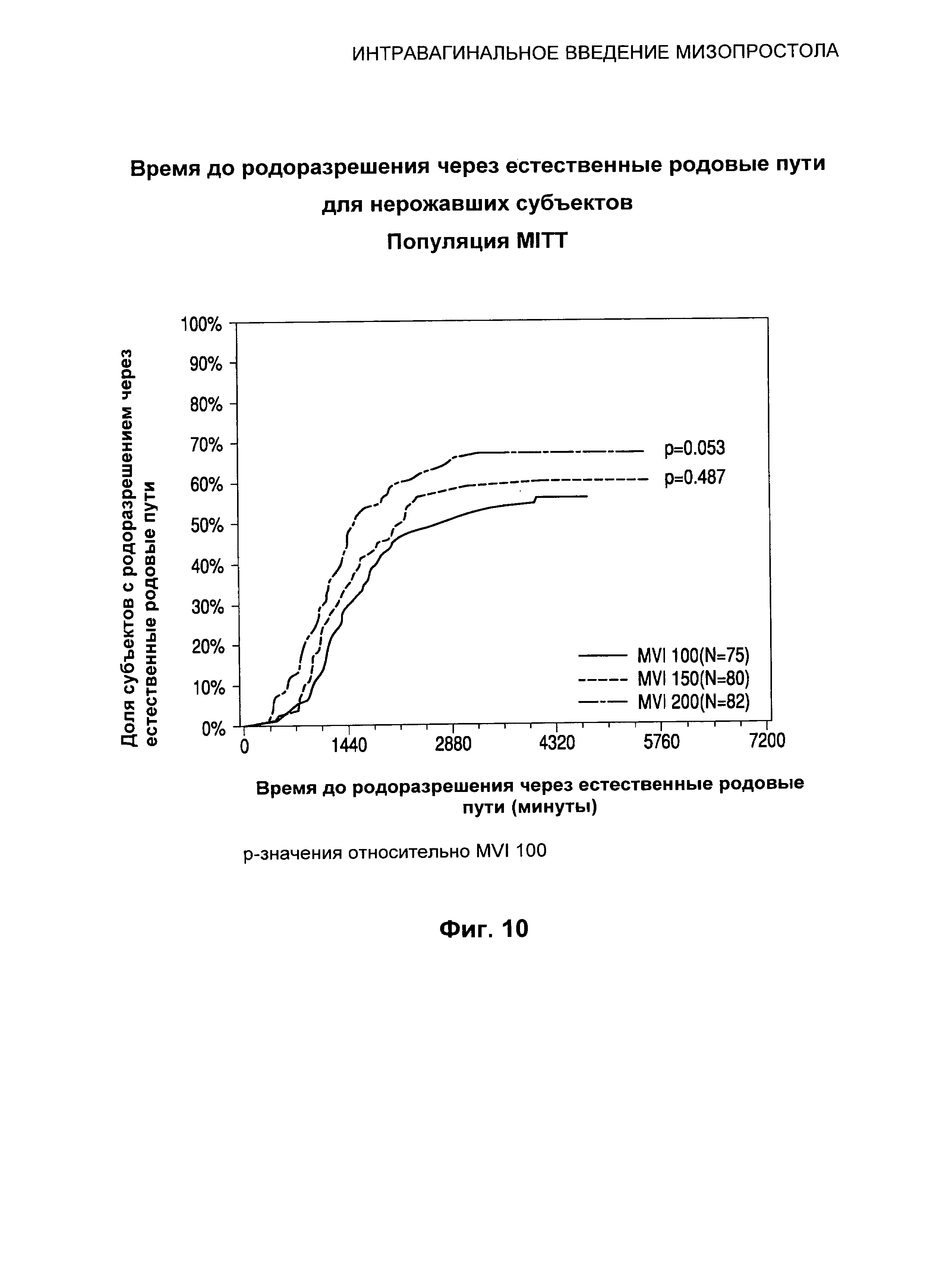
Фиг.10 иллюстрирует время до родоразрешения через естественные родовые пути для нерожавших субъектов.
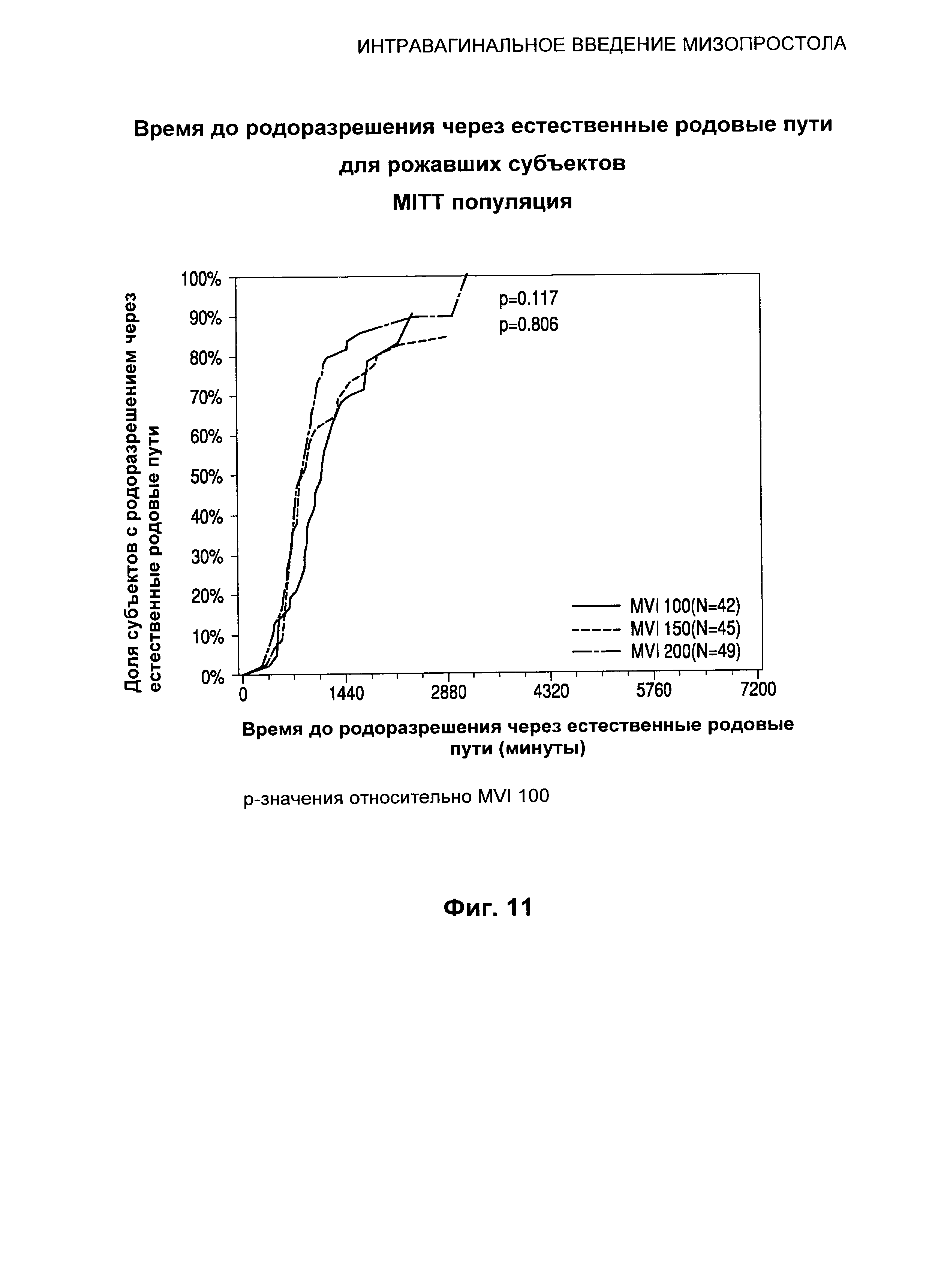
Фиг.11 иллюстрирует время до родоразрешения через естественные родовые пути для рожавших субъектов.
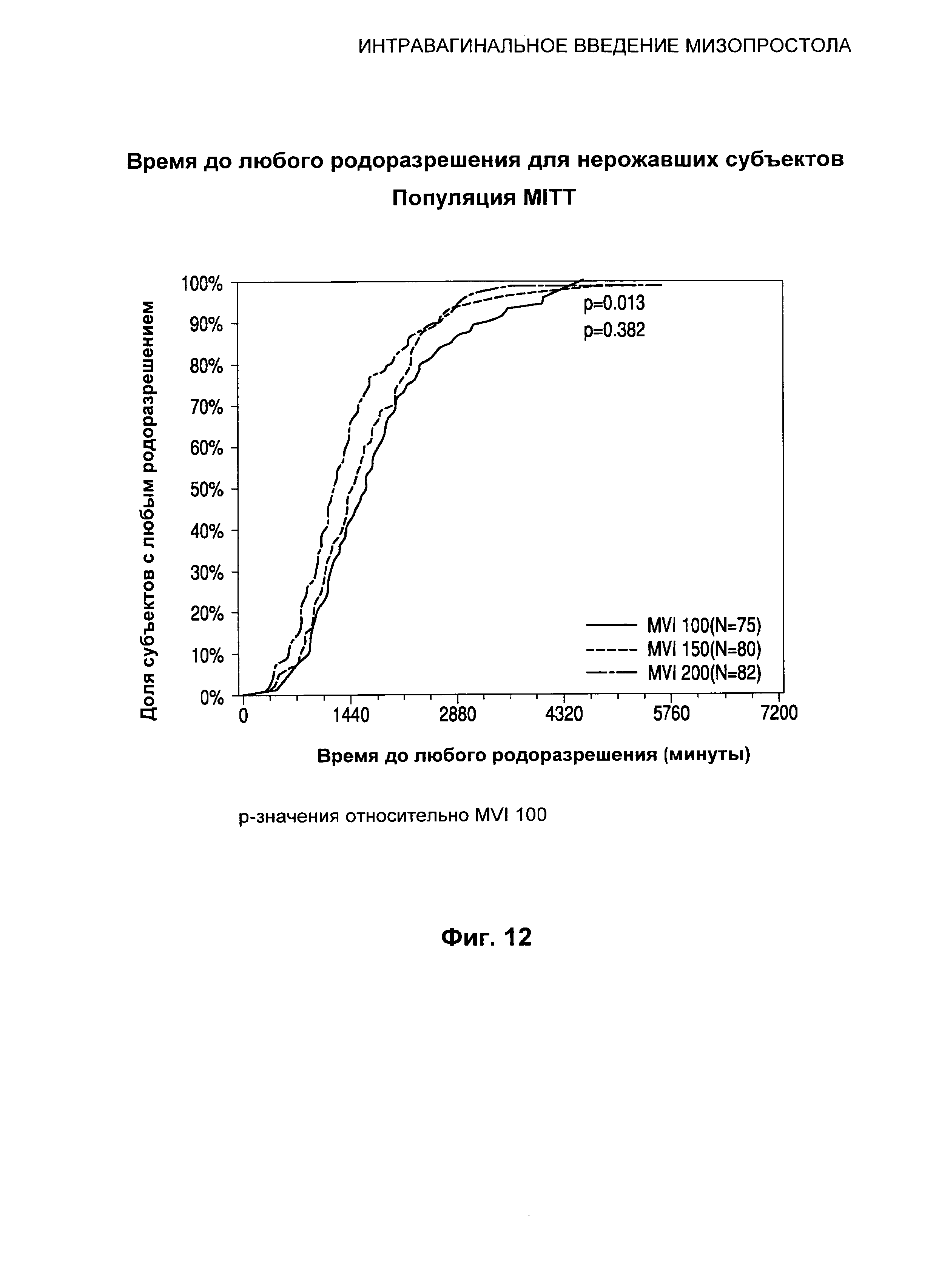
Фиг.12 иллюстрирует время до родоразрешения (через естественные родовые пути или посредством кесарева сечения) для нерожавших субъектов.
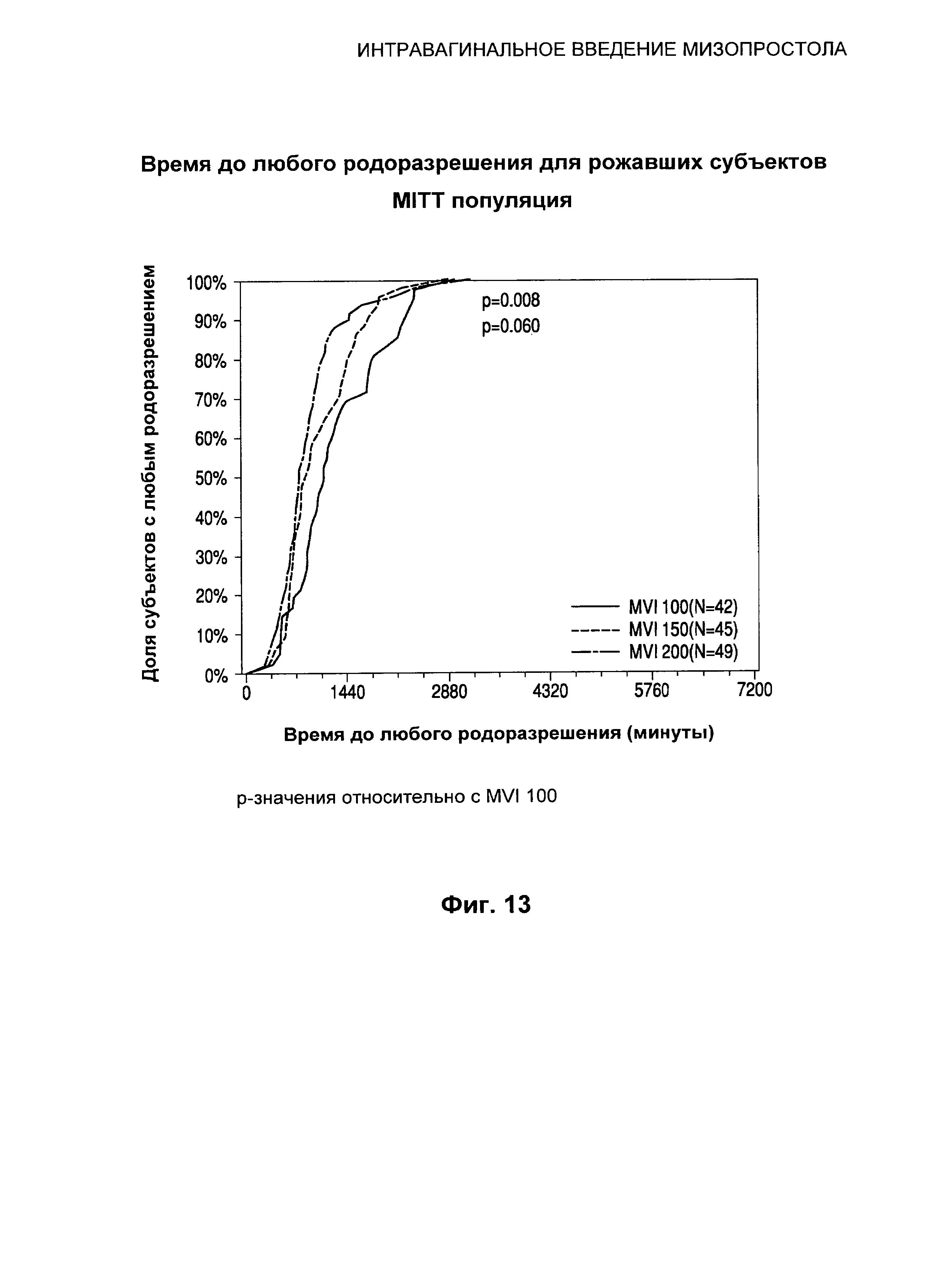
Фиг.13 иллюстрирует время до родоразрешения (через естественные родовые пути или посредством кесарева сечения) для рожавших субъектов.
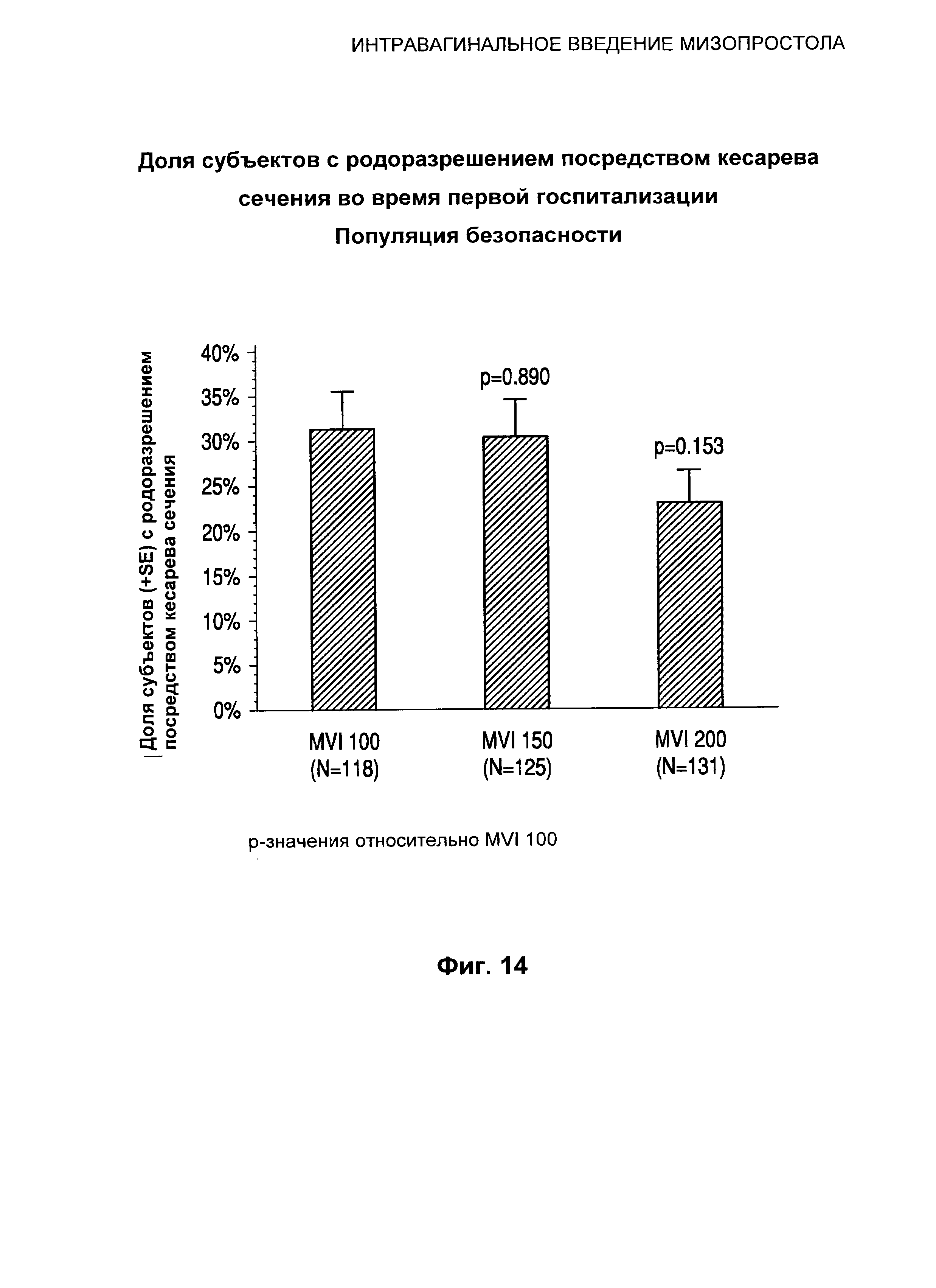
Фиг.14 иллюстрирует долю субъектов с родоразрешением посредством
кесарева сечения во время первой госпитализации.
ПОДРОБНОЕ ОПИСАНИЕ НЕСКОЛЬКИХ ВОПЛОЩЕНИЙ
В одном из воплощений предложен способ сокращения времени до начала активных родов у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения времени до родоразрешения через естественные родовые пути у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения времени до родоразрешения посредством кесарева сечения у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска необходимости использования окситоцина у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска неосуществления родоразрешения в пределах периода времени 24 часа после начала стимулирования родов у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска неосуществления родоразрешения в пределах периода времени 12 часов после начала стимулирования родов у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ увеличения вероятности родоразрешения через естественные родовые пути у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения вероятности родоразрешения посредством кесарева сечения у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска поступления в неонатальное ICU (отделение интенсивной терапии) младенца, рожденного субъектом женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска развития хориоамнионита у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска затяжных родов у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска развития неонатального сепсиса у младенца, нуждающегося в этом, рожденного субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения потребности в профилактических антибиотиках у новорожденных, нуждающихся в этом, рожденных субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения потребности в профилактических антибиотиках у беременного субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения использования антибиотиков у новорожденных, рожденных субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения использования антибиотиков у субъекта женского пола на сроке, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска длительного пребывания в стационаре (например, дольше 2 суток) субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола. Этот диапазон охватывает все значения и субдиапазоны между ними, включая пребывание в стационаре дольше 2, 3, 4, 5, 6, 7 и более суток, отмеряемые от поступления до выписки.
В одном из воплощений предложен способ снижения общей дозы окситоцина, вводимой субъекту женского пола, нуждающемуся в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения продолжительности введения окситоцина субъекту женского пола, нуждающемуся в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения необходимости введения окситоцина субъекту женского пола, нуждающемуся в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения максимальной дозы в минуту окситоцина, вводимого субъекту женского пола, нуждающемуся в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ увеличения женской удовлетворенности стимулированием родов у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска дистоции у нуждающегося в этом новорожденного, рожденного субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска маточной атонии у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска остановки родов у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска остановки раскрытия у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска медленной родовой деятельности у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска в случае диспропорции соотношения головки плода и материнского таза у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ обеспечения зрелости шейки матки беременного субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ увеличения тахисистолии у субъекта женского пола, нуждающегося в этом, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения вероятности родоразрешения посредством кесарева сечения у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения времени до начала родов у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения времени до родоразрешения через естественные родовые пути у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения времени до родоразрешения посредством кесарева сечения у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска необходимости использования окситоцина у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска неосуществления родоразрешения в пределах периода времени 24 часа после начала стимулирования родов у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска неосуществления родоразрешения в пределах периода времени 12 часов после начала стимулирования родов у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ увеличения вероятности родоразрешения через естественные родовые пути у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска поступления в неонатальное ICU младенца, рожденного субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска развития хориоамнионита у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска затяжных родов у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска развития неонатального сепсиса у младенца, рожденного субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения потребности в профилактических антибиотиках у новорожденных, рожденных субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения потребности в профилактических антибиотиках у беременного субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения использования антибиотиков у новорожденных, рожденных субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения использования антибиотиков у субъекта женского пола на сроке, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска длительного пребывания в стационаре (например, дольше 4 суток) субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения общей дозы окситоцина, вводимой субъекту женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ сокращения продолжительности введения окситоцина субъекту женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения необходимости введения окситоцина субъекту женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения максимальной дозы в минуту окситоцина, вводимого субъекту женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ увеличения женской удовлетворенности стимулированием родов у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска дистоции у новорожденного, рожденного субъектом женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска маточной атонии у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска остановки родов у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ обеспечения зрелости шейки матки беременного субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ увеличения тахисистолии у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска остановки раскрытия у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска медленной родовой деятельности у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений предложен способ снижения риска в случае диспропорции соотношения головки плода и материнского таза у субъекта женского пола, включающий интравагинальное введение мизопростола указанному субъекту женского пола.
В одном из воплощений тахисистолия увеличивается без увеличения ассоциированных замедлений частоты сердечных сокращений у плода. В одном из воплощений тахисистолия является продуктивной, эффективной и/или безопасной тахисистолией; она, например, способствует родоразрешению через естественные родовые пути.
В одном из воплощений интравагинальное введение включает интравагинальное введение эффективного количества мизопростола. Доставляемое эффективное количество определяет лечащий врач или специалист, например акушерка, неонатолог или т.п., с учетом приведенных здесь сведений. В одном из воплощений эффективным количеством является количество, которое, по мнению лечащего врача или специалиста, необходимо для достижения или увеличения вероятности достижения одного или более терапевтических эффектов. В одном из воплощений эффективным количеством является минимальное количество, необходимое для достижения или увеличения вероятности достижения одного или более терапевтических эффектов, и не является более чем необходимым. В одном из воплощений вкладыш можно титровать для обеспечения точного соответствия потребности для конкретного субъекта женского пола, поскольку он может быть извлечен после доставки именно того количества, которое необходимо.
В одном из воплощений интравагинальное введение включает интравагинальное введение мизопростола субъекту женского пола, нуждающемуся в этом, чтобы принести пользу субъекту женского пола, младенцу, рожденному субъектом женского пола, или как субъекту женского пола, так и ее младенцу или младенцам. Младенец может быть живым или умершим. Здесь термин "младенец" может относиться к плоду (будь то одноплодная или многоплодная беременность) или к новорожденному, где как подходит. Определение субъекта женского пола или младенца находится в пределах компетенции лечащего врача или специалиста, например акушерки, неонатолога или т.п., с учетом приведенных здесь сведений. В одном из воплощений у беременного субъекта женского пола, ее младенца или у обоих могут присутствовать одна или более следующих причин необходимости во введении: холестаз, пониженное шевеление плода, диабет, плановое введение, гипертензия, олигогидрамнион, переношенная беременность (срок беременности >40 недель 0 суток), преэклампсия, преждевременный разрыв плодных оболочек, предполагаемая макросомия плода (например, EFW (предполагаемая масса плода) >4000 г), IUGR (задержка внутриутробного развития), материнские гематологические факторы, необнадеживающий статус плода, доброкачественная внутричерепная гипертензия и т.п. или любая их комбинация, приводящая к решению стимулировать роды.
В одном из воплощений интравагинальное введение представляет собой одно или более из следующего: приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с катетером, содержащим мизопростол, приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с композицией, содержащей мизопростол, или комбинация двух или более из них.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, причем вкладыш имеет форму вагинального суппозитория, пессария, тампона, губки или кольца.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, причем вкладыш дополнительно содержит полимерную матрицу.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, причем вкладыш дополнительно содержит полимерную матрицу, причем полимерная матрица содержит поперечно-сшитый продукт реакции диизоцианата, триола и полиэтиленгликоля.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, причем вкладыш дополнительно содержит ленту для извлечения.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с катетером, содержащим мизопростол.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с катетером, содержащим мизопростол, и при этом катетер дополнительно содержит мизопростол-пористую поверхность, адаптированную для контакта с влагалищем.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с композицией, содержащей мизопростол.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с композицией, содержащей мизопростол, причем композиция дополнительно содержит фармацевтически приемлемый носитель, крем, гель, капсулу, лосьон или комбинацию двух или более из них.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с двумя или более из вкладыша, содержащего мизопростол, катетера, содержащего мизопростол, или композиции, содержащей мизопростол.
В одном из воплощений субъект женского пола является нерожавшим или рожавшим.
В одном из воплощений интравагинальное введение включает введение мизопростола с контролируемой скоростью высвобождения во влагалище субъекта женского пола.
В одном из воплощений риск и/или возникновение тахисистолии с необнадеживающей частотой сердечных сокращений у плода снижен.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, причем вкладыш дополнительно содержит полимерную матрицу, и при этом мизопростол высвобождается с контролируемой скорость 8 мкг в час.
В одном из воплощений введение может быть прекращено прерыванием потока мизопростола, например при введении через катетер или т.п., путем удаления катетера или удаления вкладыша. Вкладыш может быть удален рукой, щипцами или с помощью ленты для извлечения, как желательно. В одном из воплощений вкладыш извлекают с помощью ленты для извлечения. В одном из воплощений лента для извлечения дает возможность прервать лечение, когда имеет место терапевтический эффект или неблагоприятная реакция. Например, вагинальный вкладыш, содержащий мизопростол, может быть извлечен, или введение может быть прервано (например, в случае, если введение осуществляют через катетер, путем прерывания введения через катетер, извлечения катетера или т.п.), когда происходит одно или более из следующего списка, который не ограничен: начало активных родов (например, прогрессирующее раскрытие шейки матки до 4 см с частотой сокращений или ритмичными, устойчивыми, адекватными сокращениями матки, вызывающими прогрессирующее изменение шейки матки, происходящими с частотой 3 или более раз за 10 минут и продолжающимися 45 секунд или более); гипертонус матки (например, схватки, длящиеся по меньшей мере 2 минуты, также называемые тетаническими схватками или гипертонией матки); маточная тахисистолия (например, частота более 5 сокращений за период времени 10 минут, усредненная за период 30 минут); необходимость токолиза; доказательство аномалии плода (например, меконий в амниотической жидкости, ацидоз у плода или необнадеживающий паттерн частоты сердечных сокращений у плода, включая, без ограничения, потерю вариабильности, множественные замедления, тахикардию у плода, брадикардию у плода); синдром гиперстимуляции матки (например, гипертонические или тахиситолические маточные сокращения, ассоциированные с необнадеживающим паттерном частоты сердечных сокращений у плода и/или ацидозом у плода/дистресс-синдромом у плода); тахисистолия с ассоциированными замедлениями частоты сердечных сокращений у плода; другие материнские или плодные нежелательные явления, которые, по мнению лечащего врача, обуславливают необходимость прерывания введения дозы; непрерывное введение в течение 24 часов без предшествующих причин для прерывания или извлечения; и т.п.; или любая их комбинация.
В одном из воплощений интравагинальное введение включает приведение в контакт влагалища, шейки матки, матки, или любой их комбинации, субъекта женского пола с вкладышем, содержащим мизопростол, причем вкладыш дополнительно содержит полимерную матрицу, и при этом вкладыш доставляет мизопростол в течение вплоть до 24 часов. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 0,1; 0,2; 0,3; 0,4; 0,5; 0,6; 0,7; 0,8; 0,9; 1; 2; 3; 4; 5; 6; 7; 8; 9; 0; 11; 12; 13; 14; 15; 16; 17; 18; 19; 20; 21; 22; 23; и 24 часа.
В одном из воплощений скорость высвобождения определяют по количеству лекарственного средства в мизопростоловом вагинальном вкладыше ("MVI"). Количество мизопростола, присутствующего во вкладыше, которое соответственно может высвобождаться из полимерной матрицы, может составлять от 1 до 1000 мкг. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 25, 50, 75, 100, 150, 200, 250, 300, 350, 400, 500, 600, 700, 800, 900, 1000 мкг или любую их комбинацию. Другие субдиапазоны, которые не являются ограничивающими, включают диапазоны от 25 до 500 мкг; от 50 до 400 мкг; от 100 до 300 мкг; и от 150 до 250 мкг.
В одном из воплощений интравагинальное введение включает интравагинальное введение мизопростола в непрерывном и/или длительном режиме. В одном из воплощений мизопростол вводят с более или менее постоянной скоростью. В одном из воплощений мизопростол вводят непрерывно в течение длительного периода времени.
В одном из воплощений мизопростол можно вводить со скоростью в пределах от 0,1 до 500 мкг/ч. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 0,1, 0,25, 0,5, 0,75, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 25, 50, 75, 100, 150, 200, 250, 500 мкг/ч или любую их комбинацию. Другие субдиапазоны, которые не являются ограничивающими, включают диапазоны от 0,5 до 100 мкг/ч; от 1 до 75 мкг/ч; и от 1 до 10 мкг/ч.
В одном из воплощений мизопростол можно вводить в течение длительного периода времени в пределах от 0,1 до 24 часов. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 0, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20,21,22, 23 и 24 часа.
В одном из воплощений мизопростол можно вводить в течение времени в пределах от 0,1 до 48 часов до того, как произойдут роды или родоразрешение или желательно, чтобы произошли. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 0, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 36, 48 часов или любую их комбинацию.
В одном из воплощений, в случае вкладыша, мизопростол может высвобождаться из вкладыша со скоростью в пределах от 0,1 до 500 мкг/ч. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 0,1, 0,25, 0,5, 0,75, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 25, 50, 75, 100, 150, 200, 250, 500 мкг/ч или любую их комбинацию. Другие субдиапазоны, которые не являются ограничивающими, включают от 0,5 до 100 мкг/ч; от 1 до 75 мкг/ч; и от 1 до 10 мкг/ч. Возможно, что скорость высвобождения может варьировать в зависимости от индивидуума, вкладыша (например, степени лекарственной нагрузки, набухания, геометрии и т.д.), продолжительности введения и т.п. В одном из воплощений скорость высвобождения может меняться (например, скорость высвобождения±величина дисперсии) на 1-60%, причем этот диапазон включает все значения и субдиапазоны между ними, в том числе ±1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60% скорости или любую их комбинацию.
В одном из воплощений скорость введения и/или высвобождения может представлять собой среднюю скорость.
В одном из воплощений мизопростол высвобождается из вкладыша таким образом, что количество мизопростола во вкладыше снижается в линейной или приблизительно линейной зависимости от времени. С другой стороны, в одном из воплощений мизопростол высвобождается из вкладыша таким образом, что общее количество мизопростола, высвобождаемого из вкладыша, увеличивается со временем линейно или приблизительно линейно. Смотри, например, Фиг.2.
В одном из воплощений скорости высвобождения представляют собой скорости высвобождения in vivo.
В одном из воплощений интравагинальное введение включает интравагинальное введение мизопростола со скоростью в пределах от 0,1 до 500 мкг/ч за период времени в пределах от 0,1 до 24 часов. Этот диапазон включает все значения и субдиапазоны между ними, как уже описано.
В одном из воплощений мизопростол метаболизируется до мизопростоловой кислоты in vivo. В одном из воплощений мизопростоловая кислота является активным метаболитом. Соответственно, в одном из воплощений интравагинальное введение включает интравагинальное введение мизопростоловой кислоты в непрерывном и длительном режиме. В одном из воплощений количество вводимой мизопростоловой кислоты эквивалентно или пропорционально количеству вводимого мизопростола на молярной основе.
В одном из воплощений введение мизопростола, как описано в данном документе, исключает эффекты демпинга доз и болюсных доз, которые часто наблюдаются при пероральном и интравагинальном введении таблеток (или их частей), таких как Cytotec™
В одном из воплощений мизопростоловый вагинальный вкладыш содержит 200 мкг мизопростола и высвобождает мизопростол с контролируемой скоростью приблизительно 8 мкг/ч. Например, контролируемая скорость может составлять 8 мкг/ч±2 мкг/ч.
В одном из воплощений при высвобождении достаточного количества мизопростола и достижении эффекта (например, когда субъект женского пола вступил в фазу активных родов и т.д.), мизопростольный вагинальный вкладыш может быть извлечен, например, с помощью ленты для извлечения.
В одном из воплощений при интравагинальном введении активные роды у женщины наступают быстрее, чем в случаях, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение сокращает среднее время до родоразрешения через естественные родовые пути относительно случаев, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение сокращает среднее время до родоразрешения (через естественные родовые пути или посредством кесарева сечения) относительно случаев, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение увеличивает количество родоразрешений через естественные родовые пути в пределах периода времени 12 часов относительно случаев, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение увеличивает количество родоразрешений через естественные родовые пути в пределах периода времени 24 часа относительно случаев, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение снижает необходимость стимуляции или увеличения окситоцина относительно случаев, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение снижет частоту кесаревых сечений относительно случаев, когда мизопростол не вводят или вводят не интравагинально.
В одном из воплощений интравагинальное введение сокращает продолжительность времени, которое субъект женского пола проводит в родильном отделении.
В одном из воплощений интравагинальное введение приводит к сокращению времени пребывания субъекта женского пола и новорожденного в стационаре.
В одном из воплощений интравагинальное введение приводит к меньшему вмешательству врачей и/или медсестер во время родов и родоразрешения.
В одном из воплощений интравагинальное введение приводит к более высоким баллам по шкале Апгар в отношении состояния новорожденного через одну минуту после рождения.
В одном из воплощений интравагинальное введение приводит к более высоким баллам по шкале Апгар в отношении состояния новорожденного через пять минут после рождения.
В одном из воплощений интравагинальное введение приводит к более высоким баллам по шкале Апгар в отношении состояния новорожденного через одну минуту и через пять минут после рождения.
В одном из воплощений интравагинальное введение включает интравагинальное введение эффективного количества мизопростола. В одном из воплощений вводят эффективную дозу и снижают системное воздействие. В одном из воплощений вводят эффективную дозу и снижают один или более нежелательных побочных эффектов. В одном из воплощений вводят эффективную дозу и снижают тремор. В одном из воплощений вводят эффективную дозу и снижают диарею. В одном из воплощений вводят эффективную дозу и снижают тошноту. В одном из воплощений вводят эффективную дозу и снижают рвоту. Возможны комбинации.
Мизопростол (метиловый эфир (11α,13Е)-(±)-11,16-дигидрокси-16-метил-9-оксопрост-13-ен-1-овой кислоты (название в соответствии с IUPAC: метил-7-((1R,2R)-3-гидрокси-2-((S,E)-4-гидрокси-4-метилокт-1 -енил)-5-оксоциклопентил)гептаноат) (химическая формула С22H38O5, молекулярная масса 382,5)) является производным простагландина E1, в котором гидроксильная группа в положении 15 отсутствует, и имеется замещение метильной и гидроксильной группы в положении 16. Мизопростол существует в виде смеси 1:1 двух диастереоизомеров, (±)-(S)-мизопростола и (±)-(R)-мизопростола. Структура мизопростола представлена на Фиг.1.
В одном из воплощений мизопростоловый вагинальный вкладыш содержит полимерную матрицу. Полимерная матрица может представлять собой поперечно-сшитый гидрогелевый полимер, образованный из продукта реакции полиэтиленгликоля 8000, 4,4′-диизоцианата дициклогексилметана и гексантриола. Если желательно, для поддержания стабильности полимера может быть добавлен бутилированный гидроксианинизол (ВНА) в качестве антиоксиданта. Блоки полученного в результате небиоразлагаемого полимера могут быть нарезаны на слои подходящих размеров и затем пропитаны мизопростолом. Примеры мизопростолового вагинального вкладыша ("MVI") можно найти в заявке США, имеющей серийный №11/573,256, уже включенной в данное описание посредством ссылки на нее.
В одном из воплощений в MVI использована поперечно-сшитая гидрогелевая полимерная матрица, которая может иметь любую форму или любой размер.
Например, длина вкладыша, без ограничения, может составлять от 1 до 100 мм. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 80, 100 мм или любую их комбинацию. Другие субдиапазоны, без ограничения, включают от 1 до 80 мм; от 10 до 50 мм; и от 20 до 40 мм.
Например, ширина вкладыша может составлять, без ограничения, от 1 до 50 мм. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50 мм или любую их комбинацию. Другие субдиапазоны, без ограничения, включают от 1 до 40 мм; от 2 до 30 мм; и от 5 до 20 мм.
Например, толщина вкладыша может составлять, без ограничения, от 0,1 до 20 мм. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 0, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 мм или любую их комбинацию. Другие субдиапазоны, без ограничения, включают от 0,1 до 15 мм; от 0,22 до 10 мм; и от 0,5 до 5 мм.
В одном из воплощений гидрогелевый полимерный вкладыш имеет размеры 30 мм в длину, 10 мм в ширину и 0,8 мм толщиной. Он может иметь прямоугольную форму с закругленными углами. В одном из воплощений полимер содержится в ленте для извлечения. Лента для извлечения может быть изготовлена из любого фармацевтически приемлемого материала, например из тканого полиэфира или т.п. Вкладыш можно быстро и легко извлечь аккуратным вытягиванием за ленту для извлечения.
В одном из воплощений гидрогелевая полимерная матрица адсорбирует влагу и набухает, когда она находится в водной или влажной среде, например во влагалище. В одном из воплощений гидрогель не растворяется. Адсорбция воды приводит к градиенту концентраций, что облегчает высвобождение лекарственного средства мизопростол контролируемым образом. В одном из воплощений гидрогелевый полимер вкладывают высоко в задний свод влагалища. Возможно, для облегчения вкладывания можно использовать небольшие количества водорастворимых смазывающих веществ. В одном из воплощений после полного гидратирования гидрогелевый полимер может набухать в 2-3 раза по сравнению с его первоначальными размерами и может быть гибким.
В одном из воплощений, например в случае вкладыша, помещенного интравагинально, весь мизопростол или часть мизопростола высвобождается из вкладыша при введении. Например, количество мизопростола, высвободившегося из вкладыша, может составлять от 20% до 100% по массе в расчете на количество мизопростола, первоначально присутствовавшего во вкладыше. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 20, 30, 40, 50, 60, 70, 80, 90 и 100% по массе в расчете на количество мизопростола, первоначально присутствовавшего во вкладыше.
В одном из воплощений помещенный интравагинально MVI будет высвобождать весь мизопростол или часть содержащегося мизопростола в течение промежутка времени от 1 до 48 часов. Этот диапазон включает все значения и субдиапазоны между ними, в том числе 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 36, 48 часов или любую их комбинацию. В одном из воплощений высвобождается приблизительно 80% по массе от количества первоначально содержащегося мизопростола.
В одном из воплощений мизопростоловый вагинальный вкладыш высвобождает приблизительно 1/24-ю часть от общей дозы в час.
Мизопростоловый вагинальный вкладыш ("MVI") может быть приобретен у Controlled Therapeutics (Scotland) Ltd. в East Kilbride, Glasgow, UK.
Одновременно можно вводить один или более чем один MVI. Если желательно, введение можно повторять регулярно или периодически. Например, MVI можно периодически вводить каждые 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 24, 36, 48 часов или любые их комбинации. В одном из воплощений MVI вводят однократно или более чем однократно за период времени 24 часа. Опираясь на сведения, приведенные в данном описании, и знания специалиста в данной области, лечащий врач легко сможет установить надлежащую частоту введения.
В одном из воплощений MVI может быть вложен в задний свод влагалища субъекта женского пола и может оставаться на месте в течение вплоть до 24 часов.
В одном из воплощений pH окружающий среды не влияет на высвобождение мизопростола.
В одном из воплощений MVI стабилен при комнатной температуре, например при температуре 25°C. В одном из воплощений MVI можно хранить при температуре от -25°C до -10°C.
В одном из воплощений мизопростоловый вагинальный вкладыш (MVI) доставляет точную дозу мизопростола.
В одном из воплощений MVI обеспечивает длительное высвобождение мизопростола без максимальных и минимальных уровней в плазме крови и снижает инцидентность основных побочных эффектов таблеток мизопростола, таких как избыточная маточная активность и необнадеживающие паттерны частоты сердечных сокращений у плода.
В одном из воплощений однократное введение является эффективным, и количество обследований и манипуляций уменьшается, что более удобно для субъекта и снижает риск инфицирования. Введение однократной дозы может быть желательным, так как сокращает также использование фармацевтических средств и время медицинского персонала и, следовательно, затраты. В одном из воплощений введение обеспечивает предсказуемую ответную реакцию, что позволяет достоверно оценить время до родоразрешения.
В одном из воплощений субъектом женского пола является человек женского пола. В одном из воплощений субъект женского пола представляет собой млекопитающее, не являющееся человеком, например корову, овцу, свинью, лошадь, козу, кошку, собаку, домашний скот и т.п. В одном из воплощений мизопростол можно вводить интравагинально, как описано в данном документе, одному или более беременным субъектам женского пола, не являющимся людьми, для обеспечения предсказуемой ответной реакции, так чтобы время до родоразрешения можно было достоверно оценить. Термин "мкг" здесь означает микрограммы.
В одном из воплощений время до начала активных родов означает время до прогрессирующего раскрытия шейки матки до 4 см с любой частотой родовых схваток или ритмичных, устойчивых, адекватных по качеству сокращений матки, вызывающих прогрессирующее изменение шейки матки, происходящих с частотой 3 или более за 10 минут и длящихся 45 секунд или дольше.
В одном из воплощений время до родоразрешения через естественные родовые пути означает время от госпитализации до родоразрешения через естественные родовые пути.
В одном из воплощений время до родоразрешения посредством кесарева сечения означает время от госпитализации до родоразрешения посредством кесарева сечения.
В одном из воплощений женская удовлетворенность стимулированием родов означает субъективную удовлетворенность беременного субъекта женского пола временем от времени стимулирования ее родов до времени ее родоразрешения в результате такого стимулирования родов.
В одном из воплощений термины или терапевтические показания в данном документе, например снижение риска необходимости введения окситоцина, снижение риска неосуществления родоразрешения в пределах периода времени 24 часа после начала стимулирования родов, снижение риска неосуществления родоразрешения в пределах периода времени 12 часов после начала стимулирования родов, увеличение вероятности родоразрешения через естественные родовые пути, уменьшение вероятности родоразрешения посредством кесарева сечения, снижение риска поступления в неонатальное отделение, снижение риска развития хориоамнионита, снижение риска затяжных родов, снижение риска развития неонатального сепсиса, снижение необходимости введения профилактических антибиотиков, снижение использования антибиотиков, снижение риска длительного пребывания в стационаре, снижение общей дозы вводимого окситоцина, сокращение продолжительности введения окситоцина, снижение необходимости введения окситоцина, снижение максимальной дозы окситоцина в минуту, увеличение женской удовлетворенности стимулированием родов, снижение риска дистоции, снижение риска маточной атонии, снижение риска остановки родов, созревания шейки матки, увеличение тахисистолии и т.п., могут быть определены путем сопоставления результата или вероятности получения результата при введении мизопростола в соответствии с данным описанием или формулой изобретения с ожидаемым результатом или ожидаемой вероятностью получения результата без введения мизопростола в соответствии с данным описанием или формулой изобретения. В одном из воплощений любое отклонение или повышение риска, вероятности и т.п., наблюдаемое при таком сопоставлении, может быть статистически значимым, клинически значимым, значимым по мнению субъекта женского пола, которого лечат, или значимым в любой комбинации. Термины, такие как риск, вероятность и т.п., могут соответственно относиться к индивидууму или к популяции.
ПРИМЕРЫ
В представленных в данном описании экспериментах мизопростоловый вагинальный вкладыш, или MVI, состоял из поперечно-сшитого гидрогелевого полимера, образованного из продукта реакции полиэтиленгликоля 8000, 4,4′-диизоцианата дициклогексилметана и гексантриола, который пропитывали мизопростолом до указанного количества (25 мкг, 50 мкг, 100 мкг и т.д.) известными методами. MVI были получены от Controlled Therapeutics (Scotland) Ltd.
Пример 1. Фармакокинетические свойства
Исследовали фармакокинетические свойства мизопростоловых вагинальных вкладышей. Плазматические фармакокинетические параметры получали после применения вагинального вкладыша, содержащего мизопростол в дозе 25 мкг, 50 мкг, 100 мкг, 200 мкг, 300 мкг и 400 мкг для введения в течение 24 часов. В Таблице 1 представлены фармакокинетические данные по MVI у небеременных здоровых женщин и у нерожавших беременных женщин на сроке или близко к сроку.
В исследовании небеременных женщин было установлено, что фармакокинетические параметры площадь под кривой AUC0-t (0-24 ч) и максимальная концентрация Сmax пропорциональны дозе. Например, средняя AUC0-t в случае вагинального вкладыша, содержащего 100 мкг мизопростола, составляла 481 nr.ч/мл (CV (коэффициент вариации)=20,4%), и средняя Стах составляла 33,1 пг/мл (CV=40,7%). Выведение мизопростоловой кислоты из плазмы крови происходит очень быстро.
В исследовании нерожавших беременных женщин РК (фармакокинетические) параметры AUC0-removal, AUC0-t и Cmax для мизопростоловой кислоты были пропорциональны дозе в пределах депо доз от 25 до 300 мкг. Выведение мизопростоловой кислоты из системного кровотока происходило менее чем через один час после извлечения MVI (t½<1 ч).
|
Пример 2. Высвобождение in vivo у здоровых небеременных женщин перед менструацией
Исследовали характеристики высвобождения in vivo трех разных доз мизопростола из вагинальных вкладышей с контролируемым высвобождением за четыре разных промежутка времени (4, 8, 12 и 24 часов) после вкладывания их во влагалище здоровых женщин. Фармакокинетические профили трех разных доз мизопростола, доставляемых вкладышем с контролируемым высвобождением, исследовали за период времени лечения 24 часа для установления ограниченного фармакокинетического профиля перорального мизопростола 200 мкг (Cytotec®) и для оценки безопасности MVI. Проводили Фазу I открытого, одноцентрового, рандомизированного, перекрестного исследования с увеличением дозы 12 здоровых субъектов женского пола перед менструацией.
Вагинальные вкладыши с разной дозой мизопростола (100 мкг, 200 мкг и 400 мкг) оценивали в порядке возрастания дозы. В течение первых трех суток лечения каждый субъект получал одинаковую дозу мизопростола (100 мкг), рандомизированную для 4, 8 или 12 часов. На четвертые сутки лечения вагинальный вкладыш, содержащий 100 мкг мизопростола, вводили на 24 часа, и в течение этого периода времени собирали образцы крови для определения полного фармакокинетического профиля. Эту процедуру повторяли для всех трех доз. Данные по безопасности (основные показатели состояния организма и нежелательные явления) анализировали перед увеличением дозы мизопростола. Каждый использованный MVI сохраняли для анализа методом ВЭЖХ на остаточное содержание лекарственного средства. При последнем посещении каждый субъект получал одну пероральную таблетку мизопростола 200 мкг для того, чтобы получить сравнительные данные по пероральному и вагинальному путям введения. Средний процент высвобождения для трех депо доз указан в Таблице 2. Каждый MVI высвобождал приблизительно 50% лекарственного средства за 12 часов и 80% за 24 часа.
|
Высвобождение in vivo в мкг за 24 часа представлено на Фиг.2. Скорость высвобождения контролировали в течение 24 часов, и вычисленные средние скорости высвобождения для депо доз 100, 200 и 400 мкг составляли приблизительно 4,2; 7,1; и 15,3 мкг/час соответственно.
Пример 3. Эффективность и безопасность лечения в течение вплоть до 24 часов с использованием MVI
Рандомизированное, двойное слепое, многоцентровое исследование в диапазоне доз проводили для оценки эффективности и безопасности лечения в течение вплоть до 24 часов вкладышами MVI 100, MVI 150 и MVI 200. Регистрировали беременных женщин на сроке или близких к сроку, которым требовалась стимуляция родов и созревания шейки матки, и которые отвечали критериям пригодности. Нерожавших и рожавших женщин рандомизировали либо для испытания вагинального вкладыша с депо дозы мизопростола 100 мкг (с последующим добавлением окситоцина, если это было необходимо), либо для испытания вагинального вкладыша с депо дозы мизопростола 150 мкг (с последующим добавлением окситоцина, если это было необходимо), либо для испытания вагинального вкладыша с депо дозы мизопростола 200 мкг (с последующим прибавлением окситоцина, если это было необходимо). Формировали уровни регистрации по центру исследования и по количеству родов таким образом, чтобы было зарегистрировано приблизительно 216 нерожавших и 144 рожавших женщин (т.е. приблизительно 60% нерожавших и 40% рожавших). Раса, рост, масса тела, BMI (индекс массы тела), срок беременности и причины стимуляции были сходными по всем группах. MVI вкладывали в задний свод влагалища и оставляли его там на период времени вплоть до 24 часов, если не было необходимости его удаления раньше.
Статистические и аналитические данные
Статистическую значимость декларировали, если двустороннее p-значение составляло ≤0,05. Группы лечения сравнивали для определения различий относительно MVI 100 (MVI, пропитанный 100 мкг мизопростола). Все вычисления осуществляли с использованием SAS® (версия 8.2 или выше).
Исследуемые популяции
Популяция пациентов, сформированная в соответствии с назначенным вмешательством (intent-to-treat, ITT), включала всех рандомизированных субъектов, которые были рандомизированы по исследуемому лекарственному средству. Модифицированная популяция пациентов, сформированная в соответствии с назначенным вмешательством (modified intent-to-treat, MITT), включала всех рандомизированных субъектов, которых подвергали воздействию исследуемого лекарственного средства в течение какого-либо периода времени, и у которых имелись данные, зафиксированные на дату и время введения исследуемого лекарственного средства и на дату, время и способ родоразрешения. Оцениваемая популяция включала всех субъектов, которые не имели существенных нарушений протокола, и либо у которых вкладыш оставался на месте в течение по меньшей мере одного часа, либо лечение которых было прекращено раньше, чем через один час, вследствие возникновения определенных явлений.
В сумме 374 субъекта были рандомизированы по 11 центрам исследования. В сумме 373 субъекта (99,7%) прошли исследование до конца. Конечная диспозиция всех субъектов указана в Таблице 3.
|
Популяцию MITT использовали для всех анализов на эффективность. Количество родов указано в Таблице 4.
|
Родоразрешение через естественные родовые пути в пределах периода времени 12 и 24 часов при использовании вкладыша, содержащего лекарственное средство
Имело место дозозависимое увеличение доли субъектов с родоразрешением через естественные родовые пути в течение 24 часов (любое количество родов, нерожавшие и рожавшие). 76,00% субъектов с MVI 200 испытали родоразрешение через естественные родовые пути в пределах периода времени 24 часа по сравнению с 63,75% субъектов с MVI 100; эта разница не имела статистической значимости (p=0,057). У нерожавших субъектов, которые получали MVI 200, наблюдалось 15-процентное увеличение доли родоразрешения через естественные родовые пути по сравнению с субъектами, которые получали MVI 100 (67,27% по сравнению с 52,38% соответственно, p=0,137). Аналогично, у рожавших субъектов, которые получали MVI 200, наблюдалось 10-процентное увеличение доли родоразрешений через естественные родовые пути по сравнению с субъектами, получавшими MVI 100 (86,67% по сравнению с 76,32%, p=0,119). Смотри Таблицу 5.
Через 12 часов после введения исследуемого лекарственного средства имело место статистически значимое дозозависимое увеличение доли родоразрешений через естественные родовые пути (любое количество родов). Субъекты, получавшие MVI 200, имели в два раза больше родоразрешений через естественные родовые пути за 12 часов по сравнению с субъектами, получавшими MVI 100 (27,00% по сравнению с 13,75% соответственно, p=0,022). Двенадцатичасовое воздействие MVI 200 у нерожавших субъектов привело к увеличению доли родоразрешений через естественные родовые пути по сравнению с субъектами, получавшими MVI 100 (18,18% по сравнению с 7,14% соответственно, p=0,080). Аналогично, воздействие MVI 200 у рожавших женщин привело к увеличению доли родоразрешений через естественные родовые пути по сравнению с субъектами, получавшими MVI 100 (37,78% по сравнению с 21,05% соответственно, p=0,092). Смотри Таблицу 5.
|
Любое родоразрешение в пределах периода времени 12 и 24 часов при использовании вкладыша, содержащего лекарственное средство
Что касается времени от введения до любого родоразрешения (т.е. времени до родоразрешения независимо от способа родоразрешения), имело место в высокой степени значимое дозозависимое увеличение доли субъектов с родоразрешением через естественные родовые пути за 24 часа (любое количество родов, нерожавшие и рожавшие) с 72,52% субъектов, получавших MVI 200, родивших не позднее чем через 24 часа по сравнению с 52,14% субъектов, получавших MVI 100 (p<0,001). У нерожавших субъектов, которые получали MVI 200, наблюдалось более чем 20-процентное увеличение доли родоразрешений за 24 часа по сравнению с субъектами, которые получали MVI 100 (63,41% по сравнению с 42,67% соответственно, p=0,012). Аналогично, у рожавших субъекты, которые получали MVI 200, наблюдалось более чем 18-процентное увеличение доли родоразрешений за 24 часа по сравнению с субъектами, которые получали MVI 100 (87,76% по сравнению с 69,05%, p=0,016).
Оценка по методу Каплана-Мейера времени до родоразрешения через естественные родовые пути
Оценка по методу Каплана-Мейера времени до родоразрешения через естественные родовые пути продемонстрировала значительное снижение у субъектов, подвергавшихся воздействию MVI 200, по сравнению субъектами, подвергавшимися воздействию MVI 100 (p=0,018). Оценка по методу Каплана-Мейера для времени до родоразрешения через естественные родовые пути представлена в Таблице 6 и на Фиг.3. Для оценки времени до родоразрешения через естественные родовые пути по методу Каплан-Мейера использованы требуемые FDA (Управление по контролю качества пищевых продуктов, медикаментов и косметических средств США) правила цензурирования с самым длительным временем из всех назначенных С-сечений (кесаревых сечений).
|
Из Таблицы 6 видно, что улучшение на 9,3 часа наблюдается в случае использования MVI 200. Время до любого родоразрешения отражает фактическое время для всех родоразрешений. Неожиданно и желательно, это свидетельствует о том, что применение MVI 200 обеспечивает "окончательный ответ" быстрее в том, что касается способности субъектов женского пола рожать через естественные родовые пути, и тем самым предотвращает затяжные роды с неизбежными кесаревыми сечениями.
Начало активных родов
Время до начала активных родов было значительно меньше у субъектов, получавших MVI 200, по сравнению с субъектами, получавшими MVI 100 (p=0,007). Оценка по методу Каплана-Мейера в отношении времени начала активных родов представлена в Таблице 8.
|
Время до родоразрешения
Анализ времени до родоразрешения (через естественные родовые пути и посредством кесарева сечения) продемонстрировал значительное сокращение время до родоразрешения у субъектов, подвергнутых воздействию MVI 200, по сравнению с субъектами, подвергнутыми воздействию MVI 100 (p<0,001). Оценка по методу Каплана-Мейера в отношении времени до родоразрешения представлена в Таблице 9 и на Фиг.4.
|
Обеспечение зрелости шейки матки
Успех обеспечения зрелости шейки матки через 12 часов после введения MVI оценивали с использованием суммарного балла. Доля успеха была сходной во всех группах лечения.
Баллы по шкале Апгар
Не было никакой разницы в баллах по шкале Апгар для трех групп лечения MVI 100, 150 и 200.
Продолжительность родов и родоразрешения во время первой госпитализации
Как указано в Таблице 10, имело место статистически значимое, дозозависимое сокращение продолжительности родов и родоразрешения, составляющее >8 часов для субъектов, которых подвергали воздействию MVI 200, по сравнению с MVI 100 (p<0,001).
|
Введение окситоцина до родоразрешения
Имело место статистически значимое снижение доли субъектов (любое количество родов в анамнезе), которым требовалось введение окситоцина до родоразрешения в группе лечения MVI 200 (48,85%) по сравнению с группой лечения MVI 100 (70,94%) (p<0,001). Имело место также снижение доли субъектов группы MVI 150 (60,00%), которые до родоразрешения получали окситоцин, по сравнению с субъектами в группе лечения MVI 100, хотя это отличие от MVI 100 не достигало статистической значимости (p=0,067). Суммарная доза окситоцина, максимальная доза окситоцина и продолжительность использования окситоцина показали дозозависимое снижение в пользу MVI 200 по группам лечения, однако эти изменения не были статистически значимыми. Тем не менее, пониженная потребность в окситоцине является в высокой степени клинически значимой.
|
У нерожавших субъектов наблюдались результаты, подобные результатам у всех рожавших субъектов. Имело место статистически значимое снижение доли нерожавших субъектов, которым требовалось введение окситоцина до родоразрешения, в группе лечения MVI 200 (56,10%) по сравнению с группой лечения MVI 100 (78,67%) (p=0,002). Имело место также снижение в группе лечения MVI 150 (66,25%) по сравнению с MVI 100, но это снижение не достигало статистической значимости (p=0,070). Суммарная доза окситоцина, максимальная доза окситоцина и продолжительность введения окситоцина показали небольшое дозозависимое снижение во всех группах лечения, однако эти изменения не были статистически значимыми.
У рожавших субъектов имело место статистически значимое снижение доли субъектов, которым требовалось введение окситоцина до родоразрешения, в группах лечения MVI 150 и 200 (48,89% и 36,73% соответственно) по сравнению с группой лечения MVI 100 (57,14%). Средняя суммарная доза окситоцина, средняя максимальная доза окситоцина и средняя продолжительность применения окситоцина показали небольшое дозозависимое снижение во всех группах лечения.
Обсуждение эффективности
MVI 200 продемонстрировал увеличение доли родоразрешений через естественные родовые пути за 24 часа по сравнению с MVI 100 (76,00% по сравнению с 63,75% соответственно, р=0,057).
MVI 200 продемонстрировал статистически значимое увеличение доли родоразрешений через естественные родовые пути за 12 часов по сравнению с MVI 100 (27,00% и 13,75% соответственно, р=0,022).
Оценка по методу Каплана-Мейера в отношении среднего времени до родоразрешения через естественные родовые пути продемонстрировала статистически значимое сокращение среднего времени до родоразрешения через естественные родовые пути у субъектов, получавших MVI 200, по сравнению с субъектами, получавшими MVI 100 (1181,00 мин и 1744,00 мин соответственно, p=0,018).
Оценка по методу Каплана-Мейера в отношении среднего времени до родоразрешения (через естественные родовые пути и посредством кесарева сечения) продемонстрировала статистически значимое сокращение среднего времени до родоразрешения у субъектов, получавших MVI 200, по сравнению с субъектами, получавшими MVI 100 (1046,00 мин и 1403,00 мин соответственно, p<0,001).
MVI 200 продемонстрировал статистически значимое сокращение среднего времени до начала активных родов по сравнению с MVI 100 (701,00 мин и 1069,00 мин соответственно, р=0,007).
MVI 200 продемонстрировал статистически значимое снижение доли субъектов (любое количество родов в анамнезе), которым требовалось введение окситоцина до родоразрешения (48,85%), по сравнению с группой лечения MVI 100 (70,94%) (p<0,001).
MVI 200 значительно сокращал продолжительность пребывания в родильном отделении по сравнению с MVI 100 (p<0,001).
Нежелательные явления у матери/плода
Общее количество и процент субъектов с нежелательными явлениями ("АЕ") у матери/плода были сходными во всех группах лечения. Остановка родовой деятельности и хориоамнионит были ниже в случае использования MVI 200, и нарушение частоты сердечных сокращений у плода (необнадеживающая частота сердечных сокращений у плода) было ниже в случае использования MVI 150 и MVI 200. Данные приведены в Таблице 11.
|
Материнские послеродовые нежелательные явления Общее количество субъектов с материнскими послеродовыми АЕ и количество субъектов с каждым АЕ были сходными во всех группах лечения. Чаще всего регистрируемые АЕ относились к Системе организма Беременность, послеродовые и перинатальные состояния. Чаще всего сообщаемыми АЕ в этой системе организма были послеродовое кровотечение (4,8% субъектов), разрыв промежности (2,9% субъектов) и послеродовая лихорадка (2,4% субъектов). Связанных с лечением материнских послеродовых серьезных нежелательных явлений ("SAE") не было. Данные приведены в Таблице 12.
|
Неонатальные нежелательные явления
Имело место дозозависимое увеличение количества субъектов с неонатальными АЕ (39,8%, 42,4% и 48,9%) из-за более высокой частоты явлений, не связанных с исследуемым лекарственным средством, включая врожденные аномалии и пуповину вокруг шеи, в группе лечения MVI 200.
Наиболее часто регистрируемыми АЕ были нежелательные явления, относящиеся к Системе организма Беременность, Послеродовые и Перинатальные состояния (29,9% субъектов). Наиболее часто регистрируемыми АЕ в этой системе организма были пуповина вокруг шеи (12,6%), неонатальная гипербилирубинемия (11,0% субъектов) и родовая опухоль (4,3% субъектов). Неонатальных SAE, связанных с лечением, не было. Данные приведены в Таблице 13.
|
Обсуждение безопасности
При применении MVI 200 наблюдалась самая низкая частота родоразрешений посредством кесарева сечения (31,4%, 30,4% и 22,9% для групп лечения MVI 100, MVI 150 и MVI 200 соответственно). Общая частота нежелательных явлений была сходной во всех трех группах лечения.
Родоразрешения посредством кесарева сечения во всех группах были следствием нежелательных явлений (23,3% субъектов; прежде всего необнадеживающая частота сердечных сокращений у плода (11,0%) и дистоция (5,9%)), недостаточная эффективность (3,2%) и отсутствие родовой деятельности (1,6%). Родоразрешения посредством кесарева сечения, вызванные нежелательным явлением, относящимся к MVI, происходили у 2,9% субъектов (2,5%, 2,4% и 3,8% для MVI 100, MVI 150 и MVI 200 соответственно).
При применении MVI 200 наблюдалась самая высокая инцидентность маточных явлений, включая аномальные схватки (тахисистолия), влияние аномальных родов на плод (синдром гиперстимуляции матки) и гипертонус. При применении MVI 200 наблюдалась самая высокая частота прерывания введения лекарственного средства из-за нежелательного явления и самая высокая частота нежелательных явлений, связанных с лекарственными средствами. Маточные явления не приводили к увеличению частоты родоразрешений посредством кесарева сечения.
Родоразрешение посредством кесарева сечения
Данные по родоразрешению посредством кесарева сечения приведены в Таблице 15.
|
Сравнение с CervidilTM
Данные сравнения времени до родоразрешения приведены в Таблице 16.
|
Обсуждение
В исследовании 374 женщин с незрелой шейкой матки, требующей стимуляции родов, и по сравнению с более низкой дозой одного и того же продукта авторы изобретения обнаружили, что введение вкладыша, содержащего мизопростол и поперечно-сшитый гидрогелевый полимер на основе полиуретана, вызывает у женщин активные роды на 6 часов быстрее (p<0,001); сокращает среднее время до родоразрешения через естественные родовые пути на 9 часов (p=0,018); сокращает среднее время до родоразрешения на 6 часов (p<0,001); увеличивает число родоразрешений через естественные родовые пути в пределах периода времени 12 ч (р=0,022) и 24 ч (р=0,057); снижает потребность в стимуляции окситоцином; менее 50% женщин требуется окситоцин по сравнению с >70% в группе сравнения (p<0,001); снижает частоту случаев кесарева сечения на 9 процентов (31,4% против 22,9%); снижает частоту кесаревых сечений; и наблюдаемый средний балл по шкале Апгар у новорожденного составляет 8 в возрасте одна минута и 9 в возрасте пять минут.
MVI идентифицирован как эффективный агент, который безопасно могут применять женщины с момента незрелой шейки матки и отсутствия схваток для активных, эффективных родов. MVI 200 безопасно и эффективно сокращает время до родоразрешения. По сравнению с MVI 100 MVI 200 сокращает среднее время родоразрешения через естественные родовые пути (p=0,018), сокращает время до родоразрешения (p<0,001), требует меньшего использования окситоцина (p<0,001) и имеет больше родоразрешений через естественные родовые пути в пределах периода времени 12 часов (р=0,022) и 24 часа (р=0,057). Эти результаты достигаются без какого-либо негативного влияния на безопасность, что доказано снижением относительного риска родоразрешения посредством кесарева сечения для женщин, которых лечили MVI 200 (0,73, 95% Cl от 0,41 до 1,10).
Все три протестированные дозы, MVI 100, MVI 150 и MVI 200, были безопасными и хорошо переносимыми. Во время исследования не было случаев смерти и не было субъектов, прекративших исследование в связи с нежелательным явлением (АЕ). Не было неожиданных серьезных нежелательных реакций. Нежелательные явления, наблюдаемые во время исследования, были явлениями, ожидаемыми в популяции женщин в целом, и их новорожденные прошли процесс рождения.
Перед удалением лекарственного средства медсестрами и лечащими клиницистами сократительная деятельность матки, в частности тахисистолия, хорошо переносилась плодом и женщиной во всех группах лечения. Ни одно из маточных сократительных явлений не привело к родоразрешению посредством кесарева сечения при применении MVI 200 или MVI 150; один субъект, получавший MVI 100, имел родоразрешение посредством кесарева сечения из-за синдрома гиперстимуляции.
Не наблюдалось различий в частоте серьезных нежелательных явлений во время родов (SAE) для групп лечения MVI 100, 150 и 200 (25,4%, 24,8% и 22,1% соответственно). Во время родов SAE, связанные с лекарственным средством, имели место у 2,5%, 2,4% и 3,8% субъектов соответственно. Количества SAE были также низкими и сходными после родов и в неонатальные периоды, и не было родственных SAE в любой группе лечения в послеродовой период или неонатальный период.
Среди трех групп лечения наблюдалась четкая зависимость доза-ответ в пользу эффективности MVI 200. Матери, которых лечили MVI 200, вступали в роды скорее и рожали своих младенцев быстрее, причем с меньшим использованием окситоцина. Самым важным для оценки общей безопасности является то, что частота родоразрешений посредством кесарева сечения была самой низкой для женщин, получавших MVI 200. Сокращение времени до родоразрешения связано с улучшением безопасности, мерой которой служило снижение числа родоразрешений посредством кесарева сечения.
В одном из воплощений вагинальный вкладыш, содержащий мизопростол, высвобождает приблизительно 1/24-ую часть от общей дозы в час.
Пример 4 - Вторичный анализ
Вторичный анализ проводили по данным, собранным в рандомизированном контролируемом испытании мизопростолового вагинального вкладыша (MVI) (Powers BL, Rayburn WF; Misoprostol Vaginal Insert for Successful Labor Induction: A Randomized Controlled Trial. Obstet Gynecol. 2011 Mar; 117 (3): 533-541, полное содержание которого включено в данное описание посредством ссылки). Первоначальное испытание было многоцентровым, двойным слепым, рандомизированным исследованием, в котором сравнивали эффективность и безопасность трех вагинальных вкладышей с длительным высвобождением, содержащих 100 мкг мизопростола (MVI 100), 150 мкг мизопростола (MVI 150) и 200 мкг мизопростола (MVI 200). В этом исследовании были задействованы одиннадцать центров по всей стране. Коротко, участники имели возраст по меньшей мере 18 лет с небольшим количеством родов в анамнезе (три или меньше) с одноплодной беременностью и со сроком беременности по меньшей мере 36 недель 0 суток. После ультразвукового подтверждения затылочного предлежания плода каждая участница проходила кардиографическое (CTG) обследование в течение по меньшей мере 15 минут, чтобы убедиться в обнадеживающем статусе плода и подтвердить отсутствие показаний со стороны матки для активных родов.
Одна задача этого вторичного анализа состояла в том, чтобы описать частоту и синхронизацию частоты сердечных сокращений у плода (FHR) и кардиографических (CTG) аномалий и полученных в результате клинических показателей, наблюдаемых во время Фазы II исследования в дозовом диапазоне депо доз MVI 100, MVI150 и MVI 200 у субъектов, которым требовалось обеспечение созревания шейки матки для стимуляции родов.
Первоначальное исследование проводили по принципу рандомизированной, двойной слепой модели, и вагинальные вкладыши MVI 100, MVI 150 и MVI 200 были идентичными по внешнему виду. Рандомизированное назначение обеспечивали с помощью выданных компьютером, последовательно пронумерованных в произвольном порядке наборов для каждой когорты (нерожавшие и рожавшие). Действие вагинального вкладыша прекращали при начале активных родов, выпадании лекарственного средства из влагалища, окончании 24-часового периода введения дозы, осложнениях у матери/плода, включая маточные сократительные аномалии или необнадеживающий паттерн FHR, и по требованию матери. Использовали единообразные определения для маточных сократительных аномалий и других нежелательных явлений, как в предыдущем исследовании, за исключением показателей FHR и сократительной деятельности матки. Синдром гиперстимуляции определяли как сочетание любого необнадеживающего паттерна FHR с тахисистолией или гипертонусом. Показатели FHR определяли для этого протокола с использованием категорий NIHCD (Национальный институт детского здоровья и развития человека), включенных в данное описание посредством ссылки. Термин "необнадеживающий паттерн FHR, требующий немедленного клинического вмешательства" регистрировали как неблагоприятное явление для явлений Категории II и Категории III, и картина угрозы должна была быть идентифицирована. Традиционные вмешательства для лечения необнадеживающей FHR применяли, если это было целесообразно, по усмотрению лечащего врача.
В целях исследования необнадеживающий паттерн частоты сердечных сокращений у плода может быть определен как любой паттерн частоты сердечных сокращений у плода, требующий немедленного клинического вмешательства, включая одно или более из следующего: брадикардия у плода (исходная частота сердечных сокращений у плода падает до менее чем 110 ударов в минуту); тахикардия у плода (исходная частота сердечных сокращений у плода увеличивается до более чем 160 ударов в минуту); необъяснимое отсутствие нормальной изменчивости 5-15 ударов в минуту; ранние замедления (начало замедления происходит в начале сокращения; амплитуда замедления составляет 40 ударов в минуту или меньше); позднее замедление (любое замедление, когда наименьшая точка происходит через более чем 15 с после пика сокращения; амплитуда замедления составляет 40 ударов в минуту или меньше); вариабельные замедления (непостоянные по форме и по их взаимосвязи с сокращениями матки; тенденция к амплитуде 40 ударов в минуту или меньше); пролонгированные замедления (падение частоты сердечных сокращений у плода составляет 30 ударов в минуту или больше, длящееся по меньшей мере 2 мин); любые другие показатели частоты сердечных сокращений у плода, которые требуют немедленного вмешательства. В целях исследования гипертонус матки может быть определен как сокращение, длящееся по меньшей мере 2 мин; так называемые тетанические сокращения или гипертонус матки. В целях исследования маточная тахисистолия может быть определена как частота более чем пять сокращений за период времени 10 мин. В целях исследования синдром гиперстимуляции матки может быть определен как гипертонические или тахисистолические сокращения матки, ассоциированные с необнадеживающим паттерном частоты сердечных сокращений у плода и/или ацидозом плода.
В целях исследования группу лечения MVI 100 считали группой сравнения. Исходя из основного конечного показателя эффективности, получали оценку объема выборки для сравнения групп лечения MVI 100 и MVI 200. Поскольку данное исследование представляло собой исследование в диапазоне доз, группа MVI 150 была включена для того, чтобы гарантировать возможность идентификации наименьшей эффективной дозы.
Статистические анализы выполняли с использованием статистического программного обеспечения SAS, версия 8.2, и все тесты представляли собой двусторонние тесты, оцениваемые на уровне значимости 0,05. Сравнения регистрировали с использованием группы MVI 100 в качестве контроля. Для исходных характеристик непрерывные переменные оценивали с использованием однофакторного дисперсионного анализа (ANOVA) категорийных переменных, оцениваемых с использованием точного критерия Фишера или критерия хи-квадрат.
В сумме 374 женщины были включены в это исследование за период времени примерно восемь месяцев. Демографические и исходные характеристики участниц были сравнимыми в группах (Таблица 17) за исключением показаний для стимуляции: больше женщин, получавших MVI 200, подверглись плановой стимуляции и больше женщин, получавших MVI 100, подверглись стимуляции из-за гипертензии, чем в других группах. Среднее значение mBS при регистрации составляло 3 (диапазон 0-4) для всех трех групп лечения.
Удаление исследуемого вкладыша, содержащего лекарственное средство, из-за нежелательного явления было более частым в случаях MVI 200 и MVI 150 по сравнению с MVI 100, но эти нежелательные явления, приводящие к удалению, почти всегда были связаны с диагностированной в прошлом тахисистолией. Было также установлено, что этот метод дает результаты наблюдений, которые отличаются от оценки на месте, и результаты приведены в виде таблицы нежелательных явлений, которые часто были хорошо переносимыми и не приводили к отмене исследуемого лекарственного средства. Хотя было много случаев аномалий FHR и CTG, деление на категории конкретных типов аномалий и их клинических последствий в отношении кесарева сечения или неблагоприятного исхода для плода не отличалось существенно среди групп. В целом, было обнаружено, что паттерны FHR соответствуют Категории II или III NICHD (Национальный институт детского здоровья и развития человека) у большинства субъектов (58,0% в целом) на некоторой стадии их родов; большинство из них оказались не связанными с MVI. Паттерны Категории II или III, оцениваемые как связанные с использованием MVI, имели место у 9/75 (7,6%), 27/125 (21,6%) и 22/131 (16,8%) субъектов, получавших MVI 100, 150 и 200 соответственно (p=0,03 для MVI 100 относительно MVI 200). Однако NRFHR (необнадеживающая частота сердечных сокращений у плода) как причина кесарева сечения имела место у 11 (9,3%) субъектов группы MVI 100 против 18 (13,7%) субъектов группы MVI 200, то есть без значительной разницы (p=0,33).
MVI 200 ассоциировался с увеличением частоты тахисистолии (54/131, 41,2%) по сравнению с MVI 100 (23/118, 19,5%) (p<0,001, RR 2,11, 95% Cl 1,39, 3,22) и MVI 150 (32/135, 25,6%) (р=0,26, RR 1,31, 95% CI 0,82, 2,11) (Таблица 18). Тахисистолия возникала с лекарственным средством in situ у 17 (14,4%) и 50 (32,8%) субъектов группы MVI 100 и 200 соответственно (p<0,001). Паттерны FHR Категории II или III наблюдались после возникновения тахисистолии у 9 (7,6%) и 26 (19,8%) женщин в группах MVI 100 и 200 соответственно (p=0,006). Однако синдром гиперстимуляции матки возникал у 8 (6,8%), 12 (9,6%) и 16 (12,2%) субъектов групп MVI 100, 150 и 200 соответственно (p=0,49 для MVI 150 против MVI 100 и р=0,20 для MVI 200 против MVI 100) (Таблица 18).
Пути родоразрешения не различались среди групп лечения или в пределах этих групп для нерожавших пациентов и неоднократно рожавших пациентов с 28% от всех пациентов, родивших посредством кесарева сечения. Из них самым распространенным показанием для кесарева сечения была NRFHR, которая незначительно различалась между группами лечения. Время от начала тахисистолии до кесарева сечения составляло 8,3 (2,5-31,2) часов для MVI 100; 17,7 (2,1-74,2) часов для MVI 150; и 15,5 (3,3-39,1) часов у субъектов, которые рожали посредством кесарева сечения, что свидетельствует о том, что очень немногие из этих явлений были экстренными по своей природе. Неонатальные исходы также были сравнимыми между группами лечения с отсутствием различия в окрашенной меконием жидкости, аспирации мекония, баллах по шкале Апгар, неонатальной респираторной затрудненности, преходящего транзиторного тахипноэ новорожденного или поступлением в NICU.
Этот вторичный анализ рандомизированного, двойного слепого исследования с изменением дозы позволил произвести сравнение инцидентности и распределения во времени аномалий CTG и FHR, возникающих при использовании трех увеличивающихся доз мизопростола, и подтверждает профиль безопасности мизопростола, применяемого для обеспечения созревания шейки матки. Так как показания становятся все более распространенными и оказывают более сильное влияние на будущую акушерскую практику, важно идентифицировать безопасный и эффективный стимулирующий агент. В идеале, этот агент должен снижать время до родоразрешения без увеличения числа случаев кесарева сечения или риска подвергнуть опасности мать или плод.
Было продемонстрировано в начальном исследовании, что MVI 200 значительно сокращает время до родоразрешения, а также время до родоразрешения через естественные родовые пути и обеспечивает значительно большее число родоразрешений через естественные родовые пути за 12 часов или менее по сравнению с MVI 100. Он также снижает потребность в стимуляции родов окситоцином, но было обнаружено, что при его использовании наблюдается значительно больше эпизодов тахисистолии по сравнению с MVI 100. Однако эти тахосистолические явления не приводили к увеличению числа случаев кесарева сечения, связанных с аномалиями FHR или CTG, или они ассоциировались с более высокой частотой плохих неонатальных исходов. Фактически, большинство диагнозов тахисистолии ставили ретроспективно (post-hoc), и это, как полагают, указывает на то, что специалисты, обеспечивающие медицинское обслуживание исследуемых субъектов, уделяли мало внимания, когда она обнаруживалась, или что она вообще могла остаться незамеченной.
Во всех группах лечения наблюдались аномалии FHR и CTG по их показаниям, но ни одна из групп не продемонстрировала существенно отличающуюся частоту родоразрешений посредством кесарева сечения вследствие этих аномалий. Было установлено, что из участниц, которым удаляли исследуемое лекарственное средство из-за осложнения у матери/плода, и которые позднее подвергались кесареву сечению, только у 2,1% это было связано с исследуемым лекарственным средством. Из 41 участницы, у которых было родоразрешение посредством кесарева сечения на фоне аномалии CTG, ни одна не рожала за менее чем 2,11 часов, что указывает на то, что эти кесарева сечения были неэкстренными. Это свидетельствует о важном преимуществе вагинального вкладыша, содержащего мизопростол, в отличие от вагинальных таблеток, которое заключается в том, что он может быть быстро и полностью удален в случае неблагоприятного явления.
Среди групп не было значительных различий по числу случаев кесарева сечения или фетального неблагоприятного исхода, хотя 58% участниц имели паттерны Категории II или III во время родов.
Мизопростоловый вагинальный вкладыш значительно сокращал время до родоразрешения, а также до родоразрешения через естественные родовые пути и снижал потребность в увеличении дозы окситоцина. Мизопростоловый вагинальный вкладыш представляет собой безопасный, эффективный и точно дозируемый агент, обеспечивающий созревание шейки матки, и имеет дополнительное преимущество в том, что его можно быстро удалить.
Ограничения вторичного исследования включают его ретроспективный (post-hoc) характер, а также межцентровую вариабельность при сборе и интерпретации данных по этим нежелательным явлениям. Объем выборки в этом анализе также является ограничивающим, так как выборка была слишком маленькой для идентификации статистических различий при редких материнских или фетальных нежелательных явлениях. В целом, субъекты группы MVI 200 рожали быстрее и с меньшей дозой окситоцина, и хотя они чаще испытывали тахисистолию, это не было связано со значительным увеличением числа кесаревых сечений. Учитывая эти результаты, вагинальный вкладыш, содержащий мизопростол, представляет собой безопасный, общеизвестный и эффективный агент, обеспечивающий созревание шейки матки, в форме, обеспечивающей более точное дозирование, и с возможностью безопасного быстрого прерывания его действия, когда это требуется.
|
|
Содержание указанных ниже публикаций независимо включено в данное описание посредством ссылки: "Vaginal Misoprostol for Cervical Ripening and Induction of Labor (Review)" Hofmeyr, G.J., Gulmezoglu, A.M., The Cochrane Library 2009, Issue 1; "Controlled-Release Misoprostol Vaginal Insert in Parous Women for Labor Induction", Ewert, K. et al., Obstet. Gynecol. 2006; 108: 1130-7; "Pharmacokinetic Profiles of Controlled-Release Hydrogel Polymer Vaginal Inserts Containing Misoprostol", Powers, B.L., et al., J. Clin. Pharmacol. 2008; 48: 26-34; "Pharmacokinetics of a Controlled-Release Misoprostol Vaginal Insert at Term", Rayburn, W.F., et al., J. Soc. Gynecol. Investig. 2006; 13: 112-7; "Misoprostol Dose Selection in a Controlled-Release Vaginal Insert for Induction of Labor in Nulliparous Women", Castaneda, C.S., et al., Am. J. Obstet. Gynecol. 2005; 193: 1071-5; Martin JA, Hamilton BE, Sutton PD, Ventura SJ, Menacker F, Kirmeyer S, et al. "Births: Final Data for 2007". Natl Vital Stat Rep 2010; 58:1-125; Wing DA. "Labor Induction with Misoprostol". Am J Onstet Gynecol 1999;181:339-45;;Keirse MJ. "Prostaglandins in Preinduction Cervical Ripening: Meta-Analysis of Worldwide Clinical Experience". J Reprod Med 1993; 38:89-100; Rath W. A "Clinical Evaluation of Controlled-Release Dinoprostone for Cervical Ripening - A Review of Current Evidence in Hospital и Outpatient Settings". J Perinat Med 2005; 33:491-9; Alfirevic Z, Weeks A. "Oral Misoprostol for Induction of Labour". The Cochrane Database of Systemic Reviews 2006, Issue 2. Art. No.: CD001338. DOI: 10.1002/14651858.CD001338; Wing DA; "Misoprostol Vaginal Insert Consortium. Misoprostol Vaginal Insert Compared with Dinoprostone Vaginal Insert: A Randomized Control Trial". Obstet Gynecol 2008; 112: 801-12; Powers BL, Rayburn WF; " Misoprostol Vaginal Insert for Successful Labor Induction: a Randomized Controlled Trial". Obstet Gynecol. 2011 Mar; 117 (3): 533-541; Caughey AB, Sundaram V, Kaimal AJ, Cheng YW, Gienger A, Little SE, et al. "Maternal and Neonatal Outcomes of Elective Induction of Labor". Evid Rep Technol Assess 2009; 176: 1-257; Macones GA, Hankins GDV, Spong CY, Hauth J, Moore T. "The 2008 National Institute of Child Health and Human Development Workshop Report on Electronic Fetal Monitoring - Update on Definitions, Interpretation, and Research Guidelines". Obstet Gynecol 2008; 112: 661-6; Заявка Великобритании №GB 2047093, опубликованная 26 ноября 1980 г.; заявка Великобритании №GB 2047094, опубликованная 26 ноября 1980 г.; патент США №4931288, выданный 5 июня 1990 г.; патент США №5269321, выданный 14 декабря 1993 г.; заявка США серийный №11/573,256, поданная 19 апреля 2007; и WO 2004/029125, опубликованная 8 апреля 2004 г.
Данная заявка основана на и имеет приоритет предварительной заявки на патент США серийный №61,353,835, поданной 11 июня 2010 г., полное содержание которой включено в данное описание посредством ссылки на нее.