Результат интеллектуальной деятельности: СПЕКТРОФОТОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ БЕЛКА В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ
Вид РИД
Изобретение
Изобретение относится к биохимии и может быть использовано в лабораторной практике для определения содержания белка в биологических жидкостях (моче, спинномозговой жидкости, ликворе, сыворотке, плазме крови и т.д.).
На сегодняшний день самым распространенным и широко применяемым в клинической биохимии методом определения общего белка в биологических жидкостях является спектрофотометрический метод.
Известен и широко применим в клинико-биохимических исследованиях способ определения концентрации белка в биологическом материале, в основе которого лежит реакция взаимодействия ионов меди с пептидными связями в молекуле белка в присутствии сильного основания (биуретовый метод). [Dilena В.А., Penberthy L.A., Fraser C.G. Clin. Chem. 1983. V. 29. P. 553-557], [Marshall Т., Williams K.M. Clin. Chem. 2000. V. 46. P. 392-398]. Интенсивность окраски образующегося комплекса зависит от концентрации белка и может быть оценена как с помощью анализаторов (автоматических и полуавтоматических), так и обычных фотометров. Метод характеризуется высокой аналитической надежностью, специфичностью и позволяет определять белок в широком диапазоне концентраций. Однако способ не обладает чувствительностью при определении минимальных количеств белка.
Известен метод Лоури [Альтшулер Б.Ю., Раков С.С., Ткачев Г.А. Вопросы медицинской химии. 2001. №4. С. 426-438], сочетающий биуретовую реакцию и реакцию Фолина на аминокислоты, тирозин и триптофан в составе белковой молекулы. Он обладает более высокой чувствительностью по сравнению с биуретовым методом, однако возможно неспецифическое взаимодействие реактива Фолина с небелковыми компонентами (чаще всего со свободными ароматическими аминокислотами и многими другими соединениями, содержащими фенольную группу), способными оказывать влияние на данную реакцию и искажать результаты исследования.
Известны спектрофотометрические способы определения белка в биологических жидкостях, основанные на связывании протеина с органическими красителями, обеспечивающими лучшую воспроизводимость результатов. В качестве красителей могут использоваться: кумасси бриллиантовый синий (Coumassie Brilliant Blue) [Bradford M.M. Anal. Biochem. 1976. V. 72. P. 248-254], бромфеноловый синий [патент РФ №2250465, МПК7 G01N 33/52, опубл. 20.04.2005], бромкрезоловый зеленый [Инструкция по применению набора реагентов для определения содержания альбумина в сыворотке и плазме крови человека. АЛЬБУМИН ФС. Утверждена Приказом Росздравнадзора от 15 апреля 2009 г. №3004 - Пр/09 РУ № ФСР 2009/04712 от 06.02.2009 г.], пирогаллоловый красный [Инструкция по применению набора реагентов для количественного определения общего белка в моче и СМЖ с пирогаллоловым красным. ОБЩИЙ БЕЛОК ПГК ФС. «Диакон-ДС». Утверждена приказом Росздравнадзора от 20.06.2010 г. №6830-Пр/10 РУ № ФСР 2007/01435 от 07.05.2010]. В результате реакции молекул белка с органическим красителем образуется окрашенное соединение, интенсивность окраски которого пропорциональна концентрации белка в пробе.
Недостатками этих методов является неодинаковая чувствительность каждого из красителей к различным белкам, что приводит к заметному искажению результатов при использовании калибраторов различного состава и появлению дополнительных ошибок при определении общего белка в биологических жидкостях. Наличие лекарственных препаратов в исследуемых биологических жидкостях оказывает влияние на оптическую плотность растворов, кроме того, сорбция красителей на стенках кювет ограничивает применение методов в лабораторной практике для рутинных анализов.
Наиболее близким к заявляемому техническому решению является способ количественного определения белка в биологических жидкостях [патент РФ №2268476, МПК7 G01N 33/68, опубл. 20.01.2006]. Для определения концентрации белка в биологической жидкости указанным способом осуществляют:
- смешивание образца биологической жидкости с реактивом-комплексообразователем,
- инкубацию пробы в течение 10 мин при комнатной температуре,
- измерение оптической плотности пробы фотометрически при длинах волн в диапазоне 600-700 нм,
- определение концентрации белка стандартным образом.
При этом используют реактив-комплексообразователь, содержащий в качестве органического красителя пирогаллоловый красный, молибдат натрия, янтарную кислоту, ацетат натрия, низкоатомный спирт и стабилизатор, воду при следующих соотношениях компонентов (в масс. %): молибдат натрия - (0.6-1.6)×10-3; пирогаллоловый красный - (1.0-2.0)×10-3; янтарная кислота - 0.4-0.7; ацетат натрия - 0.04-0.10; низкоатомный спирт - 8.0-16.0; стабилизатор - 0.03-1.0; вода - остальное.
Реактив-комплексообразователь в качестве низкоатомного спирта может содержать этанол, метанол или другой, а в качестве стабилизатора - любой неионогенный ПАВ.
Смешивание биологической жидкости с реактивом-комплексообразователем ведут в соотношении 1:(10-50).
Недостатком прототипа является различие в чувствительности пирогаллолового красного к альбумину и белкам глобулинового ряда, что приводит к ошибкам в случае определения общего белка в биологических жидкостях при использовании калибраторов разного состава, а также возможность использования указанного способа для определения содержания общего белка только в моче и спинномозговой жидкости.
Техническим результатом заявляемого технического решения является минимизация погрешности в определении общего белка в биологических жидкостях разного вида.
Для достижения технического результата предлагается смешивать образец биологической жидкости с раствором реагента, содержащим следующие компоненты: бромпирогаллоловый красный, молибдат натрия оксалат натрия, янтарную кислоту и воду. Концентрации компонентов в растворе реагента (масс. %):
бромпирогаллоловый красный - (1.5-4.0)×10-3;
молибдат натрия - (0.5-1.5)×10-3;
оксалат натрия - 0.01-0.03;
янтарная кислота - 0.4-0.7;
вода - остальное.
Смешивают образец биологической жидкости и раствор реагента в соотношении 1:(5-200) соответственно и измеряют оптическую плотность пробы при длине волны в диапазоне 580-620 нм относительно холостой пробы, а затем определяют концентрацию белка методом градуировочного графика или методом одного эталона.
Если проводят анализ биологических жидкостей с высоким содержанием белка, например плазма или сыворотка крови, ее следует разбавлять физиологическим раствором.
Предлагаемое техническое решение имеет с прототипом следующие общие признаки:
- смешивание биологической жидкости с реактивом - комплексообразователем ведут в соотношении 1:(10-50) соответственно;
- выдерживание при комнатной температуре;
- измерение оптической плотности пробы проводят фотометрически при длинах волн в более узком диапазоне;
- раствор реагента содержит органический краситель, молибдат натрия, янтарную кислоту, ацетат натрия, взятых в концентрациях (масс. %):
органический краситель - (1.0-2.0)×10-3;
молибдат натрия - (0.6-1.6)×10-3;
ацетат натрия 0.04-0.10;
янтарная кислота 0.4-0.7;
вода - остальное.
Оксалат натрия и ацетат натрия предназначены для создания постоянного значения рН раствора реагента и поддержания буферной емкости, т.е. являются эквивалентами.
Отличительными признаками являются:
- в состав раствора реагента входит в качестве органического красителя бромпирогаллоловый красный с содержанием (1.5-4.0)×10-3 масс. %;
- в состав раствора реагента входит оксалат натрия с содержанием 0.01-0.03 масс. %, взятый в меньшем количестве;
- инкубирование можно не проводить;
- смешивание образца биологической жидкости и раствора реагента проводят в соотношении 1:(5-200), т.е. в более широком диапазоне.
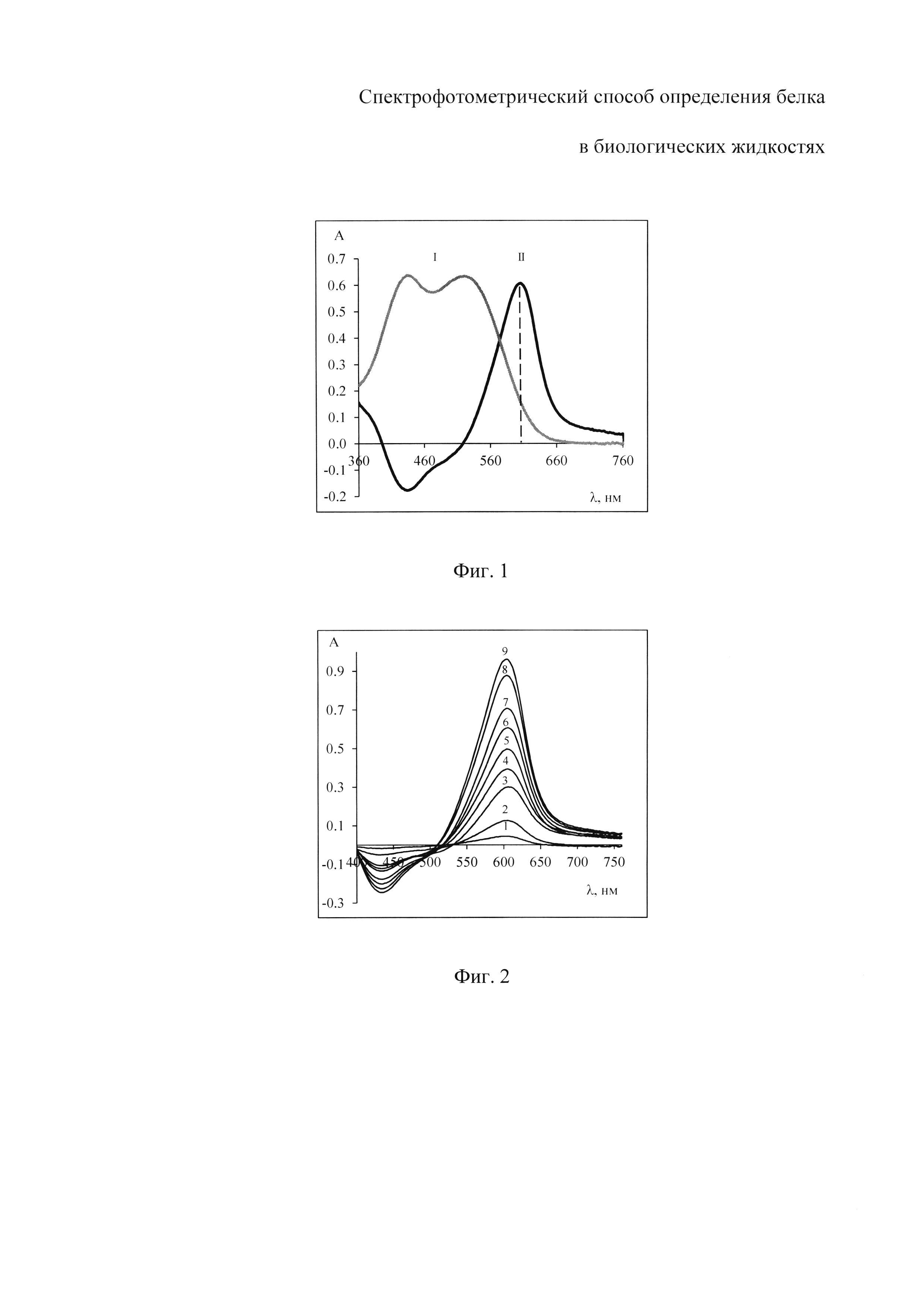
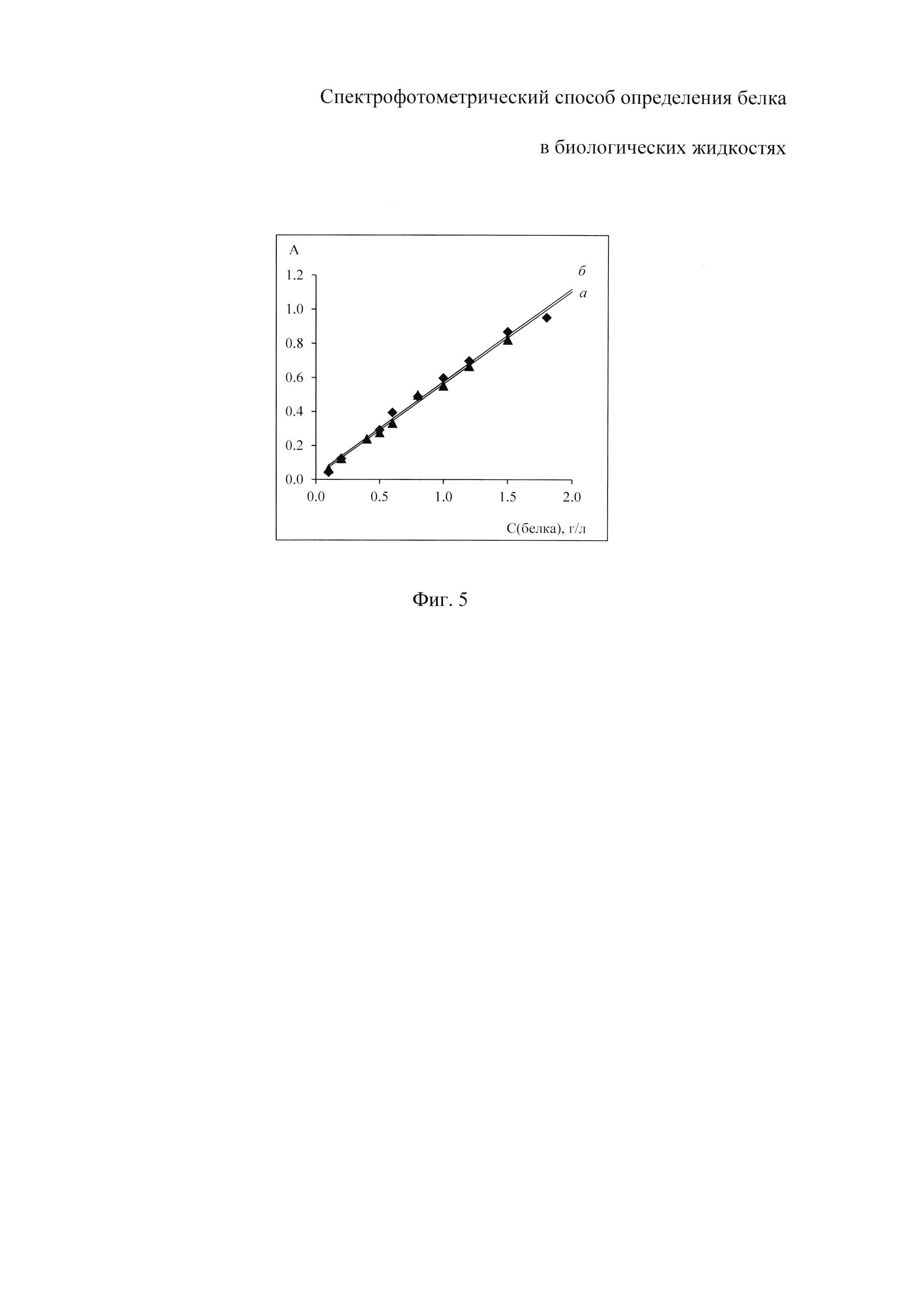
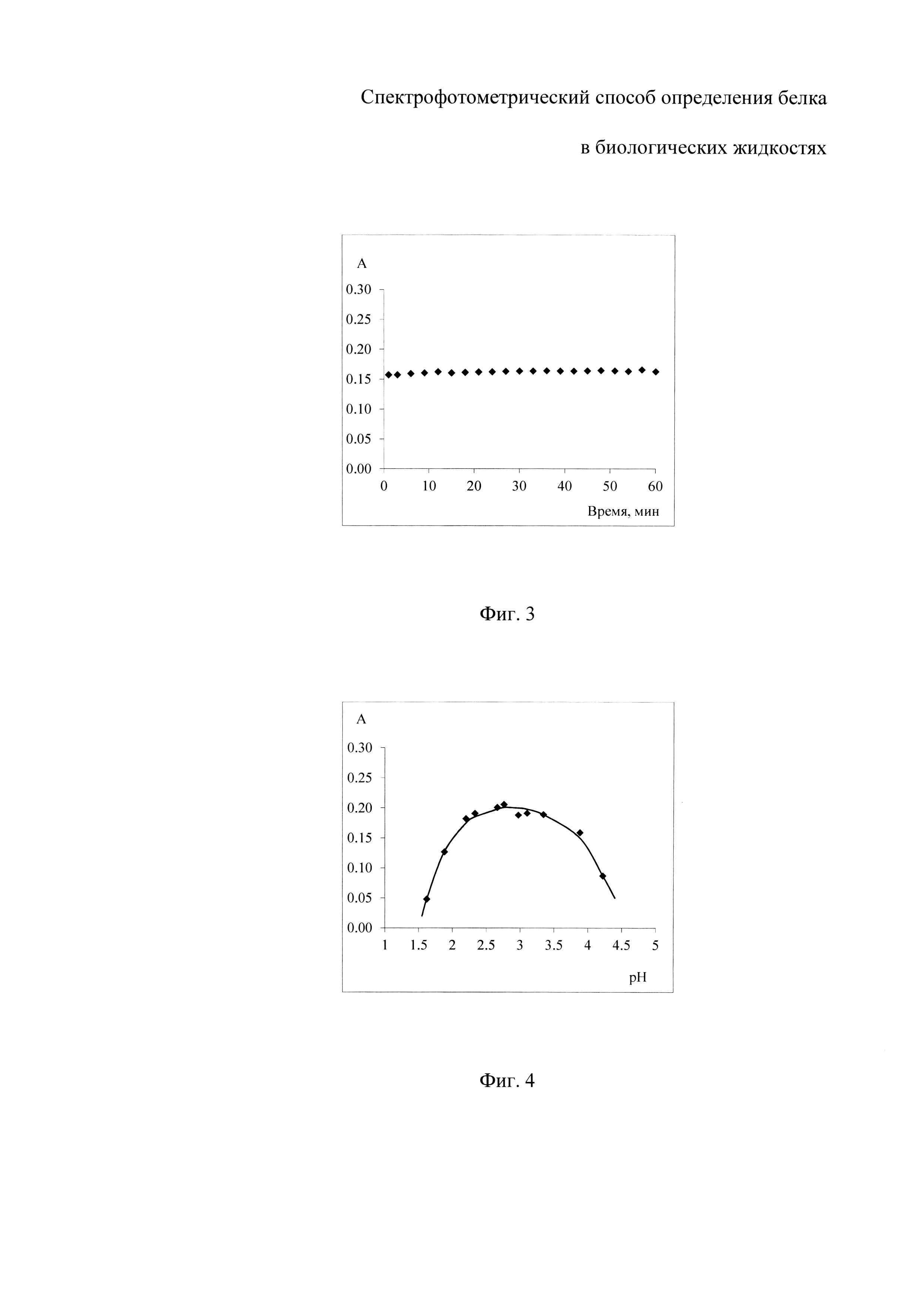
На фиг. 1 изображены спектры поглощения растворов комплекса бромпирогаллолового красного с молибденом (VI) (БПГК - Mo(VI)) - I и комплекса бромпирогаллолового красного с молибденом (VI) в присутствии белка - II с максимумом поглощения при длине волны 600 нм; на фиг. 2 - спектры поглощения растворов реагента с разной концентрацией общего белка: при 0.003 г/л - график 1; при 0.006 г/л - график 2; при 0.012 г/л - график 3; при 0.015 г/л - график 4; при 0.018 г/л - график 5; при 0.021 г/л - график 6; при 0.024 г/л - график 7; при 0.030 г/л - график 8; при 0.036 г/л - график 9; на фиг. 3 - графики зависимости оптической плотности раствора, содержащего БПГК - Mo(VI) и альбумин с концентрацией 0.002 г/л, при фиксированном значении рН и температуре 25°C от времени инкубации; на фиг. 4 - зависимость оптической плотности растворов с постоянной концентрацией альбумина 0.002 г/л от кислотности среды; на фиг. 5 - представлены градуировочные зависимости оптической плотности растворов от концентрации белка: общий белок - график а; альбумин - график б.
При осуществлении способа в результате смешения раствора реагента с раствором белка образуется трехкомпонентный комплекс БПГК - Mo(VI) - белок (фигура 1). Спектр поглощения раствора реагента имеет характерный вид с двумя максимумами поглощения - I (фиг. 1). При введении в систему молекул белка происходит образование трехкомпонентного соединения, и спектр поглощения сдвигается в область 580-620 нм - II (фиг. 1), максимум поглощения трехкомпонентного комплекса БПГК - Mo(VI) - белок наблюдается при длине волны 600 нм. При увеличении концентрации молекул белка в растворе происходит пропорциональное увеличение оптической плотности при длине волны 600 нм (фигура 2). Поскольку раствор реагента также поглощает при длине волны 600 нм, то в качестве холостой пробы следует использовать раствор, приготовленный смешиванием соответствующего объема раствора реагента и объема физиологического раствора, равного объему пробы (см. графики 1-9).
Концентрация БПГК и молибдата натрия в растворе реагента не должна быть меньше 1.5×10-3 и 0.6×10-3 масс. % соответственно, т.к. при меньших концентрациях этих компонентов сокращается диапазон линейности градуировочного графика. Использование концентраций, больших 4.0×10-3 и 1.6×10-3 масс. % соответственно, приводит к излишнему расходу реактивов.
Исследование времени формирования аналитического сигнала проводили путем измерения оптической плотности раствора, содержащего комплекс БПГК - Mo(VI) и альбумин с концентрацией 0.002 г/л, при фиксированном значении рН 2.5 и температуре 25°C через равные промежутки времени на спектрофотометре (UV-1800 «Shimadzu», Япония) в режиме «Кинетика». Полученные результаты, представленные на фигуре 3, показывают, что оптическая плотность растворов в пределах погрешности ее измерения остается постоянной в течение не менее 60 минут, что позволяет исключить обязательное инкубирование проб.
Для выбора оптимальной кислотности среды для проведения реакции между молекулами белка и реагентом готовили серию растворов с постоянной концентрацией альбумина и различной кислотностью среды и измеряли оптические плотности полученных растворов. Значение кислотности среды определяли с помощью рН-метра-иономера «Эксперт - 001». Кислотность варьировали в диапазоне значений 1.5-4.5 ед. рН добавлением разных количеств едкого натра или хлороводородной кислоты к исходному раствору в присутствии сукцинатного буфера. Эксперимент проводили для растворов с постоянной концентрацией альбумина 0.002 г/л при длине волны 600 нм. В соответствии с полученными данными был построен график зависимости оптической плотности растворов от кислотности (фигура 4) для раствора реагента с составом (масс. %): бромпирогаллоловый красный 3.5×10-3, молибдат натрия 1.0×10-3; янтарная кислота 0.6; оксалат натрия 0.01. Оптимальное значение кислотности среды для проведения реакции между комплексом БПГК-Mo(VI) и раствором белка предлагаем создавать введением янтарной кислоты с концентрацией 0.4-0.7 масс. %; и оксалатом натрия 0.01-0.03 масс. %. Введение оксалат ионов в состав раствора реагента способствует устранению их влияния при анализе белка в биологических жидкостях. Совместное присутствие оксалата натрия и янтарной кислоты способствует созданию требуемой буферной емкости раствора реагента, позволяющей сохранять оптимальное значение кислотности среды в пределах от 2.2 до 3.5 ед. рН даже при добавлении большого объема пробы. Меньшее содержание компонентов не обеспечивает достаточную буферную емкость реагента, а большее содержание приводит к неоправданно завышенному расходу реактивов.
С целью оптимизации состава раствора реагента к буферному раствору, содержащему БПГК - Mo(VI), янтарную кислоту и оксалат натрия, добавляли этиловый спирт 8.0-16.0 масс. % и поверхностно-активные вещества 0.03-1.00 масс. %. Как указано в прототипе, добавление этилового спирта в указанных количествах позволяет стабилизировать раствор реактива во времени, а добавление детергентов позволяет предотвратить выпадение осадка. Экспериментально установлено, что добавление детергентов в раствор реагента приводит к уменьшению срока хранения раствора, а добавление этилового спирта не влияет на устойчивость раствора реагента.
Исследовали диапазон линейности зависимости оптической плотности растворов от концентрации и предел обнаружения белка при использовании растворов реагента различного состава. Результаты эксперимента представлены в таблице 1.
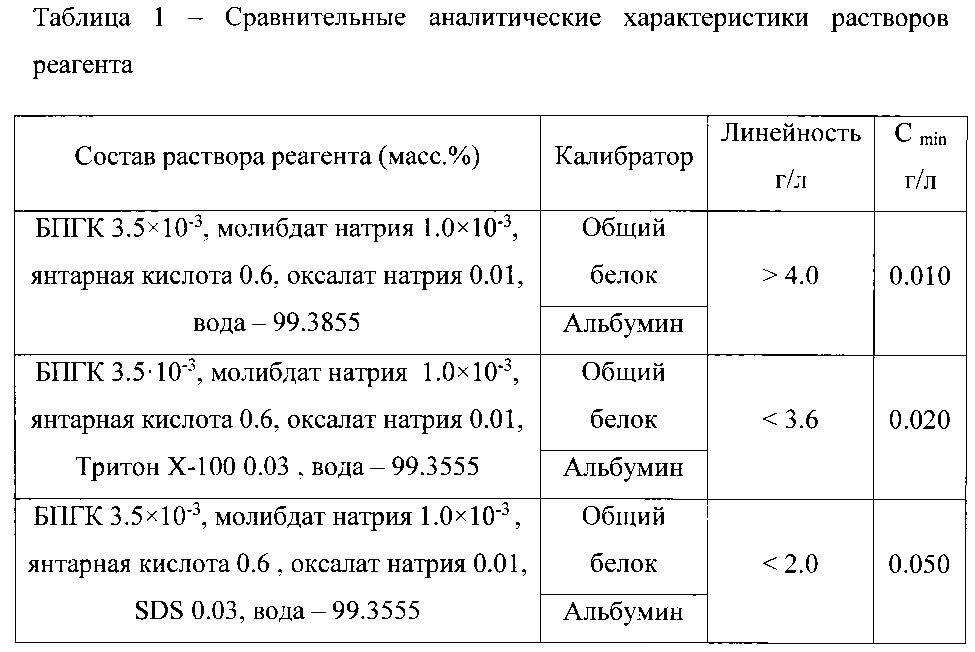
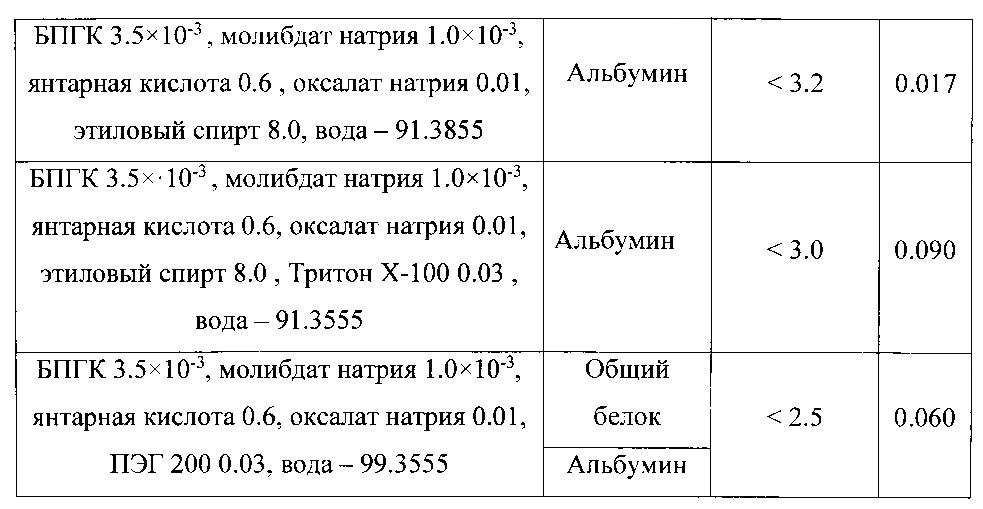
Полученные данные свидетельствуют о том, что введение в состав раствора реагента этанола и (или) детергентов не приводит к увеличению чувствительности и расширению диапазона определяемых содержаний белка. Применение более простого по составу раствора реагента, включающего только БПГК - Mo(VI), янтарную кислоту, оксалат натрия и воду, позволяет расширить диапазон линейности градуировочного графика, диапазон определяемых содержаний общего белка, а также уменьшить предел его обнаружения и экономить реактивы.
Для построения градуировочного графика в пробирки вносят раствор реагента и соответствующий объем стандартного раствора белка. Растворы перемешивают и измеряют оптическую плотность в кювете с толщиной слоя 1 см относительно холостой пробы на спектрофотометре при длине волны 600 нм. Холостая проба готовится добавлением к реагенту соответствующего объема физиологического раствора.
Градуировочные зависимости оптической плотности от концентрации альбумина и общего белка при их содержании в растворе до 2 г/л представлены на фигуре 5.
Предел обнаружения рассчитывали по общепринятой формуле:
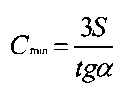
где S - стандартное отклонение фонового значения,
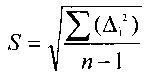
tgα - тангенс угла наклона градуировочной кривой.
Как видно из фигуры 5, градуировочные зависимости оптической плотности растворов от концентрации белка, построенные при использовании разных калибраторов - стандартного раствора альбумина и стандартного раствора общего белка - имеют одинаковый тангенс угла наклона. Значение предела обнаружения в обоих случаях составило 0.01 г/л, что говорит о практически одинаковой чувствительности реагента к белкам различной природы.
Таким образом, введение в состав раствора реагента бромпирогаллолового красного позволяет минимизировать или исключить ошибку, которая возникает в обычной практике при определении общего белка в случае использования в качестве калибратора стандартного раствора альбумина.
Проверку правильности определения общего белка в реальных объектах - образцах сыворотки крови и мочи. В первом случае результаты анализа сравнивали с данными, полученными независимым биуретовым методом. Для проб мочи использовали метод стандартных добавок. Содержание общего белка определяли по градуировочному графику и методом одного эталона. Данные эксперимента представлены в таблицах 2-3.
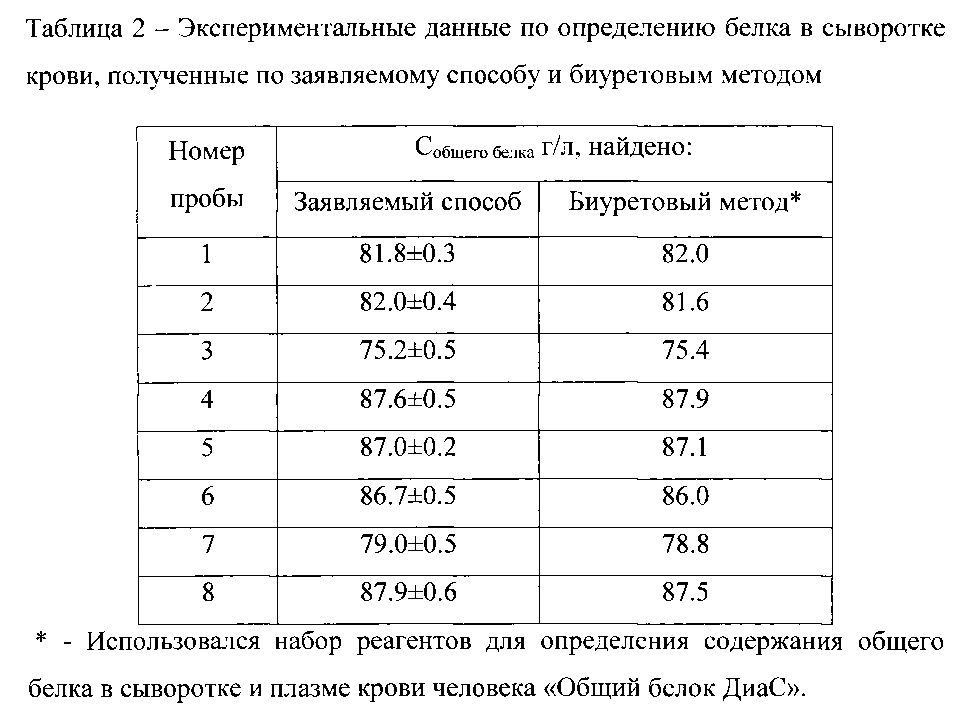
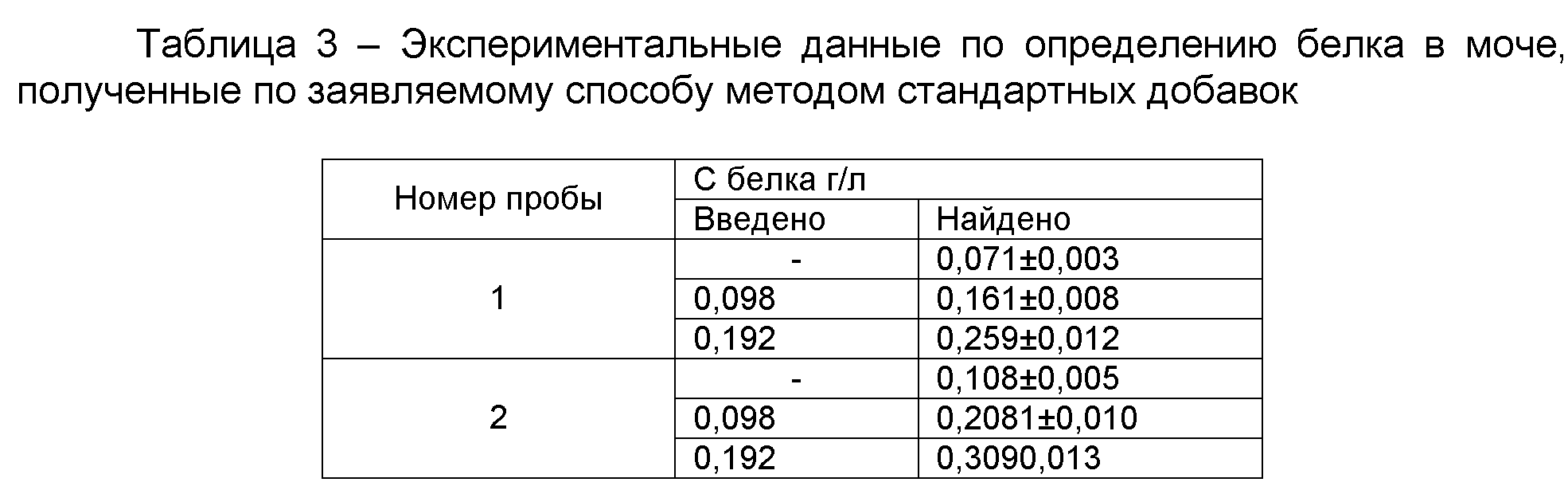
Таким образом, по сравнению с используемыми на практике способами определения общего белка в биологических жидкостях, предлагаемый способ характеризуется более широким диапазоном определяемых концентраций и большей чувствительностью.
Возможность варьирования кратности разведения анализируемых проб, а также высокая чувствительность предлагаемого способа и больший диапазон линейности позволяет проводить анализ как объектов с заведомо низким содержанием белка (моча, спинномозговая жидкость, ликвор), так и объектов, где содержание общего белка высоко (сыворотка и плазма крови). Отсутствие необходимости инкубирования проб позволяет сократить время анализа.
Одинаковая чувствительность бромпирогаллолового красного в составе предлагаемого реагента к белкам различной природы позволяет минимизировать погрешности в определении общего белка в биологических жидкостях, так как природа и состав калибратора при использовании указанного красителя не оказывает влияние на результаты определения общего белка.
Получаемый технический результат обеспечивается отличительными признаками заявляемого способа, т.е. он обладает изобретательским уровнем, новизной и может найти широкое практическое применение для количественного определения общего белка в биологических жидкостях при массовых клинико-диагностических исследованиях.