Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ЦИННАРИЗИНА
Вид РИД
Изобретение
Изобретение относится к области органической химии, в частности к способу получения (E)-1-(дифенилметил)-4-(3-фенилпроп-2-ен-1-ил)пиперазина (циннаризина).
Циннаризин - лекарственный препарат, относящийся к группе блокаторов кальциевых каналов. Он обладает сосудорасширяющим эффектом, улучшает мозговое и периферическое кровообращение, проявляет антигистаминную активность, уменьшает возбудимость вестибулярного аппарата, понижает тонус симпатической нервной системы. Циннаризин применяют при атеросклерозе сосудов головного мозга, ишемическом инсульте, черепно-мозговых травмах, головокружении, морской болезни, мигрени и других заболеваниях [Calcium Regulation by Calcium Antagonists. (ACS Symp.201). Ed. R.G. Rahwan, D.T. Witiak, 1982; Singh B.N. Br. J. Clin. Pharmacol. 1986, 21, 109S; Shupak A., Doweck I., Gordon, C.R., Spitzer O. Clin. Pharmacol. Ther. 1994, 55,670].
Результаты изобретения могут быть использованы в химии, медицинской химии и фармакологической промышленности.
Известны способы получения циннаризина на основе взаимодействия 1-(дифенилметил)пиперазина с циннамилхлоридом или коричным альдегидом, а также циннамилпиперазина с бензгидрилхлоридом или бромидом [Janssen P.A.J, патент US 2882271 (1959); Janssen P.A.J, патент DE 1086235 (1960); Weiler P. патент CH 605873 (1978); Wang J., Guan J., Li X., Xiao H., Jiang X. патент CN 103254152 (2013)]. Способы характеризуются недостаточно высоким выходом и использованием относительно труднодоступных циннамилсодержащих предшественников.
Наиболее близким к предлагаемому изобретению по типу металлокатализируемой реакции сочетания и взятому за прототип является способ получения циннаризина на основе трехкомпонентного сочетания с участием стирола, параформальдегида и 1-(дифенилметил)пиперазина в присутствии катализатора Pd(Xantphos)Cl2 [Xie Y., Hu J., Wang Y., Xia C, Huang H. J. Am. Chem. Soc. 2012, 134, 20613].
Данный метод имеет следующие недостатки:
- недостаточно высокий выход циннаризина (75%);
- высокая стоимость и токсичность Pd-катализатора.
Задачей изобретения является создание более эффективного и практичного способа получения циннаризина с более высоким выходом.
Указанная задача решается тем, что циннаризин (1) получают, согласно изобретению, Fe-катализируемым сочетанием 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), полученного аллилированием 1-(дифенилметил)пиперазина промышленно доступным (E)-1,3-дихлорпропеном (3), с фенилмагнийгалогенидом в апротонном растворителе в атмосфере инертного газа в присутствии соли железа (III).
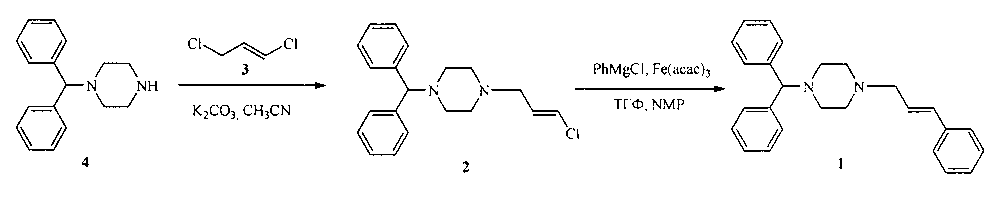
Способ осуществляют следующим образом. Смесь 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), катализатора [соли железа (III)] в апротонном растворителе и 0.5-3 М раствора фенилмагнийгалогенида в органическом растворителе (предпочтительно 1-2 М раствор PhMgCl в ТГФ) перемешивают при температуре от минус 40°С до плюс 50°С (предпочтительно при 0-25°С) в течение 0.1-8 ч (предпочтительно в течение 1-2 ч) в атмосфере инертного газа при следующем мольном соотношении реагентов [1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазин]: [соль железа (III)]: [фенилмагнийгалогенид] = 1:0.001-0.1:1-4 (предпочтительно 1:0.02:1.8).
В качестве катализатора используют соли железа (III), в частности Fe(acac)3, FeCl3, Fe(acac)2Cl, Fe(acac)Cl2, Fe(Pv)3 [предпочтительно Fe(acac)3] (асас=ацетилацетонат, Pv-пивалат).
В качестве апротонного растворителя используют простые эфиры [тетрагидрофуран (ТГФ), диметиловый эфир диэтиленгликоля (диглим), диэтиловый эфир диэтиленгликоля, диоксан] или их смеси с амидными растворителями [N-метилпирролидон (NMP), N,N-диметилформамид (ДМФА), N,N-диметилацетамид (ДМА)] (предпочтительно смесь ТГФ и NMP в объемном соотношении 300:1).
Пример 1. Получение 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2). К суспензии 1.22 г (0.011 моль) (Е)-1,3-дихлорпропена (3) и 2.07 г (0.015 моль) K2CO3 в 50 мл абсолютного ацетонитрила добавили 2.52 г (0.01 моль) 1-(дифенилметил)пиперазина (4). Перемешивали 0.5 ч при комнатной температуре, затем еще 4 ч при кипении до полной конверсии амина (4) (контроль методом ГЖХ). После охлаждения раствор фильтровали, осадок промывали этилацетатом и объединенные органические слои концентрировали. Продукт реакции очищали методом колоночной хроматографии (SiO2, гексан - этилацетат, 9:1→7:3). Выход 2.74 г (84%), бесцветные кристаллы, т.пл. 70-71°С. ИК спектр, ν, см-1: 2808, 2767, 1491, 1450, 1288, 1137, 1009, 947, 760, 706. Спектр ЯМР 1Н, δ, м. д.: 2.47 уш. с (8Н, CH2N), 2.99 д (2Н, СН2СН=, J 7 Гц), 4.22 с (1Н, Ph2CH), 5.96 д.т (1Н, СН2СН=, Jтpанc 13.2,7 Гц), 6.11 д (1Н, С1СН=, Jтpанc 13.2 Гц), 7.15 т (2Н, СНаром, J73 Гц), 7.25 т (4Н, СНаром, J 7.3 Гц), 7.40 д (4Н, СНаром, J 73 Гц). Спектр ЯМР 13С, δ, м.д.: 51.62 (2CH2N), 53.02 (2CH2N), 58.12 (СН2СН=), 76.04 (Ph2CH), 120.55 (ClCH=), 126.86 (2СНаром), 127.80 (4СНаром), 128.39 (4СНаром), 129.92 (СН2СН=), 142.54 (2Саром). Масс-спектр, m/z (Iотн, %): 326 (4) [М]+, 167 (39), 165 (23), 161 (31), 159 (100), 152 (17), 132 (16), 123 (25), 75 (25), 56 (13), 42 (17). Найдено [М]+ 326.1542. C20H23ClN2. Вычислено М 326.1550.
Пример 2. Получение (E)-1-(дифенилметил)-4-(3-фенилпроп-2-ен-1-ил)пиперазина (циннаризина) (1). К раствору 0.327 г (1 ммоль) 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), 7 мг (0.02 ммоль) Fe(acac)3 в смеси 3 мл ТГФ и 0.01 мл NMP медленно добавили по каплям при 0°С в атмосфере аргона 0.9 мл 2 М раствора PhMgCl в ТГФ. Перемешивали при комнатной температуре в течение 1 ч. Затем приливали 2 мл воды и 8 мл этилацетата, органический слой отделяли, водный слой обрабатывали этилацетатом (2×5 мл). Объединенные органические слои промывали насыщенным раствором NaCl, сушили Na2SO4 и концентрировали. Продукт реакции очищали методом колоночной хроматографии (SiO2, гексан - этилацетат, 9:1→3:1). Выход 0.331 г (90%), бесцветные кристаллы, т. пл. 120-121°С. ИК спектр, ν, см-1: 2809, 2768, 1492, 1450, 1143, 964, 749, 742, 707, 692. Спектр ЯМР 1Н, δ, м. д.: 2.52 уш.с (8Н, CH2N), 3.15 д (2Н, СН2СН=, J7 Гц), 4.23 с (1Н, Ph2CH), 6.26 д.т (1Н, СН2СН=, Jтpанc 15.9, 7 Гц), 6.49 д (1Н, PhCH=, Jтpанc 15.9 Гц), 7.13-7.28 м (9Н, СНаром), 7.34 д (2Н, СНаром, J 7.3 Гц), 7.40 д (4Н, СНаром, J 7.3 Гц). Спектр ЯМР 13С, δ, м.д.: 51.74 (2CH2N), 53.33 (2CH2N), 60.92 (СН2СН=), 76.08 (Ph2CH), 126.21 (2СНаром), 126.37 (СН2СН=), 126.80 (2СНаром), 127.36 (СНаром), 127.82 (4СНаром), 128.36 (4СНаром), 128.44 (2СНаром), 132.98 (PhCH=), 136.82 (Саром), 142.62 (2Саром). Масс-спектр, m/z (10ТН, %): 368 (1.2) [М]+, 251 (14), 202 (15), 201 (100), 167 (26), 165 (12), 152 (10), 118 (7), 117 (66), 115 (23), 91 (12). Найдено [М]+368.2249. C26H28N2. Вычислено М 368.2252.
Пример 3. Получение циннаризина (1). К раствору 0.327 г (1 ммоль) 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), 6 мг (0.02 ммоль) Fe(acac)2Cl в смеси 3 мл ТГФ и 0.01 мл NMP медленно добавили по каплям при 0°С в атмосфере аргона 0.9 мл 2 М раствора PhMgCl в ТГФ. Перемешивали при комнатной температуре в течение 1.5 ч. Операции по выделению продукта и его спектральные характеристики аналогичны приведенным в примере 2. Выход 0.325 г (88%).
Пример 4. Получение циннаризина (1). К раствору 0.327 г (1 ммоль) 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), 7 мг (0.02 ммоль) Fe(acac)3 в 3 мл ТГФ медленно добавили по каплям при 0°С в атмосфере аргона 0.9 мл 2 М раствора PhMgCl в ТГФ. Перемешивали при комнатной температуре в течение 2 ч. Операции по выделению продукта и его спектральные характеристики аналогичны приведенным в примере 2. Выход 0.313 г (85%).
Пример 5. Получение циннаризина (1). К раствору 0.327 г (1 ммоль) 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), 7 мг (0.02 ммоль) Fe(acac)3 в смеси 3 мл диглима и 0.01 мл ДМА медленно добавили по каплям при 0°С в атмосфере аргона 0.9 мл 2 М раствора PhMgCl в ТГФ. Перемешивали при комнатной температуре в течение 1.5 ч. Операции по выделению продукта и его спектральные характеристики аналогичны приведенным в примере 2. Выход 0.325 г (88%).
Пример 6. Получение циннаризина (1). К раствору 0.327 г (1 ммоль) 1-[(2E)-3-хлорпроп-2-ен-1-ил]-4-(дифенилметил)пиперазина (2), 7 мг (0.02 ммоль) Fe(acac)3 в смеси 3 мл ТГФ и 0.01 мл NMP медленно добавили по каплям при 0°С в атмосфере аргона 2 мл 1 М раствора PhMgBr в ТГФ. Перемешивали при комнатной температуре в течение 1 ч. Операции по выделению продукта и его спектральные характеристики аналогичны приведенным в примере 2. Выход 0.319 г (87%).
Предлагаемый способ имеет следующие преимущества:
- более высокий выход циннаризина (до 90%);
- низкая стоимость и малотоксичность катализатора.

