Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНО-16α,17α-ЦИКЛОГЕКСАНОПРЕГН-4-ЕН-3,20-ДИОНА
Вид РИД
Изобретение
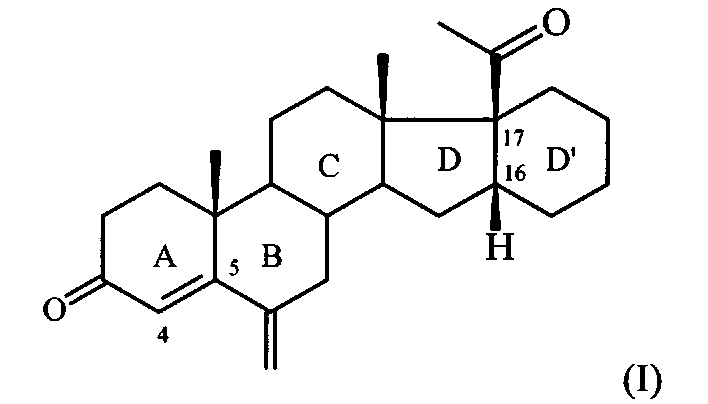
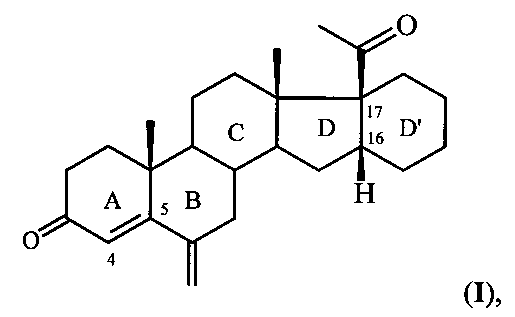
Изобретение относится к области химии природных и физиологически активных веществ, а именно к способу получения промежуточного продукта в синтезе стероидных гормонов прегнанового ряда, содержащих дополнительный шестичленный карбоцикл [М. Ibrahim-Quali. Synthesis of pentacyclic steroids. Steroids, 2008, 73, N 8, 775-97], конденсированный со стероидным скелетом в 16α,17α-положениях [А.В. Камерницкий, И.С. Левина. Прегна-D′-пентараны. Прогестины и антипрогестины. Биоорган. химия, 2005, т. 31, с. 115 и 227], а именно к способу получения 6-метилено-16α,17α-циклогексанопрегн-4-ен-3,20-диона формулы:
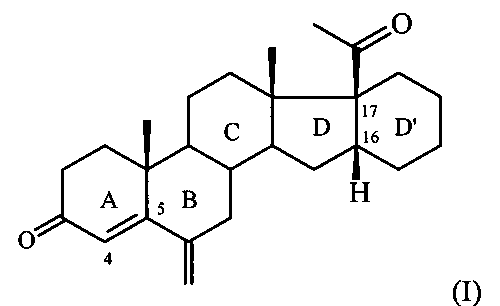
Соединение формулы I является непосредственным предшественником в синтезе высокоэффективного прогестина - 6α-метил-16α,17α-циклогексано-прогестерона.
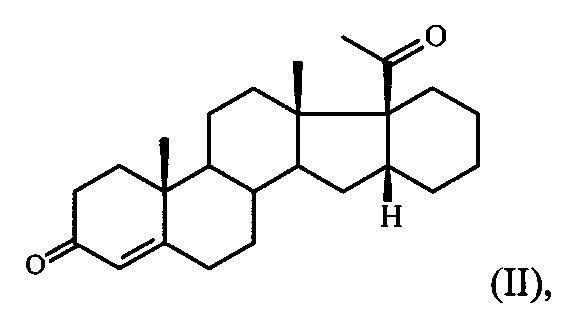
Известен единственный способ получения соединения формулы I путем прямого γ-метиленирования соединения формулы II, т.е. введение метилиденовой группы в 6-положение стероидной молекулы конденсацией сопряженного кетона II с производным формальдегида (диэтилацеталем формальдегида) в присутствии хлорокиси фосфора и ацетата натрия в растворе хлорированного углеводорода [И.С. Левина, А.В. Камерницкий. Синтез 6α-метил-16α,17α-циклогексанопрогестерона через γ-метиленирование 16α,17α-циклогексанопрегн-4-ен-3,20-диона (II). Изв. АН СССР, сер. хим., 1997, №6, 1234-35]. Выход целевого продукта не превышает 55%.

Этот способ имеет ряд существенных недостатков, которые не позволяют его использовать в промышленных масштабах, а именно достаточно жесткие условия проведения реакции (длительное кипячение реакционной смеси), необходимость хроматографической очистки продукта реакции и недостаточно высокий выход целевого продукта.
Задачей настоящего изобретения является увеличение выхода 6-метилено-16α,17α-циклогексанопрегн-4-ен-3,20-диона формулы I и упрощение технологии его получения.
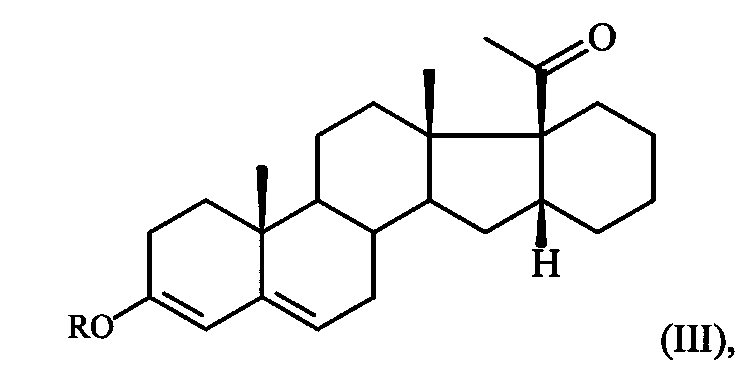
Поставленная задача достигается предлагаемым способом получения 6-метилено-16α,17α-циклогексанопрегн-4-ен-3,20-диона формулы I путем взаимодействия 16α,17α-циклогексанопрегн-4-ен-3,20-диона формулы II с триметилортоформиатом (СН(ОМе)3) в среде метанола либо с триэтилортоформиатом (СН(OEt)3) в среде этанола в присутствии пара-толуолсульфокислоты (p-TsOH) при комнатной температуре и полученную при этом реакционную массу, содержащую соответствующий 3,5-диенольный эфир формулы:
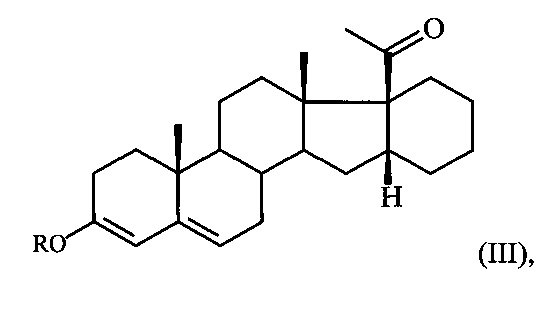
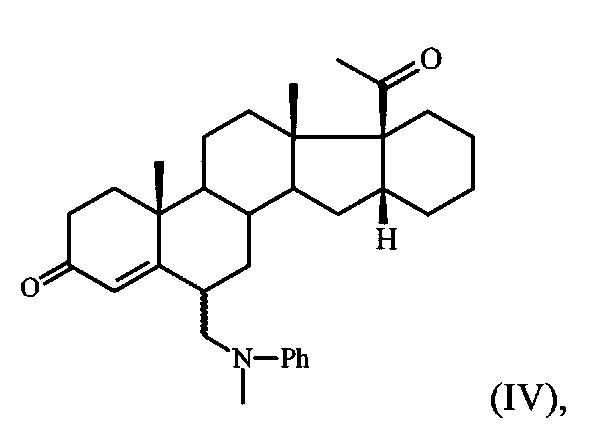
где R=Me либо Et, обрабатывают N-метиланилином и 37%-ным водным раствором формальдегида, реакционную смесь выдерживают при 35-40°С, выливают в охлажденную до температуры 8-10°С воду, содержащую гидроксид натрия, с последующим выделением полученной при этом изомерной смеси 6α- и 6β-изомеров (N-метил-N-фениламинометил)-производного формулы:
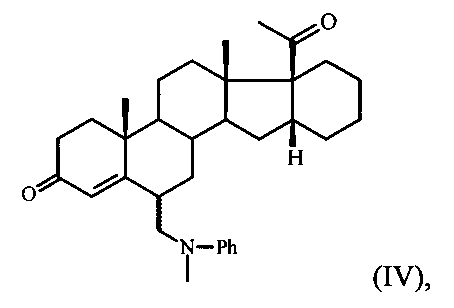
и обработкой ее концентрированной соляной кислотой при комнатной температуре с последующим выделением целевого продукта I.
Процесс протекает по следующей схеме:
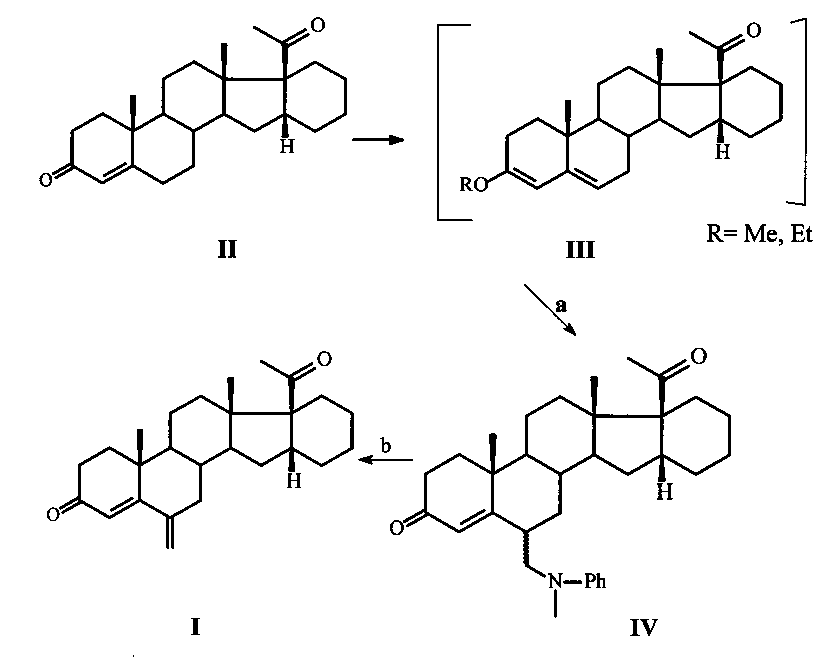
а) СН(ОМе)3 или CH(OEt)3, МеОН либо EtOH, p-TsOH, 1 ч; N-метиланалин, НСНО; b) HCl.
Общий выход целевого продукта I составляет 85%.
Отличительной особенностью способа является проведение первой стадии енолизации 4-дегидро-3-оксостероида II и второй стадии аминометилирования 3,5-диенольного эфира III водным раствором формальдегида и N-метиланилина с образованием N,N-дизамещенного 6-аминометилпроизводного IV и далее выделения целевого продукта I без дополнительной очистки с количественным выходом.
Техническим результатом предлагаемого способа является повышение выхода целевого продукта до 85%, осуществление процесса в мягких условиях (не требуется повышенной температуры), простота выделения промежуточного и целевого продуктов (не требуется хроматографического разделения получаемых соединений).
В известной научно-технической и патентной литературе отсутствует полная совокупность признаков, характеризующих предлагаемое изобретение.
Из уровня техники было неочевидным, что заявляемая последовательность стадий для данного класса стероидов - пентациклических стероидов - будет протекать в мягких условиях и с высоким выходом, так как наличие дополнительного кольца D′ могло вносить определенные изменения в течение процесса.
Изобретение может быть использовано при производстве промежуточного продукта в синтезе стероидных гормонов прегнанового ряда, которые являются ценными гормональными препаратами, применяемыми в медицине для лечения гормональных дисфункций, невынашиваемости при беременности и в качестве компонентов контрацептивов.
Изобретение иллюстрируется следующими примерами.
Пример 1.
А. В суспензию 4 г сопряженного кетона II в смеси 40 мл триметилортоформиата (СН(OMe)3) и 80 мл безводного метанола добавляют 200 мг пара-толуолсульфокислоты. Реакционную массу (суспензию) перемешивают при комнатной температуре в течение 30 мин. По окончании реакции в реакционную массу, содержащую 3,5-диенольный эфир III (R=Me), добавляют 9,2 мл N-метиланилина (изменение цвета) и 1 мл 37% водного раствора формальдегида. Суспензию нагревают до температуры ~40°С, выдерживают при этой температуре 1,5 ч, после чего раствор выливают в охлажденную до 8-10°С воду (120 мл), содержащую 1,2 г NaOH, и перемешивают при этой же температуре в течение 30 минут. Осадок отфильтровывают, промывают водой до нейтральной реакции. Получают 5,25 г смеси 6α- и 6β-изомеров (N-метил-N-фениламинометил)-производного IV (выход 98%).
В. К суспензии 3,9 г смеси изомеров IV в 50 мл ацетона добавляют по каплям 2,8 мл 32%-ной соляной кислоты. Реакционную массу (раствор) выдерживают при комнатной температуре в течение 30 минут. По окончании реакции реакционную массу разбавляют 100 мл воды и выдерживают 30 минут при комнатной температуре. Осадок отфильтровывают, промывают сначала 50 мл смеси ацетон-вода (1:2), затем водой до нейтральной реакции и сушат на воздухе. Получают 3,43 г кристаллического целевого 6-метиленпентарана I. Осадок растворяют в хлористом метилене и фильтруют через 20-кратное количество силикагеля. Силикагель промывают хлористым метиленом, фильтрат упаривают досуха, получают кристаллический остаток целевого 6-метилено-16α,17α-циклогексанопрегн-4-ен-3,20-диона I (2,74 г, 90%). Т.пл. 181-184°С (из смеси изопропиловый спирт-вода). [α]D+144 (с 1.30). Масс-спектр: найдено: m/z 391,2594 [M+Na]+. C26H36O2. Вычислено: М=380,2715. Спектр ЯМР 1Н (δ, м.д.): 0,70 с (3 Н, 18-СН3), 1,10 с (3 Н, 19-СН3), 2,15 (3 Н, 21-СН3), 2,98 м (1 Н, Н 16), 4,94-5.06 д (2 Н, С 6=СН2), 5,92 с (1 Н, Н 4).
Пример 2. Аналогично примеру 1 на стадиях А и В, из 1 г (2,7 ммоля) сопряженного кетона II, 20 мл CH(OEt)3 и 4 мл абсолютного этанола и 200 мг п-толуолсульфокислоты получают в итоге 0,87 г (85%) 6-метилено-16α,17α-циклогексанопрегн-4-ен-3,20-диона I.
Способ получения 6-метилено-16α,17α-циклогексанопрегн-4-ен-3,20-диона формулы: из 16α,17α-циклогексанопрегн-4-ен-3,20-диона формулы: отличающийся тем, что 16α,17α-циклогексанопрегн-4-ен-3,20-дион формулы II подвергают взаимодействию с триметилортоформиатом в среде метанола либо с триэтилортоформиатом в среде этанола в присутствии пара-толуолсульфокислоты при комнатной температуре и полученную при этом реакционную массу, содержащую соответствующий 3,5-диенольный эфира формулы: где R=Me либо Et, обрабатывают Ν-метиланилином и 37%-ным водным раствором формальдегида, реакционную смесь выдерживают при 35-40°С, выливают в охлажденную до температуры 8-10°С воду, содержащую гидроксид натрия, с последующим выделением полученной при этом изомерной смеси 6α- и 6β-изомеров (N-метил-N-фениламинометил)-производного формулы: и обработкой ее концентрированной соляной кислотой при комнатной температуре.