Результат интеллектуальной деятельности: СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОСТРОЙ ЛУЧЕВОЙ БОЛЕЗНИ В ЭКСПЕРИМЕНТЕ
Вид РИД
Изобретение
Изобретение относится к медицине и ветеринарии и может использоваться для лечения острой лучевой болезни.
Меланины - природные пигменты, биологически активные вещества, содержащиеся в тканях микроорганизмов, растений животных и человека (придают окраску волосам, ресницам, коже), в ряде пищевых продуктов (чай, кофе, грибы, гречиха и др.). Образуются в результате полимеризации тирозина, диоксифенилаланина или катехоламинов на белковой матрице. Химическое строение природных меланинов до сих пор окончательно не установлено вследствие их чрезвычайно сложной высокополимерной структуры.
По данным фармакологических исследований, меланины водорастворимые не токсичны. Однократное введение внутрь или внутрибрюшинно в диапазоне доз 100-3000 мг/кг не вызывало гибели мышей. При введении в течение 15 суток также не зафиксировано смертельных исходов, нарушения общего состояния, патологического изменения внутренних органов, не выявлено канцерогенного действия [1-4].
Сведения, имеющиеся в литературе, демонстрируют наличие у меланинов разнообразных биологических свойств, которые проявляются при введении внутрь или внутрибрюшинно. На мелких лабораторных животных (мыши, крысы) показано, что меланин обладает антистрессорным [1, 5], противосудорожным [5] и антимутагенным действием [6, 7]. Установлено, что меланин повышает физическую работоспособность [8], усиливает иммунную защиту организма [1, 8, 9], вызывает продукцию цитокинов, таких как ИЛ-6, ИЛ-8, туморнекротизирующий фактор, ростовой фактор эндотелия [10, 12]. Имеются сведения об успешном применении меланина в составе комплексной терапии онкологических заболеваний легких, кишечника, молочной железы, при сахарном диабете [1]. Одним из наиболее важных свойств является выраженная антиоксидантная активность. Меланины ингибируют перекисное окисление липидов в связи с их способностью перехватывать супероксидный анион радикал 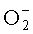 и перекисные радикалы органических соединений [2, 3, 13, 14 и др.].
и перекисные радикалы органических соединений [2, 3, 13, 14 и др.].
В базе данных литературы были обнаружены отдельные источники информации, в которых описано использование меланина в качестве радиопротектора, вводимого парентерально до воздействия ионизирующего излучения, что практически невозможно при внезапных аварийных ситуациях. В экспериментальных условиях однократное или ежедневное в течение 4-х суток внутрибрюшинное введение меланина до облучения в дозах, вызывающих гибель 40-80% мышей, повышало выживаемость на 35% и 60% соответственно [15, 16]. Показано также, что внутривенная инъекция наномеланина при радиоизотопной терапии меланомы в экспериментах на мышах не оказывала защитного действия на клетки опухоли, но при этом способствовала уменьшению поражения кроветворения [17 - прототип, 18].
При хроническом в течение 20-ти суток облучении беременных крыс в суммарной дозе ~1,25 Гр, не сопровождавшемся развитием острой лучевой болезни (ОЛБ), ежедневное внутрижелудочное введение суспензии меланина в крахмальном геле (10 мг/кг) устраняло в постнатальном периоде дефицит соматического развития крысят [8, 9]. Имеются указания на способность меланина снижать накопление радионуклидов в организме [19].
Задачей работы является исследование и доказательство возможности оптимального лечебно-профилактического (введение после облучения) использования водорастворимого меланина после радиационного воздействия в дозах, вызывающих острую лучевую болезнь (ОЛБ). Разработка позволяет повысить выживаемость облученных животных, ускорение восстановления массы тела, локомоторной активности и показателей кроветворения, нарушенных облучением.
Технический результат заключается в повышении выживаемости облученных животных, ускорении восстановления массы тела, локомоторной активности и показателей кроветворения, нарушенных облучением.
Для достижения поставленной задачи изучено влияние меланина на выживаемость, показатели кроветворения и спонтанную двигательную активность облученных мышей.
В ходе исследования было выявлено, что наилучшие эффекты достигаются при использовании меланина в растворенном виде. Причем оптимальным является растворение его в дистиллированной воде из расчета 12,5 мг на 100 мл, с использованием этой воды у животных как питьевой. Нами было выявлено, что именно в данной форме меланин способен оказывать наиболее адекватное радиорезистентное действие на уже подвергшихся острому облучению животных.
В экспериментах использовали меланин, изготовленный в соответствии с ТУ 9197-001-6735746-0, с водорастворимостью не менее 80% и концентрацией парамагнитных центров не менее 8·1017 спин/г.
Лечебная эффективность меланина, была изучена на 262 аутбредных мышах СД-1, самках массой 22-30 г. В эксперименты отбирались только клинически здоровые особи. Контрольные и подопытные группы формировались случайным выбором из равнозначных по массе животных.
Испытания лечебной эффективности меланина проведены при тотальном - остром и фракционированном радиационном воздействии. Кратковременное облучение осуществлялось на рентгеновской установке биологической РУСТ-М1 (РУБ РУСТ-М1): напряжение 200 кВ, ток пучка 2×2,5 mA, фильтр алюминиевый 1,5 мм. Мощность дозы 0,85 Гр/мин ±10%. Часть мышей облучена гамма-квантами 60Co с мощностью 1 Гр/мин на установке РОКУС-М. Дозы однократного облучения составляли 5,0; 6,5; 7,0; 7,5 Гр.
Фракционированное тотальное облучение по 0,5 Гр или 1 Гр проводили ежедневно в течение 5 суток, затем повторно после 2-дневного перерыва.
Меланин, растворенный в дистиллированной воде из расчета 12,5 мг на 100 мл, мыши получали в свободном доступе вместо питьевой воды с 1-х по 30-е сутки после однократного облучения, а при фракционированном облучении - с 1-х суток от начала облучения и по 30-е сутки после окончания облучения. В эти же сроки контрольные нелеченые животные потребляли дистиллированную воду.
Эксперименты проведены с соблюдением «Правил проведения работ с использованием экспериментальных животных, регламентированных приказом Министерства здравоохранения СССР №75 от 12.08.1987 г.».
Влияние меланина на общее состояние облученных животных оценивали по их 30-дневной выживаемости и динамике массы, которую измеряли 2 раза в неделю, а также по уровню локомоторной активности в «открытом поле» и состоянию кроветворения.
Статистическую обработку полученных в экспериментах данных проводили с помощью общепринятых методов вариационной статистики. Рассчитывали средние арифметические показатели и их стандартные ошибки во все сроки обследования. О статистической значимости различий у животных сравниваемых групп судили по критериям Стьюдента, χ2 и Вилкоксона-Манна-Уитни.
В проведенных исследованиях авторами установлено, что меланин при приеме после облучения обладает лечебным действием, проявляющимся в повышении радиорезистентности. Полученные результаты в обобщенном виде и в различных сериях представлены в таблицах 1 и 2. Облучение в дозах 6,5; 7,0 и 7,5 Гр рентгеновскими и гамма-лучами вызывало развитие костномозговой формы ОЛБ, после которой подавляющее большинство мышей в контрольных группах (68 из 70) погибло. Выживаемость нелеченых животных при наблюдении в течение 30 суток после облучения составила 20% (при СД80) и 0% (при СД100). Лечебное применение меланина с питьевой водой позволило увеличить выживаемость до 40% (при СД80) и 8,3% (при СД100). Суммарный показатель составил 16,3%, в контроле - 2,9%. Различие между группами статистически значимо (критерий χ2, p<0,01).

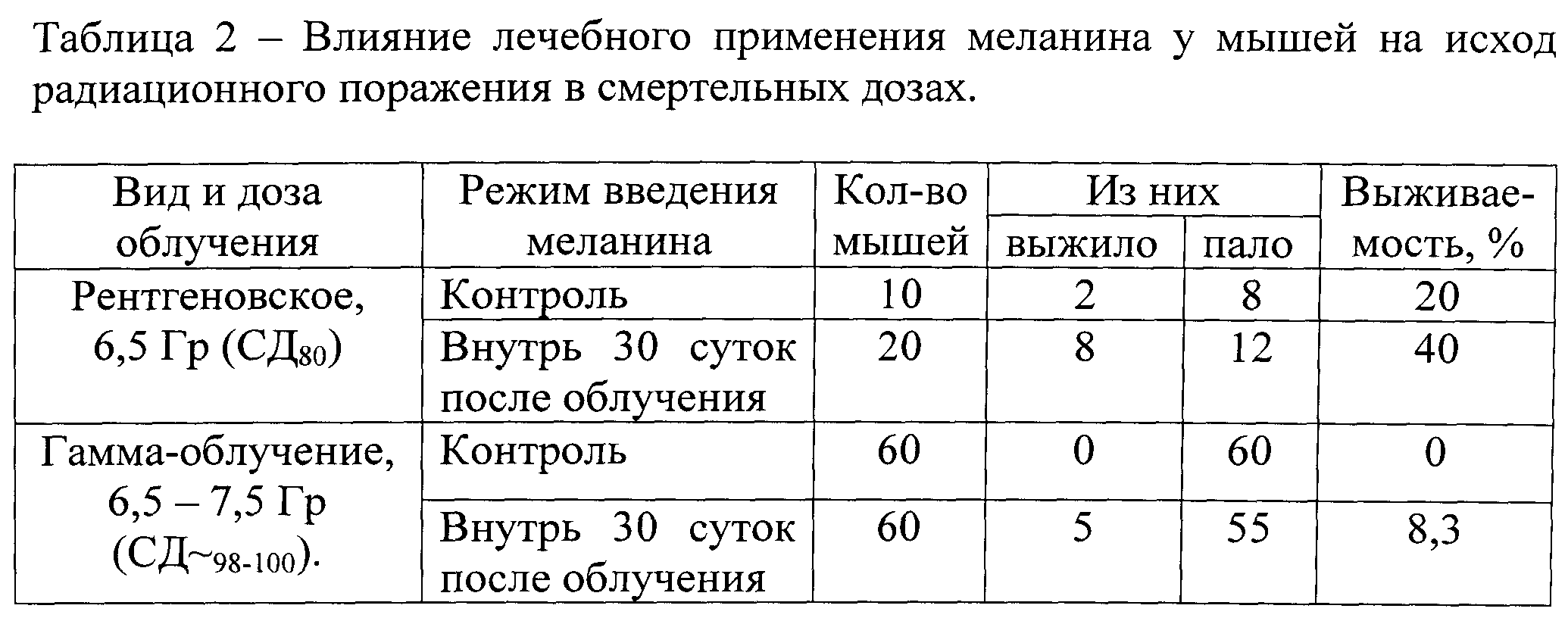
Наблюдение за клиническим состоянием животных показало также, что прием меланина после облучения способствует сохранению массы тела на более высоком уровне, чем в контроле, и ускорению ее роста в период восстановления. Различия на 18-21 сут статистически значимы (Таблица 3).

Помимо наблюдения за клиническим течением ОЛБ у подопытных мышей определяли состояние кроветворения на 8-е сут после облучения рентгеновскими лучами в сублетальной дозе 5 Гр. На таблице 4 видно, что масса тимуса, масса селезенки и количество эндогенных колониеобразующих единиц в селезенке у леченых животных существенно выше, чем у контрольных облученных мышей. Зарегистрированные различия по массе указанных органов статистически значимы (p<0,01).

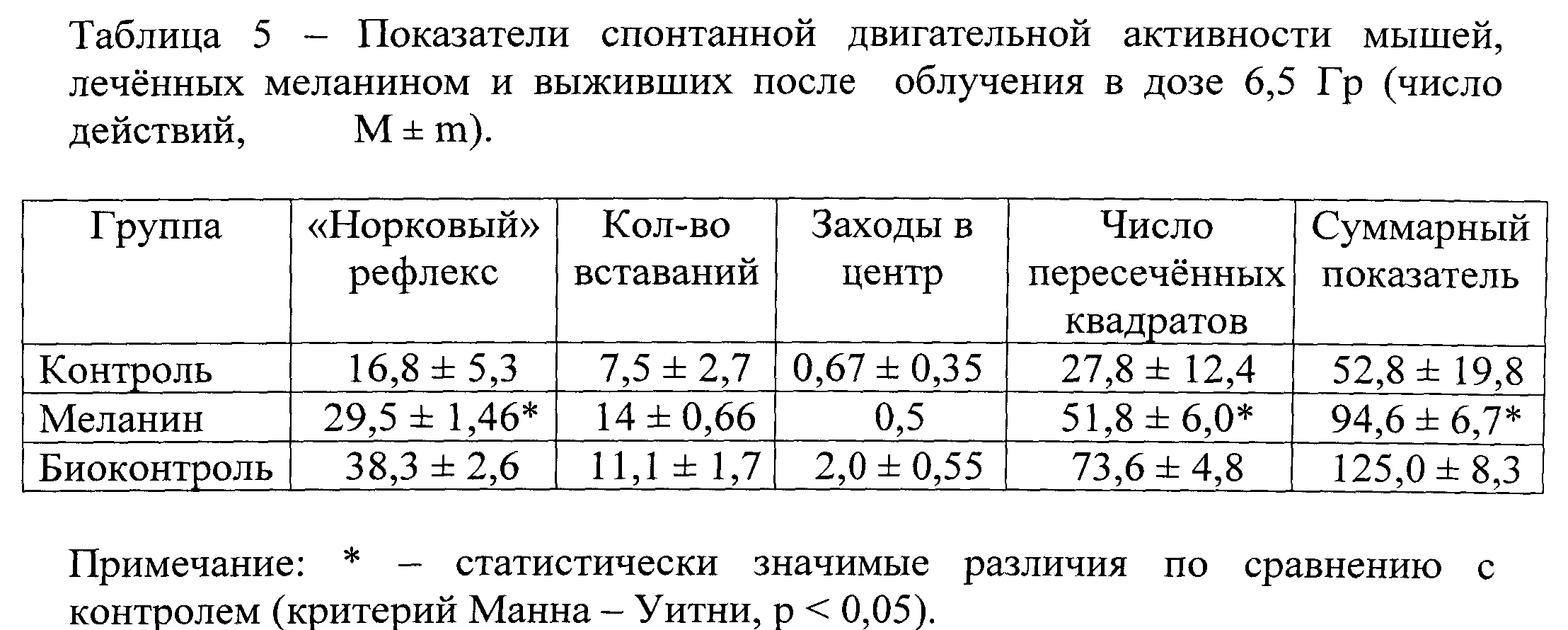
У мышей, перенесших ОЛБ, применение меланина оказало благоприятное действие на состояние локомоторной активности и психофизиологический статус. При тестировании в «открытом поле» после облучения в дозе 6,5 Гр большинство показателей (число пересеченных квадратов, количество вставаний, заглядываний в норки) у леченых мышей находились на существенно более высоком уровне, чем в контроле. Суммарный показатель составил соответственно 94,6±6,7 и 52,8±19,8 (p<0,05) при значении физиологической нормы для данного вида животных в наших экспериментах 125,0±8,3. (Таблица 5)
Лечебно-профилактический эффект меланина при фракционированном тотальном воздействии, вызвавшем у мышей клинические проявления поражения, характерные для костномозговой формы ОЛБ, проиллюстрирован в таблице 6.

В проведенных исследованиях установлено, что в контрольной группе выживаемость составила 43,7%. Лечебное применение меланина повышало выживаемость до 100% (p=0,002). Наращивание массы после окончания облучения у леченых животных отмечено уже на 7-е сут, в контроле - на 11-е сут.
Спустя 30 сут после окончания фракционированного воздействия поведенческая активность леченых мышей в «открытом поле» также была выше, чем у контрольных: 141,5±7,6 и 87,7±44 соответственно.
При меньшей дозе на фракцию 0,5 Гр и аналогичной схеме облучения в динамике изучено влияние меланина на показатели кроветворения (таблица 7).

Из представленных данных видно, что в период наибольшего угнетения кроветворения лечение меланином смягчало вызванные облучением изменения, способствуя сохранению на более высоком уровне (на 7-е сут) количества тромбоцитов в периферической крови (873±10,6×109/л, в контроле - 715±46,6×109/л; p<0,02), миелокариоцитов в костном мозге (13,7±2,8×106, в контроле - 8,1±1,17×106; p<0,1), ускоряло восстановление показателей кроветворения на 14-е и 21-е сутки.
Анализ совокупности полученных результатов позволяет сделать вывод о наличии у меланина лечебного действия при приеме внутрь после радиационного воздействия. На 2-х моделях костномозговой формы ОЛБ показано, что применение меланина повышает выживаемость, уменьшает негативное влияние облучения на динамику массы, показатели кроветворения и двигательной активности.
Таким образом, предлагаемый способ осуществляется следующим образом.
После облучения осуществляют пероральное введение животным меланина в жидкой форме. Причем используют меланин с водорастворимостью не менее 80% и концентрацией парамагнитных центров не менее 8·1017 спин/г, в растворенном виде в дистиллированной воде в эффективной концентрации. Воду с меланином используют у мышей в качестве питьевой после однократного и фракционированного острого облучения, способного вызвать острую лучевую болезнь. Воду с меланином употребляют с 1-х по 30-е сутки после однократного облучения, а в ходе фракционированного облучения с 1-х суток от начала облучения и по 30-е сутки после окончания облучения.
Пример 1. Лечебно-профилактическую противолучевую эффективность меланина изучают в опыте на 32 аутбредных мышах СД-1, самках массой 28-30 г, находящихся в условиях вивария на обычном рационе питания.
В качестве модели радиационного поражения используют фракционированное 10-кратное тотальное облучение по 1 Гр ежедневно в течение 5 сут, затем после 2-дневного перерыва повторно в том же режиме. Облучение осуществляется гамма-квантами 60Co на установке РОКУС-М (средняя мощность дозы 1 Гр/мин). Животных облучают группами по 10-16 голов в пластиковых коробках. После 1-й фракции животных делят на две равноценные по массе группы, одна из них получает для питья в свободном доступе меланин, который растворяют в дистиллированной воде (ДВ) из расчета 12,5 мг/100 мл, другая группа получает ДВ на протяжении всего периода наблюдения (до 30-х сут после окончания облучения).
Развитие ОЛБ сопровождается падением массы тела, снижением двигательной активности, отказом от корма, потерей опрятности, более выраженными у контрольных животных.
Интегральной оценкой влияния меланина на течение ОЛБ является показатель выживаемости. К 30-м суткам применение меланина обеспечило выживаемость всех животных (16 из 16), тогда как в контрольной группе выжило 7 из 16.
Таким образом, лечебное действие меланина проявилось в повышении выживаемости до 100% по сравнению с 43,7% выживших в контрольной группе. Разница между показателями статистически значима (p=0,02).
Пример 2. Лечебно-профилактическую эффективность меланина изучают на аутбредных мышах СД-1, самках массой 22-30 г, находящихся в обычных условиях вивария при свободном доступе к воде. Мыши подвергаются однократному тотальному облучению в дозе 6,5 Гр на рентгеновской установке биологической РУСТ-М1 (РУБ РУСТ-М1): напряжение 200 кВ, ток пучка 2×2,5 мA, фильтр алюминиевый 1,5 мм. Мощность дозы 0,85 Гр/мин ±10%.
Животных облучают группами в специальных пластиковых контейнерах, разделенных на индивидуальные ячейки.
Одна группа мышей сразу после облучения и далее до 30-х сут вместо водопроводной воды получает меланин, который растворяют в ДВ из расчета 12,5 мг/100 мл. В те же сроки контрольные животные потребляют ДВ. Опытные и контрольные группы формируются методом случайной выборки из равнозначных по массе животных. Наблюдение осуществляется в течение 30-ти сут, по истечении которых регистрируют количество выживших мышей в опыте и контроле.
Развитие ОЛБ сопровождается падением массы тела, снижением двигательной активности, отказом от корма, потерей опрятности, более выраженными у контрольных животных. При приеме меланина внутрь в группе леченых мышей из 20-ти выжило 8, в контрольной группе - из 10 - 2.
Таким образом, лечебный эффект меланина при остром кратковременном облучении проявился увеличением выживаемости на 20%.
Пример 3. Влияние меланина на изменение массы тела - интегральный показатель, отражающий общее состояние животных, изучают на 30-ти аутбредных мышах СД-1, самках с исходной массой 22-30 г, находящихся в условиях вивария. Распределяют животных по массе на 2 группы.
Облучение осуществляется рентгеновскими лучами в дозе 6,5 Гр на установке РУСТ-М1 (РУБ РУСТ-М1): напряжение 200 кВ, ток пучка 2×2,5 мA, фильтр алюминиевый 1,5 мм. Мощность дозы 0,85 Гр/мин ±10%. Животных облучают группами по 10-15 голов в специальных пластиковых контейнерах. После облучения одна группа получает для питья раствор меланина в ДВ из расчета 12,5 мг/100 мл, другая - ДВ на протяжении всего пострадиационного периода наблюдения в течение 30-ти сут.
В динамике 2 раза в неделю фиксируют изменения массы тела. Меланин способствует ускорению роста массы тела и ее возвращению к исходному уровню. В период 18-21-х суток у леченых мышей показатели массы составляли 18,9±1,09 и 20,9±1,2 г, в контроле - 13,5±1,24 г и 15,0±2,9 г. Разница между показателями статистически значима (критерий Стьюдента, p<0,02-0,05).
Пример 4. Влияние меланина на пострадиационное восстановление кроветворения изучают на 24 аутбредных мышах - самках СД-1 с исходной массой 22-30 г (8 - облученных леченых, 8 - облученных контрольных и 8 - необлученных, биоконтроль), находящихся в условиях вивария на обычном рационе.
Для моделирования острого радиационного поражения используют рентгеновское излучение в дозе 5 Гр на установке РУСТ-М1 (РУБ РУСТ-М1): напряжение 200 кВ, ток пучка 2×2,5 мA, фильтр алюминиевый 1,5 мм. Мощность дозы 0,85 Гр/мин ±10%. Животных облучают группами по 8 голов в пластиковых контейнерах. После облучения формируют 3 рандомизированные по массе группы, одна из которых ad libitum получает ДВ с меланином (12,5 мг/100 мл), а две другие (контроль облучения и биоконтроль) - ДВ.
На 8-е сут после облучения животных умерщвляют путем цервикальной дислокации и стандартными методами определяют массу тимуса и селезенки, подсчитывают в ней число эндогенных колоний, выявляемых после 2-часовой фиксации в жидкости Буена.
Показатели массы органов у леченых мышей составили: тимус - 32±2,9 мг; селезенка - 38,9±5,3 мг; в облученном контроле соответственно 22,1±2,0 мг и 25,8±1,6 мг; в биоконтроле - 82,6±14,4 мг и 120,8±26,0 мг. Различия между показателями облученных леченой и контрольной групп статистически значимы (по критерию Манна-Уитни, p<0,01).
Уровень эндогенных колоний в селезенке леченых животных составил 7,4±2,1, что существенно выше, чем в контрольной облученной группе 4,0±0,8.
Пример 5. Влияние меланина на ориентировочно-исследовательскую и общую локомоторную активность исследуют на 40 аутбредных СД-1, мышах самках массой 22-30 г, облученных в дозе 6,5 Гр рентгеновскими лучами на установке РУСТ-М1 (РУБ РУСТ-М1): напряжение 200 кВ, ток пучка 2×2,5 мA, фильтр алюминиевый 1,5 мм. Мощность дозы 0,85 Гр/мин ±10%. Животных, рандомизированных по массе, распределяют на 3 группы, одна из которых ad libitum с ДВ получает с 1-х суток меланин (12,5 мг/100 мл), две другие (контроль облучения и биоконтроль - необлученный) - ДВ.
По окончании периода реконвалесценции (32-34 сут) у мышей, перенесших ОЛБ, а также у интактных (биоконтроль) определяют состояние спонтанной двигательной активности в «открытом поле». Мышь помещают в центр специального манежа, пол которого разделен на секторы. В течение 3-х мин подсчитывается число стоек, пересеченных квадратов, заходов в центр, заглядываний в отверстия в полу и суммарное количество действий.
У леченых меланином мышей общий суммарный показатель составил 94,6±6,7 и был существенно выше, чем у облученных контрольных животных - 52,8±19,8, при значении физиологической нормы (биоконтроль) 125±8,3. Различия между облученными животными леченой и контрольной групп статистически значимы (критерий Манна - Уитни, p<0,05). Статистически достоверные отличия зарегистрированы в том числе по количеству заглядываний в «норки» (29,5±1,46 и 16,8±5,3) и пересеченных квадратов (51,8±6,0 и 27,8±12,4).
Таким образом, меланин повышает выживаемость животных после однократного или фракционированного радиационного воздействия в дозах, вызывающих развитие костномозговой формы ОЛБ. Эффект достигается при курсовом лечебном приеме внутрь с питьевой водой из расчета 12,5 мг/100 мл. Лечебная эффективность также клинически зарегистрирована в виде поддержания на более высоком уровне массы тела, ориентировочно-двигательной активности и некоторых показателей кроветворения.
Противолучевые свойства при практически полной безвредности, простой и удобный способ применения позволяют использовать меланин для решения задач радиационной медицины, в частности для лечения костномозговой формы радиационных поражений.
Источники литературы
1. Водорастворимый растительный меланин http//factor.net.ua/melanin/vodorasvorimyj-rastitelnyj-melanin.html. 2011.
2. Островский М.А., Донцов А.Е. Физиологические функции меланина в организме //Физиология человека. 1985. Т.11. №4. С.670-678.
3. Жеребин Ю.М., Бондаренко Н.А., Макан С.Ю. и др. Фармакологические свойства эномеланиновых пигментов //Доклады АН УССР. 1984. №3. серия 5. С.64-67.
4. Борщевская М.И., Васильева С.М. Развитие представлений о биохимии и фармакологии меланиновых пигментов //Вопросы мед. химии. 1999. Т.45. вып.1. С.13-24.
5. Жеребин Ю.М., Сава В.М., Колесник А.А., Богатский А.В. Исследования антиокислительных свойств эномеланина //ДАН СССР. 1982. 262. №1. С.112-115.
6. Алексеева Т.Н., Орещенко А.В., Куликова А.В. и др. Влияние растительного меланинового пигмента на кластогенные эффекты химических мутагенов у мышей //Ж. «Экспериментальная и клиническая фармакология». 2001. №6. С.51-61.
7. Моссэ И.Б. //Радиация и наследственность: Генетические аспекты противорадиационной защиты. Минск: Университетское изд-во. 1990. 208 с.
8. Изместьева О.С., Дубовик Б.В., Жаворонков Л.П. Экспериментальная оценка радиозащитного действия меланина на соматическое развитие при облучении в антенатальном периоде онтогенеза //Радиационная биология. Радиоэкология. 2007. Т.47. №6. С.684-689.
9. Изместьева О.С., Дубовик Б.В., Жаворонков Л.П. Экспериментальная оценка нейроэмбриопротекторных свойств меланина при облучении в антенатальном периоде развития //Радиационная биология. Радиоэкология. 2007. Т.47. №6. С.690-695.
10. El-Obeid A., Al-Harbi S., AL-Jomah N., Hassib A. Herbal melanin modulates tumor necrosis factor alpha (TNF-alpha), interleukin 6 (IL-6) and vascular endothelial growth factor (VEGF) production //Phytomedicine: international journal of phytotherapy and phytopharmacology. 2006./May; 13 (5). P.324-333.
11. El-Obeid A., Hassib A., Ponten F., Westermark B. Effect of herbal melanin on IL-8: a possible role of Toll - like receptor 4 (TLR4) //Biochemical and Biophysical research communications. 2006. Jun. 16; 344 (4); 1200-6.
12. Oberg F., Hassib A., Ahnfelt M. et. al. Herbal melanin activates TLR 4/NF-kappa В signaling pathway //Phytomedicine: international journal of phytotherapy and phytopharmacology. 2009. May; 16 (5). P.477-484.
13. Grossi G.F., Durante M., Gvalanella G. et al. Effects of melanin on high-LET radiation response of human epithelial cells //Radiation and environmental biophysics. 1998. V.37. P.63-67.
14. Жданова Н.Н. О защитном действии пигмента. Своеобразие химической структуры меланинов //Микробиология. 1970. Т. XXXXIX. вып.4. С.431-434.
15. Kunwar A., Adhihary В., Jayakumar S. et al. Melanin, a promising radioprotector: Mechanisms of actions in a mice model //Toxicol. Appl. Pharmacol. 2012. Oct. 15; 264 (2): 202-11.
16. Бердышев Г.Д. О защитном действии меланина при облучении мышей //Радиобиология. 1964. Т.4. вып.4. С.644-645.
17. Schweitzer A.D., Revskaya E., Chu P. et al. Melanin-covered nanoparticles for protection of bone marrow during radiation therapy of cancer //Int. J. Radiat. oncol. Biol. phys. 2010. V.78. №5. P.1494-1502.
18. Revskaya E., Iongco A.M., Celler R.S. et al. Radioimmunotherapy of experimental human metastatic melanoma with melanin - binding antibodies and in combination with decarbazine //Clin. Cancer. Res. 2009. V.15. №7. P.2373-2379.
19. Моссэ И.Б., Плотникова С.И., Лях П.П. и др. Радиопротектор, снижающий накопление радионуклидов в организме. //Заявка на а.с. 06.12.90. №1888566 (116992).
Способ профилактики и лечения острой лучевой болезни в эксперименте, включающий пероральное введение животным меланина в жидкой форме после облучения, отличающийся тем, что используют меланин с водорастворимостью не менее 80% и концентрацией парамагнитных центров не менее 8·10 спин/г, в растворенном виде в дистиллированной воде в эффективной концентрации, причем воду с меланином используют у мышей в качестве питьевой после однократного и фракционированного острого облучения, способного вызвать острую лучевую болезнь, при этом воду с меланином употребляют с 1-х по 30-е сутки после однократного облучения, а в ходе фракционированного облучения с 1-х суток от начала облучения и по 30-е сутки после окончания облучения.
