Результат интеллектуальной деятельности: НОВЫЙ СПОСОБ СИНТЕЗА АГОМЕЛАТИНА
Вид РИД
Изобретение
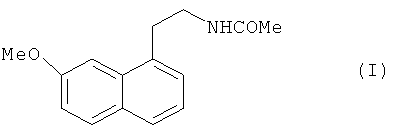
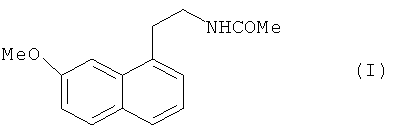
Настоящее изобретение относится к способу промышленного синтеза агомелатина или N-[2-(7-метокси-1-нафтил)этил]ацетамида формулы (I):

Агомелатин или N[2-(7-метокси-1-нафтил)этил]ацетамид обладает ценными фармакологическими свойствами.
В самом деле он имеет двойственную особенность, с одной стороны, быть агонистом рецепторов мелатонинэргической системы, а с другой стороны - антагонистом 5-HT2C рецептора. Эти свойства придают ему активность в центральной нервной системе и, в частности, при лечении тяжелых депрессий, сезонных депрессий, нарушений сна, патологии сердечно-сосудистой системы, патологии пищеварительной системы, бессонницы и утомления вследствие разницы во времени, нарушений аппетита и ожирения.
Агомелатин, его получение и терапевтическое применение описаны в Европейских патентах ЕР 0447285 и EP 1564202.
Принимая во внимание фармацевтическую пользу данного соединения, является важным получать его при помощи высокопроизводительного способа промышленного синтеза, который легко переводится в промышленный масштаб, обеспечивает получение агомелатина с высоким выходом и с превосходной чистотой.
В патенте ЕР 0447285 описан способ получения агомелатина, включающий восемь стадий исходя из 7-метокси-1-тетралона.
В патенте EP 1564202 заявитель разработал новый способ синтеза, намного более эффективный и промышленно применимый, включающий только четыре стадии исходя из 7-метокси-1-тетралона и позволяющий получить агомелатин весьма репродуктивным способом в хорошо определенной кристаллической форме.
Тем не менее, поиски новых способов синтеза, в частности, исходя из менее дорогостоящих исходных материалов, нежели 7-метокси-1-тетралон, по-прежнему представляют интерес.
Заявитель продолжил свои исследования и разработал новый способ синтеза агомелатина исходя из цианида аллила и производного ксантогената: преимущество этих новых исходных веществ состоит в том, что они являются простыми, легкодоступными в больших количествах при небольшой стоимости.
Этот способ синтеза основывается на использовании малораспространенных свободнорадикальных реакций и все же очень эффективных. Преобразование этих реакций в промышленный масштаб с использованием реакторов непрерывного действия является многообещающим по мере того, как становится легче контролировать продвижение цепной реакции.
Наряду с этим этот новый способ получения агомелатина воспроизводимым способом и без необходимости в лабораторной очистке с чистотой, совместимой с его применением в качестве фармацевтического действующего вещества. В действительности, таким образом агомелатин может быть синтезирован в 6 стадий, в ходе которых выделяют только два из промежуточных продуктов.
В частности, настоящее изобретение относится к способу промышленного синтеза соединения формулы (I):

отличающееся тем, что подвергают взаимодействию цианид аллила формулы (II):

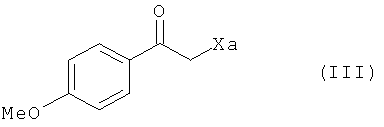
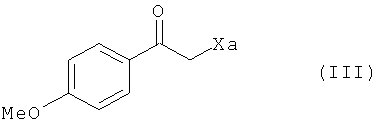
с соединением формулы (III) в присутствии свободнорадикального инициатора:

где Xa представляет собой группу -S-C(S)-OR, в которой R представляет собой линейную или разветвленную (С1-С6)алкильную группу,
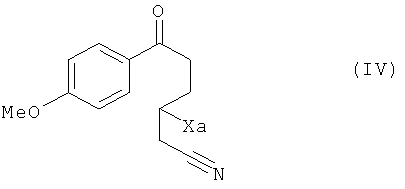
чтобы получить соединение формулы (IV):

в которой Xa является таким, как определено выше,
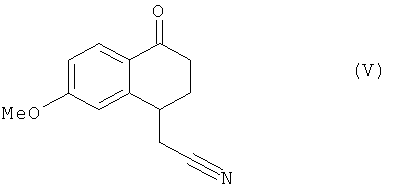
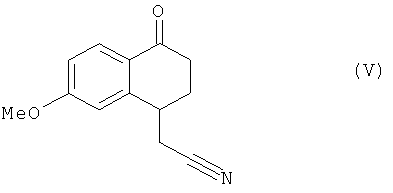
это последнее соединение по выбору может быть выделено до того, как его подвергнут реакции циклизации в присутствии свободнорадикального инициатора, чтобы образовать соединение формулы (V):

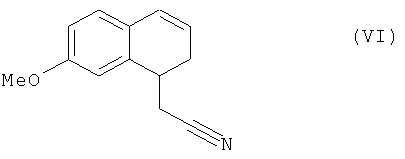
соединение формулы (V), которое также по выбору может быть выделено до того, как его подвергнут реакции восстановления/дегидратации, чтобы получить соединение формулы (VI):

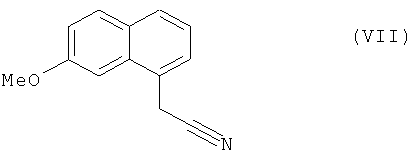
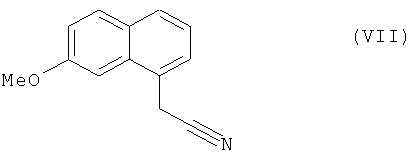
которое затем подвергают реакции ароматизации, чтобы получить соединение формулы (VII):

которое подвергают восстановлению водородом в присутствии никеля Ренея в полярной протонной среде и реакции с уксусным ангидридом, чтобы получить соединение формулы (I), которое выделяют в виде твердого вещества.
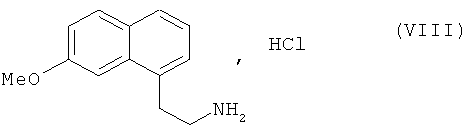
В предпочтительном варианте осуществления изобретения соединение формулы (VII) затем подвергают восстановлению водородом в присутствии никеля Ренея в среде аммиачного этанола, затем преобразуют в соль с использованием соляной кислоты, чтобы получить соединение формулы (VIII):

которое последовательно подвергают воздействию ацетата натрия и затем уксусного ангидрида, чтобы получить соединение формулы (I), которое выделяют в виде твердого вещества.
Альтернативно, соединение формулы (VII) может быть подвергнуто восстановлению водородом в присутствии никеля Ренея в среде, содержащей уксусный ангидрид в полярной протонной среде, чтобы получить соединение формулы (I), которое выделяют в виде твердого вещества.
В предпочтительном соединении формулы (III) Ха представляет собой группу -S-C(S)-OC2H5.
В способе согласно изобретению инициирование свободнорадикальных реакций осуществляют термическим способом. Предпочтительно, реакционную среду нагревают при температуре, находящейся между 50 и 140°C. Еще более предпочтительно, циклизацию осуществляют при температуре, находящейся между 130 и 135°C.
Пероксиды представляют собой свободнорадикальные инициаторы, в особенности пригодные для осуществления стадии присоединения соединения формулы (II) к соединению формулы (III) или же для проведения циклизации соединения формулы (IV), чтобы образовать соединение формулы (V). В качестве примеров, в частности, можно перечислить пероксид диизобутирила, пероксинеодеканоат кумила, пероксинеодеканоат трет-амила, пероксидикарбонат ди(2-этилгексила), пероксинеодеканоат трет-бутила, пероксидикарбонат дибутила, пероксидикарбонат дицетила, пероксидикарбонат димиристила, пероксинеогептаноат трет-бутила, пероксипивалат трет-амила, пероксид дидеканоила, перокси-2-этилгексаноат трет-амила, пероксиизобутират трет-бутила, 1,4-ди(трет-бутилперкосикарбо)циклогексана, пероксиацетат трет-бутила, пероксибензоат трет-бутила, пероксид ди-трет-амила, пероксид трет-бутил кумила, бис(трет-бутил)пероксида, пероксид дикумила, пероксид дилауроила (DLP) или пероксидикарбонат ди(4-трет-бутилциклогексила).
Предпочтительно, реакцию инициируют в присутствии пероксида дилауроила.
Количество пероксида дилауроила, применяемого при циклизации, предпочтительно составляет от 1 до 2,5 эквивалентов.
В предпочтительном варианте осуществления изобретения пероксид дилауроила добавляют в среду фракционным способом.
Реакции присоединения и/или циклизации осуществляют в растворителе, обычно применяемом в свободнорадикальной химии, таком как 1,2-дихлорэтан, дихлорметан, бензол, толуол, трифторметилбензол, хлорбензол, гексан, циклогексан, гептан, октан, этилацетат, трет-бутиловый спирт и их смеси.
Предпочтительно, применяют этилацетат в стадии присоединения соединения формулы (II) к соединению формулы (III), тогда как циклизацию соединения формулы (IV) до образования соединения формулы (V) выгодно осуществляют в хлорбензоле, этилацетате или этилбутирате. В этом последнем случае наиболее предпочтительным является хлорбензол.
Превращение соединения формулы (V) в соединение формулы (VI) выгодно осуществляют в присутствии кислоты Льюиса, такой как изопропоксид алюминия или изопропоксид самария. К тому же это превращение проводят предпочтительно в спирте (первичном или вторичном) и еще более предпочтительно в изопропаноле.
Предпочтительно, каталитическое количество п-толуолсульфоновой кислоты добавляют к смеси один раз весь тетралон (V), поглощенный в конце превращения соединения формулы (V) в соединение формулы (VI).
Ароматизацию соединения (VI) осуществляют в присутствии хинона и предпочтительно в присутствии 2,3-дихлор-5,6-дициано-1,4-бензохинона (DDQ) или тетрахлорбензохинона (TCQ). Еще более предпочтительно ароматизацию осуществляют в присутствии TCQ с нагреванием в колбе с обратным холодильником с толуолом.
Соединение формулы (II) доступно специалисту в данной области техники посредством классических химических реакций и/или описанных в литературных источниках.
Этот способ представляет особый интерес по следующим причинам:
- он позволяет получить соединение формулы (I) в промышленном масштабе с хорошими выходами исходя из простых и не очень дорогостоящих исходных веществ;
- только промежуточные продукты формулы (VI) и (VII) требуют стадии очистки и выделения.
Соединения формулы (V) и (VI), полученные способом согласно изобретению, являются новыми и пригодны в качестве промежуточных продуктов синтеза агомелатина.
Приведенные ниже примеры демонстрируют изобретение, но никоим образом не ограничивают его.
Для того чтобы обосновать реакционный путь, промежуточные продукты синтеза были систематически выделены и охарактеризованы. Тем не менее, возможно значительно оптимизировать способы, ограничивая число промежуточных продуктов. Таким образом, пример 2, приведенный подробнее ниже, соответствует тому же самому реакционному пути, который приведен в примере 1, но только с той разницей, что был выделен (7-метокси-1,2-дигидро-1-нафталенил)ацетонитрил и (7-метокси-1-нафтил)ацетонитрил.
Пример 1: N[2-(7-Метокси-1-нафтил)этил]ацетамид
Стадия A: Дитиокарбонат S-[1-(цианометил)-4-(4-метоксифенил)-4-оксобутил]-O-этила
Раствор цианида аллила (4,8 мл, 60,0 ммоль) и дитиокарбоната 5-[2-(4-метоксифенил)-2-оксоэтил]-O-этил1 (1дитиокарбонат S-[2-(4-метоксифенил)-2-оксоэтил]-О-этил, полученный в соответствии с протоколом, описанным в Batanero, В et al. J. Org. Chem. 2001, 66,320). 8,1 г (30,0 ммоль) в этилацетате (30 мл) нагревали в колбе с обратным холодильником в течение 15 минут под атмосферой азота. Во-первых, добавляют количество пероксида дилауроила (10 мол.%) к раствору в колбе с обратным холодильником. Через 1 ч 30 мин равным образом вводили другое количество пероксида дилауроила (5 мол.%). Когда реагенты были полностью израсходованы, смесь охлаждали при температуре окружающей среды и концентрировали под сниженным давлением. Затем сырую смесь очищали колоночной флеш-хроматографией (петролейный эфир - этилацетат: 95-5 до 80-20), чтобы получить соединение, указанное в заголовке в виде масла с выходом в 98%.
|
Стадия В: (7-Метокси-4-оксо-1,2,3,4-тетрагидро-1-нафталенил)ацетонитрил
Соединение стадии A, используемое в дальнейшем без очистки, растворяли в хлорбензоле (900 мл) и раствор нагревали в колбе с обратным холодильником в течение 15 минут под атмосферой азота. Затем пероксид дилауроила постепенно добавляли к раствору в колбе с обратным холодильником (10 мол.% каждые 10 мин). В конце реакции смесь охлаждали при температуре окружающей среды и концентрировали под сниженным давлением. Затем вводили ацетонитрил, чтобы осадить большую часть производных пероксида дилауроила. После этого смесь отфильтровывали, концентрировали под сниженным давлением и очищали колоночной флеш-хроматографией (петролейный эфир - этилацетат: 60-40), чтобы получить соединение, указанное в заголовке в виде твердого вещества с выходом в 40%.
MCBP (EI, m/z) Рассчит. для C13H13NO2: 215.0946; Обнаружено: 215.0946.
Стадия: (7-Метокси-1,2-дигидро-1-нафталенил)ацетонитрил
Изопропоксид алюминия (2,05 г, 10,0 ммоль) добавляли к раствору соединения, полученного в стадии B (680 мг, 3,15 ммоль) в изопропаноле (15 мл) при температуре окружающей среды. Реакционную смесь нагревали в колбе с обратным холодильником. После того как все исходные вещества были полностью израсходованы, туда добавляли несколько кристаллов моногидрата п-толуолсульфоновой кислоты и аппарат Дина Старка устанавливали на верхушку колбы. Смесь снова нагревали в колбе с обратным холодильником в течение 1 часа, в течение которого изопропанол постепенно заменяли толуолом с помощью аппарата Дина Старка. Затем добавляли раствор 1N HCl и полученные фазы разделяли. Водную фазу экстрагировали этилацетатом, тогда как органические фазы промывали насыщенным раствором NaHCO3, насыщенным раствором NaCl, затем высушивали над MgSO4, отфильтровывали и концентрировали под сниженным давлением. Остаток очищали колоночной хроматографией (петролейный эфир - этилацетат: 80-20), чтобы получить продукт, указанный в заголовке в виде масла с выходом в 85%.
МСВР (EI, m/z) Рассчит. для C13H13NO : 199.0997; Обнаружено: 199.1001.
Стадия D: (7-Метокси-1-нафтил)ацетонитрил
Способ A:
К раствору соединения, полученного на стадии C (1,0 г, 5,0 ммоль) в дихлорметане (50 мл) при температуре окружающей среды, добавляли DDQ (1,4 г, 6,0 ммоль). Реакционную смесь перемешивали в течение 2 дней, затем очищали с помощью насыщенного раствора NaHCO3. Водную фазу экстрагировали этилацетатом, тогда как органическую фазу промывали насыщенным раствором NaCl, высушивали над MgSO4, отфильтровывали и концентрировали под сниженным давлением. Остаток очищали колоночной хроматографией (петролейный эфир - этилацетат: 80-20), чтобы получить продукт, указанный в заголовке в виде твердого вещества с выходом в 55%.
Способ B:
К раствору TCQ (615 мг, 2,5 ммоль) в толуоле (1,5 мл), нагретому до 80°C, добавляли соединение, полученное на стадии C (462 мг, 2,3 ммоль), растворенное в толуоле (3,5 мл). Затем смесь нагревали в колбе с обратным холодильником в течение 2,5 ч, затем разбавляли с водой и экстрагировали петролейным эфиром. Органическую фазу промывали раствором NaOH (30 мас.%) и водой, затем высушивали над MgSO4, отфильтровывали и концентрировали под сниженным давлением. Остаток очищали колоночной хроматографией (петролейный эфир - этилацетат: 80-20), чтобы получить продукт, указанный в заголовке в виде твердого вещества с выходом в 61%.
MCBP (EI, m/z) Рассчит. для C13H11NO : 197.0841; Обнаружено: 197.0838.
Стадия E: N-[2-(7-Метокси-1-нафтил)этил]ацетамид
Реакцию осуществляли большей партией с целью оптимизировать полученный выход.
В 8 л реактор загружали 136 г никеля Ренея, 2,06 л этанола и 0,23 л воды. При перемешивании при 70°C и под 30 бар водорода медленно добавляли соединение, полученное в стадии D (0,8 кг), растворенное в уксусном ангидриде (2,4 л). В конце добавления реакционную среду перемешивали 1 час под водородом при 30 бар, затем реактор декомпрессировали и раствор отфильтровывали. После концентрирования среды остаток кристаллизовали в смеси этанол/вода 35/65, чтобы получить продукт, указанный в заголовке с выходом в 89% и химической чистотой более чем 99%.
Точка плавления: 108°C.
Пример 2: N-[2-(7-Метокси-1-нафтил)этил]ацетамид
Стадия A: (7-Метокси-1,2-дигидро-1-нафталенил)ацетонитрил
Раствор цианида аллила (6.75 мл, 84.0 ммоль) и дитиокарбоната S-[2-(4-метоксифенил)-2-оксоэтил]-О-этил1 (11.3 г, 42.0 ммоль) в этилацетате (45 мл) нагревали в колбе с обратным холодильником в течение 15 минут под атмосферой азота. В первую очередь добавляют количество пероксида дилауроила (10 моль %) к раствору в колбе с обратным холодильником. Через 1 ч 30 мин равным образом вводили другое количество пероксида дилауроила (5 моль %). После того как все исходные вещества были полностью израсходованы, смесь охлаждали при температуре окружающей среды и концентрировали под сниженным давлением. Сырую смесь растворяли в хлорбензоле (640 мл) и раствор нагревали в колбе с обратным холодильником в течение 15 минут под атмосферой азота. Затем пероксид дилауроила постепенно добавляли к раствору в колбе с обратным холодильником (10 мол.% каждые 10 мин). В конце реакции смесь охлаждали при температуре окружающей среды и концентрировали под сниженным давлением. Затем вводили ацетонитрил, чтобы осадить большую часть производных пероксида дилауроила. После этого смесь отфильтровывали, концентрировали под сниженным давлением. Половину сырого масла, полученного таким образом, растворяли в изопропаноле (100 мл) при температуре окружающей среды в присутствии изопропоксида алюминия (13.6 г, 66.6 ммоль). Реакционную смесь нагревали в колбе с обратным холодильником. После того как все исходные вещества были полностью израсходованы, туда добавляли несколько кристаллов моногидратной n-толуолсульфоновой кислоты и аппарат Дина Старка устанавливали на верхушку колбы. Смесь снова нагревали в колбе с обратным холодильником в течение 2 часов, в течение которых изопропанол постепенно заменяли толуолом с помощью аппарата Дина Старка. Затем добавляли раствор 1N HCl и полученные фазы разделяли. Водную фазу экстрагировали этилацетатом, тогда как органические фазы промывали насыщенным раствором NaHCO3, насыщенным раствором NaCl, затем высушивали над MgSO4, отфильтровывали и концентрировали под сниженным давлением. Остаток очищали колоночной хроматографией (петролейный эфир - этилацетат: 80-20), чтобы получить продукт, указанный в заголовке в виде масла с выходом в 24%.
MCBP (EI, m/z) Рассчит. для C13H13NO: 199.0997; Обнаружено: 199.1001.
Стадия B: (7-Метокси-1-нафтил)ацетонитрил
Осуществляли способом, аналогичным стадии D из примера 1.
Стадия C: N-[2-(7-Метокси-1-нафтил)этил]ацетамид
Осуществляли способом, аналогичным стадии E из примера 1.